-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Retikulární exantémy – patofyziologie, etiopatogeneze, klasifikace
Reticulate Eruptions: Pathophysiology, Etiopathogenesis, Classification
Terminology concerning livedo reticularis and livedo racemosa is not uniformly determined due to inconsistent classification in the past and to the use of different terms in different countries and medical specialties. The authors give a summary of actual knowledge about the physiology and pathophysiology of skin vascularization, about the main units of vascular supply, and angiosomes which give rise to the appearance of reticulate eruptions. They review the etiopathogenetic factors as well as the relationship of reticulate eruptions, inclusive retiform purpura to underlying systemic disorders. Practical approach to the diagnotics of reticulate eruptions is presented.
Key words:
skin vascularization – livedo reticularis – livedo racemosa – retiform purpura – livedo vasculopathy
Autoři: M. Kovačevičová; S. Švestková
Působiště autorů: Dermatovenerologická klinika FN Brno a LF MU Brno přednosta prof. MUDr. Vladimír Vašků, CSc.
Vyšlo v časopise: Čes-slov Derm, 87, 2012, No. 6, p. 211-219
Kategorie: Souborné referáty (doškolování lékařů)
Souhrn
Terminologie vztahující se k označení livedo reticularis a livedo racemosa není jednoznačně upřesněná díky nejednotné klasifikaci v minulosti a také používáním odlišných označení liveda v různých zemích a oborech. Autorky podávají přehled současných poznatků o fyziologii a patofyziologii kožního cévního zásobení, o základních jednotkách cévního zásobení, angiosomech, které podmiňují klinický vzhled retikulárních exantémů. Poskytují přehled etiopatogenetických faktorů a vztah retikulárních exantémů, včetně retiformní purpury, k systémovým onemocněním a uvádí návod praktického přístupu k jejich diagnostice.
Klíčová slova:
kožní cirkulace – livedo reticularis – livedo racemosa – retiformní purpura – livedo vaskulopatieÚVOD
Livedo reticularis a racemosa jsou poměrně časté kožní příznaky značící fialový síťovitý erytém, které mohou být projevem systémových onemocnění. Oba termíny jsou odvozeny z latinského jazyka: „livere“ znamená „modrati se“, „reticularis“ znamená síťovitý a „racemosus“ podobající se úponu vinné révy. I když uběhlo již sto let od doby, kdy Salomon Ehrmann popsal klinický obraz livedo racemosa, jasně ho odlišil od livedo reticularis a vysvětlil patofyziologické děje v postižené kůži [4], terminologie dodnes není jednotná. Četné názvy, které různí autoři, učebnice, různé obory a lékařské slovníky používají v souvislosti s těmito kožními změnami (obzvláště používání obou termínů jako synonym) vede v literatuře k mnohým nejasnostem. V české, německé a francouzské literatuře název livedo reticularis (LR), pro které je používán jako synonymum termín cutis marmorata, označuje pravidelné mramorování kůže akrálních oblastí, zejména u dětí a u mladých žen, jako reakce na expozici chladu v důsledku funkční atonie venul a hypertonie arteriol v hlubokém dermálním a subkutánním plexu. Livedo racemosa (LRa) označuje síťovitě nepravidelné modravé zbarvení kůže, které má bleskovitě lomený průběh. Je tvořené přerušovanými „oky“ sítě, která jsou většího průměru, a bývá důležitým symptomem některých závažných onemocnění. V anglosaské literatuře se oba tyto klinické stavy shrnují pod širší název livedo reticularis. Ke kožním změnám se síťovitým uspořádáním náleží i retikulární nebo retiformní purpura, která se projevuje retikulárně uspořádanými petechiemi a ekchymózami [8]. K pochopení patofyziologických dějů v oblasti těchto kožních změn je nutno připomenout základní poznatky o cévním zásobení kůže.
KOŽNÍ VASKULARIZACE
Kožní vaskularizace se sestává z tepen a žil v podkoží, které tvoří hlubokou podkožní cévní pleteň (plexus subcutaneus). Z podkožní pleteně vybíhají arterioly, které v dolních partiích stratum reticulare koria, tvoří hluboký, subdermální plexus. Ze subdermálního plexu kolmo k povrchu vybíhají arterioly do koria, větví se k zásobování kožních adnex a subpapilárně přechází v povrchový, subpapilární plexus tvořený terminálními arteriolami. Z tohoto plexu vybíhají kapilární smyčky do jednotlivých papil koria, které ve vzestupné části tvoří kapilární arteriola větvící se do 6 kapilárních kliček a přecházející za ohybem kličky v kapilární venuly (obr. 1). Kapilární venuly ústí do žilního subapilárního plexu tvořeného postkapilárními venulami [13].
Obr. 1. Základní jednotka kožní vaskularizace ve tvaru šestiúhelníku (Modifikovano podle PARSI [14]) ![Základní jednotka kožní vaskularizace ve tvaru šestiúhelníku
(Modifikovano podle PARSI [14])](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/aa30b143ca48f19080c279d65fd539a2.jpg)
Podle Unnovy teorie o základní jednotce kožní vaskularizace (Paul Gerson Unna, 1896) zásobuje každá kapilární arteriola oblast kůže ve tvaru kužele, s nepravidelně okrouhlou či šestiúhelníkovou bazí na povrchu a do hloubky směřující špičkou obsahující přívodnou ascendentní kapilární arteriolu. Na periferii těchto šestiúhelníků se nacházejí arteriovenózní anastomózy. Větvení větších cév vytváří podobné obrácené kužely, jednotky cévního zásobení (tzv. angiosomy) obsahující ve vrcholu ascendentní arterioly dermální a subukutánní, které zásobují na povrchu okrsky tvořené příslušným počtem šestiúhelníkových bazí [13]. Vrcholy kapilárních smyček se nacházejí v blízkosti dermoepidermální junkce, vzdálené asi 100 µm od bazálních keratinocytů, které vyživují. V těchto místech se odehrává výměna látek a kyslíku, a jsou tak nejdistálnějším místem cévního systému, vystaveném kolísání zevní teploty. Každá kapilární arteriola obsahuje prekapilární sfinkter, který řídí průtok krve do kapilár. Když je sfinkter otevřený, krev proudí přes kapilární síť do venul, a při jeho uzavření se krev dostává přes arteriovenózní (AV) anastomózy přímo do terminálních venul. Kapilární kličky venuly jsou místem migrace krevních buněk do extravaskulárního prostoru a výměny látkové.
REGULACE KREVNÍHO ZÁSOBENÍ KŮŽE
Na rozdíl od svalů, kde průtok krve řídí lokální metabolické podmínky, průtok krve kůží řídí vegetativní nervová soustava. Sympatická noradrenergní vlákna vyvolávají vazokonstrikci a sympatická cholinergní vlákna způsobují vazodilataci prostřednictvím acetylcholinu a vazoaktivního intestinálního peptidu. AV anastomózy mají silnou muskulární stěnu převážně se sympatickou noradrenergní inervací. V normotermických podmínkách průtok krve kůží činí přibližně 5 % srdečního systolického objemu. Při přehřátí těla dochází k vazodilataci AV anastomóz, zvětšení krevního řečiště a průtok krve kůží dosahuje 8 l/min a může představovat až 60 % srdečního systolického objemu. Tím se zvětšuje plocha k odvádění tepla z těla. Při nízkých teplotách nebo při stresu vedou podněty z hypotalamu nebo nadledvin k vazokonstrikci v periferii a snižují průtok krve kůží až na 20–50 ml/min [13].
Rychlá dilatace žil, např. při obstrukci, vyvolává venoarteriální reflex (VAR). Je to reflexní vazospazmus odpovídající přívodné tepny, aby se snížil přívod krve do oblasti s přerušeným odvodem. VAR řídí sympatické vazokonstriktorní nervy. Žilní trombóza nebo rychlá injekce sklerotizující látky do žíly vyvolávají tento reflex. Následuje bledost kůže v postižené oblasti a poté reaktivní hyperémie, která se klinický manifestuje jako erytém. Při delším trvání obstrukce dochází ke vzniku nekrózy.
PATOFYZIOLOGIE KOŽNÍCH CÉV
V centru jednotek cévního zásobení (angiosomů) tvaru obrácených šestiúhelníkových kuželů převažuje arteriální část přivádějící okysličenou krev, na periférii převažuje descendentní žilní složka s odkysličenou krví. Velikost zásobeného okrsku kožního povrchu je podmíněna velikostí příslušných cév.
Patologické změny v oblasti kožních arterií nebo žil mají za následek změny v oblasti základní jednotky kožní vaskularizace. Okysličená krev proudí z kapilární arterioly směrem k periferii, kde je průtok pomalejší. Každé zpomalení průtoku, z důvodu stázy nebo vazodilatace, v oblasti kapilár a AV kapilárních anastomóz na periferii šestiúhelníků vede ke stagnaci odkysličené krve v těchto oblastech, což se projevuje vznikem lividních prstenců rozměrů daných velikostí postižených cév (obr. 2).
Obr. 2. Kožní vaskularizace a) pravidelná síť u livedo reticularis; b) nepravidelná síť u livedo racemosa; c) retiformní purpura (Modifikováno podle DOWD P. M. [3]) ![Kožní vaskularizace
a) pravidelná síť u livedo reticularis; b) nepravidelná síť u livedo racemosa; c) retiformní purpura
(Modifikováno podle DOWD P. M. [3])](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/12b842fd4dfe8a7fef2190b2a45760d1.jpg)
Pokud je patologický proces na úrovni retikulárních žil subdermálního plexu, jsou na kůži patrné větší venózní prstence podmíněné těmito žilami.
Patologický proces v oblasti postkapilárních venul se projevuje na kůži makulami a papulami. V případě vaskulitidy malých cév, zánětlivého postižení postkapilárních venul, dochází ke vzniku makulopapulozních lézí charakteru, tzv. „palpovatelné purpury“.
Okluzí nebo vazospasmem kapilární arterioly dochází k zblednutí kůže v centru šestiúhelníku. V případě spasmu dermálních arteriol dochází ke vzniku bledých drobných makul (Bierových makul viz níže). Okluzí centrálních arterií dochází ke vzniku koagulační nekrózy, infarktu, příslušného okrsku kožního povrchu. Uzávěr drobnějších a povrchovějších tepen má za následek nekrózu ve tvaru šestiúhelníku s následným jizvením charakteru bílé atrofie. Uzávěr větších a hlouběji uložených tepen vede ke vzniku multihexagonální, hvězdicovité nekrózy a posléze jizvy rozsahu podle průsvitu postižené cévy.
U livedo reticularis se jedná o rozsáhlé postižení krevního řečiště se zpomalením průtoku krve, nejčastěji vlivem chladu, a proto se manifestuje pravidelným, stejnoměrným síťovitým erytémem. Livedo racemosa vzniká v důsledku bodového, neúplného přerušení krevního proudu menšího počtu prstenců a projevuje se nepravidelně se větvícím síťovitým erytémem s přerušenými „oky“ (obr. 2, 3).
Obr. 3. Livedo racemosa: obrazce podobající se figurám blesku, „roztrhaná síť“ 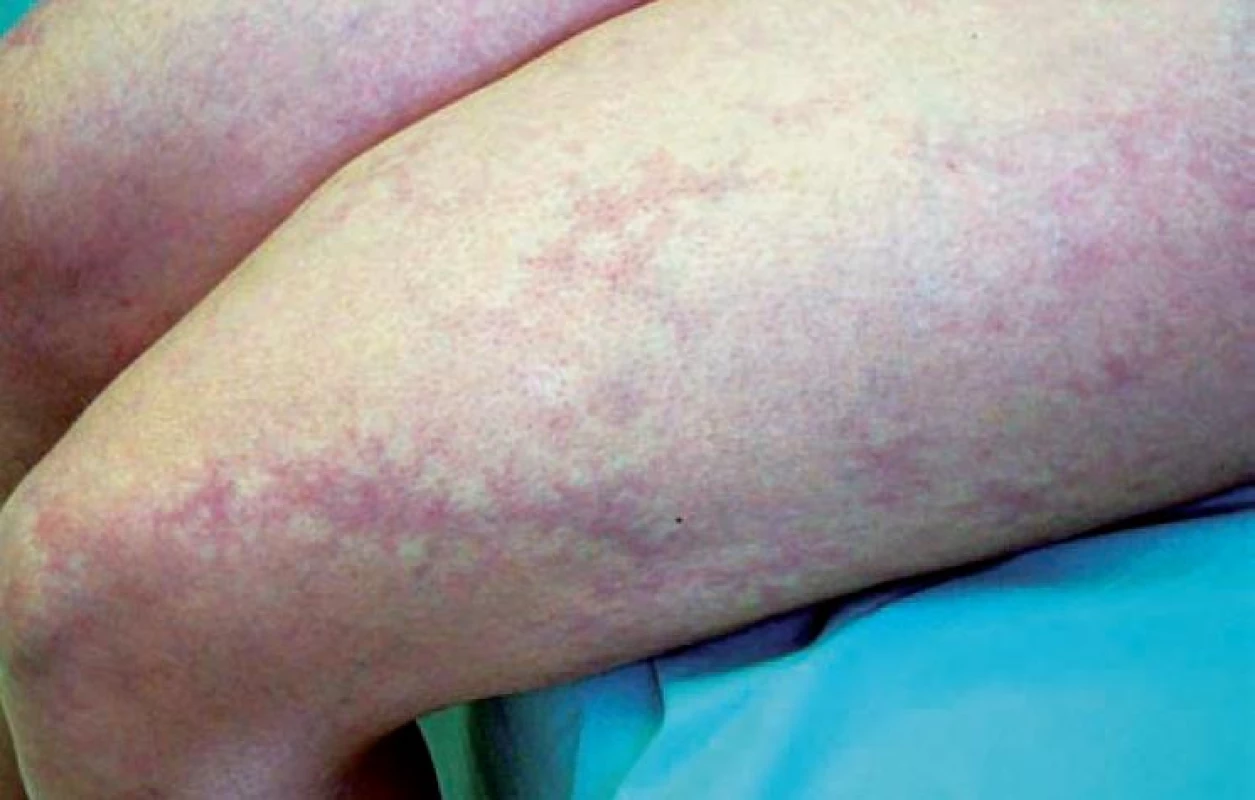
Retikulární, neboli retiformní purpura, je příznakem okluze s následnou hemoragií v oblasti drobných a středně velkých cév. Následné ukládání hemosiderinu nebo aktivace melanocytů vedou ke vzniku síťovitých pigmentací (obr. 2, 4).
Obr. 4. Livedo racemosa se síťovitou pigmentací 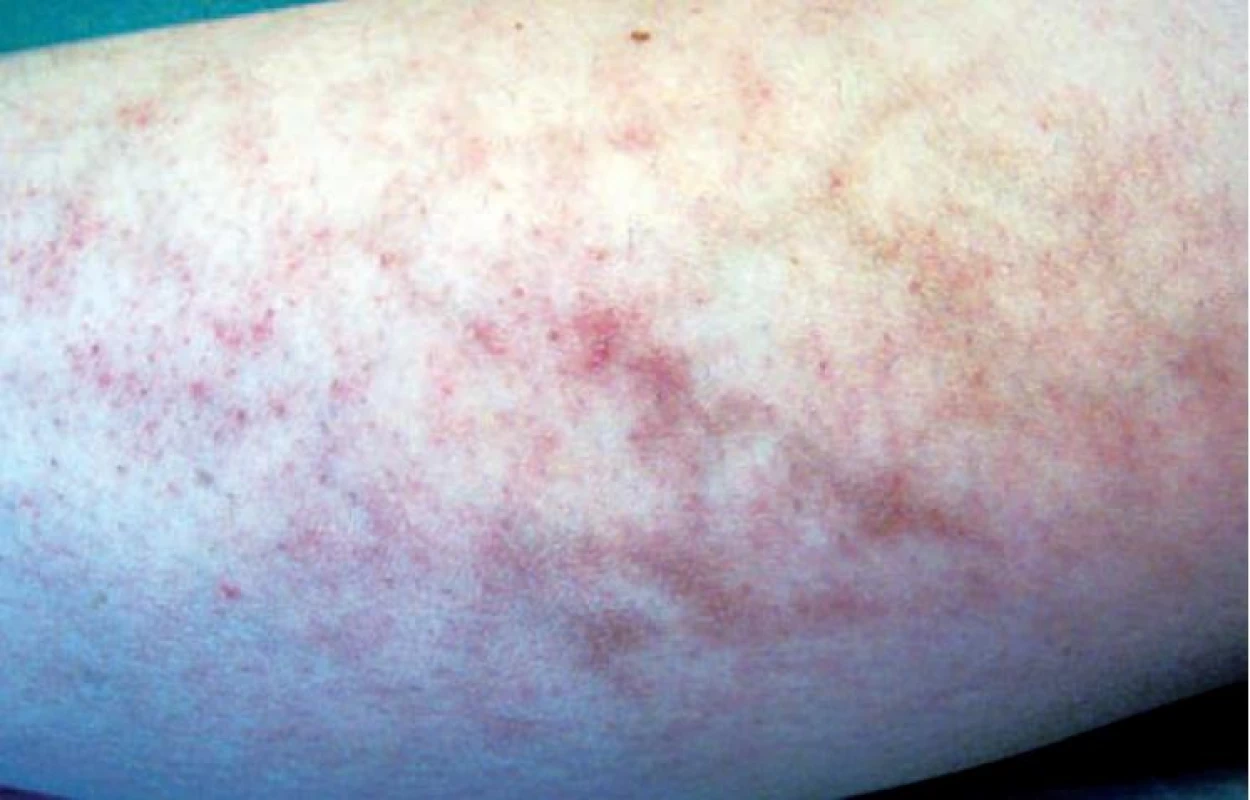
Nezánětlivá retikulární purpura, tzn. bez přítomnosti zánětlivého erytému, svědčí pro primární obliterační proces cévního lumen a okluzi drobných cév, zánětlivá retikulární purpura provázená časným výrazným erytémem ukazuje na vaskulitidu [14].
HISTOPATOLOGIE
K diagnóze u retikulárních projevů vede správně provedená biopsie, která musí zavzít i bledší centrum prstence lividního erytému [7, 14]. Biopsie z periferního lividního erytému u livedo racemosa je často nespecifická, protože modravé zabarvení je důsledkem reaktivní dilatace venul, a tak biopsie z toho místa, zpravidla neprokazuje patologický nález. Biopsie má být buď vřetenovitá velikosti 1–2 cm, nebo se doporučuje provést 2–3 biopsie průbojníkem průměru 4–5 mm zachycující podkožní tukovou tkáň [1, 11]. Většina autorů doporučuje provedení minimálně 3 biopsií z bledého centra síťovitého erytému (centrum livedo racemosa) [22]. Histologický nález záleží na vyvolávající příčině. V případě cutis marmorata a změn podmíněných dilatací či cévním spasmem je nález na cévách kůže bez patologie. Změny, zejména u livedo racemosa, mohou vznikat v důsledku vaskulitidy, kdy primární příčinou je zánět cévní stěny, či vaskulopatie, kde primární je proces obliterace cévního lumen [17] někdy následovaný v dalším průběhu sekundárními zánětlivými změnami s obrazem vaskulitidy [6]. Vaskulopatie vznikají v důsledku trombotizace (koagulopatie), embolizace (cholesterolová), depozit kalcia (calciphylaxis), intraluminální obliterace (monoklonální kryoglobulinémie), ukládání krystalů (oxalosis) aj.
U Sneddonova syndromu se v iniciální fázi se nachází lymfohistiocytární infiltrát a edém endotelových buněk (endothelitis), následovaný částečnou anebo kompletní okluzí lumen čepem z fibrinu, lymfocytů a histiocytů (obr. 5), po které do lumen cévy proliferují subendoteliální buňky a je přítomna dilatace kapilár v tunica adventicia postižené cévy. Pozdní fáze vykazuje fibrózu a retrakci postižené cévy [19].
Obr. 5. Livedo racemosa: organizované tromby s infiltrátem z lymfocytů a histiocytů (S laskavým schválením doc. MUDr. J. Feita, CSc., Ústav patologické anatomie FN brno) 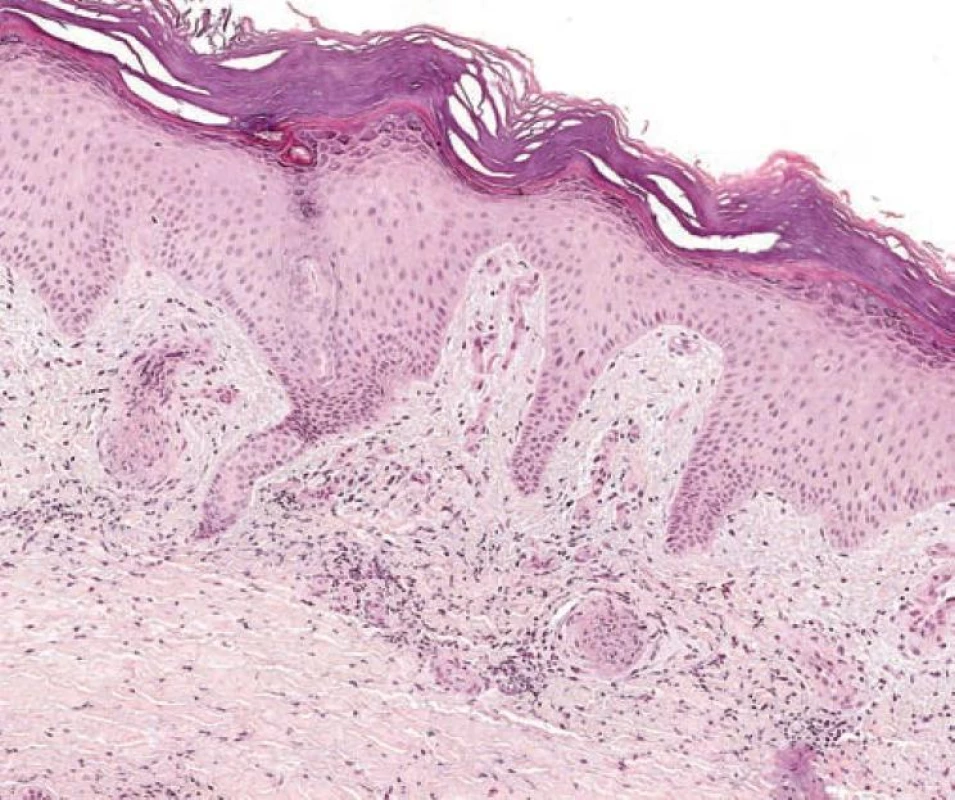
Livedo reticularis (LR)
Livedo reticularis, syn. cutis marmorata, je charakterizováno pravidelným síťovitým lividním erytémem, kde bledé makuly (oka sítě) jsou pravidelné a namodralé prstence (smyčky) stejnoměrné a nepřerušené. Při vitropresi a v teple nebo po tření kůže lividní erytém obvykle mizí, při expozici chladu se zvýrazňuje (tab. 1). Kožní změny jsou uspořádány symetricky, lokalizované nejčastěji na bércích a předloktích, kde může přecházet v často sdruženou akrocyanózu rukou, popř. na stehnech, pažích, hýždích a trupu. LR je podmíněno konstrikcí arteriol a žilní dilatací v hlubokých dermálních a podkožních cévách. Vyskytuje se až u 50 % dětí a mladých žen. Cutis marmorata v průběhu dospívání a s přibývajícím věkem zpravidla postupně vymizí. Někteří autoři podle patogeneze rozlišují 2 druhy LR, a to vazospastické a venokongestivní [14, 18].
Tab. 1. Diferenciální diagnóza livedo reticularis, livedo racemosa, retiformní purpury 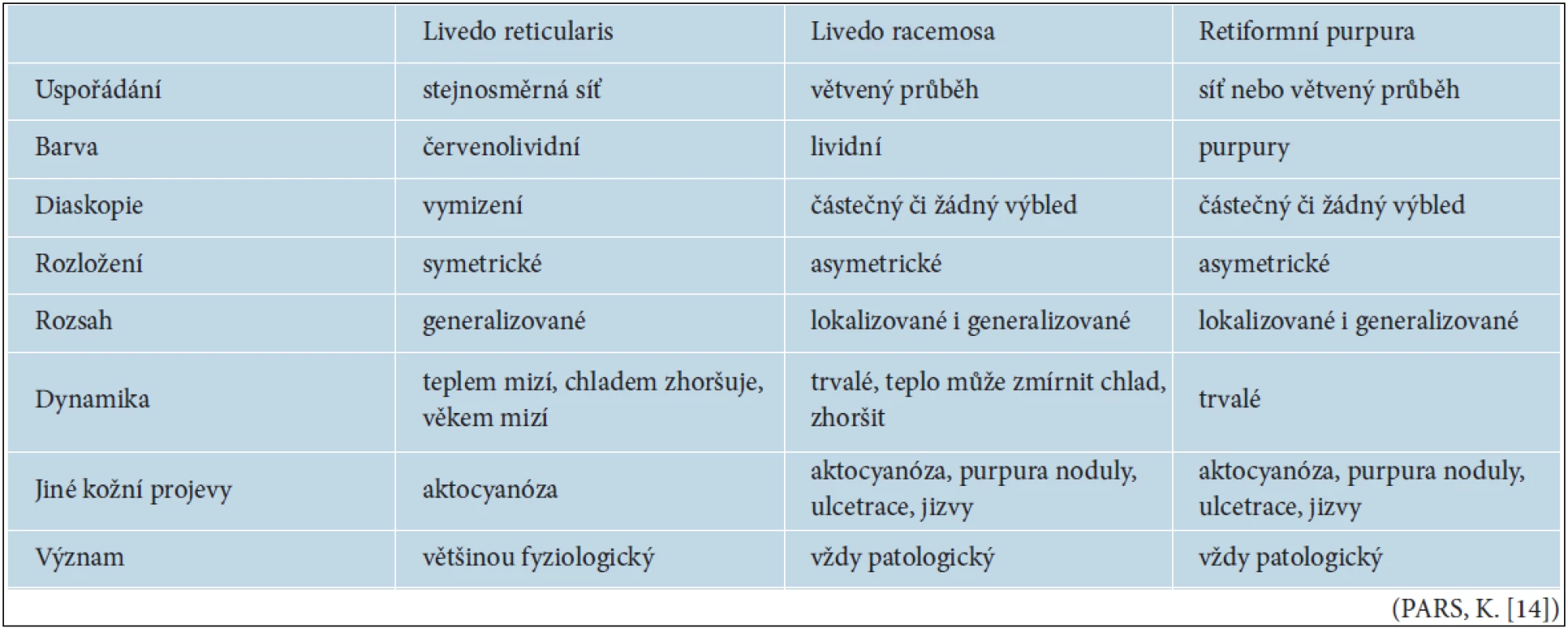
Vazospastické LR vzniká z důvodu nestability kožních vazomotorů a může být sdruženo s Raynaudovou nemocí, akrocyanózou, rosaceou, flushingem, emočním stresem, hyperhidrózou, bývá častější u kuřáků. Projevuje se jako „červenofialové zabarvení s okrskovitým probledáváním“ označované též jako pseudoleukodermaangiospasticum [18]. Bělavé okrsky na podkladě červenofialového erytému vznikají při vysokém tonusu v oblasti kožních arteriol a snížené perfuzi v periferii šestiúhelníku (obr. 6). Postižena bývají především akra, volární partie předloktí a hýždě. Změny obdobné pseudoleukoderma angiospasticum, označované jako Bierovy skvrny (syn. angiospastické makuly), se jeví jako mnohočetné bledé drobné makuly v červenofialovém pozadí v akrálních oblastech, nejčastěji na končetinách mladých osob (obr. 7). Tyto změny vznikají při venózní hyperémii během měření krevního tlaku či při svislé poloze končetin. Po odstranění manžety tonometru nebo elevaci končetiny dochází k vymizení těchto skvrn. Byly popsány i na trupu v souvislosti s těhotenstvím, kryglobulinémií, u pacienta se systémovou sklerodermií v průběhu renální krize [14, 15]. U těchto osob se pravděpodobně jedná o nadměrnou fyziologickou reakci na žilní hypertenzi provázenou vazokonstrikcí ascendentních arteriol v důsledku venoarteriálního reflexu.
Obr. 6. Pseudoleucoderma angiospasticum 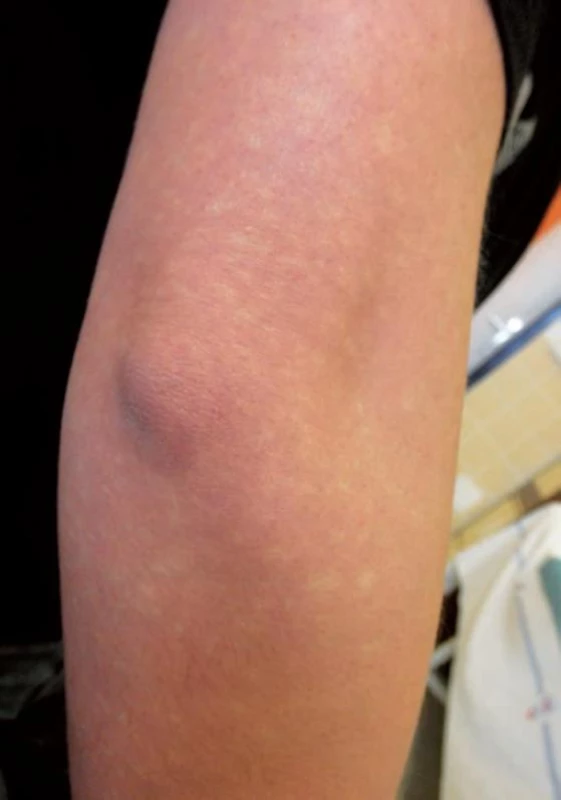
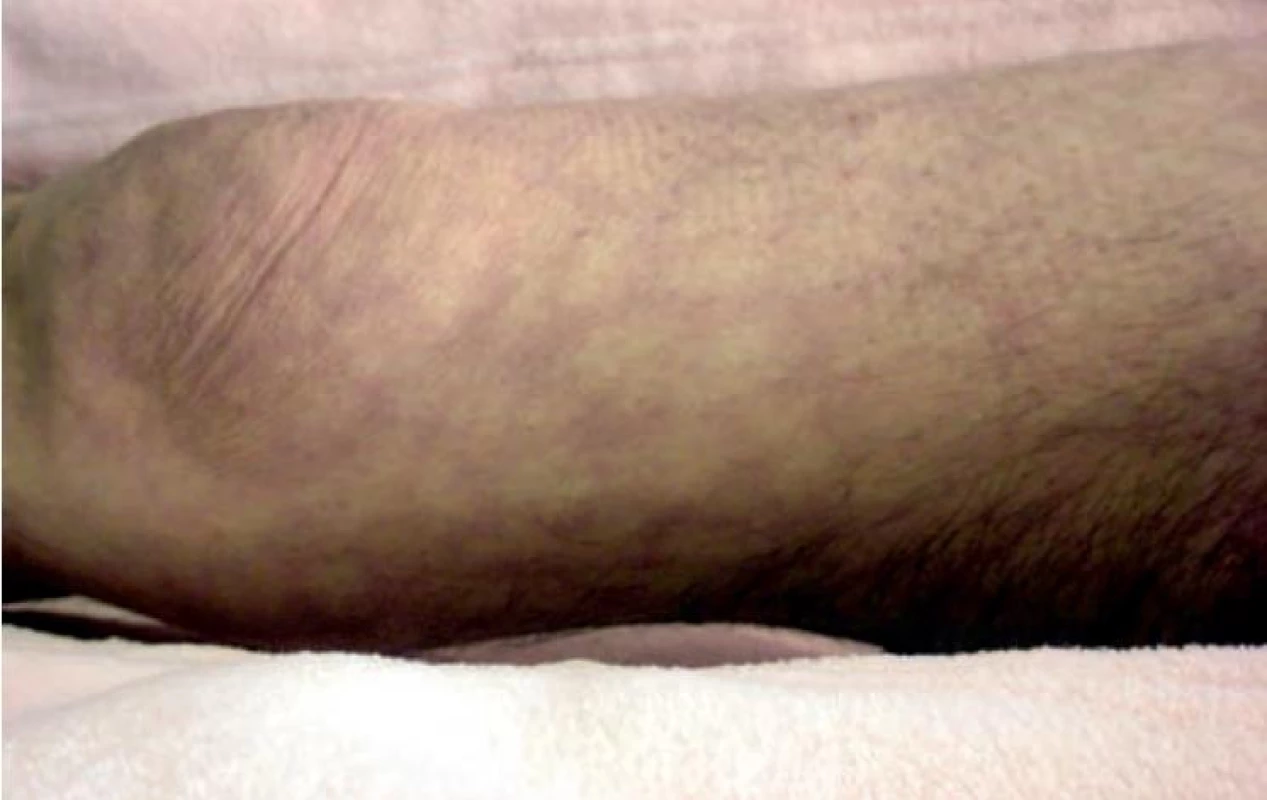
Venokongestivní LR vzniká z důvodu zpomaleného odtoku krve z kapilárního řečiště, představuje síťovité modravé zabarvení cutis marmorata (obr. 8). Příčiny městnání krve projevující se LR mohou provázet stavy z intravaskulárních příčin ovlivňující rhelogické vlastnosti krve obdobné jako u livedo racemosa (tab. 2), např. zvýšením krevní viskozity při kryoglobulinémii provázející infekci virem hepatitidy C. LR může být vyvoláno léky. Amantadinem (antiparkinsonikum, antivirotikum) vyvolané LR se vyskytuje u 2–28 % pacientů, kteří byli léčeni tímto lékem, a to častěji u žen [21]. Předpokládá se že amantadin vyvolává úbytek katecholaminů v oblasti periferních nervových zakončení, což vede k dilataci kožních venul. LR může provázet léčbu norepinefrinem, feochromocytom, karcinoid, endokrinní poruchy (hypthyreoidismus, Cushingův syndrom), pelagru, poruchy CNS (např. cévní mozkovou příhodu, roztroušenou sklerózu, Parkinosonovu chorobu) aj.
Obr. 8. Cutis marmorata: venózní prstence 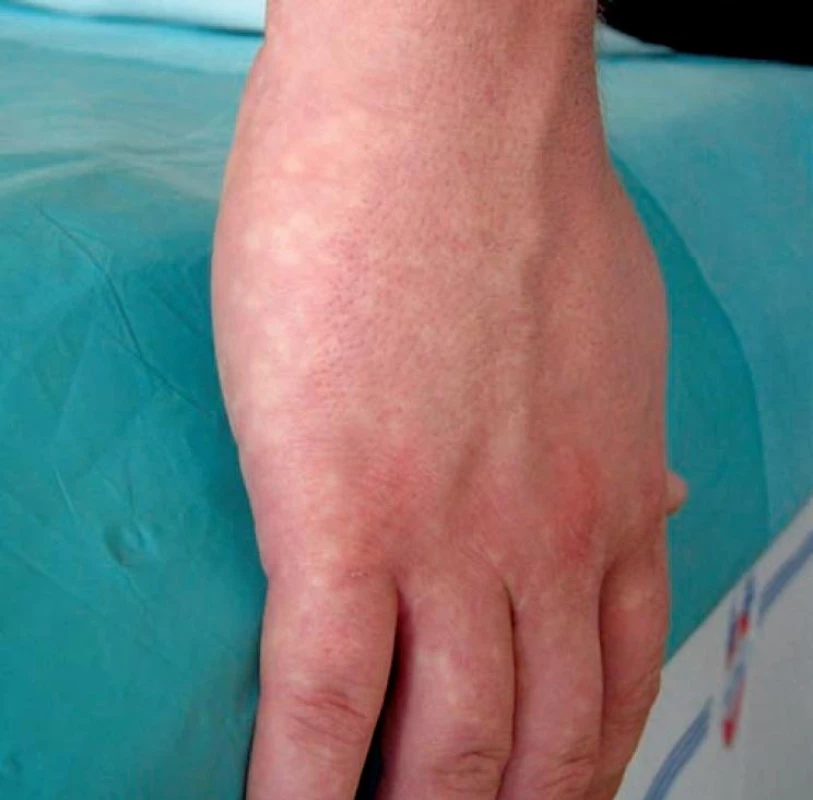
Tab. 2. Etiologie livedo racemosa 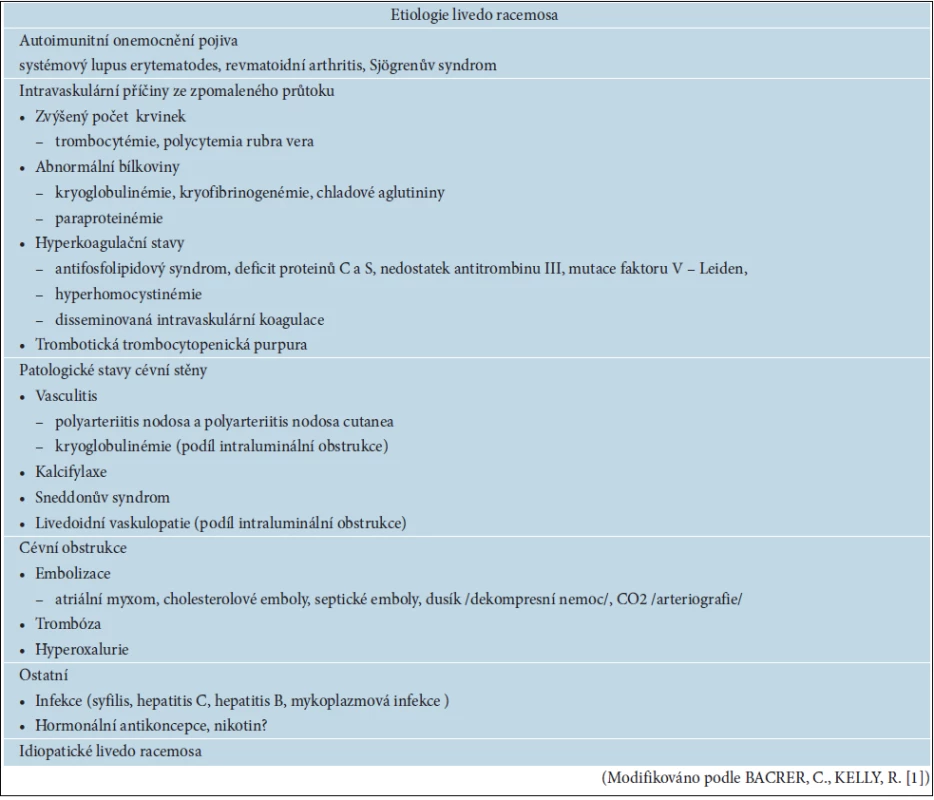
Kongenitální livedo reticularis, syn. cutis marmorata teleangiectatica congenita, je sporadická vrozená vývojová vada kožních cév. Retikulární růžový erytém postihuje nejčastěji dolní končetiny, většinou je lokalizovaný, může však postihovat i trup a horní končetiny. Může být přidružena atrofie kůže, tvorba ulcerací, kapilární a kavernózní hemangiomy a je nutno vyloučit eventuální jiné kongenitální malformace zahrnující kromě jiného glaukom, makrocefalii, abnormality kostní a neurologické. Prognóza nemocných je příznivá s výrazným zlepšením symptomatologie patrným během prvních dvou let života [7].
Livedo racemosa (LRa)
LRa je název pro nepravidelné, lividní erytémy ve tvaru rozvětveného stromu nebo obrazců blesku, který je projevem patologických změn v oblasti kožních cév. Termín livedo racemosa uvedl Ehrmann v r. 1907, odlišil ho od livedo reticularis a popsal, že jen částečně může mizet po vitropresi. Síťovitý erytém je hrubý, oka sítě jsou nepravidelná a smyčky přerušené (roztrhaná síť). Erytém je modrofialové barvy na rozdíl od livedo reticularis, kde je patrná příměs růžové barvy okysličené krve (tab. 1).
Z etiologického aspektu LRa může být idiopatické nebo častěji symptomatické (tab. 2). LRa se může projevovat pouze v určité oblasti nebo generalizovaně. Lokalizované formy LRa vyžadují stejně rozsáhlé vyšetření jako generalizované formy k upřesnění etiologie. Diagnóza idiopatického LRa se stanoví per exclusionem a vyžaduje dlouhodobé pravidelné sledování pacienta. Uvádíme některé klinické stavy spojené s projevem livedo racemosa.
Livedo vaskulopatie (LV)
Syn. livedo s letními ulceracemi, livedo vaskulitida, livedoidní vaskulitida, segmentální hyalinizující vaskulitida, PPURPLE („painful purpuric ulcers with reticular patterning of Low extremities“, bílá atrofie).
LV je trombotická vaskulopatie drobných cév dolních končetin, převážně v oblasti kotníků, kterou charakterizuje trias: livedo racemosa, bolestivé recidivující ulcerace a jizvy typu atrofie blanche [6]. Etiologicky se uvažuje o trombofilním stavu, individuální predispozici k tvorbě trombů s lokálními spouštějícími faktory. Onemocnění probíhá v atakách, jako provokující faktory se uvádějí: teplo, chlad, namáhavá dlouhá chůze, drobné úrazy v oblasti kotníků. Začíná otokem a bolestivostí kolem kotníků, a zvýrazněním kresby livedo racemosa, někdy i retiformní purpurou. Na jednom nebo více místech se během několika dní objevují hemoragické buly, po jejichž rozpadu vznikají extrémně bolestivé ischemické nebo hemoragicko-nekrotické ulcerace (obr. 9). Během několika týdnů dochází k demarkaci nekróz a pomalému hojení defektů během několika měsíců. Jizvy a bílá atrofie jsou porcelánově bílé, oválné, nebo nepravidelné ve tvaru šestiúhelníku (obr. 10). Zdá se, že atrofie blanche je výsledná změna po obstrukci a hyalinizaci drobných cév u různých onemocnění: chronické žilní insuficience, livedo vaskulopatie a papulosis maligna atrophicans Degos.
Obr. 9. Livedo vaskulopatie: livedo racemosa, retiformní purpura a hvězdicovité ulcerace s hemoragickými krustami 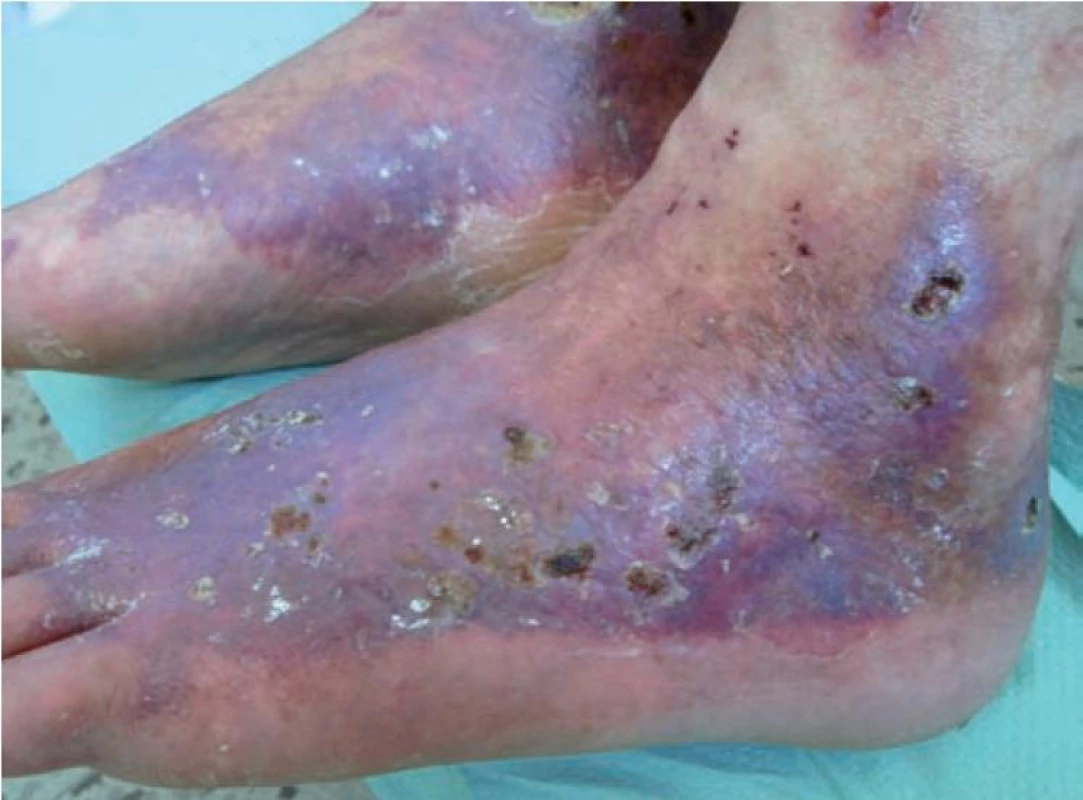
Obr. 10. bílá atrofie u pacientky s livedo vaskulopatií po zhojených ulceracích 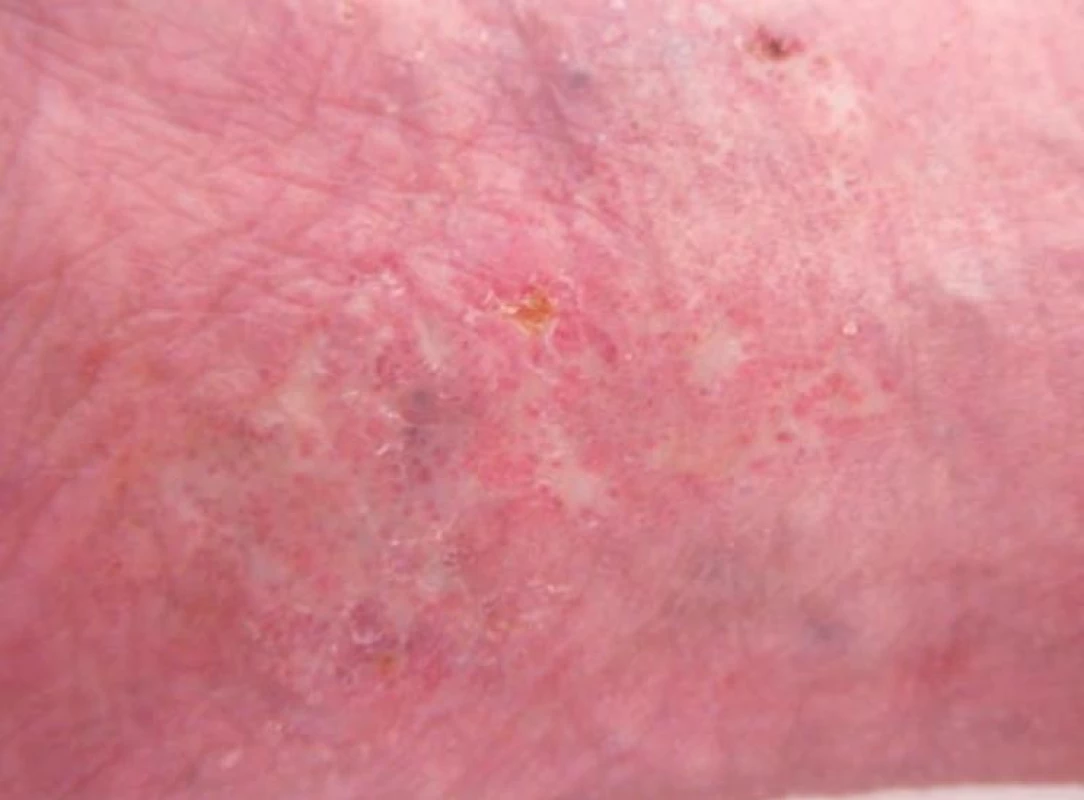
Histopatologicky se v akutních lézích na arteriích a venulách v oblasti horní a dolní dermis až po hranici s podkožní tkání nacházejí tromby z fibrinu, hemoragie a mírný perivaskulární infiltrát z lymfocytů a ojedinělých neutrofilů. V pozdějších stadiích dochází k reorganizaci trombotických čepů, subintimální proliferaci a hyalinizaci cévních stěn a dermis [17].
Embolia cutis medica mentosa
Onemocnění známé také jako livedo like dermatitis, poprvé popsal Nicolau v roce 1925 po injekci soli vizmutu v terapii syfilis. V literatuře se uvádí tato komplikace i po aplikaci jiných léků, např. penicilinu, steroidů, diklofenaku i očkovacích látek. Při intraarteriální nebo periarteriální injekci dochází ke spasmu arterie s následnou nekrózou kůže. Prvním příznakem je bledost postižené oblasti s následným cyanotickým livedo racemosa. Během několika dnů dochází k hemoragicko-nekrotickým změnám s následným vznikem příškvaru a ulcerace s cípatým okrajem.
Warfarinové nekrózy
Nekrózy kůže vyvolané warfarinem se vyskytují u pacientů s trombofilním stavem. Jsou to převažně obézní pacienti, a to perimenopauzální ženy od 1. do 10. dne po zavedení terapie warfarinem. Nejčastější lokalizací jsou prsa, stehna a gluteální oblast. Iniciální změnou je livedo racemosa, které rychle progreduje do purpurických změn s následnou nekrózou kůže.
Kalcifylaxe
Kalcifylaxe je porucha, která vede ke kalcifikaci medie a fibróze intimy kožních arteriol s následující trombotizací cév vede k ischemickým nekrózám kůže. Nejčastějí postihuje pacienty s terminálním renálním selháním. Projevuje se převážně v oblasti dolních končetin [9, 20].
Sneddonův syndrom (syn. Ehrmannův-Sneddonův syndrom)
Sneddonův syndrom je varianta generalizovaného livedo racemosa s ischemickými lézemi v cerebrovaskulárním systému a extracerebrálními trombózami arterií a žil (obr. 11) [10]. Livedo racemosa může i více let předcházet ostatním projevům. Incidence v populaci představuje 4 pacienty na 1 milion obyvatel ročně, postiženy jsou častěji ženy. Příznaky ze strany centrálního nervového systému jsou: tranzitorní ischemické ataky, apoplexie s hemiplegiemi a hemiparézy, epileptické záchvaty, psychoorganický syndrom, hemianopsie a vertigo. Etiologie onemocnění není známa, antikardiolipinové protilátky (ACLA) se nacházejí ve 20 % případů. Průběh je progresivní, stav pacienta se postupně zhoršuje v průběhu několika let, dochází k poškození srdce a ledvin. Histologický nález úspěšné biopsie z centra prstenců zahrnuje endoteliální zánět, následovaný myointimální hyperplazií s následnou okluzí lumen, fibrózou a rekanalizací postižených malých a středních cév (viz výše). Léčbu představuje především podávání aspirinu, v případě trombóz trvalá antikoagulace. Příznivější prognózu mají nemocní bez přítomnosti antifosfolipidových protilátek.
Obr. 11. Livedo racemosa generalisata 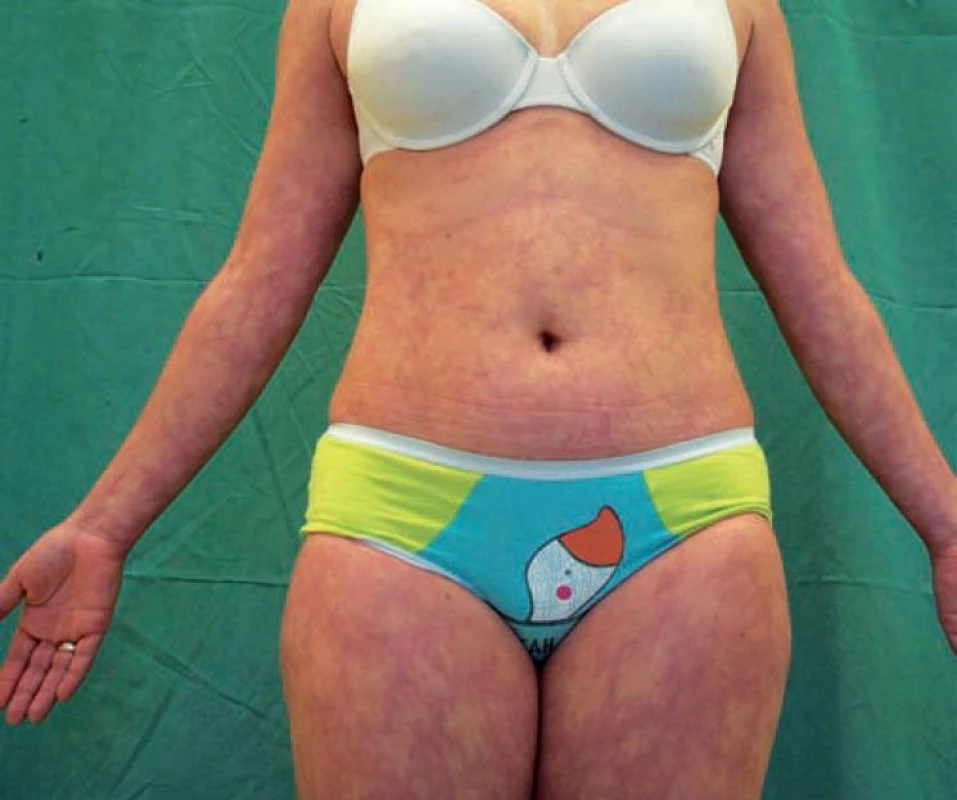
Infekční agens bylo prvním předpokládaným etiologickým faktorem u pacientů s livedo racemosa, a to u 2 pacientů se syfilis, které popsal Ehrmann 1907. Další infekce v souvislosti s výskytem LRa je tuberkulóza, v novější literatuře borelióza a infekce virem hepatitidy B a C. Je známo, že částice HCV a bílkoviny nukleokapsidy, které nemají obal, se podílejí na tvorbě imunokomplexů.
Vaskulitidy cév střední velikosti jsou charakterizovány depozity imunoglobulinů v cévních stěnách a intraluminálními depozity fibrinogenu a komplementu, což zpomaluje průtok krve a na kůži se objevuje LRa. Následně dochází k depozici fibrinu, obstrukci lumen čepem z fibrinu a trombocytů a extravazaci červených krvinek, což se projevuje retiformní purpurou.
Polyarteriitis nodosa (PAN) je systémová nekrotizující vaskulitida středních a drobných arterií. Celkové příznaky jako zvýšená teplota, celková slabost, malátnost, bolesti hlavy, myalgie a artralgie, obvykle předcházejí onemocnění delší dobu. Nejčastější je postižení ledvin v 70 % případů, dále periferního a centrálního nervového systému. U 1/3 pacientů se onemocnění projevuje polymorfními kožními změnami: LRa, ulceracemi, multiformními erytémy a panikulitidami.
Polyarteriitis nodosa cutanea benigna, syn. livedo s noduly, je nekrotizující polyarteriitis bez systémových projevů omezená jen na kůži s příznivou prognózou. Thrombangiitis obliterans, syn. endangiitis obliterans, morbus Winiwarter-Buerger, je zánětlivá okluzivní nemoc arterií dolních končetin u mladších mužů. Iniciálními změnami jsou zánětlivé změny intimy s proliferací endotelu a následnou tvorbou čepů z fibrinu a trombocytů, což postupně vede k arterioskleróze.
Antifosfolipidový syndrom je autoimunitní onemocnění, které se projevuje okluzí žil a/nebo tepen v kterémkoliv orgánu či tkáni a spontánními potraty po 10 týdnu gravidity. Laboratorně se prokazuje pozitivita alespoň jedné z následujících protilátek: lupus antikoagulans, antikardiolipinové protilátky a protilátky proti beta2 glykoproteinu 1, a to v minimálním časovém odstupu 12 týdnů mezi jednotlivými odběry [2, 12]. Tyto protilátky mohou stimulovat endotelové buňky k produkci prokoagulačních látek, jako jsou tkáňový faktor, inhibitor aktivátoru plasminogenu 1, endotelin, což vysvětluje trombózy v tepenném a žilním systému. LRa se vyskytuje u 17,5–40 % případů s antifosfolipidovým syndromem. Uthmann et al. ve studii u 52 pacientek s generalizovaným LRa zaznamenal potraty a jiné patologické stavy v 63 % případů [19].
Faktory zvyšující trombofilní stavy jako kouření a hormonální antikoncepce se nacházejí často u pacientů s livedo racemosa.
Diferenciální diagnóza
U lokalizovaného LRa vyloučit erythema ab igne. Síťovité erytémy se objevují i u jiných dermatóz, např. u retikulární erytematózní mucinózy (na trupu), při některých virových exantémech (erythema infectiosum), poikilodermie (mycosis fungoides, GVHD, dermatomyositis).
Doporučení pro praxi
Retikulární erytémy mohou být příznakem závažných, život ohrožujících onemocnění. LRa může ukazovat na zvýšené riziko opakovaných trombóz, proto je nutné náležité vyšetření a sledování nemocných s těmito příznaky [11]. Předpokladem je důkladná anamnéza rodinná a osobní cílená na příznaky trombotických a trombofilních stavů, systémových onemocnění pojiva, neurologické, postižení ledvin a jiných orgánových systémů. Musí být zvážen vliv podávaných léčiv, výkonů na cévách, předcházejících infekci včetně rizik hepatitidy C. Důležité je vyhodnocení kožních příznaků retikulárních erytémů, jejich trvání, dynamika, zhoršující faktory, lokalizace, dále přítomnost jiných kožních projevů, jako jsou ulcerace, noduly, purpura, které mohou směřovat k diagnóze vaskulitidy. Laboratorní vyšetření by mělo vycházet z anamnestických údajů a objektivního nálezu. U nemocných s retikulárním erytémem, který perzistuje a není vázán na chladovou expozici, by mělo být provedeno vyšetření na lupus antikogulant a antikardiolipinové protilátky [7]. Součástí vyšetření u perzistujících projevů by měla být kožní biopsie, která by měla zavzít jak periferní lividní prstenec, tak bledý střed prstence, případně provést biopsie vícečetné [7]. Některé laboratorní nálezy spojené s livedo racemosa jsou uvedeny v tabulce 3. U pacientů s LRa bez prokázaného etiologického faktoru a bez trombózy v anamnéze je nutno minimalizovat rizikové faktory (vysadit estrogenní hormonální antikoncepci, nekouřit, léčit případnou hypertenzi, hyperlipoproteinémii). U pacientů s pozitivními antifosfolipidovými protilátkami je možné zvážit aplikaci nízkých dávek kyseliny acetylsalicylové, i když jednoznačný účinek nebyl dosud prokázán [5]. U pacientů s trombózou v anamnéze je podávána dlouhodobá antikoagulační léčba.
Tab. 3. Některé laboratorní nálezy spojené s livedo racemosa 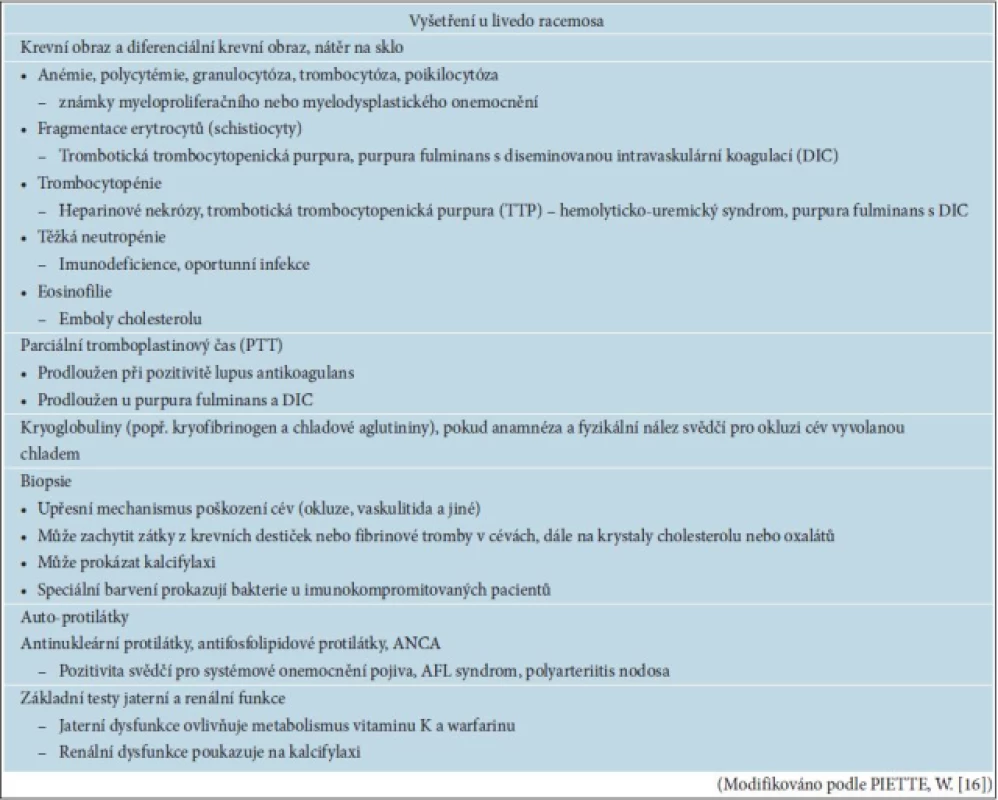
U všech pacientů s projevy LR a LRa je velmi důležitá správná diagnóza, důsledné sledování průběhu a časná léčba možných závažných komplikací.
Do redakce došlo dne 29. 10. 2012.
Kontaktní adresa
Dr. med. Milica Kovačevičová
Dermatovenerologická klinika FN Brno
Jihlavská 20
62500 Brno
e-mail: kmilica@seznam.cz
Zdroje
1. BAKER, C., KELLY, R. Other Vascular disorders. In Bolognia, J. et al. Dermatology. 2nd Ed. New York: Mosby Elsevier, 2008, p. 1615–1626, ISBN 9781416029991.
2. CETKOVSKÁ, P., PIZINGER, K., ŠTORK, J. Kožní změny u interních onemocnění. Praha: GradaPublishing, 2010, s. 101–103, ISBN 978 - 80 -247 - 1004 -4.
3. DOWD, P. M. Reactions to Cold in Rook´s Textbook in of Dermatology. 7th edition, Blackwell science 2004, s. 23.7–23.12, ISBN 0632064293.
4. EHRMANN, S. Ein neues Gefässymptom bei Lues. Wien. Med. Wochensch, 1907, 16, s. 777–782.
5. FRANCES, C. Dermatological manifestation of Hughes´antifosfolipidanti body syndrom. Lupus, 2010, 19, p. 1071–1077.
6. FRITSCH, P., ZELGER, B. Livedo-Vasculitis. Hautarzt, 1995, 46, s. 215–224.
7. GIBBS, M. B., ENGLISH, J. C., ZIRWAS, M. J. Livedo Reticularis: an up date. J. Amer. Acad. Dermatol., 2005, 52, p. 1009–1019.
8. HERRERO, C. Diagnosis and Treatment of Livedo Reticularis on the Legs. Actas Dermosifiliogr, 2008, 99, s. 598–607.
9. HORÁKOVÁ, M., POCK, L., BUREŠ, I. et al. Kalcifylaxe s kožními ulceracemi. Popis případu. Čes-slov. Derm., 2012, 3, s. 98–101.
10. KAUFMANN, R. Functional Angiopathies. In Burgdorf, W. H. C. et al. Braun-Falco’s Dermatology. 3rd Ed., SpringerVerlag, Heidelberg, 2009, p. 890–893.
10. MARTINEZ-VALLE, F., ORDI ROS, J. et al. Livedo racemosa as a marker of increased risk of recurrent thrombosis in patiens with negative anti-phospholipid antibodies. Med. Clin. (Barc), 2009, p. 767–771.
11. NYTROVÁ, P. Antifosfolipidový syndrom aneb syndrom, jenž může napodobit roztroušenou sklerózu. Neurol. Praxi, 2009, 10, 1, s. 54–57.
12. PARSI, K., PARTSCH, H., RABE, E. et al. Reticulate eruptions: Part 1. Vascular networks and physiology. Austr. J. Dermatol., 2011, 52, p. 159–166.
13. PARSI, K., PARTSCH, H. RABE, E. et al. Reticulate eruptions: Part 2. Historical perspectives, morphology, terminology and classification. Austr. J. Dermatol., 2011, 52, p. 257–244.
14. PEYROT, I. Bier’s white spots associated with scleroderma renal crisis. Clin. Exp. Dermatol., 2007, 32, 2, s. 165–167.
15. PIETTE, W. Cutaneous Manifestations of Microvascular occlusion Syndrome. In Bolognia, J. L. et al. Dermatology. 2nd Ed. New York: Mosby Elsevier, 2008, p. 331–345, ISBN 9781416029991.
16. STEIN, A. Histologie der kutanenVaskulitiden. Hautarzt, 2008, 59, s. 363–373.
17. ŠTORK, J. Choroby z poruch cirkulace. In Štork, J. et al. Dermatovenerologie. Praha: Galen 2008, s. 312–313, ISBN 978-80-7262-371-6.
18. UTHMANN, I. W. Livedo racemosa: A striking Dermatological Sign for the Antiphospholipid Syndrome. J. Rheumatol., 2006, 33, 12, s. 2379–2382.
19. VAŠKŮ, V., VAŠKŮ, J. The development of the pathophysiological concept of calciphylaxis in experiment and clinic. Pathophysiology, 2001, 7, 4, p. 231–244.
20. VOLLUM, D. I. Livedo Reticularis during Amantadine Treatment. BMJ, 1971, 2, s. 627–628.
21. WORLAB, J. Diagnostic impact and sensitivity of skin biopsies in Sneddon’s syndrome. A report of 15 cases. Br. J. Dermatol., 2001, 145, s. 285–288.
Štítky
Dermatologie Dětská dermatologie
Článek vyšel v časopiseČesko-slovenská dermatologie
Nejčtenější tento týden
2012 Číslo 6- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
- Condylomata accuminata a jejich prevence i léčba
- Miniinvazivní léčba pilonidálního sinu: laserová a podtlaková terapie jako šetrná a účinná modalita
- Proces hojení ran krok za krokem a co ho může zkomplikovat
- HydroCleanem efektivně hojíme onkologické rány po radioterapii
-
Všechny články tohoto čísla
- Retikulární exantémy – patofyziologie, etiopatogeneze, klasifikace
- Doškolování lékařů – kontrolní test
- Individualizovaná farmakoterapie ložiskové psoriázy perorálním metotrexátem: fikce nebo reálná možnost?
- Syndrom ochablého víčka vedoucí k diagnóze těžké spánkové apnoe
-
Tuberculosis verrucosa cutis –
popis případu - Klinický případ: Papulózní exantém trupu s pozitivním Darierovým příznakem
- Pigmentovaná varianta keratosis actinica a lentigo maligna – lze je dermatoskopicky rozlišit?
-
Zápis ze schůze výboru ČDS
Praha 13. září 2012 -
Zápisnica zo zasadnutia výboru SDVS
Malá zasadačka FN Nitra, Nitra 26. 5. 2012 - 6. konference akné a obličejové dermatózy
- Odborné akce 2013
- Rejstřík
- Česko-slovenská dermatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Retikulární exantémy – patofyziologie, etiopatogeneze, klasifikace
- Syndrom ochablého víčka vedoucí k diagnóze těžké spánkové apnoe
-
Tuberculosis verrucosa cutis –
popis případu - Pigmentovaná varianta keratosis actinica a lentigo maligna – lze je dermatoskopicky rozlišit?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání