-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Kožné imunologicky mediované nežiaduce účinky indukované anti-TNF alfa terapeuticky zvládnuté zmenou liečby za ustekinumab
Anti-TNF alpha-induced immune-mediated skin adverse reactions resolved by switching to ustekinumab
Immune-mediated adverse reactions are a new group of conditions that develop during anti-TNF-alpha treatment. Their etiopathogenesis remains unclear. This study describes three forms of immune-mediated adverse reactions of the skin that were diagnosed correctly. Some types of immune-mediated adverse reactions, such as palmoplantar pustular psoriasis, may persist for a long time after switching biologic agents.
Submitted: 19. 9. 2019
Accepted: 17. 11. 2019
Conflict of Interest: The authors declare that the article/ manuscript complies with ethical standards, patient anonymity has been respected, and they state that they have no financial, advisory or other commercial interests in relation to the subject matter.
Publication Ethics: This article/ manuscript has not been published or is currently being submitted for another review. The authors agree to publish their name and e-mail in the published article/ manuscript.
Dedication: This manuscript was created with the support of Johnson & Johnson Ltd., Janssen Division, EM-18429.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for bio medical papers.
Keywords:
ustekinumab – cutaneous adverse effects – anti-TNF-alpha
Autoři: Vorčáková K. 1; Horáková M. 2; Péč J. 1
Působiště autorů: Dermatovenerologická klinika JLF UK a UN Martin 1; Gastroenterologická klinika JLF UK a UN Martin 2
Vyšlo v časopise: Gastroent Hepatol 2019; 73(6): 496-500
Kategorie: IBD: Kazuistika
doi: https://doi.org/10.14735/amgh2019469Souhrn
Imunologicky mediované reakcie sú novou skupinou ochorení, ktoré ako prvé vznikli v priebehu anti-TNF-alfa liečby. Presná etiopatogenéza prejavov nie je známa. V práci prezentujeme kazuistiku pacientky, u ktorej vznikli tri rôzne formy kožných imunologicky mediovaných nežiadúcich prejavov súčasne. Tie nás viedli k správnej diagnóze. V práci rovnako upozorňujeme na fakt, že určité formy imunologicky mediovaných reakcií ako palmoplantárna pustulózna psoriáza môžu byť aktívne dlhší čas po zmene biologickej liečby.
Klíčová slova:
kožné nežiaduce účinky – anti-TNF-alfa – ustekinumab
Úvod
Biologická liečba sa stala v posledných rokoch revolučnou terapeutickou modalitou v liečbe chronických zápalových ochorení. Užívanie anti tumor nekrotizujúci faktor alfa (anti-TNF-α) preparátov so sebou prinieslo nielen nové efektívne možnosti terapie, ale aj spektrum nových nežiaducich udalostí. Kožné komplikácie patria k jedným z najčastejších. Andrade et al prezentovali sledovanie kožných nežiaducich účinkov u 732 pacientov s nešpecifickým črevným zápalovým ochorením (IBD – inflammatory bowel disease) počas užívania biologickej liečby skupiny anti-TNF-α v období 10 rokov. Práca dokázala, že až u 29 % pacientov sa rozvinul min. jeden kožný nežiaduci účinok [1]. Kožné nežiaduce účinky môžeme rozdeliť do štyroch skupín:
- I. kožné infekcie;
- II.reakcie priamo súvisiace s podaním liečby;
- III. imunologicky mediované ochorenia;
- IV. kožné malignity.
Imunologicky mediované reakcie sú novou skupinou ochorení. V roku 2004 bol publikovaný prvý prípad psoriaziformnej reakcie indukovanej infliximabom u pacienta s Crohnovou chorobou (CD – Crohn’s disease) [2]. Pre indikáciu anti-TNF-α inhibítorov v liečbe psoriázy sa pre uvedené reakcie užíva aj pojem paradoxná psoriáza [3]. Medzi ďalšie imunologicky mediované reakcie patria: vaskulitída, hidradenitis suppurativa, alopécia areata, sarkoidóza kože, dermatomyozitída, morfea, pyoderma gangrenosum, lichen ruber planus. V posledných rokoch sa v klinickej praxi stretávame aj s výskytom dvoch a viacerých imunologicky mediovaných nežiaducich účinkov súčasne u jedného pacienta. Tieto reakcie sú dôležitým diagnostických kritériom a môžu nám napomôcť pri správnej diagnostike ochorenia [4].
Kazuistika
63ročná pacientka s 20 ročnou anamnézou CD, s intoleranciou vysokých dávok kortikosteroidov a azathioprínu bola od 06/2018 nastavená na biologickú liečbu adalimumabom. Jedná sa o CD, postihnutie hrubého čreva (sigma, descendens a transversum). V osobnej anamnéze pacientky nachádzame poliekovú hepatálnu léziu, stav po prekonaní femoropopliteálnej trombózy, na základe ktorej bola následne diagnostikovaná rezistencia na aktivovaný proteín C, mutácia FV Leiden heterozygotná forma, hyperhomocysteinémia stredne ťažkého stupňa (polymorfizmus MTHFR C677T) heterozygótna forma. Pacientka bola sledovaná psychiatrom pre depresívny syndróm, ktorý bol zvýraznený pri liečbe vysokými dávkami kortikoidov. V 9/2018 na odporúčanie gastroenterológa konzultovaná na kožnej klinike Univerzitnej nemocnice v Martine (UNM) pre drobný papulózny výsev za účelom prehodnotenia kožného nálezu. Pacientka ešte pred návštevou našej ambulancie konzultovala dermatológa v spáde, ktorý hodnotil kožný nález ako možný rozvoj vaskulitických prejavov, bez indikácie systémovej a lokálnej liečby. Pri vyšetrení na našej ambulancii 25. 9. 2018 kožný v trvaní viac ako týždeň. Pacientka neuvádzala výskyt psoriázy v rodine. Pri klinickom vyšetrení na našej ambulancii bola v oblasti trupu a na stehnách prítomnosť drobných erytematoskvamóznych papúl. Šupinatenie lézií klinicky vylúčilo vaskulitídu a nález imponoval ako guttátna forma psoriázy. Pacientka mala v uvedenom čase novotvorbu hrubých šupín v kapilíciu. V oblasti dlaní sa začali vytvárať drobné erytematózne papulky. Stav bol hodnotený ako paradoxná guttátna psoriáza s prejavmi v kapilíciu, s incipientnou palmoplantárnou pustulóznou psoriázou v oblasti dlaní. V podpazuší boli prítomné prejavy folikulitídy. Uvedený nález potvrdil rozvoj liekovej reakcie s prejavmi paradoxnej hidradenitis suppurativa (obr. 1). Črevný nález bol v uvedom období stabilizovaný po 3mesačnej liečbe adalimumabom, posledná dávka adalimumabu bola podaná 21. 9. 2018. Liečbu adalimumabom sme spočiatku len dočasne prerušili a s ohľadom na drobné guttátne prejavy odporúčali zahájenie liečby UVB 311 3× týždenne. V lokálnej liečbe boli indikované emolienciá a kortikosteroidy v dňoch, kedy nebola podávaná fototerapia. V danom období bol realizovaný odber autoimunitných protilátok, ktoré boli kompletne negatívne. Pre rýchlu progresiu kožných prejavov sme sa po dohode s gastroenterológom rozhodli o definitívne ukončenie liečby adalimumabom a indikovali sme liečbu preparátom ustekinumab (obr. 2). Ustekinumab bol u pacientky zahájený 31. 10. 2018 v dávke 390 mg intravenózně spolu s podaním hydrokortizonu 100 mg, následne liečba pokračovala v dávke 90 mg subkutánně v intervale každých 8 týždňov. V celkovej liečbe pokračoval mesalazín 2 g ráno a nadroparín pre trombofilný stav. Kožný nález po mesiaci liečby ustekinumabom viedol ku výraznej regresii prejavov na trupe, v kapilíciu a v oblasti podpazušia, pretrvávali prejavy len na dlaniach (obr. 3). Napriek tomu, že prejavy na dlaniach boli v 10. týždni liečby ustekinumabom kompletne sanované, v 11. týždni došlo ešte k novému ataku palmoplantárnych pustulóznych prejavov. Pacientka v danom období začala udávať väčšie bolesti kĺbov, ktoré môžu s uvedenou reakciou súvisieť. Kontrolné kolonoskopické vyšetrenie 3/2019 bolo s nálezom: kolonoskopia úspešná do lienálnej flexury, oralnejšie sa pre fixáciu čreva nepodarilo prejsť. Zistená deformácia sigmy a descendens, s jazvami po zhojených vredoch, bez aktívnych zápalových lézií, afty ani ulcerácie nenachádzame. Nález magnetické rezonančné (MR) enterografie z 4/2019: CD, chronické zápalové zmeny c. transversum, c. descendens a c. sigmoideum. Ileocekálna oblasť a tenké črevo bez jednoznačnej patológie.
Obr. 1. A – Prejavy guttátnej psoriázy; B – prejavy hidradenitis suppurativa; C – začiatok vzniku palmoplantárnej pustulózy (25. 9. 2018).
Fig. 1. A – Guttate psoriasis; B – manifestations of hidradenitis suppurativa; C – the onset of palmoplantar pustulosis (25th of September 2018).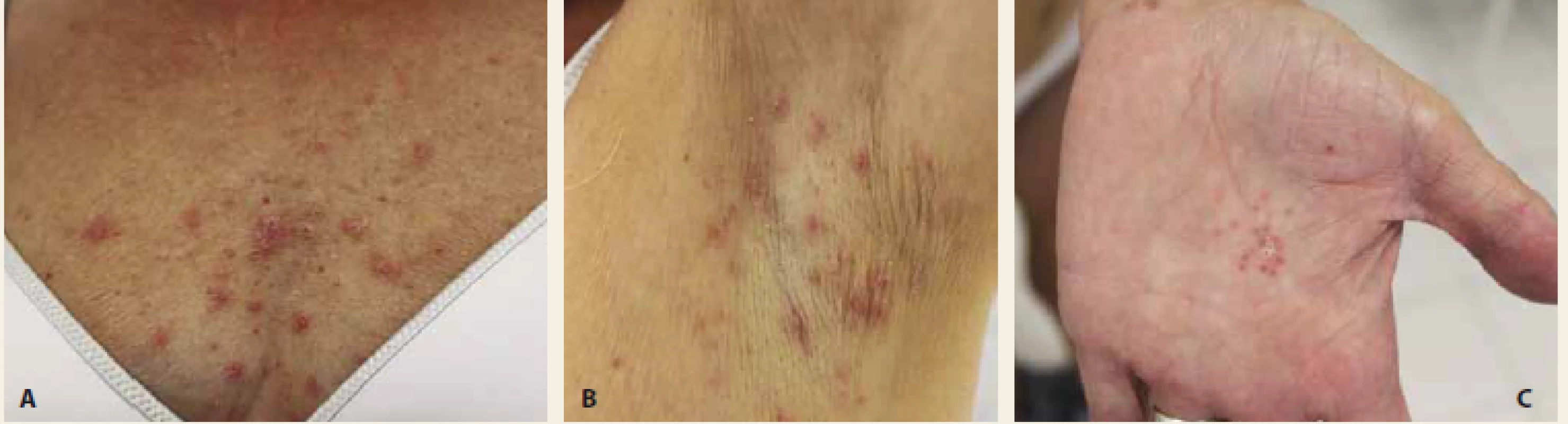
Obr. 2. A – Prejavy guttátnej psoriázy; B – prejavy hidradenitis suppurativa; C – palmoplantárna pustulózna psoriáza (18. 10. 2018).
Fig. 2. A – Guttate psoriasis; B – manifestations of hidradenitis suppurativa; C – palmoplantar pustular psoriasis (18th of October 2018).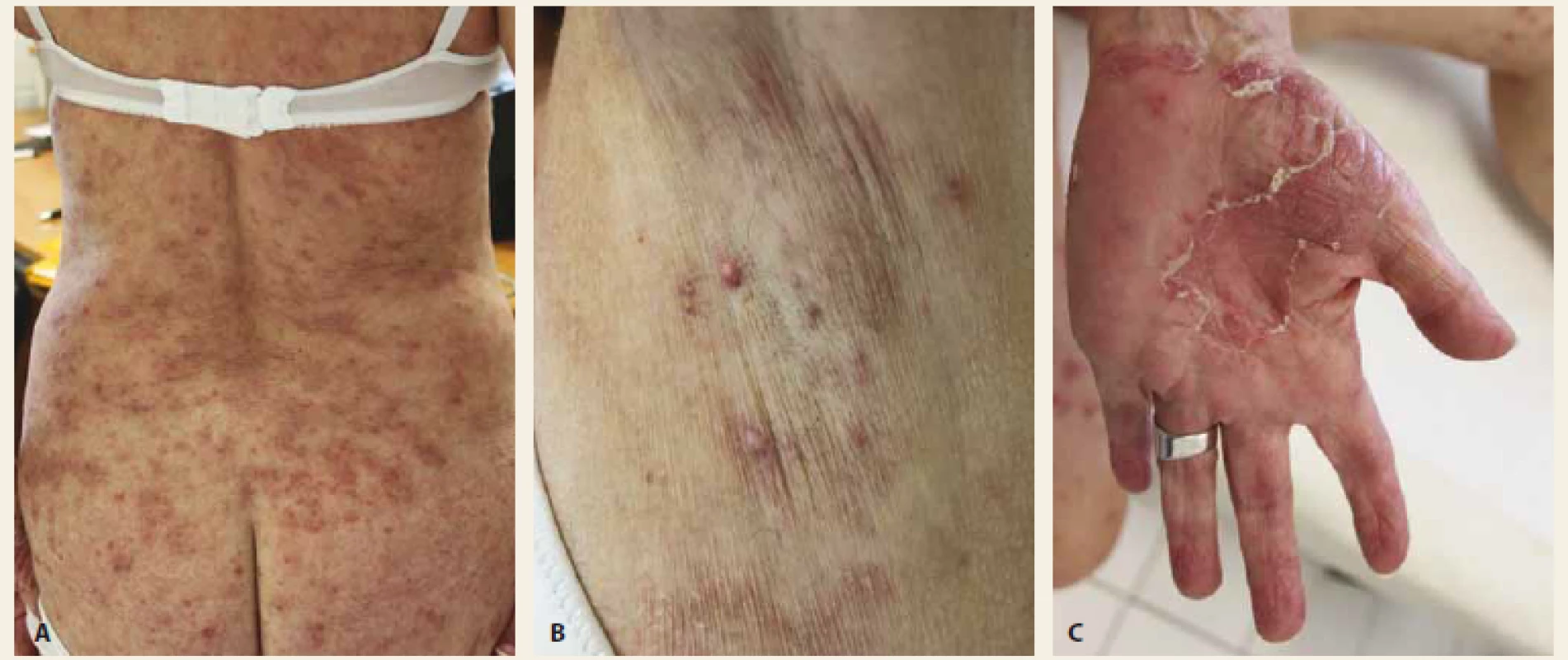
Obr. 3. Kožný nález bez prejavov guttátnej psoriázy, prejavy hidradenitis suppurativa takmer v kompletnej regresii, pretrváva palmoplantárna pustulóza (C) 27. 11. 2018.
Fig. 3. Skin finding without guttate psoriasis, hidradenitis suppurativa almost complete regression, palmoplantar pustulosis persists (C) 27th of November.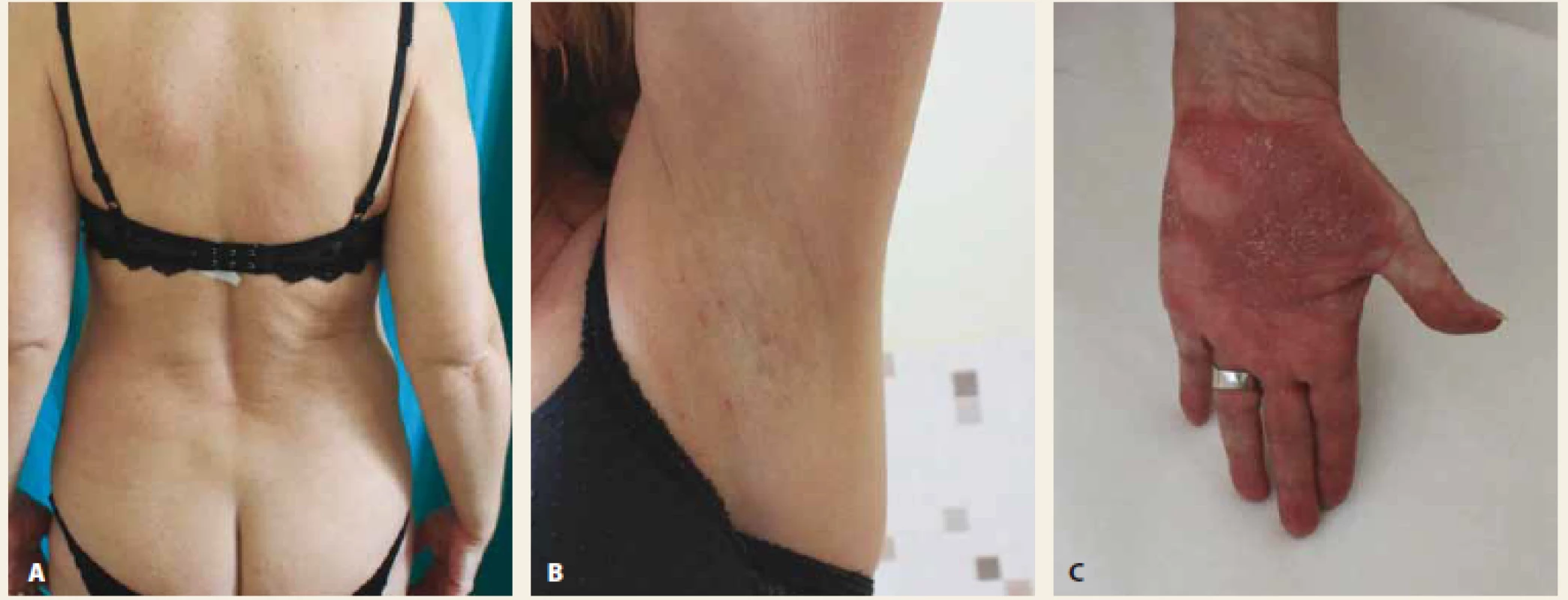
Kožný nález od 10 týždňa od zahájenia liečby ustekinumabom boli prejavy guttátnej psoriázy a hidradenitídy v kompletnej remisii. Prejavy palmoplantárnej pustulózy v oblasti dlaní a chodidiel pretrvávali v miernej aktivite až do obdobia 6/2019. U pacientky nebola pridávaná iná systémová liečba okrem ustekinumabu, v lokálnej liečbe si pacientka aplikovala kortikosteroidne externá a emolienciá. Kožné zmeny na dlaniach a rovnako aj na ploskách boli v období 6/2019 v kompletnej remisii (obr. 4). U pacientky v danom období naďalej pretrvávali artralgie.
Obr. 4. Kompletná regresia aj prejavov palmoplantárnej pustulózy 12. 6. 2018.
Fig. 4. Complete regression and manifestations of palmoplantar pustulosis 12th of June 2018.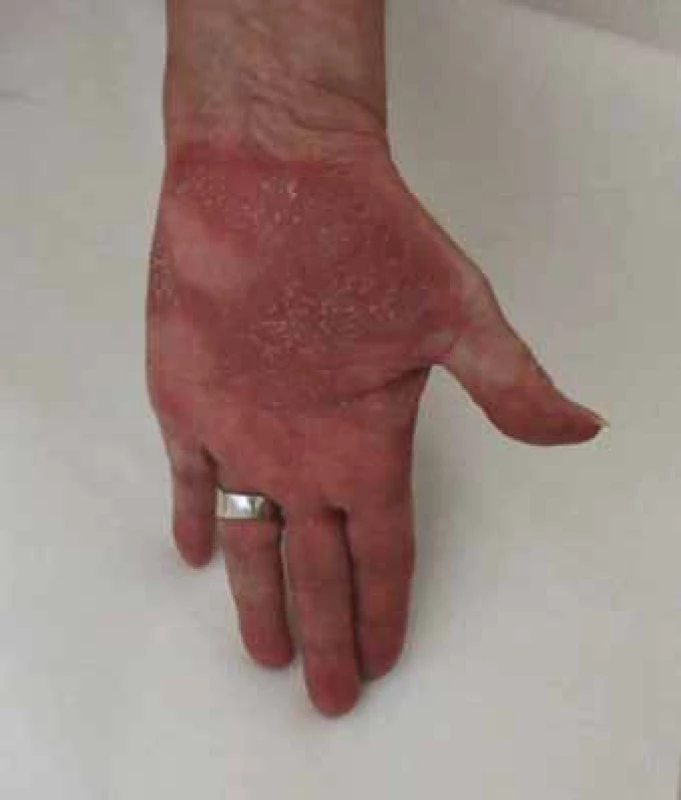
Diskusia
Podľa literárnych údajov je výskyt paradoxnej psoriázy 1,04–3,0 prípady na 1 000 paciento-rokov, percentuálne sa ich výskyt pohybuje v širokom rozmedzí od 0,6–5,3 % [5]. Klinický obraz ochorenia však nemusí byť jednoznačný a zvyčajne má iné charakteristické prejavy ako klasická chronická ložisková psoriáza. Klinická manifestácia ochorenia paradoxnej psoriázy môže mať variabilný charakter. Za paradoxnú psoriázu sa považuje nielen de novo vzniknutá psoriáza, ale aj radikálne zhoršenie už existujúcej psoriázy. Ochorenie sa prejavuje najčastejšie v oblastiach dlaní a stupají vo forme palmoplantárnej pustulózy, ktorá sa uvádza až v 56 % prípadov. Medzi ďalšie najčastejšie formy ochorenia patria chronická ložisková forma u 50 % pacientov a guttátne prejavy u 12 % pacientov. Pacienti môžu mať súčasne aj viaceré formy ochorenia (15 %) [6]. Výskyt palmoplantárnej pustulóznej psoriázy v bežnej populácii psoriatikov je výrazne nižší –1,7 % v porovnaní so 46,2–56 % výskytom u pacientov s paradoxnou reakciou [6]. Ako sme uviedli, aj u našej pacientky sa objavili ako prvé prejavy palmoplantárnej pustulózy a guttátne prejavy chronickej ložiskovej psoriázy, ktoré sú klinicky hodnotené ako dve formy ochorenia, rovnako sa v danom období rozvinula imnunologicky mediovaná reakcia hidradenitis suppurativa. Aj keď hidradenitis suppurativa rovnako ako psoriáza patrí do skupiny asociovaných ochorení s IBD [7], simultánny vznik guttátnej palmoplantárnej psoriázy, psoriázy v kapilíciu a hidradenitis suppurativa nás jednoznačne viedol k názoru, že prejavy boli indukované anti-TNF-α liečbou. Terapeutický postup je individuálny, nutné je zohľadniť komorbidity a závažnosť kožných prejavov. V prípade IBD pacientov s kompletnou remisiou ochorenia sa snažíme udržať biologickú liečbu čo najdlhšie. V prípade psoriázy je možné v prvej línii zahájenie fototerapie a lokálnej liečby, v druhej línii môžeme pridať kombinovanú imunosupresívnu liečbu (metotrexát, acitretín alebo cyklosporín), ktoré môžu ochorenie stabilizovať. V prípade našej pacientky bola kombinovaná imunosupresia kontraindikovaná s ohľadom na poliekovú hepatopatiu. Dôležitý je aj rozsah ložísk, lokalizácia a celková závažnosť prejavov. Pri paradoxných psoriaziformných reakciách môžu byť elevované izolovane anti-ds DNA, ktoré sme v prípade našej pacientky nedetegovali [8]. Ustekinumab je plne humánna monoklonová protilátka IgG1 proti interleukínu (IL) -12/23, ktorá vzniká v myších myelómových bunkových líniách použitím rekombinovanej DNA technológie. Liečbu ustekinumabom sme u našej pacientky volili z dôvodu, že ustekinumab je indikovaný nielen na liečbu CD, ale aj na liečbu chronickej ložiskovej psoriázy, len v rozdielnom dávkovacom režime. Dôležitým faktom z klinického hľadiska je, že kožné zmeny nemusia ustúpiť hneď po zahájení novej liečby. V prípade palmoplantárnej pustulózy sa nové ataky prejavov u našej pacientky vyskytli ešte aj v 11. týždni liečby ustekinumabom, aj keď chronická ložisková forma ochorenia už ustúpila. Napriek uvedeným faktom sa pokračovalo v liečbe ustekinumabom. Podľa literárnych údajov presná etiopatogenéza vzniku paradoxných psoriaziformných prejavov nie je známa. V posledných rokoch sa za zásadnú v etiopatogenéze psoriázy považuje Th 17 signálna cesta. TNF-α môže vyvolať dysreguláciu v imunitnom systéme, ktorá môže privodiť nasledovné zmeny. Aktiváciou IL-12/IL-23 cesty sa aktivuje Th 17 signálna cesta s následnou produkciou IL-1b, IL-17, IL-21 a IL-22, spolu so zvýšenou produkciou IL-17A a IL-22, hyperaktiváciou Th17 aTh1 cesty a redukciou aktivity T-regulačných lymfocytov [5,9]. Vznik imunologicky mediovaných reakcií bol popísaný aj pri biologikách s iným mechanizmom účinku (Il-12/23 inhibícia alebo IL-17 inhibítory). Ustekinumab je však toho času jedinou terapeutickou modalitou u pacientov s CD a psoriázou, ak zlyháva alebo je kontraindikovaná anti-TNF-α liečba.
Konflikt záujmov: Autori deklarujú, že text článku zodpovedá etickým štandardom, bola dodržaná anonymita pacientov, a vyhlasujú, že v súvislosti s predmetom článku nemajú finančné, poradenské ani iné komerčné záujmy.
Publikačná etika: Príspevok nebol doteraz publikovaný ani nie je v súčasnosti zaslaný do iného časopisu na posúdenie. Autori súhlasí s uverejnením svojho mena a e-mailového kontaktu v publikovanom texte.
Dedikácia: Tento článok vznikol s podporou spoločnosti Johnson & Johnson s.r.o., divízia Janssen, EM-18429.
Redakčná rada potvrdzuje, že rukopis práce splnil ICMJE kritériá pre publikácie zasielané do bio medicínskych časopisov.
Doručené: 19. 9. 2019
Prijaté: 17. 11. 2019
MUDr. Karolína Vorčáková PhD.
Dermatovenerologická klinika
JLF UK a UN Martin
Kollárova 2
036 59 Martin
Slovenská republika
Zdroje
1. Andrade P, Lopes S, Gaspar R et al. Anti-tumor necrosis factor-α-induced dermatological complications in a large cohort of inflammatory bowel disease patients. Dig Dis Sci 2018; 63 (3): 746–54. doi: 10.1007/s10620-018-4921-y.
2. Verea MM, Del Pozo J, Yebra-Pimentel MT et al. Psoriasiform eruption induced by infliximab. Ann Pharmacother 2004; 38 (1): 54–57. doi: 10.1345/aph.1C477.
3. Puig L. Paradoxical reactions: anti-tumor necrosis factor alpha agents, ustekinumab, secukinumab, ixekizumab, and others. Curr Probl Dermatology 2018; 53 : 49–63. doi: 10.1159/ 000479475.
4. Vorčáková K, Juraj P, Péčová T et al. Immune-mediated skin reactions induced by recombinant antibodies and other TNF-alpha inhibitors. [online]. Available from: https: //www.intechopen.com/books/antibody-engineering/immune-mediated-skin-reactions-induced-by-recombinant-antibodies-and-other-tnf-alpha-inhibitors.
5. Ciccarelli F, De Martinis M, Sirufo MM et al. Psoriasis induced by anti-tumor necrosis factor alpha agents: a comprehensive review of the literature. Acta Dermatovenerol Croat 2016; 24 (3): 169–174.
6. Collamer AN, Battafarano DF. Psoriatic skin lesions induced by tumor necrosis factor antagonist therapy: clinical features and possible immunopathogenesis. Semin Arthritis Rheum 2010; 40 (3): 233–240. doi: 10.1016/ j.semarthrit.2010.04.003.
7. Vinkel C, Thomsen SF. Autoinflammatory syndromes associated with hidradenitis suppurativa and/or acne. Int J Dermatol 2017; 56 (8): 811–818. doi: 10.1111/ijd.13603.
8. Vorcakova K, Pecova T, Turonova L. Anti-dsDNA antibodies and their association with paradoxical psoriasis induced by TNF alfa inhibitors. Bratislava Lek Listy 2017; 118 (4): 250–250. doi: 10.4149/BLL_2017_049.
9. Wendling D, Prati C. Paradoxical effects of anti-TNF-α agents in inflammatory diseases. Expert Rev Clin Immunol 2014; 10 (1): 159–169. doi: 10.1586/1744666X.2014.866038.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek EditorialČlánek Obezita a dětská ledvina
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2019 Číslo 6- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Editorial
- Chirurgická léčba obezity a metabolických onemocnění – nové výzvy i pro další obory
- Stanovisko Pracovní skupiny pro dětskou gastroenterologii, hepatologii a výživu České pediatrické společnosti (PSDG ČPS) k používání dietních opatření v léčbě Crohnovy nemoci u dětských pacientů
- Dieta CDED v indukční terapii Crohnovy nemoci
- Diagnostika ložiskových lézí jater u dětí s využitím kontrastní ultrasonografie
- Vitamin D – substituce po malabsorpční operaci
- Výživa a bariatricko-metabolická chirurgie
- Kožné imunologicky mediované nežiaduce účinky indukované anti-TNF alfa terapeuticky zvládnuté zmenou liečby za ustekinumab
- Ložiskové zánětlivé procesy jater
- Obezita a dětská ledvina
- Díl VI. – Příčiny úmrtí pacientů s idiopatickými střevními záněty se zaměřením na hospitalizace v závěru života pacienta
- Ružinovský gastroenterologický deň 2019 8. november 2019 ABSTRAKTA
- Zpráva z kongresu Obezitologie a bariatrie 2019, Brno
- 36th Czech and Slovak Congress of Gastroenterology
- Vzpomínka na profesora Meinharda Classena
- Novinky z výzkumu horního GIT
- Výběr z mezinárodních časopisů
- Kreditovaný autodidaktický test: dětská gastroenterologie a hepatologie obezitologie a bariatricko-metabolická chirurgie
- Alogenní mezenchymální kmenové buňky (ALOFISEL) jsou efektivní v eradikaci komplexních perianálních píštělí u Crohnovy nemoci
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Ložiskové zánětlivé procesy jater
- Dieta CDED v indukční terapii Crohnovy nemoci
- Vitamin D – substituce po malabsorpční operaci
- Alogenní mezenchymální kmenové buňky (ALOFISEL) jsou efektivní v eradikaci komplexních perianálních píštělí u Crohnovy nemoci
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



