-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaDyslipidemie u metabolického syndromu
Dyslipidemia and metabolic syndrome
Dyslipidemia is common part of the metabolic syndrome. The typical lipid disorders are hypertrigylceridemia and low HDL-cholesterol. Elevation of small LDL3 and apolipoprotein B100 are also present in most patients. Weight reduction, diet and regular physical activity are the most effective way how to treat this type of dyslipoproteinemia. Before hypolipidemic drug therapy is started, type of dyslipidemia must be considered. Fibrates are recommended in patients with hypertriglyceridemia and low HDL-cholesterol. When high LDL-cholesterol is present, statin therapy is recommended. In some patients therapy with both fibrate and statin is needed to reach target lipid levels.
Key words:
dyslipidemia – metabolic syndrome – HDL-cholesterol – triglycerides – LDL3
Autoři: V. Soška
Působiště autorů: Centrum pro diagnostiku a léčbu dyslipidemií, Oddělení klinického komplementu FN u sv. Anny, Brno, přednosta doc. MUDr. Vladimír Soška, CSc.
Vyšlo v časopise: Vnitř Lék 2005; 51(1): 77-81
Kategorie: Přehledné referáty
Souhrn
Dyslipidemie je jedním ze základních příznaků metabolického syndromu. Typickým nálezem je hypertriglyceridemie a nízký HDL-cholesterol. Pravidelným nálezem bývá také zvýšený apolipoprotein B100 a zvýšená koncentrace malých LDL3. Redukce hmotnosti, změna stravovacích návyků a pravidelná fyzická aktivita jsou základem léčby této dyslipidemie. Při výběru vhodného hypolipidemika je třeba zohlednit typ dyslipidemie. Při hypertriglyceridemii a nízkém HDL-cholesterolu jsou lékem volby fibráty. Je-li zvýšen LDL-cholesterol, jsou indikovány statiny. U části nemocných s metabolickým syndromem je vhodná léčba kombinací statinu s fibrátem.
Klíčová slova:
dyslipidemie – metabolický syndrom – HDL-cholesterol – triglyceridy – LDL3Úvod
Dyslipidemie (DLP) patří mezi základní kritéria pro stanovení diagnózy metabolického syndromu a u většiny nemocných je jeho pravidelnou součástí. Není pochyb o tom, že u těchto nemocných se DLP podílí na rozvoji kardiovaskulárních komplikací. DLP se může projevit dříve než některé ostatní příznaky metabolického syndromu. DLP u nemocných smetabolickým syndromem je charakterizována především hypertriglyceridemií a snížením HDL-cholesterolu. Hypertriglyceridemií se v tomto případě rozumí zvýšení koncentrace triglyceridů >1,7 mmol/l a snížení HDL-cholesterolu <1,0 mmol/l u mužů a <1,2 mmol/l u žen. Charakteristickou triádu DLP pak doplňuje přítomnost zvýšené koncentrace vysoce aterogenní frakce lipoproteinů o nízké hustotě, tzv. malých denzních LDL (frakce LDL3). Při podrobnějším vyšetření nemocných pak můžeme nalézt i další odchylky v lipidovém spektru: pravidelně bývá zvýšena koncentrace apolipoproteinu B100, často je prodloužena postprandiální lipemie a je zvýšený apolipoprotein C III. Také koncentrace celkového cholesterolu může být zvýšená, koncentrace LDL-cholesterolu ale bývá často normální. Zvýšení celkového cholesterolu je způsobeno především zvýšením koncentrace cholesterolu ve frakci VLDL (někdy i IDL). Pravidelně je zvýšená hladina volných mastných kyselin v séru. Při posuzování vypočtených parametrů bývá zvýšená koncentrace non HDL-cholesterolu.
Mechanizmus rozvoje DLP
Jedním z klíčových mechanizmů, který se v rozvoji DLP u metabolického syndromu uplatňuje, je zvýšená hladina volných mastných kyseliny v krvi. Mastné kyseliny, odštěpené z triglyceridů krevních lipoproteinů v kapilárách tukové tkáně, jsou v adipocytech za fyziologických okolností opět reesterifikovány na zásobní triglyceridy. Tento proces je zprostředkován ASP (acylation stimulatory protein), který je fyziologicky aktivován inzulinem [24]. Inzulinorezistence alteruje funkci ASP, takže volné mastné kyseliny nejsou reesterifikovány na triglyceridy a vrací se krevní cestou do jater. Jejich zvýšená nabídka v játrech indukuje zvýšenou syntézu triglyceridů, a následně syntézu lipoproteinů o velmi nízké hustotě (VLDL), které jsou uvolňovány do krve [6]. Ke zvýšené tvorbě VLDL v hepatocytech přispívá také hyperinzulinemie v játrech a nadbytek energetických substrátů při zvýšeném příjmu energie u obézních nemocných [11]. Jsou syntetizovány atypické VLDL, které jsou velké a velmi bohaté na triglyceridy. Jejich metabolizmus v krvi je alterován (je zpomalena jejich degradace v kapilárách tukové tkáně), protože aktivita lipoproteinové lipázy je utlumena vysokou koncentrací volných mastných kyselin a inzulinovou rezistencí [20]. Zvýšená syntéza a zpomalené odbourávání lipoproteinů bohatých na triglyceridy (VLDL, ale také chylomiker a IDL) vede k rozvoji hypertriglyceridemie.
Stejné příčiny, které vedou k alteraci metabolizmu VLDL, způsobují také „zpomalení“ metabolizmu na triglyceridy bohatých chylomiker. Důsledkem je prodloužená postprandiální lipemie. Ta se může projevit tím, že u nemocných s metabolickým syndromem nalézáme často lehce chylózní sérum, i když je dodržena předepsaná doba lačnění před odběrem krve. Zpomalené odbourávání chylomiker vede k tomu, že se zvyšuje koncentrace nejen chylomiker, ale i jejich „zbytků“ (remnantních částic). Chylomikra sama o sobě nejsou aterogenní, jejich zvýšená koncentrace nezvyšuje riziko aterosklerózy. Naproti tomu „remnanta“ chylomiker jsou silně aterogenní, jsou cytotoxická a při jejich zvýšené koncentraci se zvyšuje i koagulační aktivita faktoru VII [27]. Prodloužená postprandiální lipemie se proto podílí na zvýšeném riziku kardiovaskulárních komplikací u nemocných s metabolickým syndromem.
Částice VLDL (a také chylomikra a částice remnantní) nesou nejen triglyceridy, ale i významné množství cholesterolu. Jejich zvýšená koncentrace se proto v laboratorním nálezu může projevit jako mírné zvýšení celkového cholesterolu. Zvýšení celkového cholesterolu u nemocných s metabolickým syndromem je tedy způsobeno většinou zvýšením VLDL-cholesterolu, nikoliv LDL-cholesterolu.
Lipoproteiny bohaté na triglyceridy (VLDL) jsou fyziologicky odbourávány na intermediální částice (IDL), a z nich pak odštěpením další části triglyceridů účinkem jaterní lipázy vznikají částice LDL. Při hypertriglyceridemii je zintenzivněna výměna esterifikovaného cholesterolu a triglyceridů mezi částicemi HDL a VLDL Vznikají tak atypické lipoproteiny, ze kterých se tvoří menší částice LDL než za fyziologických okolností. Ty nesou méně esterifikovaného cholesterolu než fyziologicky se vyskytující větší LDL. Jsou označovány jako malé denzní LDL3. Množství LDL3 v krvi je tak závislé na koncentraci triglyceridů: při koncentraci triglyceridů < 1,7 mmol/l je tvorba LDL3 minimální, při vzestupu triglyceridů > 1,7 mmol/l se jejich podíl na celkovém množství LDL významně zvyšuje. Proto je u nemocných s metabolickým syndromem považována za optimální koncentrace triglyceridů < 1,7 mmol/l.
Každá částice LDL nese na svém povrchu jednu molekulu apolipoproteinu B100 (liganda pro vazbu na LDL receptor). Malé LDL obsahují méně cholesterolu než větší LDL, takže i při jejich zvýšeném počtu může být normální koncentrace LDL-cholesterolu. Protože ale nesou na svém povrchu vždy 1 molekulu apolipoproteinu B100, bývá zvýšená koncentrace apo B100. Z hlediska interpretace laboratorních nálezů je ale třeba upozornit, že koncentrace apolipoproteinu B100 nemusí korelovat s koncentrací malých denzních LDL3. Není proto možné tvrdit, že zvýšená koncentrace apo B100 při normální koncentraci LDL-cholesterolu znamená vždy přítomnost malých LDL3.
Bylo již uvedeno, že v krevním řečišti probíhá intenzivní výměna esterifikovaného cholesterolu a triglyceridů mezi lipoproteiny HDL (zdroj esterifikovaného cholesterolu) a VLDL či chylomikrony (zdroj triglyceridů). Tento přenos zprostředkuje CETP (cholesterol ester transfer protein). Čím vyšší je koncentrace VLDL (nebo chylomiker) v krvi, tím intenzivnější je tato výměna [7]. Vysoká koncentrace triglyceridy bohatých částic proto vede k ochuzení částic HDL o esterifikovaný cholesterol. Výsledkem je snížená koncentrace HDL-cholesterolu.
Cílové hodnoty krevních lipidů
Zvýšená koncentrace triglyceridů, snížená koncentrace HDL-cholesterolu a zvýšená frakce malých LDL3 jsou považovány za charakteristickou „triádu“ typickou pro metabolický syndrom. Kombinace uvedených tří metabolických odchylek v krevních lipidech přináší zvýšené riziko rozvoje časných kardiovaskulárních komplikací [1,2,3,12,16]. Je proto žádoucí dosáhnout takových hodnot krevních lipidů, které riziko kardiovaskulárních komplikací minimalizují. Evropská doporučení pro prevenci ischemické choroby srdeční v klinické praxi z roku 1998 i doporučení česká z roku 2000 (Doporučení pro prevenci ischemické choroby srdeční v dospělém věku) uvádějí cílové hodnoty krevních lipidů, uvedené v tab. 1 [4,17].
Tab. 1. Cílové hodnoty krevních lipidů platné do roku 2003. 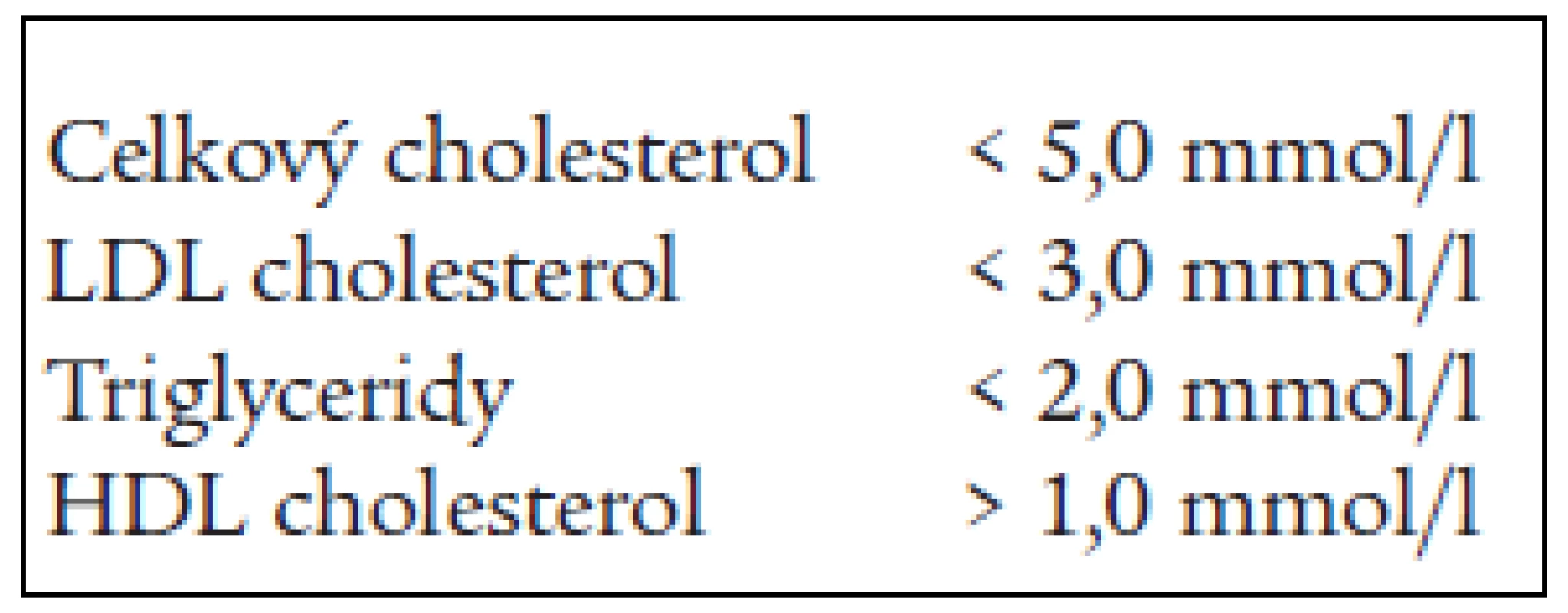
Tyto cílové hodnoty byly shodné pro primární prevenci i pro sekundární prevenci ischemické choroby srdeční. Výsledky intervenčních studií ale prokázaly, že u vysoce rizikových pacientů není dosažení uvedených hodnot postačující z hlediska prevence kardiovaskulárních komplikací [15]. Nejnovější doporučení evropských společností, prezentovaná na Evropském kardiologickém kongresu v roce 2003, proto požadované limity pro vybrané skupiny populace dále zpřísňují [8]. Stávající cílové hodnoty zůstávají v platnosti, ale pro vysoce rizikové skupiny populace (osoby s manifestním kardiovaskulárním onemocněním v prevenci a osoby v primární prevenci s velmi vysokým rizikem) se dále snižují (tab. 2).
Tab. 2. Cílové hodnoty krevních lipidů podle doporučení z roku 2003. 
Současné cílové hodnoty krevních lipidů jsou podobné těm, které udávají americká doporučení z roku 2002 [9]. Americká doporučení zavádějí navíc i nový cílový parametr „non HDL-cholesterol“. Ten nahrazuje LDL-cholesterol u osob, které mají vysokou hladinu triglyceridů (kdy nelze vypočíst LDL-cholesterol). Hypertriglyceridémie je častým nálezem právě u nemocných s metabolickým syndromem. Hodnotu non HDL-cholesterolu získáme prostým odpočtem:
HDL-cholesterol = celkový
cholesterol – HDL-cholesterol.
Cílové hodnoty „non HDL-cholesterolu“ jsou o 0,8 mmol/l vyšší, než je cílové hodnota LDL-cholesterolu (tab. 3). Význam „non HDL-cholesterolu“ vychází ze skutečnosti, že aterogenní nejsou pouze částice LDL, ale i další lipoproteiny bohatší triglyceridy (IDL, zbytky chylomiker a VLDL). Hodnota non HDL-cholesterolu tak upozorňuje na zvýšenou koncentraci všech aterogenních lipoproteinů, nejen LDL (LDL, IDL, VLDL, remnanta chylomiker).
Tab. 3. Srovnání cílových hodnot non HDL cholesterolu a LDL cholesterolu. 
Léčba dyslipidemie u metabolického syndromu
Změny životního stylu
Prvotním cílem v léčbě osob s metabolickým syndromem, který může léčit či eliminovat nejen dyslipidemii, ale i ostatní rizikové faktory (hyperinzulinemii, hyperglykemii, hypertenzi), musí být snaha o trvalé změny životního stylu. Jedná se o tyto požadavky:
- zvýšení fyzické aktivity
- redukci tělesné hmotnosti
- změna stravovacích návyků
- zákaz kouření.
Zvýšení fyzické aktivity
Z hlediska DLP má pravidelná fyzická aktivita tyto příznivé účinky: snižuje triglyceridy a non HDL-cholesterol, zvyšuje HDL-cholesterol a částečně snižuje LDL-cholesterol, pokud byl zvýšený. Fyzická aktivita by měla být „šita na míru“ každému nemocnému s metabolickým syndromem a měla by odpovídat jeho zdravotnímu stavu. Přitom se nemusí jednat o cvičení vysoké intenzity. I pohybová aktivita mírné intenzity, je-li pravidelná, má příznivý metabolický efekt a zlepšuje stav kardiovaskulárního aparátu [13].
Redukce tělesné hmotnosti
Na každý kilogram redukce hmotnosti dochází ke snížení hladiny triglyceridů o 2–3 %, zvýšení HDL-cholesterolu o 1–2 %, snižuje se celkový (i LDL) cholesterol asi o 1 %. Tento efekt se ale projeví až po určité době latence po redukci hmotnosti, kdy se hmotnost nemocného stabilizuje. V první fázi hubnutí nemusí být tyto změny patrné, někdy dokonce může dojít přechodně i k vzestupu LDL-cholesterolu a poklesu HDL-cholesterolu, což může působit na nemocného i lékaře demotivačně. Není také nutné dosažení ideálních hodnot body mass indexu (25 kg/m2). Ke zlepšení metabolického syndromu může postačovat redukce hmotnosti asi o 5 až 10 %. To má význam i z hlediska psychiky nemocného, protože to je cíl relativně snáze dosažitelný, než redukce k ideální hodnotě BMI.
Změna stravovacích návyků
Dietní opatření při léčbě DLP u metabolického syndromu se významně neliší od standardních doporučení k léčbě nemocných s dyslipidemií.
Hlavní zásady jsou následující:
- Tuky mají tvořit 25–30 % denního kalorického příjmu, z toho:
- nasycené tuky < 7 % denního energetického příjmu
- mononenasycené tuky < 20 % denního energetického příjmu
- polynenasycené tuky < 10 % denního energetického příjmu
- příjem cholesterolu < 200 mg/den.
- Bílkoviny mají tvořit < 15 % kalorického příjmu.
- Obsah rostlinné vlákniny (rozpustná vláknina) má být 10–20 g/den.
- Nejméně 5krát denně má být zařazena na jídelníček zelenina a ovoce.
- Je třeba omezit konzumaci alkoholu (alkohol zvyšuje triglyceridy, je poměrně bohatým zdrojem kalorií).
Zákaz kouření
Kromě všeobecně známých negativních účinků na kardiovaskulární aparát má kouření i přímý vliv na krevní lipidy – snižuje HDL-cholesterol. Nekouření je jednou ze základních podmínek k tomu, aby se podařilo zvýšit hladinu HDL-cholesterolu.
Farmakoterapie DLP u metabolického syndromu
Zahájení farmakoterapie
Pokud se ani při kvalifikované odborné pomoci dlouhodobě nedaří dosáhnout cílových hodnot krevních lipidů změnami životního stylu, je na místě zvážit možnosti farmakoterapie. Při volbě hypolipidemika je vždy potřeba vycházet z konkrétního nálezu v krevních lipidech [25]. Před nasazením léku je nutné opakované vyšetření krevních lipidů k potvrzení konkrétního typu DLP. Hladina krevních lipidů před zahájením farmakoterapie má být stabilní, aby bylo možno posoudit účinek nasazeného léku [23]. Pokud hladina krevních lipidů v obdobní bez farmakoterapie výrazně kolísá, není možné posoudit, zda je změna krevních lipidů po nasazení léku způsobena lékem nebo zda by k ní došlo i bez farmakoterapie. Týká se to především nemocných s diabetes mellitus nebo osob s abúzem alkoholu. Dekompenzace diabetu (i zvýšená konzumace alkoholu) vede k rozvoji sekundární DLP (především se zvyšují triglyceridy). Farmakoterapie této sekundární DLP není úspěšná. Je nutné odstranit příčiny sekundární DLP (kompenzace diabetu, omezení alkoholu), což vede poměrně rychle k úpravě DLP. Krevní lipidy u nemocných s diabetes mellitus mají být vyšetřeny pouze v období uspokojivé kompenzace diabetu.
Volba léku
Fibráty
Pokud má nemocný DLP typickou pro metabolický syndrom (snížený HDL-cholesterol, zvýšené triglyceridy, cílový LDL-cholesterol), je vhodné zvážit léčbu fibráty [5,9,19]. Fibráty příznivě ovlivňují všechny uvedené metabolické odchylky: zvyšují HDL-cholesterol, snižují triglyceridy a redukují frakci malých LDL3 [26]. U nemocných s tímto typem dyslipidemie snižují kardiovaskulární morbiditu i mortalitu v sekundární i v primární prevenci ICHS [10,14, 18]. Fibráty dostupné v současnosti na našem trhu a jejich dávkování jsou uvedeny v tab. 4. Gemfibrozil již není na našem trhu k dispozici.
Tab. 4. Fibráty dostupné na našem trhu a jejich běžné dávkování. 
Statiny
Jsou indikovány vždy u nemocných se zvýšenou hladinou LDL-cholesterolu, preferovány jsou u nemocných v sekundární prevenci [4,9,17]. Ačkoliv zvýšená koncentrace LDL-cholesterolu není typickým nálezem u pacientů s metabolickým syndromem, řada z nich nedosahuje cílových hodnot pro LDL-cholesterol např. proto, že trpí některou z jiných, geneticky podmíněných DLP [23]. U těchto osob jsou statiny lékem první volby, protože snižují kardiovaskulární mortalitu a morbiditu. U nemocných v sekundární prevenci ICHS a u mužů s velmi vysokým rizikem v primární prevenci ICHS snižují i celkovou mortalitu, pokud mají jako výchozí parametr zvýšený LDL-cholesterol [15,21,22]. Dávku statinu je vhodné postupně titrovat nebo volit různě účinné statiny tak, abychom dosáhli cílové hodnoty LDL-cholesterolu. Statiny dostupné na našem trhu a jejich běžné dávkování jsou uvedeny v tab. 5.
Tab. 5. Statiny dostupné na našem trhu a jejich průměrná denní dávka. 
Pryskyřice (sekvestranty žlučových kyselin)
Tyto léky nejsou většinou k léčbě DLP u nemocných s metabolickým syndromem vhodné. Snižují pouze LDL-cholesterol, nemají vliv na hladinu HDL-cholesterolu a mohou zvyšovat hladinu triglyceridů.
Kombinace hypolipidemik
U části nemocných s metabolickým syndromem s kombinovanou dyslipidemií (zvýšené triglyceridy, zvýšený LDL-cholesterol, snížený HDL-cholesterol) nemusí stačit monoterapie statiny nebo fibráty k dosažení cílových hladin krevních lipidů. U osob v sekundární prevenci nebo ve vysokém riziku v primární prevenci je často indikována kombinovaná léčba statin + fibrát. Tato kombinace je většinou dostatečně účinná k dosažení optimálních hodnot krevních lipidů, ale na druhé straně je třeba zvážit to, že může znamenat vyšší riziko nežádoucích účinků, především riziko myopatie. Měl by ji proto raději zahajovat lékař, který má s takovouto léčbou dostatečné zkušenosti. Nevhodný pro tuto kombinovanou léčbu je gemfibrozil, který ale již od roku 2003 není na našem trhu.
Další hypolipidemika
Kyselina nikotinová
Zatím není na našem trhu, ale její dovoz je plánován. Je zatím nejúčinnějším lékem ke zvýšení HDL-cholesterolu a efektivně snižuje jak triglyceridy, tak i cholesterol. U nemocných s metabolickým syndromem je třeba zvážit, že v některých případech může zvyšovat glykemii.
Ezetimib
Je již zaregistrován a v roce 2004 by již měl být k dispozici. Jde o selektivní inhibitor resorpce cholesterolu v enterocytech. Bude indikován především jako lék do kombinace se statiny u nemocných, u kterých monoterapie statiny nestačí k dosažení cílových hodnot LDL-cholesterolu. U osob s metabolickým syndromem proto nebude těžiště jeho použití.
Thiazolidindiony nové generace
Zatím nejsou v klinickém použití. Mechanizmus jejich účinků je podobný jako u fibrátů, tj. stimulace jaderných receptorů PPAR. Mají účinky hypolipidemické i antidiabetické a budou to v budoucnosti pravděpodobně velmi vhodné léky pro nemocné s metabolickým syndromem.
doc. MUDr. Vladimír Soška, CSc.
www.fnusa.cz
e-mail: vladimir.soska@fnusa.cz
Doručeno do redakce: 12. 1. 2004
Přijato po recenzi: 15. 7. 2004
Zdroje
1. Assmann G, Schulte H, von Eckardstein A. Hypertriglyceridemia and elevated lipoprotein(a) are risk factors for major coronary events in middle–aged men. Am J Cardiol 1996; 77 : 1179–1184.
2. Austin MA, Hokanson JE, Edwards KL. Hypertriglyceridemia as a cardiovascular risk factor. Am J Cardiol1998; 81 (4A): 7B–12B.
3. Castelli WP. Epidemiology of triglycerides: a view from Framingham. Am J Cardiol 1992; 70 : 3H–9H.
4. Cífková R et al. Prevence ischemické choroby srdeční v dospělém věku. Vnitř Lék 2000; 46 (Suppl. 14): 14–20.
5. Češka R. Cholesterol a ateroskleróza. Praha: Maxdorf 1999.
6. De Graaf J, Veerkamp MJ, Stalenhoef AF. Metabolic pathogenesis of familial combined hyperlipidaemia with emphasis on insulin resistance, adipose tissue metabolism and free fatty acids. J Royal Soc Med 2002; 95 (Suppl. 42): 46–53.
7. Eisenberg S. High-density lipoprotein metabolism. In: Betteridge DJ, Illingworth DR (Eds.): Lipoproteins in health and disease. London: Arnold 1999.
8. European guidelines on cardiovascular disease prevention in clinical practice. Third joint task force of European and other societies on cardiovascular disease prevention in clinical practice. Eur Heart J 2003; 24 : 1601–1610.
9. Expert panel on detection, evaluation, and treatment of high blood cholesterol in adults: Executive summary of the third report of the National cholesterol education program (NCEP) expert panel of detection, evaluation, and treatment of high blood cholesterol in adults (Adult treatment panel III). JAMA 2001; 285 (19): 2486–2497.
10. Frick MH, Elo O, Haapa K et al. Helsinky Heart Study: Primary prevention trial with gemfibrozil in middle aged men with dyslipidemia. N Engl J Med 1987; 317 : 1237–1245.
11. Gibbons GF, Brown AM, Wiggins D et al. The role of insulin and fatty acids in the regulation of hepatic verylow - density lipoprotein assambly. J Royal Soc Med 2002; 95 (Suppl 42): 23–32.
12. Griffin J et al. Role of plasma triglyceride in the regulation of plasma low density lipoprotein (LDL) subfractions: relative contribution of small, dense LDL to coronary heart disease risk. Atherosclerosis
1994; 106 : 241–253.
13. Jančík J, Svačinová H, Dobšák P et al. Kombinovaný trénink u nemocných se systolickou dysfunkcí levé komory srdeční. Vnitř Lék 2003; 49(4): 280–284.
14. Manninen V, Tenkanen L, Koskinen P et al. Joint effects of serum triglyceride and LDL cholesterol and HDL cholesterol concentration on coronary heart disease risk in the Helsinki Heart Study. Implications for treatment. Circulation 1992; 85 : 37–45.
15. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20 536 high–risk individuals: a randomised placebo–controlled trial. Lancet 2002; 360 : 7–22.
16. Pocock SJ, Shaper AG, Philips AN. HDL-cholesterol triglycerides and total cholesterol in ischemic heart disease. Br Med J 1989; 298 : 998–1002.
17. Prevention of Coronary Heart Disease in Clinical Practice. Summary of Recommendations of the Second Joint Task Force of European and other Societies on Coronary Prevention, 1998.
18. Rubins HB, Robins SJ, Collins D et al. Gemfibrozil for the secondary prevention of coronary heart disease in men with low levels of high-density lipoprotein cholesterol. N Engl J Med 1999; 341 : 410–418.
19. Sacks FM. For the Expert Group on HDL cholesterol: The role of high-density lipoprotein (HDL) cholesterol in the prevention and treatment of coronary heart disease: Expert group recommendations. Am J Cardiol 2000; 90 : 139–142.
20. Saxena U, Witte LD, Goldberg IJ. Release of endothelial lipoprotein lipase by plasma lipoproteins and free fatty acid. J Biol Chem 1989; 264 : 4349–4355.
21. Scandinavian Simvastatin Survival Study Group. Randomised trial of cholesterol lowering in 4444 pateints with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S). Lancet 1994; 334 : 1383–1389.
22. Shepherd J, Cobbe SM, Ford I. et al. Prevention of coronary heart disease with pravastatin in men with hypercholesterolemia. West of Scotland Prevention Study Group. N Engl J Med 1995; 333 : 1301–1307.
23. Soška V. Poruchy metabolizmu lipidů: Diagnostika a léčba. Praha: Grada 2001.
24. Van Harmelen V, Reynosdottir S, Cianflone K et al. Mechanisms involved in the regulation of free fatty acid release from isolated human fat cells by acylation stimulating protein and insulin. J Biol Chem 1999; 274 : 18243–18251.
25. Weber, P, Kocourková B, Dočekalová A et al. Hyperlipidemie – možnosti léčby u diabetiků typu II. Geriatria 1999; 3–4 : 115–122.
26. Zeman M, Žák A, Tvrzická E et al. Vliv fibrátů na složení lipoproteinů VLDL a LDL a parametry jejich oxidace u hypertriglyceridémie. Čas Lék Čes 2002; 7(141): 211–216.
27. Zilversmit DB. Atherosclerosis: a postprandial phenomen. Circulation 1979; 60 : 473–485.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek Slovo nakladateleČlánek Odkaz sira Williama OsleraČlánek Jan Lebl, Štěpánka Průhová et al. Abeceda diabetu. Příručka pro děti, mladé dospělé a jejich rodičeČlánek MyokarditidyČlánek Metabolický syndrom a sympatický nervový systém: je obstrukční spánková apnoe klíčem k pochopení?Článek ÚvodníkČlánek Hypertenze a hyperurikemie
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2005 Číslo 1- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
-
Všechny články tohoto čísla
- Slovo nakladatele
- Jaterní postižení při deficitu alfa−1−antitrypsinu
- Akutní myokarditida manifestující se obrazem transmurálního infarktu myokardu provázená akutním renálním selháním
- Význam centralizace péče o nemocné s akutním krvácením do horní části trávicího traktu
- Za profesorem MUDr. Stanislavem Havelkou
- Otevřený dopis Jiřímu Vorlíčkovi
- Bioekvivalenční studie s novými antihypertenzivy
- Komentář k Doporučení American Heart Association/American College of Cardiology Foundation pro léčbu warfarinem
- Odkaz sira Williama Oslera
- Jan Lebl, Štěpánka Průhová et al. Abeceda diabetu. Příručka pro děti, mladé dospělé a jejich rodiče
- Jiří Vítovec, Jindřich Špinar et al. Farmakoterapie kardiovaskulárních onemocnění
- Petr Cetkovský et al. Intenzivní péče v hematologii
- Individuální výběr nemocných pro silový trénink po akutním infarktu myokardu se sníženou ejekční frakcí levé komory
- Viktor Chrobok, Jaromír Astl, Pavel Komínek et al. Tracheostomie a koniotomie, techniky, komplikace a ošetřovatelská péče
- Anna Jedličková. Antimikrobiální terapie v každodenní praxi
- David Cibula, Luboslav Stárka, Jana Vrbíková et al. Syndrom polycystických ovarií
- Tomáš Skalický, Vladislav Třeška, Jiří Šanjdauf et al. Chirurgie jater
- Zpráva o kurzu Hot topics in internal medicine, Alicante, Španělsko, 16.–22. 10. 2004
- Myokarditidy
- Myelodysplastický syndrom v novém tisíciletí. Jak klasifikovat a jak léčit nemocné?
- Efekt a tolerancia kombinovanej liečby fludarabinom s cyklofosfamidom u chorých s chronickou lymfocytovou leukémiou
- Naše zkušenosti s novou organizací péče o nemocné s akutním krvácením do horní části trávicího traktu
- Silový trénink u nemocných po akutním infarktu myokardu se sníženou ejekční frakcí levé komory srdeční
- Úvod do problematiky metabolického syndromu
- Metabolický syndrom a sympatický nervový systém: je obstrukční spánková apnoe klíčem k pochopení?
- Diabetes mellitus a metabolický syndrom
- Hypertenze jako součást metabolického syndromu
- Úvodník
- Obezita a metabolický syndrom
- Dyslipidemie u metabolického syndromu
- Hypertenze a hyperurikemie
- Role pohybové léčby a tělesné zdatnosti v prevenci a léčbě metabolického syndromu
- Akutní infarkt myokardu u pacienta s anamnézou infekční endokarditidy
- Extramedulární plazmocytom štítné žlázy - vzácná příčina solitární uzlové strumy s hypertyreózou
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Jaterní postižení při deficitu alfa−1−antitrypsinu
- Myelodysplastický syndrom v novém tisíciletí. Jak klasifikovat a jak léčit nemocné?
- Hypertenze a hyperurikemie
- Myokarditidy
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



