-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Kombinovaný chirurgický management infekce hemodialyzačního cévního přístupu bakteriologickým agens Clostridium perfringens
Complex surgical management of hemodialysis vascular access infection caused by Clostridium perfringens
Infection of prosthetic hemodialysis (HD) shunts is one of the most common complications of vascular access in hemodialysis patients. The incidence of anaerobic infection is very rare. In such a case, management of treatment represents a great challenge for the surgeon. We report a complicated case of autologous hemodialysis shunt infected by Clostridium perfringens on the right forearm in a polymorbid female patient with chronic renal failure and myelodysplastic syndrome. The patient has undergone repeated establishment of HD shunt with subsequent polybacterial local infectious complications. Destructive clostridial infection developed at the site of the infectious complications. This very rare complication involving infection by an atypical bacterial agent requires rapid diagnosis and comprehensive multimodal treatment including surgical, antibiotic and supportive therapy. Clinical implications and optimal therapy is not precisely defined in these cases.
Key words:
vascular access – infection – Clostridium perfringens
Autoři: MUDr. David Janák, Ph.D.; R. Novotný
; M. Slavíková; T. Grus; J. Lindner
Působiště autorů: II. chirurgická klinika-kardiovaskulární chirurgie, 1. lékařská fakulta, Univerzita Karlova v Praze a Všeobecná fakultní nemocnice v Praze, přednosta: Prof. MUDr. J. Lindner, CSc.
Vyšlo v časopise: Rozhl. Chir., 2014, roč. 93, č. 6, s. 325-327.
Kategorie: Kazuistika
Souhrn
Infekce protetických hemodialyzačních (HD) píštělí je jedna z nejčastějších komplikací cévních přístupů u hemodialyzovaných pacientů. Výskyt anaerobní infekce je velmi vzácný. Management léčby je v tomto případě pro chirurga velkou výzvou. Referujeme komplikovaný případ infikované autologní hemodialyzační píštěle Clostridiem perfringens na pravém předloktí u polymorbidní pacientky s chronickým renálním selháním a myelodysplastickým syndromem. Pacientka po opakovaném založení HD píštěle s následnými polybakteriálními lokálními infekčními komplikacemi. V terénu infekčních komplikací se vyvinula destruktivní klostridiová infekce. U této velmi vzácné infekční komplikace netypickým bakt. agens je nutná včasná diagnostika a komplexní multimodalitní péče zahrnující chirurgickou, antibiotickou a podpůrnou terapii. Klinické implikace a optimální terapie u těchto případů nejsou přesně stanoveny.
Klíčová slova:
cévní přístup infekce – Clostridium perfringensÚvod
Celosvětová populace především v západních státech vyspělého světa stárne a tomu odpovídá i vzrůstající výskyt chronického renálního selhání a potřeba zajištění adekvátního cévního přístupu pro hemodialyzační procedury. V rozvinutých evropských zemích tvoří hemodialyzovaní pacienti 0,02–0,08 % celkové populace. Pro chronickou dialýzu je u pacientů indikováno založení arteriovenózního cévního hemodialyzačního přístupu. V dnešní době jsou přesně stanovena kritéria pro založení arteriovenózních (AV) píštělí, zahrnující komplexní pohled na pacienta vycházející z klinického stavu, úrovně renálního selhání, dominance končetiny a kvality použitelných autologních žilních štěpů versus protetických náhrad, jakožto štěpů druhé volby. Velké množství AV a protetických píštělí v celosvětové hemodialyzační populaci vede ke vzniku různorodých komplikací. Mezi komplikace provázející pacienty s HD AV píštělí patří intimální hyperplazie venózní anastomózy, krvácení z píštěle, stenóza píštěle, perigraft serom, otok končetiny, pseudoaneuryzma, tepenný steal fenomén, trombóza, neuropatie a infekční komplikace. Infekční komplikace protetických, ale i autologních píštělí mohou být velmi nepříjemné a mohou mít díky častým komorbiditám u pacientů s HD terapií fatální následky.
Kazuistika
72letá, obézní, polymorbidní, hemodialyzovaná pacientka, diabetička na inzulinoterapii s myelodysplastickým syndromem, arteriální hypertenzí, renálním selháním diabetické etiologie. Hemodialýza byla u pacientky zahájena v roce 2010 přes brachiobasilickou píštěl v levé kubitě. V květnu 2012 byla AV píštěl pro rozvoj pseudoaneuryzmatického postižení a stafylokokovou infekci zrušena. Pacientka byla od června 2012 dočasně dialyzována přes permanentní tunelizovaný HD katétr, přes vena jugularis interna vpravo. Na konci června 2012 založena radiocefalická píštěl na pravé končetině. V listopadu téhož roku došlo k infekčnímu poškození píštěle vedoucí k selhání funkce cévního přístupu a nemožnosti jeho použití k hemodialýze a bylo provedeno přesazení píštěle výše na předloktí. Tři dny po přesazení píštěle pacientka přichází s febriliemi, intermitentními třesavkami, flegmonózně prosáklým předloktím a rozvíjející se plošnou nekrózou cca 15x8 cm na pravém předloktí (Obr. 1). Pacientka s rozvíjejícím se septickým stavem. Provedeno zrušení píštěle a excize nekrotické kůže s chirurgickým debridementem rány s náběrem mikrobiologického materiálu. Nasazena intravenózní empirická terapie, hemokultury s následnou pozitivitou Klebsiella pneumonie. Z rány vykultivováno Clostridium perfringens, Enterococcus faecium, Acinetobacter, Enterobacter ESBL a kvasinky. Zahájena cílená kombinovaná antibiotická terapie zahrnující Linezolid, Oxacilin a Flukonazol. Pro febrilie, vysoké CRP a klinický stav provedena extrakce permanentního tunelizovaného HD katétru. Po iniciálním chirurgickém debridementu pokračujeme ve striktní lokální bariérové terapii monoterapeutickým neutrálním superoxidovým roztokem, převazy a lokální debridement provádíme 4krát denně (Obr. 2). Pro zlepšení hojení rány zahajujeme přetlakovou terapii kyslíkem v hyperbarické komoře po dobu 90 min. během 5 dnů s max. 2,5 ATA (absolute atmosfere). Během hospitalizace pokles zánětlivých markerů, ústup febrilií s následným zlepšením klinického stavu, hemodialýza nově zavedeným HD katétrem cestou vena femoralis l. dx. Po zlepšení lokálního nálezu zahájena terapie VAC (vacuum assisted closure) systémem. Dochází k vyčištění rány s granulací defektu (Obr. 3). Pacientka bez febrílií, v dobrém klinickém stavu s granulační tkání v plošném defektu předána na nefrologické pracoviště k další péči. Následné naše opakované kontroly pacientky se stále se zlepšujícím lokálním nálezem, čistou ránou s postupnou okrajovou epitelizací.
Obr. 1. Primární nález Fig. 1: Initial finding 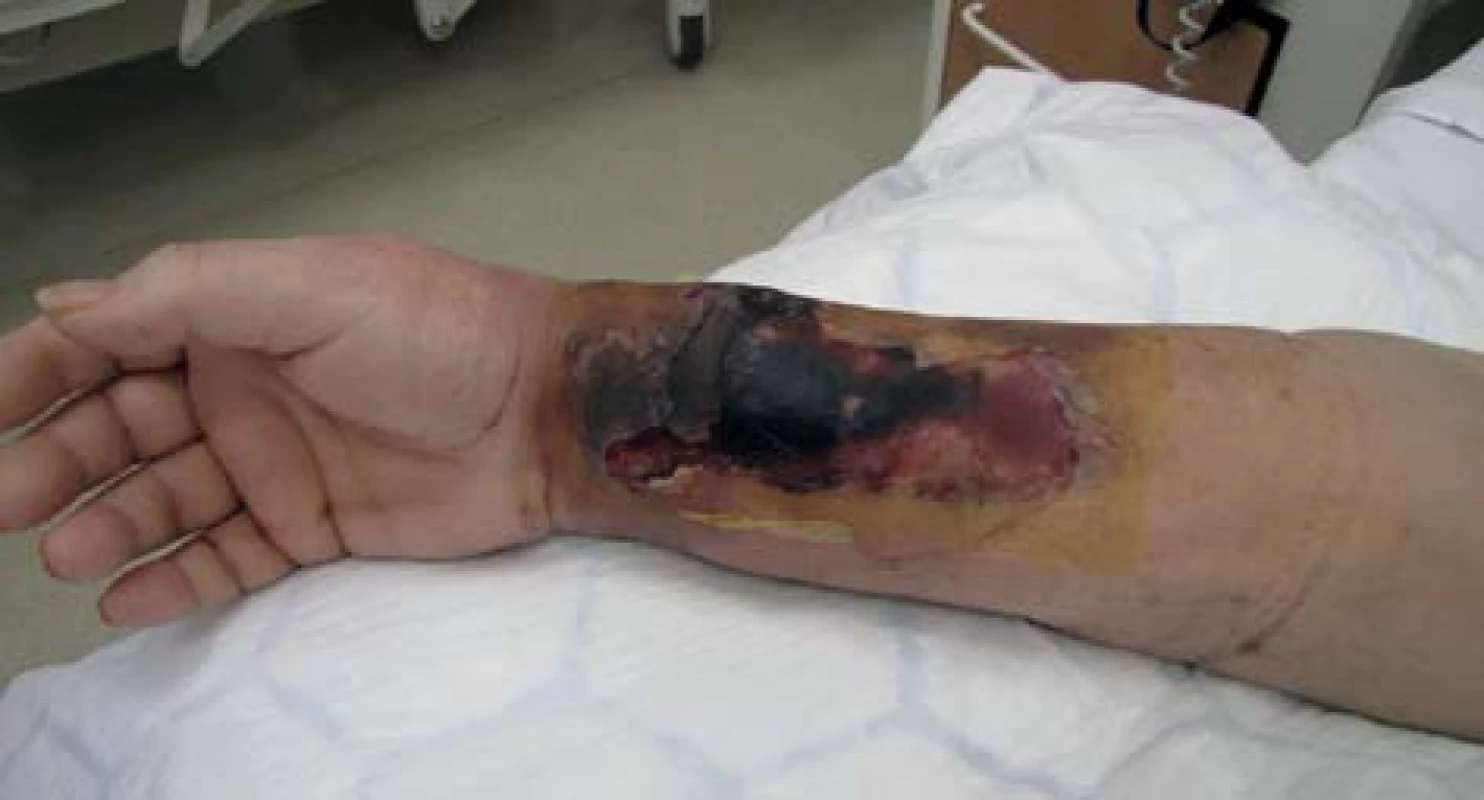
Obr. 2. Perioperační nález Fig. 2: Perioperative finding 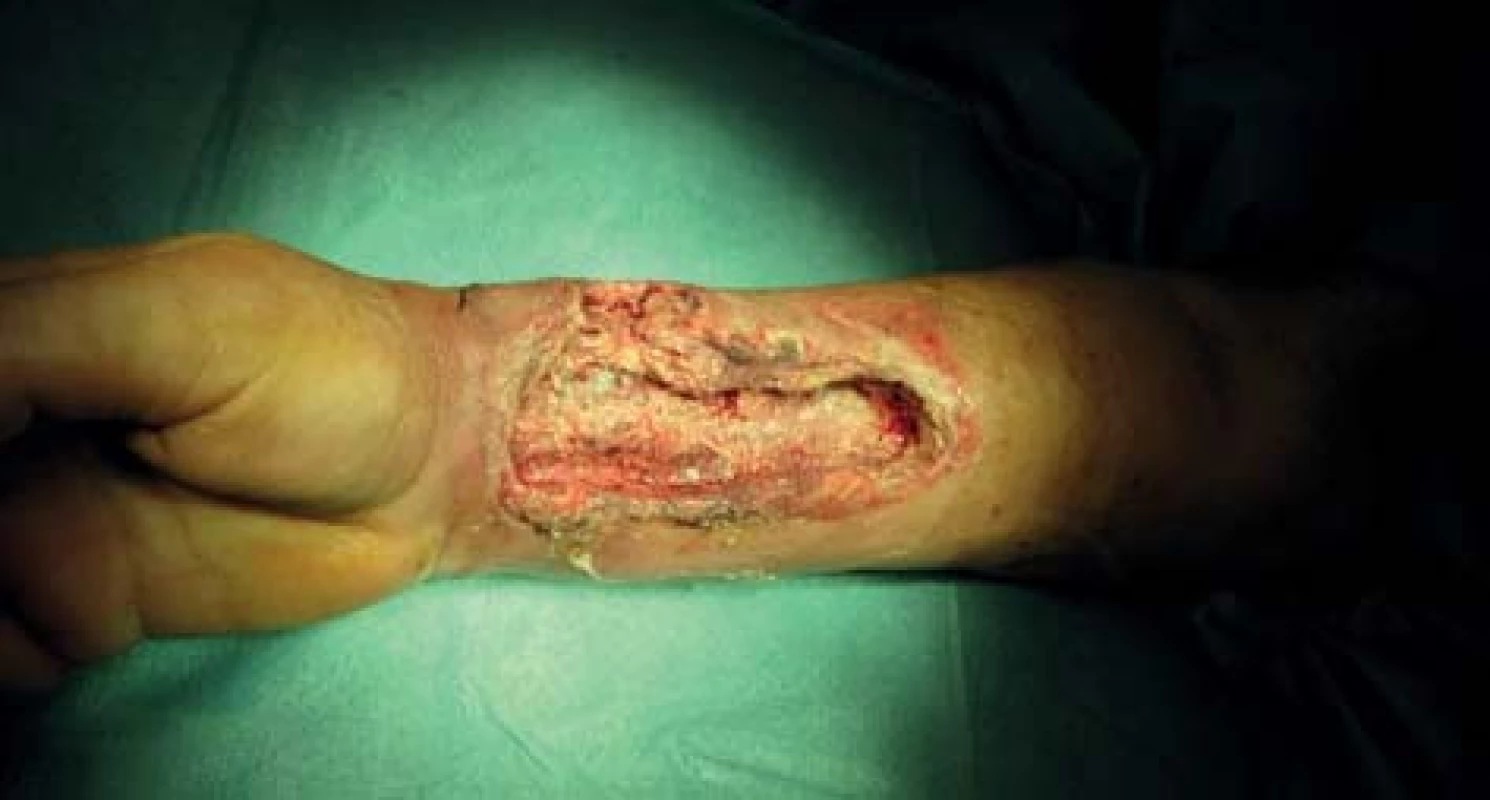
Obr. 3. Hojící se rána Fig. 3: Wound healing 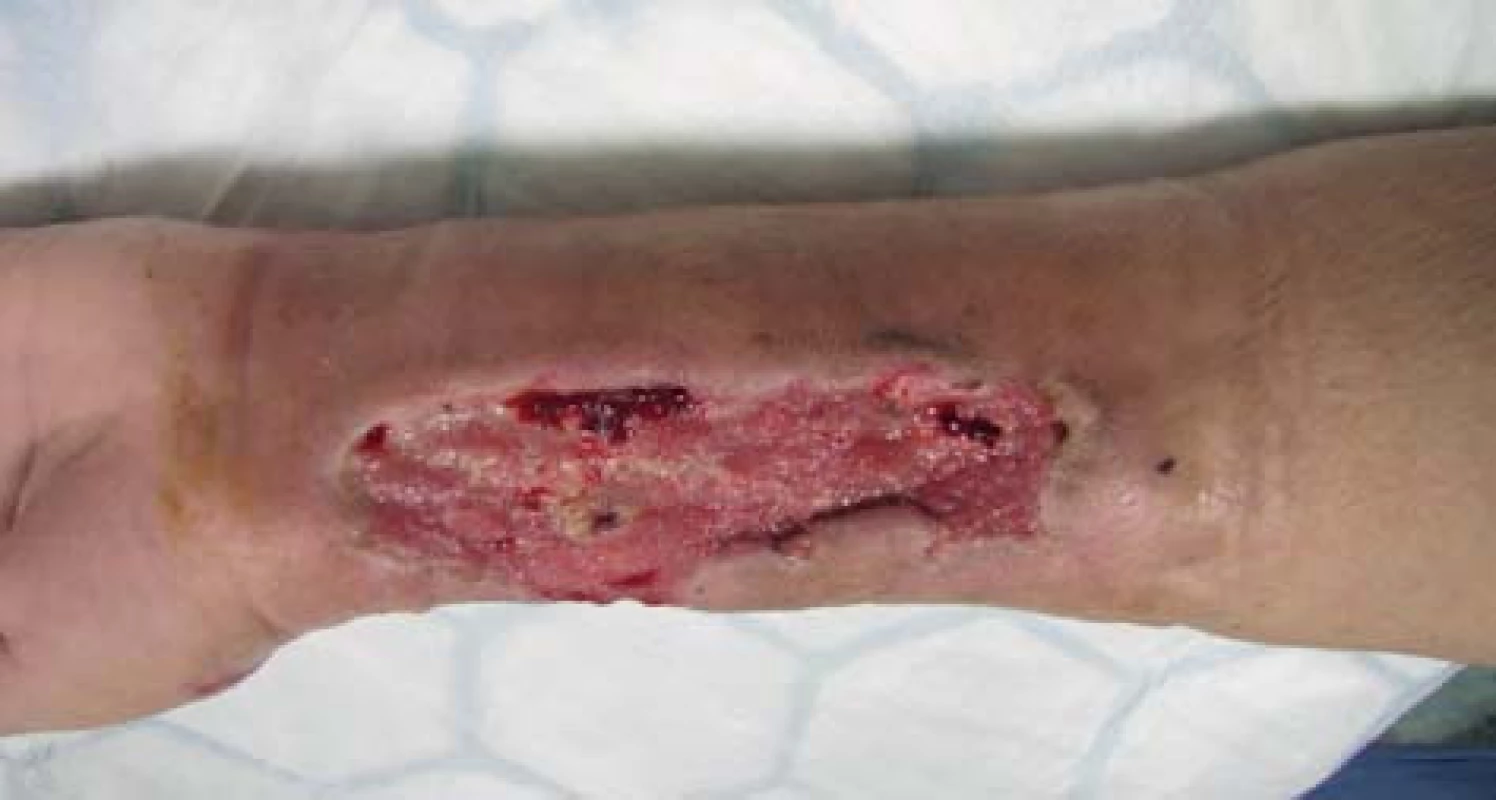
Diskuze
Infekce je nepříjemnou komplikací všech chronických dialyzovaných pacientů. Infekce signifikantně ohrožuje funkci píštěle a kvalitu života pacienta. Všeobecné faktory vedoucí ke vzniku infekce u všech typů píštělí jsou bakteremie, imunosuprese, špatná hygiena a technika opakované kanylace [1,2]. Vznik infekčních komplikací je u těchto pacientů vyšší a až 35 % z nich přijde o založený cévní zkrat pro jeho infekci v poměru 1 : 2 ve prospěch protetických píštělí [3]. Pacienti v HD programu často trpí nutričním a imunitním deficitem [4]. Infekce se nejčastěji manifestuje difuzní celulitidou nebo abscesy v místě napichování píštěle. Protetické píštěle jsou z hlediska náchylnosti rizikovější než autologní. Infekce protetických píštělí se vyskytuje u 5–20 % pacientů [5]. Velmi riziková je ruptura anastomózy z důvodu infekce protézy s následným krvácením [6]. V případě abscedující infekce je nutná chirurgická revize s prodlouženou antibiotickou terapií [5]. Ve spektru infekcí se setkáváme jak s grampozitivními bakteriemi, tak s gramnegativními bakteriemi a polymikrobiálními nálezy [7]. Nejčastější infekce jsou nálezy s grampozitivními bakteriemi, a to především Stafylococcus aureus [8]. Anaerobní infekce cévních přístupů je vzácná [9,10]. U hemodialyzovaných pacientů se předpokládá možnost potenciace anaerobních infekcí sníženým oxidačně redukčním potenciálem na buněčné úrovni [11]. Pro lokální růst Clostridium perfringens jsou důležité aminokyseliny a růstové faktory, které bakterie dokážou utilizovat z nekrotické tkáně. Specifikem klostridiových infekcí je pomalu se šířící infekce, bez časných systémových projevů [12]. Imunokompromitovaní pacienti, mezi které se pacienti v HD programu řadí, jsou k infekci náchylnější [13,14]. Inkubační doba plynaté sněti je od několika hodin až po 3 dny. Infekce se lokálně projevuje intenzivní bolestí v postižené ráně. Bolest je mnohem větší, než by se dalo očekávat vzhledem k velikosti a vzhledu rány. V okolí rány je tuhý edém, z rány vytéká řídký serózně hemoragický exsudát. Kůže v okolí rány je zprvu bledá a velmi citlivá na dotyk, během hodin dochází k třáskání. Posléze se na kůži objevují černě zbarvené puchýře a ložiska nekrózy. Z celkových příznaků dominují u pacienta neklid, horečka a hypotenze. Incidence plynaté sněti byla jedna z největších během první světové války a dosahovala u otevřených fraktur k 6 % a u otevřených ran k 1 % [15]. V dnešní době díky časné diagnostice a vhodné terapii incidence klesá, v USA je výskyt cca 3000 případů za rok [15]. Data pro Českou republiku nejsou. Mortalita je vysoká a dosahuje až 60–70 %, především tam, kde lokalizace infekce nedovoluje radikální excizi postižených tkání. Základním diagnostickým opatřením je odběr exsudátu, obsahu puchýře nebo vzorku tkáně na bakteriologické vyšetření, s následnou verifikací nálezu. Léčba musí být komplexní a musí být provedena neodkladně po stanovení diagnózy. Jejím základem jsou tři skupiny opatření, která všechna jsou pro úspěšnou léčbu nezbytná. Zahrnují chirurgický výkon, antibiotickou terapii a celkovou intenzivní podpůrnou terapii. Celková intenzivní léčba spočívá v oxygenoterapii, rehydrataci, monitoraci nemocného, dle potřeby podání oběhových podpor, transfuzí, diuretik a analgetik. V našem případě šlo o pacientku polymorbidní, imunokompromitovanou ještě myelodysplastickým syndromem. U této pacientky se potencovala imunokompetence jak z hlediska myelodysplastického syndromu, diabetu mellitu, tak i ze samotné nutnosti hemodialýzy. Přestože některé klostridiové infekce jsou exogenní, část infekcí může mít zdroj ve vlastní flóře pacientů. Rizikové je místo vpichu, a proto tedy základem prevence této infekce je dodržení pravidel asepse při napichovaní zkratu. Podkladem terapie je komplexní pohled na řešení těžkých infekcí, intravenózní cílená antibiotická terapie bránící progresi a šíření infekce. Pro lokální léčbu jsme využili hyperbarickou komoru pro zvýšení dodávky kyslíku do postižené tkáně a zvýšení oxidativně redukčního potenciálu. Klíčem je snížení produkce toxinů [17]. Dle výsledku prací zabývajících se problematikou anaerobních infekcí vyplývá, že morbidita i mortalita signifikantně klesají u kombinované terapie využívající hyperbarickou komoru, chirurgický debridement a antibiotickou terapii [18,19].
Důležitým faktorem léčby je časná a přesná diagnóza založená především na klinické symptomatologii a mikrobiologickém určení agens. Základem chirurgické intervence je opakovaný debridement, excize postižené tkáně a aplikace baktericidních látek. Pro zlepšení mikrocirkulace v tkáni jsme v našem případě po vyčištění rány použili podtlakový VAC (vacuum assisted closure) systém. Nedílnou součástí léčby pro zlepšení hojení rány po eliminaci infekce je adekvátní nutrice, korekce iontové dysbalance a diabetu mellitu.
MUDr. David Janák
Na Vrcholu 12
130 00 Praha
e-mail: David.Janak@vfn.cz
Zdroje
1. Bonomo RA, Rice D, Whalen C, et al. Risk factors associated with permanent access-site infections in chronic hemodialysis patiens. Infection Control and Hospital Epidemiology 1997;18 : 757–761.
2. Tordoir JH, Herman JM, Kwan TS, et al. Long-term follow-up of the polytetrafluoroethylene (PTFE) prosthesis as an arteriovenous fistula for haemodialysis. European Journal of Vascular Surgery 1988;2 : 3–7.
3. Schutte WP, Helmer SD, Salazar R, et al. Surgical treatment of infected prosthetic dialysis arteriovenosus grafts: total versus partial graft exciton. Am J Surg 2007;193 : 385–8, discussion 388.
4. Jaar BG, Hermann JA, Furth SL, et al. Septicemia in diabetic hemodyalisis patiens: comparison on incidence, risk factors, and mortality with non-diabetic hemodialysis patiens. Am J Kidney Dis 2000;35 : 282–92.
5. Palder SB, Kirkman RL, Whittemore AD, et al. Vascular accesss for hemodialysis: patency rates and results of revision. Ann Surg 1985;202 : 235–239.
6. Bennion RS, Wiliams RA, Wilson SE, et al. Vascular prosthetic infection. Infect Surg 1982;1 : 45–55.
7. Stevenson KB. Manamegent of hemodialysis vascular access infections. In Gray RJ. (ed): Dialysis access. Philadelphia, Lippincott Williams a Wilkins 2002;98–106.
8. Janoušek L, Baláž P, a kol. Hemodialyzační arteriovenózní přístupy. Praha, Grada Publishing 2008 : 117.
9. Marr KA, Sexton DJ, Conlon PJ, et al. Catheter related bactermia and outcome of attempted catheter salvage in patients undergoing hemodialysis. Ann Intern Med 1997;127 : 275–280.
10. Gorbach SL, Thadepalli H. Isolation of clostridium in human infections: evaluation of 114 cases. J Infect Dis 1975;131 : 581–585.
11. Brook I. Role of anaerobic bacteria in aortofemoral graft infection. Surgery 1988;104 : 843–845.
12. Oliveras A, Orfila A, Inigo V. Clostridium perfringens: an unusual pathogen infecting arteriovenous shunts for dialysis. Nephron 1998;80 : 479.
13. Kasper DL, Zaleznik lDF. Gasgangrene, antibiotic-associated colitis, and other Clostridial infections. Harrison’s principles of internal medicine. New York, McGraw-Hill 1998 : 906–910.
14. Meer RR, Songer JG, Park DL, et al. Human disease associated with Clostridium perfringens enterotoxin. Rev Environ Contam Toxicol 1997;150 : 75–94.
15. Chapnick EK, Abter EL, et al. Necrotizing soft-tissue infections. Infect Dis Clin North Am 1996;10 : 835–55.
16. Hitchcock CR, Demello FJ, Haglin JJ. Gangrene infection: New approaches to an old disease. Surg Clin North Am 1975;55 : 1403.
17. West M, Pirrene J, Chavers B, et al. Clostridium difficile colitis after kidney and kidney-pancreas transplantation. Clin Transplant 1999;13 : 318–323.
18. Thom SR. Functional inhibition of neutrophil B3 integrins by hyperbaric oxygen in car-bon monoxide mediated brain injury. Toxicol Appl Pharmacol 1993;123 : 248.
19. Heimbach R. Gas gangrene. In Kindwall E, Whelan H (eds): Hyperbaric Medicine Practice, 2nd ed. Revised. Flagstaff, AZ, Best Publishing Company 2004 : 549.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2014 Číslo 6- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Hojení análních fisur urychlí čípky a gel
- Stillova choroba: vzácné a závažné systémové onemocnění
-
Všechny články tohoto čísla
- Vědecko-výzkumná činnost v české chirurgii
- Nová strategie chirurgické léčby mnohočetného nádorového postižení jater – ALPPS
- Studie morfologie r. descendens a. circumflexae femoris lateralis jako možné cévní náhrady pro rekonstrukci koronárního řečiště pomocí angio CT vyšetření
- Karcinom tlustého střeva – zhodnocení komplikací a rizik plánovaných resekčních výkonů
- Srovnání chirurgického bypassu a subintimální rekanalizace v léčbě kritické končetinové ischemie
- Primární volvulus tenkého střeva u mladého nemocného
- Kombinovaný chirurgický management infekce hemodialyzačního cévního přístupu bakteriologickým agens Clostridium perfringens
- Klostridiová myonekróza břišní stěny – kazuistika
- Zemřel profesor Zdeněk Matějovský
- Základní principy diagnostiky a léčby sekundární peritonitidy – doporučení odborníků s podporou SIS
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Základní principy diagnostiky a léčby sekundární peritonitidy – doporučení odborníků s podporou SIS
- Primární volvulus tenkého střeva u mladého nemocného
- Klostridiová myonekróza břišní stěny – kazuistika
- Nová strategie chirurgické léčby mnohočetného nádorového postižení jater – ALPPS
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



