-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Těžká akutní pankreatitida – řešení komplikací kombinací miniinvazivních přístupů
Severe acute pancreatitis – managing complications using a combination of minimally invasive approaches
In this case report, we describe the case of a 30-year-old obese patient with severe acute pancreatitis complicated during hospitalization by the development of infected necrosis, a pseudocyst and an abscess. We demonstrate a possible solution to these complications using a combination of minimally invasive approaches. The contribution of this case report resides in that it presents a combination of the percutaneous approach and the endosonographic approach in the treatment of pancreatic necrosis. We believe that in such an extensive necrosis of the pancreas as is described in our case, this combined approach is optimal. The condition for implementing such a procedure is a well-staffed and technically equipped workplace.
Key words:
acute pancreatitis – pancreatic necrosis – pseudocyst – video-assisted endoscopic necrosectomy – pseudocystogastrostomy
Autoři: L. Doležalová 1; P. Volšanský 1; F. Neumann 1; L. Denemark 2
Působiště autorů: Oblastní nemocnice Kolín, a. s., Endoskopické centrum, primář: MUDr. P. Volšanský 1; Oblastní nemocnice Kolín, a. s., Chirurgie, primář: MUDr. L. Denemark 2
Vyšlo v časopise: Rozhl. Chir., 2014, roč. 93, č. 4, s. 216-219.
Kategorie: Kazuistiky
Souhrn
V naší kazuistice popisujeme případ 30letého obézního pacienta s těžkou akutní pankreatitidou komplikovanou v průběhu hospitalizace vznikem infikované nekrózy, pseudocysty a abscesu. Demonstrujeme řešení těchto komplikací pomocí kombinace miniinvazivních přístupů. Přínosem této kazuistiky je prezentace kombinace perkutánního a endosonografického přístupu v řešení pankreatických nekróz. Domníváme se, že při takto mimořádném rozsahu postižení pankreatu, jako je popisován v naší kazuistice, je tento kombinovaný přístup optimální. Podmínkou provádění takového postupu je dobře personálně a technicky vybavené pracoviště.
Klíčová slova:
akutní pankreatitida – nekróza – pseudocysta – videoasistovaná endoskopická nekrektomie – pseudocystogastrostomieÚVOD
Těžká akutní pankreatitida se vyskytuje u cca 15–20 % pacientů s akutní pankreatitidou a její definice je podle revidovaných Atlantských kritérií podmíněna přítomností perzistujícího orgánového selhání a přítomností lokálních komplikací (peripankreatická tekutinová kolekce, pankreatická a peripankreatická nekróza (sterilní x infikovaná), pseudocysta a ohraničená pankreatická nekróza). Nekróza pankreatu je definována jako neviabilní pankreatická tkáň velikostí přesahující 3 cm nebo 30 % objemu žlázy [1]. Vyvíjí se obvykle do 4 dnů od počátku onemocnění [3], riziko infekce stoupá s rozsahem nekrózy a dochází k ní obvykle během 2.–3. týdne od počátku onemocnění [3]. Mortalita pacientů s infikovanou nekrózou je ve srovnání se sterilní nekrózou vyšší (14–69 %) [1]. Dřívější práce uváděly v případě infikované nekrózy bez chirurgického řešení až 100% mortalitu [1,3]. Významným rizikovým faktorem je obezita – údaje studie z r. 1993 udávají 36 % mortalitu u obézních vs. 6 % u neobézních pacientů [3].
Kazuistika 1
V průběhu osmi měsíců jsme na našem endoskopickém pracovišti ošetřovali mladého obézního muže (30 let, BMI 44,6 kg/m2) s diagnózou těžké akutní pankreatitidy. Etiologie vzniku pankreatitidy nebyla z anamnestických údajů a provedených vyšetření zjevná. Dle CT vyšetření byl nekrózou postižen prakticky celý pankreas mimo procesus uncinatus, nekrotická žláza byla zavzata v objemné tekutinové kolekci a v okolí byly četné Balzerovy nekrózy (Obr. 1). Po dvou týdnech od vzniku onemocnění byly pro febrilie a vzestup zánětlivých parametrů odebrány hemokultury, empiricky nasazen cefoperazon s efektem (kultivačně později prokázána E. coli, Klebsiella pneumoniae, Enterococcus faecalis). Po přechodném zlepšení (pacient bez teplot, normalizace zánětlivých parametrů) byl devětadvacátý den hospitalizace stav pacienta komplikován rozvojem septického stavu (febrilie, zimnice, třesavka, opětovný vzestup zánětlivých parametrů). Klinicky se zvýraznilo vyklenutí v epigastriu, CT vyšetření zobrazilo bublinky plynu v místě ohraničující se tekutinové kolekce a nekrotické tkáně v retroperitoneu – vznikla „walled-off“ pankreatická nekróza [1].
Obr. 1. CT obraz rozsáhlé nekrózy pankreatu Fig. 1: CT of extensive pancreatic necrosis 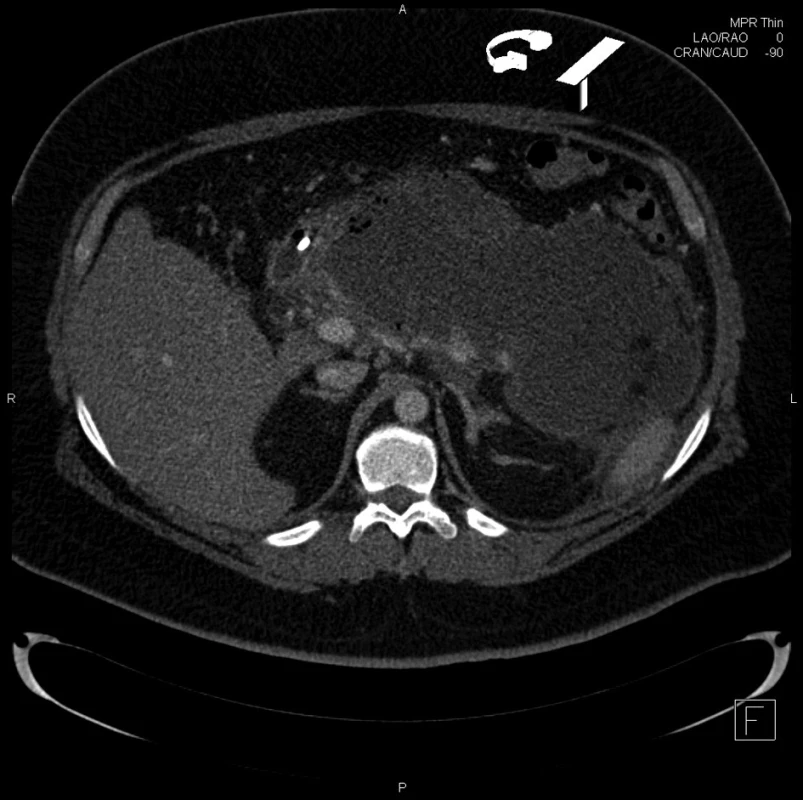
Na základě zhoršení klinického stavu byl pacient indikován k řešení suspektní infikované pankreatické nekrózy z perkutánního přístupu provedeného z oblasti levého boku (výkon 30. den od vzniku onemocnění). Nejprve jsme provedli perkutánní drenáž se zavedením 12Fr drénu (již tato šíře drénu umožnila odvod nejen kolikvované složky nekrózy, ale i drobných nekrotických hmot a výkon vedl ke zlepšení klinického stavu i vylepšení laboratorního nálezu). Při zavedení drénu byl proveden i mikrobiologický odběr a na základě výsledků kultivace byla podána cíleně antibiotika dle citlivosti (vykultivována Klebsiella pneumoniae, podán meropenem). Po několika dnech jsme kožní kanál rozdilatovali za pomoci dilatátorů a zavedli drén širší (22Fr) s cílem vytvořit si dostatečný kanál umožňující videoasistovanou endoskopickou perkutánní nekrektomii k odstranění formujících se nekrotických hmot. Dvaačtyřicátý den od vzniku onemocnění jsme přes původní otvor ve stěně břišní zavedli jícnový plně potažený metalický stent Flexella 110x20mm (ELLA CS) (Obr. 2). Videoasistovaná perkutánní nekrektomie probíhala „piece-meal“ technikou (Obr. 3–5) celkem ve 4 sezeních (po 2 týdny, poprvé 44. den od vzniku onemocnění), k uvolnění nekrotických hmot byla užita polypektomická klička a laváž 3 % H2O2. Tekutá složka nekrózy byla i nadále kontinuálně odváděna 22Fr drénem zavedeným přes jícnový stent a jímána do stomického sáčku, laváže H2O2 probíhaly denně. Krvácení při výkonech bylo minimální, čištěná dutina se pokrývala granulacemi. Po odstranění dostupných nekróz byl perkutánní přístup zrušen (64. den hospitalizace), kontrolní CT vykazovalo regresi nálezu a dobře ohraničenou pseudocystu v oblasti těla a kaudy pankreatu, kterou jsme řešili provedením pseudocystogastrostomie pod endosonografickou kontrolou pomocí double pig-tailu a metalického potaženého stentu Wallflex 80x10 mm (Boston Scientific). Výkon proběhl ve stejný den jako zrušení perkutánního přístupu. Později byl metalický stent vyměněn za druhý double pig-tail stent. Účinnost naší intervence jsme ověřili skiaskopicky podáním kontrastní látky do pseudocysty. Byla prokázána významná regrese pseudocysty. Pacient byl dimitován 78. den hospitalizace.
Obr. 2. Perkutánně zavedený metalický stent Fig. 2: Percutaneously implanted metallic stent 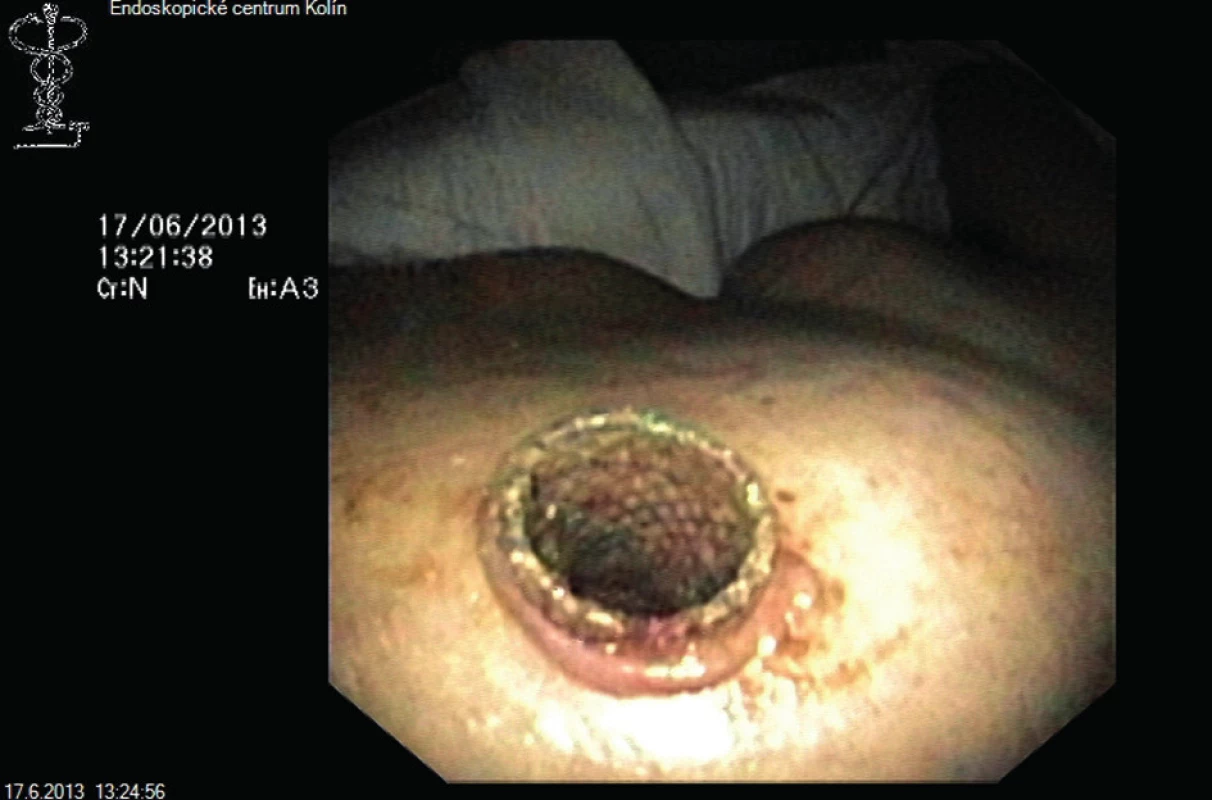
Obr. 3. Perkutánní endoskopická nekrektomie – RTG obraz Fig. 3: Percutaneous endoscopic necrectomy - X-ray finding 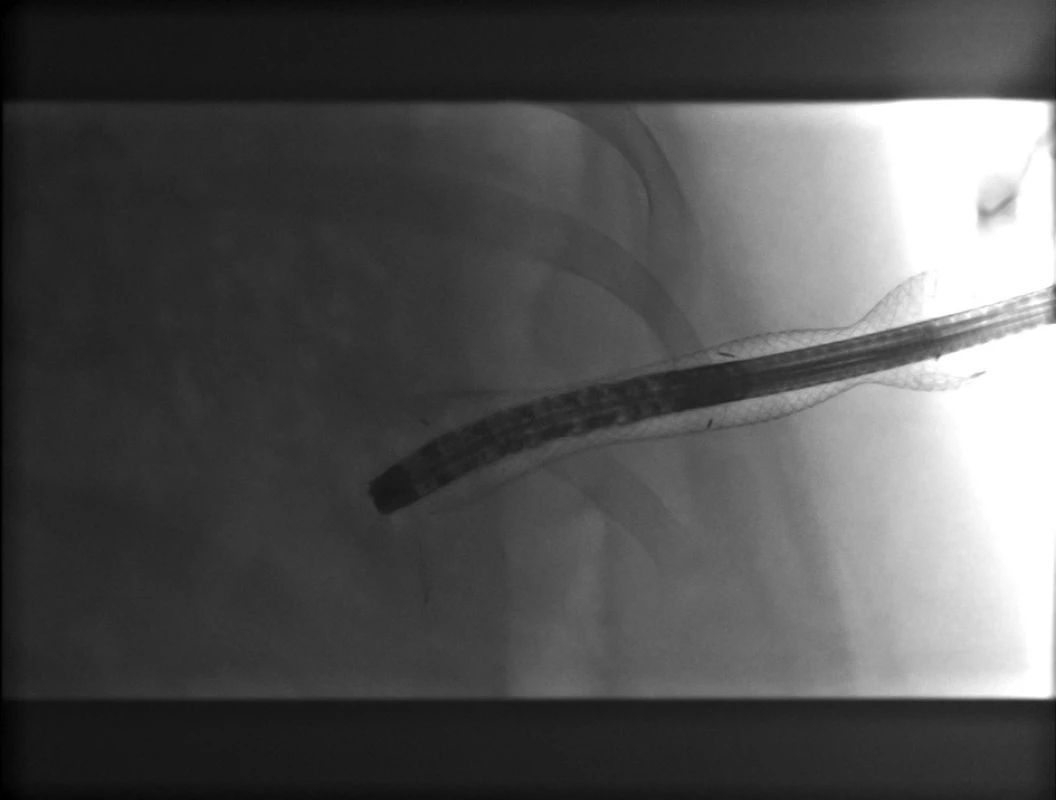
Obr. 4. Videoasistovaná endoskopická perkutánní nekrektomie Fig. 4: Video-assisted endoscopic percutaneous necrectomy 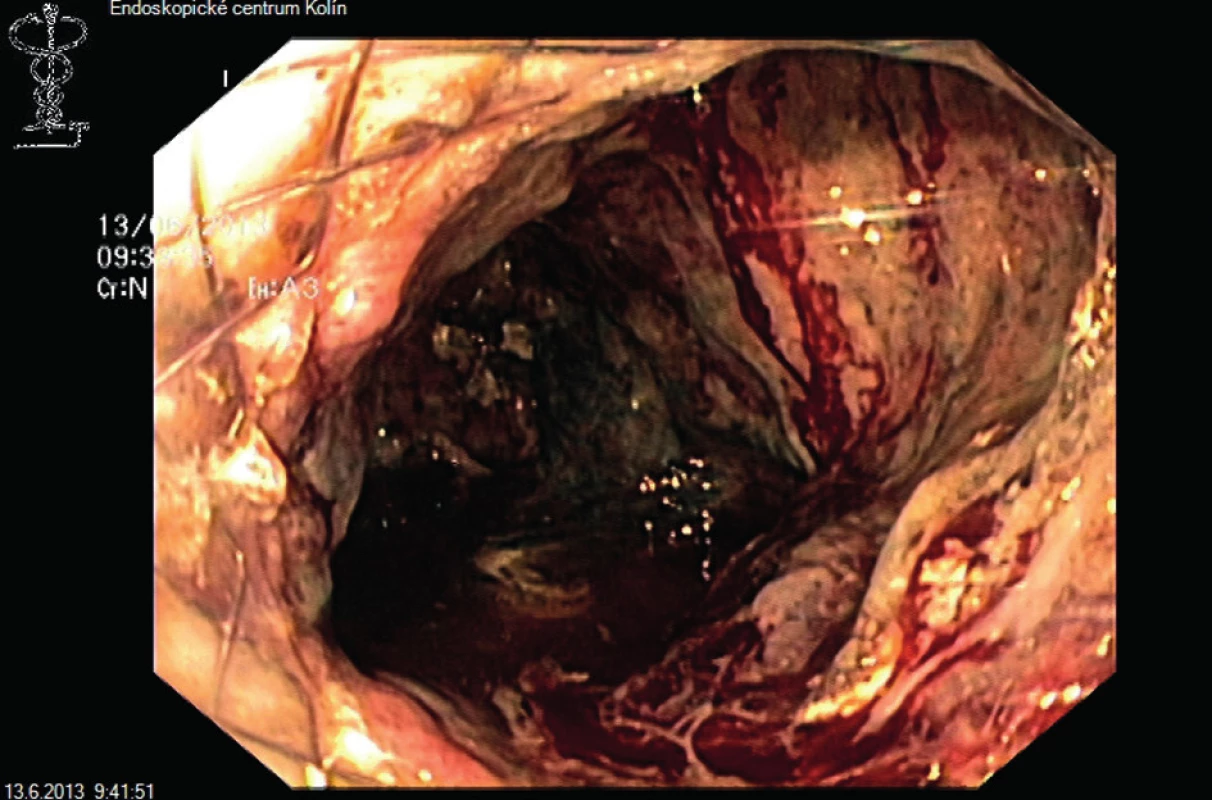
Obr. 5. Extrahovaná nekróza Fig. 5: Extracted necrosis 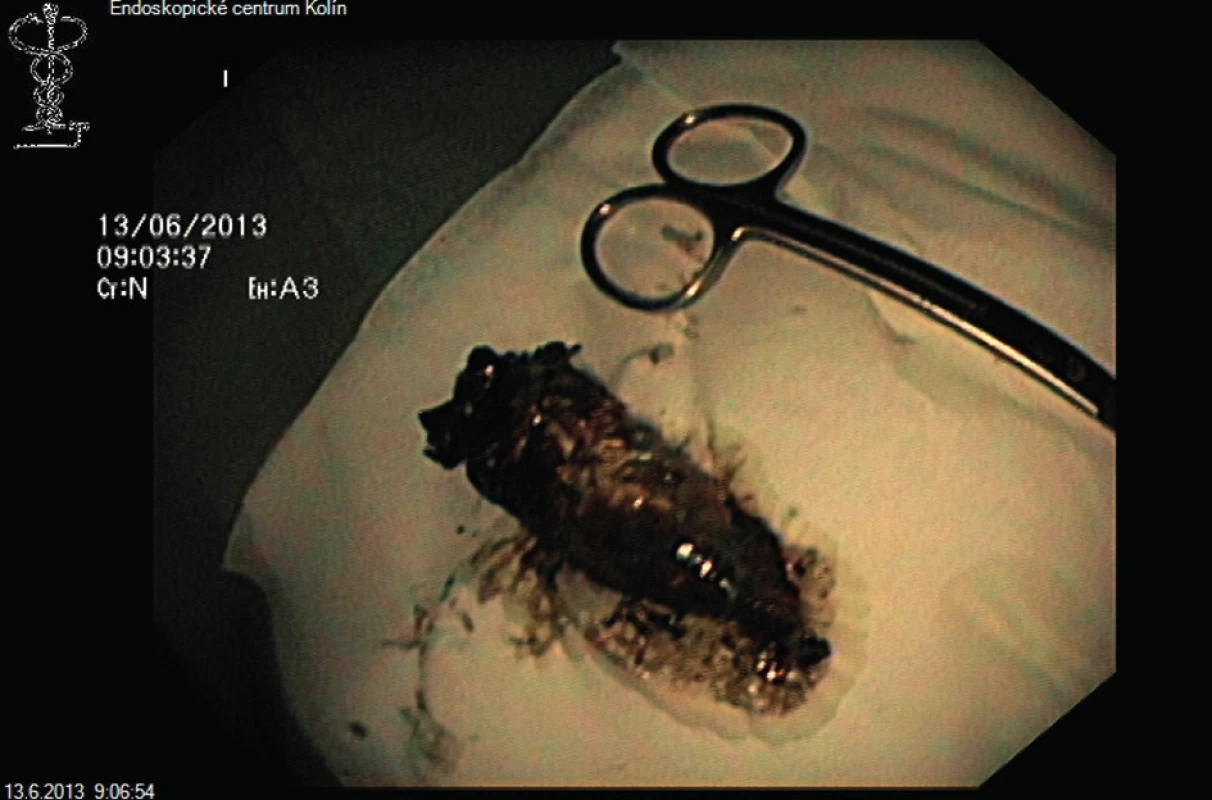
Deset týdnů od zavedení pseudocystogastrostomie CT vyšetření vykazovalo prakticky plnou regresi dutiny, pacient neměl subjektivní obtíže, proto jsme přistoupili k jejímu zrušení.
Sedmý den po výkonu však pacient vyhledal chirurgickou ambulanci pro opětovné bolesti v epigastriu, laboratorně byl zachycen vzestup zánětlivých parametrů, postupně rozvoj febrilií. Na CT se nově zobrazila kolekce tekutiny kolem S1 jater a byla suspekce na dilataci ductus pankreaticus. Proto jsme v dalším kroku zvolili provedení endoskopické retrográdní cholangiopankreatikografie a využili i možnost 3D zobrazení žlučových cest (Obr. 6). Zobrazenou stenózu ductus pankreaticus na rozhraní hlavy a těla pankreatu jsme řešili zavedením pankreatického single pig-tail stentu (5Fr, 4cm). Při následném ERCP o 5 dní později se zobrazuje za těsnou stenózou ductus pancreaticus rozsáhlá retroperitoneální kolekce tekutiny, ze které vytéká hnis. Opakované pokusy o dilataci stenózy za pomoci dilatátorů a tím umožnění účinné drenáže abscesu byly neúspěšné, proto byl zvolen off-label postup použití cystotomu. Jím jsme preparovali otvor přes stenózu a následně zavedli 7Fr nasoabscesový drén. Před intervencí na Wirsungu byl zaveden stent do ductus choledochus. Z hnisu byla vykultivována E. coli, empiricky nasazený ciprofloxacin a metronidazol byly měněny dle citlivosti na cefuroxim. Zánětlivé parametry poklesly k normě. Po týdnu byl nasoabscesový drén zrušen a byl zaveden pankreatický double pig-tail stent (7Fr). Dle kontrolního zobrazovacího vyšetření absces regredoval. Při zatím posledním ERCP o 2 měsíce později byl původní pankreatický stent vyměněn za kratší (7Fr, 3 cm) ponechaný v obliterovaném pankreatickém vývodu.
Obr. 6. 3D ERCP Fig. 6: 3D ERCP 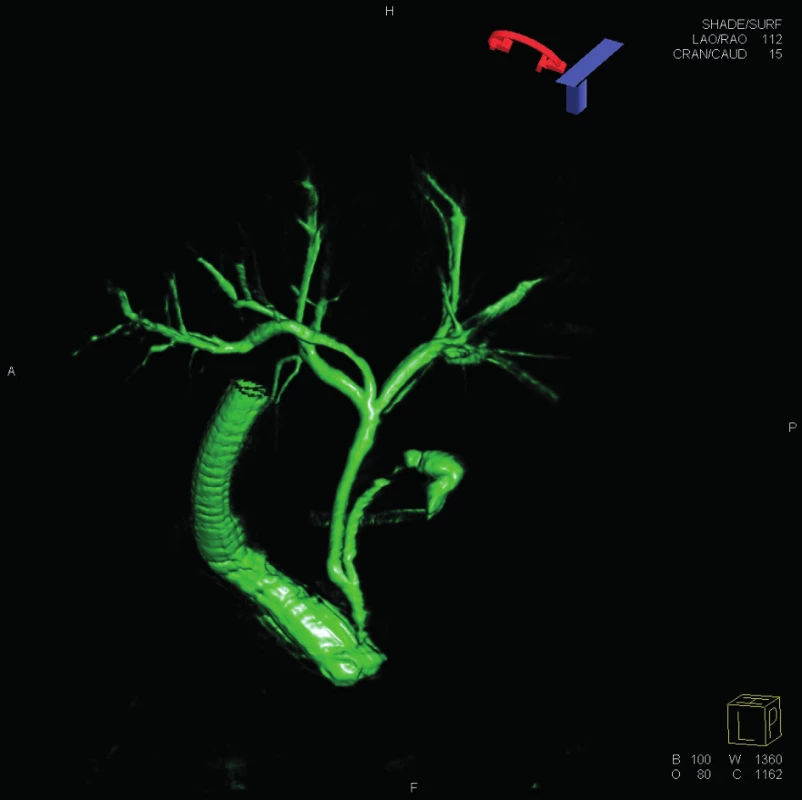
DISKUZE
V chirurgické léčbě těžké akutní pankreatitidy došlo v průběhu let k významným změnám [1,2,3,4].
Dříve platilo, že diagnóza infikované nekrózy pankreatu byla absolutní indikací k neodkladnému chirurgickému debridementu [1,3]. Nejstarší technikou byla laparotomie s nekrektomií a založením konvenční drenáže. Dalším způsobem je technika laparostomie umožňující opakované reexplorace [1,3]. Tato technika byla využívána u rozsáhlých nekróz, kde byl předpoklad dalšího vývoje. Jinou užívanou metodou byla laparotomie a následné lavážní techniky v různých obměnách. Mylně se myslelo, že bez nekrektomie povede infikovaná nekróza k téměř 100% mortalitě [1]. Postupně docházelo k odklonu od velkých chirurgických zákroků. Stejně tak docházelo i ke změnám názoru na timing výkonu – zatímco dříve byla zastávána urgentní intervence co nejdříve po diagnóze rozsáhlé nekrózy pankreatu (i sterilní, k zamezení její infekce), později se chirurgická intervence časovala s odstupem 3–4 týdnů od začátku onemocnění [3]. Bylo prokázáno, že mortalita výkonu je při časné indikaci výrazně vyšší [3].
S rozvojem radiologických a endoskopických metod docházelo k postupnému vývoji méně invazivních metod debridementu, jako jsou laparoskopický chirurgický výkon z předního nebo retroperitoneálního přístupu, transkutánní drenáž doplněná o videoasistovanou nekrektomii a endoskopická drenáž [2,3,4]. Výsledky provedených studií vykazují mortalitu chirurgického zákroku ve srovnání s miniinvazivními metodami 54 vs. 23 % [1]. K diagnostice infikované nekrózy již není nutné provádět předchozí aspiraci, vzorek k histologickému vyšetření obvykle nabíráme při miniinvazivní intervenci. Z hlediska timingu je u pacienta s infikovanou nekrózou ve stabilním stavu preferováno vyčkat s intervencí a provádět ji až po 4 týdnech od vzniku nekrózy (pro větší pravděpodobnost dosažení kolikvace nekrózy a její ohraničení fibrózní stěnou – „walled-off pancreatic necrosis“) [1,2,3]. Během této doby jsou podávána intravenózní antibiotika s dobrou penetrací do pankreatické tkáně. Při výrazném ústupu klinických obtíží a makroskopického nálezu není nutné intervenční výkon doplňovat [1,2,3,4]. I v případě nálezu abscesu lze postupovat miniinvazivně s využitím antibiotické terapie a drenáže. Úspěchu je takto dosaženo u 20–50 % pacientů [4].
Jednotlivé typy miniinvazivních přístupů mohou být vzájemně kombinovány – současně či sekvenčně [1,2]. Recentní nizozemská studie demonstrovala snížení morbidity i nákladů při step-up využití perkutánní katetrizační drenáže následované videoasistovaným retroperitoneálním debridementem.
Pozdní komplikací perkutánní drenáže může být vznik pankreatických zevních či vnitřních píštělí, z nichž část se uzavírá spontánně. Velký problém však představují perzistující zevní pankreatické píštěle.
U našeho pacienta jsme vzhledem k rozsáhlé nekróze pankreatu nepoužili v prvním kroku metodu, kterou jinak běžně užíváme (endosonograficky kontrolovanou drenáž), ale zvolili jsme perkutánní přístup. Analgosedace jsme dosahovali podáním benzodiazepinu (midazolam 5 mg i.v.) v kombinaci s opioidy (sufentanyl 4 ml i.v. či alfentanyl 1 mg i.v.). Po dosažení uspokojivé nekrektomie jsme z obav ze vniku píštělí perkutánní přístup zrušili a pseudocystu v oblasti těla a kaudy pankreatu jsme již řešili běžným endosonograficky kontrolovaným výkonem. Při načasování intervenčního zákroku jsme dodrželi doporučovaný časový odstup od vzniku onemocnění vhodný k dosažení organizace a ohraničení nekrózy.
Pacient je nyní bez subjektivních obtíží, na MR lze identifikovat prakticky jen hlavu pankreatu, sekundární diabetes mellitus vyžaduje podávání jen nízkých dávek insulinu, není nutno podávat pankreatické enzymy.
Závěr
V námi uvedené kazuistice popisujeme řešení lokálních komplikací těžké akutní pankreatitidy u morbidně obézního pacienta za pomoci kombinace miniinvazivních metod – perkutánní retroperitoneální drenáže kolikvované složky nekrózy, videoasistované perkutánní endoskopické nekrektomie solidních hmot, pseudocystogastrostomie a posléze i drenáže peripankreatického abscesu cestou pankreatického vývodu. Zatímco v minulosti byl preferován časný chirurgický otevřený výkon, v současné době je k řešení komplikací těžké akutní pankreatitidy multidisciplinárním konsenzem preferován miniinvazivní přístup, pokud možno prováděný až po 4 týdnech od počátku onemocnění, kdy je předpokládáno ohraničení nekrózy či pseudocysty. Řada pacientů se přitom klinicky zlepší i při pouhé intravenózní antibiotické terapii a dále již nevyžaduje intervenční výkon.
MUDr. Lenka Doležalová
Endoskopické centrum, Oblastní nemocnice Kolín a.s.
Žižkova 146, 28002,
Kolín II
e-mail: d.olezalova.lenka@seznam.cz
Zdroje
1. Tenner S, Baillie J, DeWitt J, et al. American College of Gastroenterology Guideline: Management of Acute Pancreatitis. The American Journal of gastroenterology 2013;9 : 1400-1413.
2. Špičák J. Léčba akutní pankreatitidy [on line]. Dostupný z www: http://zdravi.e15.cz/clanek/priloha-lekarske-listy/lecba-akutni-pankreatitidy-452141.
3. Kostka R. Možnosti chirurgické léčby nekrotizující pankreatitidy [on line]. Dostupný z www: http://www.hpb.cz/index.php? pId=07-1-05.
4. Szentkereszty Z, Kotán R, Sápy P. The role of percutaneous drainage in the treatment of severe acute pancreatitis on the bases of the modified Atlanta Classification [on line]. Dostupný z www: http://bib.irb.hr/datoteka/574951.Acute_Pancreatitis.pdf.
5. Kašpar M, Horák M. Perkutánní drenáž – možnost léčby akutní pankreatitidy [on line]. Dostupný z www: http://www.zdravky. cz/zpravodajstvi/lekarske-listy-plus/perkutanni-drenaz-moznost-lecby-akutni-pankreatitidy.
6. Tenner S, Steinberg WM. Acute pancreatitis. In: Sleisenger and Fordtranęs. Gastrointestinal and liver disease. Ninth edition. Canada, Saunders 2010 : 959–983.
7. Ferreira LE, Baron TH. Endoscopic treatment of pancreatic disease. In: Sleisenger and Fordtranęs. Gastrointestinal and liver disease. Ninth edition. Canada, Saunders 2010 : 1035–1038.
8. Krška Z. Akutní pankreatitida – komplexní problematika. Rozhl Chir 2012;12 : 692 – 696.
9. Špičák J. Akutní pankreatitida. Praha, Grada 2005.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek ÚvodČlánek Komplikace hemoroidůČlánek Akutní periproktální abscesyČlánek Poranění anorekta
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2014 Číslo 4- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Jak souvisí postcovidový syndrom s poškozením mozku?
- Hojení análních fisur urychlí čípky a gel
-
Všechny články tohoto čísla
- Agentura pro zdravotnický výzkum a grantové projekty na léta 2015–2020
- Chirurgická léčba rektokély – mnoho technik, málo jednoznačných závěrů
- Plicní metastázy – dvanáctileté zkušenosti s chirurgickou léčbou
- Pilotní studie: korekce levátorového hiátu anální páskou jako chirurgická metoda léčby střevní inkontinence
- Dlouhodobé výsledky po klasických plastikách malých pupečních kýl
- Primář Jiří Kunášek oslavil 85. jubileum
- Endometrióza hrubého čreva – kazuistika
- Těžká akutní pankreatitida – řešení komplikací kombinací miniinvazivních přístupů
- Priebojníkové excízie v dermatológii a dermatopatológii
- Úvod
- Komplikace hemoroidů
- Akutní periproktální abscesy
- Poranění anorekta
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Akutní periproktální abscesy
- Chirurgická léčba rektokély – mnoho technik, málo jednoznačných závěrů
- Komplikace hemoroidů
- Plicní metastázy – dvanáctileté zkušenosti s chirurgickou léčbou
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



