-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaKolorektální karcinom na I. chirurgické klinice VFN Praha
Autoři: V. Frýba 1; R. Fraško 1; D. Hoskovec 1; Z. Krška 1; D. Schmidt 1; E. Sedláčková 1
Působiště autorů: I. chirurgická klinika 1. LF UK a VFN v Praze, přednosta: prof. MUDr. Zdeněk Krška, CSc. 1; Onkologická klinika 1. LF UK a VFN v Praze, přednosta: Prof. MUDr. Luboš Petruželka, DrSc. 2
Vyšlo v časopise: Rozhl. Chir., 2012, roč. 91, č. 5, s. 290-293.
Kategorie: Postgraduální vzdělávání
ÚVOD
Kolorektální karcinom ve světě a v České republice
Kolorektální karcinom (CRC) je celosvětově třetím nejčastěji diagnostikovaným zhoubným nádorem u mužů a druhým nejčastějším u žen, s největší incidencí v rozvinutých zemích Evropy a Severní Ameriky, Austrálie a na Novém Zélandu. Jedná se o nádor s největší prevalencí z nádorů zažívacího traktu a logicky tak stojí v centru pozornosti lékařů [1].
Podle dat z Národního onkologického registru je ročně v ČR diagnostikováno 7900–8100 pacientů s CRC, z toho téměř 60 % ve III. a IV. stadiu onemocnění. 4300–4500 nemocných s CRC ročně zemře. Prevalence dosáhla v roce 2006 hodnoty 42 341 osob a od roku 1995 tak vzrostla o 91 %. Přežití pacientů s diagnózou CRC se v posledních 15 letech významně zlepšilo. Medián přežití u generalizovaného nádoru vrostl z 6 měsíců na 2 roky. Prostředkem, jak zastavit epidemiologickou explozi CRC, je vedle změny stravovacích návyků a životního stylu zejména plošný screening, který zachytí přednádorové stavy a časná stadia onemocnění [2].
MATERIÁL A METODA
Screening
V České republice byl celoplošný screening založený na testu na okultní krvácení ve stolici (TOKS) zaveden v roce 2000, od ledna 2009 zaznamenal screeningový program řadu změn. Osoby ve věku 50–54 let mohou absolvovat screeningový TOKS (guajakový či imunohistochemický) každý rok, od 55 let TOKS jednou za 2 roky. Nemocný si v 55 letech může zvolit primární screeningovou koloskopii na akreditovaném pracovišti. Koloskopie má především stratifikační význam. Rozdělí pacienty do skupiny nízkého rizika s kontrolou za 10 let, středního rizika s kontrolou za 3–5 let a vysokého rizika s kontrolami v intervalu 6–24 měsíců. Záleží na tom, zda je nález zcela negativní, jsou zachyceny běžné polypy, nebo dysplázie a adenomy, které lze hodnotit jako prekancerózy. Tyto léze jsou v rámci koloskopie odstraněny a histologicky vyšetřeny.
Diagnostika
Nejdůležitější postavení v diagnostice CRC má v současné době koloskopie. Zkušený endoskopista je schopen odlišit hyperplastické léze, adenomy a karcinomy. Neoplázii bez invaze do submukózy lze odstranit metodami endoskopické polypektomie (EPE), endoskopické slizniční resekce (EMR) nebo endoskopické submukózní disekce (ESD). Neoplázie s masivní submukózní invazí vyžadují chirurgické řešení. Při histologicky potvrzeném CRC je nutno provést předepsaná stagingová vyšetření, tedy stanovit lokální rozsah nádoru (T), postižení lymfatických uzlin (N) a vyloučit vzdálené metastázy (M). U nádorů tlustého střeva nám tyto informace doplňující koloskopii poskytne CT břicha a malé pánve s rentgenem plic. Daleko přesnější informaci o lokálním rozsahu nádoru potřebujeme v rozhodovacím procesu o terapii v případě lokalizace nádoru v dolních dvou třetinách rekta. Zde je nutno posoudit, zda budeme schopni provést totální mezorektální excizi (TME) přímo, či zda je nutná neoadjuvantní chemoradioterapie. Hloubku invaze do stěny rekta a vztah invaze nádoru k mezorektální fascii a ke svěračům a postižení uzlin nejlépe zhodnotí magnetická rezonance (NMR) [3]. Nemocní s postižením uzlin, s infiltrací nádoru menší než 1 mm od mezorektální fascie a infiltrací nádoru do intersfikterické roviny nejsou vhodní k primárnímu chirurgickému výkonu. PET/CT pro stanovení lokálního rozsahu onemocnění nepřináší žádné nové informace a je vhodné spíše k vyšetření rozsahu metastatického postižení. Součásti předoperačního stagingu by měl být i odběr nádorových markerů CEA a Ca 19.9. Nezbytnou součástí vyšetření je rovněž pečlivé odebrání rodinné anamnézy k vyloučení geneticky podmíněných syndromů, při podezření na ně odeslání pacienta na genetické vyšetření.
Terapie
I v dnešní době má chirurgie v terapii CRC zásadní význam, ačkoli je zcela správně kladen důraz na interdisciplinární spolupráci, která jako jediná může přinést další zlepšení léčebných výsledků. Cílem chirurgické léčby je úplné odstranění primárního nádoru s disekcí spádových lymfatických uzlin, event. radikální odstranění vzdálených metastáz, tedy R0 resekce. U nádorů céka a vzestupného tračníku je prováděna pravostranná hemikolektomie, pro nádory jaterního ohbí a přilehlé části transverza rozšířená pravostranná hemikolektomie. Resekce příčného tračníku je málo častá pro nízký výskyt nádorů v této lokalizaci. Nádory lokalizované v lienální flexuře a sestupném tračníku vyžadují levostrannou hemikolektomii, nádory sigmatu jsou indikací k resekci sigmatu a nádory rectosigmoideálního přechodu a proximálních 2/3 rekta pro nízkou resekci. Stran onkologické radikality jsou poněkud kontroverzní velmi nízké resekce v dolní polovině až třetině rekta. Variantou k velmi nízkým resekcím je abdominoperineální amputace rekta dle Milese s trvalou sigmoideostomií. Jednoznačnou indikací k amputaci je primární dysfunkce svěračů s inkontinencí, nádorová infiltrace svěračů a nediferencované formy karcinomu postihující dolní třetinu rekta.
Pokroky v neoadjuvantní chemoradioterapii a technický rozvoj staplerového instrumentária umožnily akceptovat z hlediska radikality kontinentní resekci 2 cm, podle některých prací i 1 cm pod tumorem, oproti původně proklamované 5cm hranici pod nádorem z 80–90 let. Na druhou stranu je pravdou, že nemocní s karcinomem distálního rekta po neoadjuvantní chemoradioterapii mají často nefunkční svěrače, takže amputační výkon jim může mnohdy zajistit lepší kvalitu života než velmi nízká resekce [4, 5]. Při vícečetných synchronních nádorech tračníku, u nemocných s familiární polypózou (FAP) nebo s hereditárním nepolypózním kolorektálním karcinomem (HNPCC), je indikována kolektomie, při současném postižení konečníku proktokolektomie s trvalou ileostomií nebo ileo-pouch anální anastomózou (IPAA). V centru zájmu chirurgů i onkologů stojí v současné době resekční výkony při metastatickém postižení jater (viz článek Vývoj operativy onemocnění jater a žlučových cest) [6, 7].
Onkologická léčba
Předoperační (neoadjuvantní) radioterapie je indikována u nemocných s nádory rekta prorůstajícími celou stěnou do perirektálního tuku a/nebo s invazí do lymfatických uzlin [8]. Našimi specialisty z Onkologické kliniky VFN je nejčastěji používána aplikace 50–60Gy během 6–7 týdnů v kombinaci s chemoterapií. Operace následuje za 6–8 týdnů. Právě po této vysoké dávce s dobrým efektem na lokální kontrolu je však častá inkontinence.
Adjuvantní chemoterapie je u CRC jednoznačně indikována při postižení lymfatických uzlin (st. III) nebo u nádorů st. II prorůstajících do okolí T4NOMO. Pro ostatní nádory st. II její přínos není jednoznačný. Doporučuje se, předcházel-li ileozní stav, perforace střeva nebo když je přítomna nízká diferenciace nádoru, perineurální šíření, angioinvaze nebo lymfangioinvaze. Nejúčinnějším adjuvantním režimem je kombinace FOLFOX 4 (5-fluorouracil/leukovorin/oxaliplatina), jeho nevýhodou je senzorická neuropatie po oxaliplatině. Lze použít De Gramontův režim (kombinace bolusového a kontinuálního fluorouracilu s leukovorinem) a kapecitabin v monoterapii, zvláště u starších a komorbidních nemocných nevhodných pro kombinovanou terapii. Intermitentní podávání chemoterapie v adjuvantním podání trvá cca půl roku, tj. např. 12 cyklů chemoterapie FOLFOX 4 ve 14denních intervalech. Strategie léčby pokročilého CRC přesahuje rámec tohoto sdělení.
Tab. 1. Počty provedených výkonů na I. chirurgické klinice VFN Praha v letech 2000–2010 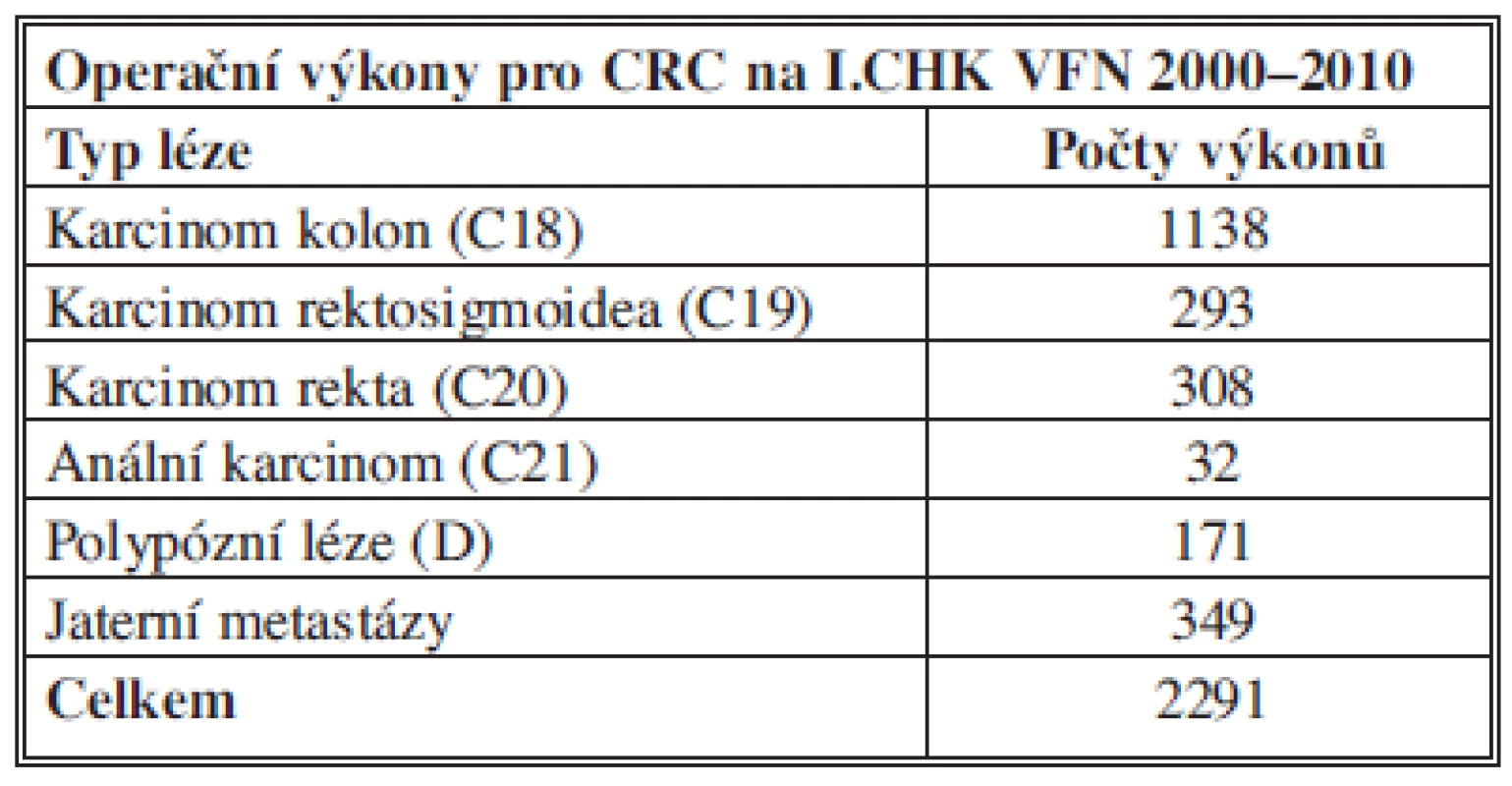
Tab. 2. Odoperovaní pacienti v roce 2011 podle stadia onemocnění 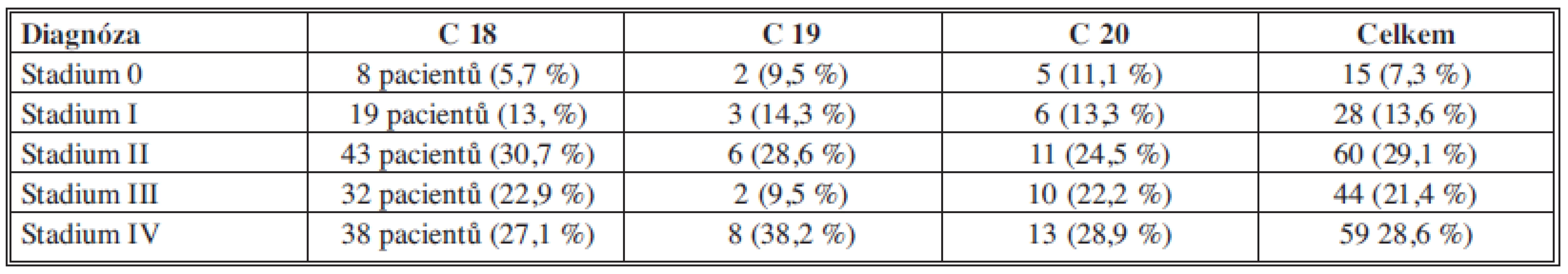
VÝSLEDKY
Celkový počet pacientů s diagnózou CRC odoperovaných na I. chirurgické klinice VFN v letech 2000–2010 byl 2291. V posledním sledovaném roce 2011 bylo operováno 206 pacientů s CRC. Když srovnáme typy provedených operací v roce 2001 a 2011, nejčastěji prováděnými výkony pro tuto diagnózu zůstávají pravostranná hemikolektomie (19, resp. 23 %), resekce sigmatu (20 %), nízká přední resekce (21, resp. 9 %). Zajímavý je nárůst počtu jaterních resekcí z 6 na 13 %.
Při porovnání akutních operací pro CRC bylo v roce 2001 provedeno celkem 25 výkonů. Z toho byla provedena 5krát bypassová operace, 6krát resekční výkon s anastomózou a 14krát byla založena stomie. Z celkového počtu operovaných v roce 2001 (129 nemocných) tvoří těchto 25 nemocných 19 % (Graf 1). V roce 2011 bylo akutně operováno celkem 16 pacientů. Z toho byl proveden 8krát resekční výkon s anastomózou, 3krát Hartmannova operace a 5krát byla založena stomie. Z celkového počtu operovaných v roce 2011 (206 pacientů) tvoří těchto 16 nemocných 7,8 % (Graf 2). Podíl miniinvazních výkonů pro CRC v roce 2011 činil 18 %.
Graf 1. Spektrum operačních výkonů pro CRC 2001 
Graf 2. Spektrum operačních výkonů pro CRC 2011 
DISKUZE
CRC na I. chirurgické klinice
Naši pacienti s verifikovaným CRC jsou standardně prezentováni na pravidelném indikačním semináři, kde je ve spolupráci s gastroenterologem, onkologem a radiodiagnostikem navržena optimální terapie. Pacienti indikovaní k chirurgickému výkonu jsou operování v následujících 1–2 týdnech. U primárních tumorů provádíme celé spektrum resekčních výkonů otevřeným způsobem či laparoskopicky. U tumorů v oblasti rekta ve stadiu Tis a T1 provádíme transanální výkony endoskopickou cestou (TEM) [8]. U pokročilých nádorů pak kryodestrukci jako paliativní zákrok, u pacientů s resekabilní recidivou CRC exstirpaci lokoregionálních recidiv, u metastatického postižení jater resekční výkony jater, dále i RFA (radiofrekvenční ablace – zničení nádorového ložiska působením tepelného účinku vysokofrekvenčního proudu ve vymezeném okrsku tkáně) a IRE (miniinvazní technologie, při které je využívána metoda tzv. ireverzibilní elektroporatizace, kdy nedochází k negativním termickým efektům na okolní tkáně) [10, 11, 12]. V souvislosti s CRC a operacemi na rektu je nutno zmínit účast chirurgů naší kliniky na onkogynekologických výkonech, kdy za poslední 3 roky bylo provedeno 35 resekcí rektosigmoidea či rekta v rámci zadních či totálních exenterací pánve [13, 14, 15].
ZÁVĚR
Operace pro CRC jsou rutinními výkony na našem chirurgickém pracovišti s přibližně 200 odoperovanými pacienty ročně. Pokles akutně operovaných nemocných v desetiletém srovnání si vysvětlujeme zlepšením předoperační přípravy pacienta umožňující často elektivní výkon, z části se podílejí screeningové programy [16]. Naopak zřetelně narůstající množství jaterních resekcí pro CRC v souboru u nás operovaných a sledovaných pacientů je nejspíše dáno vysokou prevalencí pacientů s touto diagnózou a zároveň rozvojem onkologické léčby a tím prodlouženým přežíváním generalizovaných nemocných. Mírně nižší podíl miniinvazivních výkonů (18 % v roce 2011) je dán spektrem našich pacientů, u kterých je resekce kolon často spojena s výkonem na játrech. I. chirurgická klinika funguje jako superkonziliární pracoviště, kde jsou operováni nemocní s množstvím komorbidit, které jsou limitujícím faktorem pro laparoskopický přístup.
Zhruba 50 % odoperovaných pacientů v roce 2011 bylo ve III. a IV. stadiu, což odpovídá celorepublikovým statistikám [2].
MUDr. Vladimír Frýba
I. chirurgická klinika 1. LF UK VFN
U Nemocnice 2
128 08 Praha 2
e-mail: vladimir.fryba@vfn.cz
Zdroje
1. Becker HD, Hohenberger W, Junginger T, et al. Chirurgická onkologie, 1. Vydání, Praha, Grada, 2005 : 457–545.
2. Národní onkologický registr, www.uzis.cz.
3. Taylor FG, Quirke P, Heald RJ, et al. MERCURY study group.: One millimetre is the safe cut-off for magnetic resonance imaging prediction of surgical margin status in rectal cancer Br J Surg 2011 Jun;98(6):872–9. doi: 10.1002/bjs.7458. Epub 2011 Apr 8.
4. Do L, Syed N, Puthawala A, et al. Low-lying rectal cancer with anal canal involvement: abdominoperineal or low anterior resection after neoadjuvant chemoradiotherapy, Gastrointest Cancer Res. 2011;4(3):90–95.
5. Glättli A, Barras JP, Metzger U. Is there still a place for abdominoperineal resection of the rectum? Eur J Surg Oncol 1995;21(1):11–5.
6. Gallagher DJ, Kemeny M. Improving response and outcomes for patients with liver-limited metastatic colorectal cancer, Clin Colorectal Cancer 2010;9 Suppl 1:S36–43.
7. Grothey A. Medical treatment of advanced colorectal cancer in 2009, Ther Adv Med Oncol 2009 Sep;1(2):55–68.
8. Ondrák M, Šefr R, Eber Z. Transanální endoskopická mikrochirurgie a její postavení v chirurgii rekta – review. Rozhl Chir 2011;90 : 450–6.
9. Velenik V, Ocvirk J, Music M, et al. Neoadjuvant capecitabine, radiotherapy, and bevacizumab (CRAB) in locally advanced rectal cancer: results of an open-label phase II study. Radiat Oncol 2011;(31)6 : 105.
10. Wiggermann P, Jung EM, Stroszczynski C. Radiofrequency ablation? is a technique finished? Radiologe 2012;52(1):9–14.
11. Künzli BM, Abitabile P, Maurer CA. Radiofrequency ablation of liver tumors: Actual limitations and potential solutions in the future. World J Hepatol 2011;3(1):8–14.
12. Govindarajan N. Irreversible Electroporation for Treatment of Liver Cancer, Gastroenterol Hepatol (NY) 2011;(5):313–316.
13. De Wever I. Pelvic exenteration: surgical aspects and analysis of early and late morbidity in a series of 106 patients. Acta Chir Belg 2011;111(5):273–81.
14. Ferenschild FT, Vermaas M, Verhoef C. Total pelvic exenteration for primary and recurrent malignancies. World J Surg 2009;33(7):1502–8.
15. Gürlich R, Cibula D, Babjuk M, et al. Exenterační výkony v pánvi. Rozhl Chir 2005;84 : 403–09.
16. Sasaki K, Kazama S, Sunami E, et al. One-stage segmental colectomy and primary anastomosis after intraoperative colonic irrigation and total colonoscopy for patients with obstruction due to left-sided colorectal cancer. Dis Colon Rectum 2012;55(1):72–8.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek Úvodní slovo
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2012 Číslo 5- Význam intraartikulární viskosuplementace kyselinou hyaluronovou u obézních pacientů s osteoartrózou kolene
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Vliv regulace pH na snížení výskytu peristomálních komplikací a bolesti
- Sinogel: Nová synergie v léčbě osteoartikulárních onemocnění
-
Všechny články tohoto čísla
- Úvodní slovo
- Prevence TEN v chirurgii, prolongovaná tromboprofylaxe
- K úmrtí profesora MUDr. Zbyňka Vobořila, DrSc.
- Developments in pancreatic surgery at the 1st Surgical Department 1st Faculty of Medicine, Charles University and General University Hospital in Prague
- Outcomes of complex therapy in female patients after breast-saving surgery for breast carcinoma at the 1st Surgical Department 1st Faculty of Medicine, Charles University and General University Hospital in Prague during a ten-year follow up period
- Zlomeniny pilonu tibie – krátké shrnutí problematiky a kazuistiky
- Dějiny traumatologie na I. chirurgické klinice v Praze
- Stoletý krok v chirurgické léčbě ileózních stavů
- Chirurgická onemocnění jícnu a žaludku na prahu 21. století
- Kolorektální karcinom na I. chirurgické klinice VFN Praha
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Prevence TEN v chirurgii, prolongovaná tromboprofylaxe
- Zlomeniny pilonu tibie – krátké shrnutí problematiky a kazuistiky
- Stoletý krok v chirurgické léčbě ileózních stavů
- Chirurgická onemocnění jícnu a žaludku na prahu 21. století
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



