-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Chirurgická technika odběru tenkého střeva pro transplantaci
Surgical Harvesting of Small Bowel Intended for Transplantation
The small intestine transplantations represent a logical alternative to final total parenteral nutrition in patients with chronic intestinal failures. It is considered a life - saving procedure in patients with intestinal failure, where standard treatment procedures cannot be further implemented. Perfect harvesting technique is very important for succesful clinical small bowel transplantation. The authors studied the surgical view of the small intestinal transplant harvesting and monitored differences in ischemic injuries to jejunum and ileum depending on duration of the cold ischemia time. The study is one of the inital works in the planned intestinal transplantation clinical programme.
Key words:
small intestine transplantation – surgical collection technique – ischemic injury
Autoři: M. Kudla; P. Baláž; M. Oliverius; M. Adamec
Působiště autorů: Klinika transplantační chirurgie IKEM, přednosta: prof. MUDr. M. Adamec, CSc.
Vyšlo v časopise: Rozhl. Chir., 2007, roč. 86, č. 6, s. 297-299.
Kategorie: Monotematický speciál - Původní práce
Souhrn
Transplantace tenkého střeva představuje logickou alternativu k definitivní totální parenterální výživě u pacientů s chronickým střevním selháním. Považuje se za život zachraňující zákrok u pacientů se střevním selháním, kteří nemohou být již dále léčeni standardními postupy. Předpokladem úspěšné transplantace je dokonale zvládnutá technika odběru. V naší studii jsme se zabývali chirurgickou stránkou odběru štěpu tenkého střeva a sledováním rozdílu ischemického poškození jejuna a ilea v závislosti na době studené ischemie. Projekt je jedním z prvních kroků v připravovaném klinickém programu transplantace střeva.
Klíčová slova:
transplantace tenkého střeva – chirurgická technika odběru – ischemické poškozeníÚVOD
Transplantace tenkého střeva (TxS) je indikována u pacientů s ireverzibilním selháním střeva, kde lze očekávat smrt do jednoho roku při léčbě totální parenterální výživou. Mezi nejčastější indikace k TxS patří tzv. syndrom krátkého střeva, různé geneticky podmíněné dysfunkce enterocytů a ztráta motility střeva [1]. V posledních letech došlo k výraznému zlepšení přežívání pacientů i štěpů tenkého střeva. Bylo dosaženo jednoroční přežití štěpů i příjemců přes 80 % [2]. Díky tomu transplantace tenkého střeva opustila pole experimentální a stala se standardní metodou léčby pacientů se střevním selháním. Dobrý výsledek TxS je určen souhrou několika faktorů. Základním předpokladem je kvalitní odběr střevního štěpu, minimalizace prezervačního poškození, dobře technicky provedená transplantace a včasné zachycení pooperačních komplikací (chirurgické komplikace časné i pozdní, rejekce, infekce …) a jejich účelná léčba. V naší studii jsme se zaměřili na zvládnutí chirurgické techniky odběru tenkého střeva u kadaverózního dárce a na stanovení stupně ischemického poškození střevního štěpu.
MATERIÁL A METODY
Provedli jsme odběr tenkého střeva u 6 dárců splňujících kritéria pro multiorgánový odběr. Průměrný věk dárců činil 58 let (32–71 let). Poměr muži: ženy činil 2 : 4. Jako příčina smrti mozku se vyskytlo 3x intracerebrální krvácení, 2x asfyxie a 1x kraniotrauma. Po odběru a perfuzi celého tenkého střeva roztokem Custodiolu jsme odebrali 5 kusů 10 cm dlouhých vzorků jejuna (skupina A) a 5 kusů 10 cm dlouhých vzorků ilea (skupina B). Tyto vzorky jsme skladovali v roztoku Custodiolu při teplotě 4 °C po dobu 1, 6, 9, 12 a 24 hodin (doba studené ischemie). Po této době jsme provedli histologické vyšetření vzorků standardní technikou (fixace v 10% formalinu, zalití do parafínových bločků, vytvoření 3–5 μm tenkých řezů a jejich obarvení hematoxylin-eosinem) a hodnotili jsme stupeň morfologického poškození podle Parkovy klasifikace [3] (Tab. 1).
Tab. 1. Histopatologické hodnocení transplantovaného střeva podle Parka Tab. 1. Histopathological assessment of the transplanted intestine according to Park 
CHIRURGICKÁ TECHNIKA ODBĚRU TENKÉHO STŘEVA
Ve většině případů je odběr střeva určeného k transplantaci součástí multiorgánového odběru. V naší pilotní studii jsme prováděli odběr pouze u pacientů, u kterých byl indikován izolovaný odběr ledvin a v žádném případě nesmělo dojít ke zhoršení kvality odebíraných ledvin.
Střední laparotomií od procesus xyphoideus k symfyse si vytvoříme dostatečný přístup do břišní dutiny. Nejprve provedeme důkladnou revizi celé břišní dutiny k odhalení případné malignity dárce či jiných skutečností, které by kontraindikovali odběr. Tenké střevo zabalíme do vlhké teplé roušky a během odběru se snažíme s ním co nejméně manipulovat, protože tenké střevo je orgán extrémně citlivý na veškeré inzulty, které by mohly mít po transplantaci fatální důsledky pro příjemce. Preparací v retroperitoneu a uvolněním kolon descendens včetně hepatální flexury si ozřejmíme a připravíme k pozdější kanylaci subrenální úsek aorty a dolní duté žíly. Mezi ligaturami přerušíme dolní mezenterickou tepnu. Kocherovým manévrem mobilizujeme duodenum a ozřejmíme z laterální strany odstup horní mezenterické tepny (AMS – arteria mesenterica superior) a subhepatální průběh dolní duté žíly. Uvolníme proximální část horní mezenterické tepny, abychom zjistili případný odstup akcesorní pravé jaterní tepny. Kraniálně od horní mezenterické tepny obejdeme aortu a připravíme se na případné okamžité zahájení perfuze orgánů (např. při oběhové nestabilitě pacienta). V případě multiorgánového odběru, jehož součástí je i odběr jater, je třeba aortu obejít těsně pod bránicí. Skeletizujeme mezenterium v oblasti ileocékálního přechodu a podvážeme větve vasa ileocolica jdoucí k céku, zachováme odstupy pro terminální ileum. Závěsnou ligaturou si označíme kaudální konec střevního štěpu těsně před ileocékálním přechodem. Podvážeme a mezi ligaturami přerušíme vasa colica dextra a vasa colica media. Deliberujeme D3 úsek duodena a první jejunální kličku, kde si opět závěsnou ligaturou označíme proximální konec štěpu. Dalším krokem je preparace proximálního úseku vena portae, která vzniká soutokem vena mezenterica superior a vena lienalis. Podvazujeme drobné žíly jdoucí do vena mesenterica superior z duodena a z pankreatu. Střevní štěp nyní tvoří celé tenké střevo od první jejunální kličky až k oblasti terminálního ilea na cévní stopce tvořené arteria mesenterica superior a vena portae. Nyní jsme připraveni ke společné perfuzi ledvin a tenkého střeva. Po celkovém podání heparinu (250 j/kg) infrarenálně zakanylujeme aortu a dolní dutou žílu. Zasvorkujeme či podvážeme aortu nad odstupem arteria mesenterica superior a zahájíme společnou perfuzi střeva a ledvin roztokem Custodiolu. Obvyklé množství spotřebovaného perfuzního roztoku činí 3–5 litrů a je závislé na dokonalé kvalitě perfuze štěpu tenkého střeva, která se projeví odbarvením mezenteria i střevní stěny. Po skončení perfuze zvyklým způsobem explantujeme obě ledviny. Lineárním staplerem či mezi ligaturami přerušíme proximální a distální konec střevního štěpu, odebereme horní mezenterickou tepnu včetně terčíku aorty a přerušíme horní mezenterickou žílu v oblasti soutoku s v. lienalis a štěp vyjmeme a umístíme do roztoku Custodiolu (Obr. l, 2).
Obr. 1. Schéma odběru štěpu tenkého střeva Pic. 1. The small intestine graft collection – A scheme AMS, VMS – a., v. mesenteria superior 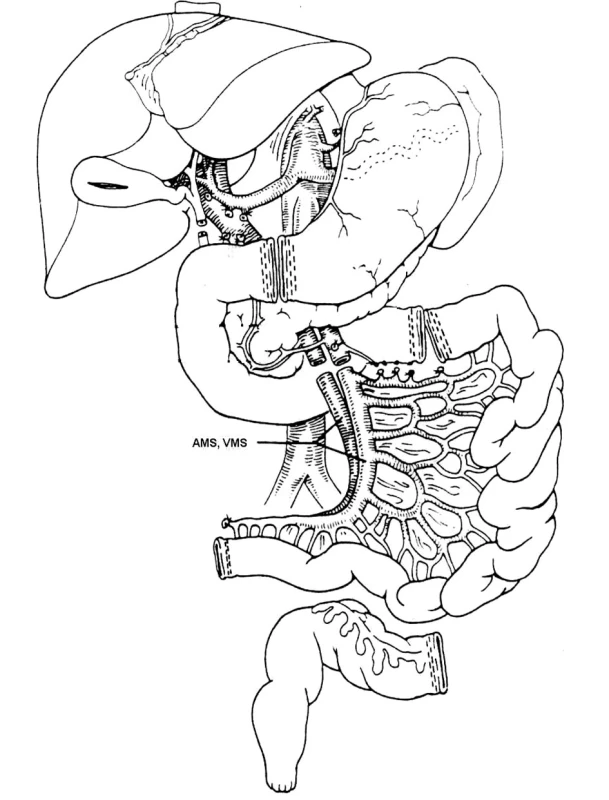
Obr. 2. Odebraný štěp tenkého střeva. V pinzetách a. mesenteria superior a v. mesenteria superior Pic. 2. The collected small intestinal graft. The a. mesenteria superior and v. mesenteria superior held in pincers 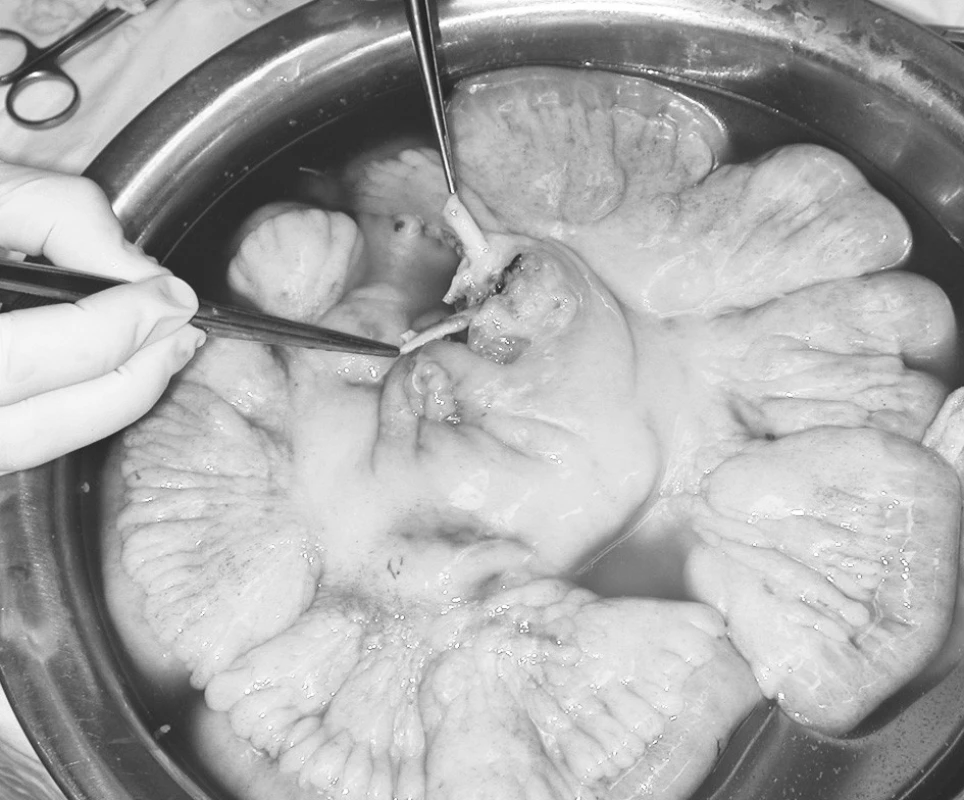
MORFOLOGICKÝ NÁLEZ POŠKOZENÍ STŘEVA
Po zhodnocení histologického obrazu jejuna po jednohodinové studené ischemii činil průměrný stupeň poškození 0,1, po 6 hodinách 2,1, po 9 hodinách 2,1 a po 12 a 24 hodinách 2,5 pro jejunum a 0; 1,1; 1,3; 2 a 2,1 pro ileum (Tab. 2). Mezi skupinou A (jejunum) a skupinou B (ileum) nebylo dosaženo statisticky významného rozdílu (Mannův-Whitneyův test) v žádných časech.
Tab. 2. Stupeň poškození štěpu v závislosti na době studené ischemie Tab. 2. Graft damage depending on the cold ischemia period duration 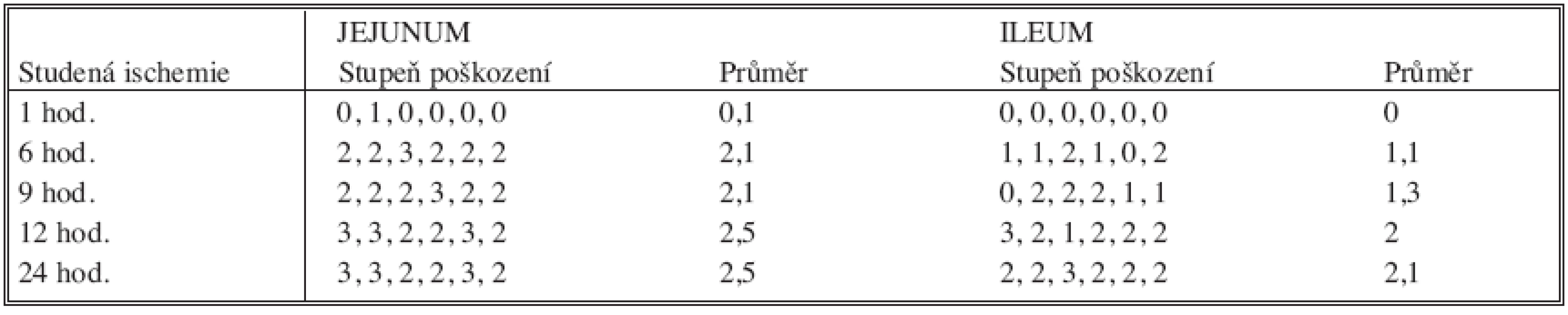
DISKUSE
Hlavním cílem naší práce bylo dokonalé zvládnutí techniky odběru štěpu tenkého střeva z kadaverózního dárce. Projekt je současně jedním z prvních kroků v připravovaném klinickém programu transplantace střeva na našem pracovišti. Jde o operaci, která by zkušenému chirurgovi vyškolenému v transplantační problematice a po nezbytném zácviku neměla činit větší problémy. Je však nutné upozornit na několik úskalí. Během výkonu je třeba věnovat zvýšenou pozornost tepenným anomáliím, jako je například akcesorní pravá jaterní tepna odstupující z horní mezenterické tepny. Přibližně u 1 % populace se vyskytuje společný odstup AMS a truncus coeliacus. Obě tyto anomálie mohou zkomplikovat společný odběr tenkého střeva a jater v rámci multiorgánového odběru, avšak nečiní ho nemožným. Dále je nutné mít celé tenké střevo zabalené v teplé vlhké roušce a manipulovat s ním co možná nejméně, zvláště se vyvarovat tahům za mezenterium, které by mohly mít za následek cévní komplikace po transplantaci, které ve většině případů vedou ke ztrátě štěpu.
Dalším cílem bylo zjistit, zda se liší citlivost jejuna a ilea k ischemickému poškození. Má to význam jednak pro volbu úseku střeva při odběru střeva pro příbuzenskou transplantaci a také je udáván vyšší výskyt rejekcí u orgánů postižených ischemicko - reperfuzním poškozením [4]. Z našich výsledků vyplývá, že není rozdílu v senzitivitě na ischemické poškození jednotlivých úseků tenkého střeva (jejunum vs. ileum). Dále jsme zjistili, že po uplynutí ohodinové studené ischemie již nedochází k tak rychlému prohloubení morfologických změn střeva. Tento výsledek je překvapivý, protože naše předchozí pokusy na potkanech ukazují výrazný nárůst ischemického poškození mezi šestou a devátou hodinou, proto jsme volili i časy odběrů vzorků s důrazem na 9. hodinu [5]. V klinice se udává doba studené ischemie pro transplantaci tenkého střeva v rozmezí 6–12 hodin.
Projekt byl schválen etickou komisí s multicentrickou působností při IKEM a FTNsP pod č.j. 477/04.
Práce byla podpořena grantem IGA MZ ČR -NR/8896-3.
MUDr. M. Kudla
Klinika transplantační chirurgie IKEM
Vídeňská 1958/9
140 21 Praha 4
e-mail: michal.kudla@centrum.cz
Zdroje
1. Kudla, M., Baláž, P., Adamec, M. Transplantace tenkého střeva. Čas. Lék. Čes., 2005, 144 : 438–440.
2. O‘Keefe, S. J. D. Candidacy for Intestinal Transplantation. Am. J. Gastroenterol., 2006, 101 : 1644–1646.
3. Park, P., Wallander, J., Tufveson, G., Haglund, U. Cold ischemia and reperfusion injury in a model of small bowel transplantation in the rat. Eur. Surg. Res., 1991, 23 : 1–8.
4. Boros, P, Bromberg, J. S. New cellular and molecular immune pathways in ischemia/reperfusion injury. Am. J. Transplant., 2006, Apr; 6(4): 652–658.
5. Baláž, P., Matia, I., Jackanin, S., Pomfy, M., Froněk, J., Ryska, M. Morphological changes of small bowel graft in Wistar rats after preservation injury. Bratisl. Lek. Listy, 2004; 105(2): 62–64.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2007 Číslo 6- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Je chirurgie věda nebo řemeslo?
- Komentář
- Pyogenní abscesy jater
- Komplikace laparoskopické apendektomie
- Kontroverze v indikaci chirurgické léčby při akutním krvácení při vředové chorobě gastroduodena
- Odložená rekonstrukce defektů měkkých tkání obličeje
- Chirurgická technika odběru tenkého střeva pro transplantaci
- Benigní lymfoepiteliální cysta pankreatu – kazuistika
- Akutní masivní krvácení z rekanalizované umbilikální žíly jako komplikace portální hypertenze
- Synchrónny nádor rekta a obličky. Kazuistika
- Infikovaná pseudoaneuryzma a. brachialis – raritní kazuistika u dlouholetého intravenózního narkomana
- Laparoskopické řešení epidermoidní cysty sleziny – kazuistika
- Nová evropská norma pro operační roušky a pláště
- Metastatické onemocnění páteře
- Komentář
- Osobní vzpomínka na doc. MUDr. Milana Schücka, CSc.
- Zpráva ze studijní cesty – Leuven 2006
- Zápis z jednání schůze výboru ČCHS dne 9. 2. 2006
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Laparoskopické řešení epidermoidní cysty sleziny – kazuistika
- Komplikace laparoskopické apendektomie
- Pyogenní abscesy jater
- Metastatické onemocnění páteře
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



