-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Máme v roce 2009 dostatek důkazů o tom, zda nemocným indikovaným k srdeční resynchronizační léčbě implantovat biventrikulární kardiostimulátor nebo kardioverter-defibrilátor?
Do we have sufficient evidence in 2009 to decide whether to implant biventricular pacemaker or cardioverter-defibrillator to cardiac resynchronization therapy patients?
Do we have sufficient evidence in 2009 to decide whether to implant biventricular pacemaker or cardioverter-defibrillator to cardiac resynchronization therapy patients? Cardiac resynchronization therapy represents one of the standard non‑pharmacological treatment of severe heart failure in patiens with significant left ventricle dysfunction and ventricular dyssynchrony. The choise of device has to consider the potential benefit of the therapy – the comorbidities, the life expectancy but also the cost‑effectiveness and the potential complications related to the device. New devices provide information about the hemodynamical status of this heart failure patient population allowing early detection of heart failure decompensation – for example using home monitoring – avoiding recurrent hospitalisations from this reason. Based on analysis of recent clicinal studies, in 2009 we do not have enough data if for patients with CRT indication is the biventricular ICD better compared to the biventricular pacemaker. The only one exception are patients with end‑stage heart failure, NYHA IV class, where the implant of biventricular pacemaker is preferred.
Keywords:
cardiac resynchronization therapy – heart failure – ICD – pacemaker
Autoři: M. Táborský; P. Neužil
Působiště autorů: Kardiocentrum, Nemocnice Na Homolce, Praha
Vyšlo v časopise: Kardiol Rev Int Med 2009, 11(1): 16-19
Souhrn
Srdeční resynchronizační léčba představuje v současné době jednu ze standardních variant nefarmakologické léčby pokročilého srdečního selhání u pacientů s významnou systolickou dysfunkcí levé komory srdeční a komorovou dyssynchronií. Při výběru systému je nutné brát v úvahu potenciální přínos zvolené léčby, doprovodná onemocnění, předpokládanou dobu přežívání pacienta, ale také efektivnost nákladů a výskyt možných komplikací spojených s použitím zvoleného přístroje. Nové implantáty v současnosti poskytují informace o hemodynamickém stavu pacientů trpících srdečním selháním a umožňují tak detekovat dekompenzaci srdečního selhání v raném stadiu – např. pomocí domácího monitoringu – a zabránit opakovaným hospitalizacím pacientů z tohoto důvodu. Na základě analýzy výsledků současných klinických studií nemáme v roce 2009 dostatek důkazů, že pro nemocné s indikací srdeční resynchronizační léčby je jednoznačně lepší ICD ve srovnání s kardiostimulátorem. Jedinou výjimku tvoří nemocní v terminální fázi srdečního selhání, NYHA IV klasifikace, kde je jednoznačně preferována implantace biventrikulárního kardiostimulátoru.
Klíčová slova:
srdeční resynchronizační léčba – srdeční selhání – ICD – kardiostimulátorÚvod
Srdeční resynchronizační léčba se stala od konce 90. let jednou z plně akceptovaných variant nefarmakologické léčby pokročilého srdečního selhání u nemocných refrakterních na medikamentózní léčbu s průkazem systolické dysfunkce levé komory a komorové dyssynchronie [1–2]. Vede ke zmírnění symptomů, vyšší toleranci zátěže a lepší kvalitě života [3–7]. Srdeční resynchronizační léčba má také příznivý vliv na remodelaci levé komory do tří měsíců, kdy dochází k významnému snížení end systolického a end diastolického objemu levé komory a k signifikantnímu zvýšení ejekční frakce (EF) levé komory [3–7]. Na základě nedávných studií, které byly navrženy speciálně s cílem vyhodnotit vliv srdeční resynchronizační léčby na morbiditu a mortalitu, bylo prokázáno podstatné zkrácení hospitalizace, zejména z důvodu dekompenzovaného městnavého srdečního selhání, a významné snížení rizika úmrtí ze všech příčin a náhlé srdeční smrti, a to včetně případů, kdy při srdeční resynchronizační léčbě nedocházelo prokazatelně ke kardioverzi a defibrilaci [6–8], což je velmi zajímavá skutečnost.
V posledních deseti letech došlo k zásadnímu technickému pokroku v oblasti srdeční resynchronizační léčby. Nové speciálně navržené účelové nástroje, jako jsou vodicí pouzdra určená ke katetrizaci koronárního sinu nebo levokomorové elektrody zaváděné pomocí ultratenkého vodiče původně určeného pro perkutánní transluminální koronární angioplastiky (Percutaneous Transluminal Coronary Angioplasty – PTCA), vedly k významně vyšší úspěšnosti implantace, která v rozsáhlých studiích dosahovala více než 90% [6–7]. Po stanovení indikace k srdeční resynchronizační terapii je proto nutné vybrat co nejvhodnější systém.
Výběr systému k srdeční resynchronizační léčbě:
Biventrikulární kardiostimulátor (Cardiac Resynchronization Therapy – Pacemaker – CRT-P) vs biventrikulární kardioverter-defibrilátor (Cardiac Resynchronization The-rapy – Defibrillator – CRT-D)?
Zastánci preference biventrikulárních implantabilních kardioverterů-defibrilátorů (Implantable Cardioverter Defibrillator – ICD) opírají svoji teorii o prevalenci náhlé srdeční smrti u pacientů trpících městnavým srdečním selháním, která v různých klinických studiích prováděných v posledních 20 letech dosahovala 35 až 45% [9–10]. Stojí za zmínku, že za posledních několik desítek let došlo k poklesu její prevalence, a to v důsledku příznivého účinku farmakologické léčby, která zahrnuje zejména ACE inhibitory, sartany, betablokátory, spironolakton a v poslední době eplerenon [10–12].
Výsledky studie MERIT-HF ukazují, že mezi všemi příčinami úmrtí je množství případů náhlé srdeční smrti (NSS) nepřímo úměrné závažnosti městnavého srdečního selhání. V souladu s tím došlo k NSS u 64% pacientů zařazených do funkční skupiny II podle NYHA ve srovnání s 59% pacientů ve třídě III a 33% nemocných ve třídě IV a na rozdíl od 56% případů úmrtí v důsledku konečného stadia srdečního selhání. Naproti tomu lze u pacientů ve funkční třídě II a III přičítat srdečnímu selhání pouze 12%, resp. 26% úmrtí [10]. Ve studii MUSTIC tvořily u kandidátů na srdeční resynchronizační léčbu případy náhlého úmrtí 50% smrtelných kardiovaskulárních příhod [13], zatímco ve studii CARE-HF bylo na konci průměrné doby sledování v délce 29 měsíců označeno za náhlé 35% všech úmrtí [7–8]. Tato zjištění vedou k otázce, zda by nebylo vhodné implantovat biventrikulární defibrilátor (CRT-D) systematicky u všech kandidátů na srdeční resynchronizační léčbu. Nehledě na významné zastoupení komorových tachyarytmií mezi různými příčinami náhlé smrti však na základě komorové defibrilace nelze předejít všem příhodám, protože úmrtí může být způsobeno i jinými mechanizmy, např. asystolií nebo elektromechanickou disociací.
Výběr systému závisí také významně na tom, zda je implantát určen k primární nebo sekundární prevenci NSS. Indikace k sekundární prevenci se týká pacientů, kteří přežili srdeční zástavu, či nemocných s dokumentovanými hemodynamicky nestabilními komorovými tachyarytmiemi. Studie AVID, CASH a CIDS zabývající se otázkou sekundární prevence prokázaly 20–30% snížení celkové mortality a 33–59% pokles výskytu úmrtí v důsledku arytmií, ke kterému došlo na základě použití implantabilního kardioverteru-defibrilátoru (ICD) [14–16]. Máme tedy dostatek důkazů o tom, že implantaci CRT-D by se měli podrobit kandidáti z důvodu sekundární prevence NSS. Klinickou vhodnost této volby potvrdila dále jasně studie MIRACLE-ICD [17].
Problematika primární prevence u pacientů s městnavým srdečním selháním je výrazně komplikovanější. Jedním z důležitých údajů, které je nutné vzít v úvahu, je etiologie základní kardiomyopatie, tj. otázka, zda se jedná o ischemickou či neischemickou kardiomyopatii. Přínos ICD u pacientů po infarktu myokardu (IM), u nichž došlo k rozvoji ischemické kardiomyopatie, potvrdily všechny tři studie – MADIT I, MUSTT a MADIT II [18–20]. Výsledky studie MADIT II potvrdily účinnost použití ICD u pacientů, kteří byli do studie zařazeni nikoli na základě poruchy srdečního rytmu, ale na základě LV EF < 30% po jednom měsíci od infarktu myokardu [20]. Ve studii MADIT II, kde většina pacientů zůstala v 75% na léčbě ACE inhibitory a v 70% na léčbě beta adrenergními blokátory ve funkční třídě I nebo II podle NYHA, vedla preventivní implantace ICD po dvou letech k 31% snížení celkové mortality a k 61% snížení úmrtnosti v důsledku arytmií. Přínos implantace ICD byl dokonce větší u pacientů, u nichž byl na povrchovém EKG komplex QRS širší než 120 ms, přičemž pokles mortality v tomto případě dosahoval 63%. Je nutné poznamenat, že u pacientů po IM byl přínos implantace ICD podstatně vyšší ve skupině nemocných s velmi závažnou dysfunkcí levé komory (EF < 25%), a to ve studiích zabývajících se otázkou primární i sekundární prevence. Primárně preventivní studie DINAMIT s časnou preventivní implantací ICD po IM (do 40 dnů) neměla žádný vliv na snížení celkové mortality [21].
Výsledky studie SCD-HeFT znovu rozpoutaly diskuzi ohledně primární prevence náhlé smrti u pacientů s neischemickými kardiomyopatiemi [22]. V dříve provedených studiích CAT a AMIOVIRT se totiž neprokázal příznivý vliv implantace ICD na celkovou mortalitu v případě pacientů s neischemickými kardiomyopatiemi [23–24].
Do studie SCD-HeFT bylo zařazeno přes 2 500 pacientů s jasně definovanými ischemickými i neischemickými kardiomyopatiemi funkční třídy NYHA II nebo III a EF levé komory < 35%. Průměrný věk této populace byl 60 let a průměrná hodnota ejekční frakce levé komory (Left Ventricular Ejection Fraction – LV EF) činila 25%. Skupina pacientů účastnících se studie byla rozdělena do tří skupin: jedna skupina nemocných užívala místo antiarytmika placebo (při optimální farmakoterapii srdečního selhání), druhé byl podáván amiodaron v dávce upravené podle tělesné hmotnosti a třetí skupina byla léčena pomocí ICD. Roční mortalita představovala 7% (tj. 35% po pěti letech ve skupině pacientů, kterým bylo podáváno placebo), přičemž doba přežití ve skupině nemocných léčených amiodaronem byla stejná. Naproti tomu byla celková mortalita po pěti letech ve skupině pacientů s implantovaným ICD o 23% nižší, což odpovídá 7% snížení absolutního rizika úmrtí. Na základě analýzy předem určených podskupin se zjistilo, že implantace ICD je pro pacienty zařazených do funkční skupiny II podle NYHA přínosnější z hlediska úmrtnosti než pro pacienty ve funkční skupině III, zatímco v případě pacientů trpících ischemickými a neischemickými kardiomyopatiemi je její přínos stejný.
Také výsledky studie COMPANION potvrdily účinnost léčby pomocí ICD u pacientů s ischemickými a neischemickými kardiomyopatiemi [5]. Tato studie ukázala, že srdeční resynchronizační léčba, ať už s ICD nebo bez něj, vedla ke snížení primárního sledovaného parametru, kterým bylo úmrtí ze všech příčin a hospitalizace, o 20%, což bylo z hlediska léčby statisticky významné. Výskyt úmrtí a opakované hospitalizace z kardiovaskulárních příčin byl v obou skupinách pacientů léčených pomocí srdeční resynchronizační terapie (Cardiac Resynchronization Therapy – CRT) ve srovnání s nemocnými léčenými pouze na základě optimální medikamentózní terapie o 30% nižší a kombinovaný sledovaný parametr tvořený výskytem úmrtí a hospitalizace z důvodu městnavého srdečního selhání byl v obou skupinách, kterým byla aplikována srdeční resynchronizační léčba, nižší o 35%. Sekundární sledovaný parametr, tj. mortalita ze všech příčin, však byl signifikantně nižší (o 36%) ve skupině CRT + ICD ve srovnání se skupinou pacientů léčených na základě optimální farmakologické terapie. CRT + optimální farmakologická léčba vedla k 24% snížení celkové mortality ve srovnání se samostatnou medikamentózní léčbou, což byl rozdíl na hranici významnosti (p = 0,06). Je však nutné zdůraznit, že studie COMPANION nebyla primárně navržena ke srovnání CRT-P a CRT-D.
Nedávno publikované výsledky studie CARE-HF situaci dále komplikují. Na konci průměrné doby sledování v délce 29 měsíců vedla srdeční resynchronizační terapie spojená s optimální medikamentózní léčbou k 37% snížení kombinovaného sledovaného parametru tvořeného mortalitou ze všech příčin a opakovanou hospitalizací z kardiálních příčin (p < 0,001) a dále ke snížení celkové mortality o 36% (p < 0,002). Přibližně 35% výskyt případů náhlého úmrtí byl v obou skupinách podobný. Studie CARE-HF prodloužená na průměrnou dobu 37 měsíců však potvrdila trvalý pozitivní vliv srdeční resynchronizační terapie na celkové přežívání (–40%; p < 0,0001), který byl doprovázen nižším výskytem úmrtí spojeným s městnavým srdečním selháním (–45%; p < 0,003) a významně nižším výskytem případů náhlého úmrtí (–46%; p < 0,005). Je nutno zmínit, že v této studii nebylo zjištěno nic, co by umožňovalo preferovat léčbu ICD.
Zatímco se v případě městnavého srdečního selhání jedná o syndrom, kterým trpí převážně populace blížící se k 75 letům věku, byli do výše zmíněných klinických studií zařazováni pacienti ve věku mezi 60 a 65 lety. U nemocných s městnavým srdečním selháním se kromě toho často vyskytují i další závažná onemocnění – diabetes, hypertenze, hypercholesterolemie a řada dalších. Nelze proto doporučit jasnou strategii, pokud jde o implantaci CRT-P či CRT-D. Velmi jednoduchým by bylo doporučení implantace systémů CRT-D všem kandidátům srdeční resynchronizační léčby. To se však vzhledem k velmi rozdílné ceně jednotlivých přístrojů (CRT-D jsou 3–5krát dražší než CRT-P), vysokému věku a závažným doprovodným chorobám v případě některých pacientů jeví jako nevhodné. U některých nemocných navíc může jít o čistě funkční indikaci, která neopravňuje k implantaci CRT-D – např. u pacientů ve funkční klasifikaci NYHA IV [22]. Např. ve studii MADIT II nebyl prokázán příznivý vliv ICD u pacientů s glomerulární filtrací < 35ml/min/1,73 m2.
U nemocných, u kterých je srdeční resynchronizační léčba indikována z důvodu sekundární prevence náhlé smrti (při dokumentované závažné komorové tachykardii či fibrilaci komor), je vhodné systematicky implantovat CRT-D v případě, že jsou z fyziologického hlediska v „přijatelném“ zdravotním stavu. Biologický stav nemocných, u nichž je implantace ICD indikována z důvodu primární prevence, je při výběru přístroje nutné zjišťovat komorbidity a určit prognózu ještě pečlivěji. Mladším pacientům, kteří jsou i potenciálními kandidáty transplantace srdce, by se měla provést implantace CRT-D nehledě na to, zda mají ischemickou či neischemickou kardiomyopatii (bridge to the transplant). Naopak u starších pacientů se závažnými doprovodnými onemocněními, kratší dobou očekávaného přežívání a pacientů ve funkční klasifikaci NYHA IV, je vhodnější použít biventrikulární kardiostimulátor (CRT-P). Největší problém představuje „šedá zóna“ mezi těmito dvěma typy populace. Pacienta a jeho rodinu je nutné podrobně informovat o výhodách a nevýhodách, které nabízí každý z těchto systémů, zejména o riziku nevhodných terapií, které se pojí s CRT-D.
Moderní technologie v diagnostice a prognóze srdečního selhání
Moderní technologie umožňují pomocí dostupných funkcí vyhodnotit důležité údaje, jako jsou aktivita pacienta, progrese či regrese srdečního selhání, frekvence a délka epizod fibrilace síní, a celou řadu dalších cenných informací. Nedávné výsledky studie MID-HEFT založené na měření transthorakální impedance otevřely nové možnosti [25]. Při hyperhydrataci dochází totiž ke snížení impedance mezi pravokomorovou elektrodou a ICD. Naopak léčba srdečního selhání a odstranění přetížení tekutinami vede ke zvýšení nitrohrudní impedance. Tato studie, do níž bylo zařazeno 33 pacientů hospitalizovaných z důvodu srdeční dekompenzace, ukázala, že dva týdny před hospitalizací dochází k poklesu nitrohrudní impedance v průměru o 12%. Výsledky této studie prokázaly rovněž nepřímou závislost mezi vzestupem nitrohrudní impedance na jedné straně a poklesem kapilárního tlaku v plicích a přetížením cév na straně druhé (r = –0,90; p < 0,001). Algoritmus založený na míře poklesu nitrohrudní impedance může být varováním pro pacienta a lékaře, pokud jde o hrozící nebezpečí přetížení tekutinami v plicních cévách, které by mohlo vést ke snížení počtu hospitalizací či přinejmenším ke zkrácení nemocničního pobytu. Další hemodynamické hodnoty, mj. nejvyšší endokardiální akcelerace (Peak), tlak v levé síni, tlak v pravé komoře či tlak v plicních arteriích, jsou ve fázi zkoumání nebo ověřování. Současně dostupné přístroje jsou také schopny analyzovat změny sinusového rytmu, zejména na fibrilaci síní, která je velmi často spojena s projevy časné levostranné srdeční dekompenzace.
Počet implantací CRT-D se jistě v budoucnu zvýší, a to i v případě, že vezmeme v úvahu takové důležité faktory, jako jsou věk pacientů a jejich doprovodná onemocnění. Nezdá se, že by diskuzi týkající se vhodnosti CRT-P proti CRT-D bylo možné vyřešit v roce 2009 na základě stávajících důkazů a studií, protože k tomu, abychom mohli doložit, že CRT-D vede ve srovnání s CRT-P alespoň ke 4% absolutnímu poklesu celkové mortality při 90% výpovědní hodnotě, by bylo nutné sledovat po dobu tří let 1 600 pacientů v každé z těchto skupin [8]. Pomocí aplikace nových technologií, zejména v kombinaci s některou z forem telemonitoringu (např. systém Home Monitoring, Biotronik, Inc.), lze hodnotit stav městnavého srdečního selhání a optimalizovat jeho léčbu zejména v časném stadiu rozvoje jeho dekompenzace. Na definitivní výsledek této diskuze si jistě budeme muset počkat nejméně dalších pět let, kdy budou k dispozici výsledky nových velkých studií se srdeční resynchronizační léčbou, nicméně některé jasné indikace v jednotlivých podskupinách byly již jednoznačně uvedeny. Situace v České republice v oblasti srdeční resynchronizační léčby – použití CRT-P vs CRT-D za rok 2008 je dokumentována na obr. 1.
Obr. 1. Poměr implantovaných biventrikulárních kardiostimulátorů (CRT- P) a kardioverterů-defibrilátorů (CRT- D) v České republice v roce 2008. Registry TKS a ICD PS AKS ČKS. 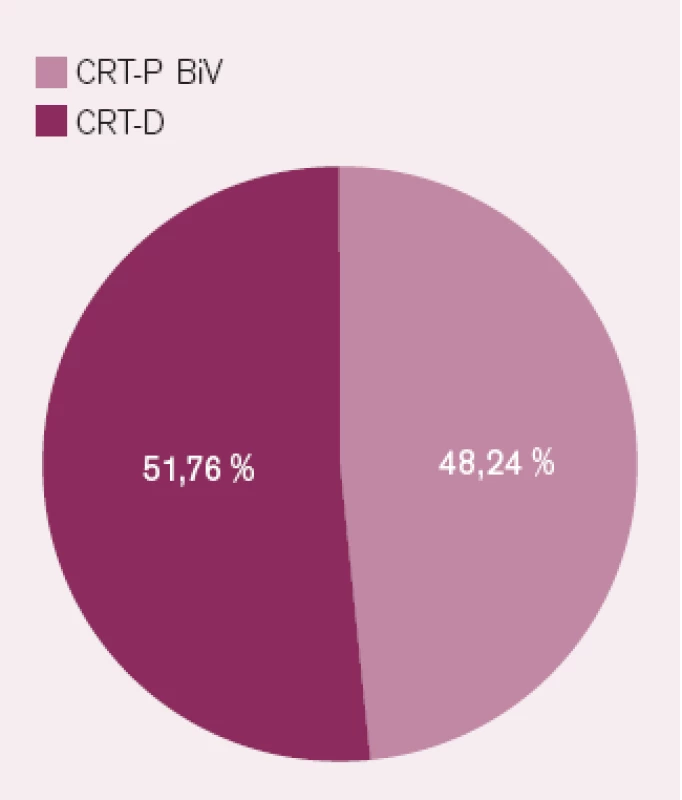
Doručeno do redakce 18. 2. 2009
Přijato po recenzi 26. 2. 2009
doc. MUDr. Miloš Táborský, CSc., FESC, MBA
Kardiocentrum, Nemocnice Na Homolce, Praha
milos.taborsky@homolka.cz
Zdroje
1. Táborský M, Kautzner J, Bytešník J et al. Zásady pro implantace kardiostimulátorů, implantabilních kardioverterů-defibrilátorů a srdeční resynchronizační léčbu. Cor Vasa 2005; 47 : 59–68.
2. Epstein AE, DiMarco JP, Ellenbogen KA et al. ACC/AHA/HRS 2008 guidelines for Device-Based Therapy of Cardiac Rhythm Abnormalities. Circulation 2008; 117: e350–e408.
3. Cazeau S, Leclercq C, Lavergne T et al. Effects on multisite biventricular Pacing in patiens with heart failure and intraventricular delay. N Eng J Med 2001; 344 : 873–880.
4. Auricchio A, Stellbrink C, Sack S et al. Pacing Therapies in Congestive Heart Failure (PATH-CHF). J Am Coll Cardiol 2002; 39 : 2026–2033.
5. Bristow MR, Saxon LA, Boehmer J et al. Comparison of Medical Therapy, Pacing, and Defibrillation in Heart Failure (COMPANION) Investigators. N Engl J Med 2004; 350 : 2140–2150.
6. Abraham WT, Fischer WG, Smith AL et al. MIRACLE Study Group. Multicenter InSync Randomized Clinical Evaluation. Cardiac resynchronization therapy. N Engl J Med 2002; 346 : 1845–1853.
7. Cleland JG, Daubert JC, Erdmann E et al. Cardiac Resynchronization-Heart Failure (CARE-HF) Sudy Investigators. The effect of cardiac resynchronization therapy on morbidity and mortality in heart failure. N Eng J Med 2005; 352 : 1539–1549.
8. Cleland JG, Daubert JC, Erdmann E et al. Longer‑term effects of cardiac resynchronization therapy on mortality in heart failure. Eur Heart J 2006; 27 : 1928–1932.
9. Flather MD, Yusuf S, Køber et al. Long‑term ACE‑inhibitor therapy in patiens with heart failure or left-ventricular dysfunction: a systematic overview of data from individual patiens. ACE-Inhibitor Myocardial Infarction Collaborative Group. Lancet 2000; 355 : 1575–1581.
10. The MERIT-HF study group. Effect of metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomised Intervention Trial in Congestive Heart Failure (MERIT-HF). Lancet 1999; 353 : 2001–2007.
11. Pitt B, Zannad F, Remme WJ et al. The effect of spironolactone on morbidity and mortality in patiens with severe heart failure. N Engl J Med 1999; 341 : 709–717.
12. Pitt B, Remme W, Zannad F et al. Eplerenone Post Acute Myocardial Infarction Heart Failure Efficacy and Survival Study. N Engl J Med 2003; 348 : 1309–1321.
13. Linde C, Leclercq C, Rex S et al. Long‑term benefits of biventricular pacing in congestive heart failure: results from the MUltisite STimulation in cardiomyopathy (MUSTIC) study. J Am Coll Cardiol 2002; 40 : 111–118.
14. Kuck KH, Cappato R, Siebels J et al. Randomized comparison of antiarrhythmic drug therapy with implantable defibrillators in patients resuscitated from cardiac arrest : the Cardiac Arrest Study Hamburg (CASH). Circulation 2000; 102 : 748–754.
15. Connolly SJ, Gent M, Roberts RS. Canadian Implantable Defibrillator Study (CIDS) a randomized trial of the implantable cardioverter defibrillator against amiodarone. Circulation 2000; 101 : 1297–1302.
16. AVID Inestigators. A comparison of antiarrhythmic-drug therapy with implantable defibrillators in patiens resuscitated from near-fatal ventricular arrhythmias. The Antiarrhythmics versus Implantable Defibrillators (AVID) Investigators. N Engl J Med 1997; 337 : 1576–1583.
17. Young JB, Abraham WT, Smith AL et al. Combined cardiac resynchronization therapy and implantable cardioversion defibrillation in advanced chronic heart failure: the MIRACLE ICD Trial. JAMA 2003; 289 : 2685–2694.
18. Moss AJ, Hall WJ, Cannom DS et al. Improved survival with an implanted defibrillator in patiens with coronary disease at high risk for ventricular arrhythmia. Multicenter Automatic Defibrillator Implantation Trial Investigators. N Engl J Med 1996; 335 : 1933–1940.
19. Buton AE, Lee KL, DiCarlo L et al. Electrophysiologic testing to identify patiens with coronary artery disease who are at risk for sudden cardiac death. Multicenter Unsustained Tachycardia Trial Investigators. N Engl J Med 2000; 342 : 1937–1945.
20. Moss AJ, Zareba W, Hall WJ et al. Prophylactic implantation of a defibrillator in patiens with myocardial infarction and reduced ejection fraction. N Engl J Med 2002; 346 : 877–883.
21. Hohnloser SH, Kuck KH, Dorian P et al. Prophylactic use of a implantable cardioverter-defibrillator after acute myocardial infarction. N Engl J Med 2004; 351 : 2481–2488.
22. Bardy GH, Lee KL, Mark DB et al. Sudden Cardiac death in Heart Failure Trial (SCD-HeFT) Trial. N Engl J Med 2005; 352 : 225–237.
23. Strickberger SA, Hummel JD, Bartlett TG et al. AMIOVIRT Investigators. Amiodarone versus implantable cardioverter-defibrillator: randomized trial in patiens with non‑ischemic dilated cardiomyopathy and asymptomatic nonsustained ventricular tachycardia – AMIOVIRT. J Am Coll Cardiol 2003; 41 : 1707–1712.
24. Bänsch D, Antz M, Boczor S et al. Primary prevention of sudden cardaic death in idiopathic dilated cardiomyopathy: the Cardiomyopathy Trial (CAT). Circulation 2002; 105 : 1453–1458.
25. Yu CM, Wang L, Chau E et al. Intrathoracic impedance monitoring in patiens with heart failure: correlation with fluid status and feasibility of early warning preding hospitalization. Circulation 2005; 112 : 841–848.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie Kardiologie
Článek vyšel v časopiseKardiologická revue – Interní medicína
Nejčtenější tento týden
2009 Číslo 1- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
-
Všechny články tohoto čísla
- Ischemicko-reperfuzní poškození po srdeční zástavě a protektivní účinky hypotermie
- Máme v roce 2009 dostatek důkazů o tom, zda nemocným indikovaným k srdeční resynchronizační léčbě implantovat biventrikulární kardiostimulátor nebo kardioverter-defibrilátor?
- Současný stav srdeční resynchronizační léčby u nemocných se srdečním selháním
- Studie JUPITER a co nám říká?
- Studie PRoFESS – Prevention Regimen for Effectively Avoiding Second Stroke
- Chronologie akutního koronárního syndromu
- XVIIIth European Meeting on Hypertension 22nd Scientific Meeting of the International Society of Hypertension Berlín, 14.–19. června 2008
- Galerie autorů
- Nemoci a „nemůcky“
- Chirurgická léčba fibrilace síní – zamyšlení elektrofyziologa nad jejími perspektivami a indikacemi
- Chirurgická léčba fibrilace síní
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Ischemicko-reperfuzní poškození po srdeční zástavě a protektivní účinky hypotermie
- Chirurgická léčba fibrilace síní
- Současný stav srdeční resynchronizační léčby u nemocných se srdečním selháním
- Galerie autorů
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



