-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Diabetes mellitus 2. typu ve stáří
Type 2 diabetes mellitus in old age
Older patients with diabetes suffer increased morbidity and mortality in comparison to elderly patients without diabetes. Other frequent problems in these patients are polypharmacy, functional disability and geriatric syndromes – cognitive impairment, depression, urinary incontinence and falls. When deciding about the treatment and glycaemic targets it is necessary to take into account the pa-tient‘s level of independence and his or her physical and mental abilities. Risk of hypoglycaemia, which is increased in this group of patients and which might lead to impaired cognitive function and functional disability, is an important factor in choosing antidiabetic medication.
Key words:
older patients – diabetes – hypoglycaemia – geriatric syndromes
Autoři: MUDr. Martina Lášticová
Působiště autorů: III. interní gerontologická a metabolická klinika LF UK a FN Hradec Králové
Vyšlo v časopise: Geriatrie a Gerontologie 2014, 3, č. 2: 88-91
Kategorie: Přehledové články
Souhrn
Starší pacienti s diabetem mají vyšší morbiditu a mortalitu oproti nediabetickým pacientům. K častým problémům těchto pacientů patří polypragmazie, funkční dis-abilita a geriatrické syndromy – kognitivní poruchy, deprese, močová inkontinence a pády. Při rozhodování o způsobu léčby a stanovování cílů léčby je nutné zvážit samostatnost, pohybové a mentální schopnosti pacienta. Důležitým faktorem při výběru antidiabetické medikace je riziko hypoglykemie, které je v této skupině pacientů zvýšené a může vést ke zhoršování kognitivních funkcí a funkční disabilitě.
Klíčová slova:
starší pacienti – diabetes mellitus – hypoglykemie – geriatrické syndromyÚvod
Prevalence diabetu mellitu 2. typu celosvětově stoupá v souvislosti s narůstajícím výskytem obezity a stárnutím populace. Ze všech věkových skupin je prevalence diabetu nejvyšší u starších jedinců a dosahuje vrcholu ve věku 60–74 let(9). Starší dospělí s diabetem jsou stejně jako mladší diabetici ohroženi rozvojem akutních i chronických mikrovaskulárních a makrovaskulárních komplikací, ale absolutní riziko rozvoje kardiovaskulárních komplikací je u nich mnohem vyšší.
Také morbidita a mortalita seniorů s diabetem je vyšší než u nediabetiků(6). U těchto pacientů se často setkáváme s polypragmazií, funkční disabilitou a geriatrickými syndromy – kognitivními poruchami, depresí, močovou inkontinencí, pády a bolestí(19). Cíle léčby diabetu ve stáří jsou obdobné jako u mladších pacientů a zahrnují normalizaci glykemie a ovlivnění rizikových faktorů. Větší pozornost je ale u křehkých jedinců věnována prevenci hypoglykemie, hypotenze a lékovým interakcím při časté polypragmazii(11).
Patogeneze diabetu ve stáří
Starší pacienti mohou mít dlouhotrvající diabetes 2. i 1. typu, který byl zjištěn ve středním věku, případně i dříve, nebo se můžeme setkat s nově vzniklým onemocněním (diagnostikovaným po 65. roce věku). Ve vyšším věku vzniklý diabetes mellitus 1. typu je autoimunitně podmíněný a progreduje často pomalu (LADA – latent autoimmune diabetes of adults). S věkem roste riziko rozvoje diabetu 2. typu vlivem zvyšující se inzulinové rezistence a poruchy funkce β-buňky. S věkem spojená inzulinová rezistence je pravděpodobně primárně spojená s obezitou, sarkopenií a fyzickou inaktivitou(2). Již dříve byl popsán s věkem spojený pokles funkce pankreatických ostrůvků(8) a proliferační kapacity ostrůvků(13).
Léčba diabetu ve stáří
Populace geriatrických pacientů je značně heterogenní. Podle funkčního stavu je rozdělujeme do 3 skupin: zdatní, křehcí a ostatní senioři. Zdatní senioři mají výbornou výkonnost a diagnostický a terapeutický přístup k nim může být stejný jako u mladších jedinců. Křehcí jedinci jsou ohroženi rizikem pádů, zhoršením kognitivních schopností, psychickou labilitou, nestabilním stavem při komorbiditách. Většina pacientů patří do skupiny ostatní senioři, u kterých chorobné a involuční změny zhoršují adaptabilitu, regulační mechanismy a toleranci zátěže. Toto dělení do velké míry ovlivňuje přístup k léčbě diabetu(22).
Glykemické cíle
V současnosti není k dispozici dostatek dat, na základě kterých by bylo možné stanovit optimální hodnoty glykemie u seniorů. Hyperglykemie a osmotická diuréza zvyšují riziko dehydratace a zhoršují zrak a kognitivní funkce(15), což přispívá k funkčním poruchám a zvýšenému riziku pádů. Na druhé straně, starší pacienti tolerují relativně vyšší glykemie vzhledem k vyššímu glykemickému prahu. Častěji se u nich setkáváme s vedlejšími účinky antidiabetické medikace, zejména s hypoglykemií, která může vést k dalším závažným komplikacím, jako jsou pády a kardiovaskulární příhody. Glykemické cíle by měly být stanoveny na základě individualizovaných kritérií a předpokládané délky života(20).
Cílové hodnoty glykovaného hemoglobinu u starších pacientů v dobrém funkčním stavu, bez kognitivních poruch a očekávanou délkou života nad 10 let jsou obdobné jako u mladších pacientů (<53 mmol/mol). Pro pacienty s dlouhotrvajícím diabetem s kardiovaskulárními komorbiditami jsou doporučovány hodnoty HbA1c mezi 53-63 mmol/mol. Individualizované cíle mohou být ještě vyšší pro křehké seniory s výrazným funkčním omezením a závažnými komorbiditami, kde je nejdůležitější zachování kvality života, prevence hypoglykemie a zabránění symptomům hyperglykemie a akutních hyperglykemických komplikací(10, 20).
Hodnoty glykovaného hemoglobinu nemusí spolehlivě odpovídat kompenzaci diabetu v mnohých situacích, s nimiž se ve stáří často setkáváme. Týká se to anemie a dalších stavů, které ovlivňují délku života erytrocytů, chronického onemocnění ledvin, nedávného akutního onemocnění nebo hospitalizace a chronického onemocnění jater.
Prevence hypoglykemie
U geriatrické populace je výrazně zvýšené riziko hypoglykemie, která může vést ke zhoršení kognitivních funkcí a zhoršení funkčních schopností. Ve stáří se častěji setkáváme s neuroglykopenickými příznaky hypoglykemie (závratě, slabost, delirium, zmatenost); adrenergní symptomy (třes, pocení, palpitace) jsou méně časté. Tyto symptomy jsou často hodnoceny jako primární neurologické onemocnění (např. tranzitorní ischemická ataka) a výskyt hypoglykemie je pacienty i zdravotníky podhodnocen. Hypoglykemické epizody u seniorů zvyšují riziko kardiovaskulárních příhod a autonomní kardiovaskulární dysfunkce(1). Těžké hypoglykemie vyžadující hospitalizaci jsou také spojeny se zvýšeným rizikem rozvoje demence, zejména při opakovaných epizodách(24). Předcházení hypoglykemii je proto důležitým faktorem při volbě terapeutických prostředků a stanovení glykemických cílů. Inzulinová sekretagoga, jako deriváty sulfonylurey a glinidy, a inzulin by proto měly být používány u geriatrických pacientů s opatrností.
Úprava životního stylu
Dieta, redukce hmotnosti a pravidelná fyzická aktivita jsou základní opatření ke zlepšení glykemické kontroly. U starších diabetiků je však nutné zvážit některé další aspekty. Starší pacienti mohou být ohroženi podvýživou vlivem nechutenství, poruchy chuti a čichu, polykacích obtíží, problémů s chrupem a funkčních poruch vedoucích k obtížím při přípravě a konzumaci stravy. Příliš restriktivní stravovací doporučení mohou přispět k dalšímu riziku. BMI nemusí být přesným ukazatelem stupně obsahu tuku v těle u některých seniorů kvůli změnám tělesného složení vlivem stárnutí(23). Efekt redukce hmotnosti na zlepšení prognózy není obvykle po 70. roce prokazatelný a obézní mohou mít i lepší prognózu než štíhlí – tzv. paradox obezity(21). Sarkopenie se může vyskytnout jak u starších dospělých s nadváhou, tak s podváhou. Obezita potencuje pokles fyzické zdatnosti dané stárnutím a zvyšuje riziko zranitelnosti. Záměrné snižování hmotnosti u starších dospělých s nadváhou nebo obezitou může potenciálně zhoršovat sarkopenii, kostní denzitu a malnutrici(14).
S věkem dochází k úbytku svalové hmoty a síly a u diabetu může být pokles výraznější v důsledku komplikací diabetu, komorbidit a hospitalizací. Intervence zahrnující fyzickou aktivitu zlepšují funkční stav seniorů s diabetem i bez diabetu. Starší diabetici by proto měli být motivováni ke cvičení obdobně jako ostatní pacienti s diabetem(3). Dostatečným pohybem je chůze, optimálně by měla být pravidelná asi 30 minut denně. Zvýšení fyzické aktivity, i menší intenzity a frekvence, je přínosné pro zachování svalové hmoty a síly i u křehkých nemocných s horším zdravotním stavem.
Farmakologická léčba
Pro skupinu pacientů seniorů není k dispozici dostatek dat zabývajících se farmakoterapií. Všechny skupiny antidiabetických léků mají v populaci seniorů své limitace. Farmakoterapie musí být u těchto pacientů individualizována s ohledem na funkční stav pacienta a jeho komorbidity. U starších pacientů se setkáváme se zvýšeným rizikem nežádoucích účinků léků kvůli změnám ve farmakokinetice a farmakodynamice. Tyto změny mohou vést ke zvýšenému riziku hypoglykemie, potřebě podávání snížených dávek některých léků a nutnosti sledování renálních funkcí za účelem minimalizace nežádoucích účinků(12, 19).
Metformin je lékem první volby v léčbě diabetu 2. typu. Jeho předností, ze které mohou profitovat starší pacienti, je nízké riziko hypoglykemií. Na druhé straně musí být u seniorů používán s opatrností z důvodu rizika laktátové acidózy. Starší pacienti mají často poruchu renálních funkcí i při normální hladině kreatininu. Snížení dávky je doporučováno při hodnotách odhadované glomerulární filtrace (eGFR) mezi 30–60 ml/min a kontraindikován je při eGFR pod 30 ml/min(12). V případě léčby metforminem musí být senior poučen o nutnosti jeho vysazení v případě akutního onemocnění či v případě rentgenového vyšetření s použitím jodové kontrastní látky.
Deriváty sulfonylurey. Nejčastějším nežádoucím účinkem derivátů sulfonylurey, zejména u preparátů s dlouhodobým účinkem, je hypoglykemie. Použití dlouho působících preparátů (např. glibenklamid) není proto u seniorů vhodné. Riziko hypoglykemie je zvýšené při vynechání jídla, sníženém příjmu potravy, v případě abúzu alkoholu, snížení renálních funkcí, srdečním selhání, onemocnění gastrointestinálního traktu(18).
Glinidy. Repaglinid a nateglinid jsou léky s podobným mechanismem účinku jako deriváty sulfonylurey. Krátký poločas účinku lze využít k ovlivnění postprandiální hyperglykemie a pro populaci seniorů představuje výhodu pro nízké riziko hypoglykemií.
Thiazolidindiony. Pioglitazon je lékem snižujícím inzulinovou rezistenci. Výhodou je možnost použití u pacientů s renální insuficiencí a nízké riziko hypoglykemie. Zkušenosti u geriatrické populace jsou ale malé a jejich využití je limitováno vysokou cenou, rizikem fraktur a retence tekutin u pacientů se srdečním selháním. V poslední době se objevily údaje o riziku vzniku karcinomu močového měchýře.
Inhibitory α-glukosidázy. Akarbóza inhibuje v gastrointestinálním traktu štěpení polysacharidů a disacharidů a snižuje tak postpranidální vzestup glykemie. Má nízké riziko hypoglykemie. Limitujícím faktorem při jejím využití je gastrointestinální intolerance.
Inkretinová mimetika. Jde o relativně novou skupinu léků, jejichž účinek využívá tzv. inkretinový efekt, v důsledku kterého perorálně podaná glukóza vyvolává větší stimulační účinek na sekreci inzulinu než i.v. aplikovaná glukóza (obr. 1). Za tento efekt odpovídá několik gastrointestinálních peptidů, z nichž největší význam má GLP-1 (glucagon-like peptide 1). Tyto léky mají nízké riziko hypoglykemie a vedou k redukci hmotnosti. K nežádoucím účinkům patří nauzea, zvracení, průjem. Nevýhodou je i injekční podávání a vysoká cena.
Obr. 1. Snížení inkretinového efektu u diabetu 2. typu Zdroj: Nauck M, Stöckmann F, Bert R, Creutzfeldt W. Reduced incretin effect in Type 2 (non-insulin-dependent) diabetes. Diabetologia 1986; 29(1):46–52. 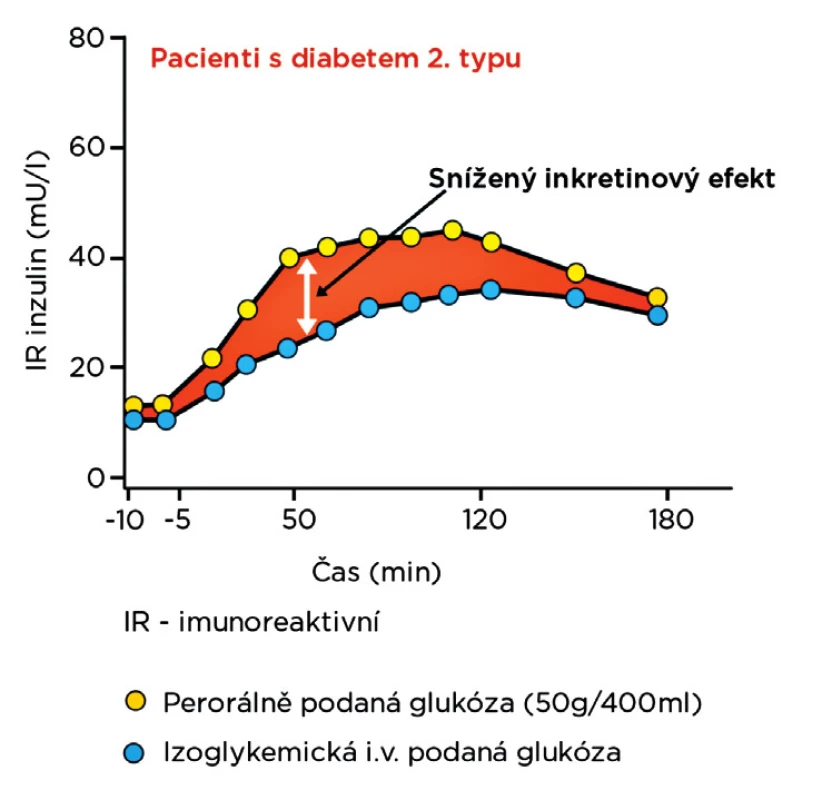
Inhibitory dipeptidyl peptidázy IV (DPP-IV). Enzym dipeptidyl peptidáza IV inaktivuje bioaktivní peptidy, včetně GLP-1 a GIP (glucose dependent insulinotropic polypeptide). Na rozdíl od inkretinových mimetik jsou podávány perorálně. Na trhu je několik preparátů této lékové skupiny. Jejich výhodou je nízké riziko hypoglykemie, možnost použití i u pacientů s renální insuficiencí a také to, že jsou váhově neutrální. U této skupiny existují již studie dakládající vysokou bezpečnost podávání u starší populace(5).
Inzulin. U některých pacientů, zejména u těch s dlouhotrvajícím diabetem s deficitem inzulinu, se neobejdeme bez inzulinoterapie. Bezpečnější jsou inzulinová analoga, u kterých je nižší riziko hypoglykemie. Před zahájením léčby inzulinem je nutné zhodnotit samostatnost, fyzické a mentální schopnosti pacienta, umožňující adekvátní nastavení dávky a aplikaci inzulinu. Preferujeme jednodušší režimy (např. kombinaci jedné dávky dlouhodobého analoga a perorálních antidiabetik anebo premixovaný inzulin v 1–2 denních dávkách). Aplikace inzulinu agenturou domácí péče, případně spojená s monitorací glykemie umožní život v domácím prostředí i u seniorů, kteří nejsou schopni samostatné spolehlivé a bezpečné aplikace.
Geriatrické syndromy a diabetes mellitus
Kognitivní deficit. Diabetes mellitus je spojen s vyšším rizikem demence(7). Kognitivní dysfunkce je překážkou v samostatné léčbě, selfmonitoringu a léčbě komplikovanými režimy. V případě zhoršení glykemické kontroly, zhoršení compliance a častých hypoglykemií je na tuto možnost nutné myslet a přehodnotit kognitivní schopnosti nemocného. U pacientů s demencí je zásadní kontrolovat příjem stravy, podávání léků a inzulinu.
Deprese je u geriatrické populace častá a zůstává často nediagnostikovaná(4). U starších pacientů by měl být prováděn pravidelný screening deprese při každé změně zdravotního stavu. Adekvátní léčba deprese může vést ke zlepšení glykemické kontroly pacienta.
Polypragmazie. U seniorů se často setkáváme s užíváním mnoha léků. S jejich počtem klesá adherence pacienta k léčbě a zvyšuje se výskyt vedlejších účinků a interakcí, které mohou zhoršovat zdravotní stav křehkého pacienta. Při každé návštěvě pacienta je vhodné revidovat užívanou medikaci a upravovat ji podle aktuálního stavu a potřeb nemocného.
Pády. Etiologie pádů u seniorů s diabetem je multifaktoriální. Přispívá k nim přítomnost diabetické polyneuropatie, svalová slabost, funkční disabilita, poruchy zraku, osteoartróza a výskyt hypoglykemií(17). Intenzivní léčba může být prospěšná pro nižší riziko rozvoje chronických komplikací diabetu, na druhé straně ale může vést ke zvýšenému výskytu hypoglykemií a tím riziku pádů. V prevenci pádů křehkých geriatrických pacientů je přínosná méně intenzivní léčba a zachování svalové síly pravidelným cvičením.
Závěr
Přístup k léčbě diabetu u starších pacientů se v posledních letech zásadně mění. Musí být individualizován s ohledem na jejich celkový stav, komorbidity a fyzické a mentální schopnosti. U seniorů bez závažnějších komorbidit, s očekávanou délkou života více než 10 let mohou být cílové hodnoty glykemické kontroly obdobné jako u mladších pacientů. Vyšší cílové hodnoty jsou bezpečnější pro křehké pacienty s mnohočetnými komorbiditami s kratší předpokládanou délkou života (tab. 1). Individuální přístup vyžaduje i edukace zaměřená na změnu životního stylu, úpravu diety a pravidelnou fyzickou aktivitu. Kromě nemocného je vhodné do procesu edukace zahrnout i nejbližší příbuzné pacienta.
Tab. 1. Doporučené cílové glykemie při léčbě diabetu 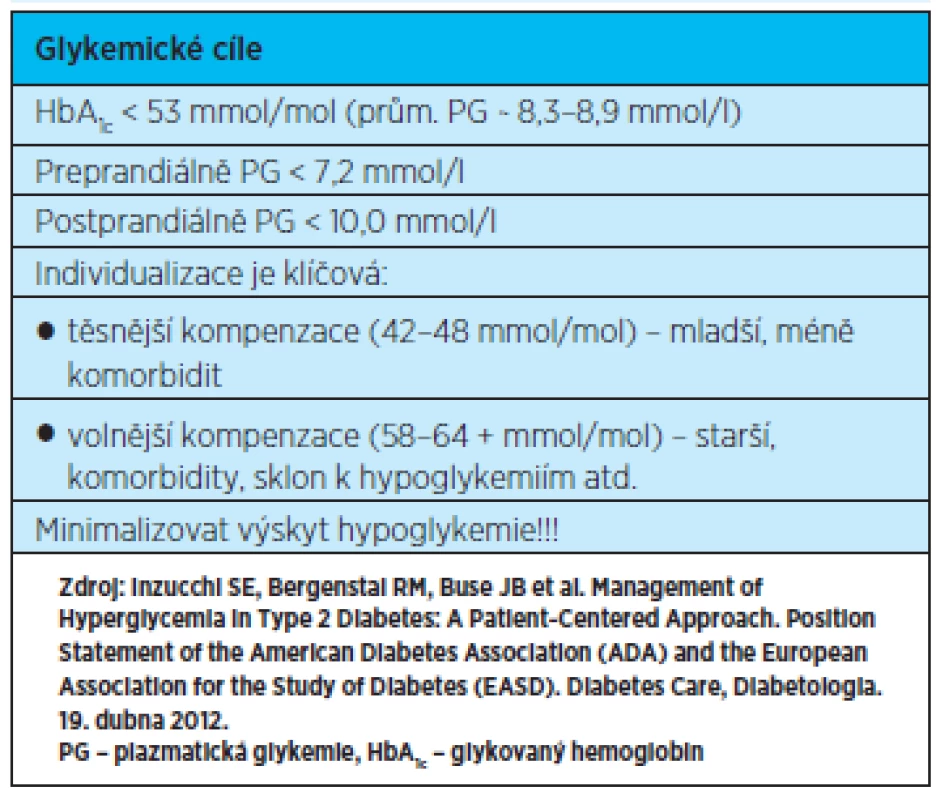
MUDr. Martina Lášticová
e-mail: martina.lasticova@fnhk.cz
Absolvovala Jeseniovu lékařskou fakultu Univerzity Komenského v Martině v roce 2003. Po ukončení studia nastoupila na interní oddělení nemocnice Chrudim. Od roku 2007 pracuje v Diabetologickém centru III. interní gerontologické a metabolické kliniky FN Hradec Králové. Atestaci z vnitřního lékařství získala v roce 2011, z diabetologie a endokrinologie v roce 2013. Píše články do odborných časopisů a je spoluautorkou monografie Diabetologie pro farmaceuty. Věnuje se i pregraduální výuce na LF UK v Hradci Králové.
Zdroje
1. Adler GK, Bonyhay I, Failing H, et al. Antecendent hypoglycemia impairs autonomic cardiovascular function: implications for rigorous glycemic control. Diabetes 2009; 58 : 360.
2. Amati F, Dubé JJ, Coen PM, et al. Physical inactivity and obesity underlie the insulin resistance of aging. Diabetes Care 2009; 29: e176–e179.
3. American Diabetes Association. Standards of medical care in diabetes, 2012; 35 (Suppl. 1): S11–S63.
4. Anderson RJ, Freedland KE, Dlouze RE, et al. The prevalence of comorbid depression in adults with diabetes: a meta-analysis. Diabetes Care 2001; 24 : 1069.
5. Barnett AH, Husman H, Jones R et al. Linagliptin for patiens aged 70 years or older with type 2 diabetes inadequately controlled with common antidiabetes treatments: a randomised, double-blind, placebo-controlled trial. Lancet 2013; 382 (9902):1413–1423.
6 . Betel MA, Sloan FA, Belsky D, Feinglos MN. Longitudinal incidence and prevalence of adverse outcomes of diabetes mellitus in elderly patients. Arch Intern Med 2007; 167 : 921.
7. Biessels GJ, Staekenborg S, Brunner E, et al. Risk of dementia in diabetes mellitus: a systematic review. Lancet Neurol 2006; 5(1): 64–74.
8. Chang AM, Halter JB. Aging and insulin secretion. Am J Physiol Endocrinol Metab 2003; 284: E7–E12.
9. Cowie CC, Rust KF, Ford ES, et al. Full accounting of diabetes and prediabetes in the U.S. population in 1988–1994 and 2005–2006. Diabetes Care 2009; 32 : 287.
10. Inzucchi SE, Bergenstal RM, Buse JB, et al. Management of Hyperglycemia in Type 2 Diabetes: A Patient-Centered Approach. Position Statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care, Diabetologia. 19 April 2012
11. Ligthelm RJ, Kaiser M, Vora J, Yale JF. Insulin use in elderly adults: risk of hypoglycemia and strategy for care. J Am Geriatr Soc 2012; 60 : 1564.
12. Lipska KJ, Bailey CJ, Inzucchi SE. Use of metformin in the setting of mild-to-moderate renal insufficiency. Diabetes Care 2011; 34 : 1431–1437.
13. Maedler K, Schumann DM, Schulthess F, et al. Aging correlates with decreased beta-cell proliferative capacity and enhanced sensitivity to apoptosis: a potential role for Fas and pancreatic duodenal homeobox-1. Diabetes 2006; 55 : 2455–2462.
14. Miller SL, Wolfe RR. The Danger of weight loss in the elderly. J Nutr Health Aging 2008; 12 : 487–491.
15. Mooradian AD, Perryman K, Forten, et al. Cortical function in elderly non-insulin dependent diabetic patients. Behavioral and electrophysiologic studies. Arch Intern Med 1988; 148 : 2369.
16. Nauck M, Stöckmann F, Bert R, Creutzfeldt W. Reduced incretin effect in Type 2 (non-insulin-dependent) diabetes. Diabetologia 1986; 29(1): 46–52.
17. Schwarz AV, Vittinghof E, Sellmeyer DE, et al. Diabetes-related complications, glycemic control, and falls in older adults. Diabetes Care 2008; 31(3): 391–396.
18. Shorr RI, Ray WA, Daugherty JR, Griffin MR. Incidence and risk factors for serious hypoglycemia in older persons using insulin or sulfonylureas. Arch Intern Med 1997; 157 : 1681.
19. Short RI, Ray WA, Daugherty JR, Griffin MR. Individual sulfonylureas and serious hypoglycemia in older people. J Am Geriatr Soc 1996; 44 : 751–755.
20. Sue Kirkman M, Briscoe VJ, Clark N, et al. Diabetes in older adults: a consensus report. J Am Geriatr Soc 2012; 60 : 2342.
21. Svačina Š. Obezitologie a teorie metabolického syndromu. Praha, Triton 2013.
22. Svačina S, Karen I, Juračková B. Diabetes mellitus – léčba u starších pacientů v ČR. Doporučené diagnostické a terapeutické postupy pro všeobecné praktické lékaře. www.svl.cz
23. Villareal DT, Banks M, Skener C, et al. Physical frailty and body composition in obese elderly men and women. Obes Res 2004; 12 : 913–920.
24. Whitmer RA, Karter AJ, Arge K, et al. Hypoglycemic episodes and the risk of dementia in older patiens with type 2 diabetes mellitus. JAMA 2009; 301 : 1565.
Štítky
Geriatrie a gerontologie Praktické lékařství pro dospělé Protetika
Článek EditorialČlánek Anabolická rezistence
Článek vyšel v časopiseGeriatrie a Gerontologie
Nejčtenější tento týden
2014 Číslo 2- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
- Trazodon pohledem praktického lékaře
-
Všechny články tohoto čísla
- Kam směřuje evropská geriatrie
- Editorial
- Farmakoterapie seniorů v domovech důchodců
- Efektivita a návaznost jednotlivých systémů péče o geriatrického pacienta
- Posuzování stupně závislosti pro účely příspěvku na péči na základě funkčního hodnocení stavu seniora
- Diabetes mellitus 2. typu ve stáří
- Anabolická rezistence
- Pregraduální výuka geriatrie a Evropské curriculumpro výuku geriatriena lékařských fakultách doporučené UEMS-Sekcí geriatrické medicíny
- Geriatrie a Gerontologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Posuzování stupně závislosti pro účely příspěvku na péči na základě funkčního hodnocení stavu seniora
- Diabetes mellitus 2. typu ve stáří
- Farmakoterapie seniorů v domovech důchodců
- Anabolická rezistence
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




