-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Kožní projevy u chronické renální insuficience
Dermatological examination in patients with renal insufficiency usually reveals numerous skin and nail changes related to dialysis. The article explains specific and non-specific skin changes in chronic renal insufficiency such as pruritus, perforating and bullous diseases, calciphylaxis and recently described clinical entity – nephrogenic systemic fibrosis. The above mentioned complications could decrease quality of life in dialysed patients and some of them could also increase morbidity and even mortality. That is why an early dermatologic examination and proper treatment recommendation could improve quality of life in these patients.
Key words:
hemodialysis – peritoneal dialysis – chronic renal insufficiency – pruritus – perforating dermatoses – bullous dermatoses – nephrogenic systemic fibrosis – calciphylaxis
Autoři: P. Cetkovská
Působiště autorů: Dermatovenerologická klinika LFUK a FN v Plzni přednosta prof. MUDr. Karel Pizinger, CSc.
Vyšlo v časopise: Čes-slov Derm, 83, 2008, No. 2, p. 56-60
Kategorie: Souborné referáty (doškolování lékařů)
Souhrn
Dermatologické vyšetření pacientů s ledvinným selháním většinou zjistí četné změny na kůži a nehtech, které souvisejí s dialyzační terapií. V článku jsou vysvětleny specifické a nespecifické kožní projevy chronické ledvinné insuficience, jako jsou pruritus, perforující a bulózní nemoci, kalcifylaxe a až nedávno popsaná klinická jednotka – nefrogenní systémová fibróza. Tyto komplikace mohou znepříjemňovat život dialyzovaných pacientů, ale některé také mohou vést k vyšší morbiditě a dokonce i mortalitě, proto včasné vyšetření dermatologem a doporučení správné léčby může zlepšit kvalitu života těchto nemocných.
Klíčová slova:
hemodialýza – peritoneální dialýza – chronické selhání ledvin – pruritus – perforující dermatózy – bulózní dermatózy – nefrogenní systémová fibróza – kalcifylaxeÚVOD
V posledních letech se na celém světě pozoruje významný každoroční nárůst výskytu chronického selhání ledvin. Selhání ledvin je definováno jako stav, kdy pro přežití nemocného je nutné zahájit terapii dialýzou či provést transplantaci ledviny. Vzrůst počtu pacientů jen v USA se odhaduje až na 2 miliony do roku 2030 z celkového počtu 500 000 nemocných s ledvinným selháním v letošním roce (11).
Kožní projevy u chronického selhání ledvin se mohou rozdělit na nespecifické a specifické změny (tab. 1.). Kromě těchto změn se mohou také pozorovat různé infekce, polékové reakce a po případě kožní manifestace systémových nemocí, které způsobily selhání ledvin, jako jsou diabetes mellitus, lupus erythematosus, sklerodermie či vaskulitidy (4). Kožní problémy u pacientů po transplantaci ledvin byly popsány již v časopise Česko-slovenská dermatologie v roce 2007.
Tab. 1. Kožní projevy u dialyzovaných pacientů 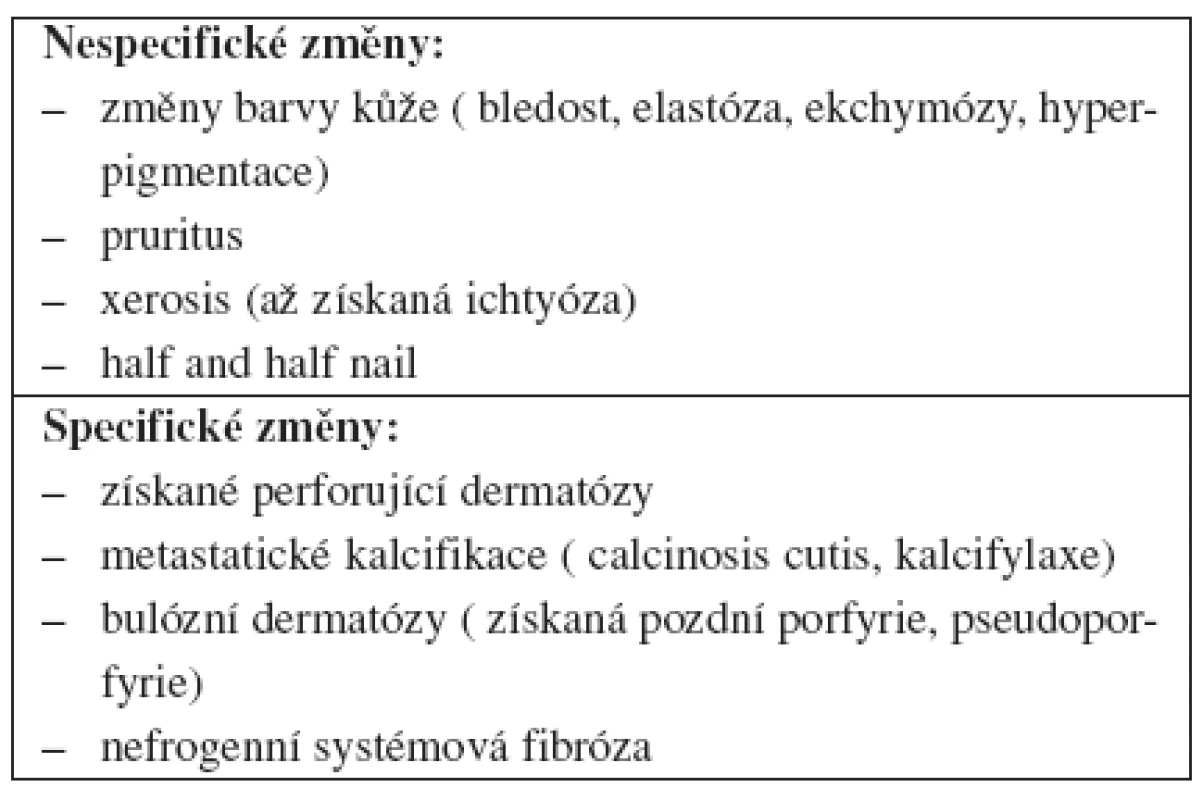
Nespecifické změny
Mezi nespecifické projevy chronického renálního selhání patří změny barvy kůže, kdy je kůže buď anemicky bledá, nebo žlutošedě difúzně pigmentovaná až tmavě hnědě pigmentovaná v místě solární lokalizace. Difúzní hyperpigmentace je způsobena zvýšenou produkcí melaninu následkem zvýšení špatně dialyzovatelného melanostimulačního hormonu (MSH). Žlutavý odstín je vyvolán uloženými lipochromy a karotenoidy v dermis a podkoží, břidlicové zbarvení je přisuzováno ukládání hemosiderinu. Časté jsou také projevy krvácení do kůže vyvolané poruchou koagulace při abnormální funkci krevních destiček či po aplikaci antikoagulancií (4).
Charakteristické je zvláštní zbarvení nehtů u asi 10 až 40 % pacientů léčených hemodialýzou, kdy proximální část nehtu je bělavě zbarvená a distální část je červenohnědá („half and half nail“) následkem vyššího obsahu melaninu.
U 50 až 92 % nemocných se pozoruje xerosis cutis, kdy pokožka nejvíce nad extenzory končetin je nápadně suchá, popraskaná a olupuje se. Může vzniknout až ichthyosis acquisita (1,15). Přesná příčina není známá a ani přímé měření transepidermální ztráty vody v epidermis nemocných s ledvinným selháním neukázalo signifikantní rozdíly od zdravých lidí (18).
Vůbec nejčastějším kožním symptomem chronického ledvinného selhání je pruritus. Donedávna byl označován jako uremický pruritus, ale protože nepostihuje nemocné v urémii při akutním renálním selhání, doporučuje se používat spíše termín pruritus při chronickém ledvinném selhání (11). Výskyt pruritu podle literatury kolísá od 22 do 90 % nemocných léčených dlouhodobě hemodialýzou nebo peritoneální dialýzou. V posledních letech se zdá, že prevalence pruritu klesá (7, 14, 16).
Patogeneze svědění je dosud neznámá. Teoreticky se zvažovala souvislost s xerózou kůže, sekundární hyperparatyreóza, dysregulace vápníku a fosfátů, zvýšené množství mastocytů a vyšší hladina histaminu, hypervitaminóza A, hypovitaminóza D, uvolnění pruritogenních cytokinů během dialýzy, excitace volných nervových zakončení v kůži uremickými toxiny, alergické reakce a jiné faktory. V poslední době výzkum ukazuje, že hlavní roli mají imunitní změny a dysbalance v endogenním opioidergickém systému – neuropeptidech (11). Pruritus se může objevit na podkladě proinflamačního stavu při změnách v imunitním systému. Proto také imunomodulační terapie, jako fototerapie a terapie inhibitory kalcineurinu, jej potlačují. Také různé opiodní receptory mají rozdílný vliv na pruritus, protože např. antagonisticky působící přípravek na μ-receptor naltrexon zmírňuje svědění, ale na druhou stranu agonista κ-receptoru nalfurafin také příznivě ovlivňuje pruritus a exkoriace.
Vždy je třeba vyloučit i jiné příčiny pruritu, protože nemocní trpí současně dalšími nemocemi, jako jsou jaterní, endokrinní či myeloproliferační nemoci, nebo mohou mít skabies či dermatózy, které bývají doprovázené pruritem (13).
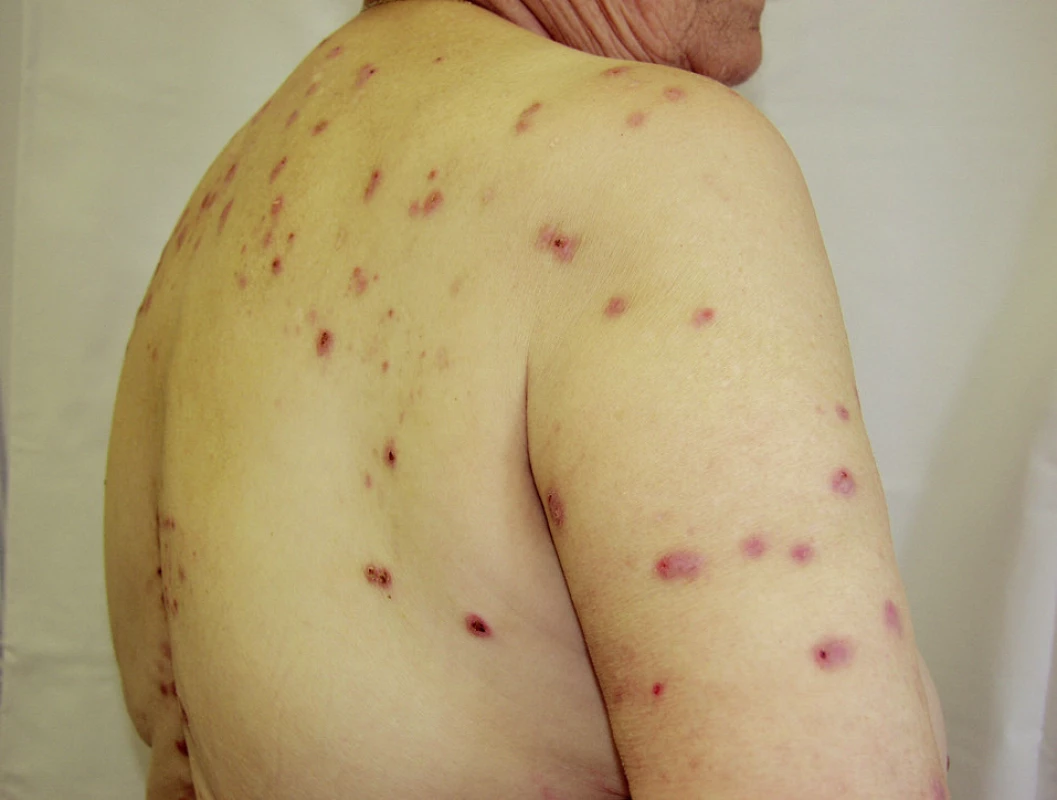
Pruritus začíná většinou až po několika měsících dialýzy a bývá úpornější v době před hemodialýzou, ve čtvrtině případů je trvalý. Může být lokalizovaný nebo generalizovaný, nejvíce jsou postižena záda. Intenzita často souvisí se stupněm xerózy kůže (12, 18). Obtíže bývají horší v noci, v klidu a vedou k poruchám spánku. V mezinárodní studii sledující 18 000 dialyzovaných pacientů bylo zjištěno, že pruritus vede k 17% zvýšení rizika úmrtí a příčinou tohoto rizika je nejspíše právě nespavost (12). Následkem škrábání vznikají exkoriace, lichenifikace a hyperkeratotické exulcerované hrboly napodobující prurigo nodularis (obr. 1). Laboratorně se zjišťují vyšší hladiny C-reaktivního proteinu, vápníku a fosfátů v séru.
Obecná léčebná doporučení zahrnují pobyt v chladném prostředí, volný oděv a časté používání emoliencií, nejlépe s vyšším obsahem vody. Ve studiích se osvědčily přípravky obsahující endokannabinoidy a γ-linolenovou kyselinu. Nově se také doporučuje lokální aplikace takrolimu. Z celkové terapie se běžně používají málo účinná sedativní antihistaminika. Antiepileptikum gabapentin podávané opatrně po dialýze ovlivňuje příznivě úporný pruritus. S různým úspěchem se také zkouší podávání aktivního uhlí, cholestyraminu, erytropoetinu, thalidomidu a ondansetronu (11, 13). Z fyzikální terapie se jeví jako nejvíce účinná metoda fototerapie širokospektrým UVB zářením, která snižuje produkci pruritogenního interleukinu-2, oslabuje diferenciaci Th1 lymfocytů, zabraňuje uvolnění neuropeptidů, jako je substance P, a potlačuje degranulaci žírných buněk. Také úzkopásmové UVB záření může být efektivní (2, 5).
V dnešní době se již nepozorují další nespecifické změny svědčící pro velmi pokročilé selhání ledvin, jako je bílý poprašek způsobený krystalky močoviny ve vousech a na trupu v místě potních žláz („uremic frost“) nebo erythema papulatum uremicum s tvorbou velkých papulí na erytémovém podkladě na dlaních, ploskách a obličeji.
Specifické dermatózy
Při chronickém selhání ledvin je snížené vylučování fosfátů a porušen příjem vápníku, což způsobuje sekundární hyperparatyreózu. Při ní dochází k mobilizaci kalcia a fosfátů z kostí, což může vyvolat metastatickou kalcifikaci do kůže (calcinosis cutis), kdy se okolo velkých kloubů a na špičkách prstů najdou tvrdé hrboly modravé barvy, někdy s vylučováním křídového materiálu (4, 13). Projevy se spontánně hojí při normalizaci hladin vápníku a fosfátů.
Kalcifikace malých a středně velkých cév (kalcifická uremická arteriolopatie, kalciphylaxis) je život ohrožující stav způsobující progresivní kožní ischémii a nekrózu. Onemocnění postihuje hlavně obézní bílé ženy, pacienty léčené hemodialýzou, ale i po transplantaci, s cukrovkou a zvýšenými hladinami vápníku a fosfátů. V patogenezi se předpokládají poruchy v kalcifikaci kostí a cév na podkladě molekulárních a cytochemických změn systému regulujícího minerální ukládání a resorpci kostí. V nedávné retrospektivní studii pacientů s kalcifylaxí bylo zjištěno, že 77 % nemocných bylo léčeno dialýzou a 69 % ze zbývajících nedialyzovaných pacientů trpělo ledvinným poškozením, proto selhání ledvin je považováno za nejdůležitější patogenní faktor (17). Jako další rizikové faktory se udávají také jaterní postižení, vysoká sérová hladina hliníku, warfarinizace, deficit proteinu C a S a podávání solí vápníku a vitaminu D (7, 17).
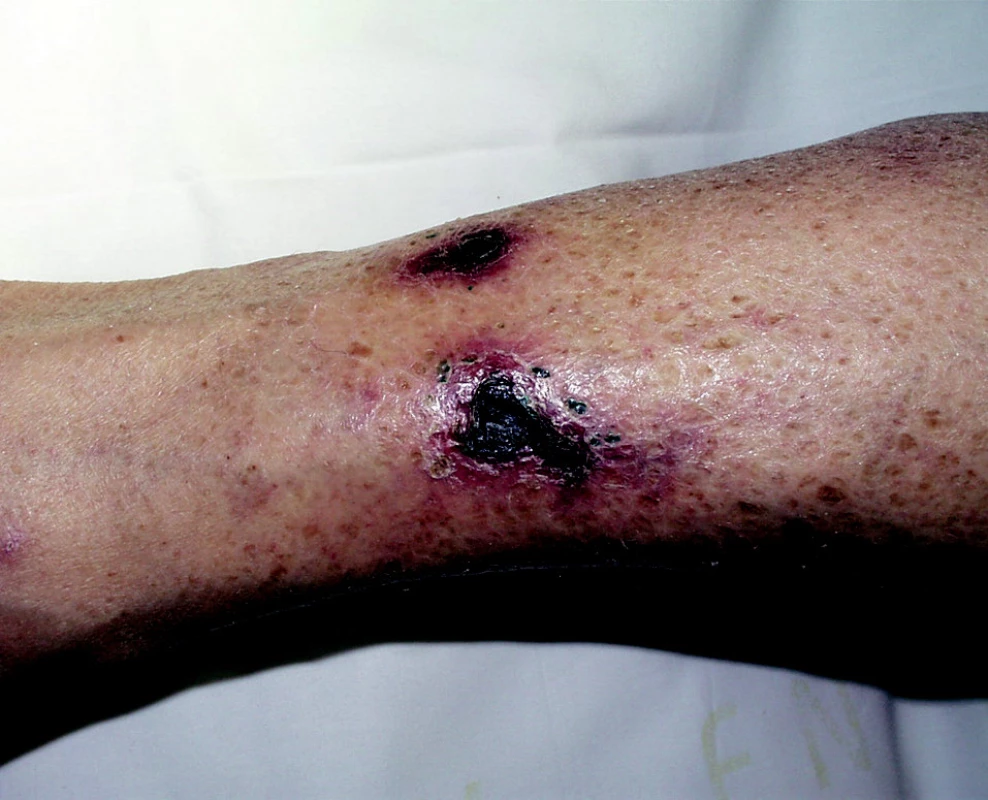
Klinicky se projevuje buď jako symetrická akrální gangréna s bolestivými ložisky na bércích (obr. 2) nebo jako destruktivní nekrotická kalcifikující panikulitida na prsou, hýždích a břiše (obr. 3). Zpočátku se tvoří symetricky bolestivá skvrnitá nafialovělá ložiska, připomínající livedo reticularis, postupně vznikají hemoragické puchýře a až během týdnů se vytvoří velmi bolestivé hluboké nekrotické vředy, které mohou být příčinou autoamputace prstů či penisu (obr. 4). Mortalita při proximálním postižení je 50 až 80 %, nejčastější příčinou úmrtí je sepse. Diagnóza se stanoví podle anamnézy renálního selhání, klinických rysů a podle histologického nálezu kalcifikace tunica media a proliferace intimy arteriol a malých tepen v koriu a podkoží, někdy s patrným fibrinovým trombem v luminu (1). Nemocní mohou mít jak nízké, tak vysoké hladiny parathormonu, proto jeho stanovení v souvislosti s touto komplikací nemá smysl (17).
Obr. 3. Kalcifylaxe připomínající panikulitidu. 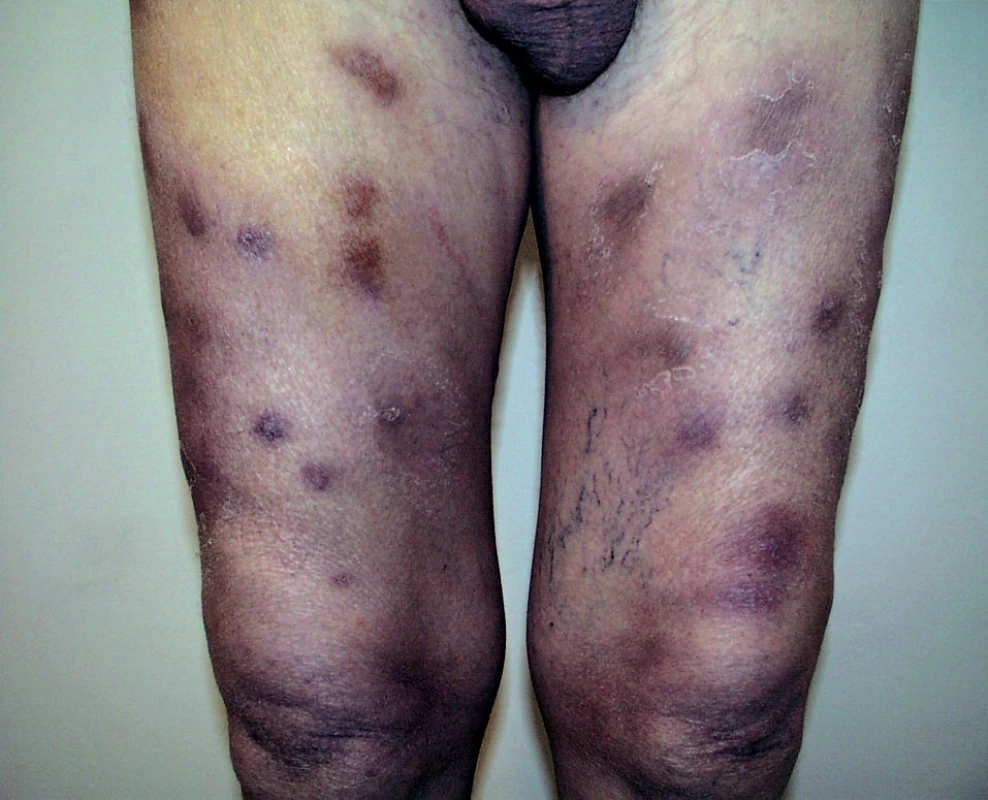
Obr. 4. Rozsáhlá nekróza při kalcifylaxi. 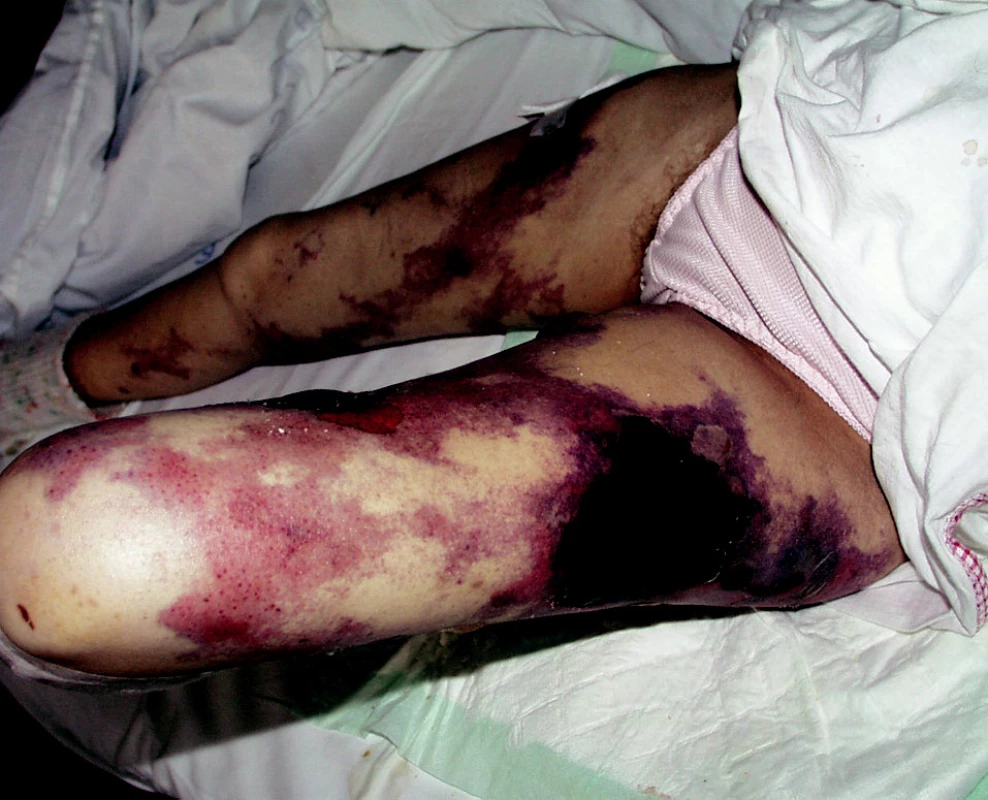
Terapie spočívá ve snížení hladiny fosforu pomocí diety a vazačů fosfátů, zejména těmi, které neobsahují vápník, jako je sevelamer nebo lanthan (7). Podání systémových kortikosteroidů nemá význam. Paratyroidektomie má smysl pouze v případě přítomné hyperparatyreózy, pak může vést k rychlému zhojení a vymizení bolesti. Důležité je intenzivní ošetřování vředů, chirurgický debridement a podání antibiotik k zabránění sepse. U dialyzovaných pacientů je vhodná hyperbarická oxygenoterapie, která je až v 50 % úspěšná (17).
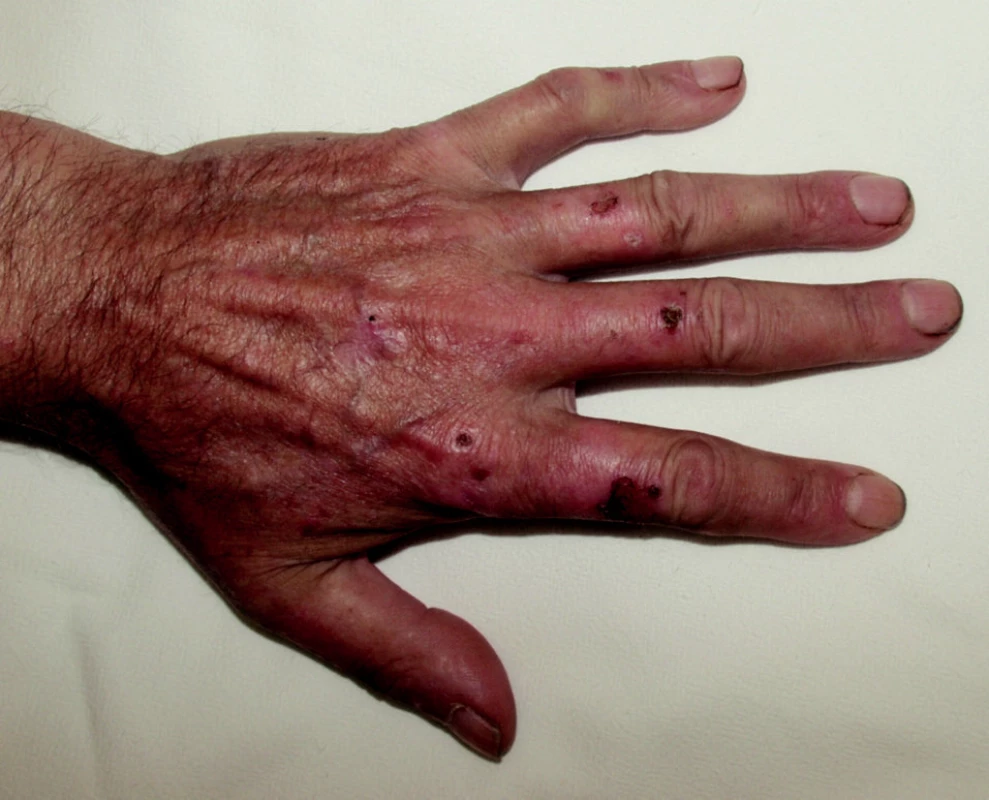
Bulózní dermatózy se pozorují u 1,2 až 9 % dialyzovaných pacientů a zahrnují pseudoporfyrii a pozdní kožní porfyrii (13). Pseudoporfyrie je chronické puchýřnaté onemocnění u pacientů s chronickým ledvinným selháním, léčených hemodialýzou nebo peritoneální dialýzou. Klinicky připomíná porphyria cutanea tarda, ale hladiny porfyrinů v séru, moči a stolici nejsou zvýšené. Charakteristické jsou drobné subepidermální puchýře, jizvy, hyperpigmentace a milia v místech sluneční expozice na hřbetech rukou (obr. 5). Hypertrichóza a sklerodermiformní změny nebývají přítomny. Příčina nemoci je nejasná, zvažují se různé faktory jako fotoaktivní léky, aluminium hydroxid, hemosideróza, silikonové částice, erytropoetin a volné kyslíkové radikály. Podíl na vzniku kožních změn mohou mít také změny v dermálních kapilárách a snížená oxygenace podkoží během dialýzy, což usnadní vznik puchýřů po mechanickém poranění. K léčení se používají pouze lokální přípravky k zabránění sekundární infekce, důležitá je fotoprotekce (8, 9).
Porphyria cutanea tarda se může také u pacientů vyskytnout, ale odlišení od pseudoporfyrie je obtížné, protože i asymptomatičtí dlouhodobě dialyzovaní nemocní mívají vyšší plazmatické hladiny uroporfyrinů. Choroba může vznikat na podkladě ztížené schopnosti vylučovat porfyriny, které jsou špatně dialyzovatelné konvenčními membránami. Dalším navrženým mechanismem je azotémie způsobující snížení aktivity uroporfyrinogen dekarboxylázy (8,9).
Histopatologické rysy obou nemocí jsou stejné. Jde o subepidermální puchýř, někdy s nápadně zachovalým reliéfem dermálních papil na spodině a s řídkým perivaskulárním lymfocytovým infiltrátem. Intraepidermálně v krytbě puchýře se mohou najít tzv. housenkovitá tělíska (z angl. caterpillar), což jsou eozinofilně se barvící podlouhlá tělíska obsahující kolagen IV. Nález je specifický pro porfyrii, ale bývá přítomen v méně než v polovině případů. Při přímé imunofluorescenci jsou v dermoepidermální junkci patrné granulární uloženiny imunoglobulinu IgG a C3 a v horním koriu zesílené krevní cévky připomínající koblihy (z angl. doughnut-like blood vessels), cytoidní tělíska bývají spíše u pozdní kožní porfyrie než u pseudoporfyrie (1). Nepřímá imunofluorescence je negativní.
Celková terapie bývá obtížná, chlorochin není účinný při anurii. Lze zkusit venepunkce jen s 50–100 ml krve týdně, popřípadě v kombinaci s erytropoetinem. Důležitá je fotoprotekce (13).
Perforující dermatózy jsou souhrnný název pro různé nemoci jako perforující nemoc při urémii, morbus Kyrle, reaktivní perforující kolagenóza, perforující folikulitida a elastosis perforans serpiginosa. Při těchto nemocech jsou součásti koria, jako jsou kolagenní a elastická vlákna, vytlačovány skrz epidermis.
Reaktivní perforující kolagenóza, morbus Kyrle a perforující folikulitida jsou nejvíce popisovány u pacientů s chronickým selháním ledvin na podkladě diabetické nefropatie. Choroba postihuje až 10 % dialyzovaných pacientů většinou afro-karibského původu. Zejména na končetinách nad extenzory v místech ochlupení a tření vznikají úporně svědící seskupené kónické papuly až hrboly s centrální hyperkeratotickou zátkou (obr. 6). Změny mohou být i na obličeji a ve kštici. Projevy se hojí spontánně za vzniku hyperpigmentovaných jizviček, současně se však tvoří nové.
Obr. 6. Perforující dermatóza. 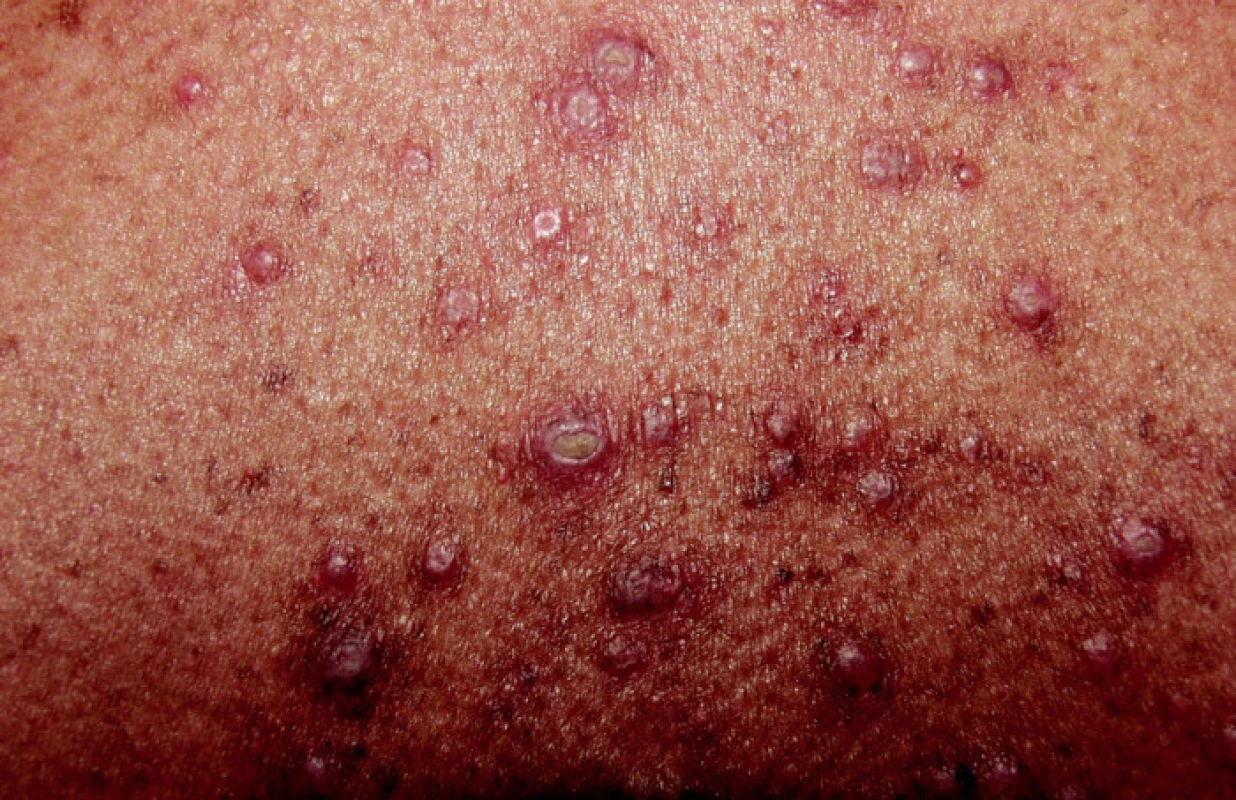
Patogeneze je neznámá, předpokládá se, že jde o abnormální epidermální proliferaci jako odpověď na povrchní traumatizaci při pruritu a současné diabetické vaskulopatii. Histologicky se najde transepidermální kanálek vyplněný keratotickou zátkou s bazofilně se barvícími degenerovanými vlákny kolagenu a různým počtem zánětlivých buněk. Při folikulitidě se může nalézt i stočený chlup. V okolní epidermis je akantóza (1, 13). V léčbě se osvědčila fototerapie úzkopásmovým UVB zářením, lokální ošetřování tretinoinem či účinnými kortikosteroidy a kryoterapie jednotlivých projevů (10).
Nefrogenní systémová fibróza (původně nazvaná nefrogenní fibrotizující dermopatie) je multisystémové onemocnění nedávno popisované v různých dialyzačních centrech u pacientů s ledvinným selháním. První případy se objevily až v roce 1997 a zcela nedávno se zjistilo, že komplikace postihuje ty pacienty s akutním či chronickým ledvinným selháním, kteří podstoupili vyšetření nukleární magnetickou rezonancí s i.v. aplikací kontrastní látky obsahující gadolinium. K rozvoji onemocnění došlo v rozmezí 2–11 týdnů po podání kontrastní látky (3). Patogeneze není zatím objasněna, jako možné faktory se zvažují hyperkoagulační stavy, cévní chirurgické výkony, nedávné selhání transplantátu, metabolická acidóza. Často vzniku předchází buď cévní chirurgický výkon nebo epizoda žilní trombózy, které jsou důvodem radiodiagnostického vyšetření.
Onemocnění připomíná klinicky i histologicky systémovou sklerodermii. Projevuje se hyperpigmentovanou, tuhou, napjatou pokožkou symetricky na končetinách, vzhledu pomerančové kůže. Na rozdíl od sklerodermie nebývá postižen obličej. Následkem sklerotizace kůže a podkoží dochází ke kontrakturám a snížené hybnosti kloubů končetin. Později může dojít i k fibrotizaci vnitřních orgánů (např. myokardu, plic, jater, ledvin, kostí či svalů). Onemocnění má rychlý progresivní průběh s vysokou mortalitou – 48 % (6). Histologicky se zjistí zesílené kolagenní svazky, uloženiny mucinu v dermis a zvýšené množství fibrocytů a elastických vláken.
V léčbě se doporučuje okluze s kalcipotriolem, plazmaferéza, extrakorporální fotoferéza a celkové kortikosteroidy. Zkouší se také rychlé zavedení dialýzy, která může odstranit většinu podané kontrastní látky. V roce 2006 bylo vydáno doporučení FDA, aby byla věnována zvýšená pozornost pacientům s pokročilou renální insuficiencí, kteří podstupují MR vyšetření s podáním kontrastní látky obsahující gadolinium (6).
Závěr
Kožní projevy chronického selhání ledvin mohou vést ke zvýšené morbiditě a dokonce i mortalitě nemocných. Se zavedením dialýzy se zvyšuje doba přežívání pacientů, což umožňuje vznik mnohých kožních změn. Tyto kožní potíže bývají v praxi často přehlížené. Jejich včasné odhalení a správné léčení může významně zlepšit kvalitu života pacientů s chronickým ledvinným selháním.
Došlo do redakce: 17.12.2007
Doc. MUDr. Petra Cetkovská, Ph.D.
Dermatovenerologická klinika FN a LFUK, Plzeň
Dr. E. Beneše 13
306 99 Plzeň
E-mail: cetkovska@fnplzen.cz
Zdroje
1. ABDELBAQI-SALHAB, M., SHALHUB, S., MORGAN, MB. A current review of the cutaneous manifestations of renal disease. J Cutan Pathol, 2003, 30, p. 527-538.
2. ADA S., SEςKIN D., BUDAKOGLU I., et al. Treatment of uremic pruritus with narrowband ultraviolet B phototherapy: an open pilot study. J Am Acad Dermatol, 2005, 53, p.149-151.
3. BROOME, DR., GIRGUIS, MS., BARON, PW., et al. Gadodiamide-Associated Nephrogenic Systemic Fibrosis: Why Radiologists Should Be Concerned Am. J. Roentgenol, 2007, 188, p. 586-592.
4. CALLEN, JP. Cutaneous nephrology. In: CALLEN, JP., JORIZZO, JL. (Eds) Dermatological signs of internal disease. Elsevier Science Ltd., 3rd Ed, 2003, p.271-274.
5. CETKOVSKÁ, P., KOŠŤÁLOVÁ, D., EISELT, J. Léčba uremického pruritu UVB fototerapií. Čes-slov Derm, 1992, 67, s. l54-157.
6. COWPER, SE. Nephrogenic Fibrosing Dermopathy. [NFD/NSF Website]. 2001-2007. Available at http://www.icnfdr.org.
7. FINUCANE, KA., ARCHER, CB. Dermatological aspects of medicine: recent advances in nephrology. Clin Exper Dermatol, 2005, 30, p.98-102.
8. GREEN, JJ., MANDERS, SM. Pseudoporphyria. J Am Acad Dermatol, 2001, 44, p.100-108.
9. MALINA, L. Pseudoporfyrie. Čes-slov Derm, 2007, 82, s.12-15.
10. OHE, S., DANNO, K., SASAKI, H., et al. Treatment of acquired perforating dermatosis with narrowband ultraviolet B. J Am Acad Dermatol , 2004, 50, p.892-894.
11. PATEL, TS., FREEDMAN, BI., YOSIPOVITCH, G. An update on pruritus associated with CKD. Am J Kidney Dis, 2007, 50, p. 11-20.
12. PISONI, RL., WIRKSTRÖM, B., ELDER, SJ., et al. Pruritus in haemodialysis patients: international results from the Dialysis outcomes and praktice patterns study. Nephrol Dial Transplant, 2006, 21, p. 3495-3505.
13. ROBINSON-BOSTON, L., DiGIOVANNA, JJ.: Cutaneous manifestations of end stage renal disease. J Am Acad Dermatol, 2000, vol.43, p.975-986.
14. SZEPIETOWSKI, JC. et al.: Uremic pruritus: a clinical study of maintenance hemodialysis patients. J Dermatol, 2002, 29, p.621-627.
15. ŠTORK, J. Kožní symptomatologie u pacientů v chronickém hemodialyzačním léčení. Čes-slov Derm, 1988, 63, s. 256-265.
16. UDAYAKUMAR, P., et al. Cutaneous manifestations in patients with chronic renal failure on hemodialysis. Indian J Dermatol Venereol Leprol, 2006, 72, p.119-125.
17. WEENIG, RH., SEWELL, LD., DAVIS, MDP., et al. Calciphylaxis: natural history, risk factor analysis and outcome. J Am Acad Dermatol, 2007, 56, p.569-579.
18. YOSIPOVITCH, G., DUQUE, MI., PATEL, TS., et al. Skin barrier structure and function and their relationship to pruritus in end-stage renal disease. Nephrol Dial Transplant, 2007, 22, p. 3268-3272.
Štítky
Dermatologie Dětská dermatologie
Článek vyšel v časopiseČesko-slovenská dermatologie
Nejčtenější tento týden
2008 Číslo 2- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
- Condylomata accuminata a jejich prevence i léčba
- HydroCleanem efektivně hojíme onkologické rány po radioterapii
- Proces hojení ran krok za krokem a co ho může zkomplikovat
-
Všechny články tohoto čísla
- 12. Kongres European Society of Cosmetic and Aesthetic Dermatology (ESCAD) a 2. Mezinárodní sympozium
- Odborné akce v r. 2008
- Neví někdo dosud snad, co znamená zkratka SAD?
- Kožní projevy u chronické renální insuficience
- Doškolování lékařů – Kontrolní test
- Atopické epikutánní testy – metodika a význam
- Spinocelulární karcinom v 61 let staré jizvě po popálení
- Primární kožní difuzní velkobuněčný B-lymfom dolních končetin: Popis případu a přehled literatury
- Amelanotický a akrolentiginózní melanom
- Klinický případ: Folikulárně vázané makulopapuly a pustuly v obličeji
- 12. kongres Evropské společnosti pro kosmetickou a estetickou dermatologii (EASCAD) a 2. Mezinárodní sympozium estetické medicíny
- Zápis ze schůze výboru ČDS konané dne 17. ledna 2008 v Praze
- Zápis ze schůze výboru ČDS konané dne 21. února 2008 v Praze
- Zápisnica zo zasadnutia výboru Slovenskej dermatovenerologickej spoločnosti dňa 14. 12. 2007
- Zpráva z 66. výročního mítinku Americké dermatologické akademie
- Česko-slovenská dermatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Kožní projevy u chronické renální insuficience
- Amelanotický a akrolentiginózní melanom
- Atopické epikutánní testy – metodika a význam
- Klinický případ: Folikulárně vázané makulopapuly a pustuly v obličeji
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání