-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Štúdium lokálnych anestetík: Časť 206*
Micelizácie vybraných kvartérnych amóniových solí odvodených od heptakaínu
Study of local anaesthetics: Part 206*
Micellization of selected of quaternary ammonium salt derived from heptacaineMicellization of selected quaternary ammonium compounds derived from heptacaine have been studied by absorption spectroscopy in the UV/VIS spectral region with the use of a pyrene probe. The compounds studied in the aqueous solution have been marked as H22, H26, H27, H29, H34, H + Al and H + B and the derivative marked as H34 was studied in a 3 mol/l ethanol solution at the temperature of 25 °C. In the homologous series of the studied bromides H22, H26, H27 and H29, cmc was observed to be dependent on the number of carbon atoms nc in the hydrophobic chain: ln (cmc) = –3.131–0.421nC. The Free Gibbs energy necessary for the transfer of a methyl group of the alkyl chain from the water phase to the inner part of the micelle at the temperature of 25 °C is (–0.421 ± 0.034)RT.
Key words:
heptacaine • quaternary ammonium compounds • critical micelle concentration • pyrene • Boltzmann-sigmoidal equation • alcohol
Autoři: Jana Gališinová; Jozef Čižmárik; Eva Salanci; Andrea Gálusová; Lenka Stopková; Fils Andriamainty
Vyšlo v časopise: Čes. slov. Farm., 2015; 64, 144-148
Kategorie: Původní práce
Souhrn
Použitím absorpčnej spektroskopie UV/VIS s pyrénom bola preskúmaná micelizácia vybraných kvartérnych amóniových solí odvodených od heptakaínu (látky s pracovným označením H22, H26, H27, H29, H34, H37, H + Al a H + B) vo vodných prostrediach a derivát H34 v 3 mol/l etanolovom roztoku pri teplote 25 °C. V homologickom rade študovaných bromidov H22, H26, H27 a H29 hodnoty cmc exponenciálne závisia od počtu atómov uhlíka nC v hydrofóbnom reťazci: ln (cmc) = –3,131–0,421nC. Voľná Gibbsova energia prenosu jednej metylénovej skupiny alkylového reťazca z vodnej fázy do vnútra micely pri teplote 25 °C má hodnotu (–0,421 ± 0,034)RT.
Kľúčové slová:
heptakaín • kvartérne amóniové soli • kritická micelová koncentrácia • pyrén • sigmoidálna-Boltzmannova rovnica • alkoholÚvod
Dlhoročným predmetom štúdia Katedry farmaceutickej chémie Farmaceutickej fakulty Univerzity Komenského v Bratislave sú bázické estery substituovanej kyseliny fenylkarbámovej, ktoré preukazujú lokálne anestetickú, β-adrenolytickú, antiarytmickú, spazmolytickú, antivírusovú či antimikrobiálnu aktivitu1). Cieľom tohto výskumu bola a je syntéza takých derivátov, ktoré vykazovali silnú biologickú aktivitu, vysokú stabilitu a čo najmenšie nežiaduce účinky ako systémovú toxicitu či dráždivosť. Výsledkom tohto rozsiahlého štúdia bol výskum a vývoj štyroch nových originálnych potenciálnych liečiv, a to: pentakaíniumchloridu, heptakaíniumchloridu, karbizokaíniumchloridu ako lokálnych anestetík a látky H + B (heptakaíniumbenzylchloridu), ktorý okrem lokálnej anestézie vykazoval aj antiarytmické účinky.
Molekuly týchto derivátov májú amfifilnú povahu, kde charakteristický intermediárny, spojovací reťazec predstavuje karbamátová skupina –NH-COO - s najčastejšie dvojuhlíkovým reťazcom, ktorý môže byť cyklizovaný či vetvený. Hydrofóbnu časť tvorí substituované benzénové jadro. Hydrofilná polárna hlavička je prezentovaná kvartérnym dusíkom, ktorý môže byť súčasťou heterocyklu.
Výsledkom dvojakej povahy molekuly takýchto látok je, že už v nízkej koncentrácii v roztoku preukazujú dva významné a charakteristické typy správania sa: adsorpcia na medzipovrchoch a agregácia v roztoku. Vzniknuté koloidné agregáty sa nazývajú micely a v závislosti od tvaru amfifilnej látky a od jej koncentrácie v roztoku nadobúdajú rôzne podoby.
Akonáhle sa dosiahne kritická micelová koncentrácia (cmc), pri ktorej sa v roztoku začína formácie miciel, dochádza k mimoriadnym zmenám. Zo závislostí niektorých fyzikálno-chemických vlastností od koncentrácie amfifilnej látky je možné rozličnými metódami a postupmi stanoviť hodnotu cmc.
Hodnoty kritických micelových koncentrácií vybraných derivátov substituovanej kyseliny fenylkarbámovej sa determinujú využitím absorpčnej spektroskopie vo UV oblasti spektra pomocou molekuly pyrénu ako sondy.
Cieľom predloženej práce je štúdium agregačných vlastností roztokov vybraných kvartérnych amóniových solí odvodených od heptakaínu vo vodnom a pyrénovom prostredí pri teplote 25 °C.
Pokusná časť
Študované látky
Vybrané kvartérne amóniové soli odvodené od heptakaínu boli zosyntetizované podľa práce Čižmárika a spol.2, 3) sú uvedené v tabuľke (tab. 1). Všetky študované deriváty sú biele kryštalické látky.
Tab. 1. Študované kvartérne amóniové soli odvodené od heptakaínu 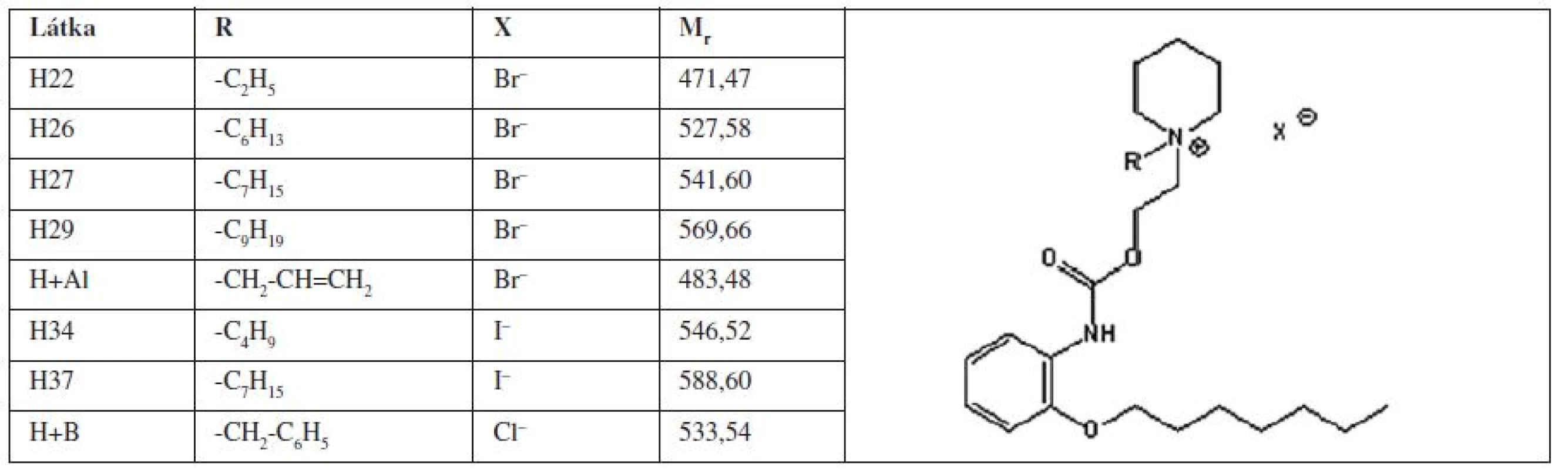
Chemikálie
Pyrén, puriss. p.a., pre fluorescenciu, ≥ 99,0 %, central CHEM; etanol UV, ~ 96 % (v/v), central CHEM; aqua purificata.
Prístroje
Spektrofotometer Analytik Jena SPEKOL 1300 (Nemecko); teplomer VARIO THERM MAX; ultrazvukový kúpeľ Bandelin Sonorex (Nemecko).
Rozpustnosť vo vode
Látky H22, H26, H+Al a H+B boli vo vode ľahko rozpustné, bromidy H27, H29 mierne rozpustné, jodid H37 ťažko rozpustný, zatiaľ čo jodid H34 vo vode prakticky nerozpustný. Preto bola látka H34 študovaná v 3 mol/l etanolovom roztoku. V menej koncentrovaných etanolových prostrediach sa uvedený derivát vyzrážal. Pre uvedenie látky H37 do roztoku bol použitý ultrazvuk a zahrievanie do 40 °C opakovane.
Pracovný postup
Príprava pyrénového roztoku
Bol pripravený zásobný roztok pyrénu s c = 0,0012 mol/l rozpustením výpočtom zisteného množstva pyrénu v etanole UV (~ 96% (v/v)) pomocou ultrazvuku (15 min). Experimentálny 2 μmol/l pyrénový roztok sa získal zriedením zásobného roztoku nasledujúcim postupom v závislosti od objemu meraného roztoku vzorky: 5 μl pyrénového roztoku do 3 ml roztoku vzorky, 4,2 μl do 2,5 ml, resp. 3,3 μl do 2 ml meraného roztoku. Takto nízka koncentrácia etanolu vo vzorke nie je schopná ovplyvniť správanie sa surfaktantu v roztoku.
Príprava zásobných roztokov vzoriek
Zásobné roztoky študovaných látok sa pripravili rozpustením výpočtom stanoveného množstva látky vo vode. K meranému zásobnému roztoku sa pridal taký objem pyrénového zásobného roztoku, aby sa dosiahla 2 μmol/l koncentrácia pyrénu v roztoku vzorky. Postupným riedením zásobného roztoku látky boli pripravené roztoky s nižšími koncentráciami vo vhodne zvolených intervaloch a to takým spôsobom, aby sa zachovala koncentrácia pyrénu v meranom roztoku.
Absorpčné spektrum pyrénu
Pyrén preukazuje charakteristické absorpčné spektrum so silnými a slabými píkmi v UV oblasti spektra. Jeho UV spektrum v podstate vedie k určeniu cmc surfaktantu.
Absorpčné spektrum pyrénu ukazuje osem píkov silných (s) a slabých (w, angl. weak) pri 232w, 242s, 252w, 260w, 272s, 308w, 320s a 336s nm, ako je znázornené v grafu 14).
Graf 1. Príklad absorpčných spektier pyrénu v rôznych prostrediach<sup>4)</sup> 
Výsledky a diskusia
Podľa pracovného postupu boli pripravené zásobné roztoky skúmaných derivátov vo vode i etanolový zásobný roztok pyrénu. Riedenia roztokov sa uskutočnili priamo v meranej kyvete. Pomocou spektrofotometra SPEKOL 1300 boli merané absorpčné spektrá látok v prítomnosti 2 μmol/l pyrénu v rozmedzí vlnových dĺžok 200–400 nm pri teplote 25 °C proti zodpovedajúcemu porovnávaciemu roztoku.
V absorpčných spektrách každého nariedeného roztoku študovanej látky sa sledovali nezastreté hlavné pyrénové píky pomocou komerčného programu WinASPECT a zaznamenávali sa im odpovedajúce hodnoty absorbancií pri daných vlnových dĺžkach.
Hodnoty kritických micelových koncentrácií boli stanovené zo závislostí Atot od koncentrácie c látky v roztoku, ktorá vykazuje charakateristický sigmoidálny priebeh.
V absorpčných spektrách vybraných kvartérnych amóniových solí odvodených od heptakaínu vo vodnom prostredí v prítomnosti pyrénu boli charakteristické pyrénové píky nezastreté pri vlnových dĺžkach 336 nm a 320 nm.
Pre ilustráciu grafy 2 až 5 zobrazujú závislosti súčtu absorbancií všetkých hlavných pyrénových píkov (Atot) od koncentrácie látky (c) v roztoku pri 25 °C a majú charakteristický sigmoidálny priebeh so stúpajúcou tendenciou. Vnútorné grafy predstavujú závislosti absorbancií (A) jednotlivých pyrénových píkov od koncentrácie látky.
Graf 2. Závislosť súčtu absorbancií hlavných pyrénových píkov (A<sub>tot</sub>) od koncentrácie (c) látky H22 vo vodnom prostredí pri 25 °C Vnútorný graf: závislosť absorbancie (A) jednotlivých pyrénových píkov (336 nm a 320 nm) od koncentrácie študovanej látky 
Graf 3. Závislosť súčtu absorbancií hlavných pyrénových píkov (A<sub>tot</sub>) od koncentrácie (c) látky H + Al vo vodnom prostredí pri 25 °C Vnútorný graf: závislosť absorbancie (A) jednotlivých pyrénových píkov (336 nm a 320 nm) od koncentrácie študovanej látky 
Graf 4. Závislosť súčtu absorbancií hlavných pyrénových píkov (A<sub>tot</sub>) od koncentrácie (c) látky H + B vo vodnom prostredí pri 25 °C Vnútorný graf: závislosť absorbancie (A) jednotlivých pyrénových píkov (336 nm a 320 nm) od koncentrácie študovanej látky 
Graf 5. Závislosť súčtu absorbancií hlavných pyrénových píkov (A<sub>tot</sub>) od koncentrácie látky H34 (c) v 3 mol/l etanolovom prostredí pri 25 °C Vnútorný graf: závislosť absorbancie (A) jednotlivých pyrénových píkov (336 nm a 320 nm) od koncentrácie študovanej látky 
Hodnoty kritických micelových koncentrácií boli determinované zo závislostí Atot od koncentrácie c surfaktantu fitovaním sigmoidálnou Boltzmannovou funkciou podľa nasledujúcej rovnice:
kde ai a af sú iniciálne a konečné (angl. final) asymptoty sigmoidy, x ako nezávislá premenná je koncentráciou surfaktantu, x0 je stred sigmoidy a Δx nezávislé rozmedzie, kde dochádza k náhlej zmene.
Táto funkcia poskytuje dve hodnoty X1 a X2, jednu pri x0 a ďalšiu pri (x0 + 2Δx). Pomer x0/Δx je návodom pre rozlíšenie, ktorá z nich je považovaná za cmc. Pre amfifilné systémy, ktorých (x0/Δx) < 10, platí, že X1 = cmc = x0, a pre systémy, kde (x0/Δx) > 10, zase X2 = cmc = (x0 + 2Δx)4, 5).
V prípade vodných roztokov všetkých študovaných derivátov mal pomer x0/Δx hodnotu menšiu ako 10, teda hodnota X1 sa považuje za cmc a nadobúda hodnotu x0. Determinované hodnoty kritických micelových koncentrácií vybraných kvartérnych amóniových solí odvodených od heptakaínu a parametre všetkých sigmoidálnych funkcií (počet fitovaných bodov z, počet atómov uhlíka nC v hydrofóbnom reťazci, hodnoty x0, Δx, pomer x0/Δx, koeficient determinácie R2, chi-kvadrát (χ2), hodnoty X1, X2) sú uvedené v súhrnnej tabuľke 2).
V porovnaní s hodnotou cmc heptakaíniumchloridu (cmc = 1,97 · 10–2 mol/l), ktorá bola stanovená fluorimetrickou metódou s pyrénom i 13C NMR spektroskopiou (cmc = 2,06 · 10–2 mol/l), boli všetky hodnoty cmc skúmaných kvartérnych amóniových solí nižšie.
Z tabuľky 2 možno vidieť, že determinovaná hodnota cmc zlúčeniny H+B (X = Cl–) bola o trochu nižšia ako pri látke H + Al (X = Br–) v dôsledku zvýšenej lipofility6, 7) a prítomnosti Cl– ako protiiónu7–10). Z tabuľky 2 možno vidieť, že determinovaná hodnota cmc zlúčeniny H + B bola len o trochu nižšia ako pri látke H + Al.
Tab. 2. Parametre fitovaných funkcií s determinovanými hodnotami cmc vybraných kvartérnych amóniových solí odvodených od heptakaínu pri 25 °C 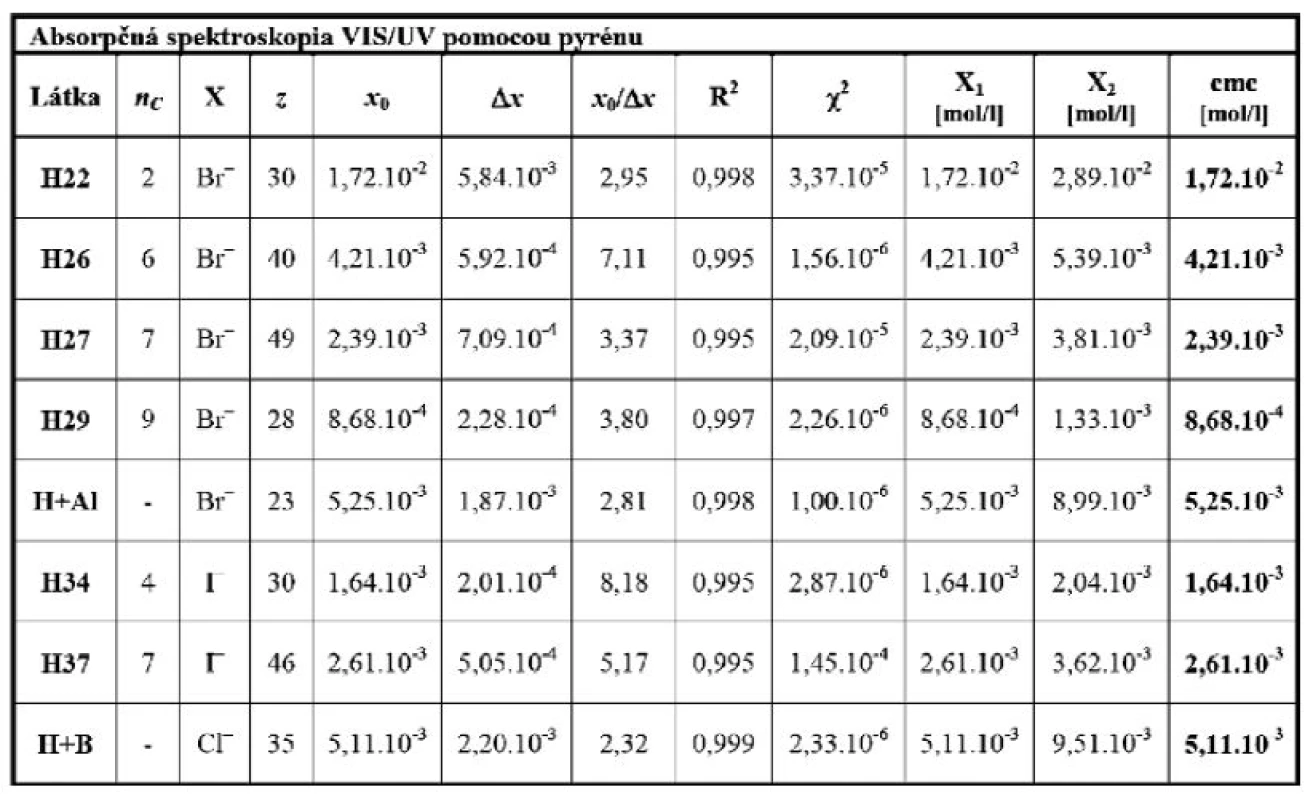
V homologickom rade študovaných bromidov H22, H26, H27 a H29 hodnoty cmc exponenciálne závisia od počtu atómov uhlíka nC v alkylovom reťazci11), resp. hodnoty ln(cmc) závisia od nC lineárne podľa vzťahu: (ln (cmc) = –3,131–0,421nC). Voľná Gibbsova energia prenosu jednej metylénovej skupiny alkylového reťazca z vodnej fázy do vnútra micely pri teplote 25 °C má hodnotu (–0,421 ± 0,034)RT podľa rovnice:
kde parameter B predstavuje príspevok každej metylénovej skupiny ku kritickej micelovej koncentrácii a je smernicou závislosti ln(cmc) od nC, R je molová plynová konštanta a T je termodynamická teplota.
Z tabuľky 2 tiež vyplýva, že stanovená hodnota cmc jodidu H37 je len o málo vyššia ako jeho bromidového analógu, tak ako hovorí teória o miere viazanosti protiiónov7, 11).
Osobitným prípadom stanovenia cmc pomocou absorpčnej spektroskopie bol derivát H34 (nC = 4, X = I–). Príprava jeho vodného roztoku bola neúspešná, ako bolo uvedené vyššie, preto sme postupne pripravili jeho etanolový roztok. Koncentrácia etanolu v konečnom zásobnom roztoku bola 3 mol/l. Všeobecne prítomnosť etanolu v roztoku zvyšuje hodnoty cmc iónových surfaktantov6, 7, 12, 13) a rovnako prítomnosť aniónu I – menej podporuje micelizáciu oproti protiiónom Br– a Cl– 8, 9, 14).V konečnom dôsledku bola hodnota cmc jodidu H34 nižšia ako predpokladaná cmc = 8,1 · 10–3 mol/l pri bromidovom deriváte s nC = 4 v homologickom rade podľa funkcie ln(cmc) = –3,131–0,421nC. Vplyv veľkého množstva etanolu ako aditíva na hodnotu cmc skúmaného derivátu bol výrazný. Takýto pokles v hodnotách cmc vplyvom alkoholu s krátkym reťazcom vo vyššej koncentrácii bol pozorovaný aj pri pentakaíniumchloride (graf 6) a v roku 2011 podobný priebeh zaznamenali Gališinová s kolektívom15).
Graf 6. Závislosť kritickej micelovej koncentrácie pentakaíniumchloridu od koncentrácie metanolu v jednotlivých roztokoch (mol/l) 
Metanol ako organické aditívum triedy II7) zvyšuje hodnotu cmc roztoku surfaktantu oproti jeho vodnému roztoku7, 12, 13, 15–17). A so zvyšujúcou sa koncentráciou alkoholu v roztoku hodnota cmc ešte stúpa13).
Pri pentakaíniumchloride v metanolových prostrediach hodnota cmc stúpala s koncentráciou metanolu len pri 0,2 mol/l a 0,3 mol/l. Pri vyššej koncentrácii tohto alkoholu (0,4 mol/l a 0,5 mol/l) hodnota cmc klesala (graf 6). Podobný priebeh bol pozorovaný v práci15).
Prídavok alkoholu narúša štruktúru solvatovanej vrstvy micely (solvatovanej vody na povrchu), alebo prednostne solvatuje molekuly rozpustenej látky. Je známe, že alkohol s dlhším uhlíkovým reťazcom penetruje do palisádovej vrstvy miciel a znižuje cmc surfaktantu7, 18–21). A hoci v prípade pentakaíniumchloridu v metanolových prostrediach ide o alkohol s krátkym uhlíkovým reťazcom, predpokladáme, že pri ich vyššej koncentrácii v roztoku dochádza k penetrácii do micely, čím sa zníži cmc, a teda sa podporí schopnosť tvorby miciel. Alebo sa pravdepodobne začnú tvoriť samotné metanolové agregáty, dochádza k desolvatácii rozpustenej študovanej látky, cmc preto klesne. Pre potvrdenie tohto deja je však potrebné uskutočniť ďalšie merania s využitím iných experimentálnych techník.
Stret záujmu: žiadny.
Došlo 8. júna 2015
Prijato 25. júna 2015
doc. Mgr. Fils Andriamainty, PhD. • J. Gališinová • J. Čižmárik • E. Salanci • A. Gálusová • L. Stopková
Farmaceutická fakulta UK
Katedra farmaceutickej chémie
Odbojárov 10, 832 32 Bratislava, SR
e-mail: andriamaint1@uniba.sk
*Part 205: Čes. slov. Farm. 2014; 63, 160–163.
Zdroje
1. Pokorná M. Vztah struktury a lokálně anestetického účinku ve skupině esterů alkoxysubstituované kyseliny fenylkarbámové. Čes. slov. Farm. 1998; 47, 14–20.
2. Čižmárik J., Mazáň Š., Švec P., Borovanský A. Štúdium lokálnych anestetík LXVIII: Kvartérne amóniové soli heptakaínu a jeho pentyloxyanalógu. Čes. slov. Farm. 1978; 27(10), 427–431.
3. Čižmárik J., Mazáň Š., Švec P., Borovanský A. Quarternary Ammonium Salts of Heptacaine. Die Pharmazie 1978; 33(11), 762–763.
4. Basu Ray G., Chakraborty I., Moulik S. P. Pyrene absorption can be a convenient method for probing critical micellar concentration (cmc) and indexing micellar polarity. J. Coll. Interf. Sci. 2006; 294, 248–254.
5. Aguiar J., Carpena P., Molina-Bolívar J. A., Carnero Ruiz C. J. On the determination of the critical micelle concentration by the pyrene 1 : 3 ratio method. J. Coll. Interf. Sci. 2003; 258, 116–122.
6. Holmberg K., et al. Surfactants and Polymers in Aqueous Solution, 2nd edition. Chichester: John Wiley & Sons, Ltd. 2002.
7. Rosen M. J. Surfactants and Interfacial Phenomena, 3nd edition. Hoboken: John Wiley & Sons, Inc. 2004.
8. Andriamainty F., Čižmárik J. Thermodynamic study of local anaesthetics based on heptacainium chloride derivates. Part 163: Study of local anaesthetics. Die Pharmazie 2003; 58(6), 440–441.
9. Andriamainty F., Čižmárik J., Malík I. Štúdium lokálnych anestetík: Časť 185. Termodynamické parametre heptakaíniumchloridu v prostredí roztoku NaBr. Čes. slov. Farm. 2008; 57(6), 260–264.
10. Hiemenz, P. C., Rajagopalan, R. Principles of Colloid and Surface Chemistry, 3nd edition. New York: Marcel Dekker, Inc. 1997.
11. Andriamainty F., Čižmárik J., Uhríková D., Balgavý P. Study of local anesthetics. Part 168. Critical micelle concentration of alkoxy homologs of local anesthetic heptacainium chloride determined by ion selective electrode. Sci. Pharm. 2005; 73(1), 17–25.
12. Blažej A., Hodul P., Markušová E., Novák L., Paulovič M., Vyskočil I. Tenzidy. Bratislava: Alfa 1977.
13. Carpena P., Aguiar J., Bernaola-Galván P., Carnero Ruiz C. Problems associated with the treatment of conductivity-concentration data in surfactant solutions: simulations and experiments. Langmuir. 2002; 18, 6054–6058.
14. Healy T. W., Drummond C. J., Grieser F., Murray B. S. Electrostatic surface potential and critical micelle concentration relationship for ionic micelles. Langmuir1990; 6, 506.
15. Gališinová J., Čižmárik J., Andriamainty F., Malík I. Štúdium lokálnych anestetík: Časť 195. Štúdium micelizácie pentakaíniumchloridu v metanolových a etanolových roztokoch. Čes. slov. Farm. 2011; 60(6), 290–295.
16. Andriamainty F., Čižmárik J., Mariščáková Z. Štúdium lokálnych anestetík: Časť 160. Stanovenie kritickej micelovej koncentrácie série piperidínoetylesterov 3-alkoxyfenylkarbámovej kyseliny. Čes. slov. Farm. 2002; 51(3), 154–156.
17. Chalabala M., a kol. Technologie léků. Praha: Galén 1997.
18. Akhter M. S. Effect of solubilization of alcohols on critical micelle concentration of non-aqueous micellar solutions. Coll. Surf. 1999; 157, 203–210.
19. Akhter M. S., Al-Alawi S. M. Influence of alcohols on the critical micelle concentration of non–aqueous micellar solutions. Colloids and Surfaces 2000; 164, 247–255.
20. Akhter M. S., Al-Alawi S. M. Micellar behaviour of cetyltrimethyl-ammonium bromide in N-methyl acetamide – alkanol and N,N-dimethyl acetamide – alkanol mixtures. Coll. Surf. 2002; 196, 163–174.
21. Tomi T., Maeda T., Satake I., Hayakawa K. Micelle formation of a cationic surfactant in the presence of 1,n-alkanediol and the miscibility of alcohols in micelles. Coll. Surf. 2009; 346, 28–33.
Štítky
Farmacie Farmakologie
Článek vyšel v časopiseČeská a slovenská farmacie
Nejčtenější tento týden
2015 Číslo 4- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Ukažte mi, jak kašlete, a já vám řeknu, co vám je
- Přerušovaný půst může mít významná zdravotní rizika
-
Všechny články tohoto čísla
- Stanovenie flavonoidov v prírodnom materiáli metódou HPLC
-
Účinnost fytoterapie v podpůrné léčbě diabetes mellitus typu 2
III. Momordika (Momordica charantia) - Legislativní aspekty vývoje zdravotních prostředků
- Influence of Ganoderma lucidum (Curt.: Fr.) P. Karst. on T-cell-mediated immunity in normal and immunosuppressed mice line CBA/Ca
-
Štúdium lokálnych anestetík: Časť 206*
Micelizácie vybraných kvartérnych amóniových solí odvodených od heptakaínu - Preskripce humánních léčivých přípravků na veterinárních lékařských předpisech
- Úvod do všeobecnej a klinicky aplikovanej biochémie.
- Praktická apiterapia.
- Česká a slovenská farmacie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Preskripce humánních léčivých přípravků na veterinárních lékařských předpisech
- Stanovenie flavonoidov v prírodnom materiáli metódou HPLC
-
Účinnost fytoterapie v podpůrné léčbě diabetes mellitus typu 2
III. Momordika (Momordica charantia) - Legislativní aspekty vývoje zdravotních prostředků
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání






