-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Štúdium lokálnych anestetík: Časť 205*
Štúdium stability heptakaíniumchloridu a karbizokaíniumchloridu zrýchleným neizotermickým testom
Studies of local anaesthetics: Part 205*
Studies of stability of heptacainium chloride and carbisocainium chloride using an accelerated non-isothermal testThe paper studies the kinetics of alkaline hydrolysis and stability under non-isothermal conditions of heptacainium chloride and carbisocainium chloride in the medium of aqueous-ethanolic solution of sodium hydroxide c = 0.1 mol/l and buffer solutions of values of pH 7.0 and pH 8.0. The results of the study of the kinetics of hydrolysis by means of anon-isothermal test – rate constants and activation energy values served as the basis for exact evaluation of the stability of these potential pharmaceuticals. The objective of the paper links up with the previous studies of these substances.
Keywords:
heptacainium chloride • carbisocainium chloride • stability • non-isothermal kinetics
Autoři: Mária Stankovičová; Andrea Lašáková; Veronika Medlenová; Želmíra Bezáková; Jozef Čižmárik
Působiště autorů: Katedra farmaceutickej chémie, Farmaceutická fakulta Univerzity Komenského, Bratislava, SR
Vyšlo v časopise: Čes. slov. Farm., 2014; 63, 160-166
Kategorie: Původní práce
*Časť 204: Čes. slov. Farm. 2014; 63, 22–25.
Souhrn
Práca sa zaoberá štúdiom kinetiky alkalickej hydrolýzy astability za neizotermických podmienok heptakaíniumchloridu akarbizokaíniumchloridu v prostredí vodno-etanolového roztoku hydroxidu sodného c = 0,1 mol/l a tlmivých roztokov s hodnotami pH 7,0 a pH 8,0. Výsledky štúdia kinetiky hydrolýzy neizotermickým testom – rýchlostné konštanty a hodnoty aktivačnej energie sú podkladom pre exaktné vyhodnotenie stability týchto potenciálnych liečiv. Práca svojím zameraním nadväzuje na predchádzajúce štúdie týchto látok.
Kľúčové slová:
heptakaíniumchlorid • karbizokaíniumchlorid • stabilita • neizotermická kinetikaÚvod
Študované látky heptakaíniumchlorid a karbizokaíniumchlorid
V rámci štúdia stability derivátov kyseliny fenylkarbámovej v práci hodnotíme heptakaíniumchlorid a karbizokaíniumchlorid, potenciálne liečivá s chemickým názvom: 1-2-(2-(heptyloxyfenylkarbamoyloxy))-etylpiperidíniumchlorid a N-(2-metyl-2-(2-heptyloxyfenylkarbamoyloxy)-etyl)-dietylamóniumchlorid. Látky boli pripravené na Katedre farmaceutickej chémie Farmaceutickej fakulty UK v Bratislave ako potenciálne liečivá, u ktorých bol preukázaný lokálnoanestetický a antidysrytmický účinok1–4), preto boli pre výhodné terapeutické parametre podrobené mnohostrannému výskumu5–11).
Heptakaíniumchlorid bol pripravený v rámci štúdia vplyvu alkoxysubstitúcie na lokálne anestetickú účinnosť bázických esterov kyseliny fenylkarbámovej. Patrí do homologickej série 30 látok, piperidinoetylesterov kyseliny 2-, 3-, 4-alkoxy (metoxy až decyloxy) fenylkarbámovej1). Podrobné farmakologické testy ukázali, že táto látka je 100-krát účinnejšia pri povrchovej anestézii ako kokaín a 171-krát účinnejšia pri infiltračnej anestézii ako štandard prokaín, pri toxicite 500 mg/kg. Výhodné farmakologické parametre heptakaínu boli dôvodom pre jeho hlbší farmakologický, morfologický a histologický výskum3). Antiarytmická účinnosť heptakaínu sa experimentálne potvrdila po aplikácii arytmogénneho adrenalínu4). Látka bola podrobená štúdiu stability6) a kinetike alkalickej hydrolýzy8) aj v porovnaní s bázickými analógami heptakaínu9, 10). Novšie štúdie heptakaíniumchloridu boli zamerané na separáciu metódou HPLC spolu s karbizokaíniumchloridom a pentakaíniumchloridom11) ako aj s polohovými izomérmi12). Metóda HPLC sa využila aj pri štúdiu degradácie heptakaíniumchloridu a karbizokaíniumchloridu v moči, ľudskom a králičom sére13). Štúdium interakcie homológov heptakaíniumchloridu s biologickými membránami a ich lipidovými dvojvrstvami fosfatidylcholínu získanými z vaječného žĺtka sa pozorovali pomocou spin label ESR spektroskopie. Lokálne anestetický účinok a inhibičný účinok na aktivitu (Ca-Mg) ATPázy sarkoplazmatického retikula sa zvyšoval s počtom atómov uhlíka v alkyloxy substituente po heptyloxy a hexyloxy derivát14). Ďalšie práce boli zamerané na stanovenie kritickej micelárnej koncentrácie (CMC) heptakaíniumchloridu a jeho derivátov pomocou spektrofotometrie v UV oblasti spektra v prítomností rôznych aditív15, 16) a rozpúšťadiel17). Pozornosť bola venovaná formulácii heptakaíniumchloridu do hydrogélov na báze chitosanu18), sledovaniu vplyvu pomocných látok na uvoľňovanie tohto liečiva a na jeho lokálne-anestetický účinok19).
Karbizokaíniumchlorid bol pripravený zahriatím ekvimolárneho množstva bázického alkoholu a odpovedajúceho izokyanátu v prostredí bezvodého toluénu päťhodinovým zahrievaním zmesi. Po ochladení bol toluénový roztok pretrepaný vodou, toluénová vrstva vysušená, prefiltrovaná a toluén oddestilovaný. Zvyšok bol rozpustený v bezvodom éteri a konečné látky vo forme hydrochloridu alebo oxalátu boli získané pridaním ekvimolárneho množstva éterického roztoku suchého chlorovodíku alebo kyseliny šťaveľovej. Látky boli prekryštalizované z vhodného rozpúšťadla a podrobené ďalšiemu štúdiu2). Index lokálnoanestetického účinku karbizokaínu pri povrchovej anestézii dosahuje hodnotu 251 pri porovnaní s účinnosťou kokaínu, pri infiltračnej anestézii hodnotu 416 pri porovnaní s účinnosťou prokaínu. Látka vykazuje aj antiarytmickú účinnosť2). V rámci komplexného štúdia karbizokaíniumchloridu boli vypracované niektoré postupy pre analytické hodnotenie substancie. Boli sledované termické vlastnosti, spektrálne charakteristiky, rozpustnosť a chromatografické chovanie. K stanoveniu obsahu bola navrhnutá acidimetrická titrácia v nevodnom prostredí, extrakčná titrácia v dvojfázovom systéme a extrakčné fotometrické stanovenie na základe tvorby iónového páru s farbivom5). Ďalej bola hodnotená stabilita karbizokaíniumchloridu a jeho 1% vodného roztoku, ktoré boli pripravené v čase potreby pomocou skúšok odolnosti. Sledovali sa pôsobenie zmeny teploty, vplyv elektromagnetického žiarenia v UF oblasti spektra, vplyv kyslého prostredia za použitia kyseliny octovej, vplyv oxidačného skúmadla peroxidu vodíka o rôznej koncentrácii. Pre vyhodnotenie testov sa zvolili fyzikálno-chemické metódy: tenkovrstvová chromatografia a spektrofotometria v ultrafialovej oblasti. Stabilita vodného roztoku karbizokaíniumchloridu s koncentráciou 0,1% sa sledovala v závislosti od času. Zmeny v zložení roztoku karbizokaínu, uchovávaného na svetle a v tme pri laboratórnej teplote, sa sledovali v pravidelných mesačných intervaloch už spomenutými metódami. Merala sa absorbancia roztoku pri vlnovej dĺžke druhého absorpčného maxima. Roztok sa vyhodnocoval aj organolepticky7). Výsledky štúdia kinetiky alkalickej hydrolýzy karbizokaíniumchloridu v prostredí vodno-etanolových roztokov hydroxidu sodného c = 0,1 mol/l ako aj v prostredí tlmivých roztokov sú v práci8). Pozornosť bola venovaná aj HPLC separácii tejto látky11, 13). Lokálne anestetikum karbizokaín má chirálne centrum v spojovacom reťazci, tvorí dva optické izoméry. Predpokladá sa, že tieto dva enantioméry majú rôzne farmakologické vlastnosti a biologické aktivity. Z tohto dôvodu bolo cieľom oddelenie enantiomérov pomocou HPLC s cyklodextrínom ako stacionárnou fázou20).
Neizotermické testy stability
Neizotermické testy stability boli navrhnuté ako atraktívny a alternatívny druh metód ku konvenčným izotermickým testom stability. Ich výhoda spočíva v určení kinetických parametrov reakcie pri jednom pokuse, čím sa skráti dĺžka jeho trvania. Hlavným princípom neizotermických testov je zmena teploty v priebehu pokusu pomocou vopred nastaveného programu, napr. s využitím teplotného gradientu. Skutočnosť, že sa teplota mení s časom, musí byť zohľadnená pri vyčíslení rýchlosti reakcie. Táto metóda má aj určité nevýhody. Jednou z nich sú náklady na meraciu techniku a komplikovanejšie vyhodnotenie pokusu, ktoré spočíva v matematickom vyjadrení diferenciálnych rovníc opisujúcich závislosť reakčnej rýchlosti od teploty a času21).
Mnohí autori opísali a navrhli rôzne teplotné programy rastu teploty. Jedným z nich bol aj Rogers, ktorý využíval logaritmický rast teploty v priebehu pokusu a použil nasledovnú teplotno-časovú funkciu22):
1/T0 – 1/Tt = b·1n (1 + t), [1]
kde T0 je teplota v K na začiatku experimentu, Tt je teplota v príslušnom čase t, t je čas (h) a b je konštanta úmernosti charakterizujúca rast teploty (K–1).
Aplikovaním do Arrheniovej rovnice dostaneme23):
1n f = 1n k0 – 1n (1 + EA·b/R) +
(1 + EA · b/R) ·1n (1 + t), [2]
kde k0 je rýchlostná konštanta na začiatku experimentu, EA je aktivačná energia, R je univerzálna plynová konštanta 8,315 J·mol–1.K–1, b je konštanta úmernosti charakterizujúca rast teploty a f je pre reakciu prvého poriadku (ln (A0 /At)).
Nanášaním hodnôt ln(ln A0/At) = f [1n (t + 1)] dostaneme priamku, kde smernicou priamky je [(EA·b/R) + 1] a úsek na osi y je rovný ln k0 – ln ((EA·b/R ) + 1). A0 je absorbancia v čase t = 0, At je absorbancia v čase t. Pri známej hodnote konštanty úmernosti rastu teploty b a hodnoty R môžeme vypočítať aktivačnú energiu rozkladnej reakcie a z úseku na osi y môžeme vypočítať k0. Pomocou hodnôt EA a k0 môžeme vypočítať rýchlostnú konštantu pre zvolenú teplotu21, 23) podľa vzťahu:.
ln k20 = ln k0 – EA · (1/T1 – 1/T2)/R [3]
Pokusná časť
Študované látky, použité chemikálie a prístroje
Študované látky heptakaíniumchlorid, Mr = 398,98 a karbizokaíniumchlorid, Mr = 400,99 boli pripravené vo forme hydrochloridov na Katedre farmaceutickej chémie FaF UK1, 2). Všetky použité chemikálie boli čistoty p.a. Pre sledovanie priebehu spektier látok v UF oblasti spektra sme použili UV-1800 SHIMADZU UV Spektrofotometer a na temperovanie roztokov Termostat Memmert WB 10, Nemecko.
Sledovanie stability študovaných látok neizotermickým testom vo vodno-etanolovom roztoku NaOH a v tlmivých roztokoch s hodnotou pH 7,0 a pH 8,0
Roztoky študovaných látok s koncentráciou 0,001 mol/l sme podrobili hydrolýze vo vodno-etanolovom roztoku NaOH c = 0,1 mol/l, kde koncentrácia etylalkoholu bola 50 % V/V, vo vodno-etanolovom tlmivom roztoku s hodnotou pH 7,0 a iónovou silou μ = 0,1 mol/l pripravenom z 0,58 g NaOH, 3,40 g KH2PO4 a 0,78 g KCl na celkový objem 500,0 ml v zmesi prevarenej destilovanej vody a s objemom 250,0 ml etylalkoholu; vo vodno-etanolovom tlmivom roztoku s hodnotou pH 8,0 a iónovou silou μ = 0,1 mol/l pripravenom rovnakým spôsobom z 0,92 g NaOH, 3,40 g KH2PO4 a 0,145 g KCl. Priebeh hydrolýzy sme sledovali pomocou spektrofotometrie v UV oblasti spektra. Spektrum pripravených roztokov sme zmerali a zaznamenali absorbanciu pri štyroch vlnových dĺžkach – 280 nm, 236 nm, 294 nm a 296 nm oproti slepému roztoku. Táto absorbancia prislúchala hodnote A0 v čase t = 0 h. Roztok sme preliali do 100,0 ml odmernej banky a vložili do vytemperovaného termostatu na požadovanú teplotu. V rámci experimentu sme v určitých časových intervaloch postupne odoberali vzorku, ochladili ju na laboratórnu teplotu, zmerali jej absorbanciu pri štyroch vlnových dĺžkach 280 nm, 236,60 nm, 294 nm a 296 nm oproti slepému roztoku a zvyšovali teplotu. Pre uvedené intervaly rastu teploty sme zvlášť vyhodnotili konštanty úmernosti rastu teploty b podľa rovnice [1]. Z nameraných hodnôt absorbancie sme pomocou rovnice [2] vyhodnotili neizotermický test stability študovaných látok.
Výsledky a diskusia
Heptakaíniumchlorid
Princípom neizotermických testov je zvyšovanie teploty v pravidelných časových intervaloch podľa zvoleného teplotného programu. Výhoda použitia tejto progresívnej neizotermickej kinetiky spočíva v získaní hodnôt potrebných pre určenie kinetických koeficientov rozkladných reakcií, resp. v predpovedaní stability za oveľa kratší čas v priebehu jedného pokusu. V priebehu sledovania kinetiky alkalickej hydrolýzy vo vodno-etanolovom roztoku NaOH (c = 0,1 mol/l) s koncentráciou etanolu 50 % V/V sme odoberali vzorku každých 20 min a zvyšovali teplotu v rozsahu 40–82 °C, každých 30 min sme zvyšovali teplotu v rozsahu 66–90 °C, a každých 40 min v rozsahu 66–88 °C. Na začiatku pokusu (t = 0 h) sme zmerali absorbanciu A0 vzorky, ktorú sme ešte nepodrobili hydrolýze pri vlnových dĺžkach λ = 236 nm; 280 nm; 294 nm; 296 nm. Pri rovnakých vlnových dĺžkach sme postupne zaznamenávali A v príslušnom čase. Pre každý teplotný program sme vykonali dve paralelné merania, v práci uvádzame výsledky len z jedného merania pre daný interval teplôt. Pre zistenie hodnoty aktivačnej energie bolo potrebné vypočítať pre každé meranie rast teploty b (odvodený z Rogersovho vzťahu [1]), ktorý bol číselne vyjadrený smernicou priamky funkcie 1/T0 – 1/Tt = f [ln (1 + t)], kde T0 je termodynamická teplota na začiatku pokusu, Tt v príslušnom čase t. Rozborom nameraných hodnôt absorbancií sme zistili, že je výhodnejšie kvôli eliminácii pozadia použiť rozdiel absorbancií pri vlnových dĺžkach (A280 nm – A294 nm) pri teplotnom programe v rozsahu teplôt 66–90 °C, 66–88 °C. Pri meraní v rozsahu teplôt 40–82 °C sme využili absorbanciu nameranú pri vlnovej dĺžke λ = 294 nm, ktorá počas celého experimentu rástla. Pre výpočty rýchlostných konštánt hydrolýzy k0 pri začiatočnej teplote sme použili lineárnu časť závislosti funkcie ln [ln(A0/At)] = f [ln (1 + t)] pre rozsah teplôt 66–90°C, 66–88 °C, ln [ln(Att/A0)] = f [ln (1 + t)] pre rozsah teplôt 40–82 °C. Takýto postup je doporučený na elimináciu prípadných odchýliek od linearity autormi Kerstenom a Göberom21). Hodnoty rýchlostných konštánt pri začiatočnej teplote sme vypočítali podľa rovnice [2], kde výraz [ln k0 – ln (1 + EA·b/R)] predstavuje úsek priamky uvedenej funkcie. Hodnotu aktivačnej energie EA sme vypočítali zo smernice priamky, s použitím b, konštanty úmernosti charakterizujúcej rast teploty a R univerzálnej plynovej konštanty. Z kinetickej rovnice 1. poriadku sme vypočítali príslušný polčas rozkladu chemickej reakcie t1/2. Podľa rovnice [3] sme vypočítali rýchlostnú konštantu reakcie pri t = 20 °C. V tabuľke 1 sú uvedené koeficienty lineárnych závislostí pre rovnice [2] a [3]. Hodnota a1 je smernica, a0 je úsek, n je počet meraní, r je korelačný koeficient. Výsledné hodnoty rýchlostných konštánt k0, polčasu rozkladu spolu s aktivačnými parametrami pre hydrolýzu heptakaíniumchloridu vo vodno-etanolovom roztoku NaOH c = 0,1 mol/l sú zhrnuté v tabuľke 2. V tabuľke 3 sú uvedené výsledky stability v tlmivých roztokoch. V grafe 1 sú uvedené závislosti pre rast teploty v intervale 40–82 °C v grafe 2 je príklad vyhodnotenia neizotermického testu.
Tab. 1. Hodnoty b (K<sup>–1</sup>) pre rast teploty a koeficienty lineárnych závislostí na výpočet hodnôt E<sub>A</sub> (kJ·mol<sup>–1</sup>) a k<sub>0</sub> (h<sup>–1</sup>) hydrolýzy heptakaíniumchloridu za neizotermických podmienok 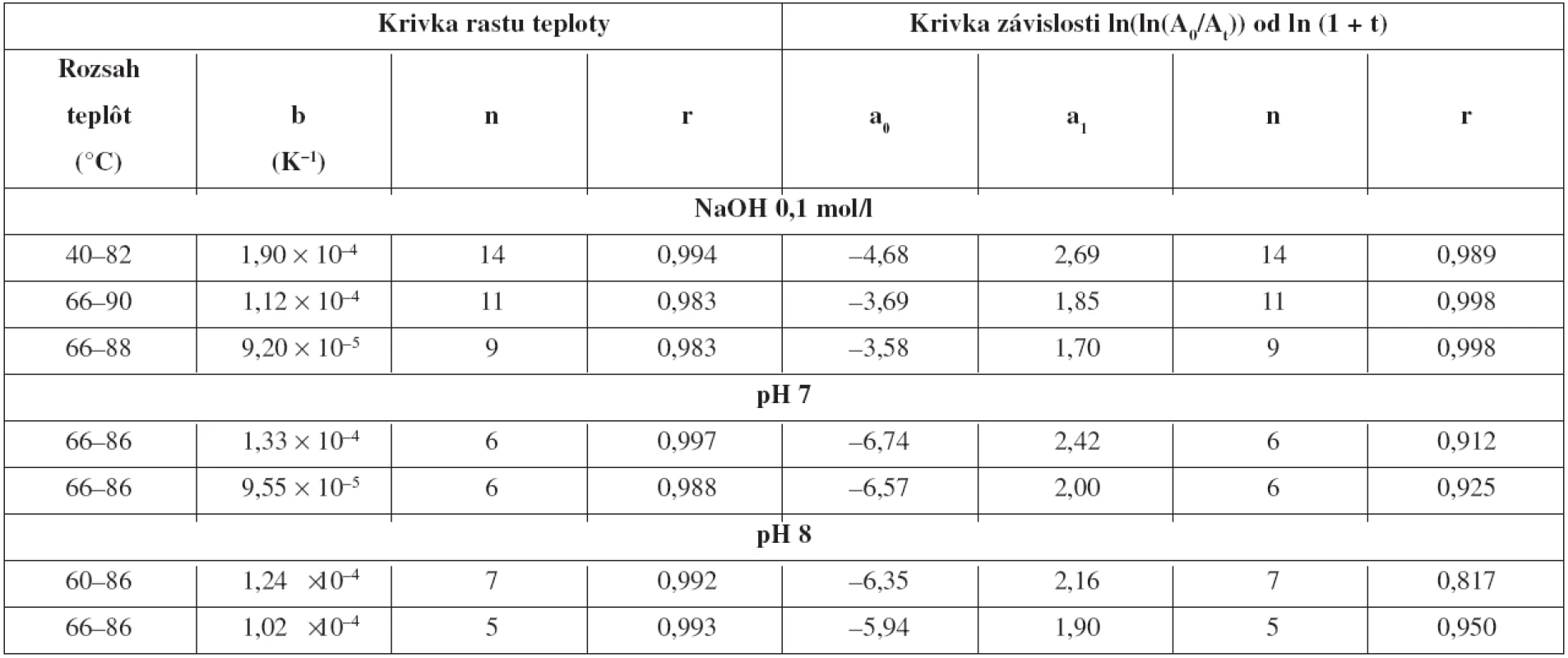
Tab. 2. Prehľad výsledkov štúdia stability heptakaíniumchloridu vo vodno-etanolovom roztoku NaOH c = 0,1 mol/l pri neizotermickom teste 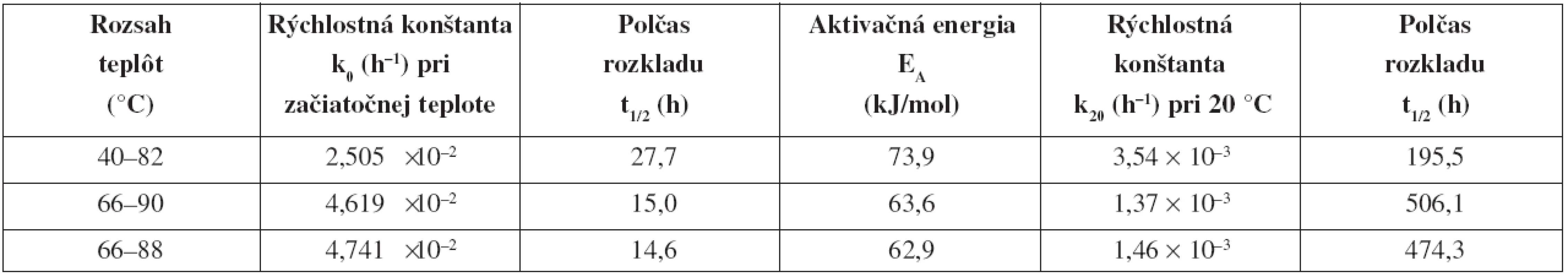
Tab. 3. Prehľad výsledkov štúdia stability heptakaíniumchloridu v tlmivých roztokoch pri neizotermickej hydrolýze 
Graf 1. Rast teploty (K<sup>–1</sup>) v rozsahu 40–82 °C pre heptakaíniumchlorid 
Graf 2. Vyhodnotenie neizotermického testu heptakaíniumchloridu v rozsahu teplôt 40–82 °C v prostredí vodno-etanolového roztoku hydroxidu sodného c = 0,1 mol/l 
Dosiahnuté výsledky štúdia priebehu alkalickej hydrolýzy heptakaíniumchloridu neizotermickým testom v intervale teplôt v rozsahu 40–82 °C sa približne zhodujú s už dosiahnutými výsledkami pri izotermickom teste v práci8), kde výsledná hodnota aktivačnej energie EA = 78,2 kJ/mol a rýchlostná konštanta 1. poriadku pri teplote 40 °C je 1,83·10–2 h–1.
Karbizokaíniumchlorid
Priebeh hydrolýzy karbizokaíniumchloridu za neizotermických podmienok sme vyhodnocovali pomocou spektrofotometrie v ultrafialovej oblasti v prostredí vodno-etanolového roztoku hydroxidu sodného s koncentráciou c = 0,1mol·l–1 a v tlmivých roztokoch s hodnotami pH 7,0 a pH 8,0. Priebeh hydrolýzy sme sledovali v intervale rastu teploty 60–88 °C v prostredí hydroxidu sodného 0,1 mol/l a v intervale 66–86 °C v prostredí tlmivých roztokov. Pre získanie presnejších výsledkov boli uskutočnené dve paralelné merania, v prostredí tlmivých roztokov tri merania. Predchádzajúce výsledky štúdia kinetiky hydrolýzy tejto látky poukázali, že rýchlosť reakcie je nižšia v porovnaní s heptakaínom. V spojovacom reťazci v polohe αα metyl tieni karbamátovú funkčnú skupinu, a tým znižuje možnosť prístupu OH – iónov k nej. Pri nižších teplotách sa hodnoty absorbancíí karbizokaínu menia len nepatrne aj napriek niekoľkohodinovému zahrievaniu, resp. sa vracajú na počiatočnú hodnotu8). Preto sme zvolili vyššiu teplotu na začiatku reakcie. Príklad rastu teploty v rozsahu teplôt 60–88 °C je v grafe 3. V grafe 4 je príklad vyhodnotenia neizotermického testu hydrolýzy karbizokaíniumchloridu v prostredí hydroxidu sodného 0,1 mol/l pri neizotermickej hydrolýze v rozsahu teplôt 60–88 °C pri vlnovej dĺžke 294 nm. V tabuľkách 4 a 5 sú výsledky hydrolýzy karbizokaíniumchloridu za neizotermických podmienok v uvedených prostrediach.
Graf 3. Rast teploty (K<sup>–1</sup>) v rozsahu 60–88 °C pre karbizokaíniumchlorid 
Graf 4. Vyhodnotenie neizotermického testu karbizokaíniumchloridu v rozsahu teplôt 60–88 °C v prostredí vodno-etanolového roztoku hydroxidu sodného c = 0,1 mol/l 
Tab. 4. Hodnoty b (K<sup>–1</sup>) pre rast teploty a koeficienty lineárnych závislostí na výpočet hodnôt E<sub>A</sub> (kJ . mol<sup>–1</sup>) a k<sub>0</sub> (h<sup>–1</sup>) hydrolýzy karbizokaíniumchloridu za neizotermických podmienok 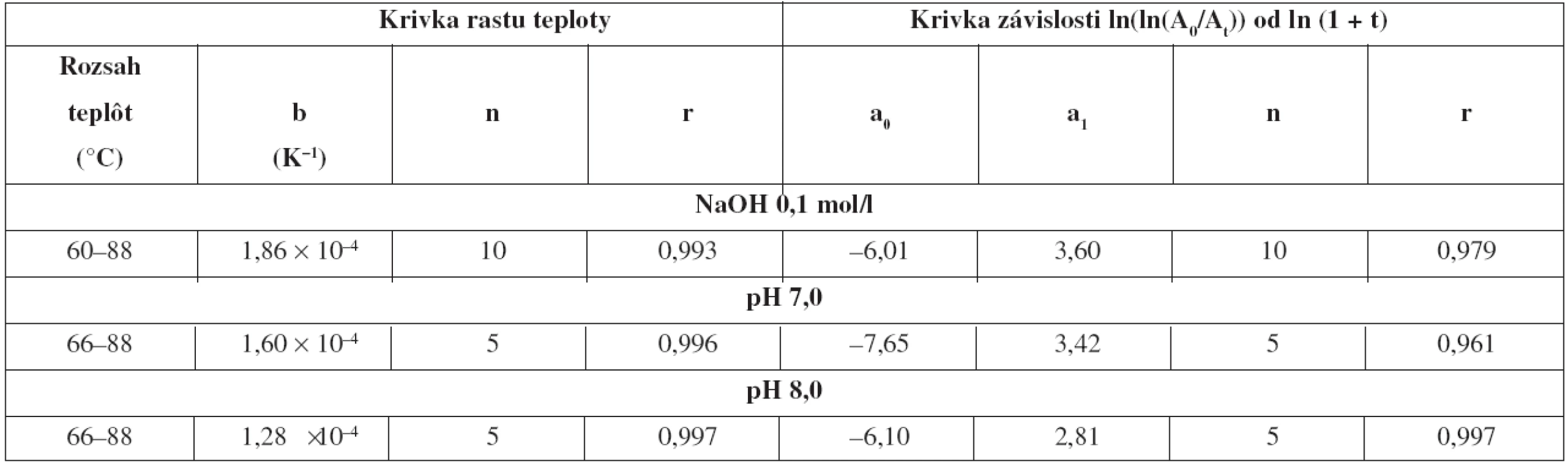
Tab. 5. Prehľad výsledkov štúdia stability karbizokaíniumchloridu v roztoku hydroxidu sodného c = 0,1 mol/l a v tlmivých roztokoch pri neizotermickej hydrolýze 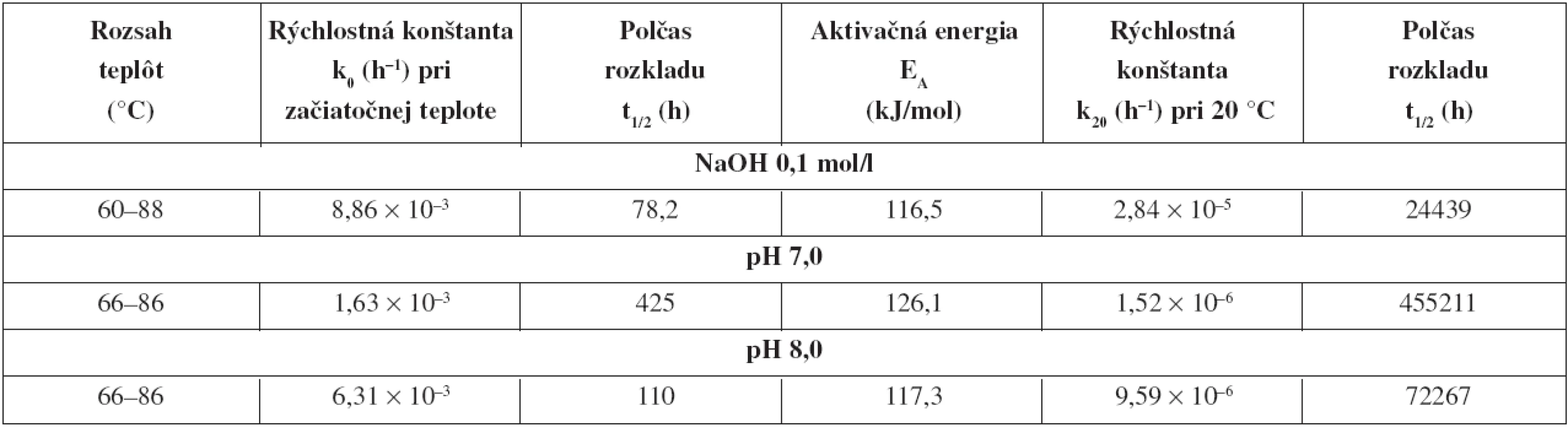
Porovnaním výsledkov štúdia kinetiky hydrolýzy karbizokaíniumchloridu za neizotermických podmienok s výsledkami štúdia dosiahnutými v experimentoch za izotermických podmienok8) môžeme konštatovať, že hodnota aktivačnej energie v práci8) sa zhoduje s výsledkom neizotermického testu. Rovnako hodnoty rýchlostných konštánt v prostredí tlmivého roztoku pH 7,0 a v prostredí hydroxidu sodného 0,1 mol/l sú rádovo blízke.
Metóda štúdia stability liečiv neizotermickým testom má výhodu v tom, že v rámci jedného experimentu sa dajú získať parametre potrebné na výpočet času použiteľnosti liečiva, čím sa ušetrí čas aj energia. Na druhej strane je nevyhnutné si vopred zistiť vhodné podmienky experimentu pre študované liečivo, na čo je potrebné štúdium stability, resp. kinetiky hydrolýzy za izotermických podmienok.
Stret záujmov: žiadny.
Došlo 27. května 2014 / Přijato: 25. června 2014
doc. RNDr. Mária Stankovičová, CSc. (∗) • A. Lašáková • V. Medlenová • Ž. Bezáková • J. Čižmárik
Katedra farmaceutickej chémie, Farmaceutická fakulta Univerzity Komenského
Odbojárov 10, 832 32 Bratislava, SR
e-mail: stankovicm@fpharm.uniba.sk
Zdroje
1. Čižmárik J., Borovanský A., Švec P. Štúdium lokálnych anestetík LII. Piperydinoetylestery kyselín alkoxyfenylkarbámových. Acta Facult. Pharm. Univ. Comenianae 1976; 29, 76–77.
2. Beneš P., Švec P., Kozlovský J., Borovanský A. Bazické estery kyselin o-alkoxykarbanilových s lokálně anestetickým a antiarytmickým účinkem. Čes. slov. Farm. 1978; 27, 167–172.
3. Švec P., Čižmárik J., Béderová E., Borovanský A. Štúdium lokálnych anestetík LIII. Farmakologické vlastnosti heptakaínu. Acta Facult. Pharm. Univ. Comenianae 1976; 29, 96–99.
4. Kozlovský J., Čižmárik J., Pešák M., Inczinger F., Borovanský A. Antiarrhythmic activity of heptacaine and some of its derivatives. Arzneim.-Forsch 1982; 32, 1032–1036.
5. Blešová M., Bachratá M., Bezáková Ž., Beneš L., Borovanský A. Analytické hodnocení karbizokaíniumchloridu. Čes. slov. Farm. 1985; 34, 163–167.
6. Bezáková Ž., Čižmárik J., Blešová M., Bachratá M., Borovanský A. Štúdium lokálnych anestetík. LXXXII. Stabilita heptakaíniumchloridu. Farm. Obzor 1986; 55, 19–24.
7. Bezáková Ž., Bachratá M., Blešová M., Borovanský A. Stabilita karbizokaíniumchloridu a pentakaíniumchloridu. Farm. Obzor 1986; 55, 195–203.
8. Stankovičová M., Bachratá M., Bezáková Ž., Blešová M., Čižmárik J., Borovanský A. Štúdium kinetiky alkalickej hydrolýzy karbizokaíniumchloridu, pentakaíniumchloridu a heptakaíniumchloridu. Čes. slov. Farm. 1987; 36, 9–15.
9. Stankovičová M., Čižmárik J., Bachratá M. Kinetics of alkaline hydrolysis of heptacaine chloride basic analogues. Chem. Papers 1990; 44, 171–176.
10. Stankovičová M., Bezáková Ž., Lukášová-Masná P., Lukáš L. Kinetics of alkaline hydrolysis of potential local anaesthetics – The basic esters of phenylcarbamic acids. Acta Facult. Pharm. Univ. Comenianae. 2009; 56, 128–135.
11. Čižmárik J., Lehotay J., Bednáriková A. Štúdium lokálnych anestetík CLVII. Chromatografické vlastnosti pentakaínu, karbizokaínu, heptakaínu a jeho 3 - a 4-polohových izomérov v RP systéme HPLC. Čes. slov. Farm. 2001; 50, 233–237.
12. Lehotay J., Čižmárik J., Hromuľáková K. HPLC of heptacaine position isomers. Pharmazie 1996; 51, 731–733.
13. Lehotay J., Čižmárik J., Branšteterová E. Study of local anesthetics. Part 128. HPLC study of the degradation of heptacaine and carbisocaine in urine, human and rabbit serums. Acta Pharmaceutica Hungarica, 1995; 65, 95–96.
14. Gallová J., Andriamainty F., Uhríková D., Balgavý P. Interaction of local anesthetic heptacaine homologs with phosphatidylcholine bilayers: spin label ESR study. Biochim. Biophys. Acta – Biomembranes. 1997; 1325, 189–196.
15. Andriamainty F., Čižmárik J., Malík I., Horváth S. Štúdium lokálnych anestetík: Časť 183. Micelizácia a termodynamické parametre heptakaíniumchloridu v prostredí KBr. Čes. slov. Farm. 2008; 57, 119–125.
16. Gališinová J., Čižmárik J., Andriamainty F., Malík I. Štúdium lokálnych anestetík: Časť 193. Štúdium vplyvu teploty a prídavku soli na micelizáciu heptakaínium-perchlorátu vo vodnom prostredí. Čes. slov. Farm. 2010; 59, 272–276.
17. Čižmárik J., Andriamainty F., Malík I., Sedlárová E. Štúdium lokálnych anestetík. Časť 176. Štúdium micelizácie a termodynamických parametrov heptakaíniumchloridu vo vodnom a alkoholickom prostredí. Farm. Obzor 2007; 76, 133–138.
18. Čižmárik J., Vitková Z., Herdová P. Štúdium lokálnych anestetík: Časť 196. Formulation of the local anaesthetic heptacaine into hydrogel on the basis of chitosan. Čes. slov. Farm. 2012; 61, 60–61.
19. Vitková Z., Gardavská K., Čižmárik J., Rak J. Influence of auxiliary substances on the release of heptacaine from the drug form. Acta Pharmaceutica Hungarica. 1996; 66, 191–195.
20. Čižmárik J., Lehotay J., Hromuľáková K., Pokorná M., Lacuška M. HPLC separation of enantiomers of carbisocaine. Pharmazie 1997; 52, 402.
21. Kersten D., Göber B. Chemische Stabilitätsprüfung von Arzneimitteln im Lang - und Kurzzeittest-Methodenvergleich. Pharmazie 1984; 39, 218–219.
22. Rogers A. R. An accelerated storage test with programmed temperature rise. J. Pharm. Pharmacol. 1963; 15, 101T–105T.
23. Beňo P., Truplová E., Ostrovská V., Stankovičová M. Stabilita liečiv a liekov. 1. vyd. Bratislava: Veda 2003.
Štítky
Farmacie Farmakologie
Článek vyšel v časopiseČeská a slovenská farmacie
Nejčtenější tento týden
2014 Číslo 4- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Ukažte mi, jak kašlete, a já vám řeknu, co vám je
- Přerušovaný půst může mít významná zdravotní rizika
-
Všechny články tohoto čísla
- Změny v redakci časopisu Česká a slovenská farmacie
- Metabolický syndrom – dysregulace endokrinních funkcí tukové tkáně
-
Štúdium lokálnych anestetík: Časť 205*
Štúdium stability heptakaíniumchloridu a karbizokaíniumchloridu zrýchleným neizotermickým testom - In vivo testovanie nových ultrakrátko pôsobiacich β-blokátorov s efektom na systolický krvný tlak a tepovú frekvenciu
- Výhrada svědomí v profesi farmaceuta
- Racionalizace v československém lékárenství ve 20. století – farmaceutická sekce Komise pro racionalisaci a normalisaci v lékařství, zvěrolékařství a lékárnictví – 2. část*
- XXXVI. pracovní dny Radiofarmaceutické sekce České společnosti nukleární medicíny čls jep
-
Intoxikácie hubami, rastlinami a živočíšnymi toxínmi.
Extrakčné metódy vo farmaceutickej technológii.
- Česká a slovenská farmacie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Výhrada svědomí v profesi farmaceuta
- Metabolický syndrom – dysregulace endokrinních funkcí tukové tkáně
- Racionalizace v československém lékárenství ve 20. století – farmaceutická sekce Komise pro racionalisaci a normalisaci v lékařství, zvěrolékařství a lékárnictví – 2. část*
- XXXVI. pracovní dny Radiofarmaceutické sekce České společnosti nukleární medicíny čls jep
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



