-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Prof. Milan Brázdil: Stane se cenobamát přelomovým lékem pro farmakorezistentní epilepsii?
2. 12. 2022
V rámci XXV. postgraduálního kurzu epileptologie, „Dnů Jiřího Dolanského“, který se uskutečnil v říjnu 2022 v Praze, proběhlo rovněž sympozium společnosti Angelini Pharma nazvané „Na cestě k životu bez záchvatů“. V jednom z vystoupení se přednosta I. neurologické kliniky LF MU a FN u sv. Anny v Brně prof. MUDr. Milan Brázdil, Ph.D., zaměřil na představení nového protizáchvatového léku cenobamátu, jehož vstup na český trh se očekává v lednu 2023.
Lék, který mění pravidla hry?
Profesor Brázdil svou přednášku nazval „Cenobamát, příběh začíná?“ a hned v úvodu vyslovil naději, že tento příběh bude mít dobrý konec. Díky svému duálnímu mechanismu účinku toto léčivo může představovat kýžený průlom v přídatné terapii fokálních záchvatů. V USA byl cenobamát schválen Úřadem pro kontrolu léčiv a potravin (FDA) v indikaci fokálních epileptických záchvatů již v listopadu 2019. „V článcích, které tehdy vycházely v odborném tisku, se o něm psalo jako o léku, který ‚mění pravidla hry‘,“ připomněl autor sdělení.
Přestože se na trhu vyskytuje velké množství protizáchvatových léků a další přibývají, má podle profesora Brázdila vývoj nových antiepileptik stále svůj smysl. Žádný z dosavadních léků zatím nevedl k úplné bezzáchvatovosti u všech pacientů, nadále zůstává asi 30 % farmakorezistentních jedinců.
InzerceCenobamát je indikovaný k přídatné léčbě fokálních záchvatů se sekundární generalizací nebo bez ní u dospělých pacientů s epilepsií, kteří zůstali farmakorezistentní navzdory předchozí léčbě nejméně 2 antiepileptiky. Včasný zásah přitom zásadně zvyšuje šanci na úspěšnou léčbu.
Co ukázal klinický výzkum i studie z reálné praxe?
Cenobamát podobně jako jiné protizáchvatové léky prošel rozsáhlým klinickým testováním, kterého se zúčastnilo celkem přes 2500 pacientů. Dohromady proběhlo 22 studií fáze I, dále 1 studie k ověření konceptu a 2 placebem kontrolované studie účinnosti a bezpečnosti (C013 a C017):
- Multicentrická randomizovaná dvojitě zaslepená studie fáze II C013 hodnotila účinnost a tolerabilitu cenobamátu (v cílové dávce 200 mg) proti placebu u pacientů s fokálními záchvaty, kteří i přes léčbu 1−3 antiepileptiky zůstávali farmakorezistentní. Ve skupině s dávkou 200 mg cenobamátu bylo během 6týdenní udržovací fáze 28,3 % pacientů zcela bez záchvatu, ve skupině s placebem pouze 8,8 % [1].
- Podobně koncipovaná studie fáze II C017 se lišila pouze spektrem testovaných dávek (100, 200 a 400 mg denně). Ve větvi léčené dávkou 400 mg bylo 21 % pacientů zcela bez záchvatů a u 28 % došlo ke snížení počtu záchvatů o 90 % [2].
Obr. Klíčové výsledky studie C017
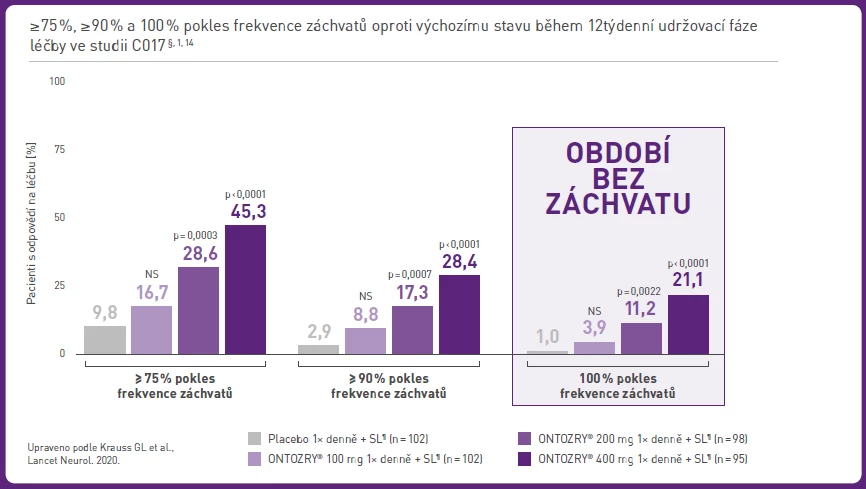
Profesor Brázdil upozornil, že se jedná o atypické výsledky: „Srovnání jednotlivých randomizovaných klinických studií, které byly prováděny v poslední době s různými protizáchvatovými léky, ukazuje, že u většiny z nich je dosaženo stavu bez záchvatů, ale jde pouze o nízké jednociferné hodnoty.“
Dosud probíhající otevřená studie bezpečnosti (C021), které se zúčastnilo téměř 1400 pacientů, potvrdila dobrou snášenlivost léku [3]. Po roce zůstalo na cenobamátu 80 % pacientů, po 2 letech 70 %, po 5 letech 60 %. Z výsledků tedy vyplývá, že k dramatickému snížení počtu pacientů v průběhu dlouhodobé terapie nedochází [4].
Klinická data z reálné praxe následně potvrdila dobré výsledky předchozích studií:
- Eliott et al. hodnotili účinnost cenobamátu u 45 dospělých a dospívajících pacientů: 16 % z nich dosáhlo při ročním sledování plné kompenzace onemocnění a 60 % patřilo k respondérům (pokles frekvence záchvatů ≥ 50 %) [5].
- Oklahomská studie, která testovala cenobamát u 28 dospělých pacientů s fokálními epileptickými záchvaty v klinické praxi, ukázala, že u 48 % došlo k vymizení záchvatů po dobu 6 měsíců [6].
Hlavní body k zapamatování
Závěrem autor sdělení shrnul jako klíčové následující body:
- Existuje „slušná šance“, že cenobamát naplní realistická očekávání – může být novým přelomovým protizáchvatovým lékem s vysokou účinností i u pacientů s farmakorezistentní epilepsií a mohl by jim poskytnout naději na dosažení bezzáchvatovosti.
- Při správném používání by neměl být problém s tolerabilitou cenobamátu. Důležité v praxi je, aby nasazování tohoto léku nebylo příliš rychlé a aby byl dodržován postup doporučený v SPC, tedy postupnou titrací po 2 týdnech navýšit dávku z 12,5 mg na 25 mg a dále každé 2 týdny na 50 mg, 100 mg, 150 mg až do cílové dávky 200 mg denně, s možností v případě potřeby ji stejným způsobem (o 50 mg každé 2 týdny) dále navyšovat až do 400 mg denně.
- Současně však tento lék může vyžadovat od ošetřujícího lékaře znalost možných farmakokinetických interakcí a jejich respektování, což souvisí s jeho extenzivní metabolizací v játrech.
„V této fázi předpokládám, že cenobamát bude podáván pacientům, u nichž selhala předchozí antiepileptická léčba. Nenechme se proto znervóznit, pokud nemocných bez záchvatů nebude hned 60 nebo 70 procent. Teprve když se začne podávat v časných fázích, objeví se jeho maximální potenciál,“ uzavřel své vystoupení profesor Brázdil. Celou jeho přednášku můžete ze záznamu zhlédnout zde.
(lkt)
Zdroje:
1. Chung S. S., French J. A., Kowalski J. et al. Randomized phase 2 study of adjunctive cenobamate in patients with uncontrolled focal seizures. Neurology 2020; 94 (22): e2311–e2322, doi: 10.1212/WNL.0000000000009530.
2. Krauss G. L., Klein P., Brandt C. et al. Safety and efficacy of adjunctive cenobamate (YKP3089) in patients with uncontrolled focal seizures: a multicentre, double-blind, randomised, placebo-controlled, dose-response trial. Lancet Neurol 2020; 19 (1): 38–48, doi: 10.1016/S1474-4422(19)30399-0.
3. Sperling M. R., Klein P., Aboumatar S. et al. Cenobamate (YKP3089) as adjunctive treatment for uncontrolled focal seizures in a large, phase 3, multicenter, open-label safety study. Epilepsia 2020; 61 (6): 1099–1108, doi: 10.1111/epi.16525.
4. French J. A., Chung S. S., Krauss G. L. et al. Long-term safety of adjunctive cenobamate in patients with uncontrolled focal seizures: open-label extension of a randomized clinical study. Epilepsia 2021; 62 (9): 2142–2150, doi: 10.1111/epi.17007.
5. Elliott T., Ridley-Pryor T., Gienapp A. J., Wheless J. W. Initial real-world experience with cenobamate in adolescents and adults: a single center experience. Pediatr Neurol 2022; 129 : 19–23, doi: 10.1016/j.pediatrneurol.2022.01.001.
6. Connor G. S., Williamson A. Effectiveness and safety of adjunctive cenobamate for focal seizures in adults with developmental disability treated in clinical practice. Epilepsy Behav Rep 2022; 18 : 100533, doi: 10.1016/j.ebr.2022.100533.
7. Brázdil M. Cenobamát, příběh začíná? XXV. postgraduální kurz epileptologie, „Dny Jiřího Dolanského“, Praha, 7. 10. 2022. Dostupné na: https://www.kongres.tv/epilepsie2v/na-cest%C4%9B-k-%C5%BEivotu-bez-z%C3%A1chvat%C5%AF
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Štítky
Neurologie
Nejnovější kurzy
Autoři: MUDr. Jana Zárubová, MUDr. Jana Amlerová, Ph.D., MUDr. Adam Kalina
Autoři: doc. MUDr. Martin Pail, Ph.D.
Přejít do kurzů
Nejčtenější tento týden Celý článekPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




