-
Medical journals
- Career
NOVÉ TRENDY V ROZTROUŠENÉ SKLERÓZE
Authors: M. Kövári
Authors‘ workplace: Rehabilitační klinika Malvazinky, Praha prim. MUDr. H. Liščáková
Published in: Rehabil. fyz. Lék., 16, 2009, No. 1, pp. 6-10.
Category: Original Papers
Overview
Autorka v přehledném článku shrnuje současné poznatky o epidemiologii, diagnostice a terapii roztroušené sklerózy (RS) v České republice a v závěru upozorňuje i na důležitost komplexní rehabilitace, která je však pro pacienty v ČR zatím pouze omezeně dostupná.
Klíčová slova:
roztroušená mozkomíšní skleróza, ataka, McDonaldovy kritéria, léky DMD, komplexní rehabilitaceÚVOD
Roztroušená skleróza (RS) je nejčastější neurologické autoimunitní onemocnění mladých dospělých. Začíná obvykle mezi 20. - 40. rokem věku a jen zřídka je diagnostikována před 10. a po 60. roce věku (6). V současné době máme v ČR zhruba 13 tisíc nemocných s RS a jejich počet stále stoupá. Incidence onemocnění se odhaduje na 8-10/100 tisíc pacientů.
První příznaky se často objevují v období hormonálních změn (po porodu a při menarché). Onemocnění je u žen proto častější než u mužů, a to zhruba v poměru zhruba 2-3 : 1.
Epidemiologie RS
Česká republika patří mezi země s vyšším výskytem RS - prevalence činí zhruba 30 nemocných na 100 000 obyvatel. Svou roli hraje zřejmě homogenita obyvatelstva – evropská bílá populace má vyšší výskyt RS než orientálci či Afričané.
Situace je dále determinována geografickým gradientem. Četnost onemocnění je nejvyšší v severním mírném pásmu. Obviňuje se určité spektrum virů v našem klimatickém pásmu a také nižší syntéza vitamínu D díky méně intenzivnímu slunečnímu svitu. Moderní vědecké výzkumy totiž potvrzují jeho výrazné protizánětlivé účinky. Velký podíl nepochybně mají i genetické faktory. Dědí se určitá vyšší vnímavost k autoimunitním chorobám. Poslední studie také hovoří o tom, že RS se dvakrát častěji vyskytuje u kuřáků než u nekuřáků.
Etiopatogeneze RS
Každý z nás má i v dospělosti určité množství autoagresivních T-lymfocytů vnímavých ke složkám myelinu, které jsou v klidové formě v thymu či hlubokých krčních uzlinách. Protože se myelin během našeho života průběžně obnovuje, tak se i jeho rozpadové produkty dostávají do těchto hlubokých krčních uzlin. Může se pak stát, že u některých geneticky disponovaných jedinců dojde náhle k reaktivaci těchto lymfocytů a poté k vyplavení do oběhu a překročení hematoencefalické bariéry do tkáně CNS.
Tam se spustí zánětlivá kaskáda, a to za účasti cytokinů, interleukinů, interferonu gama a B-lymfocytů přeměněných v plazmatické buňky (4). Výsledkem je vznik zánětlivých ložisek, tzv. plaka v bílé míšní hmotě, které vidíme na MRI. Klinicky mohou být některá ložiska pro pacienta asymptomatická, některá však způsobí neurologický deficit různé závažnosti (záleží na lokalizaci plaky). Protože myelin je však naštěstí schopen částečné reparace, dochází u pacientů hlavně zpočátku k úplné či částečné úzdravě z ataky. V posledních letech bylo zjištěno, že již při prvních atakách může dojít nejen k poškození myelinu, ale i k zpřetrhání většího množství axonů (7).
PŘÍZNAKY ROZTROUŠENÉ SKLERÓZY
Klinický projev ložisek RS je závislý na jejich lokalizaci v bílé míšní hmotě. U 85 % pacientů se onemocnění projeví tzv. atakovitou formou onemocnění. Ataka je definována jako vznik nových příznaků nebo výrazné zhoršení již existujících bez souvislosti s horečkou trvající více než 24 hodin.
Nejčastější příznaky u RS
Pacienti často přicházejí s paresteziemi či dysesteziemi různých částí těla, s motorickým deficitem (centrální monoparézy, hemiparézy či nejčastěji paraparézy dolních končetin). Typická je retrobulbární optická neuritida se zamlženým vizem, bolestivými pohyby bulbu a normálním nálezem na očním pozadí. Časté jsou i různé formy postižení mozkových nervů: okohybné poruchy, diplopie, nystagmus, obrna lícního nervu, neuralgie trigeminu. Velmi stresující jsou pro pacienta poruchy rovnováhy, vzniklé díky poruchám mozečku (doprovázené intenčním třesem, porušenou koordinací pohybu, pocitem nejistoty v prostoru), poruchou zadních míšních provazců s ataxií spinálního původu a závratěmi kmenového původu. Při těchto formách závrati při neurologickém vyšetření pak nacházíme dysharmonické tonické úchylky končetin a nystagmus. Pacienti si dále stěžují i na sfinkterové obtíže – imperativní mikci, časté noční močení, někdy naopak na retenci moči a obstipaci. Vše dále mohou doprovázet poruchy koncentrace, kognice a výrazná únava díky difuznímu zánětu CNS.
Jak stanovit diagnózu RS
Diagnóza RS je založená hlavně na klinickém obrazu a následně podpořená vyšetřeními MRI mozku a krční míchy (obr. 1) a vyšetřením mozkomíšního moku. Základem stanovení diagnózy před érou MRI bylo, že pacient prodělal alespoň dvě ataky vysvětlitelné ze dvou různých ložisek CNS.V 90. létech minulého století vznikl požadavek rychlejšího stanovení diagnózy a časného nasazení účinné léčby. V roce 2001 byla publikována tzv. McDonaldova diagnostická kritéria, která umožnila stanovit diagnózu u pacientů již záhy po první atace. Tato kritéria byla částečně revidována v roce 2005 (tab. 1).
Image 1. Typický MRI nález u RS. (Zapůjčeno z oddělení magnetické rezonance Nemocnice na Homolce.) 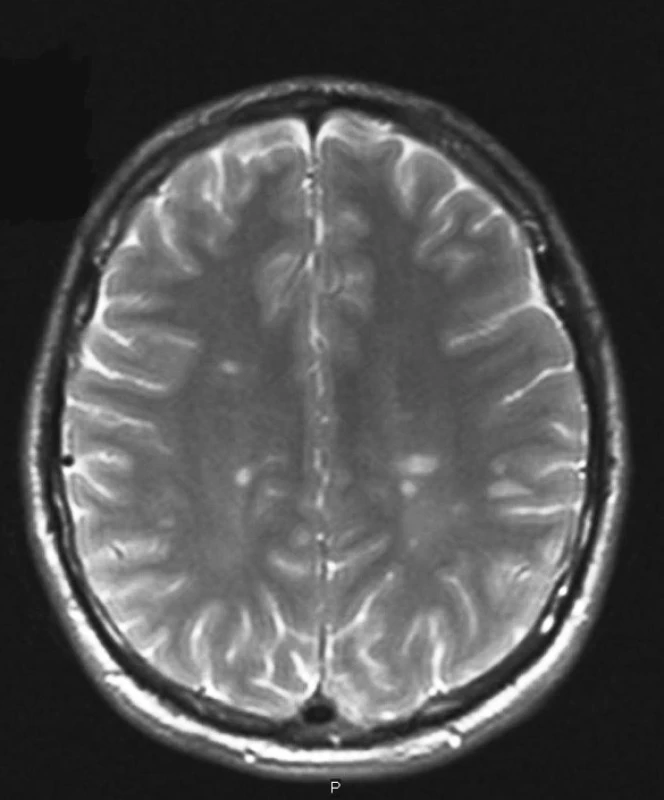
Table 1. Revidovaná McDonaldova diagnostická kritéria RS z roku 2005. 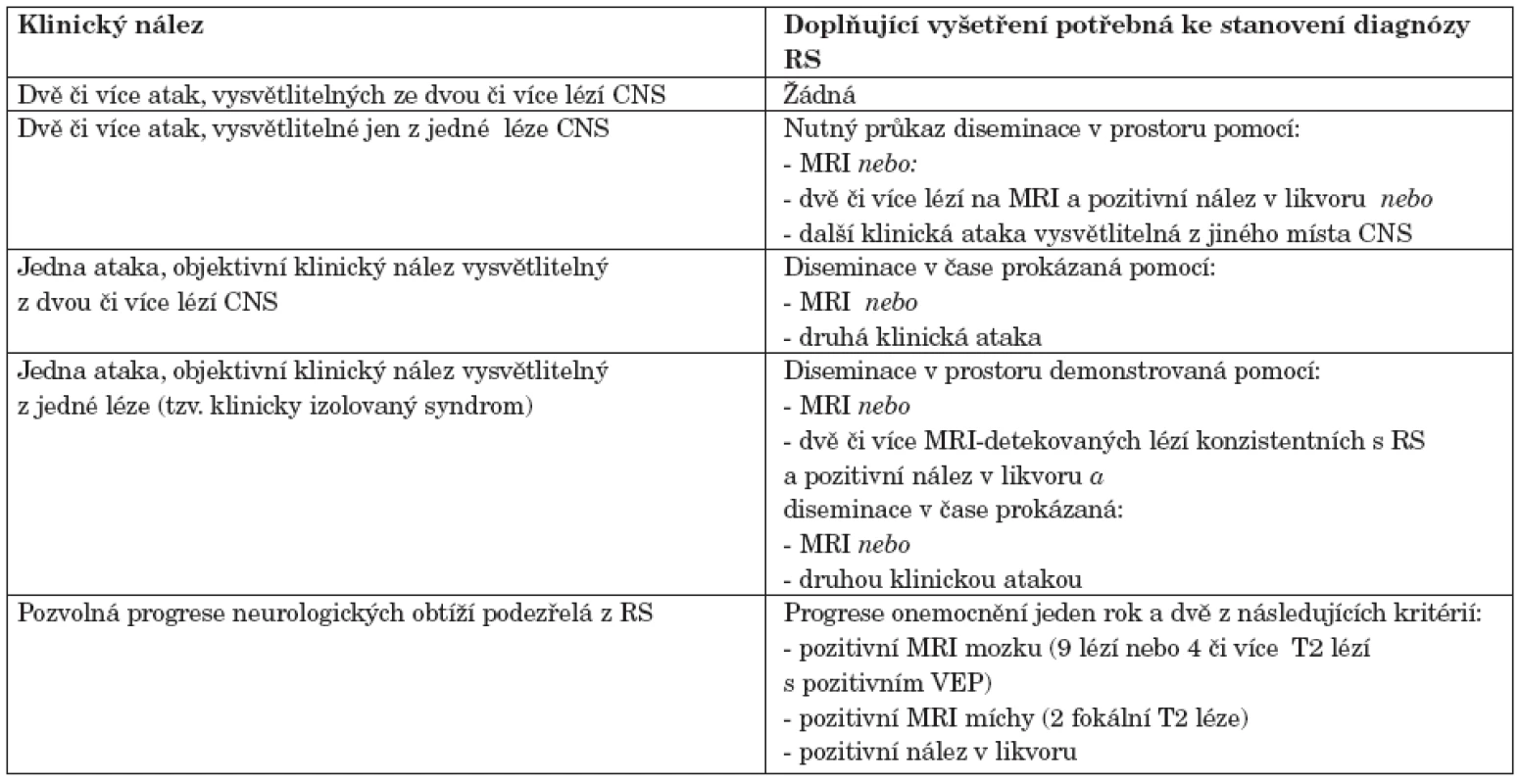
Vysvětlivky: VEP – vizuální evokované potenciály. MRI průkaz v prostoru: nutné splnění 3 z následujících kritérií: - nejméně jedna gadolinium-enhancující léze nebo 9 T2 hyperintenzních lézí, pokud není léze enhancující - nejméně jedna léze infratentoriální - alespoň jedna juxtakortikální léze - alespoň 3 léze periventrikulární. MRI průkaz v čase: - průkaz nové gadolinium enhancující léze nejméně 3 měsíce od první ataky, nebo - detekce nové T2 léze při kontrolním MRI mozku nejméně 1 měsíc od ataky. Pozitivní nález v likvoru: - průkaz oligoklonálních protilátek metodou izoelektrické fokusace, které nejsou přítomny v séru, nebo zvýšený IgG index v likvoru. Podle nových diagnostických kritérií stačí u pacienta s jednou klinickou atakou k průkazu diagnózy potvrdit vznik další nové léze na MRI, a to nejméně s odstupem jednoho měsíce po atace první. Diagnóza je dále podpořena vyšetřením mozkomíšního moku průkazem typických oligoklonálních pásů v alkalické oblasti při izoelektrické fokusaci moku. Tyto pásy prokazují intrathékální syntézu IgG v mozkomíšním moku. Zároveň je vyloučeno případné infekční agens.
FORMY ROZTROUŠENÉ SKLERÓZY
V současné době rozlišujeme čtyři základní formy RS:
- Forma relaps-remitentní (RR forma – 85 % pacientů) – typické je střídání atak s remisemi.V mezidobí je pacient bez neurologického deficitu či pouze s minimálním reziduálním nálezem. Typická je u 85 % pacientů.
- Forma relabující-progredientní (RP forma – 3 %pacientů). Zde nová ataka nasedá na přetrvávající neurologický deficit.
- Forma sekundárně progresivní (SP forma) – do této formy přejde zhruba 50 % pacientů s RR formou po 10-15 letech onemocnění. Typické je vymizení atak a naopak pozvolný nárůst neurologického deficitu.
- Forma primárně progresivní (PP forma – 10 % pacientů) – zde dochází k pozvolnému zhoršování stavu bez jasných atak již od počátku onemocnění.
Diferenciální diagnóza RS
Diferenciálně diagnosticky je nutno vyloučit lymskou boreliózu, cervikální myelopatii, nádorová onemocnění, cévní malformace CNS, Wilsonovu chorobu, jiná autoimunitní onemocnění CNS (vaskulitidy), akutní diseminovanou encefalomyelitidu (ADEM), vzácné formy leukodystrofií a spinocerebellární degenerace.
FUNKČNÍ ZHODNOCENÍ STAVU PACIENTA
Pro rychlou orientaci v neurologickém nálezu pacienta standardně používáme tzv. Kurtzkeho škálu – EDSS (expanded disability status scale), kde pacienta škálujeme od 0-10 stupňů (9). Dostupné jsou i jiné testy škálování – např. Multiple Sclerosis Functional Composite scale (1) a Multiplex Sclerosis Impact Scale (8). V detailech odkazuji na dostupnou odbornou literaturu.
Terapeutické možnosti v léčbě RS
V posledních zhruba patnácti letech prodělaly terapeutické postupy obrovský vývoj. Prokázalo se, že je důležité zahájit léčbu co nejdříve. V prvních pěti letech trvání choroby totiž dochází k největší axonální ztrátě, a tím i k nárůstu atrofie mozku a míchy. Díky tomu dochází k vyčerpání funkčních rezerv CNS. Přitom pacient v tomto období může trpět jen minimálním neurologickým deficitem.
Zlomovým momentem v terapii bylo uvedení prvního interferonu beta do praxe v roce 1993 a pravidelné sledováním pacientů pomocí MRI. Před rokem 1950 byli pacienti s RS v podstatě bez terapie. Poté se začalo aplikovat ACTH, následovaly pak steroidy v nízké dávce a od roku 1975 azathioprin. Nejdříve se léčily pouze ataky a až v posledních zhruba 20 letech se postupně začala podávat i chronická léčba.
Léčba akutní ataky
Zlatý standardem v léčbě ataky je i.v. podání methylprednisolonu v dávce 3-5 gramů rozděleně v několika dnech. Protizánětlivý efekt této jednorázové kúry trvá zhruba devět týdnů. Po odeznění efektu však dochází často k novému vzplanutí onemocnění.
Léčba dlouhodobá
Touto léčbou se snažíme snížit aktivitu nemoci, tím snížit progresi onemocnění a zabránit tak rychlé invalidizaci pacienta. V současné době mezi léky první volby patří interferony beta a glatiramer acetát. Některé z těchto léků se v rámci EU nasazují již po první atace onemocnění. V České republice, bohužel, tyto léky po prvé atace nasazovány nejsou. Jsou zde stanovena indikační kritéria léčby pro pacienty s vysokou aktivitou choroby: pacient musí prodělat 2 ataky v posledním roce nebo 3 ataky za 2 roky, aby byla léčba pojišťovnou uhrazena, zároveň jeho EDSS nesmí přesáhnout hodnotu 4.5.
Interferony beta se objevily v léčbě poprvé v roce 1993 a v současné době máme k dispozici tři druhy interferonů: interferon beta 1b - preparáty Betaferon a Rebif 22 a 44 a interferon beta 1a – Avonex. Interferony zasahují na mnoha úrovních imunitních reakcí – obecně lze říci, že jejich účinek je protizánětlivý - antivirový, antiproliferativní a imunomodulační.
V roce 2001 se v léčbě začíná používat glatiramer acetát (GA) - preparát Copaxone. Je to první antigen - specifická terapie RS. Jedná se o kopolymer čtyř aminokyselin (alanin, glycin, lysin, tyrosin), které se nejčastěji opakují v myelinovém bazickém proteinu – důležité součásti myelinu. GA indukuje v CNS záměnu autoagresivních Th1 lymfocytů za tzv. Th2 lymfocyty, které jsou naopak protizánětlivé. Díky tomuto specifickému zásahu GA nemá celkové imunosupresivní účinky na imunitní systém (5). Navíc tyto specifické TH2 lymfocyty jsou schopny produkce tzv. BDNF faktoru (brain derived neurotrofic factor), který nejspíše slouží k ochraně axonů v situaci imunitního útoku (7).
Jak interferony beta tak glatiramer acetát zhruba o 1/3 snižují tvorbu nových ložisek na MRI, snižují počet atak a jejich tíži. Ukazuje se též, že snižují nárůst atrofie mozku a oddalují nástup sekundární progrese onemocnění.
Zcela nově je schválena k léčbě monoklonální protilátka proti alfa-4-integrinu – preparát natalizumab ( Tysabri). Jedná se o první tzv. biologickou léčbu RS. Natalizumab je protilátka proti adhezivní molekule autoagresivního T-lymfocytu. Obsazením této adhezivní molekuly se zabrání jeho průniku přes hematoencefalickou bariéru. Výsledky léčby jsou zatím nejlepší ze všech dostupných preparátů – po dvou letech užívání se snižuje počet nových lézí na MRI o 68 %. Kvůli možným nežádoucím účinkům (určité riziko vzniku progresivní multifokální leukoencefalopatie) a vysoké ceně preparátu je tato léčba používána jako lék 2. volby pro pacienty s vysokou aktivitou choroby a po dodržení určitých bezpečnostních kritérií (2). Preparát se podává ve formě infuze jednou měsíčně.
Mezi léky druhé volby patří dále různé druhy cytostatik a imunoglobuliny(IVIG). Cyto-statika můžeme podávat samostatně nebo kombinovat jak s kortikoidy, s interferony či glatiramer acetátem. V léčbě RS používáme tato cytostatika: cyklofosfamid a mitoxantron, mykofenolát mofetil, cyclosporin A.
Pacientkám během prvních šesti měsíců po porodu podáváme 1x měsíčně intravenózní imuno-globuliny, které snižují riziko vzniku ataky a její tíži v poporodním období. IVIG se také podávají u pacientů, kteří nemohou užívat interferony či glatiramer acetát.
V sekundárně progredientní fázi hlavně zpočátku podáváme pravidelné pulzy se solumedro - lem a cyklofosfamidem, event. mitoxantromem či IVIG. V průběhu této fáze však začíná převažovat degenerace před zánětem a imunosupresivní léčba nemívá velký efekt. S narůstajícím neurologickým deficitem pak stále více narůstá význam rehabilitace.
U pacientů, kteří neprofitují z žádné dostupné terapie a dochází k rychlému zhoršování jejich zdravotního stavu, někdy zvažujeme i autologní transplantaci kostní dřeně. Ta se navrhuje a provádí pouze v superspecializovaných RS centrech ve spolupráci s hematology.
Celosvětově probíhají četné studie i s novými preparáty – parenterálními i perorálními - v současné době např. s fumarátem, laquinomidem, cladribinem, FTY 720 a monoklonálními protilátkami alemtuzumabem a rituximabem (3).
Samostatnou kapitolou je dále léčba symptomatická – myorelaxancia, antidepresiva, analgetika či koanalgetika, léky ovlivňující sfinkterové obtíže, prevence osteoporózy, event. léky ovlivňující únavu pacienta - odkazuji na podrobnější neurologickou literaturu.
REHABILITACE U PACIENTŮ S RS
Soustavná rehabilitace pacientů v České republice byla a je stále velkým problémem. Chybí zde totiž síť specializovaných pracovišť zabývajících se touto problematikou. Dále se postrádá týmová mezioborová spolupráce, která by vedla k péči nejen o fyzický stav pacienta, ale i o jeho psychiku a pomáhala mu udržet jeho práceschopnost. Rehabilitační léčba je jiná v období ataky a jiná v období remise. V atace omezujeme pohybové aktivity a snažíme se redukovat četnost komplikací souvisejících s imobilitou. Provádíme dechovou gymnastiku, cévní cvičení, protahování spastických končetin a podobně.
Pacienta v remisi a s minimálním neurologickým deficitem se snažíme udržet v co nejlepší fyzické a psychické kondici. Součástí rehabilitace by proto měla být i pravidelná aerobní zátěž. Doporučuje se trénink o intenzitě, který odpovídá individuálně naměřené hodnotě 60 % max. spotřeby kyslíku. Tato intenzita zátěže je určena na základě spiroergometrického vyšetření. Doporučujeme jízdu na rotopedu, na veslařském trenažéru, rychlejší chůzi, plavání, jízdu na kole nebo běh. Frekvenci těchto aktivit doporučujeme alespoň 3x týdně 20-30 minut. Zdůrazňuji, že mírná únava není důvodem k omezení pohybových aktivit, a naopak lze ji vhodným pohybovým programem snížit (10).
U pacientů s již vyvinutým neurologickým deficitem přicházejí na řadu speciální rehabilitační postupy. Jde především o cvičení na neurofyziologickém podkladě – Vojtovu reflexní terapii, proprioceptivní neuromuskulární facilitaci, různé antispastické postupy. Používáme i myofasciální postupy, mobilizační a měkké techniky hlavně periferních kloubů končetin, různé metody posturální aktivace. S progredující invaliditou se stává důležitým nácvik správného stereotypu chůze, výběr a používání vhodných kompenzačních pomůcek. Ucelený rehabilitační program by měl zahrnovat dále ergoterapii, urorehabilitaci, pravidelnou péči logopeda, opakované lázeňské či rekondiční pobyty a nelze opomenout i důležitou péči psychologa či psychiatra.
Díky zkušenostem z našeho rehabilitačního pracoviště mohu závěrem vyjádřit přesvědčení, že pacienti z komplexního rehabilitačního intenzivního programu opravdu velmi profitují. A je naším velkým přáním, aby se dostupnost sítě rehabilitačních pracovišť pro pacienty s RS stále rozšiřovala.
Martina Kövari
Rehabilitační klinika Malvazinky
U Malvazinky 5
155 00 Praha 5
Sources
1. CUTTER, G. R., BAIER, M. L. ET AL.: Development of a multiple sclerosis funkctional composite as a clinical trial outcome measure. Brain, 122, 1999, s. 871-882.
2. GOLD, R., JAWA, A., MILLER, D. H. et al.: Expert opinion: Guidelines for the use of natalizumab in multiple sclerosis patients previously treated with immunomodulating therapies.
3. GREGG BLEVINS, M. D., ROLAND MARTIN, M. D.: Future immunotherapies in multiple sclerosis – semin. Neurol., 23, 2003, 2, s. 147-158.
4. HAVRDOVÁ, E, a kol.: Neuroimunologie. Maxdorf Praha, 2001, s. 200-208.
5. HAVRDOVÁ, E. a kol.: Neuroimunologie, Maxdorf Praha, 2001, s. 212-214.
6. HAVRDOVÁ, E.: Roztroušená skleróza. Triton, Praha, 2002, s. 16-18.
7. HAVRDOVÁ, E. Roztroušená skleróza, zánět nebo degenerace? Neurologie pro praxi, 2007, 2, s. 99-101.
8. HOBART, J., CAMPING, D.: The multiple sclerosis impact scale: a new patient-based outcome measure. Brain, 124, 2001, s. 962-973.
9. KURTZKE, J. F.: Rating impariment in multiple sclerosis: an expanded disability status scale (EDSS). Neurology, 33, 1983, s. 1444-1452.
10. ŘASOVÁ, K, ŠAVRDOVÁ, E.: Rehabilitace u roztroušené sklerózy. Neurologie pro praxi, 2005, 1, s. 306-309.
Labels
Physiotherapist, university degree Rehabilitation Sports medicine
Article was published inRehabilitation & Physical Medicine

2009 Issue 1-
All articles in this issue
- JAK VLASTNĚ FUNGUJE VOJTOVA METODA?
- NOVÉ TRENDY V ROZTROUŠENÉ SKLERÓZE
- HODNOCENÍ MOTORIKY RUKY PACIENTŮ V CHRONICKÉM STADIU PO CÉVNÍ MOZKOVÉ PŘÍHODĚ - TAPPING TESTEM PRSTŮ A TESTEM DEVÍTI OTVORŮ A KOLÍKŮ
- VERTEBROBAZILÁRNÍ KOMPLIKACE PŘI MANIPULAČNÍ LÉČBĚ KRČNÍ PÁTEŘE
- JE MASÁŽ SKUTEČNĚ TAK ÚČINNÁ JAK SE PŘEDPOKLÁDÁ?
- PSYCHOSOCIÁLNE RIZIKOVÉ FAKTORY V REHABILITÁCII KARDIAKOV
- SROVNÁNÍ EFEKTIVITY SLATINNÉ VANY A SLATINNÝCH ZÁBALŮ V ALTERNATIVNÍM PODÁNÍ
- INFORMOVANOST MATEK O MOTORICKÉM VÝVOJI DÍTĚTE DO OBDOBÍ DOSAŽENÍ BIPEDÁLNÍ LOKOMOCE
- Rehabilitation & Physical Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- HODNOCENÍ MOTORIKY RUKY PACIENTŮ V CHRONICKÉM STADIU PO CÉVNÍ MOZKOVÉ PŘÍHODĚ - TAPPING TESTEM PRSTŮ A TESTEM DEVÍTI OTVORŮ A KOLÍKŮ
- VERTEBROBAZILÁRNÍ KOMPLIKACE PŘI MANIPULAČNÍ LÉČBĚ KRČNÍ PÁTEŘE
- JAK VLASTNĚ FUNGUJE VOJTOVA METODA?
- SROVNÁNÍ EFEKTIVITY SLATINNÉ VANY A SLATINNÝCH ZÁBALŮ V ALTERNATIVNÍM PODÁNÍ
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

