-
Medical journals
- Career
Využití telemetrického monitorování intrakraniálního tlaku v diferenciální diagnostice idiopatické nitrolební hypertenze – kazuistika
Authors: V. Vybíhal 1; A. Mrlian 1; E. Neuman 1; R. Uhmannová 2; A. Šprláková-Puková 3; M. Smrčka 1
Authors‘ workplace: Neurochirurgická klinika, LF MU a FN Brno, přednosta: Prof. MUDr. M. Smrčka, Ph. D., MBA 1; Oční klinika, LF MU a FN Brno, přednosta: Prof. MUDr. E. Vlková, CSc. 2; Radiologická klinika, LF MU a FN Brno, přednosta: Prof. MUDr. V. Válek, CSc., MBA 3
Published in: Rozhl. Chir., 2014, roč. 93, č. 2, s. 82-86.
Category: Case Report
Podpořeno projektem (Ministerstva zdravotnictví) koncepčního rozvoje výzkumné organizace 65269705 (FN Brno).
Overview
Idiopatická nitrolební hypertenze je stavem, kdy dochází ke zvýšení intrakraniálního tlaku bez známé příčiny. Jednorázové změření hodnoty intrakraniálního tlaku poskytuje údaj pouze v daném časovém okamžiku. Proto jsme u pacientky s kolísavou cefaleou a významnou poruchou zraku provedli telemetrické monitorování nitrolebního tlaku, kdy bylo celkem získáno 226,2 hodiny záznamu při běžných denních aktivitách. Elevace intrakraniálního tlaku nebyla během monitorace prokázána, proto jsme pacientku neindikovali ke zkratovému výkonu.
Klíčová slova:
idiopatická nitrolební hypertenze – telemetrie – intrakraniální tlakÚvod
Idiopatická nitrolební hypertenze je stavem, kdy dochází ke zvýšení intrakraniálního tlaku (ICP) bez známé příčiny. Největším rizikem je pro pacienta vážné poškození zraku, až jeho ztráta. Pro stanovení diagnózy je nutná přítomnost příznaků nitrolební hypertenze, oftalmologické příznaky, nepřítomnost jiných organických příčin nitrolební hypertenze a verifikace elevovaného ICP při lumbální punkci.
Jednorázové změření hodnoty ICP poskytuje údaj pouze v daném časovém okamžiku. Ke kontinuální monitoraci je možno použít klasické ICP čidlo, jež ale představuje otevřený systém, který vzhledem k určitému riziku infekce lze použít pouze pro krátkodobou monitoraci [1]. Navíc není výhodné u dětí a u nespolupracujících pacientů a je limitováno pouze na použití ve zdravotnických zařízeních. Naopak použití telemetrické monitorace ICP odstraňuje tyto nedostatky a umožňuje získat data v delším časovém horizontu a v domácím prostředí.
V práci je prezentována kazuistika využití telemetrické monitorace ICP v diferenciální diagnostice idiopatické nitrolební hypertenze.
Kazuistika
Pacientka, 55letá žena, udávala bolesti hlavy kolísavé intenzity trvající asi 8 let, dále 5 let postupné zhoršování zraku, kdy došlo až ke koncentrickému zúžení zorného pole (trubicové vidění). Pacientka byla operována pro kataraktu oboustranně před 4 lety a je sledována pro adenom hypofýzy, který je ale bez kontaktu se strukturami zrakové dráhy. Tlak při námi provedených lumbálních punkcích se pohyboval v rozmezí od 160 do 190 mm vodního sloupce vleže. Pacientka udávala výraznou úlevu od bolestí hlavy po odpouštění mozkomíšního moku během lumbální punkce.
Vzhledem k tomu, že etiologie poškození zraku s výrazným zúžením zorného pole byla nejasná a pacientka udávala výraznou úlevu od bolestí hlavy po odpuštění mozkomíšního moku, rozhodli jsme se u pacientky provést telemetrické měření intrakraniálního tlaku.
K telemetrickému měření jsme použili komerčně dostupný produkt firmy Raumedic obsahující vlastní telemetrické čidlo pro měření ICP (Neurovent-P-tel), čtecí zařízení (Raumedic TDT 1 readP) a přenosné záznamové zařízení s USB portem (Raumedic Datalogger MPR1). K systému je dodáváno programové vybavení pro ukládání a zpracování dat (Raumedic Datalogger Vers. 1.7), které je schopno exportovat získaná data v excelovském formátu. To nám umožnilo ke zpracování dat současně využít Microsoft® Excel ve verzi 2003, ve kterém jsme ke strukturalizaci a statistickému zpracování objemných dat použili makra vytvořená v Microsoft® Visual Basic.
Implantaci telemetrického čidla jsme po dohodě s pacientkou provedli v celkové anestezii během 10denní hospitalizace. Poloobloukovitou incizi v pravém Kocherově bodě jsme použili k vytvoření lůžka pro telemetrické čidlo. Přes trepanační návrt jsme je pak po protnutí tvrdé pleny zavedli do mozkové tkáně a následně provedli suturu rány a zkontrolovali funkčnost systému (Obr. 1). Celý výkon trval 18 minut. Po implantaci ICP čidla jsme provedli kontrolní vyšetření výpočetní tomografií, které potvrdilo jeho korektní zavedení bez komplikací (Obr. 2).
Image 1. Implantace telemetrického ICP čidla (Neurovent-P-tel) – poloobloukovitá incize, kdy je pak přes trepanační návrt zavedeno čidlo do mozkové tkáně Fig. 1: Implantation of the telemetric ICP sensor (Neurovent-P-tel) – a semi-arc incision with introduction of the sensor into the brain through a burr hole 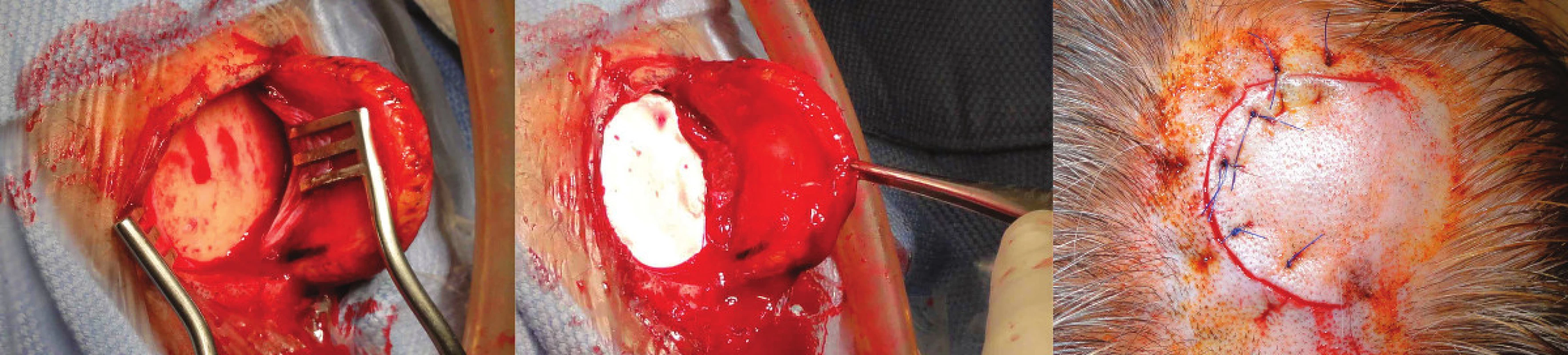
Image 2. Kontrolní vyšetření výpočetní tomografií potvrzující korektní polohu ICP čidla Fig. 2: Postoperative computed tomography confirming the correct position of the ICP sensor 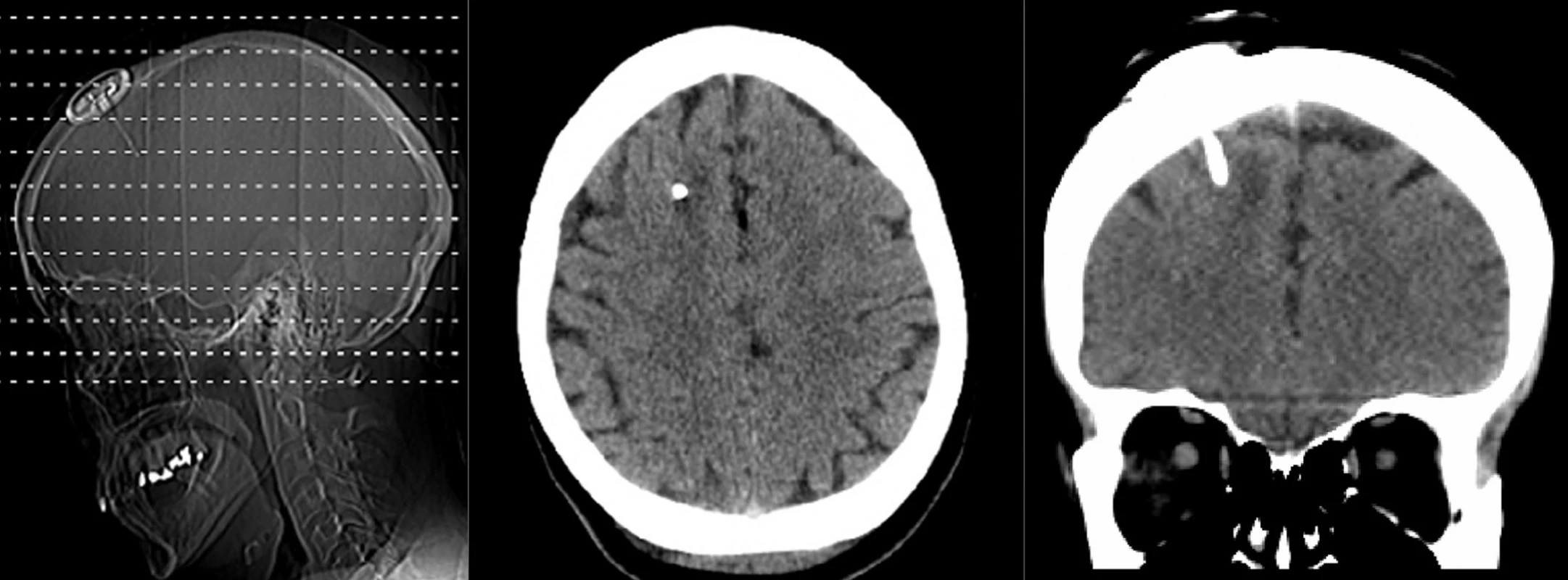
Pacientka byla seznámena s používáním přístroje. Monitoraci jsme provedli zpočátku za hospitalizace, kdy se pacientka zaučila v ovládání přístroje, ale především ambulantně, v domácím prostředí (Obr. 3). Pacientka si vedla záznamový deník, kam si zapisovala časové údaje, případné potíže, vykonávané činnosti atd. Po ukončení monitorace bylo pacientce v lokální anestezii telemetrické ICP čidlo extrahováno během třídenní hospitalizace (Obr. 4). Doba výkonu nepřesáhla 10 minut.
Image 3. Pacientka během prováděné monitorace telemetrického měření ICP Vlevo na obrázku na hlavě čtecí zařízení (Raumedic TDT 1 readP) a vpravo na obrázku kolem pasu umístěné přenosné záznamové zařízení s USB portem (Raumedic Datalogger MPR1). Fig. 3: Patient during ICP telemetry monitoring measurements The reader (Raumedic TDT 1 readP) located on the head on the left side of the picture and the recording device with USB port (Raumedic Datalogger MPR1) placed around the waist on the right side of the picture. 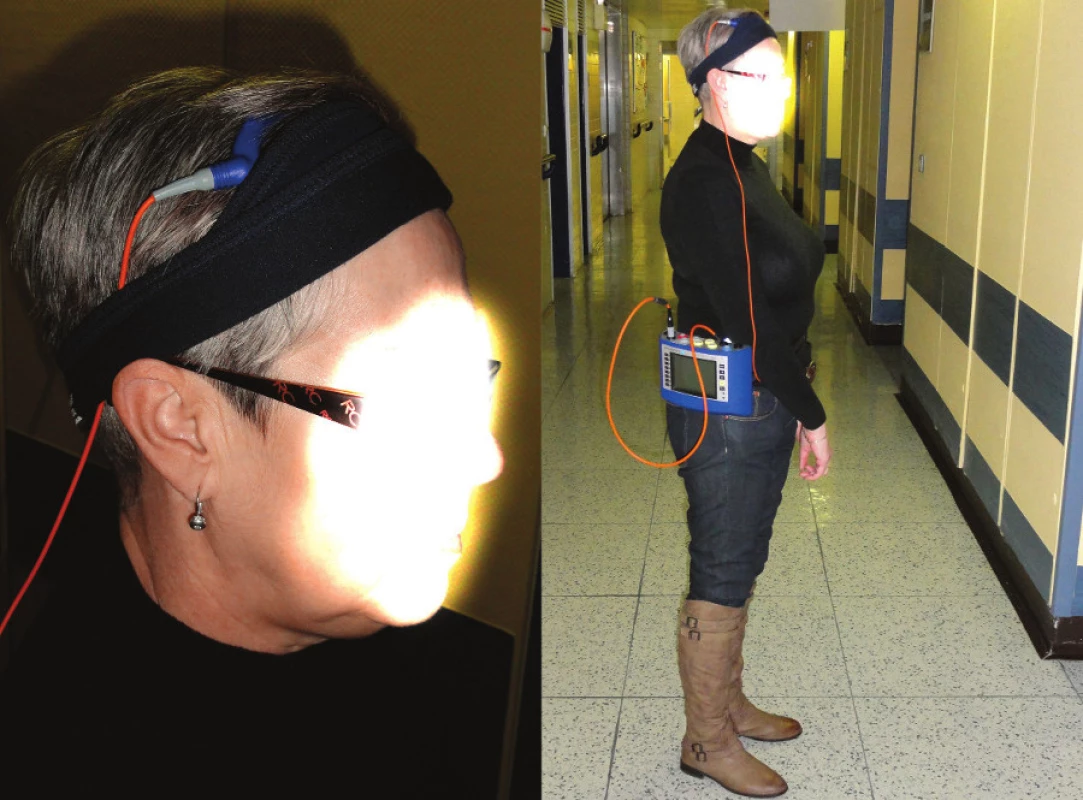
Image 4. Extrakce telemetrického ICP čidla bez známek nepříznivé reakce na implantát Fig. 4: Extraction of the telemetric ICP sensor with no signs of its side effects 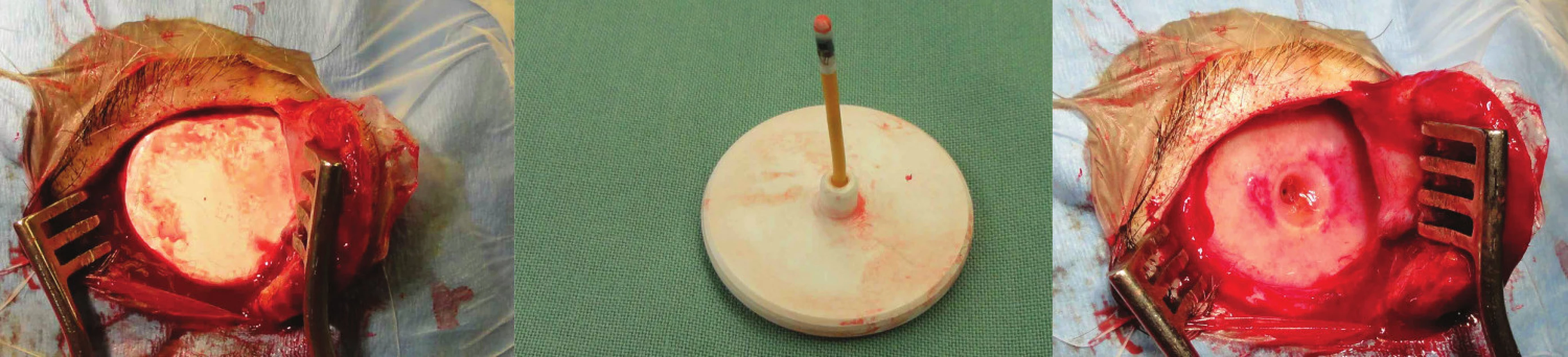
V průběhu telemetrického monitorování jsme během 18 dní získali celkem 817 772 hodnot ICP, což znamená, že bylo monitorováno přesně 13 571 minut, tj. 226,2 hodiny (9,4 dne). Přístroj pacientka aktivovala jak ve dne, tak i v noci pokaždé, když jí to umožňovala situace, bez závislosti na potížích. Data jsme stahovali po 4 až 5 dnech, abychom uvolnili místo v paměti přístroje pro další monitoraci. Po přefiltrování hodnot jsme se pak mohli zaměřit na přesné konkrétní úseky, které nás zajímaly (Obr. 5). V době udávané cefaley pacientkou nedošlo ke zvýšení ICP. Jeho průměrná hodnota byla –1,2±3,0 mmHg s mediánem –0,6 mmHg, modem –0,5 mmHg, minimem –11,4 mmHg a maximem 14,5 mmHg. Hodnota mezi 10 mmHg a 15 mmHg byla zaznamenána celkem devětkrát. Nitrolební hypertenzi jsme tedy pomocí telemetrického monitorování u pacientky neprokázali, a to ani při atakách bolestí hlavy. Proto jsme provedení zkratové operace neindikovali. Pacientka je léčena konzervativně oftalmologem a neurologem a dispenzarizována na naší klinice. Klinický stav pacientky je nadále stacionární.
Image 5. Znázornění ICP křivky v programu Raumedic Datalogger Vers. 1.7 Fig. 5: Representation of the ICP curve in the Raumedic Datalogger Vers. 1.7 software 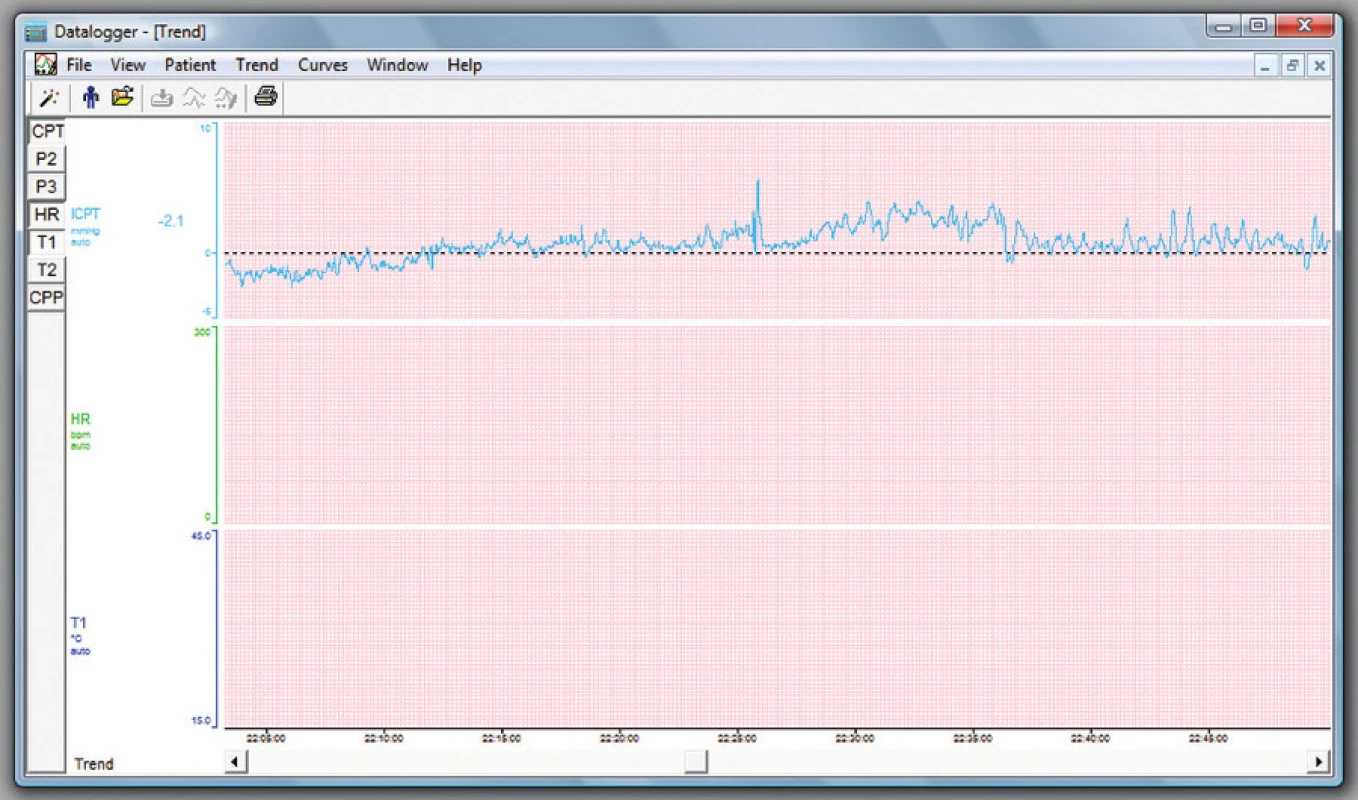
Diskuze
Monitorování ICP je používáno u řady neurologických a neurochirurgických onemocnění [2]. Indikace jsou jasně stanoveny v případě traumatického postižení mozku [3], ale univerzálně akceptované doporučení není a indikace v ostatních případech bývají někdy rozdílné mezi jednotlivými pracovišti [4].
Místa měření ICP mohou být různá: intraventrikulárně, intraparenchymově, epidurálně, subdurálně nebo subarachnoidálně. Nejčastěji je používána lokalizace intraparenchymová. V případě komunikujících likvorových cest může být hodnota ICP získána pomocí lumbální punkce [5]. Invazivně lze měřit ICP pomocí zevní komorové drenáže nebo použitím ICP čidla ve formě mikrosenzoru. Získané hodnoty pomocí zevních komorových drenáží a mikrosenzorů jsou v obou případech přesné a srovnatelné [6]. Nicméně společnou vlastností mikrosenzorů je, že je nelze po zavedení znovu zkalibrovat s výjimkou pneumatických čidel firmy Spiegelberg, která se kalibrují automaticky každou hodinu [7]. Tato nemožnost opakované kalibrace pak způsobuje tzv. „zero drift“, kdy vzniká diference mezi počáteční kalibrací na nulovou hodnotu a hodnotou získanou při extrakci čidla. Nejvíce k tomuto inklinují mikrosenzory na fibrooptickém principu, zatímco čidla pracující na piezoelektrickém principu (Codman MicroSensor nebo Raumedic Neurovent-P ICP senzor) vykazují minimální rozdíly [8–10]. Nevýhodou zevní komorové drenáže je zase vyšší frekvence výskytu infekcí a nefunkčnosti [1,7,8,11,12].
Hlavní výhodou nového telemetrického zařízení k monitoraci ICP je možnost dlouhodobého měření při každodenních činnostech a v domácím prostředí, a to zejména u pacientů s intermitentními známkami elevace ICP [13]. Systém je bezpečný, uživatelsky přívětivý a ovládání je i pro pacienty jednoduché. Zvukový alarm navíc informuje o překročení nastavených kritických hodnot a o přerušení snímání. Doporučená doba implantace by neměla přesáhnout 29 dní, po které je garantována přesnost čidla ±2 mmHg. Nicméně podle některých autorů je možné prodloužení monitorace nad stanovený limit bez komplikací [13]. Citero et al., kteří otestovali 99 čidel Neurovent-P, se nesetkali se žádnou infekcí a u 2 pacientů zaznamenali drobné hemoragie nevyžadující neurochirurgickou intervenci [9]. Výhodou čidla je také kompatibilita s magnetickou rezonancí, stejně jako u čidel firmy Spiegelberg nebo Codman, na rozdíl od některých jiných nekompatibilních čidel obsahujících feromagnetické komponenty [14,15].
Mezi nejčastější indikace telemetrického monitorování ICP patří ověření průchodnosti ventrikulostomie spodiny třetí komory, zjištění dysfunkce shuntu nebo předrénování, monitorace ICP u idiopatické či sekundární nitrolební hypertenze nebo u kraniostenóz. Zejména u dětí je noninvazivní monitorace ICP dobře tolerována a je daleko komfortnější [13].
Znalost hodnot dlouhodobého monitorování ICP nám poskytuje další informace o výsledku operace a patogenezi některých neurochirurgických onemocnění, a pomáhá tak v rozhodování o dalším terapeutickém postupu [16–19].
Závěr
Telemetrické monitorování ICP může být významným nástrojem v diferenciální diagnostice idiopatické nitrolební hypertenze. Umožňuje získání velkého množství dat při běžných denních činnostech, které bychom jinak nebyli schopni získat, a stává se tak nezastupitelným pomocníkem v indikaci pacientů k případné zkratové operaci.
Zkratky
ICP – intrakraniální tlak (intracranial pressure)
MUDr. Václav Vybíhal, Ph.D.
Neurochirurgická klinika
LF MU a FN Brno
625 00 Brno, Jihlavská 20
e-mail: vvybihal@fnbrno.cz
Sources
1. Bekar A, Dogan S, Abas F, et al. Risk factors and complications of intracranial pressure monitoring with a fiberoptic device. J Clin Neurosci 2009;16 : 236–240.
2. Raboel PH, Bartek J Jr., Andersen M, et al. Intracranial pressure monitoring: invasive versus non-invasive methods – a review. Critical Care Research and Practice 2012: Article ID 950393.
3. Bratton SL, Chesnut RM, Ghajar J, et al. Guidelines for the management of severe traumatic brain injury. VI. Indications for intracranial pressure monitoring. Journal of Neurotrauma 2007;24(Suppl. 1):S37–S44.
4. Forsyth RJ, Wolny S, Rodrigues B. Routine intracranial pressure monitoring in acute coma. Cochrane Database of Systematic Reviews 2009;3:Article ID CD002043.
5. Lenfeldt N, Koskinen LOD, Bergenheim AT, et al. CSF pressure assessed by lumbar puncture agrees with intracranial pressure. Neurology 2007;68(2):155–158.
6. Bratton SL, Chesnut RM, Ghajar J, et al. Guidelines for the management of severe traumatic brain injury. VII. Intracranial pressure monitoring technology. Journal of Neurotrauma 2007;24 (Suppl. 1):S45–S54.
7. Lang JM, Beck J, Zimmermann M, et al. Clinical evaluation of intraparenchymal Spiegelberg pressure sensor. Neurosurgery 2003;52 : 1455–1459.
8. Gelabert-Gonzalez M, Ginesta-Galan V, Sernamito-Garcia V, et al. The Camino intracranial pressure device in clinical practice. Assessment in a 1000 cases. Acta Neurochirurgica 2006;148 : 435–441.
9. Citero G, Piper I, Chambers IR, et al. Multicenter clinical assessment of the raumedic Neurovent-P intracranial pressure sensor: a report by the brainIT group. Neurosurgery 2008;63 : 1152–1158.
10. Leskot T, Reina V, le Manach Y, et al. In vivo accuracy of two intraparenchymal intracranial pressure monitors. Intensive Care Medicine 2011;37 : 875–879.
11. Hong WC, Tu YK, Chen YS, et al. Subdural intracranial pressure monitoring in severe head injury: clinical experience with the Codman MicroSensor. Surgical Neurology 2006;66(Suppl. 2): S8–S13.
12. Koskinen LOD, Olivecrona M. Clinical experience with the intraparenchymal intracranial pressure monitoring Codman microsensor system. Neurosurgery 2005;56 : 693–698.
13. Welschehold S, Schmalhausen E, Dodier P, et al. Neurosurgery 2012;70(Suppl. 1):44–49.
14. Shellock FG. Biomedical implants and devices: assessment of magnetic field interactions with a 3.0-Tesla MR system. Journal of Magnetic Resonance Imaging 2002; 16 : 721–732.
15. Stendel R, Heidenreich J, Schilling A, et al. Clinical evaluation of a new intracranial pressure monitoring device. Acta Neurochirurgica 2003;145 : 185–193.
16. Fadrus P, Smrčka V, Smrčka M, et al. Monitorování intraparenchymového a intrahematomového tlaku při stereotaktické evakuaci spontánních intracerebrálních hematomů. Cesk Slov N Neurol 2005;68 : 303–309.
17. Frim DM, Goumnerova LC. Telemetric intraventricular pressure measurements after third ventriculocisternostomy in a patient with noncommunicating hydrocephalus. Neurosurgery 1997;41 : 1425–1428.
18. Chapman PH, Cosman E, Arnold M. Telemetric ICP monitoring after surgery for posterior fossa and third ventricular tumors. Technical note. J Neurosurg 1984;60 : 649–651.
19. Richard KE, Block FR, Weiser RR. First clinical results with a telemetric shunt-integrated ICP-sensor. Neurol Res 1999;21 : 117–120.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2014 Issue 2-
All articles in this issue
- Deset let endovenózní ablace varixů, úspěchy, neúspěchy a budoucnost
- Transarteriální chemoembolizace pomocí „drug eluting beads“ (TACE DEB) u nemocných s radikálně neodstranitelným hepatocelulárním karcinomem (HCC)
- Problematika klostridiové kolitidy na chirurgickém pracovišti
- Využití acelulárních biologických xenotransplantátů v lokální léčbě Lyellova syndromu
- Využití telemetrického monitorování intrakraniálního tlaku v diferenciální diagnostice idiopatické nitrolební hypertenze – kazuistika
- Problematika stanovení bezpečných resekčních okrajů u karcinomu rekta
- Problematika stanovení bezpečných resekčních okrajů u nádorů parenchymatózních orgánů
- Problematika stanovení bezpečných resekčních okrajů patologem v mamární onkochirurgii
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Problematika stanovení bezpečných resekčních okrajů u nádorů parenchymatózních orgánů
- Problematika stanovení bezpečných resekčních okrajů u karcinomu rekta
- Problematika stanovení bezpečných resekčních okrajů patologem v mamární onkochirurgii
- Problematika klostridiové kolitidy na chirurgickém pracovišti
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

