-
Medical journals
- Career
Komplex hyaluronanu a jodu - Hyiodine® - nová metoda při terapii diabetických defektů
Authors: L. Sobotka 1; V. Velebný 2; A. Šmahelová 1; M. Kusalová 1
Authors‘ workplace: Klinika gerontologická a metabolická Lékařské fakulty UK a FN, Hradec Králové, přednosta prof. MUDr. Luboš Sobotka, CSc. 1; Contipro, a. s., Dolní Dobrouč, ředitel RNDr. Vladimír Velebný 2
Published in: Vnitř Lék 2006; 52(5): 417-422
Category: Diabetes and other subjects (infection, dermatovenerology and rheumatology) Hradec Králové 3 to 4 June 2005
Overview
Komplikované diabetické defekty jsou velmi obtížně léčitelné a často vedou k amputacím dolních končetin. Na našich pracovištích byla vyvinuta originální metoda léčby diabetických defektů, která je založena na kombinaci vysokomolekulárního hyaluronanu a jódu - Hyiodine®. Cílem naší studie bylo posouzení účinku této nové metody na hojení komplikovaných diabetických defektů.
Metodika:
Vliv preparátu Hyiodine® byl studován u 22 nemocných s komplikovanými diabetickými defekty. Hyiodine® byl buď aplikován přímo na defekt a nebo (častěji) byla rána pokryta nebo vyplněna gázou nasycenou preparátem Hyiodine®. Po té byla rána pokryta několika vrstvami suché sterilní gázy.Výsledky:
Během 2-6 týdnů po zahájení převazů se kromě dvou všechny defekty vyplnily granulační tkání. Kompletní zhojení defektu bylo pozorováno u 18 nemocných během 6-20 týdnů po zahájení léčby v závislosti na charakteru, lokalizaci a rozsahu defektu. Dva pacienti jsou stále léčeni preparátem Hyiodine®, u obou je však pozorováno výrazné zlepšení stavu. Léčba nebyla úspěšná u dvou nemocných se současným ischemickým postižením při arteriální okluzi.Závěr:
Z našich výsledků je patrné, že komplex hyaluronanu s jódem je nová efektivní metoda pro léčbu komplikovaných diabetických defektů, u nichž není postiženo arteriální zásobení.Klíčová slova:
léčba ran - diabetes mellitus - diabetický defekt - hyaluronan - jód - Hyiodine®Úvod
Diabetes mellitus bývá velmi často komplikován vznikem povrchových i hlubokých kožních defektů. Tyto léze postihují zejména dolní končetiny, kde mohou způsobovat nejen poruchu kožního krytu, ale současně i postižení podkoží, šlach a kloubních pouzder a osteomyelitidu. Komplikované defekty jsou velmi častou příčinou amputací dolních končetin. Patogeneze diabetických defektů je komplexní. Na jejich vzniku se mimo jiné podílí polyneuropatie s poruchou citlivosti [1], mikroangiopatie, makroangiopatie, zhoršená schopnost obrany vůči infekci, porucha metabolizmu prostaglandinů [2]. Podle posledních představ souvisí porucha hojení a vznik diabetických defektů s přítomností pokročilých produktů glykozylace a jejich prooxidačním působením [3]. Následkem je častý vznik diabetických defektů a současně porušená regenerační schopnost organizmu, která se projevuje porušením hojení ran [4,5]. I přes pokroky v léčbě a kompenzaci diabetu představují diabetické defekty složitý léčebný problém, a to především pokud jsou infikovány. Nezřídka končí amputací, která je následována nákladným procesem rehabilitace a velmi často znamená podstatné zhoršení kvality života nemocných.
Kyselina hyaluronová (HA) je nedílnou součástí extracelulární matrix téměř všech orgánů v našem organizmu. Jde o lineární polysacharid, v němž se střídají disacharidové jednotky složené z kyseliny glukuronové a N-acetyl-glukosaminu. Unikátní vlastností HA, která má vztah k řadě jejích funkcí v organizmu, je její schopnost vázat vodu. Ve vodních roztocích je HA konfigurována do flexibilních svinutých řetězců a sama je schopna vázat asi 1000krát více vody než je její vlastní hmotnost. V tomto ohledu je HA nejvíce hydrofilní molekulou v našem organizmu. V různých tkáních existují komplexy HA s ostatními makromolekulami. Velmi dobře jsou charakterizovány hyaldheriny ve chrupavce. Zde má k HA vysokou afinitu především proteoglykan chondroitin sulfát. Kyselina hyaluronová se podílí i na modulaci zánětlivé reakce, její nízkomolekulární štěpy stimulují novotvorbu kapilár. Částečným potlačením kontaktní inhibice stimuluje buněčné dělení v oblasti hojení. Z uvedených důvodů byly činěny pokusy o využití HA při převazech chronických a nehojících se ran. V tomto smyslu však nedošlo k očekávanému efektu, zřejmě i vlivem štěpení HA působením bakteriálních hyaluronidáz.
Jód je spolehlivým dezinfekčním prostředkem, který bezpečným způsobem dekontaminuje ránu. Jeho dezinfekční schopnost je dokonalá a vedlejší účinky jeho podávání jsou nepatrné. Přítomnost jódu může navíc stabilizovat molekulu kyseliny hyaluronové, neboť svým dezinfekčním účinkem eliminuje možný vliv bakteriálních hyaluronidáz.
Hyiodine® je komplex biotechnologicky vyrobené kyseliny hyaluronové (totožné s lidskou hyaluronovou kyselinou) a jódu. Jako součást lokální terapie má Hyiodine® unikátní antiadhezivní účinky, současně zabraňuje maceraci okolní kůže a zlepšuje podmínky pro granulaci a epitelizaci (hojení) rány. Cílem naší práce bylo posoudit použití uvedeného preparátu na průběh hojení diabetických defektů.
Metoda
Použití komplexu vysokomolekulárního hyaluronanu s jódem bylo studováno u 22 nemocných s komplikovanými diabetickými defekty na dolních končetinách. Téměř polovina z nich měla defekt postihující kostní struktury, dvanáct nemocných mělo odhalené šlachy a kloubní pouzdra (tab. 1).
Table 1. Zastoupení jednotlivých diabetických defektů u skupiny sledovaných nemocných. 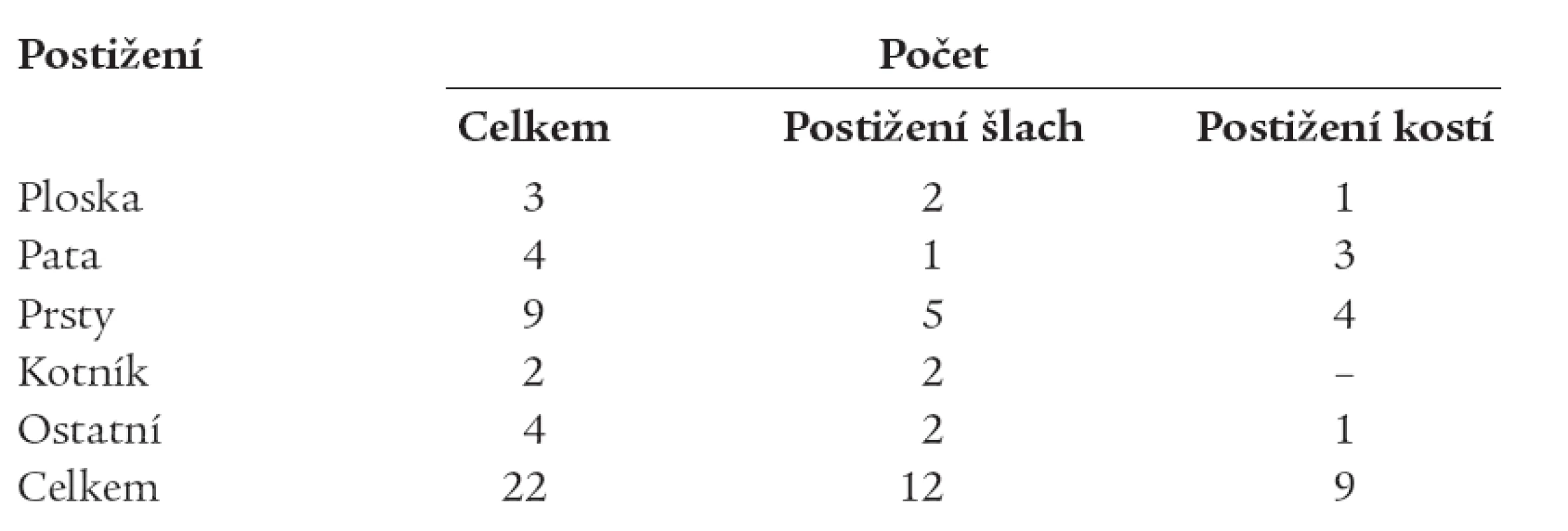
Preparátem Hyiodine® byla nasycena sterilní gáza, která byla přiložena na diabetický defekt. V případě hlubokých defektů byl preparát rovněž aplikován přímo do defektu a tento byl opět překryt sterilní gázou navlhčenou v preparátu Hyiodine®. Diabetický defekt byl po té vždy překryt několika vrstvami suché sterilní gázy a převázán obinadlem nebo přelepen náplastí. Diabetické defekty byly převazovány každých 24 hodin.
Průběh hojení defektu byl dokumentován každých 14 dní pomocí digitálního fotoaparátu Camedia (firmy Olympus).
Výsledky
K úplnému zhojení defektu došlo u 18 nemocných. U 2 nemocných dosud terapie pokračuje přes významné zmenšení rozsáhlého defektu. U zbývajících 2 nemocných muselo dojít k amputaci dolní končetiny. V obou případech nemocných, kterým byla povedena amputace, byl diagnostikován uzávěr bércových tepen, který nebylo možno řešit angioplastikou ani chirurgicky. Délka léčení u skupiny nemocných, u nichž došlo ke zhojení defektu, je uvedena v tab. 2. V tabulce nejsou uvedeny údaje o nemocných, u nichž byla provedena amputace pro neřešitelný uzávěr bércových tepen.
Table 2. Délka léčby diabetických defektů preparátem Hyiodine®. 
Příklady využití preparátu jsou uvedeny na obr. 1 - 12.
Image 1. Rozsáhlý defekt na plosce nohy s postižením patní kosti. 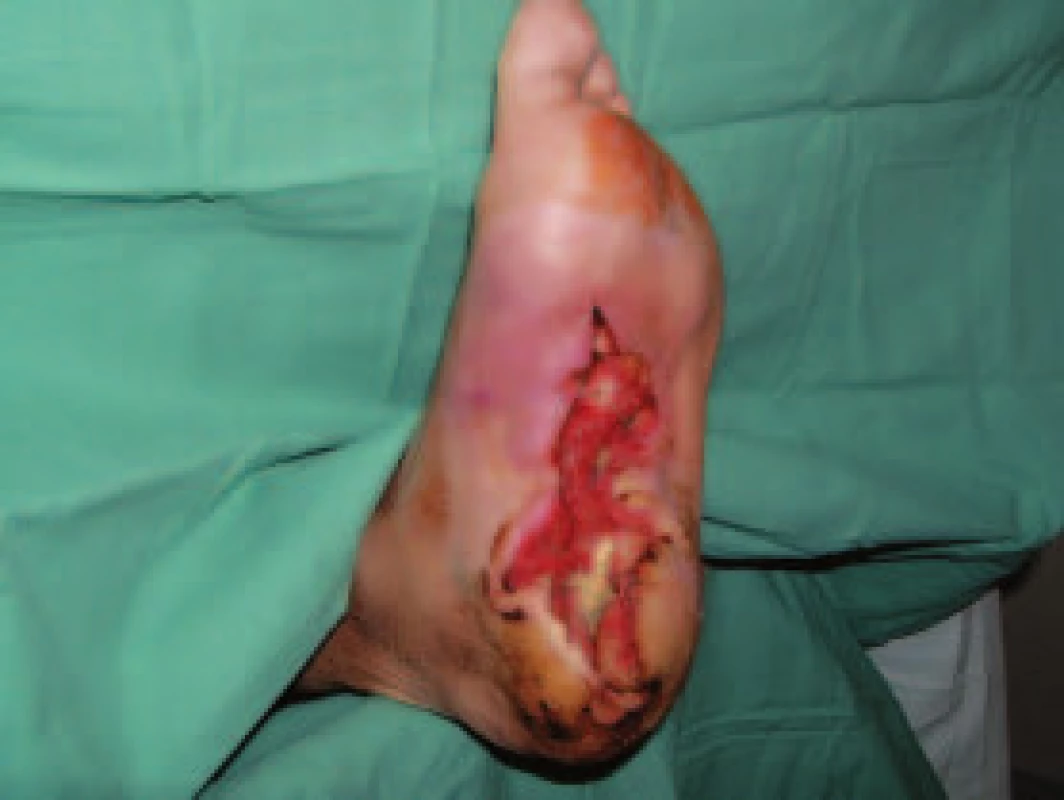
Pacient č. 1 Image 2. Nález po 6 týdnech léčby preparátem Hyiodine®. 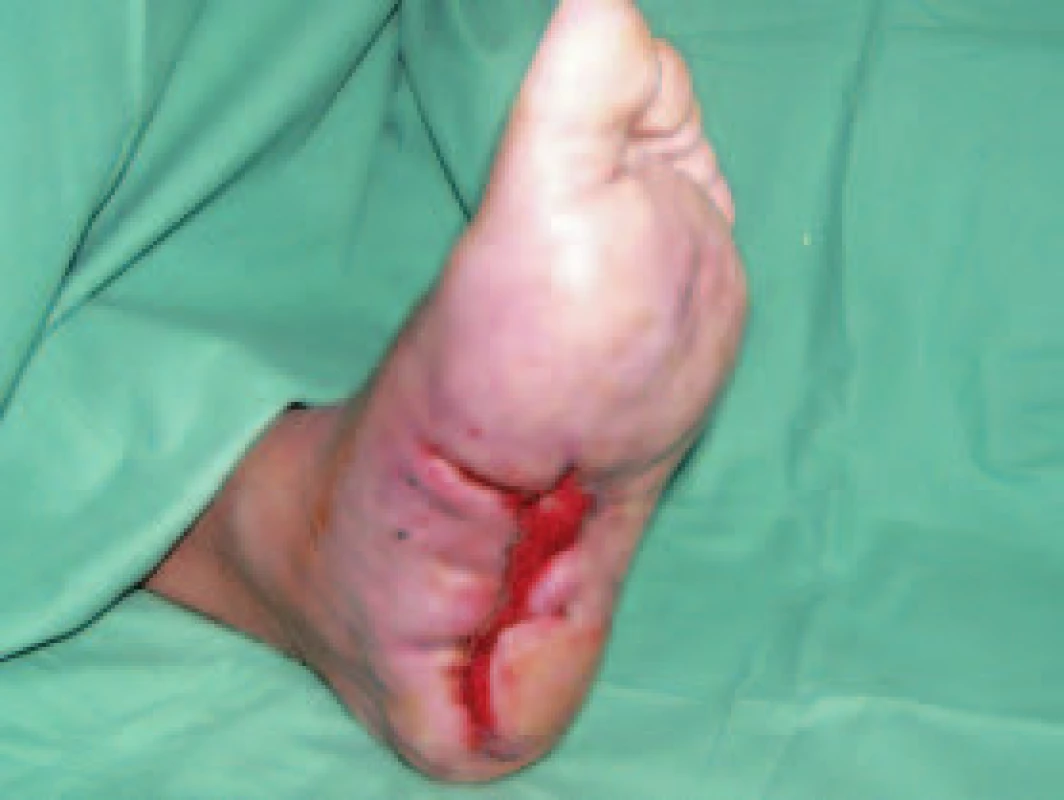
Pacient č. 1 Image 3. Zhojení defektu po 12 týdnech léčby preparátem Hyiodine®. 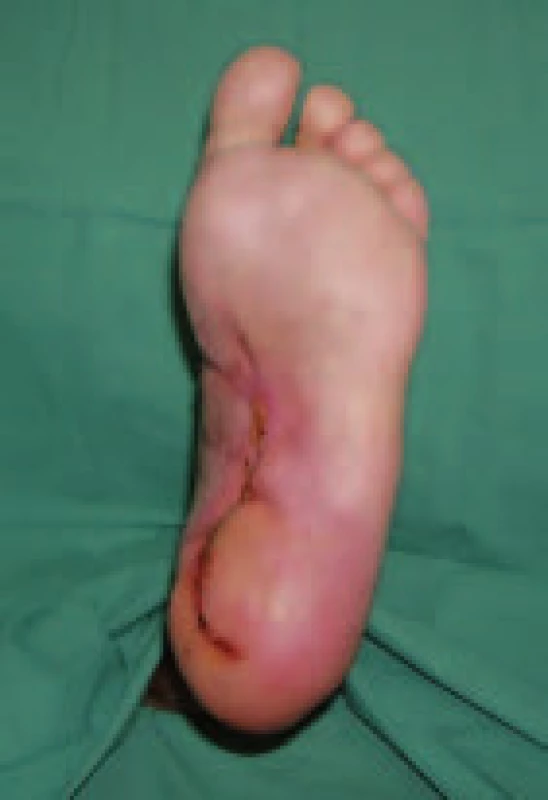
Pacient č. 1 Image 4. Hluboký defekt mezi 4. a 5. prstem pravé nohy. 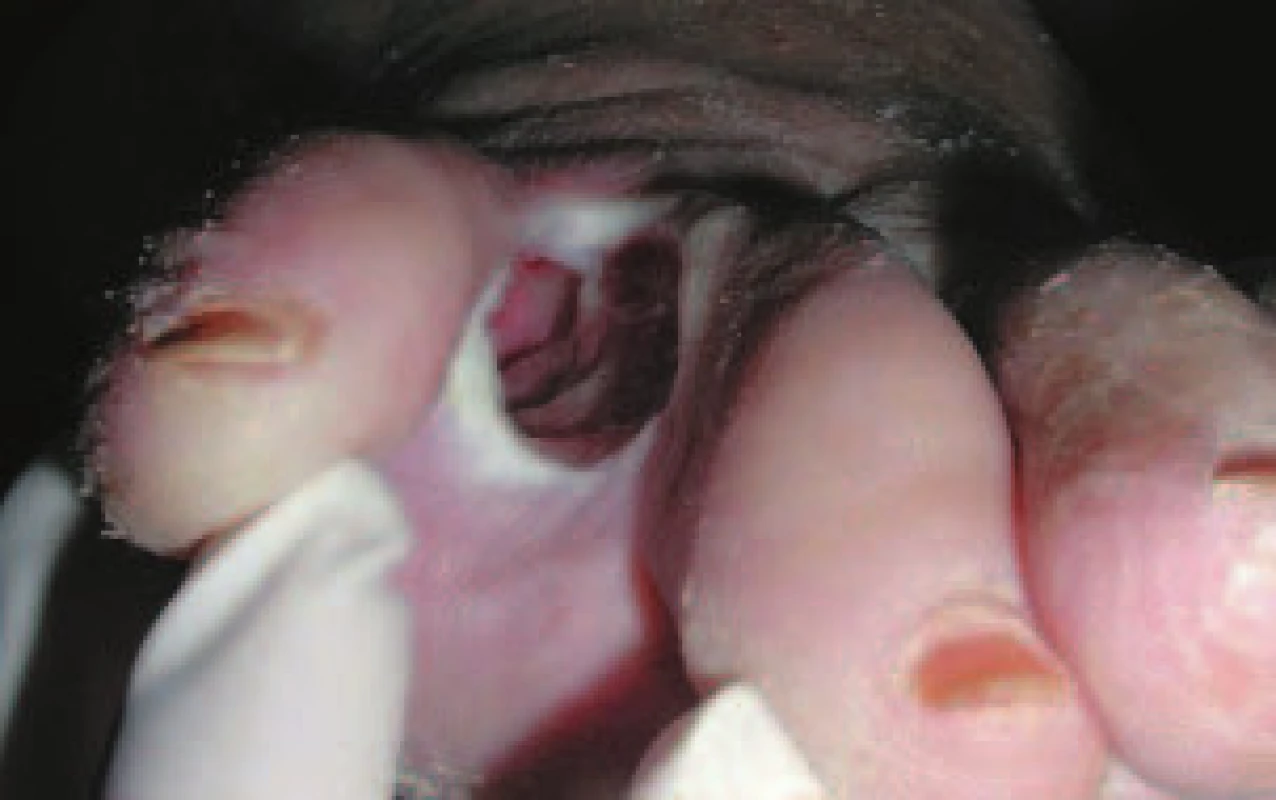
Pacient č. 2 Image 5. Nález po 3 týdnech léčby preparátem Hyiodine®. 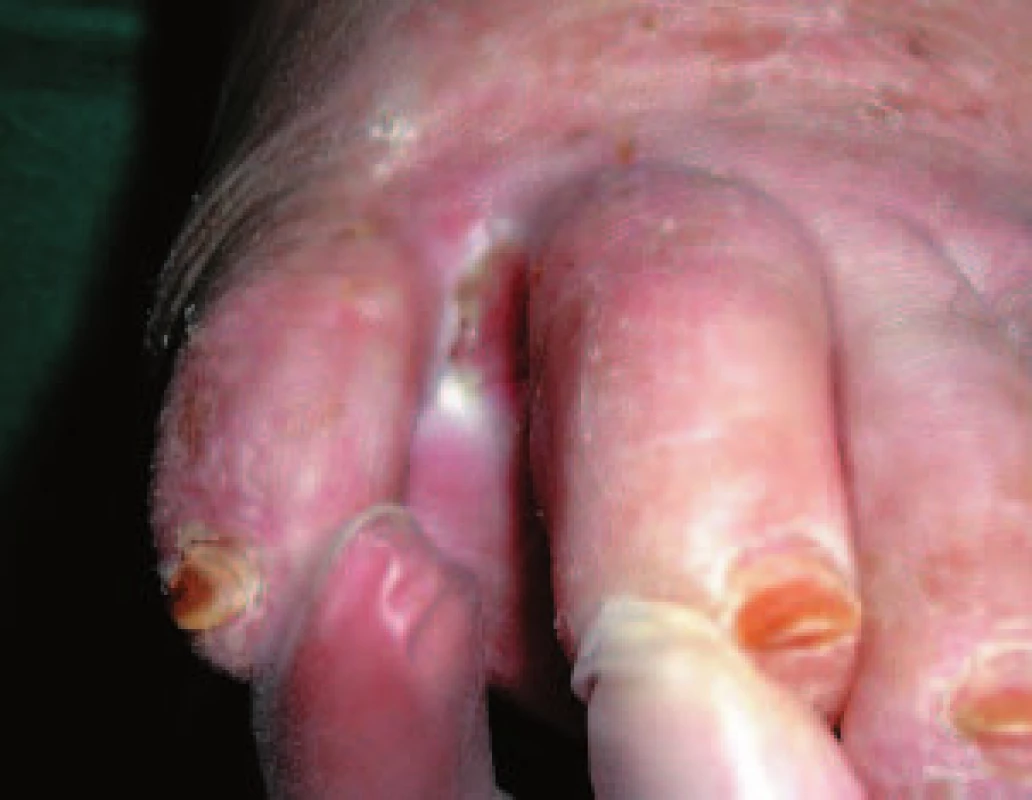
Pacient č. 2 Image 6. Zhojení defektu po 7 týdnech léčby preparátem Hyiodine®. 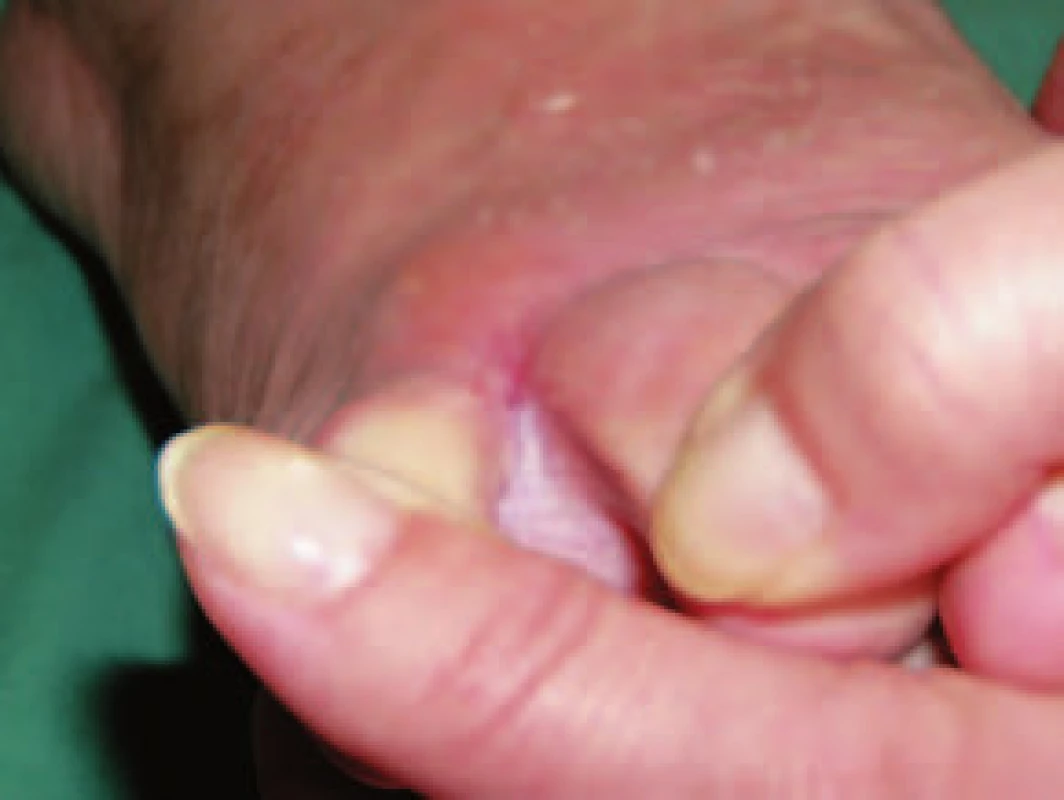
Pacient č. 2 Image 7. Hluboký defekt na patě s podélným rozštěpem patní kosti. 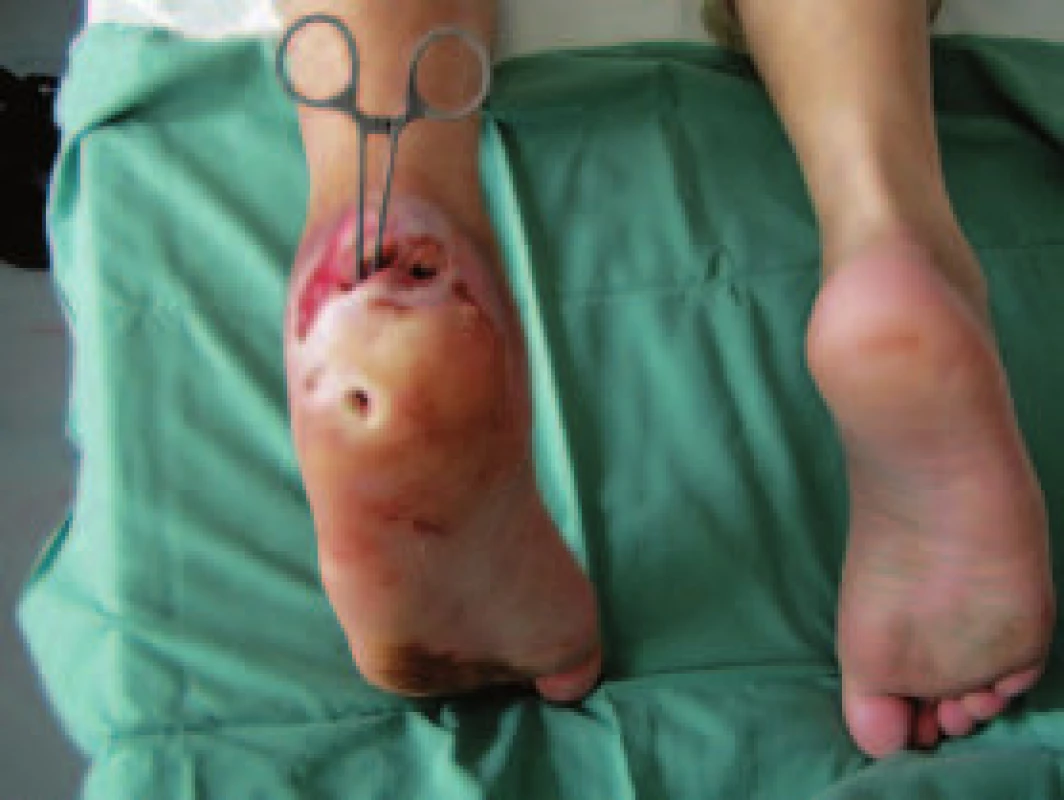
Pacient č. 3 Image 8. Hluboký defekt na patě s podélným rozštěpem patní kosti – detail. 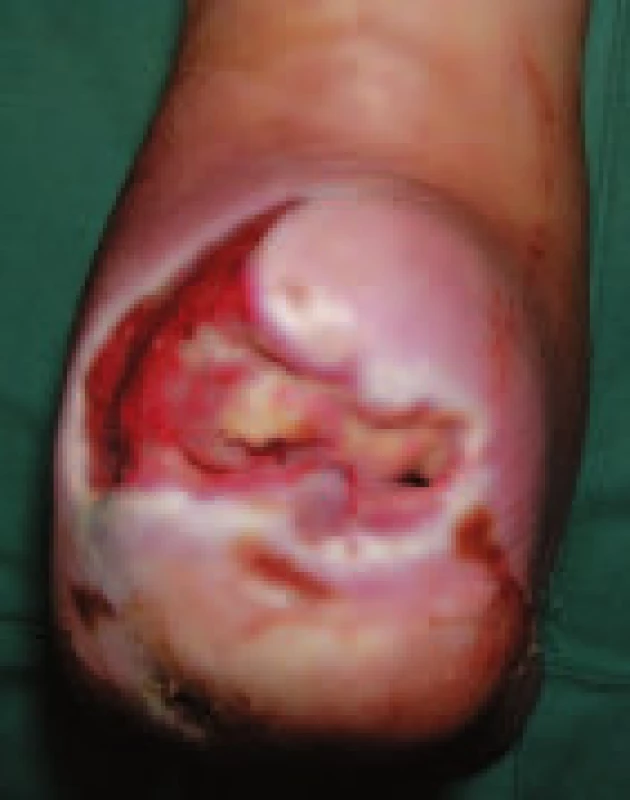
Pacient č. 3 Image 9. Zhojení defektu po 4 měsících léčby preparátem Hyiodine®. 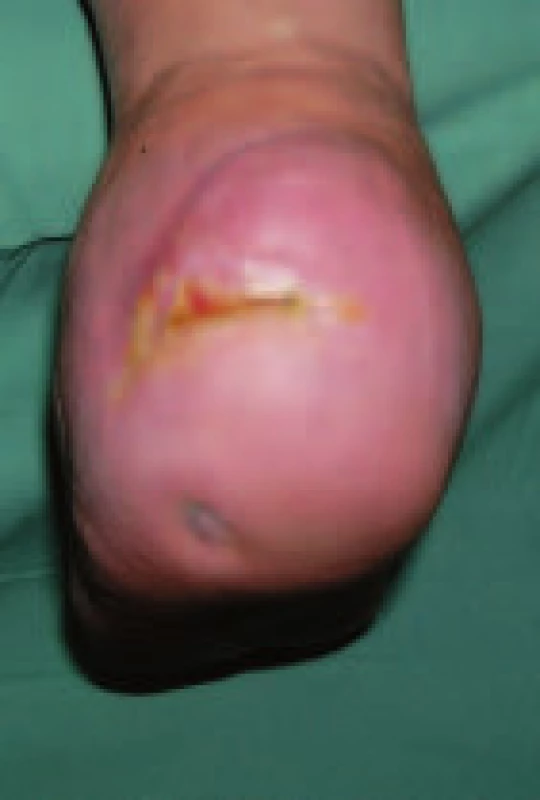
Pacient č. 3 Image 10. Hluboký defekt na plosce nohy po amputaci 3. prstu s píštělemi. 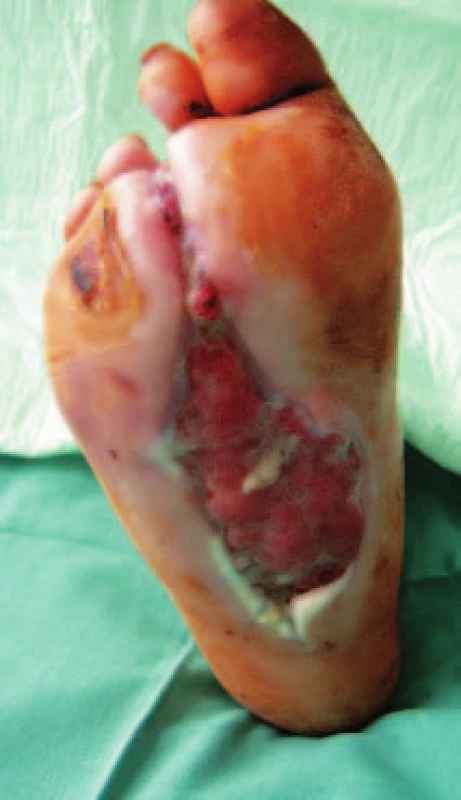
Pacient č. 4 Image 11. Stav po 9 týdnech léčby preparátem Hyiodine®. 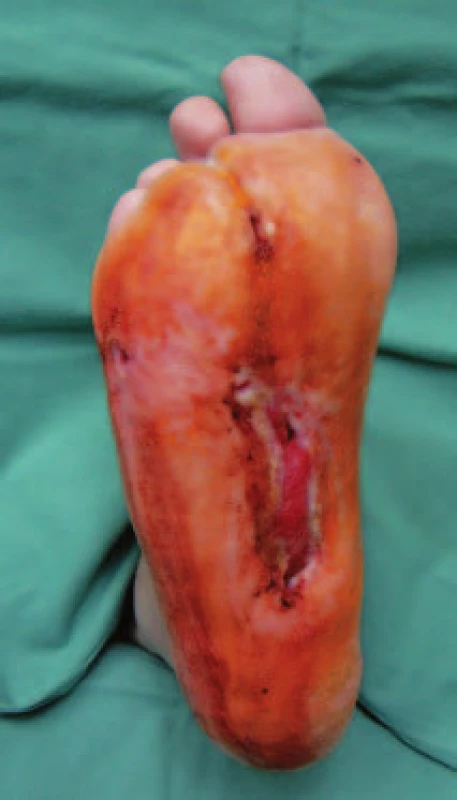
Pacient č. 4 Image 12. Zhojení defektu po 4 měsících léčby preparátem Hyiodine®. 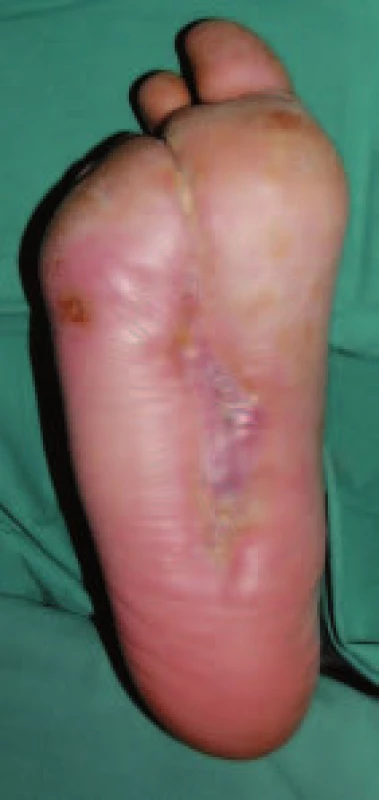
Pacient č. 4 Kromě dvou nemocných, u nichž byl během léčby diagnostikován neřešitelný uzávěr bércových tepen, došlo ke zhojení a nebo k podstatnému zlepšení defektu u všech nemocných, kteří byli léčení komplexem hyaluronanu a jódu.
Preparát Hyiodine® byl výborně snášen a během celého průběhu lokální léčby nedošlo k žádným nežádoucím projevům. Rovněž nebyly pozorovány alergické reakce na lokální aplikaci komplexu hyaluronanu sodného a jódu.
Diskuse
Kyselina hyaluronová či její estery byly zkoušeny v celé řadě indikací. Klasicky je hyaluronan používán při léčbě artrotických postižení [6], a to částečně i vzhledem k možným změnám její molekulové hmotnosti [7]. Možné využití hyaluronanu při hojení rozsáhlých ran může souviset s jeho vztahem k regeneračním procesům u různých živočichů. Syntéza a zvýšený obrat hyaluronanu je například typický pro regenerující končetinu čolka [8]. Degradační produkty kyseliny hyaluronové mají vztah k angiogenezi v granulační tkáni [9] i k regenerační aktivitě [10], což může částečně souviset i se stimulací CD 44 receptorů [11].
V naší studii jsme se zabývali vlivem komplexu vysokomolekulárního hyaluronanu a jodu na hojení diabetických defektů. Použití uvedeného komplexu nebylo dosud v literatuře popsáno a ani používáno. Kombinace hyaluronanu s jódem byla použita ze dvou důvodů. Jód je dosud nepřekonaným dezinfekčním prostředkem, který může omezit šíření infekce v oblasti operační rány. Potlačení bakteriálního růstu pak může zabránit bakteriální degradaci hyaluronanu a zajistit jeho přítomnost v místě hojení. O tom svědčí i naše předběžné výsledky; po 24 hodinách byla v místě převazu přítomná vysokomolekulární hyaluronová kyselina (dosud nepublikováno). Literární údaje o účinku hyaluronanu na proces hojení nejsou jednotné. Pozitivní účinek byl pozorován u hojení defektů v epitelu močového měchýře králíků [12], či u hojení poškozených menisků [13]. Naopak v některých případech nebyly pozitivní účinky hyaluronanu pozorovány [14]. Povzbudivé výsledky u hojení ran na dolních končetinách byly pozorovány během použití esterů kyseliny hyaluronové [15]. O použití kombinace hyaluronanu s jodem však nejsou v literatuře žádné údaje.
Smyslem naší práce bylo posoudit vliv komplexu hyaluronanu a jódu na hojení diabetických defektů. Šlo o pilotní studii, při níž byl použit registrovaný preparát Hyiodine®, který byl u nás dosud používán jako vlhké krytí, určené především pro rozsáhlé pooperační rány, rozpadlé sutury a podobně. Výrazný hojivý účinek u nemocných s těžkými diabetickými defekty byl proto velmi povzbudivý. Přesná znalost mechanizmu pozitivního účinku kombinace hyaluronanu s jódem na hojení diabetických defektů není však dosud jasná a vyžádá si další studium.
Uvedená práce byla podpořena výzkumným záměrem MŠM 0021620820.
prof. MUDr. Luboš Sobotka, CSc.
www.lfhk.cuni.cz
e-mail: pustik@lfhk.cuni.cz
Doručeno do redakce: 4. 11. 2005
Přijato k otištění: 4. 11. 2005
Sources
1. Piaggesi A. Research development in the pathogenesis of neuropathic diabetic foot ulceration. Curr Diab Rep 2004; 4 : 419-423.
2. Kampfer H, Schmidt R, Geisslinger G et al. Wound inflammation in diabetic ob/ob mice: functional coupling of prostaglandin biosynthesis to cyclooxygenase-1 activity in diabetes-impaired wound healing. Diabetes 2005; 54 : 1543-1551.
3. Ahmed N. Advanced glycation endproducts-role in pathology of diabetic complications. Diabetes Res Clin Pract 2005; 67 : 3-21.
4. Arana V, Paz Y, Gonzalez A et al. Healing of diabetic foot ulcers in L-arginine-treated patients. Biomed Pharmacother 2004; 58 : 588-597.
5. Komesu MC, Tanga MB, Buttros KR et al. Effects of acute diabetes on rat cutaneous wound healing. Pathophysiology 2004; 11 : 63-67.
6. Graf J, Neusel E, Schneider E et al. Intra-articular treatment with HA in osteoarthritis of the knee joint: a controlled clinical trial versus mucopolysaccharide polysulfuric acid ester. Clin Exp Rheumatol 1993;11 : 367-373.
7. Balazs EA, Watson D, Duff IF et al. Hyaluronic acid in synovial fluid: I: molecular parameters of hyaluronic acid in normal and arthritic human fluids. Arthritis Rheum 1967; 10 : 357-376.
8. Toole BP, Gross J. The extracellular matrix of the regenerating newt limb: synthesis and removal of hyaluronate prior to differentiation. Dev Biol 1971; 25 : 57-77.
9. West DC, Hampson IN, Arnold F et al. Angiogenesis induced by degradation products of hyaluronic acid. Science 1985; 228 : 1324-1326.
10. Chen WYJ, Abatangelo G. Functions of hyaluronan in wound repair. Wound Repair Regen 2000; 7 : 79-89.
11. McKee CM, Penno MB, Cowman M et al. Hyaluronan (HA) fragments induce chemokine gene expression in alveolar macrophages: the role of HA size and CD-44. J Clin Invest 1996; 98 : 2403-2413.
12. Takahashi K, Takeuchi J, Takahashi T et al. Effects of sodium hyaluronate on epithelial healing of the vesical mucosa and vesical fibrosis in rabbits with acetic acid induced cystitis. J Urol 2001; 166 : 710-713.
13. Ishima M, Wada Y, Sonoda M et al. Effects of hyaluronan on the healing of rabbit meniscus injured in the peripheral region. J Orthop Sci 2000; 5 : 579-584.
14. Gomez S, Herreras JM, Merayo J et al. Effect of hyaluronic acid on corneal haze in a photorefractive keratectomy experimental model. J Refract Surg 2001; 17 : 549-554.
15. Edmonds M, Bates M, Doxford M et al. New treatments in ulcer healing and wound infection. Diabetes Metab Res Rev 2000; 16(Suppl 1): S51-S54.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2006 Issue 5-
All articles in this issue
- Nemocniční nákazy a diabetes
- Diabetes mellitus a imunizace
- Úloha diabetologa při infekčním onemocnění diabetika
- Patogeneze postižení pojivové tkáně při diabetes mellitus
- Metabolické jaderné receptory PPAR a kůže
- Kožní změny při diabetu z pohledu dermatologa
- Hojení kožních afekcí u syndromu diabetické nohy při hospitalizaci
- Infekce a syndrom diabetické nohy v terénní praxi
- Komplex hyaluronanu a jodu - Hyiodine® - nová metoda při terapii diabetických defektů
- Uroinfekce u diabetiků
- Respirační infekce a terapie inhalačním inzulinem
- Metabolizmus glukózy a účinky inzulinu v sepsi
- Kožní projevy hyperlipidemie u diabetiků z pohledu internisty
- Mykózy a diabetes
- Kožní komplikace terapie diabetes mellitus
- Difuzní idiopatická skeletální hyperostóza a souvislost s metabolickými parametry
- Revmatologické manifestace při diabetes mellitus
- Metabolické kostní choroby a diabetes
- Dna a diabetes
- Glukokortikoidy a diabetes mellitus
- Anagrelid v léčbě esenciální trombocytemie a dalších myeloproliferací s trombocytemií sledovaných v registru pacientů v ČR
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Kožní změny při diabetu z pohledu dermatologa
- Glukokortikoidy a diabetes mellitus
- Difuzní idiopatická skeletální hyperostóza a souvislost s metabolickými parametry
- Kožní komplikace terapie diabetes mellitus
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

