-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Diagnostika a léčba komunitní pneumonie dospělých
Autoři: V. Kolek; M. Kolář
; V. Kašák; J. Beneš; J. Dindoš
Působiště autorů: Česká pneumologická a ftizeologická společnost České lékařské společnosti J. E. Purkyně, Společnost infekčního lékařství České lékařské společnosti J. E. Purkyně
Vyšlo v časopise: Vnitř Lék 2011; 57(10): 858-866
Kategorie: Doporučené postupy
Klinické doporučení se týká odborností: 205 – pneumologie a ftizeologie, 001 – praktický lékař pro dospělé, 101 – interní lékařství, 203 – infekční lékařství, 206 – klinická farmakologie, 802 – lékařská mikrobiologie.
Definice
Pneumonie je akutní zánět v oblasti respiračních bronchiolů, alveolárních struktur a plicního intersticia. Klinicky je stav definován jako nález čerstvého infiltrátu na skiagramu hrudníku spolu s nejméně 2 příznaky infekce respiračního traktu (nejčastěji kašel, dále dušnost, bolest na hrudníku, horečka a poslechový nález).
Komunitní pneumonie (CAP) vznikají při běžném životním styku, mimo nemocniční prostředí a bez vztahu k zdravotnickým výkonům. Způsobují je běžné patogeny, zpravidla citlivé na antimikrobiální léky.
Kromě komunitních pneumonií rozeznáváme ještě pneumonie nozokomiální (HAP), pneumonie vázané na zdravotnická zařízení (HCAP), ventilátorové pneumonie (VAP) a pneumonie u imunokompromitovaných jedinců (PIIH).
Etiologie
Nejčastějšími původci CAP v našich podmínkách jsou Streptococcus pneumoniae, Mycoplasma pneumoniae, Chlamydophila pneumoniae a Haemophilus influenzae, mohou to být i Moraxella (Branhamella) catarrhalis, Staphylococcus aureus a také různé viry, včetně viru chřipky. U starších osob a u osob s přidruženými nemocemi jsou záněty plic častěji vyvolané i dalšími gramnegativními bakteriemi (Klebsiella pneumoniae, Legionella pneumophila, Escherichia coli, vzácněji Pseudomonas aeruginosa). Zvláštní problematiku mají pneumonie aspirační (patogeny jsou anaerobní a mikroaerofilní bakterie z dutiny ústní, enterobakterie nebo i Staphylococcus aureus) a tuberkulózní. Vysloveně vzácnými agens jsou Chlamydophila psittaci a Coxiella burnetii.
Klasifikace onemocnění
V poslední době se v péči o nemocné upřednostňují praktické aspekty hodnotící závažnost pneumonie ve vztahu k celkovému stavu pacienta a jeho rizikovým faktorům. Tyto aspekty pak spolu s typem „pravděpodobného“ agens určují způsob léčby, která může být empirická nebo cílená, ambulantní nebo formou hospitalizace, popřípadě i na jednotce intenzivní péče. Takto jsou definovány pneumonie lehká, středně těžká a těžká.
Většina etiologických agens vytváří podobný klinický obraz, proto byly zavrženy termíny typická a atypická pneumonie, které se snažily charakterizovat klinické příznaky podle různých etiologických agens. Z mikrobiologického hlediska se nadále používá termín typické agens pro klasické bakterie [nejčastěji Streptococcus pneumoniae, Haemophilus influenzae, Moraxella (Branhamella) catarrhalis aj.] a atypické agens pro bakterie obtížně kultivovatelné, závislé na hostitelské buňce (nejčastěji Mycoplasma pneumoniae, Chlamydophila pneumoniae, event. Legionella pneumophila), v širším pojetí i viry.
Specifickou problematiku mají vedle komunitních pneumonií (CAP) pneumonie nozokomiální (HAP), pneumonie u imunokompromitovaných jedinců (PIIH), pneumonie vázané na zdravotnická zařízení (HCAP) nebo ventilátorové pneumonie (VAP).
Diagnózy podle MKN 10: J 11.0, J 12.0–9, J 13, J 14, J 15.0–9, J 16.0, J 16.8, J 17.0–8, J 18.0–9, J 69.0–3, J 85.0–3, J 86.0, J 86.9, J 90, J 91, J 96.0, J 96.1, J 96.9.
Epidemiologické charakteristiky onemocnění
Pneumonie je nejčastější plicní infekční onemocnění, jehož mortalita zásadně neklesá ani v době stále účinnějších antibiotik. V rozvinutých zemích je pneumonie nejčastější infekční příčinou smrti. V ČR roční incidence pneumonie přesahuje 100 000 případů, přes 20 000 osob je hospitalizováno a 3 000 na pneumonii zemře. V celosvětovém měřítku jsou pneumonie 3. nejčastější příčinou mortality, umírá 3 až 5 milionů lidí ročně. Častější výskyt pneumonie bývá v dětství do 5 let života a potom ve stáří, dále u kuřáků a nemocných závislých na alkoholu a jiných návykových látkách. Větší riziko vzniku je u nemocných s vleklým onemocněním respiračního a kardiálního ústrojí (městnavé srdeční selhávání), cerebrovaskulárním onemocněním či renálním selháváním, u diabetiků a u nemocných s malignitou a dalšími poruchami imunity, včetně iatrogenně navozené (imunosupresiva, chemoterapie, biologická terapie). Specifickým rizikovým faktorem je mentální postižení.
Kvalifikační předpoklady
- Lehká (nekomplikovaná) pneumonie je obvykle léčena praktickými lékaři nebo ambulantními pneumology a internisty.
- Závažnější stavy ošetřují pneumologové, internisté nebo infektologové a jiní odborní lékaři na lůžkových odděleních.
- Těžké pneumonie vyžadují hospitalizaci na jednotkách intenzivní péče nebo oddělení ARIM. Zvláště specializované jsou jednotky intenzivní péče při pneumologických a infektologických pracovištích.
- Některé komplikace pneumonií vyžadují interdisciplinární přístup s účastí chirurga, kardiologa nebo ortopeda.
- Biochemická, hematologická a mikrobiologická vyšetření provádějí příslušná oddělení laboratorního komplementu.
- Výběr vhodného antimikrobiálního léku konzultují antibiotická centra.
- Radiologická vyšetření provádějí a hodnotí radiologové a pneumologové.
- Endoskopická vyšetření provádějí pneumologové s bronchologickou erudicí.
- Spirometrická vyšetření screeningového typu mohou provádět vyškolení praktičtí lékaři nebo internisté, komplexní funkční diagnostiku plic provádějí pneumologové.
- Lázeňskou léčbu poskytují pacientům s těžkým průběhem onemocnění zařízení vyčleněná přílohou současně platné novelizace Zdravotního řádu.
Technické a personální předpoklady
Technické, personální, hygienické a bezpečnostní požadavky ambulancí, standardních lůžkových zařízení pro poskytování akutní péče a jednotek intenzivní péče; mikrobiologická a biochemická laboratoř; radiodiagnostické, bronchologické a spirometrické pracoviště. Rozsah požadavků v konkrétním případě je dán závažností nemocí (viz výše).
Vstupní podmínky procesu péče
Anamnéza a základní příznaky
V anamnéze hraje důležitou roli údaj o cestování a o stavu imunity, výskyt infekčních nemocí v rodině, kontakt s nemocnými zvířaty a předchozí hospitalizace nebo medikace antibiotik. Typickými příznaky CAP jsou horečky, někdy spojené s třesavkou a zimnicí, u starších nemocných se zmateností. Vzestup tělesné teploty však může být i pozvolný, se zvyšujícími se subfebriliemi po předchozím zánětu horních cest dýchacích. Kašel může být suchý nebo s expektorací různé kvality a kvantity, včetně hemoptýzy, pleurální bolest a dušnost mohou být různého stupně v závislosti na rozsahu infiltrace. Poslechovým nálezem jsou chrůpky, trubicové, kompresivní nebo oslabené dýchání, může být slyšet krepitus. Poklep bývá ztemnělý v oblasti výpotku, nad ním může být bubínkový. RTG obrazem je typicky různě rozsáhlá a různě homogenní infiltrace nebo retikulonodulace. Výpotek bývá volně uložený, někdy může být ohraničený, uložený interlobárně nebo subpulmonálně. Jako průvodní jev u pneumokokové pneumonie se vyskytuje herpes labialis. V rámci celkových projevů se objevují bolesti hlavy, svalů a kloubů, nauzea, zvracení a pocity slabosti. Laboratorně může být přítomna leukocytóza s posunem doleva v diferenciálním rozpočtu krevního obrazu, pravidlem je zvýšená sedimentace erytrocytů a vyšší koncentrace CRP (event. prokalcitoninu) v séru. Vyvolávající agens pneumonie bývá rozpoznáno nanejvýš v 50 % případů. V současnosti stoupá vliv mykoplasmových, chlamydiových a virových pneumonií, jejichž podíl dosahuje více než 30 %, část infekcí je smíšená (2–20 %, dle různých publikovaných studií).
Možné komplikace
Mezi plicní komplikace patří pleuritida, empyém, plicní absces, plicní gangréna, ARDS (syndrom akutní dechové tísně), atelektáza a následné bronchiektazie. Mimoplicní komplikace vznikají nejčastěji zanesením původců krví do vzdálených orgánů, mohou však být i důsledkem imunopatologické reakce. Pneumonie může být provázena artritidou, otitidou, nefritidou, endokarditidou, meningitidou, peritonitidou a také sepsí a septickým šokem. Po pneumonii mohou přetrvávat trvalé funkční poruchy i morfologické změny.
Vstupní kritéria pacienta
Vstupní kritéria hodnotí základní skupiny pro posouzení rizika mortality. Pro tyto potřeby bylo vytvořeno několik kritérií, z nichž se nejvíce používají 3: britská CURB, německá CRB-65 a americké hodnocení PSI (Pneumonia Severity Index) dle Fineho.
Pro ambulantní rozhodování je jednodušší škála Britské hrudní společností (BTS), tzv. systém CURB, který hodnotí stav vědomí (zmatenost), renálních funkcí (urea nad 7 mmol/l), základní projevy respirace (dechová frekvence nad 30/min) a hodnoty krevního tlaku (systola pod 90 mm Hg, diastola od 60 mm Hg). Za každý uvedený znak se přiděluje bod a hodnocením takto vzniklé šestistupňové škály stoupá mortalita pneumonie od 0,7 % (při stupni 0) ke 40 % (tab. 1).
Tab. 1. Britský systém určování rizika mortality – CURB. 
Německý systém zcela eliminuje potřebu laboratorních vyšetření, když místo hodnoty močoviny používá věkový parametr. Hodnotou rizika je věk nad 65 let. Tento systém je standardně používán v německých nemocnicích napojených na síť CAPNETZ (tab. 2).
Tab. 2. Německý systém určování rizika mortality – CRB-65. 
Systém PSI Americké hrudní společnosti (ATS) je pokládán za nejpropracovanější z hlediska hodnocení rizika mortality u hospitalizovaných nemocných s pneumonií. Nemocní jsou zařazování do skupin dle počtu rizikových bodů, které se přidělují dle specifikovaných kritérií (tab. 3). Skupin dle propočteného rizika mortality je 5. Skupiny také určují způsob léčby (ambulantní, formou hospitalizace, event. hospitalizace na JIP). Nemocným bez komorbidity ve věku do 50 let nejsou přidělovány rizikové body a jejich očekávaná mortalita je velmi nízká (0,1 %). Od 50 let věku již přibývá rizikových faktorů, každý rok znamená nárůst o 1 bod, u žen se rizikovost počítá až od 55 let. Po připočtení dalších rizikových bodů je pak ve skupině V riziko mortality již 29,2 % (tab. 4).
Tab. 3. Riziková kritéria dle systému PSI (USA). 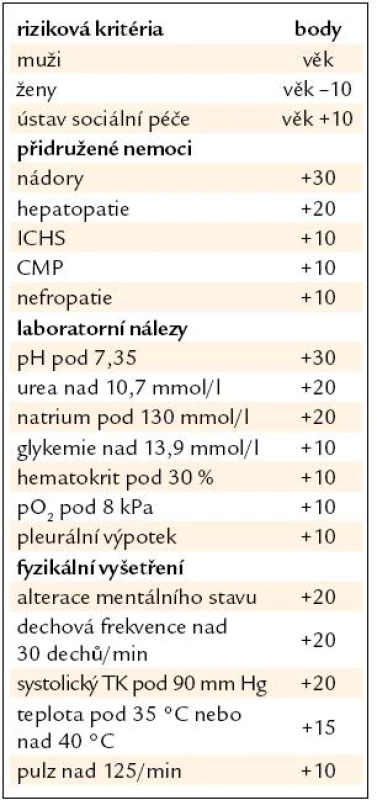
Tab. 4. Rizikové skupiny dle PSI systému. 
U nerizikových pacientů (skupina I) je zásadním požadavkem urychlené podaní antibiotika v ambulantní péči. Pokud je to možné, mělo by se i u těchto lehkých pneumonií odebrat sputum na mikroskopické a kultivační vyšetření.
Ve skupině II a III mohou být starší pacienti nebo nemocní s vážnějšími příznaky a komorbiditou. U nich se doporučuje ambulantně zahájit antibiotickou léčbu, ale předpokládá se další kontakt nebo vyšetření do 48–72 hod. I zde je vhodné provést vyšetření sputa, při kontrole pak laboratorní vyšetření dle přidružených nemocí. Je-li 3. den stav uspokojivý, pokračuje se v ambulantním způsobu léčby. Při zhoršení celkového stavu je možné vyměnit antibiotikum nebo hospitalizovat. Při rozvaze o hospitalizaci u středně těžké pneumonie je vhodné provést kultivaci krve.
Skupinu IV a V tvoří vysoce rizikoví nemocní, u nichž je hospitalizace nutná. Umístění na JIP vyžadují pacienti se závažnou respirační insuficiencí, poruchou vědomí, s příznaky šoku a metabolickým rozvratem. Zvláštní péči vyžadují nemocní s prokázanou bakteriemií, příznaky sepse nebo jinými komplikacemi.
Kritéria těžké pneumonie byla vypracována jako samostatná klinická doporučení. Při rozhodování o přijetí konkrétního pacienta rozhoduje také jeho sociální a adaptační status.
Kritéria těžké pneumonie – umístění na JIP
Malá kritéria (přítomnost aspoň 2 z následujících znaků): dechová frekvence nad 30/min, PaO2/FiO2 pod 250, hypotenze (systola pod 90 mm Hg, diastola pod 60 mmHg), RTG nález bilaterálně, RTG nález ve více než 2 lalocích.
Velká kritéria (stačí jeden znak): potřeba umělé ventilace, nárůst infiltrace na RTG plic o 50 % během 48 hod při klinickém horšení, nutnost podávání vazopresorů déle než 4 hod (septický šok), kreatinin séra nad 177 μmol/l nebo zhoršení renálního selhání.
Partneři prvního kontaktu: LSPP, praktický lékař, pneumolog, infektolog, ZZS, lékaři urgentních příjmů a oddělení ARIM.
Formy prevence: očkování proti chřipce a proti pneumokokovým infekcím.
Vlastní proces péče
Základní vyšetření:
- anamnéza,
- fyzikální vyšetření,
- sedimentace erytrocytů, CRP v séru,
- krevní obraz, diferenciální rozpočet leukocytů,
- močovina, kreatinin, jaterní testy,
- vyšetření saturace hemoglobinu kyslíkem (pulzní oxymetrie),
- skiagram hrudníku ve dvou projekcích (zadopřední a boční),
- mikrobiologické vyšetření, v závislosti na příznacích nemoci (viz níže).
Poznámka: Za nutné minimum lze považovat anamnézu, fyzikální vyšetření a skiagram hrudníku. Pulzní oxymetrie se provádí na příjmových odděleních lůžkových zařízení.
Doplňkové vyšetření:
- výpočetní tomografie plic,
- bronchoskopie s bronchoalveolární laváží,
- funkční vyšetření plic,
- vyšetření respirace (krevní plyny, acidobazická rovnováha),
- vyšetření prokalcitoninu v séru,
- EKG,
- imunologické vyšetření při podezření na stav s primárním nebo sekundárním oslabením imunity pacienta.
Mikrobiologické vyšetření
Použití níže uvedených vyšetření závisí na klinických projevech nemoci, tíži celkového stavu nemocného a na epidemiologických souvislostech. V úvahu připadá zejména:
- mikroskopické a kultivační vyšetření sputa (při expektoraci),
- hemokultivace (zejména při náhle vzniklé těžší pneumonii),
- detekce antigenů legionel a pneumokoků v moči,
- vyšetření pleurálního výpotku (pokud je přítomen),
- vyšetření bronchoalveolární tekutiny nebo plicní tkáně (při použití invazivní diagnostiky),
- sérologické vyšetření (při podezření na špatně kultivovatelné patogeny jako příčinu nemoci),
- molekulární a genetické metody (ve zvláštních případech, viz níže).
Odběr sputa má smysl u nemocných se zřetelnou expektorací. Speciální barvení (dle Ziehl-Neelsena) a kultivace jsou nezbytné k průkazu mykobakterií, imunofluorescenční techniky se používají k průkazu virů nebo legionel. Při posuzování výsledků je nutné zvažovat možnost kontaminace sputa v dutině ústní. Materiál by měl být pokud možno odebrán před zahájením antibiotické léčby, jinak může poskytovat falešně negativní nebo zkreslené výsledky.
Kultivace krve se provádí při podezření na bakteriemii (horečky provázené třesavkou) a u hospitalizovaných pacientů, nejlépe 2–3krát při vzestupu teplot.
Sérologicky se v krvi mohou prokazovat specifické IgM, IgA a IgG protilátky proti respiračním virům, Chlamydophila pneumoniae, Chlamydophila psittaci, Mycoplasma pneumoniae, Legionella sp. a Coxiella burnetii. Protilátky typu IgM mohou být prokazatelné koncem 2. týdne nemoci, k vzestupu IgG protilátek obvykle dochází za 4–6 týdnů od začátku nemoci. Jedno vyšetření zpravidla nestačí k určení etiologie, je nutné sledovat dynamiku hladin protilátek. Provádějí se párové nebo vícenásobné odběry, ve vzájemném odstupu 2–4 týdnů. Přetrvávání vysokých titrů má velký rozptyl. Sérologické vyšetření nemá vliv na iniciální léčbu.
Antigeny legionel a pneumokoků lze detekovat v moči, je však třeba brát v úvahu, že tato metoda detekuje jen nejčastěji se vyskytující sérovary.
Molekulárně genetické metody (na principu PCR) se uplatňují především při diagnostice pomalu rostoucích nebo špatně kultivovatelných patogenů, např. mykobakterií, chřipkového viru, legionel nebo mykotických patogenů včetně Pneumocystis jiroveci.
Pleurální výpotek se získává punkcí pohrudniční dutiny. Jeho kultivační vyšetření má význam především před podáním antibiotik. Cytologicky je parapneumonický výpotek charakterizován výskytem neutrofilních leukocytů. Hustý, někdy zapáchající výpotek hnisavého vzhledu se nachází u empyému.
Cílené odběry se u závažných stavů získávají pomocí kartáčkové biopsie, bronchoalveolární laváže nebo transparietální punkce plic tenkou jehlou. Tracheální punkce nebo punkce plic se provádějí jen na některých pracovištích. Při diferenciálně diagnostických potížích je někdy třeba provést chirurgickou plicní biopsii.
Diagnostika pneumonie je samozřejmě jiná při ambulantní činnosti, kdy se provádí základní klinické vyšetření, skiagram hrudníku a event. vyšetření sputa, než při hospitalizaci s použitím široké škály doplňujících vyšetření.
Diferenciální diagnostika
Příznaky podobné pneumonii mohou vyvolat i jiné nemoci, např. plicní karcinom, tuberkulóza, plicní embolie, septické embolizace při pravostranné infekční endokarditidě nebo levostranná kardiální insuficience.
Pro odlišení je třeba zvážit anamnestické údaje, rychlost nástupu potíží, charakter teplot a celkové projevy onemocnění. Je třeba řádně zhodnotit radiologické nálezy a správně posoudit účinek antimikrobní léčby. Při pochybnostech o diagnóze pneumonie a při neadekvátní reakci na léčbu je nutné indikovat bronchoskopii při podezření na karcinom plic, mikrobiologická vyšetření na průkaz mykobakterií a tuberkulinový kožní test při podezření na tuberkulózu, perfuzní a ventilační scintigrafii plic, angioCT, EKG, NT-pro BNP a další kardiologická vyšetření při úvahách o plicní embolii nebo jiném kardiovaskulárním onemocnění.
Prognóza
Prognóza je dána uvedenými věkovými a jinými rizikovými faktory a dále přítomností bakteriemie. Výrazně se zhoršuje u polymorbidních nemocných, především s malignitou.
Léčba
Ambulantní léčba
Protiinfekční léčba – ambulantně se iniciálně podávají antimikrobní léky zásadně empiricky. Interval od kontaktu s lékařem k nasazení léku by neměl být delší než 8 hod. Pokud je to možné, lze provést odběr na mikrobiologické vyšetření (sputum na mikroskopické a kultivační vyšetření) a následně usměrnit léčbu cíleně, je-li to nutné. V případě přetrvávání potíží při léčbě je vhodná další návštěva pacienta doma nebo vyšetření v ordinaci po 2–4 dnech, kdy lze opakovat mikrobiologické testy nebo vyšetřit zánětlivé markery (krevní obraz nebo CRP) a event. vyměnit antimikrobní lék za lék jiné terapeutické skupiny (tab. 5).
Tab. 5. Antibakteriální léky doporučené u empirické ambulantní léčby komunitní pneumonie podle posledních zahraničních konsenzů. 
Protiinfekční léčba trvá 7–10 dnů u typických agens, minimálně 10–14 dnů u atypických agens a až 21 dnů u infekce legionelami. V poslední době se léčba zkracuje a byly publikovány i studie o ekvivalenci účinku při podávání některých makrolidů (azitromycin) v délce 3–5 dnů, kdy se v plicní tkáni vytvoří terapeutické hladiny na dobu minimálně 10 dnů.
Doplňková léčba – podávají se antitusika a analgetika při pleurální bolesti. Důležitý je dostatečný přísun tekutin, kalorií a vitaminů. Význam podávání mukolytik dle charakteru kašle a bronchodilatancií při dušnosti je sporný.
Kontrolní ambulantní vyšetření se má provést nejpozději 2 týdny od zahájení léčby. Po 6 týdnech je možné provést kontrolní skiagram hrudníku a fyzikální vyšetření. Opakovat laboratorní vyšetření má smysl v případě zjištění odchylek od normy při vzniku nemoci nebo při zhoršení stavu pacienta. Základní spirometrické vyšetření je přínosné po závažnějším průběhu pneumonie nebo při existenci jiné plicní nemoci. Při zjištění ventilační poruchy je nutné doplnit základní spirometrii komplexním vyšetřením plicních funkcí.
Léčba hospitalizovaných nemocných
Protiinfekční léčba – u závažných infekcí (viz výše) je nutné nemocného hospitalizovat a urychleně podat empiricky antibiotika. Antibiotická léčba by měla být zahájena do 2–4 hod od začátku hospitalizace. Je vhodné učinit maximum pro určení patogenu a na základě cílených odběrů usměrnit iniciální antimikrobiální léčbu. Antibiotika je možné podávat zpočátku intravenózně 2–5 dnů, později perorálně (sekvenční nebo sestupná léčba) podle klinického zlepšení. Doporučuje se iniciální podání kombinace antibiotik. Často je potřebný individuální přístup. Při obvyklém průběhu dochází ke zlepšení celkového stavu a alespoň k částečnému poklesu teplot do 3 dnů. Regrese laboratorních známek může mít prodlevu další 1–2 dny za ústupem celkového dyskomfortu. Prognostický význam má pokles CRP. Poslechový nález přetrvává déle, radiologický nález se může v počáteční fázi i zhoršit a přetrvává až měsíc.
Za optimální je považována kombinace beta-laktamových antibiotik (aminopeniciliny nebo cefalosporiny) s makrolidy. Tato kombinace vykázala na základě více studií zkrácení hospitalizace i snížení mortality. Novější studie ukazují minimálně stejnou účinnost monoterapie respiračními fluorochinolony při zkrácení délky hospitalizace.
Cílové skupiny lze rozdělit na nemocné mladšího věku bez rizikových faktorů, starší nemocné s komorbiditou a nemocné s podezřením na možnost pseudomonádové infekce (tab. 6). U mladších nemocných stačí podat kombinaci makrolidového antibiotika s aminopenicilinem bez inhibitoru beta-laktamáz nebo s cefalosporinem II. generace. U rizikových nemocných (dle Fineho kritérií) je lépe podávat aminopeniciliny spolu s inhibitory beta-laktamáz nebo cefalosporiny III. generace (cefotaxim, ceftriaxon) s makrolidy. Nemocní s rizikem pseudomonádové infekce jsou jedinci s chronickým onemocněním plic (bronchiektaziemi, cystickou fibrózou apod.) často užívající antibiotika, u nichž se už kultivačně Pseudomonas aeruginosa vyskytla. V léčbě těchto nemocných se uplatňují podle výsledků citlivosti fluorochinolony II. generace (ciprofloxacin), aminoglykosidy, piperacilin/tazobaktam, ceftazidim nebo karbapenemy.
Tab. 6. Antibiotika u hospitalizovaných nemocných s CAP. 
U aspirační pneumonie je vhodným lékem klindamycin, linkomycin nebo tigecyklin. U pneumonie vyvolané stafylokoky je lékem volby klindamycin (jedná-li se o citlivý kmen) nebo linezolid.
Doplňková léčba – je vhodná nebulizace, podání antitusik a analgetik, podání nízkomolekulárních heparinů, doplňování tekutin a kalorií infuzemi. Sledují se životní funkce jako krevní tlak, srdeční frekvence, dechová frekvence a saturace periferní krve kyslíkem. Při hypoxemii je indikována oxygenoterapie.
Jak bylo uvedeno, možností je řada, ale přesto nelze každého nemocného ideálně zařadit. Dalšími modifikacemi jsou „neklinická – sociální hospitalizace“, léčba nemocných, kterým bylo již podáno jiné antibiotikum nebo léčba při podezření na aspirační pneumonii.
Pokud je během léčby identifikován patogen vyvolávající pneumonii, je možné přejít na cílenou léčbu – deeskalační terapie (tab. 7).
Tab. 7. Antibiotika doporučená pro cílenou léčbu komunitně získané pneumonie. 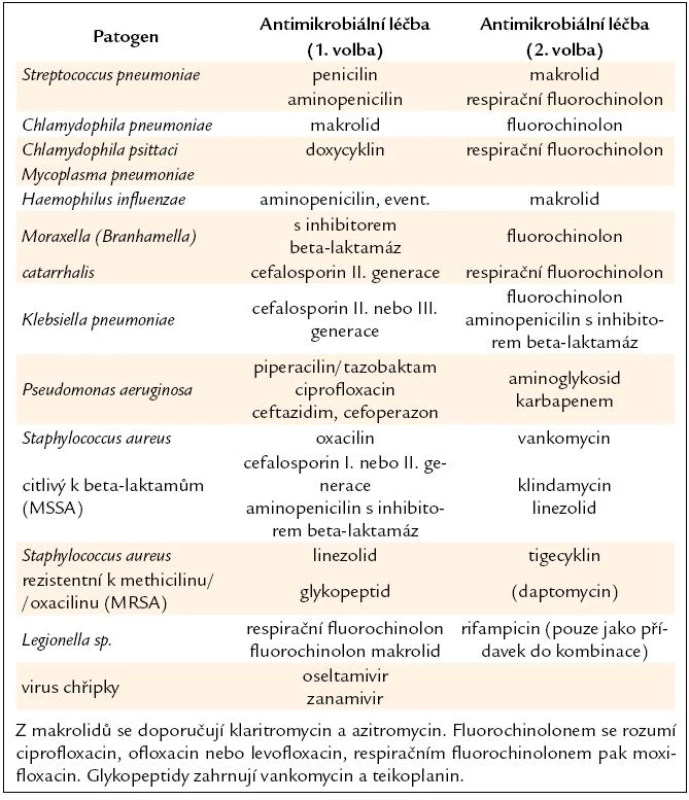
Léčba na JIP nebo na oddělení ARIM
Komplexní léčba spočívá v zajištění průchodnosti dýchacích cest a neinvazivní podpory dýchání, event. intubace a kardiopulmonální resuscitace. Provádí se stálé monitorování životních funkcí (krevní tlak, pulz, dechová frekvence, hodnoty krevních plynů, bilance sérových iontů a tělesných tekutin atd.). Cílená intravenózní léčba antimikrobními léčivy se průběžně vyhodnocuje po konzultacích s antibiotickým střediskem. Důležité je zvlhčování vdechovaného vzduchu a odsávání sekretů z dutiny ústní a u ventilovaných pacientů z dýchacích cest, s event. cílenými odběry na mikrobiologické vyšetření. Doporučuje se profylaxe nízkomolekulárními hepariny. Význam podávání imunoglobulinů, kortikoidů nebo statinů není jednoznačně doložen.
Léčba komplikací
Zánětlivé komplikace je nutné řešit intenzivní antimikrobiální léčbou. Hrudní empyém nebo komplikovaný absces vyžadují evakuační punkci nebo drenáž dutiny pohrudniční. Při neúspěchu této terapie se provádí revize pohrudniční dutiny, případně je provedena dekortikace a pleurektomie. Při rozsáhlé devastaci plicní tkáně se uvažuje o plicní resekci. Mezními chirurgickými přístupy je fenestrace hrudní stěny se zevním hojením empyému či torakoplastika.
Výstupní kritéria pacienta
Kritéria bezpečného propuštění z nemocnice jsou jednoduché znaky, které určují možnost propuštění s minimalizací rizika rehospitalizace nebo pozdního vzniku komplikací. Patří sem normální teplota, normální srdeční a dechová frekvence, stabilizovaný krevní tlak, dostatečná saturace krve kyslíkem, normální stav vědomí, schopnost perorálního příjmu potravy a léků. Optimálně by měl být pacient vyléčen ad integrum. Může přetrvávat funkční porucha dýchání a mohou vznikat následky komplikací a jejich léčby.
Dispenzarizace nemocných a posudková problematika
U nemocných s lehkou formou ambulantně léčené pneumonie stačí jedno kontrolní vyšetření do 2–4 týdnů. Provádí se kontrolní skiagram hrudníku, event. spirometrie, krevní obraz a kontrolní sérologické a biochemické vyšetření. Při přetrvávajících patologických nálezech jsou nutná další pomocná diferenciálně diagnostická vyšetření. Dechová gymnastika a rekondice se může doplnit lázeňskou léčbou u komplikovaných a recidivujících pneumonií, zvláště u pacientů s následnou funkční poruchou ventilace. Těžké funkční poruchy vedou k invalidizaci (obr. 1).
Obr. 1. Vývojový diagram. Komunitně získaná pneumonie u dospělých. 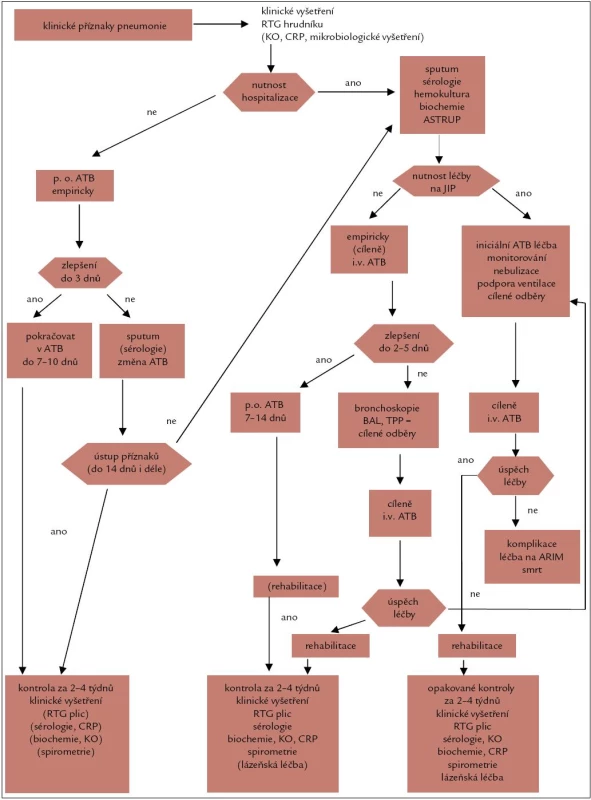
U všech komplikovaných a recidivujících pneumonií je třeba vyloučit jiné základní onemocnění, jako je karcinom plic, imunitní defekt, embolizace, bronchiektazie a jiné. U nemocných, kteří byli intubováni déle než 7 dnů, a/nebo při známkách tracheální stenózy se doporučuje kontrolní bronchoskopie do 3 měsíců k vyloučení postintubační stenózy.
Ekonomická a etická problematika
Důležité je časné stanovení správné diagnózy a co nejrychlejší zahájení antimikrobiální léčby. Tento postup snižuje počty nutných hospitalizací, které tvoří 90 % celkových léčebných nákladů u komunitně získaných pneumonií a celkem asi 10 % nákladů na celkovou nemocniční péči. Sociální dopad mají pneumonie u starších lidí, např. v domovech sociální péče nebo léčebnách pro dlouhodobě nemocné. U ležících nemocných jsou často příčinou smrti. Při volbě antibiotik je třeba vzít v úvahu epidemiologickou bezpečnost s ohledem na možnost vzniku a šíření rezistence.
Použité zkratky
- ARDS (adult respiratory distress syndrome) – syndrom akutní dechové tísně
- ARIM – oddělení anestezie, resuscitace a intenzivní medicíny
- CAP (community-acquired pneumonia) – komunitní pneumonie
- HAP (hospital-acquired pneumonia) – nozokomiální pneumonie
- HCAP (health care-associated pneumonia) – pneumonie vázaná na zdravotnická zařízení
- CHOPN – chronická obstrukční plicní nemoc
- JIP – jednotka intenzivní péče
- NT-proBNP – natriuretický protein
- PIIH (pneumonia in immunocompromised host) – pneumonie u imunokompromitovaných jedinců
- PCR (polymerase chain reaction) – polymerázová řetězová reakce
- VAP (ventilator-associated pneumonia) – ventilátorová pneumonie
prof. MUDr. Vítězslav Kolek, CSc.
www.fnol.cz
e-mail: vitezslav.kolek@fnol.cz
Doručeno do redakce: 21. 3. 2011
Zdroje
1. Kolek V. Pneumonie – diagnostika a léčba. Praha: Triton 2003.
2. Niederman MS, McCombs JS, Unger AN et al. The cost of treating community-acquired pneumonia. Clin Ther 1998; 20 : 820–837.
3. Guest JF, Morris A. Community-acquired pneumonia: the annual cost to the National Health Service in the United Kingdom. Eur Respir J 1997; 10 : 1530–1534.
4. Loddenkemper R. European Lung WhiteBook. Charlesworth Gr.: Huddersfield 2004.
5. File TM. Community-acquired pneumonia. Lancet 2003; 362 : 1991–2001.
6. Barlow GD, Lamping DL, Davey PG et al. Evaluation of outcomes in community-acquired pneumonia: a guide for patients, physicians, and policy-makers. Lancet Infect Dis 2003; 3 : 476–488.
7. Woodhead M, Blasi F, Ewig S et al. European Respiratory Society; European Society of Clinical Microbiology and Infectious Diseases. Guidelines for management of adult lower respiratory trect infections. Eur Respir J 2005; 26 : 1138–1180.
8. Mandell LA, Bartlett JG, Dowell FS et al. Infectious Diseases Society of America. Update of practice quidelines for the management of community-acquired pneumonia in immunocompetent adults. Clin Infect Dis 2003; 37 : 1405–1433.
9. Macfarlane JT, Boldy D. 2004 update of BTS pneumonia guidelines: What’s new? Thorax 2004; 59 : 364–366.
10. Kolek V. Standard diagnostiky a léčby komunitně získané pneumonie dospělých. Bulletin ČPFS 1995; 5 : 9–12.
11. Dean NC, Silver MP, Bateman KA et al. Decreased mortality after implementation of a treatment guideline for community-acquired pneumonia. Am J Med 2001; 110 : 451–457.
12. Martinez JA, Horcajada JP, Almela M et al. Addition of a macrolide to a b-lactam-based empirical antibiotic regimen is associated with lower in-hospital mortality for patients with bacteraemic pneumococcal pneumonia. Clin Infect Dis 2003; 36 : 385–395.
13. Gleason PP, Meehan TP, Fine JM et al. Associations between initial antimicrobial therapy and medical outcomes for hospitalized elderly patients with pneumonia. Arch Int Med 1999; 159 : 2561–2572.
14. Kolek V, Fila L, Fojtů H et al. Pneumonie vyžadující hospitalizaci: výsledky dvouleté multicentrické studie v České republice. Int Med Prax 2003; 7 : 347–352.
15. de Roux A, Ewig S, García E et al. Mixed community-acquired pneumonia in hospitalised patients. Eur Respir J 2006; 27 : 795–800.
16. File TM Jr, Plouffe JF Jr, Breiman RF et al. Clinical Characteristics of Chlamydia pneumoniae infection as the sole cause of community-Acquired Pneumonia. Clin Infect Dis 1999; 29 : 426–428.
17. File TM Jr, Tan JS. International guidelines for the treatment of community – acquired pneumonia in adults. The role of macrolides. Drugs 2003; 63 : 181–205.
18. Koivula I, Stén M, Mäkelä PH. Prognosis after community-acquired pneumonia in the elderly: a population-based 12 year follow-up study. Arch Int Med 1999; 159 : 1550–1555.
19. Metlay JP, Atlas SJ, Borowsky LH et al. Time course of symptom resolution in patients with community-acquired pneumonia. Respir Med 1998; 92 : 1137–1142.
20. Halm EA, Fine MJ, Kapoor WN et al. Instability on hospital discharge and the risk of adverse outcomes in patients with pneumonia. Arch Intern Med 2002; 162 : 1278–1284.
21. Fine MJ, Smith MA, Carson CA et al. Prognosis and outcomes of patients with community-acquired pneumonia. A meta-analysis. JAMA 1996; 275 : 134–141.
22. Lim WS, van der Eerden MM, Laing R et al. Defining community acquired pneumonia severity on presentation to hospital: an international derivation and validation study. Thorax 2003; 58 : 377–382.
23. Rhew DC, Tu GS, Ofman J et al. Early switch and early discharge strategies in patients with community-acquired pneumonia: a meta-analysis. Arch Intern Med 2001; 161 : 722–727.
24. Waterer GW, Somes GW, Wunder-rink RG. Monotherapy may be suboptimal for severe bacteraemic pneumococcal pneumonia. Arch Intern Med 2001; 161 : 1837–1842.
25. Ewig S, Ruiz M, Torres A et al. Pneumonia acquired in the community through drug-resistant Streptococcus pneumoniae. Am J Respir Crit Care Med 1999; 159 : 1835–1842.
26. Ho PL, Tse WS, Tsang KW et al. Risk factors for acquisition of levofloxacin-resistant Streptococcus pneumoniae: A case-control study. Clin Inf Dis 2001; 32 : 701–707.
27. Kolář M, Urbánek K, Čekanová L. Podklady pro racionální antibiotickou léčbu komunitních bakteriálních infekcí. Klin Farmakol Farmac 2003; 17 : 22–24.
28. Kolář M. Komunitní pneumonie z pohledu mikrobiologa. Stud Pneumol Phthiseol 2003; 63 : 164–167.
29. Capelastequi A, España PP, Quintana JM et al. Validation of a predictive rule for the management of community-acquired pneumonia. Eur Respir J 2006; 27 : 151–157.
30. Mandell LA, Wunderink RG, Anzueto A et al. Infectious Diseases Society of America. American Thoracic Society. Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults. Clin Infect Dis 2007; 44 (Suppl 2): S27–S72.
31. Kolek V, Kašák V, Skřičková J et al. Pneumologie: Vybrané kapitoly pro praxi. Praha: Maxdorf Jessenius 2010.
32. Woodhead M, Blasi F, Ewig S et al. European Society of Clinical Microbiology and Infectious Diseases. Guidelines for management of adult lower respiratory tract infections. Eur Respir J 2005; 26 : 1138–1180.
33. Bukghardt O, Welte T. 10 years’ experience with pneumococcal quinolone moxifloxacin. Expert Rev Anti Infect Ther 2009; 7 : 645–668.
34. Torres A, Muir JF, Corris P et al. Effectiveness of oral moxifloxacin in standard first-line therapy in community-acquired pneumonia. Eur Respir J 2003; 21 : 135–143.
35. Welte T, Petermann W, Schürmann D et al. MOXIRAPID Study Group. Treatment with sequential intravenous or oral moxifloxacin was associated with faster clinical improvement than was standard therapy for hospitalized patients with community-acquired pneumonia who received initial parenteral therapy. Clin Infect Dis 2005; 41 : 1697–1705.
36. Torres A, Garau J, Arvis P et al. MOTIV (MOxifloxacin Treatment IV) Study Group. Moxifloxacin monotherapy is effective in hospitalized patients with community-acquired pneumonia: The MOTIV Study – a randomized clinical trial. Clin Infect Dis 2008; 46 : 1499–1509.
37. Jakubec P, Kolek V, Kolář M. Klinické doporučení diagnostiky a léčby těžké pneumonie. Praha: Dashofer 2009.
38. Kolek V, Kolář M, Kašák V et al. Klinické doporučení diagnostika a léčby komunitní pneumonie dospělých. Praha: Dashofer 2006.
39. Beneš J, Bartošová D, Beran J et al. Infekční lékařství. Praha: Galén 2009.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2011 Číslo 10- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Magnosolv a jeho využití v neurologii
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
- Kritické zhodnocení optimální farmakoterapie u kandidátů srdeční resynchronizační léčby – zkušenosti jednoho centra
- Náklady na rehospitalizaci pacientů s akutním srdečním selháním
- Očkování proti virové hepatitidě B u pacientů s chronickým selháním ledvin – dvacetileté zkušenosti
- Normální hodnoty tlaků v plicním oběhu u zdravých osob v klidu a při cvičení
- Resynchronizačná liečba srdcového zlyhávania – stále veľa otáznikov
- Diagnostický algoritmus synkop: integrativní přístup
- Léčba akutní exacerbace chronické obstrukční plicní nemoci za hospitalizace a na lůžku intenzivní péče
- Úloha centrálneho nervového systému v etiopatogenéze chorôb periférnych orgánov
- Prognostické faktory u chronické lymfocytární leukemie
- Diagnostika a léčba komunitní pneumonie dospělých
- Benígny solitárny vred slepého čreva
- MR dokumentované vymizení infiltrace infundibula hypofýzy u pacientů s histiocytózou z Langerhansových buněk po léčbě 2-chlorodeoxyadenosinem
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Normální hodnoty tlaků v plicním oběhu u zdravých osob v klidu a při cvičení
- Léčba akutní exacerbace chronické obstrukční plicní nemoci za hospitalizace a na lůžku intenzivní péče
- Resynchronizačná liečba srdcového zlyhávania – stále veľa otáznikov
- Prognostické faktory u chronické lymfocytární leukemie
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



