-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaEliminácia rizika prenosu vírusu hepatitídy B transfúziou vo fáze možnej okultnej HBV infekcie
Elimination the risk of hepatitis B virus transfusion-transmitted infection in the phase of possible occult HBV infection
Introduction:
The risk of transfusion transmitted hepatitis B virus currently still exists. The occult hepatitis B virus infection, defined by presence of HBV DNA in the liver tissue (with detectable or undetectable HBV DNA in serum, in absence HBsAg), can by occurs by transmission of hepatitis B virus of blood transfusion. Absence of HBsAg in blood of evidently healthy individuals does not mean absence of circulating hepatitis B virus and blood containing anti-HBc may be infectious, when containing HBV DNA. The source of HBV infection by blood transfusion or by organs can be carrier of the occult hepatitis B virus infection.Material and methods:
Presence of anti-HBc positive HBsAg negative blood donors has been pursued and observed during five-years period in two regions. There were 126 anti-HBc positive and HBsAg negative samples from areas with high prevalence of anti-HBc and higher prevalence HBsAg positivity in comparison in other parts of Slovakia examined for HBV DNA determination. The samples were divided into 4 groups according to the level of anti-HBs antibodies (high, sufficient, insufficient and without anti-HBs). For HBsAg, anti-HBc and anti-HBs were used CMIA ARCHITECT methods, for HBV DNA deternination were used COBAS Ampli/Prep COBAS TaqMan HBV Test version 2.0 and for ALT examination was used GPT/ALT BPC BioSed test.Results:
In region Bratislava has been tested 110.639 samples with positive anti-HBc results in 666 (0,60%) samples and in Dunajská Streda region 11.457 samples with positive anti-HBc results in 198 (1,72%) samples. The highest percentage of anti-HBc positive blood donors in Dunajská Streda region were in 30-50 years. 37 percent of anti-HBc positive blood donors had ALT level higher than reference value and 67% had normal level. In 126 anti-HBc positive and HBsAg negative samples HBV DNA was not detected.Discussion and conclusion:
Examination of anti-HBc in blood donor samples significantly and reliably contributes to elimination of risk of transmission HBV infection in phase of the occult HBV infection with detectable or undetectable (very low levels in donors sera) HBV DNA.Key words:
occult HBV infection, OBI, HBsAg, anti-HBc antibodies, anti-HBs antibodies, HBV DNA, NAT, anti-HBs titer, cccDNA, „only” anti-HBc
Autoři: E. Ščepkinová; J. Gašparovič 1 2
Působiště autorů: Národná transfúzna služba SR, Bratislava 1; Slovenská zdravotnícka univerzita, Národné referenčné centrum pre vírusové hepatitídy, Bratislava 2
Vyšlo v časopise: Transfuze Hematol. dnes,20, 2014, No. 2, p. 67-74.
Kategorie: Souhrnné práce, původní práce, kazuistiky
Souhrn
Úvod:
Riziko transfúziou prenesenej infekcie vírusom hepatitídy B v súčasnej dobe stále existuje. Jednou z možností prenosu je prenos formou okultnej HBV infekcie, ktorá je definovaná ako prítomnosť HBV DNA v pečeňovom tkanive (s jej detekovateľnou alebo nedetekovateľnou hladinou v sére, v neprítomnosti HBsAg). Neprítomnosť HBsAg v krvi zjavne zdravých jedincov nemusí vždy znamenať neprítomnosť cirkulujúceho vírusu hepatitídy B a krv obsahujúca anti-HBc protilátky môže byť infekčná, keď obsahuje HBV DNA. Nosiči okultnej HBV infekcie môžu byť zdrojom prenosu HBV krvnou transfúziou alebo orgánmi.Materiál a metódy:
Bol sledovaný a porovnaný výskyt anti-HBc špecificky reaktívnych (pozitívnych) HBsAg negatívnych darcov krvi za obdobie piatich rokov v dvoch regiónoch. Za účelom zistenia možného výskytu okultnej HBV infekcie bolo 126 anti-HBc pozitívnych a HBsAg negatívnych vzoriek z oblasti s vysokou prevalenciou anti-HBc a z oblasti s vyššou prevalenciou HBsAg pozitivity v porovnaní s inými oblasťami Slovenska vyšetrených na prítomnosť HBV DNA. Vzorky boli rozdelené do štyroch skupín podľa výšky titra anti-HBs protilátok (s vysokým, dostatočným, nedostatočným titrom a bez anti-HBs). Na vyšetrenie HBsAg, anti-HBc a anti-HBs boli použité metódy typu CMIA ARCHITECT, na vyšetrenie HBV DNA bola použitá metóda COBAS Ampli/Prep COBAS TaqMan HBV Test version 2.0. Na vyšetrenie ALT sa použil test GPT/ALT BPC BioSed.Výsledky:
Počas piatich rokov testovania bolo v regióne Bratislava vyšetrených 110 639 odberov, z čoho bolo 666 odberov (0,60 %) anti-HBc pozitívnych a v regióne Dunajská Streda 11 457 odberov z čoho bolo 198 odberov (1,72 %) anti-HBc pozitívnych. Najvyššie percento anti-HBc pozitívnych darcov krvi v regióne Dunajská Streda bolo vo vekovej kategórii 30–50 ročných, 37 % z nich malo hladinu ALT nad referenčnou hodnotou a skupinu anti-HBc pozitívnych darcov s normálnou hladinou ALT v tomto regióne tvorilo 63 %. U žiadnej z vyššie uvedených 126 anti-HBc pozitívnych a HBsAg negatívnych vzoriek vyšetrených na HBV DNA nebola zistená jej prítomnosť.Diskusia a záver:
Zavedenie vyšetrovania anti-HBc protilátok u darcov krvi významne a spoľahlivo prispieva k eliminácii rizika prenosu HBV transfúziou vo fáze možnej okultnej HBV infekcie s detekovateľnou alebo nedetekovateľnou (pri jej veľmi nízkych hladinách v sére) prítomnosťou HBV DNA.Kľúčové slová:
okultná HBV infekcia, OBI, HBsAg, anti-HBc protilátky, anti-HBs protilátky, HBV DNA, NAT, titer anti-HBs, cccDNA, „only” anti-HBcÚvod
Infekcia vírusom hepatitídy B patrí medzi jednu z najčastejších infekcií na svete. Vírus hepatitídy B môže vyvolať jednak akútne ochorenia, ktoré prebiehajú od asymptomatických foriem až po ťažké, niekedy fulminantné hepatitídy, jednak dlhodobé infekcie od relatívne benigného asymptomatického nosičstva až po rýchle progredujúcu chronickú hepatitídu s rizikom vzniku cirhózy pečene alebo hepatocelulárneho karcinómu.
Celosvetovo asi 2 miliardy ľudí je počas života infikovaných vírusom hepatitídy B, pričom počet chronicky infikovaných dosahuje až 350 miliónov (1).
V súčasnej dobe stále existuje aj riziko transfúziou prenesenej infekcie vírusom hepatitídy B.
Prenos sa môže uskutočniť:
- a) vo fáze pre-sérokonverznej „window periódy” (v sére nie sú prítomné žiadne antigény ani protilátky, dá sa ale zistiť DNA vírusu), infektivita krvných komponentov získaných od darcov v tomto štádiu je veľká, častosť prenosu je ale veľmi nízka (2).
- b) formou infekcie s imunovariantnými vírusovými mutantami, ktoré nemusia byť zistené v súčasnej dobe dostupnými screeningovými testami. V transfuziológii sú najvýznamnejšie „surface mutanty” (práve tie nemusia byť zachytené screeningovými testami) (3).
Sú dva spoľahlivé spôsoby na zamedzenie prenosu HBV mutantov: - testovanie anti-HBc (4)
- testovanie NAT (5)
- c) formou okultnej HBV infekcie (je to stav po prekonanej hepatitíde B, kedy je v pečeni a niekedy aj v sére detekované malé množstvo HBV DNA bez detekcie sérového HBsAg). Okultná HBV infekcia je spojená s perzistenciou vírusového genómu v pečeni vo forme cccDNA – kovalentne uzavretej cirkulárnej DNA, ktorá je veľmi stabilná a odolná. Etabluje sa v jadre hepatocytu a integruje sa do genómu hostiteľa s následnou silnou supresiou vírusovej replikácie a génovej expresie (6).
Kompletná eradikácia HBV infekcie pravdepodobne neexistuje a replikácia vírusu môže byť reaktivovaná pri niektorých imunosupresívnych stavoch, kedy sa vymyká spod imunologickej kontroly.
Nosiči HBV infekcie môžu byť zdrojom transmisie krvou alebo orgánmi (7).
Podstata tejto pomerne novej biologickej entity ešte stále nie je objasnená.
Jej najväčší význam spočíva paradoxne nie v hepatológii ale v transfuziológii. Väčšina okultných HBV infekcií je asymptomatických, preto sú len náhodne zisťované screeningovým vyšetrením veľkej populácie (do čoho patrí aj screening darcov krvi).
Prvýkrát bola zistená a pomenovaná pred viac ako 30 rokmi prípadom transfúziou prenesenej HBV infekcie HBsAg negatívnym a anti-HBc „only” pozitívnym darcom (bez anti-HBs protilátok) (8).
Jej definície sa rokmi menili, v roku 2008 bola Európskou asociáciou pre štúdium pečene definovaná ako: prítomnosť HBV DNA v pečeni jedincov (s detekovateľnou alebo nedetekovateľnou hladinou HBV DNA v sére), ktorí sú v súčasnej dobe dostupnými screeningovými testami testovaní ako HBsAg negatívni a definovanou cut-off hodnotou DNA v sére < 200 IU/ml (9, 10).
Na Slovensku sa v roku 2008 začali u darcov krvi vyšetrovať protilátky proti core antigénu vírusu hepatitídy B (anti-HBc) ako ďalší z testov na hepatitídu B, okrem dovtedy používaného vyšetrenia povrchového antigénu vírusu hepatitídy B (HBsAg).
Anti-HBc protilátky indikujú prebiehajúcu alebo odoznetú infekciu vírusom hepatitídy B. Sú zistené v sére krátko po objavení sa povrchového antigénu HBsAg, sú prítomné aj po jeho vymiznutí a pretrvávajú spolu s protilátkami anti-HBs po celý život. Môžu byť jediným sérologickým markerom vírusovej hepatitídy B a potenciálne infekčnej krvi.
Protilátky proti povrchovému antigénu vírusu hepatitídy B (anti-HBs) neutralizujú HBsAg a u jedincov infikovaných vírusom hepatitídy B sa objavujú v sére po vymiznutí HBsAg. Detekcia protilátok anti-HBs spolu s protilátkami anti-HBc u asymptomatických jedincov znamená, že u týchto jedincov prišlo k predchádzajúcemu kontaktu s HBV. Vznikajú tiež po vakcinácii proti hepatitíde B, ich prítomnosť je dôležitá na ochranu pred infekciou vírusom hepatitídy B.
Materiál a metódy
Bol sledovaný a porovnaný výskyt anti-HBc špecificky reaktívnych (pozitívnych), HBsAg negatívnych darcov krvi za obdobie piatich rokov v dvoch regiónoch, pričom v jednom z nich (Dunajská Streda a blízke okolie) nedochádza k vzájomnému miešaniu darcov z iných oblastí. A práve v tomto regióne bolo zistené štatisticky významne odlišné a veľmi vysoké percento anti-HBc pozitívnych jedincov, po príčine ktorého sa pátralo. Boli sledované a vyhodnotené parametre HBsAg, anti-HBc, anti-HBs, ALT a vekové kategórie anti-HBc pozitívnych darcov. 126 anti-HBc pozitívnych a HBsAg negatívnych vzoriek z oblasti Dunajskej Stredy a ďalšej rizikovej oblasti východného Slovenska, (kde je aj vyššia prevalencia HBsAg pozitivity v porovnaní s inými oblasťami Slovenska) bolo vyšetrených na HBV DNA jednotlivo, nie v pooloch.
Metodiky použité na vyšetrovanie sú:
- ARCHITECT HBsAg Qualitative II (ABBOTT)
- ARCHITECT anti-HBc II (ABBOTT)
- ARCHITECT anti-HBs (ABBOTT)
Všetky tieto metodiky patria do typu metodík CMIA (chemiluminiscenčná imunoanalýza na mikročasticiach), kde množstvo antigénu alebo protilátky vo vy-šetrovanej vzorke (ľudská plazma alebo sérum) je priamo úmerné relatívnym svetelným jednotkám (RLU) detekovaných optickým systémom analyzátora ARCHITECT.
Na vyšetrenie ALT sa použil test GPT/ALT (BPC BioSed). Je to kvantitatívna kinetická UV metóda na stanovenie hladiny enzýmu alaninaminotransferázy (ALT) v ľudskom sére alebo plazme. Meranie sa uskutočňuje na plnoautomatickom analyzátore KVADRO.
Na vyšetrenie DNA HBV sa použila metóda COBAS Ampli/Prep COBAS TaqMan HBV Test version 2.0 (ROCHE) založená na princípe stanovenia množstva vírusovej HBV DNA pomocou kvantifikačného štandardu HBV. Amplifikuje nukleové kyseliny na identifikáciu DNA vírusu hepatitídy B v ľudskom sére a plazme. Analyzátor po ukončení amplifikácie vypočíta koncentráciu HBV DNA v testovanej vzorke. Dolná hranica záchytnosti metodiky je 9 IU/ml pre plazmu a 19 IU/mlpre sérum.
Výsledky
Za obdobie piatich rokov bolo spolu vyšetrených v regióne Bratislava 110 639 odberov, z čoho bolo 666 odberov (0,60 %) anti-HBc pozitívnych a v regióne Dunajská Streda 11 457 odberov z čoho bolo 198 odberov (1,72 %) anti-HBc pozitívnych (2,86 x vyšší výskyt anti-HBc pozitivity).
Najmä v prvom roku vyšetrovania bolo percento anti-HBc pozitívnych jedincov v regióne Dunajská Streda veľmi vysoké, z čoho vyplýva výrazný rozdiel medzi týmito dvomi sledovanými oblasťami.
Počas jednotlivých rokov vyšetrovania bol zistený štatisticky významný rozdiel výskytu anti-HBc pozitivity medzi sledovanými regiónmi. Ako udáva graf 1, najväčší rozdiel bol zistený v roku 2008 a najmenší v roku 2011.
Graf 1. Výskyt anti-HBc pozitivity. 
**p<0,01 ***p<0,001 V niektorých mesiacoch roka 2008 bolo v tomto regióne percento anti-HBc pozitívnych darcov krvi enormne vysoké až okolo 7 % (graf 2).
Graf 2. Rok 2008 Dunajská Streda – % výskytu anti-HBc pozitivity v jednotlivých mesiacoch. 
Graf 3 udáva percentuálne zastúpenie jednotlivých vekových kategórií anti-HBc pozitívnych darcov krvi z regiónu Dunajská Streda.
Graf 3. Dunajská Streda – výskyt anti-HBc pozitivity v súvislosti s vekom. 
Výšku titra neutralizačných (protektívnych) anti-HBs protilátok u anti-HBc pozitívnych darcov z tohto regiónu udáva graf 4.
Graf 4. Dunajská Streda – titre neutralizačných anti-HBc protilátok u anti-HBc pozitívnych dárcov. 
U 37 % týchto darcov sa zistilo zvýšenie ALT nad referenčné hodnoty (graf 5).
Graf 5. Dunajská Streda – hladiny ALT u anti-HBc pozitívnych dárcov. 
HBV DNA bola vyšetrená u 126 anti-HBc pozitívnych, HBsAg negatívnych vzoriek získaných z oblasti Dunajskej Stredy (oblasť s vysokou prevalenciou výskytu anti-HBc protilátok) a z oblasti východného Slovenska (oblasť s vyššou prevalenciou HBsAg pozitivity než v iných oblastiach Slovenska).
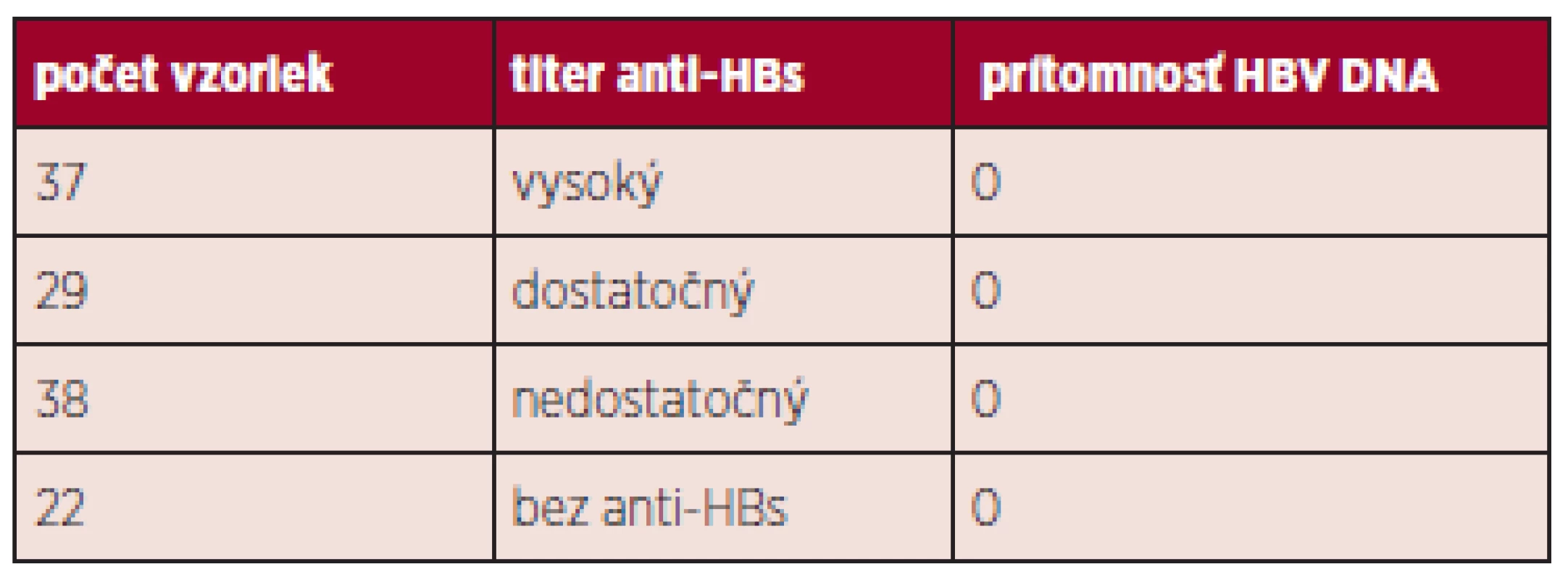
Podľa zistenej výšky titra anti-HBs protilátok boli tieto vzorky rozdelené do jednotlivých skupín:
- a/ vysoký titer (nad 500 mIU/ml)
- b) dostatočný titer (100–500 mIU/ml)
- c) nedostatočný titer (pod 100 mIU/ml)
- d) bez anti-HBs protilátok
U žiadnej z vyšetrovaných vzoriek nebola zistená prítomnosť HBV DNA (tab. 1).
Algoritmus vyšetrenia pri zistenej anti-HBc pozitivite znázorňuje schéma 1.
Schéma 1 
Algoritmus vyšetrenia pri zistenej anti-HBc špecifickej reaktivite (pozitivite). Diskusia
Kľúčovou úlohou v transfuziológii je zaistiť bezpečnosť transfúznych prípravkov z hľadiska možného prenosu infekcií prenášaných krvou.
V prípade hepatitídy B riziko prenesenej infekcie aj v súčasnej dobe stále existuje.
Pre zamedzenie prenosu infekcie vo fáze pre-sérokonverznej „window periódy” (v sére nie sú prítomné žiadne antigény ani protilátky, dá sa ale zistiť DNA vírusu) je potrebné NAT testovanie. Infektivita krvných komponentov získaných od darcov v tomto štádiu je veľká, častosť prenosu je ale veľmi nízka, napr. v roku 2008 American Red Cross metódou NAT testoval 3,7 miliónov HBsAg a anti-HBc negatívnych krvných jednotiek na prítomnosť HBV DNA. Jej prítomnosť bola zistená v 9 darcoch (1 : 410 000) (11).
Pre zamedzenie prenosu infekcie s imunovariantnými vírusovými mutantami, z ktorých niektoré nemusia byť v súčasnej dobe zistené dostupnými screeningovými testami, je potrebné testovanie anti-HBc a NAT testovanie (4, 5).
Najdiskutovanejšia je otázka zamedzenia prenosu HBV formou okultnej HBV infekcie. Vyšetrovanie anti-HBc protilátok nepochybne zohráva dôležitú, ak nie hlavnú úlohu pri zamedzení prenosu HBV touto formou. U darcov s okultnou HBV infekciou nemusí NAT testovanie detekovať veľmi nízku vírusovú nálož a tieto prípady môžu byť infekčné.
Je dokázané, že infektivita krvných komponentov získaných od darcov s okultnou HBV infekciou je viac ako 10x nižšia než infektivita krvných komponentov získaných od darcov nachádzajúcich sa vo fáze pre-sérokonverznej „window periódy” ale je až 100x častejšia (2).
U jedincov s okultnou HBV infekciou je množstvo HBV DNA vyššie v hepatocytoch než v sére. Predpokladá sa, že uzdravenie sa z akútnej vírusovej hepatitídy B nemá za následok kompletnú vírusovú elimináciu, ale že imunitný systém udržiava veľmi nízke množstvo vírusu v organizme (12). Vírus je trvale prítomný v pečeni a môže dôjsť k jeho reaktivácii pri imunosupresívnych stavoch (13).
Ako uvádzajú niektoré štúdie, darcovia s izolovanými anti-HBc protilátkami tzv. anti-HBc „only” reactive (bez anti-HBs), majú tak extrémne nízke hladiny HBV DNA, že nie sú detekovateľné štandardnými NAT testami v skupinových vzorkách (MP-NAT) a dokonca ani vo vzorkách testovaných individuálne (ID-NAT). Nízka vírusová nálož v HBV DNA pozitívnych vzorkách naznačuje, že minipooly NAT nedetekujú väčšinu potenciálne infekčných krvných jednotiek od anti-HBc pozitívnych darcov (14). Testy na HBV DNA musia byť extrémne citlivé, vzorky sa nesmú testovať v pooloch ale jednotlivo, aj tak sú možné falošne negatívne výsledky.
Urbani a kol. (15) poukazujú na to, že anti-HBc sérologické testy sa dajú používať ako kvalifikovaná náhrada NAT testovania a pre celkové zvýšenie bezpečnosti pri hodnotení rizika okultnej hepatitídy B v periférnej krvi.
Riziko okultnej HBV infekcie spojenej s anti-HBc séropozitivitou bolo dokázané a prítomnosť protilátkovej odpovede na HBc antigén môže byť považovaná za výstražný marker okultnej HBV infekcie (15).
Po zavedení NAT testovania v transfuziológii sa predpokladalo, že riziko prenosu infekcie vírusmi HIV, HBV a HCV sa zredukuje na minimum. Zdá sa, že v prípade prenosu HBV to neplatí, pretože najmä chronickí HBV nosiči majú vírusovú nálož pod hranicou detekčného limitu a nedetekovateľné HBsAg (16).
Veľmi diskutovanou je aj otázka úlohy výšky titra anti-HBs protilátok u anti-HBc pozitívnych darcov. Veľa publikovaných prác udáva, že ich úloha je veľmi dôležitá a že u anti-HBc pozitívnych jedincov s dostatočnou hladinou anti-HBs protilátok (> 100 mIU/ml) nebola identifikovaná HBV DNA a nemali by preniesť infekciu na príjemcu (17). Experimenty na šimpanzoch potvrdzujú tieto teoretické predpoklady. Po inokulácii ľudskej krvi obsahujúcej anti-HBc, HBV DNA a anti-HBs s určitou známou koncentráciou nedošlo k prenosu infekcie, v porovnaní s inokuláciou toho istého množstva bez anti-HBs, ktorá už spôsobila infekciu (18). Chýbajú samozrejme údaje o tom, či toto so 100% istotou platí aj u ľudí. Cenné údaje a skúsenosti môžu poskytnúť look-back sledovania u príjemcov krvi, u ktorých bola potvrdená hepatitída B a kde je predpoklad, že bola prenesená transfúziou.
Anti-HBc pozitívne krvné prípravky bez anti-HBs protilátok alebo s ich nízkym titrom môžu byť infekčné u imunosuprimovaných príjemcov (19). Neutralizačná schopnosť nízkeho titra anti-HBs môže byť nedostatočná v prítomnosti vysokej vírusovej nálože. Samozrejme je potrebné brať do úvahy aj objem transfundovaného prípravku.
Pre pacientov s imunosupresívnou liečbou môže byť nebezpečná aj inokulácia nízkej infekčnej dávky s prítomnosťou anti-HBs. Imunologický status príjemcu krvi hrá dôležitú úlohu v získaní potransfúznej hepatitídy typu B. Udáva sa, že okolo 50 % všetkých transfundovaných krvných prípravkov v západnej Európe je podaných príjemcom s určitým stupňom imunodeficiencie (20).
Candotti a spol. (21) v roku 2009 uviedli, že u približne 90 % anti-HBc pozitívnych darcov krvi sa zisťujú aj protilátky anti-HBs. Zostávajúce percenta tvoria anti-HBc pozitívni darcovia bez anti-HBs protilátok (22, 23).
Tieto pozorovania sa zhodujú aj s nami prezentovanými výsledkami. Zistili sme, že až 97,5 % anti-HBc pozitívnych darcov z oblasti s vysokou prevalenciou anti-HBc má protilátky anti-HBs s rôznymi titrami. Tieto zistenia dokazujú, že títo jedinci prekonali HBV infekciu, alebo u nich došlo v minulosti ku kontaktu s HBV. Zostávajúcich 2,5 % tvoria anti-HBc „only” pozitívni darcovia (bez anti-HBs protilátok).
WHO doporučuje považovať za minimálny ochranný titer anti-HBs 10 mIU/ml a za hranicu dobrej imunity považuje výšku titra 100 mIU/ml.
Podľa niektorých údajov z literatúry u pacientov s hepatitídou B, u ktorých došlo k uzdraveniu spontánne alebo ako odpoveď na terapiu interferónom, nebola identifikovaná HBV DNA v prípade, keď titer anti-HBs bol vyšší ako 100 mIU/ml (17).
Nízka hladina HBV DNA bola publikovaná nielen u anti-HBc „only” pozitívnych darcov krvi, ale aj u jedincov s nízkymi hladinami anti-HBs (< 100 mIU/ml) (20).
Dve nemecké štúdie prezentujú 6 anti-HBc pozitívnych a HBV DNA pozitívnych darcov, ktorých titer anti-HBs bol vyšší ako 100 mIU/ml (24, 25).
V kazuistikách niekoľkých nami zistených anti-HBc pozitívnych darcov, ktorí absolvovali hepatologické vyšetrenie sa takisto vyskytujú prípady dokázanej prítomnosti HBV DNA aj pri hladine anti-HBs protilátok 200 mIU/ml alebo pod 100 mIU/ml (26).
V niektorých krajinách je prijatý sérologický testovací algoritmus kedy po zistení anti-HBc pozitivity nasleduje vyšetrenie titra anti-HBs (anti-HBs ≥ 100 mIU/ml = pravdepodobne neinfekčný jedinec) alebo implementácia vysoko senzitívneho HBV DNA screeningu. Toto je ale oblasť neutíchajúcich diskusií rôznych autorov.
Po zavedení vyšetrovania anti-HBc protilátok (ako jedného z povinne vyšetrovaných parametrov u darcov krvi po každom odbere), sa v Národnej transfúznej službe SR všetci darcovia so zistenou špecifickou reaktivitou (pozitivitou) anti-HBc pri absencii vyšetrovania HBV DNA trvalo vyraďujú. U každého anti-HBc pozitívneho darcu je vyšetrený titer anti-HBs protilátok.
Najmä v prvom roku vyšetrovania anti-HBc protilátok bolo percento anti-HBc pozitívnych jedincov najmä v regióne Dunajská Streda veľmi vysoké, z čoho vyplýva aj výrazný rozdiel medzi dvomi sledovanými oblasťami (3,34x vyšší výskyt v regióne Dunajská Streda).
Trvalým vyraďovaním týchto darcov sa percento anti-HBc pozitivity v tomto regióne v ďalších sledovaných rokoch významne znižovalo. K zníženiu počtu anti-HBc pozitívnych darcov došlo aj v bratislavskom regióne (graf 1).
Výška titra anti-HBs protilátok poukazuje na stupeň imunity jedinca voči HBV a v prípade trvalého vyradenia pomáha odpovedať na otázky ohľadom prípadného očkovania darcu krvi alebo jeho odoslania na ďalšie sledovanie hepatológom alebo infektológom (schéma 1).
Niektoré krajiny povoľujú použiť na transfúziu krvné prípravky s titrom anti-HBs ≥ 100 mIU/ml (27, 28).
V našej štúdii, v žiadnej zo 126 vyšetrených anti-HBc pozitívnych vzoriek, sme nenašli prítomnosť HBV DNA. Bolo medzi nimi aj 22 „only” anti-HBc pozitívnych darcov.
Je namieste zamyslieť sa nad niekoľkými skutočnosťami:
- Aj keď je použitý NAT test dostatočne citlivý, neobsahuje vyšetrovaná vzorka nedetekovateľné množstvo HBV DNA?
- Môže zohrávať úlohu aj obdobie, kedy je vzorka na vyšetrenie odobratá? Všetky vzorky na vyšetrenie HBV DNA v tejto štúdii boli odobraté v deň odberu krvi, kedy by sa darca mal cítiť absolútne zdravý.
- Za úvahu stojí aj fakt, že „only” anti-HBc pozitívni darci s dokázaným kontaktom s HBV v minulosti, nevykazujú žiadny stupeň imunity voči HBV, ich imunitný systém nebol schopný vyvinúť efektívnu imunologickú kontrolu (21, 29), spája sa tento stav len s možným nebezpečenstvom prenosu HBV na príjemcu transfúzie prípadne orgánov alebo sú títo jedinci takisto ohrození v prípade ďalšieho kontaktu s HBV – reinfekcia?
Testovanie anti-HBc (aj v prípade, keď je NAT screening zavedený) má svoju úlohu v screeningovom algoritme redukcie reziduálneho rizika transfúziou prenesenej HBV infekcie za účelom vyradenia potenciálnych HBV nosičov v darcovskej populácii (30).
Paul-Ehrlichov inštitút popísal 7 z 18 prípadov dokázaného prenosu HBV krvnými prípravkami, ktorým sa dalo zabrániť, keby boli vyšetrené anti-HBc protilátky (31).
V Nemecku bolo testovanie anti-HBc zavedené v októbri 2008 už po skúsenostiach testovania HBV DNA v minipooloch (31). Bolo zistené, že testovanie anti-HBc identifikovalo väčšinu nosičov okultnej HBV infekcie, ktorí boli zodpovední za 50–60 % všetkých HBsAg negatívnych ale HBV pozitívnych darovaní (32). Pri súbežnom vysoko senzitívnom NAT testovaní poolov 96 vzoriek bolo identifikovaných len 67 % OBI nosičov a 87 % HBsAg negatívnych pre-sérokonverzných prípadov (32).
Strata potenciálnych darcov môže byť redukovaná ak anti-HBc pozitívni darcovia sú ďalej testovaní na anti-HBs a krvná plazma darcov, ktorých titer anti-HBs je ≥ 100 mIU/ml a sú negatívni pri testovaní HBV DNA, je použitá na komponentové spracovanie (32).
Hranicu titra anti-HBs ≥ 100 mIU/ml ako bezpečnú ale nemožno považovať za pravidlo a je často diskutovaná ( 33 ).
V našej práci sme sledovali aj hladiny ALT u anti-HBc pozitívnych darcov v regióne s vysokou prevalenciou anti-HBc (Dunajská Streda). Títo darcovia boli rozdelení do troch skupín: s hladinami ALT v norme, s hladinami ALT nad referenčnou hodnotou použitej metodiky, ale prípustnými pre transfúzny prípravok a s hladinami ALT nad referenčnou hodnotou použitej metodiky a neprípustnými pre transfúzny prípravok (graf 5). Kritérium pre vyradenie transfúznych prípravkov je dvojnásobok referenčnej hodnoty. Sú to zaujímavé ale ničím nepodložené výsledky, ktoré spadajú len do kategórie úvah, či súvisia s anti-HBc pozitivitou alebo ide o zvýšenie hladiny ALT, ktoré s ňou nijako nesúvisí, ani s iným infekčným ochorením pečene. V súvislosti s anti-HBc pozitivitou je samozrejme najzaujímavejšia skupina darcov (2%) s hladinami ALT nad referenčnou hodnotou a už neprípustnými pre transfúzny prípravok. Pri absencii vyšetrovania anti-HBc protilátok by 35 % anti-HBc pozitívnych darcov z tohto regiónu s hladinami ALT nad referenčnou hodnotou, ale prípustnými pre transfúzny prípravok, bolo pripustených k odberu.
Záver
Podarilo sa zistiť, že v regióne Dunajská Streda sa v 70-tych rokoch minulého storočia vyskytoval vysoký počet prípadov hepatitídy B v detskom veku a preto sa v tejto oblasti zisťuje v súčasnom období percentuálne vyšší počet jedincov s pozitívnymi anti-HBc protilátkami.
V žiadnej na HBV DNA vyšetrenej anti-HBc pozitívnej vzorke s rôznymi titrami anti-HBs protilátok ani v „only” anti-HBc pozitívnej vzorke z tejto oblasti sa nezistila jej prítomnosť testovaním týchto vzoriek jednotlivo.
Zavedenie vyšetrovania anti-HBc protilátok aj keď je spojené s vyradením určitého počtu darcov, významne a spoľahlivo prispieva k eliminácii rizika prenosu infekcie HBV transfúziou vo fáze možnej okultnej HBV infekcie s detekovateľnou alebo nedetekovateľnou (pri jej veľmi nízkych hladinách v sére) prítomnosťou HBV DNA. Definitívne eliminuje HBV infikovaných darcov v štádiu OBI a tak pomáha redukovať prenos HBV s potenciálnymi následkami hlavne medzi imunokompromitovanými príjemcami, novorodencami a príjemcami s imunosupresívnou liečbou.
Riziko prenosu HBV infekcie pri absencii NAT testovania pretrváva v štádiu pre-sérokonverznej „window periódy”. Toto obdobie sa dá takisto skrátiť používaním najnovších vysoko senzitívnych testov na screeningové vyšetrovanie HBsAg. Ako udávajú NAT kvantifikačné panely najcitlivejšie testy v súčasnom období sú so senzitivitou 0,08 ng/ml, čo zodpovedá 102-267 HBV DNA IU/ml (30, 34, 35).
Podiel autorov na rukopise
E. Ščepkinová - príprava štúdie, príprava vzoriek, screeningové vyšetrenia, napísanie rukopisu, kontrola rukopisu
J. Gašparovič – príprava štúdie, vyšetrenia NAT, revízia rukopisu
Poďakovanie
Práca vznikla s podporou grantu CEVA (Centrum edukácie a výskumu ABBOTT) č. projektu: 02/2012 – Výskyt okultnej infekcie vírusom hepatitídy B u darcov krvi s pozitívnymi anti-HBc protilátkami
Doručeno do redakce: 21. ledna 2014
Přijato po recenzích: 16. dubna 2014
RNDr. Eleonóra Ščepkinová
Národná transfúzna služba SR
Ďumbierska 3/L
831 01 Bratislava
e-mail: scepkinova@ntssr.sk
Zdroje
1. Lavanchy D. Hepatitis B virus epidemiology, disease, burden, treat-ment and current and emerging prevention and control. J Viral Hepat 2004; 11 : 97-107.
2. Allain JP. Occult hepatitis B virus infection. Transfus Clin Biol 2004; 11 : 18-25.
3. Servant-Dumas A, Mercur Darty M, Wind F, Alloi Ch, Surean C, Laperche S. Variable capacity of 13 hepatitis B virus surface antigen assays for the detection of HBsAg mutants blood samples. J Clin Virology 2012; 53 : 338-345.
4. Zeiler T, Karger R, Slonka J, Ketschner V, Radsak K. Introduction of anti-HBc testing of blood donors in Germany. Transfus Med 2006; 16 : 441-443.
5. Gerlich W. Breakthrough of hepatitis B virus escape mutants after vaccination and virus reactivation. J Clin Virol 2006; 36 : 518-522.
6. Raimondo G, Pollicino T, Romano L, Zanetti AK. A 2010 update on occult hepatitis B infection. Pathol Biol (Paris) 2010; 58 : 254-7.
7. Glebe D. AREVIR Meeting Bonn 2009: Occult hepatitis B virus infection.
8. Tabor E, Hoofnagle JH, Smallwood LA, et al. Studies of donors who transmit postransfusion hepatitis. Transfusion 1979; 19 : 725-731.
9. Raimondo G, Navarra G, Mondello S, et al. Occult hepatitis B virus in liver tissue of individuals without hepatitis disease. J Hepatol 2008; 48 : 743-746.
10. Raimondo G, Allain JP, Brunettto MR, et al. Statements from the Taormina expert meeting on occult hepatitis B virus infection. J Hepatol 2008; 49 : 652-657.
11. Hollinger FB. Occult hepatitis B in blood donors. Oral presentation, 3rd International Tehran hepatitis congress, 2010.
12. Weber B, Muhlbacher A, Melchior W. Detection of an acute asymptomatic HBsAg negative hepatitis B virus infection in a blood donor by HBV DNA testing. J Clin Virology 2005; 32 : 67-70.
13. Berger A, Preiser W, Katchel HG, Sturmer M, Doerr HW. HBV reactivation after kidney transplantation. J Clin Virology 2005; 32 : 162-165.
14. Kuhns MC, Busch MP. New strategies for blood donor screening for hepatitis B virus: nucleic acid testing versus immunoassay methods. Mol Diagn Ther 2006; 10 : 77-91.
15. Urbani S, Fagnoni F, Missale G, Franchini M. The role of anti-core antibody response in the detection of occult hepatitis B virus infection. Clin Chem Lab Med 2010; 48 : 23-29.
16. Screening donated blood for transfusion-transmissible infections. WHO 2010, Recommendations.
17. Kleinman, SH, Kuhns MC, Todd DS, et al. Frequency of HBV DNA detection in US blood donors testing positive for the presence of anti-HBc: implications for transfusion transmission and donor screening. Transfusion 2003; 43 : 696-704.
18. Prince AM, Lee DH, Brotman B. Infectivity of blood from PCR-positive, HBsAg-negative, anti-HBc positive cases of resolved hepatitis B infection. Transfusion 2001; 41 : 329-332.
19. Niederhauser C, Weigand T, Candotti D. Fatal outcome of hepatitis B virus transfusion-transmitted infection. Vox Sang 2010; 98 : 504-507.
20. Allain JP, Henk W, Lucey RCH. A European perspective of the management of donors and units testing positive for hepatitis B virus DNA. Transfusion 2006; 46 : 1256-1258.
21. Candotti D, Allain JP. Transfusion-transmitted hepatitis B virus infection. J Hepatol 2009; 51 : 798-809.
22. Panigraphi R, Biswas A, Datta S, et al. Anti-hepatitis B core antigen testing with detection and characterization of occult hepatitis B virus by an in house nucleic acid testing among blood donors in Behrampur, Ganjam, Orisa in southeastern India, implications for transfusion. Virol J 2010; 7 : 204.
23. Allain JP, Candotti D, Soldan K, et al. The risk of hepatitis B virus infection by transfusion in Kumasi, Ghana. Blood 2003; 101 : 2419-2425.
24. Roth WK, Webwe M, Petersen D, et al. NAT for HBV and anti-HBc testing increase blood safety. Transfusion 2002; 42 : 869-875.
25. Hennig H, Puchta I, Luhm J, et al. Frequency and load of hepatitis B virus DNA in first - time blood donors with antibodies to hepatitis B core antigen. Blood 2002; 100 : 2637-2641.
26. Ščepkinová E, Sviteková K: Môže byť anti-HBc reaktívny jedinec darcom krvi? Ústna prezentácia – XIV. Česko-slovenský kongres o infekčných chorobách, 2010, Pec pod Sněžkou.
27. Minuk GY, Sun DF, Uhanova Z, et al. Occult hepatitis B virus infection in a North American community-based population. J Hepatol 2005; 42 : 480-485.
28. Liu CJ, Chen DS, Chen PJ. Epidemiology of HBV infection in Asian blood donors: emphasis on occult HBV infection and the role of NAT. J Clin Virology 2006; 36 : 33-34.
29. Candotti D, Grabarczyk P, Ghiazza P. Characterization of occult hepatitis B virus from blood donors carrying genotype A2 or genotype D strains. J Hepatol 2008; 49 : 537-547.
30. Niederhauser Ch. Reducing the risk of hepatitis B virus transfusion-transmitted infection. J Blood Med 2011; 2 : 91-102.
31. Burger R, Offergeld R. Testing plasma donations for hepatitis B core antigen (anti-HBc) in order to improve safety of cellular blood components and of quarantined fresh frozen plasma. Bundesgesundsheitsbl Gesundheitsforsh Gesundheitsschutz 2005; 48 : 698-699.
32. Roth WK. Hepatitis and blood transfusion. ISBT Science series 2007; 2 : 178-183.
33. Grob P, Jilg W, Bornhak H. Serological pattern „anti-HBc alone” report on a Workshop. J Med Virol 2000; 62 : 450-455.
34. Stramer SL. Pooled HBV DNA testing by nucleic acid amplification: implementation or not? Transfusion 2005; 45 : 1242-1246.
35. Biswas R, Tabor E. Comparative sensitivity of HBV NATs and HBsAg assays for detection of acute HBV infection. Transfusion 2003; 43 : 788-798.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2014 Číslo 2- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Definice a klasifikace chronického onemocnění ledvin dle KDIGO
-
Všechny články tohoto čísla
- Hodnocení exprese antigenu CD45 u pacientů s mnohočetným myelomem a jeho vliv na dobu do první progrese nebo relapsu
- Chronická myelomonocytová leukémia – prehľad súčasných diagnostických a liečebných možností
- Eliminácia rizika prenosu vírusu hepatitídy B transfúziou vo fáze možnej okultnej HBV infekcie
- Mechanismy navozené imunotolerance nádorových buněk u chronické lymfatické leukemie a možnosti jejich detekce metodami průtokové cytometrie
- Hrodek O. Early molecular response predicts outcomes in patients with chronic myeloid leukemia in chronic phase treated with frontline nilotinib or imatinib
- Hrodek O. Therapy-related acute myeloid leukemia and myelodysplastic syndromes in patients with Hodgkin lymphoma: a report from the German Hodgkin Study Group
- Hrodek O. Duration of anticoagulant therapy for deep vein thrombosis and pulmonary embolism
- Hrodek O. Pretransplant administration of imatinib for allo-HSCT in patients with BCR-ABL–positive acute lymphoblastic leukemia
- Hrodek O. Comparison of horse and rabbit antithymocyte globulin in immunosuppressive therapy for refractory cytopenia of childhood
- Hrodek O. Long-term outcome with dasatinib after imatinib failure in chronic-phase chronic myeloid leukemia: follow-up of a phase 3 study
- Hrodek O. Bone marrow fibrosis in 66 patients with immune thrombocytopenia treated with thrombopoietin-receptor agonists: a single-center, long-term follow-up
- Hrodek O. How I treat leukemia during pregnancy
- Hrodek O. What is the relevance of Ikaros gene deletions as a prognostic marker in pediatric Philadelphia-negative B-cell precursor acute lymphoblastic leukemia?
- XXVIII. olomoucké hematologické dny s mezinárodní účastí
- Přehled produkce transfuzní služby ČR za rok 2013 (transfuzní přípravky i plazma pro frakcionaci)
- Vyhlášení ceny Janssen 2014
- Autotransfuze v České republice v roce 2013
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Chronická myelomonocytová leukémia – prehľad súčasných diagnostických a liečebných možností
- Eliminácia rizika prenosu vírusu hepatitídy B transfúziou vo fáze možnej okultnej HBV infekcie
- Hodnocení exprese antigenu CD45 u pacientů s mnohočetným myelomem a jeho vliv na dobu do první progrese nebo relapsu
- Mechanismy navozené imunotolerance nádorových buněk u chronické lymfatické leukemie a možnosti jejich detekce metodami průtokové cytometrie
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání