-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Polyneuropatie u pacientov s diabetes mellitus
Polyneuropathies in patients with diabetes mellitus
With an increasing prevalence of diabetes mellitus in the population predominantly of the world’s developed countries, the prevalence of complications of the primary disease linearly rises as well. One of them is diabetic neuropathy which to a large degree contributes to morbidity and indirectly also mortality related to diabetes. The term diabetic neuropathy is understood as peripheral neuropathy, caused by a direct effect of hyperglycemia engaged in a cascade of complex processes which damage the nervous fibres. The process results in the characteristic clinical picture reflecting the damage to the sensory, motor as well as autonomic peripheral nerves. The aim of this paper is not to produce a detailed analysis of the diagnosis of diabetic neuropathy, it aims to draw attention to the incidence of “non-diabetic” neuropathies in patients with diabetes mellitus. It is apparent that patients with diabetes and peripheral neuropathy are often incorrectly recorded with diabetic neuropathy, although their disorder may be autoimmunely conditioned, treatment-induced or toxic neuropathy. That is why we decided to also focus in this paper, apart from diabetic neuropathy, on the most frequently occurring peripheral neuropathies that could clinically mimic diabetic neuropathy, may be associated with it, or they occur along with it. These involve chronic demyelination inflammatory polyneuropathy, metformin-induced neuropathy, “insulin neuritis” and alcohol neuropathy. With regard to the relatively high prevalence of the aforementioned neuropathies it is always necessary to consider their incidence also in patients with diabetes mellitus.
Key words:
antidiabetic drugs, axonal – demyelination changes, diabetes mellitus, electromyography, hyperglycemia, nervous fibres, neuropathy
Autoři: Peter Matejička; Michal Minár
Působiště autorů: II. neurologická klinika LF UK a UNB, Nemocnica akad. L. Dérera, Bratislava
Vyšlo v časopise: Forum Diab 2018; 7(3): 140-146
Kategorie: Prehľadové práce
Souhrn
S rastúcim výskytom diabetes mellitus v populácii prevažne rozvinutých krajín sveta lineárne pribúda aj výskyt komplikácií základného ochorenia. Jednou z nich je aj diabetická neuropatia, ktorá sa v nemalej miere podieľa na morbidite a nepriamo aj mortalite spojenej s diabetom. Pod pojmom diabetická neuropatia sa chápe periférna neuropatia, ktorá je spôsobená priamym účinkom hyperglykémie zapojenej v kaskáde zložitých procesov, ktorých výsledkom je poškodenie nervových vlákien. Výsledkom tohto procesu je typický klinický obraz vyplývajúci z poškodenia senzitívnych, motorických a taktiež aj autonómnych periférnych nervov. Cieľom tohto článku nie je detailný rozbor diagnózy diabetickej neuropatie, ale upriamenie pozornosti na výskyt „nediabetických“ neuropatií u pacientov s diabetes mellitus. Je zrejmé, že pacienti s diabetom a periférnou neuropatiou sú často mylne vedení s diagnózou diabetickej neuropatie, hoci sa môže jednať o autoimunitne podmienené, liečbou indukované alebo toxické neuropatie. Preto sme sa rozhodli v tomto článku venovať okrem diabetickej neuropatie aj najčastejšie sa vyskytujúcim periférnym neuropatiám, ktoré môžu diabetickú neuropatiu klinicky imitovať, môžu byť s ňou asociované, alebo prebiehajú súčasne. Jedná sa o chronickú demyelinizačnú zápalovú polyneuropatiu, metformínom indukovanú neuropatiu, „inzulínovú neuritídu“ a alkoholovú neuropatiu. Vzhľadom na relatívne vysokú prevalenciu týchto neuropatií je nutné mať vždy na zreteli ich výskyt aj u pacientov s diabetes mellitus.
Kľúčové slová:
antidiabetiká, axonálne – demyelinzačné zmeny, diabetes mellitus, elektromyografia, hyperglykémia, nervové vlákna, neuropatia
Úvod
Zmeny v ľudskom správaní a životnom štýle majú za následok to, že za posledné desaťročie celosvetovo dramaticky stúpla incidencia diabetes mellitus (DM). Epidemický nárast výskytu je najmä pri DM 2. typu (resp. pri DM ako súčasti tzv. metabolického syndrómu) [1]. Svetová zdravotnícka organizácia predpokladá, že celosvetový výskyt DM narastie z 171 miliónov v roku 2000 na 366 miliónov v roku 2030 [2]. V spojení s genetickou predispozíciou, osobitne v určitých etnických skupinách, je DM 2. typu (DM2T) spôsobený environmentálnymi faktormi a faktormi životného štýlu, ako sú sedavý spôsob života, nadmerný príjem potravy a obezita. Pre redukciu morbidity a mortality následkom diabetu a jeho mikro - a makrovaskulárnych komplikácií je nutný integrovaný, medzinárodný prístup [3].
Najčastejšou a jednou z najzávažnejších komplikácií DM1T aj DM2T je periférna diabetická neuropatia (senzorimotorická alebo autonómna). Jej prevalencia sa pohybuje okolo 8 % u novodiagnostikovaných pacientov a u > 50 % pacientov s dlhšie trvajúcim diabetom [1].
Je nutné mať na zreteli, že pacienti s DM môžu mať okrem diabetickej polyneuropatie (DPN) pridružený aj iný typ neuropatie, ktorú je nutné včas diagnostikovať a liečiť. Medzi najčastejšie patria napríklad autoimunitne podmienené neuropatie (konkrétne chronická zápalová demyelinizačná polyneuropatia – CIDP), neuropatie indukované liekmi (vrátane antidiabetík), alkoholová neuropatia, neuropatie pri deficite vitamínu B12, hereditárne neuropatie, neuropatie pri vaskulitídach. U pacientov s DM sa môže samozrejme vyskytnúť akákoľvek iná neuropatia, avšak sú určité typy, ktoré sa často „skrývajú“ za DPN, a z toho dôvodu sú často poddiagnostikované. Preto je nutné, aby špecialisti brali do úvahy možnú koincidenciu diabetickej neuropatie s ostatnými typmi periférnych neuropatií.
Diabetické neuropatie
Diabetická neuropatia (nazývaná aj diabetická polyneuropatia – DPN) predstavuje klinicky heterogénny syndróm poškodenia periférnych, vrátane kraniálnych či autonómnych nervov. U diabetikov s DM1T je prevalencia DPN vo veku do 30 rokov 18 %, vo veku > 30 rokov 58 %. U pacientov s DM2T má pri stanovení diagnózy neuropatiu 14 % a za ďalších 10 rokov trvania diabetu už 32 % pacientov [4]. Medzi nezávislé rizikové faktory pre vznik diabetickej neuropatie patrí okrem hyperglykémie aj vek, fajčenie, abúzus alkoholu, hypertenzia, obezita a hypercholesterolémia [5]. Príčina diabetickej neuropatie nie je do dnes úplne objasnená. Všeobecne sa predpokladá komplexný mechanizmus vzniku. Etiopatogenéza DPN zahŕňa:
- hyperglykémiou aktivovanú polyolovú cestu
- neenzymatickú glykáciu makromolekúl, predovšetkým neurónových proteínov
- oxidačný stres
- zvýšenú aktivitu proteínkinázy C (β izoforma)
- poruchu metabolizmu esenciálnych mastných kyselín
Komplexný patogenetický mechanizmus umožňuje na jednej strane liečebne ovplyvniť rôzne etáže procesu, no na druhej strane je príčinou doposiaľ neuspokojivých terapeutických výsledkov [6].
Klinický obraz diabetickej neuropatie
Najbežnejšie symptómy DPN sú parestézie a dysestézie, ktoré pacienti popisujú ako chodenie po vode alebo po vate. Bolesti prevažne akrálnych častí dolných končatín sú najčastejšie pichavé (udávané ako bodanie ostrými predmetmi), niekedy tupé či mučivé, akoby pacienti držali dolné končatiny v ľadovej vode. Vyskytujú sa taktiež krampy, predovšetkým v oblasti flexorov predkolenia či palcov. Tieto symptómy spĺňajú charakter neuropatickej bolesti a môžu sa vyskytnúť v akomkoľvek štádiu ochorenia [7].
Zhoršenie vibračnej citlivosti sa udáva ako jednoznačný príznak DPN. Hypestézia a hypoalgézia je taktiež typickým príznakom, ktorému často predchádza hyperestézia a hyperalgézia. Výpadok reflexov Achillových šliach sa zvyčajne vyskytuje simultánne. V pokročilých štádiách DPN dochádza k parézam a atrofiám príslušných svalov predovšetkým na dolných končatinách. Uvedené symptómy sú veľmi často sprevádzané príznakmi autonómnej neuropatie. Tie sa môžu samozrejme vyskytovať aj samostatne, resp. môžu nezriedka predchádzať senzorimotorické príznaky [8].
Klasifikácia diabetickej neuropatie
Vzhľadom na poznanie rôznych klinických syndrómov spojených s poškodením periférnych nervov, ako aj ich vzájomné prekrývanie, je takmer nemožné vytvoriť univerzálnu klasifikáciu diabetickej neuropatie. O systemizáciu rozličných prejavov sa pokúšalo veľa autorov – použitím rôznych kritérií, či už klinických, topografických, ale aj subklinických, morfometrických či neurofyziologických znakov poškodenia periférneho neurónu. Vďaka tomu existuje množstvo klasifikácií DPN. Celosvetovo je zatiaľ stále najuznávanejšia klasifikácia podľa Thomasa a jej novšia modifikácia podľa Boultona, ktoré rozlišujú difúznu symetrickú polyneuropatiu od fokálnej či multifokálnej neuropatie [9,10]. Táto klasifikácia obsahuje aj kritériá so zreteľom na intenzitu neuropatie (subklinická a klinická). V tab. 1 je uvedená modifikovaná Thomasova klasifikácia.
Tab. 1. Modifikovaná Thomasova klasifikácia. Upravené podľa [9,10] ![Modifikovaná Thomasova klasifikácia.
Upravené podľa [9,10]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/bba651f982d3a9af5c9ca9fe06678209.jpeg)
Akútne senzitívne neuropatie
Akútne senzitívne neuropatie (ASN) sú zriedkavé formy, vyskytujú sa pri slabej metabolickej kontrole (napr. pri ketoacidóze) alebo pri náhlej zmene v kontrole glykémie (napr. pri výraznej hypoglykémii v rámci tzv. inzulínovej neuritídy). Sú charakterizované akútnym začiatkom ťažkých senzitívnych symptómov so zvýraznením v nočných hodinách pri relatívne malom neurologickom náleze na dolných končatinách [10].
Chronické senzorimotorické distálne polyneuropatie
Chronická senzorimotorická distálna polyneuropatia je najčastejšie sa vyskytujúca forma diabetickej neuropatie, pri ktorej sa u > 50 % pacientov vyskytujú pálivé bolesti, pálivé alebo bodavé pocity, parestézie, hyperestézie a taktiež často hlboké/tupé skľučujúce bolesti. Tieto neuropatické bolesti sa typicky zhoršujú v noci a postihujú prevažne dolné končatiny (akrálne časti), zriedka môžu byť príznaky výraznejšie na horných končatinách. Viac ako polovica pacientov môže byť asymptomatická a diagnóza je stanovená dôkladným neurologickým vyšetrením alebo v niektorých prípadoch je odhalená až pri vzniku nebolestivých ulcerácií na nohách. Taktiež bývajú vyjadrené príznaky periférnej autonómnej dysfunkcie (teplé alebo studené nohy – niekedy s rozšírenými vénami na dorze nohy), poruchy sudomotoriky (suchá koža a otlaky v miestach zvýšeného tlaku na kožu) alebo ortostatická hypotenzia [10].
Fokálne a multifokálne neuropatie
Fokálne a multifokálne mononeuropatie mávajú rýchly nástup a sú výsledkom involúcie n. medianus (5,8 % všetkých diabetických neuropatií), n. ulnaris (2,1 %), n. radialis (0,6 %) a bežne n. fibularis. Neuropatie kraniálnych nervov sú extrémne zriedkavé (0,05 %). Najčastejšie z kraniálnych nervov sú postihnuté n. III, IV, VI a VII a sú pravdepodobne spôsobené mikrovaskulárnymi „infarktami“, ktoré vo väčšine prípadov odoznievajú spontánne v priebehu niekoľkých mesiacov. Pre elektrofyziologický nález je typické spomalenie rýchlosti vedenia ako aj pokles amplitúdy akčných potenciálov, čo svedčí pre axonálne – demyelinizačné poškodenie. Naproti tejto teórii o mikrovaskulárnych infarktoch, je u viac ako tretiny pacientov s DM prítomná chronická kompresia nervov (tzv. entrapment) najčastejšie n. ulnaris, n. medianus, n. fibularis a n. plantaris medialis. Pacienti s DM majú taktiež často spinálnu lumbálnu stenózu, na čo sa musí myslieť pre odlíšenie od proximálnej neuropatie či amyotrofie. Elektromyografia je kľúčovou vyšetrovacou metódou pre vylúčenie entrapmentu ako aj spinálnej stenózy (samozrejme v kombinácii s magnetickou rezonanciou) [11].
Autonómne neuropatie
Diabetické autonómne neuroaptie (DAN) vplývajú signifikantne na morbiditu ako aj mortalitu u niektorých pacientov s DM. Prevalencia DAN sa pohybuje u pacientov s DM1T medzi 1–90 % a pri DM2T medzi 20–73 % [12]. Najčastejšie autonómne funkcie, ktoré bývajú poškodené vplyvom DM s ich symptómami a diagnostickým postupom, sú zhrnuté v tab. 2. Tieto jednotlivé symptómy autonómnej dysfunkcie by mali byť cielene zisťované v dôkladnej anamnéze, obzvlášť tie, ktoré môžu mať fatálne následky.
Tab. 2. Najčastejšie poškodené autonómne systémy, ich príznaky a nutné vyšetrenia. Upravené podľa [10] ![Najčastejšie poškodené autonómne systémy, ich príznaky a nutné vyšetrenia. Upravené podľa [10]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/72d29f298ca403322af584ecf4c897f9.jpeg)
Medzi hlavné klinické manifestácie DAN patrí pokojová tachykardia, intolerancia námahy, ortostatická hypotenzia, obstipácia, gastroparéza, erektilná dysfunkcia, sudomotorická dysfunkcia a zhoršenie neurovaskulárnych funkcií [10]. Kardiovaskulárna autonómna neuropatia je stredobodom záujmu v rámci DAN, vzhľadom na riziko náhlej kardiálnej smrti [13].
Diagnostika diabetickej neuropatie
Základným predpokladom v diagnostike diabetickej neuropatie je klinické neurologické vyšetrenie. Dôležitá je podrobná anamnéza, pretože po subjektívnych ťažkostiach a príznakoch je často u diabetikov nutné aktívne pátrať cielenými otázkami [14]. Je vypracované a stále upresňované množstvo vyšetrovacích postupov s vytváraním určitých skórovacích systémov, ktoré umožňujú zaklasifikovať neuropatiu – či už podľa miery postihnutia [15], alebo prítomnosti/neprítomnosti polyneuropatie [16, 17].
Z pomocných vyšetrovacích metód v diagnostike DPN zohráva kľúčovú úlohu elektromyografia (EMG). Nie je však špecifická len pre diagnostiku DPN, ale aj pri neuropatiách inej etiológie. Základom EMG vyšetrenia je meranie rýchlosti vedenia motorickými vláknami periférnych nervov. Princíp spočíva v stimulácii a registrácii sumačných akčných motorických potenciálov (CMAP) a senzitívneho nervového akčného potenciálu (SNAP) prostredníctvom povrchových kožných elektród. Ďalšími metódami stimulačnej EMG, ktoré môžeme v diagnostike DPN použiť, je vyšetrenie H–reflexu či F–vlny [18].
U pacientov s klinicky rozvinutým DM dochádza k spomaleniu rýchlosti vedenia motorickými a senzitívnymi nervami, avšak u 20 % diabetikov, ktorí nemajú žiadne klinické príznaky neuropatie, sú taktiež abnormálne elektrofyziologické nálezy [17]. Okrem rýchlosti vedenia hodnotíme aj amplitúdu odpovedí (CMAP či SNAP), ktorých pokles svedčí pre axonálne poškodenie, zatiaľ čo spomalenie vedenia hovorí o demyelinizačnom poškodení. Pri neurografii sledujeme prevažne silné myelinizované nervové vlákna (dlhých nervov). V diagnostike a najmä v diferenciálnej diagnostike neuropatií je nutné realizovať aj ihlovú elektromyografiu. Toto vyšetrenie je dôležité hlavne u menej častých foriem diabetickej proximálnej alebo trupovej neuropatie.
EMG vyšetrenie je bez rizika pre pacienta, je možné ho opakovať s časovým odstupom a sledovať tak vývoj ochorenia, prípadne efekt liečby. Je taktiež dobe reprodukovateľné, aj s prihliadnutím na fakt, že často kontrolné EMG robí iný elektromyografista, resp. na inom EMG prístroji. Pre odhalenie signifikantných zmien na EMG je však nutné dodržať dostatočný časový odstup medzi dvoma vyšetreniami (aspoň 6 mesiacov) [17,19].
EMG vyšetrenie môže byť úplne normálne u pacientov s DPN tenkých vlákien, pri ktorej sú často výrazné klinické ťažkosti (neuropatické bolesti). Stanovenie intraepidermálnej hustoty tenkých vlákien z kožnej biopsie je metódou, ktorou sa dá na niektorých pracoviskách objektivizovať neuropatia tenkých vlákien [20].
Neuropatie asociované s diabetes mellitus
Diabetická neuropatia, obzvlášť jej najčastejšia forma – symetrická distálna senzorimotorická PNP – si zaslúži veľmi dôkladnú diagnostiku. Diferenciálne diagnostické problémy môžu nastať najmä u starších diabetikov (prevažne DM2T). Symetrická PNP ako aj fokálne neuropatie môžu byť prejavom aj iných ochorení, ktoré sa väčšinou manifestujú až v neskoršom veku (amyloidóza, gamapatie, porfýrie, systémové ochorenia, pečeňové ochorenia a iné), alebo ich môže spôsobiť aj iná príčina (chronická zápalová demyelinizačná PNP – CIDP, niektoré lieky, abúzus alkoholu, deficit vitamínov, neuroborelióza, malígne nádory, toxické látky). Preto je nutné vždy zvážiť aj iné príčiny neuropatie [17]. Podľa viacerých zdrojov od 10 % do 50 % pacientov s diabetes mellitus má popri DPN aj iný typ neuropatie [21, 22]. Nadmernú pozornosť pri stanovení diagnózy DPN je treba venovať prípadom s rýchlym rozvojom neuropatie, predovšetkým s asymetrickými a skorými motorickými príznakmi, pokiaľ sa neuropatia rozvinie krátko po manifestácii diabetu, a taktiež v prípade progresívneho priebehu neuropatie pri optimálne kompenzovanom diabete [23].
V tab. 3 sú uvedené diagnózy, na ktoré je nutné myslieť v rámci diferenciálnej diagnostiky DPN.
Tab. 3. Diferenciálna diagnostika PNP u pacientov s DM. Upravené podľa [18] ![Diferenciálna diagnostika PNP u pacientov s DM. Upravené podľa [18]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/4d53284a6836841f9af33ec1042f41d8.jpeg)
V tomto článku sme sa v rámci diferenciálnej diagnostiky DPN rozhodli bližšie venovať typom neuropatií, s ktorými sa u diabetikov môžeme v klinickej praxi stretnúť relatívne častejšie, resp. úzko súvisia s diabetom, a to sú: chronická zápalová demyelinizačná polyneuropatia (CIDP), liekmi indukovaná neuroaptia (metformínom indukovaná neuropatia a „inzulínová neuritída“) a alkoholová neuropatia.
Chronická zápalová demyelinizačná polyneuropatia
Chronická zápalová demyelinizačná polyneuroaptia (CIDP) je ochorenie charakterizované multifokálnymi demyelinizačnými zmenami na periférnych nervoch (5% postihnutie nervov CNS) na autoimunitnom podklade, charakterizované stratou sily a citlivosti. Nástup klinického obrazu je najčastejšie v priebehu 8 a viac týždňov, avšak často sa môže ochorenie vyvíjať počas mnohých mesiacov či dokonca rokov. V iniciálnom štádiu bývajú v popredí senzitívne príznaky, na rozdiel od akútnej zápalovej demyelinizačnej polyneuropatie (Guillainov–Barrého syndróm). Priebeh ochorenia môže byť relaps – remitujúci alebo chronicky progresívny. Vrchol výskytu ochorenia je v 6. až 7. dekáde života. Prevalencia ochorenia je 8,9/100 tisíc. CIDP postihuje mužov rovnako často ako ženy [24,25].
Diagnóza CIDP je založená na charakteristickom klinickom obraze, EMG a vyšetrení cerebrospinálneho likvoru. Objektívne je prítomná slabosť proximálnych a distálnych svalov a poruchy citlivosti. Môžu byť prítomné parestézie, avšak výrazná bolesť nie je charakteristická pre CIDP. Slabosť končatín je väčšinou dosť výrazná aj napriek nevýrazným (alebo neprítomným) svalovým atrofiám. Pri CIDP sú postihnuté prevažne dlhé senzitívne vlákna (propriocepcia), menej tenké vlákna (vnímanie bolesti a teploty). Myotatické reflexy bývajú na hranici výbavnosti alebo úplne nevýbavné. Postihnutie kraniálnych nervov sa vyskytuje približne u 16 %, svalový deficit v bulbárnej oblasti či deficit respiračných svalov sa vyskytuje raritne. U menej ako 10 % pacientov sa CIDP manifestuje poškodením dominantne senzitívnych dráh [26].
V diagnostike neuropatií je kľúčové elektromyografické vyšetrenie, čo platí aj pre CIDP. V EMG je nález spomaleného vedenia, ako aj prolongácia terminálnej latencie v motorických nervoch, prítomné sú bloky vedenia a časová disperzia. Senzorické akčné potenciály majú výrazne nízku amplitúdu alebo úplne chýbajú. Existuje asi 16 elektrodiagnostických kritérií pre CIDP avšak v súčasnosti sa stále akceptujú revidované EMG kritériá podľa expertov z EFNS/ENS z roku 2010 [26,27].
V cerebrospinálnom likvore bývajú často mierne zvýšené hodnoty proteinorachie bez významnejšej pleocytózy [26].
Pomocnou metódou v diagnostike CIDP (ako aj pri odlíšení od DPN) je biopsia nervu, avšak v prípade negatívneho nálezu zápalových demyelinizačných zmien nie je diagnóza CIDP vylúčená.
Niektoré štúdie upriamujú pozornosť na možnú asociáciu medzi CIDP a DM [28]. Na druhej strane sa v iných prácach táto asociácia nedokázala [24]. Brill et al v 2016 vyhodnotili na základe dostupnej literatúry vedecké práce zaoberajúce prevalenciou CIDP a asociáciou s DM za obdobie 2009 až 2013, na základe čoho prišli k záveru, že prevalencia CIDP je vyššia u pacientov s DM ako u pacientov bez DM [29]. Či je DM možným rizikovým faktorom pre vznik CIDP, stále ostáva neobjasnené.
Vzhľadom na to, že CIDP v porovnaní s DPN je relatívne dobre liečiteľná neuropatia (kortikoidy, imunoglobulíny, cytostatiká), u pacientov s diabetom je na ňu nutné vždy myslieť. V tab. 4 sú uvedené hlavné rozdiely (v klinickom ako aj EMG náleze) medzi DPN a CIDP.
Tab. 4. Hlavné rozdiely medzi DPN a CIDP 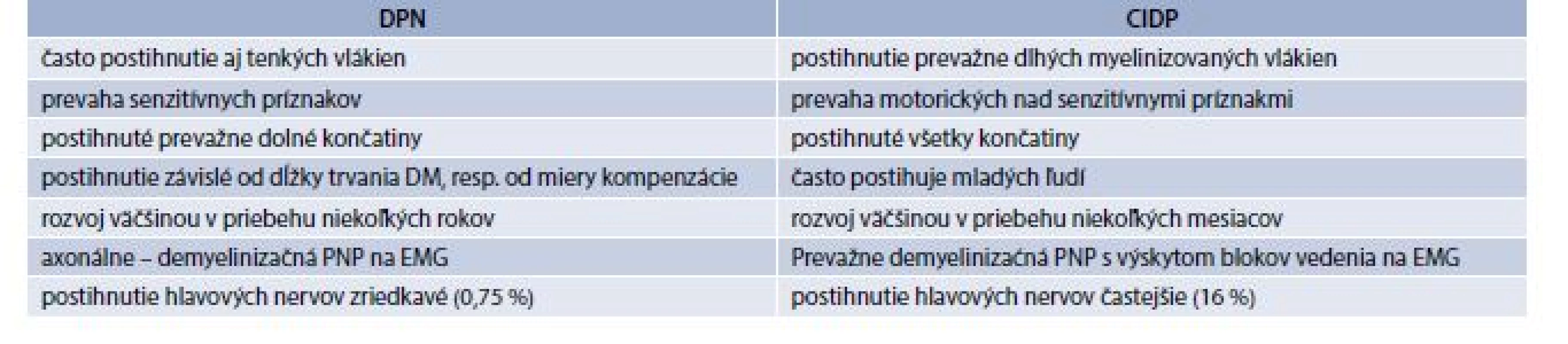
Polyneuropatie indukované antidiabetikami
Metformínom indukovaná neuropatia
Metformín je „základný kameň“ v liečbe DM2T. Po celom svete je rutinne predpisovaný viac ako 120 miliónom pacientov [30]. Viacerými observačnými a intervenčnými štúdiami bola dokázaná asociácia medzi dlhodobým užívaním metformínu a deficitom vitamínu B12. Prevalencia hypovitaminózy B12 pri liečbe metformínom podľa rôznych zdrojov varíruje medzi 5,8 % a 52 % [31].
Jedinou klinickou prezentáciou deficitu vitamínu B12 môže byť neuropatia, ktorá sa prejavuje identicky ako diabetická polyneuropatia. Neuropatia pri hypovitaminóze B12 môže prebiehať aj subklinicky a taktiež súčasne s DPN, čo môže často spôsobovať diagnostické rozpaky [32].
Podľa poslednej práce Olta a Oznasa hypovitaminóza B12 indukovaná metformínom signifikantne nezvyšuje frekvenciu výskytu periférnej neuropatie [33]. Podľa Ahmeda et al takmer tretina pacientov s DM2T mala deficit vitamínu B12, avšak tento deficit nebol asociovaný s vyšším výskytom periférnej neuropatie. Zistili taktiež, že čierna rasa vplýva na deficit vitamínu B12 ako protektívny faktor [34].
Vzhľadom na tieto skutočnosti, stále nie je jasné, do akej miery vplýva liečba metformínom u pacientov s DM2T na predpokladanú zvýšenú prevalenciu neuropatie.
Inzulínová neuritída
Liečbou indukovaná neuropatia u pacientov s diabetes mellitus sa môže vyvinúť pri náhlej úprave glykémií (predovšetkým inzulínom) u tých pacientov, ktorí mali pred liečbou dlhodobo hyperglykémiu. Tento typ neuropatie je považovaný za raritnú komplikáciu liečby DM a nazýva sa taktiež inzulínová neuritída (IN) [35].
Inzulínová neuritída je najčastejšie charakterizovaná akútnym bolestivým začiatkom a autonómnou dysfunkciou v súvislosti s rýchlou úpravou glykemických hodnôt. Bolesti sú väčšinou pálivé alebo vystreľujúce, distálne alebo difúzne, s proximálnym šírením a často sprevádzané alodýniou a hyperalgéziou. Autonómne symptómy sa objavujú v rovnakom čase alebo krátko po nástupe bolestí. Neuropatia postihuje dominantne tenké vlákna (autonómne a somatosenzorické) s minimálnym alebo žiadnym poškodením silných myelinizovaných vlákien (negatívne klinické či EMG vyšetrenie silných senzitívnych vlákien). Autonómne testy môžu odhaliť pokročilú alebo aj ťažkú sympatikovú a parasympatikovú dysfunkciu. U niektorých pacientov môže už na začiatku dominovať poškodenie vegetatívneho nervového systému, čo sa prejavuje ortostatickou hypotenziou a synkopami. Presné dáta o frekvencii výskytu inzulínovej neuritídy zatiaľ nie sú známe, v niektorých prácach sa na malých súboroch udáva až u 10,9 % pacientov s diabetickou neuropatiou [36].
Inzulínová neuritída sa od najčastejšie sa vyskytujúcej DPN líši vo viacerých aspektoch. Neuropatické bolesti majú akútny začiatok na rozdiel od pomalého nástupu pri DPN [37]. Bolesť pri IN má výrazne vyššiu intenzitu a nezaberá dostatočne na analgetiká (vrátane opioidov), v porovnaní s DPN, ktorá často „zaberá“ aj na nesteroidné antiflogistiká. Taktiež distribúcia aj charakter bolestí sú rozdielne (pri DPN skôr distálne, pri IN alodýnia a hyperalgézia). Autonómne symptómy sú bežné, vznikajú akútne v porovnaní s relatívne nízkym výskytom, pomalým nástupom a pomalou progresiou pri DPN [37].
Je nutné zdôrazniť, že príznaky pri IN sú často reverzibilné, preto je nutné pri liečbe DM a výskyte periférnej neuropatie myslieť aj na liekmi indukované neuropatie.
Alkoholová neuropatia
Pacienti s DM pravidelne konzumujúci alkohol majú vyššie riziko rozvoja PNP a v rozvinutých krajinách je alkoholová neuropatia druhou najčastejšou po diabetickej neuropatii [38]. Vzhľadom na rastúcu spotrebu alkoholu v populácii preto treba aj u diabetikov myslieť na tento typ PNP.
Prevalencia periférnej neuropatie u chronických alkoholikov sa odhaduje medzi 25–66 % a postihuje častejšie ženy [39]. Za najvýznamnejší faktor sa považuje dĺžka konzumácie a celková dávka alkoholu. V patogenéze sa uplatňuje, okrem priameho toxického účinku alkoholu na axóny, aj nutričný alebo vitamínový deficit a porucha utilizácie, predovšetkým tiamínu. Etanol znižuje jeho resorpciu z čreva, znižuje jeho zásoby v pečeni a bráni jeho fosforylácii, ktorá ho konvertuje na aktívnu formu [39]. Rozlišujú sa dve základné formy alkoholovej neuropatie – bez deficitu tiamínu (senzitívna a bolestivá distálna neuroaptia s poruchou tenkých vlákien) a s deficitom tiamínu (senzitívne aj motorické príznaky s postihnutím tenkých aj silných vlákien). Zvyčajne sa neuropatia manifestuje najskôr senzitívnymi symptómami na nohách, ktoré spĺňajú kritériá pre neuropatickú bolesť. Ďalšia progresia pri pokračovaní v konzumácii alkoholu zahŕňa aj postihnutie silných senzitívnych vlákien s rozvojom senzitívnej ataxie, ktorá sa môže kombinovať aj so spinálnou ataxiou pri súčasnej karencii vitamínu B12. Motorický deficit je menej nápadný než senzitívne symptómy a je výrazný u plne rozvinutých foriem s obrazom chabej paraparézy. Alkoholová neuropatia je často sprevádzaná výraznými sudomotorickými poruchami (hyperhidróza) na horných aj dolných končatinách v rámci postihnutia autonómnych vlákien (vlhké a studené nohy aj ruky). Z laboratórnych testov je v rutínnom biochemickom vyšetrení zistená elevácia transamináz (hlavne gama–glutamyltransferáza – GMT), hypoalbuminémia a v krvnom obraze často makrocytóza. Na EMG je typický nález distálnej symetrickej axonálnej (alebo axonálne-demyelinizačnej) motorickej a senzitívnej neuropatie (nález podobný ako pri DPN). Likvorologické vyšetrenie je normálne. Liečba je podmienená abstinenciou a zahŕňa dostatočnú suplementáciu tiamínu a dostatočný prísun proteínov. Prognóza je priaznivá, avšak zlepšenie neuropatie sa objavuje až po niekoľkých mesiacoch, za predpokladu dodržiavania zdravej životosprávy a alkoholovej abstinencie [40].
Záver
Diabetická neuropatia je najčastejšia forma periférnej neuropatie v rozvinutých krajinách sveta, avšak je nutné mať na mysli, že nie všetci pacienti s diabetes mellitus a periférnym nervovým poškodením majú neuropatiu spôsobenú samotným diabetom. Množstvo štúdií upriamuje pozornosť na prítomnosť ďalších príčin vzniku neuropatie u diabetikov. Podľa viacerých zdrojov až u 10–50 %pacientov s DM sa môže podieľať na neuropatii okrem vplyvu základného ochorenia aj iná príčina, dokonca aj kombinácia viacerých. Patria sem napríklad neurotoxicita liekov, abúzus alkoholu, deficit vitamínu B12, renálne ochorenia, chronická zápalová demyelinizačná polyneuropatia, hereditárne neuropatie, vaskulitídy a iné. Z tohto dôvodu je nutné pri manažmente pacienta s diabetes mellitus vnímať ochorenie komplexne a komplikácie ochorenia (ako je diabetická neuropatia) riešiť individuálne so zreteľom na možnosť koincidencie s inými, často zákernejšími a ťažšie diagnostikovateľnými ochoreniami. Správna diagnostika periférnej neuropatie u pacienta s diabetes mellitus je kľúčová, vzhľadom na to, že na rozdiel od diabetickej neuropatie, ostatné vyššie uvedené neuropatie vieme často úspešne a dlhodobo liečiť.
Zoznam skratiek
PNP – polyneuropatia
DPN – diabetická polyneuropatia
CIDP – chronická zápalová demyelinizačná polyneuropatia
IN – inzulínová neuritída
EMG – elektromyografia
CMAP – sumačný akčný potenciál motorickej jednotky
SNAP – senzitívny nervový akčný potenciál
DM – Diabetes mellitus
ASN – akútna senzitívna neuropatia
DAN – diabetická autonómna neuropatia
Doručené do redakcie: 22. 10. 2018
Prijaté po recenzii: 30. 11. 2018
MUDr. Peter Matejička
Zdroje
1. Edwards JL, Vincent AM, Cheng HT, Feld - man EL: Diabetic neuropathy: mechanisms to management. Pharmacol Ther 2008; 120(1): 1–34. Dostupné z DOI: <http://dx.doi.org/10.1016/j.pharmthera.2008.05.005>.
2. Wild S, Roglic G, Green A et al. Global prevalence of diabetes: esti - mates for the year 2000 and projections for 2030. Diabetes Care 2004; 27(5): 1047–1053.
3. Zimmet P, Alberti KG, Shaw J. Global and so - cietal implications of the diabetes epidemic. Nature 2001 ;414(6865): 782–787. Dostupné z DOI: <http://dx.doi.org/10.1038/414782a>.
4. Dyck PJ, Thomas PK. Peripheral neuropathy. 4rd ed. Elsevier Saunders: 2005. ISBN 978–0721694917.
5. Shaw J, Zimmet PZ. The epidemiology of diabetic neuropathy. Diabetes Rev 1999; 7(4): 245–252.
6. Mazanec R, Bojar M, Nedělka T. Diabetická neuropatie z pohledu neurologa. Neurol Praxi 2009; 10(6): 378–383.
7. Tešić D, Cvijanović M, Pantelinac P. Akutna bolna neuro-patija. Med Pregl 1995;48(11–12):425–8.
8. Cvijanović M, Ilin M, Slankamenac P et al. The sensitivity of electromyonurography in the diagnosis od Diabetic polyneuropathy. Med Pregl 2011; 64(1–2): 11–14.
9. Thomas PK. Classification, differential diagnosis and staging of diabetic peripheral neuropathy. Diabetes 1997; 46(Suppl 2): S54–S57.
10. Boulton AJ, Vinik AI, Arezzo JC et al. American Diabetes Association Diabetic neuropathies: a statement by the American Diabetes Association. Diabetes Care 2005 ;28(4): 956–962.
11. Vinik A, Mehrabyan A, Colen L et al. Focal entrapment neuropathies in diabetes (Review). Diabetes Care 27(7): 1783–1788, 2004
12. Dimitropoulos G, Tahrani AA, Stevens MJ. Cardiac autonomic neuropathy in patients with diabetes mellitus. World J Diabetes 2014;5(1):17–39. Dostupné z DOI: <http://dx.doi.org/10.4239/wjd.v5.i1.17>.
13. Pop-Busui R, Evans GW, Gerstein HC et al. [Action to Control CardiovascularRisk in Diabetes Study Group]. Effects of cardiac autonomic dysfunction on mortality risk in the Action to Control Cardiovascular Risk in Diabetes (ACCORD) trial. Diabetes Care 2010; 33(7): 1578 - 1584. Dostupné z DOI: <http://dx.doi.org/10.2337/dc10–0125>.
14. Duby JJ, Campbell RK, Setter SM et al. Diabetic neuropathy: An intensive review. Am J Health-Syst Pharm 2004; 61(2): 160–173; quiz 175–6.
15. Dyck PJ, Davies JL, Wilson DM et al. Risk Factors for Severity of Diabetic Polyneuropathy: intensive longitudinal assessment of the Rochester Diabetic Neuropathy Study cohort. Diabetes Care 1999; 22(9): 1479–1486.
16. Meijer JW, Smit AJ, Lefrandt JD et al. Back to Basics in Diagnosing Diabetic Polyneuropathy With the Tuning Fork! Diabetes Care 2005; 28(9): 2201–2205.
17. Vinik AI, Pittenger GL, Barlow P et al. Diabetic Neuropathies. In: LeRoith D, Taylor SI, Olefsky JM. Diabetes mellitus A fundamental and clinical text. Lippincot Williams and Williams: Philadeplhia 2003 : 1331–1363. ISBN 978–0781740975.
18. Vondrová H. Diagnostika a diferenciální diagnostika diabetické polyneuropatie. Neurol Praxi 2010; 11(1): 41–44.
19. Wilbourn AJ. The diabetic neuropathies. In: Brown WF, Bolton CF. Clinical electromyography. 2nd ed. Butterworths: Boston 1987; 329–364. ISBN 978–0409951639
20. Vlcková-Moravcova E, Bednarik J, Belobradkova J et al. Small fibre involvement in diabetic patients with neuropathic foot pain. Diabet Med 2008; 25(6): 692–699. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1464–5491.2008.02446.x>.
21. Gorson KC, Ropper AH. Additional causes for distal sensory polyneuropathy in diabetic patients. J Neurol Neurosurg Psychiatry 2006; 77(3): 354–358. Dostupné z DOI: <http://dx.doi.org/10.1136/jnnp.2005.075119>.
22. Lozeron P, Nahum L, Lacroix C et al. Symptomatic diabetic and non-diabetic neuropathies in a series of 100 diabetic patients. J Neurol 2002, 249(5): 569–575. Dostupné z DOI: <http://dx.doi.org/10.1007/s004150200066>.
23. Ziegler D. Painful diabetic neuropathy: advantage of novel drugs over old drugs? Diabetes Care 2009; 32(Suppl 2: S414–S419. Dostupné z DOI: <http://dx.doi.org/10.2337/dc09-S350>.
24. Laughlin RS, Dyck PJ, Melton LJ et al. Incidence and prevalence of CIDP and the association of diabetes mellitus. Neurology 2009, 73(1): 39–45. Dostupné z DOI: <http://dx.doi.org/10.1212/WNL.0b013e3181aaea47>.
25. Koller H, Kieseier BC, Jander S et al. Chronic inflammatory demyelinating polyneuropathy. N Engl J Med 2005; 352(13): 1343–1356. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMra041347>.
26. Koski CL, Baumgarten M, Magder LS et al. Derivation and validation of diagnostic criteria for chronic inflammatory demyelinating polyneuropathy. J Neurol Sci 2009, 277(1–2): 1–8. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jns.2008.11.015>.
27. Bednařík J. Chronická zánětlivá demyelinizační neuropatie. Neurológia Praxi 2016; 17(1): 16–21.
28. Haq RU, Pendlebury WW, Fries TJ et al. Chronic inflammatory demyelinating polyradiculoneuropathy in diabetic patients. Muscle Nerve 2003, 27(4):465–470. Dostupné z DOI: <http://dx.doi.org/10.1002/mus.1250>.
29. Bril V, Blanchetteb CM, Nooneb KM et al. The dilemma of diabetes in chronic inflammatory demyelinating polyneuropathy, J Diabetes Complications 2016; 30(7): 1401–1407. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jdiacomp.2016.05.007>.
30. Viollet B, Guigas B, Sanz Garcia N et al Cellular and molecular mechanisms of metformin: an overview. Clin Sci (Lond) 2012;122(6):253–270. Dostupné z DOI: <http://dx.doi.org/10.1042/CS20110386>.
31. Reinstatler L, Williamson RS, Garn JV et al. Association of biochemical B₁₂ deficiency with metformin therapy and vitamin B₁₂ supplements: the National Health and Nutrition Examination Survey, 1999–2006. Diabetes Care 2012; 35(2):327–333. Dostupné z DOI: <http://dx.doi.org/10.2337/dc11–1582>.
32. Briani C, Dalla Torre C, Citton V et al. Cobalamin deficiency: clinical picture and radiological findings. Nutrients 2013; 5(11): 4521–4539. Dostupné z DOI: <http://dx.doi.org/10.3390/nu5114521>.
33. Olt S, Oznas O. Investigation of the vitamin B12 deficiency with peripheral neuropathy in patients with type 2 diabetes mellitus treated using metformin. North Clin Istanb 2017; 4(3): 233–236. Dostupné z DOI: <http://dx.doi.org/10.14744/nci.2017.98705>.
34. Ahmed MA, Muntingh G, Rheeder P. Vitamin B12 deficiency in metformin-treated type-2 diabetes patients, prevalence and associationwith peripheral neuropathy. BMC Pharmacol Toxicol 2016; 17(1): 44. Dostupné z DOI: <http://dx.doi.org/10.1186/s40360–016–0088–3>.
35. Dabby R, Sadeh M, Lampl Y et al. Acute painful neuropathy induced by rapid correction of serum glucose levels in diabetic patients. Biomed Pharmacother 2009; 63(10): 707–709. Dostupné z DOI: <http://dx.doi.org/10.1016/j.biopha.2008.08.011>.
36. Gibbons CH, Freeman R. Treatment-induced diabetic neuropathy: a reversible painful autonomic neuropathy. Ann Neurol 2010; 67(4): 534–41. Dostupné z DOI: <http://dx.doi.org/10.1002/ana.21952>.
37. Tesfaye S, Vileikyte L, Rayman G et al. Painful diabetic peripheral neuropathy: consensus recommendations on diagnosis, assessment and management. Diabetes Metab Res Rev 2011; 27(7): 629–638. Dostupné z DOI: <http://dx.doi.org/10.1002/dmrr.1225.>.
38. Elgendy R, Deschênes SS, Burns RJ et al. Alcohol consumption, depressive symptoms, and the incidence of diabetes-related complications. J Diabetes 2018. Dostupné z DOI: <http://dx.doi.org/10.1111/1753–0407.12822>.
39. Ambler Z. Poruchy periferních nervů. Triton: Praha 2013. ISBN 9788073877057.
40. Mazanec, R, Baumgartner D, Potočková V. Toxická neuropatie. Neurol Praxi 2017; 18(1): 20–24.Štítky
Diabetologie Endokrinologie Interní lékařství
Článek Z odbornej literatúry
Článek vyšel v časopiseForum Diabetologicum
Nejčtenější tento týden
2018 Číslo 3- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
- Neurologické komplikácie a neuropsychiatrické komorbidity diabetes mellitus
- Polyneuropatie u pacientov s diabetes mellitus
- Kardiální autonomní neuropatie jako závažná komplikace diabetes mellitus
- Neuropsychiatrické komplikácie diabetes mellitus
- Poruchy rovnováhy pri diabetes mellitus
- Diabetes mellitus u staršího komplikovaného pacienta
- Proximálna diabetická amyotrofia: kazuistiky
- Kongres Európskej asociácie pre srdcové zlyhávanie (HFA ESC) 26.–29. mája 2018, Viedeň
- Z odbornej literatúry
- Forum Diabetologicum
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Polyneuropatie u pacientov s diabetes mellitus
- Poruchy rovnováhy pri diabetes mellitus
- Proximálna diabetická amyotrofia: kazuistiky
- Kardiální autonomní neuropatie jako závažná komplikace diabetes mellitus
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



