-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Diabetická nefropatia: diagnostika, prevencia a liečba
Autoři: Adrián Okša; Peter Ponťuch; Viera Spustová; Emil Martinka; Zuzana Némethyová; Vladimír Uličiansky
Působiště autorů: za výbor Slovenskej nefrologickej spoločnosti, za výbor Slovenskej diabetologickej spoločnosti
Vyšlo v časopise: Forum Diab 2013; 2(2-Suppl 1): 1-6
Kategorie: Diabetická nefropatia: odporúčané postupy SNS a SDS
Odporúčané postupy Slovenskej nefrologickej spoločnosti a Slovenskej diabetologickej spoločnosti
1 Úvod
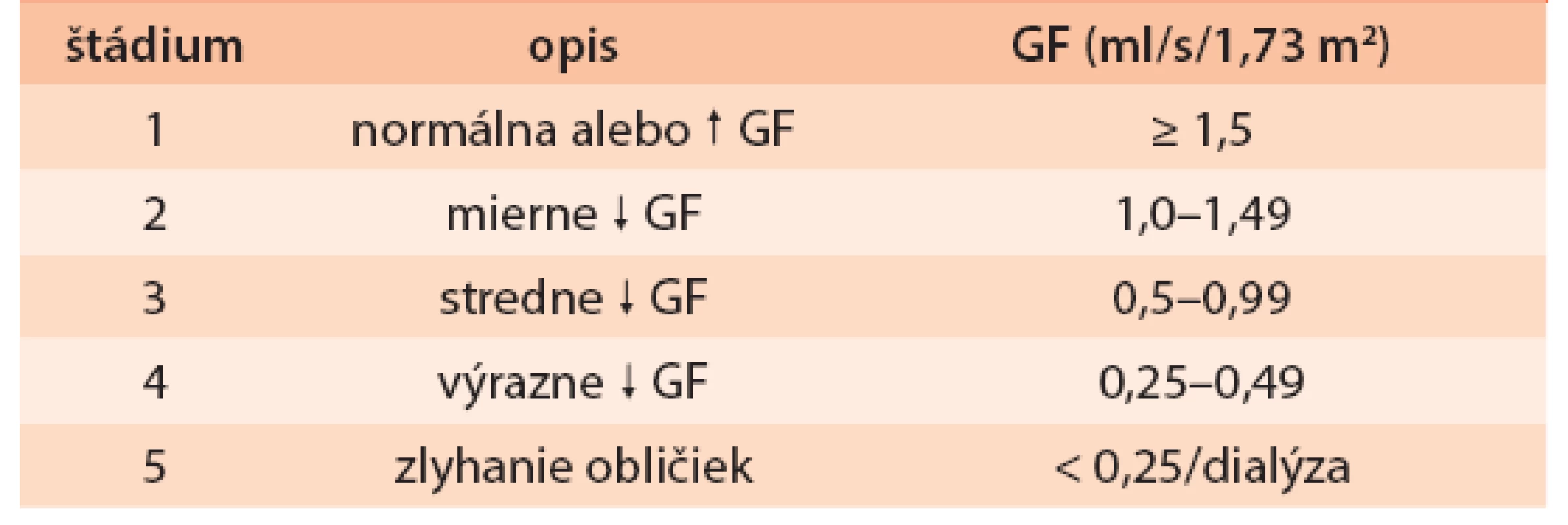
Chronické choroby obličiek (CKD – chronic kidney disease) sa stali – podobne ako diabetes mellitus – celosvetovým zdravotníckym problémom. Ich výskyt narastá do epidemických rozmerov v rozvinutom aj rozvojovom svete. Na základe všeobecne akceptovanej klasifikácie CKD podľa americkej National Kidney Foundation (NKF KDOQI) tab. 1, sa ich prevalencia v rôznych krajinách odhaduje na 9–13 %. Pacienti s terminálnym zlyhaním obličiek, resp. dialyzovaní tvoria len nepatrnú časť populácie (asi 0,1 %), väčšina chorých sa nachádza v prvých 3 štádiách s normálnou až stredne zníženou glomerulovou filtráciou (GF). Práve tieto štádiá chronických nefropatií zostávajú často nediagnostikované, čo prispieva k progresii choroby až do chronického zlyhania obličiek (CHZO). V USA a v Európe je v súčasnosti diabetes mellitus najčastejšou príčinou CHZO s podielom okolo 40 %. Navyše predstavujú CKD, rovnako ako diabetes, významný faktor kardiovaskulárneho rizika a kombinácia oboch rapídne zhoršuje celkovú prognózu pacienta.
2 Epidemiológia
Epidemiologické údaje o diabetickej nefropatii (DN) sú spoľahlivejšie u diabetikov 1. typu, u ktorých je možné presnejšie stanoviť trvanie diabetu. V tejto skupine bývala prevalencia DN (bez ohľadu na jej štádium) 30–40 % po 15–20 rokoch trvania diabetu. Novšie štúdie z viacerých európskych krajín uvádzajú podstatne nižší výskyt manifestnej DN (< 10 %), ako aj progresie do CHZO (< 3 %) pravdepodobne v súvislosti s lepšou kontrolou glykémie a krvného tlaku. U diabetikov 2. typu existujú v prevalencii DN veľké rasové a etnické rozdiely, ale v Európe je v súčasnosti renálne riziko porovnateľné s diabetom 1. typu. Podľa štatistickej ročenky NCZI malo u nás v roku 2010 manifestnú DN 11,7 % diabetikov a CHZO na podklade DN 32,4 % pacientov v pravidelnej dialyzačnej liečbe.
3 Patogenéza a morfologický obraz
Pre vznik DN je rozhodujúce diabetické prostredie s chronickou hyperglykémiou, ktorá spôsobuje zmeny v štruktúre a funkcii všetkých súčastí filtračnej bariéry – endotelu, glomerulovej bazálnej membrány (GBM) a podocytov, ako aj mezangia a tubulárnych buniek. Na tomto procese sa podieľajú viaceré mechanizmy: neenzýmová glykácia proteínov s tvorbou produktov pokročilej glykácie (AGEs), polyolová cesta metabolizmu glukózy, zvýšená aktivita intrarenálneho renín-angiotenzínového systému (RAS), zvýšená produkcia rastových faktorov a cytokínov s prozápalovými a proliferatívnymi účinkami v mezangiu, endotelová dysfunkcia, znížený obsah fyziologických glykozaminoglykanov v GBM, znížená expresia nefrínu a iných proteínov filtračnej bariéry produkovaných podocytmi a iné. Súčasne sa od skorého štádia vývoja DN uplatňujú hemodynamické zmeny so zvýšenou perfúziou glomerulov, intraglomerulovou hypertenziou a hyperfiltráciou, ktoré potencujú vývoj glomerulosklerózy a sekundárnej tubulointersticiálnej fibrózy. Pre účasť genetických faktorov na patogenéze DN svedčí jej častejší výskyt v rodinách pacientov pri oboch typoch diabetu: identifikoval sa možný podiel génových polymorfizmov viacerých zložiek RAS, aldózoreduktázy, proteínkinázy C a i.
DN nemá špecifický morfologický obraz. V prvých štádiách sa pozoruje zhrubnutie GBM, neskôr expanzia mezangia s hromadením extracelulárnej hmoty a rozvojom glomerulosklerózy (typická je nodulárna, ale častejšia difúzna forma), ktorá vedie postupne k oklúzii kapilárnych slučiek a zániku glomerulov. V pokročilom štádiu DN býva prítomná hyalinóza arteriol, atrofia tubulov a fibróza interstícia.
4 Klinický obraz
Perzistentná mikroalbuminúria je zvyčajne prvým klinickým prejavom DN pri diabete 1. typu (DM1T) a markerom vzniku DN pri diabete 2. typu (DM2T). Typický vývoj DN pri diabete 1. typu je zhrnutý v tab. 2, s. S2. Takýto priebeh môže byť dnes významne modifikovaný intenzifikovanou inzulínovou liečbou, ako aj štandardným používaním inhibítorov RAS: oba postupy znižujú albuminúriu/proteinúriu a spomaľujú pokles GF (podrobnejšie v časti 6).
Tab. 2. Vývoj DN pri diabete 1. typu 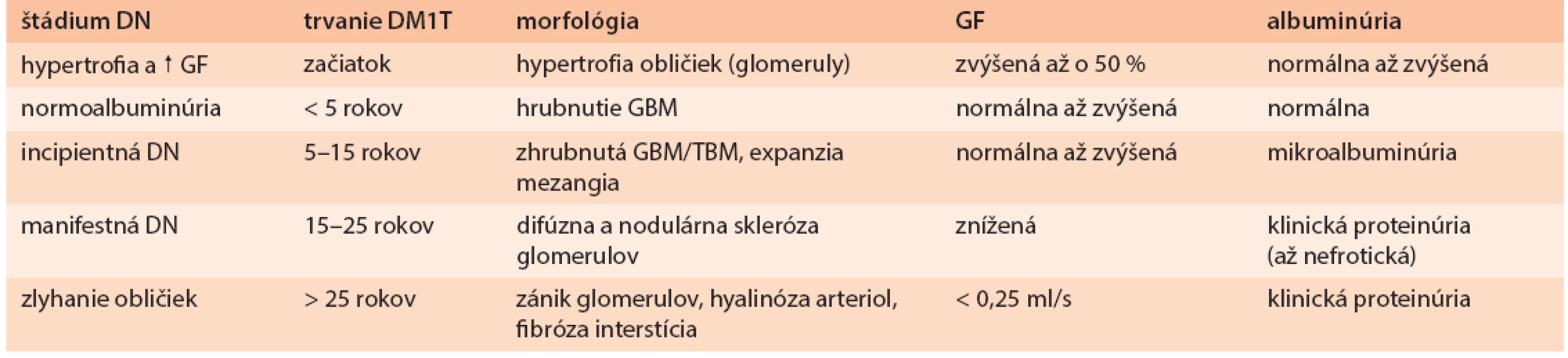
G(T)BM – glomerulová (tubulárna) bazálna membrána Kým pri DM1T existuje pomerne dobrá korelácia medzi trvaním diabetu, histopatologickým nálezom v obličkách a stupňom albuminúrie či poklesom GF (štádiá DN podľa Mogensena), situácia pri DM2T je odlišná: v bioptických štúdiách u diabetikov 2. typu s mikroalbuminúriou malo asi 40 % zmeny typické pre DN, 30 % normálny nález a 30 % nediabetické zmeny. Priebeh DN je pri DM2T ovplyvnený vyšším vekom a komorbiditami (ateroskleróza, esenciálna hypertenzia, chronické srdcové zlyhávanie, obezita a iné). U časti diabetikov 1. aj 2. typu sa poškodenie obličiek prejavuje najskôr poklesom GF bez prítomnosti mikroalbuminúrie, preto skríning DN má novšie zahŕňať aj výpočet GF. Diferenciálna diagnostika nefropatie u diabetika je zhrnutá v časti 5.2.
5 Diagnostika
5.1 Skríning
Skríning DN zahŕňa vyšetrenie mikroalbuminúrie a výpočet GF. Oba parametre by sa mali stanovovať najmenej raz do roka, a to po 5 rokoch trvania diabetu 1. typu a od určenia diagnózy diabetu 2. typu. Diagnostické kritériá DN pri rôznych spôsoboch stanovenia mikroalbuminúrie uvádza tab. 3. Americká diabetologická asociácia (ADA) aj NKF odporúčajú vyšetrenie pomeru koncentrácie albumínu a kreatinínu v náhodnej (väčšinou rannej) vzorke moču, ktorý má dostatočnú senzitivitu a špecifickosť v porovnaní so zbernými metódami (> 85%) a odstraňuje ich nevýhody. Pre možnosť spontánnej alebo liečbou navodenej regresie vyžaduje nález mikroalbuminúrie potvrdenie aspoň v 2 vzorkách z 3 odobratých v rozmedzí 3–6 mesiacov. Súčasne je potrebné vylúčenie interferencie (falošnej pozitivity) najčastejšie pri fyzickej záťaži, (uro)infekcii, horúčke, výraznej hyperglykémii, hypertenzii a srdcovom zlyhávaní.
Tab. 3. Vyšetrenie albuminúrie 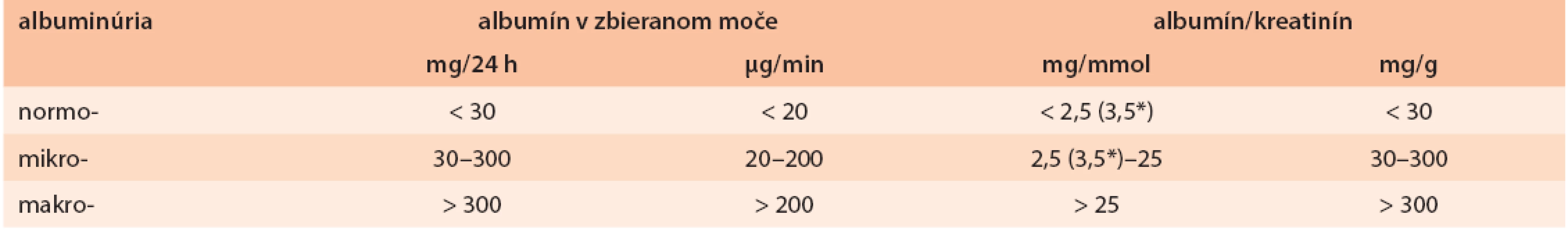
* u žien Na výpočet GF sa dnes preferuje zjednodušená rovnica MDRD-4 (podľa štúdie Modification of Diet in Renal Disease), ktorá okrem koncentrácie sérového kreatinínu (Krs) zohľadňuje vek, pohlavie a rasu:
GF [ml/s/1,73 m2] = 547,1535* × Krs -1,154 [µmol/l] × vek -0,203 × (0,742 u žien) × (1,21 u afroameričanov)
* pri medzinárodne štandardizovanej metóde stanovenia Krs má koeficient hodnotu 515,3832
Ďalšie metódy výpočtu GF (napr. CKD-EPI) sa v súčasnosti overujú. Starší spôsob výpočtu clearance kreatinínu podľa Cockcrofta-Gaulta je menej presný (najmä pri oboch krajných hodnotách GF, u obéznych a starších ľudí). Samotný sérový kreatinín je veľmi hrubým ukazovateľom renálnych funkcií, a nemal by sa v diagnostike CKD používať bez súčasného výpočtu GF, ktorý umožňuje aj určenie štádia nefropatie (tab. 1, s. S1). Kalkulácia GF by sa mala stať bežnou súčasťou vyšetrenia kreatinínu v každom biochemickom laboratóriu.
Výpočet GF má aj svoje úskalia, o ktorých musí najmä nefrológ vedieť: nezohľadňuje faktory ovplyvňujúce koncentráciu kreatinínu v sére, ako je podiel živočíšnych bielkovín v strave, výživové doplnky s obsahom kreatínu (metabolizuje sa na kreatinín), svalová záťaž (kreatín → kreatinín), zmeny v tubulárnej sekrécii kreatinínu, lieky (fibráty!), extrarenálny clearance kreatinínu a pod. Výpočet väčšinou nadhodnocuje skutočnú GF, a to tým viac, čím je vyššia, a nedá sa použiť pri náhlych zmenách GF. Tieto poznatky treba vziať do úvahy pri diagnostike a klasifikácii štádia DN.
5.2 Diferenciálna diagnostika
U väčšiny diabetikov s chronickou nefropatiou sa dá predpokladať jej diabetický pôvod, ak je prítomná:
- makroalbuminúria (klinická či manifestná proteinúria) alebo
- mikroalbuminúria spolu s diabetickou retinopatiou, resp. mikroalbuminúria pri DM1T trvajúcom najmenej 10 rokov
V ostatných prípadoch treba starostlivo zvážiť aj možnosť nediabetickej nefropatie, ktorá vyžaduje odlišný terapeutický postup. V diferenciálnej diagnostike pomáha, ak sa súčasne berie do úvahy nielen stupeň albuminúrie, ale aj GF (štádium nefropatie), tab. 4.
Tab. 4. Pravdepodobnosť DN u diabetika podľa albuminúrie a GF (podľa NKF) 
DN- – diagnóza DN nepravdepodobná; DN+ – diagnóza DN pravdepodobná ↑ – rast rizika DN (vysvetlenie v texte) Typické, a dokonca aj pokročilé diabetické zmeny na glomeruloch sa dajú nájsť u časti pacientov s normálnou alebo mierne zníženou GF (štádium 1–2). Na začiatku rozvoja DN (ale aj iných nefropatií) totiž obličky hyperfiltrujú a nález tzv. normálnej GF môže znamenať už významnú stratu funkcie. Preto majú aj títo pacienti zvýšené riziko DN, najmä ak sú prítomné ďalšie rizikové faktory ako nedostatočná kontrola glykémie, dlhšie trvanie diabetu, hypertenzia, retinopatia, tzv. vyššia normálna albuminúria, iná než biela (europoidná) rasa a rodinná anamnéza DM2T, DN, hypertenzie, či kardiovaskulárnych chorôb. Ďalší pokles GF pod 1 ml/s pri normoalbuminúrii síce prítomnosť DN nevylučuje, ale pravdepodobnejšie sú nediabetické zmeny podobne ako pri výraznom znížení GF (štádium 4–5) s mikroalbuminúriou. Diferenciálno-diagnostické úvahy komplikuje aj fakt, že liečba blokátormi RAS môže spôsobiť posun od makroalbuminúrie do mikroalbuminúrie, resp. od mikroalbuminúrie do normoalbuminúrie.
Čiastočnú pomoc pri diferenciálnej diagnostike nefropatie u diabetika predstavuje nález diabetickej retinopatie. Senzitivita a špecifickosť retinopatie ako markera DN sa významne líši podľa stupňa albuminúrie. Pri mikroalbuminúrii je vysoká predovšetkým negatívna prediktívna hodnota (takmer 100%), t. j. absencia retinopatie svedčí s vysokou pravdepodobnosťou proti DN. Pri makroalbuminúrii je naopak vyššia pozitívna prediktívna hodnota, t. j. prítomnosť retinopatie poukazuje s vysokou pravdepodobnosťou na DN.
Okolnosti, pri ktorých treba u diabetika myslieť na nediabetickú nefropatiu, možno zhrnúť nasledovne:
- chýbanie diabetickej retinopatie (najmä u diabetikov 2. typu s mikroalbuminúriou)
- nízka GF s normoalbuminúriou a mikroalbuminúriou, rýchly pokles GF
- rýchly nárast proteinúrie
- rezistentná hypertenzia
- pokles GF > 30 % behom 2–3 mesiacov po začatí liečby blokátormi RAS
- príznaky inej systémovej choroby
V odôvodnených prípadoch je indikovaná renálna biopsia.
6 Prevencia a liečba
V prevencii a liečbe DN má zásadný význam kontrola glykémie, liečba hypertenzie, dyslipoproteinémie a úprava diétneho režimu s obmedzeným príjmom bielkovín.
6.1 Kontrola glykémie
Randomizované kontrolované štúdie ukázali, že zníženie koncentrácie HbA1c pod 7 % pri intenzifikovanom inzulínovom režime spomaľuje rozvoj mikroalbuminúrie, resp. jej progresiu do makroalbuminúrie u oboch typov diabetu. Slabšie sú dôkazy o tom, že takýto postup spomaľuje aj pokles GF (väčšinou malé súbory pacientov s nižšou štatistickou silou). Spoločným nedostatkom uvedených štúdií je, že zahrnuli len málo pacientov s pokročilejšou DN v štádiu 3–5. U týchto diabetikov (najmä 1. typu) je riziko hypoglykémie pri intenzifikovanej liečbe niekoľkonásobne vyššie pre znížený clearance inzulínu, ako aj zníženú glukoneogenézu v obličkách. Stav vyžaduje starostlivé monitorovanie glykémie, prípadne zníženie dávky inzulínu.
S poklesom GF sa znižuje aj eliminácia niektorých perorálnych antidiabetík, alebo ich aktívnych metabolitov obličkami. Prehľad použiteľnosti jednotlivých antidiabetík a inzulínov pri zníženej GF prináša tab. 5, s. S4.
Tab. 5. Podávanie hypoglykemizujúcich liekov pri rôznych štádiách CKD (K/DOQI) 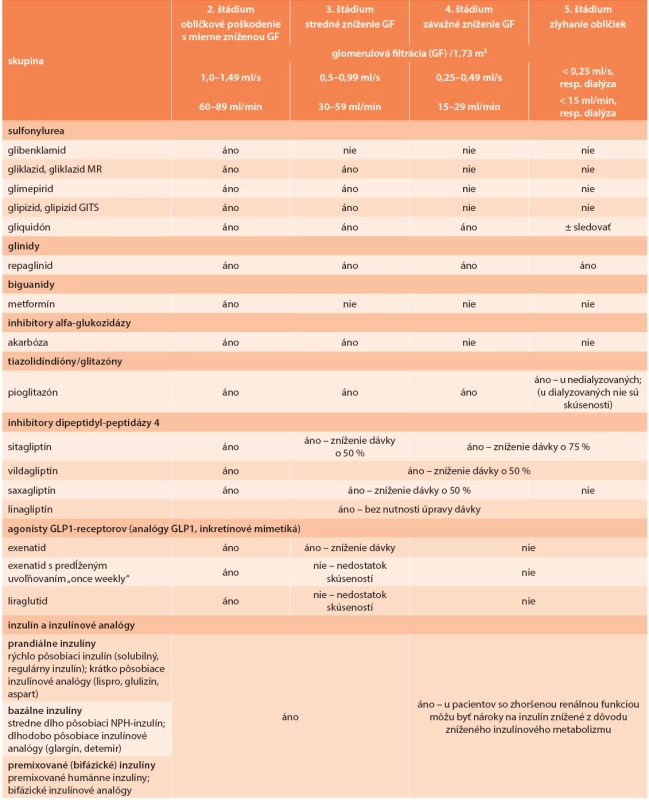
Aj u diabetikov na hemodialýze alebo peritoneálnej dialýze má dobrá glykemická kompenzácia význam pre spomalenie progresie ostatných mikrovaskulárnych a makrovaskulárnych komplikácií a dokázateľne zlepšuje prežívanie pacientov.
6.2 Liečba hypertenzie
V liečbe hypertenzie u diabetika s nefropatiou sú preferované inhibítory angiotenzín konvertujúceho enzýmu (ACEI) alebo blokátory angiotenzínových receptorov (ARB). Obe skupiny liečiv znižujú albuminúriu a spomaľujú progresiu nefropatie viac ako iné antihypertenzíva (renoprotektívny efekt nezávislý od zníženia krvného tlaku). Randomizované kontrolované štúdie u diabetikov 1. typu priniesli viac dôkazov pre renoprotektívny účinok ACEI bez ohľadu na výšku albuminúrie, kým u diabetikov 2. typu s mikroalbuminúriou bol efekt ACEI a ARB porovnateľný a u diabetikov 2. typu s makroalbuminúriou prevažovali dôkazy o ARB (tab. 6). ACEI sa osvedčili aj u normoalbuminurických diabetikov 1. a 2. typu s hypertenziou (primárna prevencia DN), resp. u normoalbuminurických normotenzných diabetikov 1. typu s hyperfiltráciou. Zatiaľ chýbajú dôkazy pre indikáciu ACEI/ARB u pacientov s normálnou albuminúriou, normálnym krvným tlakom a normálnou GF.
Tab. 6. Použitie ACEI a ARB v prevencii a liečbe DN 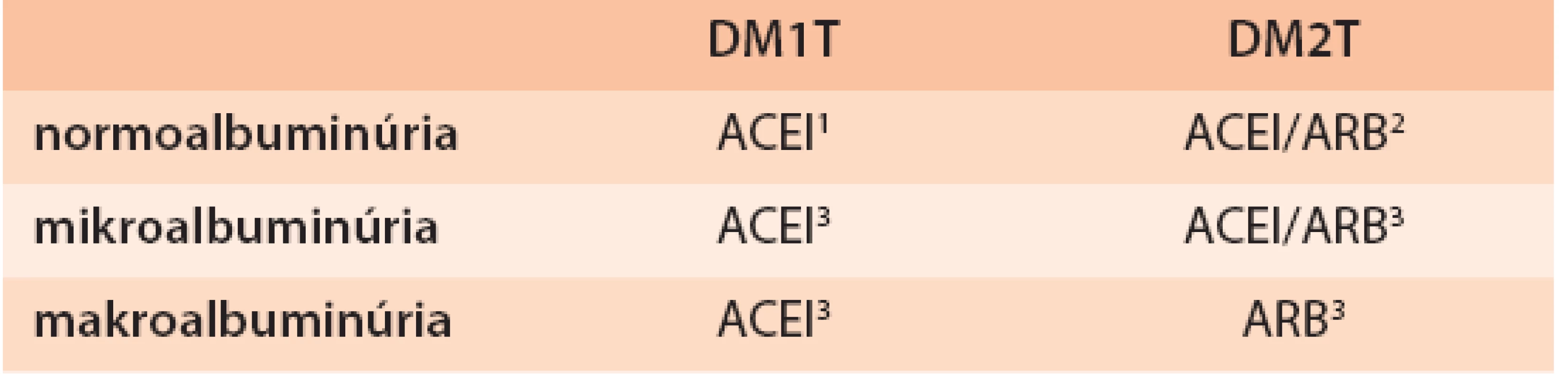
1 pri hypertenzii, resp. normotenzii so ↑GF 2 pri hypertenzii 3 väčšinou pri hypertenzii, ale efekt nezávislý od ↓TK Cieľový krvný tlak u diabetika s nefropatiou je (bez ohľadu na výšku albuminúrie) < 130/80 mm Hg, čo sa u väčšiny chorých dá dosiahnuť len kombináciou antihypertenzív.
V odporúčaniach NKF je liekom prvej voľby do kombinácie s ACEI/ARB diuretikum, ktoré účinok blokátorov RAS potencuje, bráni hyperkaliémii a retencii sodíka a vody. V malých dávkach a najmä v kombinácii s blokátormi RAS nie sú nepriaznivé metabolické účinky diuretík výrazné. Dihydropyridínové blokátory kalciových kanálov (vrátane amlodipínu) by sa mali používať len v kombinácii s ACEI/ARB, samotné progresiu DN nespomaľujú a môžu zvyšovať albuminúriu. V menších štúdiách znižovali albuminúriu nad rámec zníženia krvného tlaku verapamil a karvedilol. Použitie ostatných antihypertenzív ako aj nefarmakologických opatrení sa riadi všeobecnými zásadami liečby hypertenzie. Otvorená je otázka kombinácie ACEI a ARB, ktorá v niekoľkých štúdiách znížila albuminúriu viac ako monoterapia, zatiaľ však chýbajú presvedčivé dôkazy o účinku duálnej blokády RAS na spomalenie progresie DN. U pacientov s vysokým kardiovaskulárnym rizikom môže táto kombinácia progresiu nefropatie naopak urýchliť (štúdia ONTARGET) podobne ako kombinácia ACEI/ARB s inhibítorom renínu aliskirenom u diabetikov 2. typu (štúdia ALTITUDE). Proteinúriu pri DN znižuje aj kombinácia ACEI/ARB s antagonistom aldosterónu spironolaktónom, resp. supramaximálne (2 - až 4-násobne vyššie ako maximálne odporúčané) dávky ACEI/ARB, ale dlhodobá účinnosť a bezpečnosť takejto liečby zatiaľ nie je overená.
Celý rad ďalších liečiv (parikalcitol, glykozaminoglykany, antagonisty endotelínových receptorov, inhibítor proteínkinázy C ruboxistaurín, inhibítor AGEs pyridoxamín, antifibrotikum pirfenidon a iné) mal v kontrolovaných štúdiách antiproteinurický efekt nezávislý od zníženia krvného tlaku, ale spomalenie progresie DN zatiaľ dokumentované nebolo.
6.3 Liečba dyslipoproteinémie
Diabetici s nefropatiou majú väčšinou aterogénny lipoproteínový fenotyp (zvýšená koncentrácia triacylglycerolov, znížený HDL-cholesterol a mierne zvýšený alebo normálny LDL-cholesterol s malými denznými časticami LDL). Pretože každá chronická nefropatia predstavuje rizikový ekvivalent pre kardiovaskulárne choroby (riziko u diabetika s DN je 2 - až 4-krát vyššie ako u diabetika bez DN), má sa liečba dyslipoproteinémie u týchto pacientov riadiť odporúčaniami pre najrizikovejšie skupiny. Cieľový LDL-cholesterol má byť < 2,6 mmol/l, ale prospešné môže byť zníženie až na hodnoty < 1,8 mmol/l. Preferujú sa statíny, ktoré dokázateľne znižujú kardiovaskulárne riziko u diabetikov s nefropatiou v štádiu 1–3, pre štádium 4 zatiaľ dôkazy chýbajú. Dávky statínov (okrem atorvastatínu) treba redukovať zvyčajne pri GF < 0,5 ml/s, kým pre fibráty sa odporúčala redukcia už pri GF < 1 ml/s, resp. náhrada statínmi pri kreatininémii okolo 180 µmol/l. V nedávnej veľkej štúdii (FIELD) bola liečba fenofibrátom v plnej dávke u diabetikov 2. typu účinná a bezpečná pri GF > 0,5 ml/s. Ezetimib úpravu dávky nevyžaduje.
Dyslipoproteinémia môže zvyšovať albuminúriu a urýchliť progresiu nefropatie, ale na definitívne potvrdenie renoprotektívneho účinku statínov v kontrolovaných štúdiách sa stále čaká.
U diabetikov 2. typu na hemodialýze statíny napriek významnej redukcii LDL-cholesterolu väčšinou neznížili kardiovaskulárnu morbiditu a mortalitu. Tento výsledok je v zhode s predchádzajúcimi poznatkami z observačných štúdií o inverznom vzťahu medzi koncentráciou cholesterolu a mortalitou u dialyzovaných pacientov a naznačuje možnú odlišnú patogenézu kardiovaskulárnych chorôb v tejto skupine.
6.4 Nízkobielkovinová diéta
Prítomnosť nefropatie stavia diabetika pred náročnú úlohu zmeniť diétny režim a okrem doterajších obmedzení znížiť aj príjem bielkovín. Aj tu môže nefrológ účinne spolupracovať pri edukácii, motivácii a kontrole pacienta. Viaceré štúdie u pacientov s CKD dokázali renoprotektívny efekt diéty so zníženým obsahom bielkovín (0,8 g/kg/deň) a tento účinok bol výraznejší u diabetikov ako nediabetikov. V prevencii malnutrície pri takejto diéte by mali 50–75 % z celkového množstva bielkovín tvoriť proteíny s vysokou biologickou hodnotou (hydina, ryby, sója). Znížený kalorický príjem z redukcie proteínov (5–10 %) treba hradiť komplexnými sacharidmi (cereálie, ovocie, zelenina). V pokročilejšom štádiu nefropatie (CKD 3–4) alebo pri vysokej proteinúrii je možné znížiť príjem bielkovín na 0,6 g/kg/deň v kombinácii s ketoanalógmi aminokyselín v dostatočnej dávke.
7 Spolupráca nefrológa a diabetológa
Spolupráca nefrológa s diabetológom, prípadne s inými špecialistami je v prevencii a liečbe DN kľúčová. Hoci príprava a realizácia náhradnej eliminačnej liečby pri terminálnom zlyhaní obličiek zostáva nezameniteľnou úlohou nefrológa, ťažisko jeho práce sa v súlade s celosvetovým trendom presúva na včasné štádiá chorôb obličiek s cieľom zabrániť ich progresii, ako aj vývoju sprievodných extrarenálnych (najmä kardiovaskulárnych) komplikácií. K tomu smerujú aj odporúčania rôznych odborných spoločností pre diabetickú nefropatiu.
Podľa NKF je vhodné konzultovať diabetika v nefrologickej ambulancii pri:
- zistení nefropatie alebo potrebe diferenciálnej diagnostiky
- rezistentnej hypertenzii
- nastavení nízkobielkovinovej diéty (edukácia, motivácia, kontrola)
- liečbe osobitných skupín diabetikov s nefropatiou (deti, tehotné ženy, starí pacienti)
ADA vo svojich najnovších štandardoch liečby diabetu odporúča venovať pozornosť potenciálnym komplikáciám CKD pri odhadovanej GF < 1 ml/s/1,73 m2, resp. odoslanie pacienta k nefrológovi pri:
- nejasnej etiológii nefropatie
- ťažkostiach s liečbou pacienta
- pokročilej nefropatii
Vzhľadom na nezanedbateľný podiel nediabetických nefropatií u diabetikov 2. typu, ako aj možnosť atypického priebehu samotnej DN (pozri časť 5. Diagnostika) je včasná diferenciálna diagnostika nefrológom veľmi dôležitá. Od úrovne GF < 1 ml/s/1,73 m2 (trvajúcej najmenej 3 mesiace), alebo pri klinickej proteinúrii >0,5 g/24 h by mal byť diabetik dispenzarizovaný aj v nefrologickej ambulancii.
Zdroje
1. National Kidney Foundation: KDOQI™ Clinical Practice Guidelines and Clinical Practice Recommendations for Diabetes and Chronic Kidney Disease. Am J Kidney Dis 2007; 49(Suppl 2): S1-S180.
2. American Diabetes Association: Standards of medical care in diabetes – 2012. Diab Care 2012; 35(Suppl 1): S4-S10.
3. Doporučené postupy České nefrologické společnosti a České diabetologické společnosti ČLS JEP při diabetickém onemocnění ledvin. Dostupné z WWW: http://www.nefrol.cz/index.php?&desktop=clanky&action=view&id=462.
4. Bakris GL. Overview of diabetic nephropathy. Dostupné z WWW: http://www.uptodate.com/contents/overview-of-diabetic-nephropathy?source=search_result&search=Overview+of+diabetic+nephropathy&selectedTitle=1%7E150.
5. Ponťuch P. Diabetická nefropatie. Grada Publishing: Praha 2003. ISBN 80-247-0312-2.
6. Okša A, Spustová V. Nefropatia pri diabetes mellitus – skríning, prevencia a liečba v spolupráci diabetológa a nefrológa. Diabetes Obezita 2007; 7(Suppl): 6–13.
7. Uličiansky V, Schroner Z, Galajda P, Mokáň M, Némethyová Z. Algoritmus liečby diabetes mellitus 2. typu 2011 v klinickej praxi. Diabetes Obezita 2011; 11(22): 9–32.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseForum Diabetologicum
Nejčtenější tento týden
2013 Číslo 2-Suppl 1- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
Nejčtenější v tomto čísle
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání