-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Chirurgie nehtového aparátu: úvod do problematiky, přehled operačních technik a naše zkušenosti u vybraných onemocnění nehtového aparátu
Nail surgery: Introduction, Review on Surgical Techniques and Our Experience in Selected Nail Diseases
Nail surgery is a special field of dermatosurgery that requires comprehensive knowledge of nail structure and function. The main indications of the nail unit surgery are pigmentary changes, subungual tumors and nail plate deformities. Authors describe an universal algorithm of nail surgery techniques performed in selected diseases of the nail apparatus.
Key words:
nail unit – nail surgery – biopsy – excision – extirpation
Autoři: R. Litvik 1,2; M. Paciorek 2
Působiště autorů: Kožní oddělení Fakultní nemocnice Ostrava primářka MUDr. Yvetta Vantuchová, Ph. D. 1; Centrum plastické chirurgie a chirurgie ruky Fakultní nemocnice Ostrava primář MUDr. Bronislav Vřeský 2
Vyšlo v časopise: Čes-slov Derm, 88, 2013, No. 4, p. 155-168
Kategorie: Souborné referáty (doškolování lékařů)
Souhrn
Chirurgie nehtového aparátu je delikátní oblastí dermatochirurgie vyžadující důkladnou znalost stavby a funkce nehtového aparátu. Hlavními indikacemi chirurgického výkonu nehtového aparátu jsou zejména pigmentové projevy, subunguální tumory a deformity nehtových plotének. Autoři přehledně popisují obecný algoritmus operací nehtového aparátu se základními chirurgickými technikami a jeho aplikaci u vybraných onemocnění nehtového aparátu.
Klíčová slova:
nehtový aparát – nehtová chirurgie – biopsie – excize – exstirpaceANATOMIE NEHTOVÉHO APARÁTU
Nehty jsou ve dvou rovinách mírně konvexně zakřivené rohovinové ploténky z tvrdého keratinu, který se na rozdíl od rohoviny epidermis neolupuje. Nehtová ploténka leží na nehtovém lůžku a vyrůstá z nehtové matrix, která je ze 2/3 kryta zadním nehtovým valem, z 1/3 prosvítá pod proximálním koncem ploténky jako lunula. Distálněji pak matrix přechází do řidšího epitelu nehtového lůžka, které přechází v oblasti hyponychia v kůži bříška prstů. Nehtová ploténka je obklopena dvěma postranními nehtovými valy, jedním zadním (proximálním) nehtovým valem, jehož epidermis přechází na nehtovou ploténku (eponychium); distální konec nehtové ploténky je volný a přečnívá špičku prstu. Nehty rostou po celý život kontinuálně, průměrná rychlost růstu je asi 0,12 mm za den, nehty na nohou rostou pomaleji než na rukou [3]. Nehty chrání velmi citlivé konce falang, zvyšují taktilní čití prstů a ulehčují uchopení malých předmětů [31]. Kompletní ztráta nehtu postihuje negativně funkci a také kosmetický vzhled postiženého prstu.
VÝZNAM NEHTOVÉ CHIRURGIE
Chirurgie nehtového aparátu je delikátní oblastí dermatochirurgie vyžadující důkladnou znalost biologie, anatomie a histologie nehtového aparátu. Jakákoli operace nehtového aparátu by měla zachovat jeho funkci a kosmetický vzhled, zejména u nehtového aparátu prstů rukou [26, 27]. Hlavními indikacemi chirurgického výkonu nehtového aparátu jsou zejména pigmentové projevy (odlišení pigmentových névů a melanomu), subunguální tumory a deformity nehtových plotének [26, 27, 28]. Přístup k subunguálním projevům je možný po odstranění korespondující oblasti nehtové ploténky, poté lze biopsií získat materiál k histologickému vyšetření a tím ke stanovení přesné diagnózy. Prováděné biopsie v oblasti nehtového lůžka by měly být provedeny striktně podélně (longitudinálně), zatímco biopsie nehtové matrix příčně (horizontálně, transverzálně) [26, 27, 28]. Jakmile je stanovena exaktní diagnóza subunguálního tumoru, je volena radikální excize, pokud možno se zachováním vzhledu i funkce nehtového aparátu. Radikálnímu odstranění subunguálních nádorů by mělo předcházet rentgenové vyšetření kostních struktur distálních falang. U maligních nádorů nehtového aparátu (melanom, karcinomy, sarkomy) není většinou možné nehtový aparát ponechat in situ, nezbytná je amputace distální falangy (operace podle Lapiduse) nebo celého prstu v metakarpofalangeálním kloubu [4, 25, 26].
Obecný algoritmus operací nehtového aparátu
- a) Nezbytná je pečlivá indikace chirurgického výkonu nehtového aparátu s písemným poučením pacienta ve formě informovaného souhlasu o zvoleném výkonu, jeho rizicích, komplikacích a možných alternativách. U pacientů s diabetes mellitus, onemocněními periferních cév, s kolagenózami a imunodeficitem jakékoli etiologie by měly být, pokud je to možné, voleny pouze konzervativní diagnosticko-terapeutické postupy.
- b) Požadavky na instrumentárium v nehtové chirurgii jsou stejné jako u aseptické kožní chirurgie. Vhodné jsou zejména nehtové klíšťky, nůžky dlouhé střední, sada jemných preparačních očních nůžek, sada Freerových elevátorů a kostní kleště.
- c) Postižený prst by si měl pacient před operačním výkonem umýt antiseptickým mýdlem.
- d) Před vlastním operačním výkonem provádíme důkladnou dezinfekci operačního pole, zejména prstu a přilehlých meziprstních prostor.
- e) Po dezinfekci následuje zarouškování operačního pole.
- f) Chirurgický výkon na nehtovém aparátu provádíme technikou svodné anestezie podle Obersta (proximální digitální blok), a to lokálním anestetikem (1% roztok trimecainu, 0,5% roztok bupivacainu) bez přidání adrenalinu [6, 13, 15, 39]. Začínáme kolmým vpichem jehly na dorsu základního článku prstu s pomalým vstřikováním 1,5–2 ml roztoku anestetika k digitálnímu nervu, který probíhá plantárně, respektive palmárně. Jehlu po instilaci anestetika úplně nevytahujeme a těsně před vytažením ji otáčíme směrem pod kůži dorza článku prstu a zde deponujeme 2 ml roztoku anestetika a přitom posunujeme špičku jehly až na druhou stranu, kde infiltrujeme malé místo prakticky intradermálně. Jehlu vytáhneme a v kontralaterálním místě, kde již máme zaručeno znecitlivění, vpíchneme jehlu kolmo k druhému digitálnímu nervu a vstříkneme 1,5–2 ml roztoku anestetika. Vyčkáme 10 minut k plnému rozvinutí účinku lokální anestezie, zásadně nezačínáme operovat, pokud nemáme úplnou necitlivost. Distální digitální blok s infiltrací 1 ml roztoku lokálního anestetika přímo do nehtových valů se využívá méně, je přísně kontraindikován u bakteriálních infekcí nehtového aparátu.
- g) Operujeme zásadně v bezkrevnosti pro přehlednost operačního pole, která přispívá k přesnému operačnímu výkonu. Na bázi proximální falangy, v místě, kde jsme prováděli lokální anestezii, přikládáme turniket a ischémii navozenou turniketem můžeme využít po dobu 15–20 minut. Jako turniket používáme gumovou hadičku, kterou po stažení zajistíme peánem nebo kochrem. Je možné použít také okraj sterilní gumové rukavice [6, 26, 29].
- h) Vlastní technika chirurgického výkonu bude specifikována u jednotlivých metod, respektive klinických jednotek.
- i) Po ukončení chirurgického výkonu opláchneme operační pole fyziologickým roztokem, aplikujeme neadherentní krytí s obsahem povidon jódu a uvolníme turniket.
- j) Na závěr přiložíme kompresivní krytí. Je vhodné posadit pacienta ještě na půl hodiny do čekárny s elevovanou operovanou končetinou. První převaz provádíme za 24 hodin od výkonu z důvodu včasného záchytu možné ischémie z nadměrně komprimujícího krytí. Následující den pacient doma provádí 1krát denně koupele v antiseptickém roztoku. Stehy odstraňujeme za 10–12 dnů od provedeného výkonu a pacienta důkladně poučíme o preventivních opatřeních [34, 36, 39, 42].
PŘEHLED CHIRURGICKÝCH TECHNIK POUŽÍVANÝCH PŘI OPERACÍCH NEHTOVÉHO APARÁTU
Ablace (avulze) nehtové ploténky
Rozlišujeme parciální nebo totální ablaci nehtové ploténky. Parciální nehtovou ablaci provádíme nejčastěji podélně (klasická parciální, longitudinální ablace nehtové ploténky u laterálních nehtových valů) nebo méně často příčně (parciální transverzální ablace distální nebo proximální poloviny nehtové ploténky). Ablace nehtové ploténky slouží k obnažení subunguálního prostoru a ke snadnému přístupu k patologickým projevům. V žádném případě se nejedná o metodu, kterou využíváme k léčbě zarůstajících nehtů (viz níže). Totální ablace nehtové ploténky je dnes vyhrazena pouze pro případy chronické, terapeuticky rezistentní onychomykózy nebo akutní subunguální bakteriální infekce. V ostatních případech volíme parciální nehtové ablace podélné či příčné, na které v dalším kroku navazují diagnostické biopsie a terapeutické excize abnormalit subunguálního prostoru (biopsie nehtového lůžka a nehtové matrix) [4, 6, 17, 26, 27].
Parciální ablace nehtové ploténky v algoritmu operace nehtového aparátu
Nehtovou ploténku discidujeme rovnými nůžkami od distálního, volného okraje a pokračujeme v prostřižení nehtové ploténky až k proximálnímu nehtovému valu. Rozpolcení nehtové ploténky musí být šetrné, hrot nůžek tlačíme k nehtové ploténce tak, aby co nejméně poranil nehtové lůžko. Prostřižení nehtové ploténky musí být i přes eponychium na bázi. Poté uchopíme část nehtové ploténky do branží peánu a rotačními pohyby odloučíme nehtovou ploténku od nehtového lůžka. Šetrněji lze nehtovou ploténku odstranit z nehtového lůžka pomocí Freerova elevátoru, tuto metodu upřednostňují některá pracoviště před rotačním odloučením nehtové ploténky peánem [4, 6, 17, 26, 27, 28, 39].
Totální ablace nehtové ploténky v algoritmu operace nehtového aparátu
Rozpolcení nehtové ploténky provádíme jako u parciální nehtové ablace, discizi vedeme středem nehtové ploténky. Následně rotačními pohyby odstraníme obě poloviny nehtové ploténky. Pokud byla indikací totální ablace nehtové ploténky onychomykóza, pak po totální ablaci nehtové ploténky následuje odstranění subunguální hyperkeratózy nehtového lůžka exkochleační lžičkou. Na takto provedený chirurgický výkon navazuje lokální a systémová antimykotická terapie. Při léčbě onychogryfózy, pachyonychie nebo jiných výrazných deformit nehtové ploténky přináší totální nehtová ablace jen krátkodobý a přechodný efekt. Většinou je nehtová matrix ireverzibilně postižena, v těchto případech volíme kombinaci totální ablace nehtové ploténky s kompletní destrukcí matrix (totální matrixektomie excizí nebo fenolizací, viz podrobně v oddíle pojednávajícím o zarůstajících nehtech). Tento výkon by neměl být proveden u pacientů s poruchami prokrvení distálních partií prstů (diabetes mellitus, ischemická choroba dolních končetin, kolagenózy), výsledkem by bylo komplikované hojení s možností rozvoje gangrény a sepse [4, 6, 17, 26, 27, 28, 39].
Biopsie a excize nehtového aparátu
Ke stanovení přesné diagnózy, léčbě benigních a maligních nádorů a také řady zánětlivých onemocnění nehtového aparátu rutinně provádíme v nehtové chirurgii biopsie a excize nehtového lůžka, nehtové matrix, nehtových valů a nehtové ploténky (obr. 1, 2) [6, 17, 26, 27, 28].
Obr. 1. Biopsie a excize nehtového aparátu [26] 1 – longitudinální biopsie laterálního nehtového valu 2 – průbojníková biopsie zadního nehtového valu 3 – klínovitá excize zadního nehtového valu 4 – longitudinální biopsie nehtového lůžka 5 – průbojníková biopsie nehtového lůžka 6 – průbojníková biopsie nehtové matrix 7 – transverzální biopsie nehtové matrix 8 – longitudinální excize laterálního nehtového valu HO – hyponychium, M – matrix, NL – nehtové lůžko, ZNV – zadní nehtový val, DF – distální falanga ![Biopsie a excize nehtového aparátu [26]
1 – longitudinální biopsie laterálního nehtového valu
2 – průbojníková biopsie zadního nehtového valu
3 – klínovitá excize zadního nehtového valu
4 – longitudinální biopsie nehtového lůžka
5 – průbojníková biopsie nehtového lůžka
6 – průbojníková biopsie nehtové matrix
7 – transverzální biopsie nehtové matrix
8 – longitudinální excize laterálního nehtového valu
HO – hyponychium, M – matrix, NL – nehtové lůžko,
ZNV – zadní nehtový val, DF – distální falanga](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/09632af977579fcd7d8030b03918d305.jpg)
Obr. 2. Biopsie nehtového aparátu A: transverzální biopsie nehtové matrix po odklopení zadního nehtového valu [6] B: průbojníková biopsie nehtové matrix po odklopení zadního nehtového valu [6] C: technika klínovité excize patologického projevu zadního nehtového valu [27] ![Biopsie nehtového aparátu
A: transverzální biopsie nehtové matrix po odklopení zadního nehtového valu [6]
B: průbojníková biopsie nehtové matrix po odklopení zadního nehtového valu [6]
C: technika klínovité excize patologického projevu zadního nehtového valu [27]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/a19a6714cf4615b13e62feb8cf1897bd.jpg)
Biopsie a excize nehtového lůžka
Biopsie a excize nehtového lůžka slouží především k přesnému stanovení diagnózy fokálních abnormalit nehtového lůžka, zejména pigmentových projevů a subunguálních tumorů nehtového aparátu. Izolované abnormality nehtového lůžka jsou přístupny bioptickému vyšetření po snesení části nehtové ploténky nad vlastním projevem.
Biopsie a excize nehtového lůžka v algoritmu operace nehtového aparátu
Po snesení nehtové ploténky nad patologickým projevem (parciální ablace nehtové ploténky podélná nebo příčná) následuje diagnostická biopsie průbojníkem (punch biopsie) s uvolněním vzorku preparačními očními nůžkami nebo klasická, diagnosticko-terapeutická, přísně longitudinální, eliptická excize abnormality. Pokud je defekt vzniklý biopsií větší než 3 mm, provádíme suturu vzniklého defektu monofilamentem 5/0 nebo 6/0. Modifikací výše uvedeného postupu je technika dvojité průbojníkové biopsie (double punch biopsie), kdy provedeme vlastní snesení nehtové ploténky nad abnormalitou průbojníkem o průměru 4–6 mm. Do vzniklého defektu v nehtové ploténce pak zasuneme průbojník průměru 3 mm a provedeme rotační excizi s uvolněním vzorku nehtového lůžka preparačními očními nůžkami (obr. 3) [6, 17, 26, 27, 28].
Obr. 3. Technika dvojité průbojníkové biopsie A: přiložení průbojníku o průměru 4 mm k nehtové ploténce B: rotační excize nehtové ploténky za vzniku kruhovitého defektu C: vložení průbojníku o průměru 3 mm do defektu po biopsii nehtové ploténky D: realizace biopsie nehtového lůžka 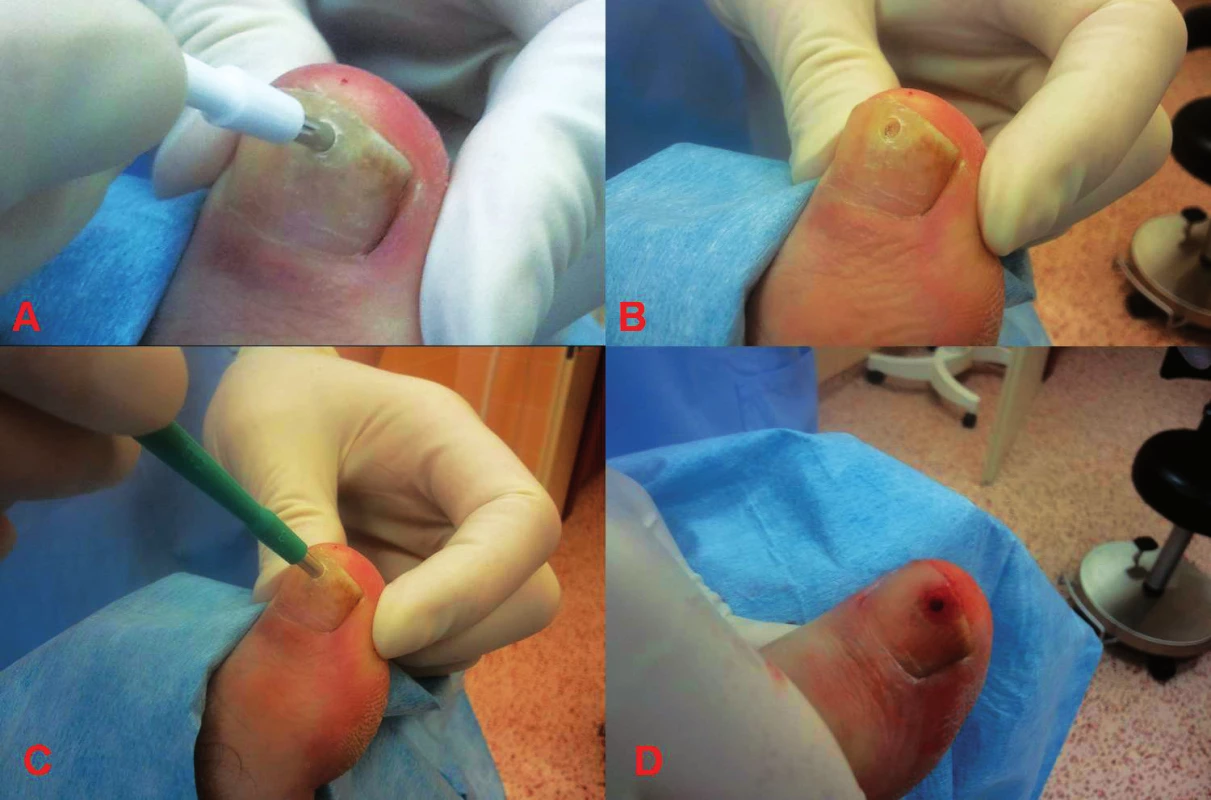
Biopsie a excize nehtové matrix
Biopsie a excize nehtové matrix provádíme u stavů fokálních abnormalit matrix (pigmentové projevy, tumory) a u dystrofií nehtových plotének vznikajících na podkladě postižení nehtové matrix (viz obr. 2).
Biopsie a excize nehtové matrix v algoritmu operace nehtového aparátu
Matrix lze vizualizovat dvěma technikami. Pokud se abnormalita nachází v distální třetině matrix viditelné pod nehtovou ploténkou v oblasti lunuly, provádíme totální ablaci nehtové ploténky nebo parciální příčnou ablaci proximální části nehtové ploténky. Ablace nehtové ploténky umožní přístup k distální třetině matrix. Proximální 2/3 nehtové matrix vizualizujeme tak, že provedeme incize v místech přechodu zadního (proximálního) nehtového valu ve valy laterální, a provedeme separaci eponychia od nehtové ploténky Freerovým elevátorem. Takto připravený zadní nehtový val odklopíme proximálně a odhalíme nehtovou matrix. Po vizualizaci nehtové matrix následuje provedení průbojníkové biopsie. Nejčastěji volíme průbojník maximálně do průměru 3 mm, neboť průbojníkové biopsie v oblasti nehtové matrix nad 3 mm zvyšují riziko vzniku iatrogenního, trvalého poškození nehtové ploténky. Možná je také drobná, fusiformní, přísně transverzální (horizontální) excize matrix se suturou vzniklého defektu monofilamentem 6/0. Sutura nesmí být pod napětím, neboť nehtová matrix je velmi citlivá na jakékoli změny tlaku. Po provedené biopsii a/nebo excizi pak zadní nehtový val překlopíme zpět do výchozí anatomické pozice jako kožní lalok a provedeme suturu nářezů zadního nehtového valu monofilamentem 4/0–5/0. Všechny biopsie a excize nehtové matrix musí respektovat okraj lunuly; není přípustná technika longitudinální excize ani průbojníková biopsie větší než 3 mm [6, 17, 26, 27, 28].
Podélná biopsie a excize laterálního nehtového valu
Longitudinální biopsie laterálního nehtového valu se využívá v nehtové chirurgii zcela rutinně k diagnostice patologických projevů na laterálním nehtovém valu, longitudinální excize pak k léčbě longitudinálních melanonychií, laterálně uložených abnormalit nehtového aparátu a k léčbě zarůstajících nehtů.
Podélná biopsie a excize laterálního nehtového valu v algoritmu operace nehtového aparátu
Vychází-li pigmentace z oblasti nehtové matrix (longitudinální melanonychie), nebo se jedná o oblast zarůstajícího nehtu či jinou abnormalitu, je nutné nejprve provést parciální ablaci nehtové ploténky nad pigmentovým projevem, respektive zarostlým nehtem, a pak radikální longitudinální eliptickou excizi zahrnující v excidátu hyponychium, nehtové lůžko, nehtovou matrix a proximální nehtový val. Vzniklý defekt uzavíráme transunguální suturou laterálního nehtového valu k nehtovému lůžku monofilamentem 3/0 (minimalizaci rizika vzniku nehtové dystrofie) [6, 17, 26, 27, 28].
Biopsie a excize zadního nehtového valu
Biopsie zadního nehtového valu se využívá k upřesnění diagnostiky dermatóz zadního nehtového valu, zejména se jedná o kolagenózy, fokální tumory, myxoidní cysty a řešení paronychií (obr. 2).
Biopsie a excize zadního nehtového valu v algoritmu operace nehtového aparátu
Provádíme průbojníkové biopsie nejčastěji se suturou vzniklého defektu monofilamentem 4/0 nebo klasické V-biopsie s uvolňujícími incizemi na jedné nebo obou stranách zadního nehtového valu se suturou vzniklého defektu monofilamentem 4/0. U terapeuticky refrakterního chronického paronychia, benigních a maligních tumorů zadního nehtového valu lze provést také radikální excizi celého zadního nehtového valu s dohojením defektu per secundam intentionem.
Akutní infekce nehtových valů a nehtového lůžka (paronychia) by měla být léčena konzervativě systémovými antibiotiky a lokálními antiseptiky. Pokud nedojde ke zlepšení během 24–48 hodin, pak následuje chirurgická intervence. Infekce v oblasti zadního nehtového valu řešíme horizontální incizí, zatímco infekce laterálních nehtových valů incizí longitudinální. Často spolu s incizí odstraňujeme část nehtové ploténky, pokud je infekční postižení masivní, odstraňujeme celou nehtovou ploténku. Neléčené trvající záněty nehtového lůžka a nehtových valů mohou trvale poškodit nehtovou matrix s rozvojem ireverzibilní onychodystrofie. Je nutno pamatovat na skutečnost, že infekce nehtového aparátu se mohou šířit nejen lokálně ke kostem, kloubům a měkkým tkáním, ale podél šlachových pochev mohou postihnout také vzdálené oblasti ruky, respektive nohy [6, 17, 18, 26, 27, 28].
Biopsie nehtové ploténky
Pro úplnost výčtu biopsií a excizí struktur nehtového aparátu zmiňujeme také biopsii nehtové ploténky, kterou využíváme zejména k odlišení mykotické onychodystrofie od ostatních onychodystrofií. U distálně laterálního typu onychomykózy odstraníme část volného okraje nehtové ploténky nehtovými klíšťkami a vzorek odesíláme k histologickému vyšetření. Pokud se jedná o proximální formu onychomykózy, pak biopsii nehtové ploténky realizujeme technikami parciální nebo totální ablace nehtové ploténky či průbojníkovými biopsiemi tak, jak byly tyto techniky popsány výše [6, 17, 18, 26, 27, 28].
CHIRURGICKÉ ŘEŠENÍ VYBRANÝCH ONEMOCNĚNÍ NEHTOVÉHO APARÁTU
Zarůstající nehty
Definice a epidemiologie
Zarůstající nehet (unguis incarnatus) je onemocnění, které je definováno jako zanoření laterálního okraje nehtové ploténky do přilehlé nehtové rýhy s pronikáním nehtové ploténky do měkkých tkání nehtových valů. Unguis incarnatus je běžným onemocněním nehtového aparátu, počet nově diagnostikovaných zarůstajících nehtů se v Anglii odhaduje na 10 000 případů za rok. Onemocnění postihuje jedince kteréhokoliv věku, častěji jsou postiženi sportovně aktivní mladí muži ve druhém a třetím deceniu. Nejčastěji je postižena nehtová ploténka palce nohy v oblasti mediálního nehtového valu [67, 68].
Etiopatogeneze
Příčinou zarůstání nehtů bývá zejména chybné stříhání volného okraje nehtové ploténky semicirkulárně (do obloučku). Během odrůstání nehtové ploténky dochází k mechanickému dráždění měkkých tkání nehtových valů okrajem nehtové ploténky, k zanoření okraje nehtové ploténky do přilehlé nehtové rýhy a k dalšímu pronikání ploténky nehtu do měkké tkáně nehtového valu. Okraj nehtové ploténky je pak zanořen do měkkých tkání nehtových valů, trvale zde mechanicky dráždí jako cizí těleso, které působí chronický průběh zánětlivých projevů. Důsledkem tohoto trvalého dráždění je bolestivost, iritace, otok perionychiální zóny, růst hypergranulací a hypertrofie nehtových valů.
Z ostatních příčin zarůstání nehtových plotének se uvádí dlouhodobá traumatizace perionychiální zóny těsnou obuví, vbočení palce u příčně ploché nohy a vzácně mykotické onemocnění nehtové ploténky [29, 34]. Nově jsou popisovány zvýšené počty případů polékových zarůstajících nehtů a paronychií. Jedná se o HIV pozitivní pacienty léčené indinavirem (inhibitor proteinázy HIV) a lamivudinem (nukleozidový inhibitor reverzní transkriptázy HIV) [12]. Až u 15 % pacientů léčených everolimem a temsirolimem, selektivními inhibitory mTOR („mammalian target of rapamycin“ – cílový receptor pro rapamycin u savců) a u 10–15 % pacientů léčených inhibitory receptoru pro epidermální růstový faktor (gefitinib, erlotinib, panitumumab a cetuximab) vznikají užíváním těchto preparátů poléková paronychia a zarůstající nehty [8, 40, 57, 61]. Mechanismus vzniku polékových paronychií a zarůstajících nehtů není znám.
Mezi predispoziční faktory zarůstání nehtových plotének řadíme hyperhidrózu, diabetes mellitus, akromegalii, obezitu, ischemickou chorobu dolních končetin. Některé z těchto predispozičních faktorů se sdružují do non-hereditárního Steiglederova syndromu, který zahrnuje unguis incarnatus u chlapců mezi 12.–16. rokem věku, poruchu glukózové tolerance, palmoplantární hyperhidrózu a růstovou akceleraci končetin. Tento syndrom nebývá vždy plně vyjádřen [34, 62].
Klinický obraz
V roce 1869 popsal německý chirurg Carl Emmert tři stadia onemocnění a tato Emmertova klasifikace klinického obrazu zarůstajících nehtů se používá dodnes [52].
První, zánětlivé stadium je charakterizováno zarudnutím, otokem a bolestivostí měkkých tkání perionychiální zóny. Není přítomna sekrece ani granulace. Ve druhém, hnisavém stadiu jsou zánětlivé změny zvýrazněny, známky prvního stadia jsou vystupňovány a je přítomná charakteristická hnisavá sekrece (viz obr. 4). Ve třetím, hypergranulačním stadiu jsou přítomny známky obou stadií onemocnění, ke kterým se připojuje hypergranulace a hypertrofie nehtového valu.
Obr. 4. Zarůstající nehty I. A: zarůstající nehty obou halluxů, II. stadium podle Emmerta B: plastika nehtového valu podle Bartletta C: technika dlahování nehtové ploténky flexilou podle Schulteho-Neumanna [29] D: pooperační snímek dlahování nehtové ploténky podle Schulteho-Neumanna ![Zarůstající nehty I.
A: zarůstající nehty obou halluxů, II. stadium podle Emmerta
B: plastika nehtového valu podle Bartletta
C: technika dlahování nehtové ploténky flexilou podle Schulteho-Neumanna [29]
D: pooperační snímek dlahování nehtové ploténky podle Schulteho-Neumanna](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/0f1823b4908f24759911fa14f76e32d9.jpg)
Diagnostika a diferenciální diagnostika
Diagnostika zarůstajících nehtů je provedena na základě klinického obrazu a obvykle nečiní potíže. Neměli bychom zapomenout pátrat po Steiglederově syndromu či mykotickém onemocnění nehtové ploténky. Pod obrazem unguis incarnatus se může skrývat také amelanotická forma akrolentiginózního melanomu, což by nemělo být nikdy opomenuto v diferenciální diagnostice [38]. Dále je nutné rozlišení zarůstajících nehtů od paronychií. U paronychií nedochází k zarůstání nehtové ploténky do měkkých tkání, ale ostatní příznaky, jako je zarudnutí, otok, bolestivost a hnisavá sekrece z měkkých tkání nehtového aparátu, jsou přítomny.
Léčba
Léčba unguis incarnatus zahrnuje konzervativní léčebné postupy, chirurgické metody léčby a důležitá jsou rovněž preventivní opatření.
Konzervativní léčebné metody
Konzervativní léčebné postupy jsou indikovány při prvním stadiu onemocnění. Kromě lokální aplikace antiseptik a koupelí končetiny, např. v roztoku hypermanganu, nemocným doporučujeme vkládání drobného smotku hydrofilní gázy pod nehtovou ploténku v oblasti postiženého postranního nehtového valu. Smotek gázy nadzvedává nehtovou ploténku a chrání nehtový val před dalším tlakem nehtové ploténky. Smotek gázy může být napuštěn antiseptikem a nemocný si jej 1–2krát denně vyměňuje. Nehet se nesmí stříhat a tato konzervativní léčba trvá řadu týdnů, než ustoupí příznaky zánětu a nehet svým růstem přesáhne délku bříška prstu [34, 39].
Chirurgické léčebné metody
Chirurgická léčba je indikovaná u druhého a třetího stadia onemocnění. Je popsáno velmi mnoho chirurgických technik k léčbě zarůstajícího nehtu. Obecně lze chirurgické techniky rozdělit do dvou skupin. První skupinu tvoří výkony šetřící nehtovou matrix, druhou skupinu tvoří výkony redukující nehtovou matrix [34, 67, 68].
Do skupiny výkonů šetřících nehtovou matrix patří:
- Plastika podle Bartletta, při které odstraňujeme nadbytečnou tkáň podélnou excizí kůže a podkoží pod postiženým nehtovým valem se suturou (obr. 4, 5) [6, 29].
- V roce 1998 bylo popsáno konzervativní dlahování nehtové ploténky podle Schulteho a Neumanna. Na hranu nehtové ploténky se nasune podélně incidovaná pružná flexila, která se fixuje náplastí k perionychiální tkáni a zůstává ponechána in situ do úplného zhojení (viz obr. 4) [47, 56].
- Ablace nehtové ploténky (parciální nebo totální) je metoda radikální a jednoduchá, spojená s vysokým rizikem recidivy onemocnění po výkonu. Ústup potíží trvá zpravidla jen do té doby, než doroste podstatná část nehtové ploténky, to je za 2–4 měsíce [29, 39].
Obr. 5. Zarůstající nehty II. A: plastika nehtového valu podle Bartletta B: technika Hanekeho operace [4] C: pacient se zarůstajícími nehty III. stadia podle Emmerta před operací D: týž pacient za 2 týdny po operaci podle Hanekeho ![Zarůstající nehty II.
A: plastika nehtového valu podle Bartletta
B: technika Hanekeho operace [4]
C: pacient se zarůstajícími nehty III. stadia podle Emmerta před operací
D: týž pacient za 2 týdny po operaci podle Hanekeho](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/1ce348d43da02914e44e5c4edb1d9d18.jpg)
Nehtovou matrix redukující výkony
Tyto výkony obecně zahrnují parciální ablaci nehtové ploténky s parciální destrukcí nehtové matrix. Parciální matrixektomie je prováděna klasickou excizí, exkochleací ostrou lžičkou, chemickou destrukcí fenolem či hydroxidem sodným, elektrokoagulací nebo laserem (CO2 laser, Er:YAG laser) [4, 5, 6].
Mezi chirurgické výkony redukující nehtovou matrix patří:
- Emmertova operace, která zahrnuje parciální ablaci nehtové ploténky s klínovitou excizí přilehlé nehtové matrix, nehtového lůžka a nehtového valu. Není prováděna sutura, hojení defektu probíhá per secundam intentionem [51, 52].
- Hanekeho operace kombinuje parciální ablaci laterální části nehtové ploténky s resekcí příslušné části matrix, nehtového lůžka a hypertrofického nehtového valu (viz oddíl longitudinální biopsie laterálního nehtového valu). Je provedena sutura nehtového valu k nehtové ploténce. Tento typ operace lze kombinovat s chemickou matrixektomií, kdy k destrukci příslušné části nehtové matrix používáme 70 % fenol nebo 10–20 % hydroxid sodný. Rovněž lze u této operace využít k parciální destrukci matrix laser či kryodestrukci (viz obr. 5) [6, 29, 42, 43, 44].
- Matrix lze zcela odstranit (totální matrixektomie podle Zadika, v modifikacích podle Fowlera a Scotta) po naříznutí obou konců proximálního nehtového valu, tento proximálně odklopit a odhalit tak nehtovou matrix, tu pak vyříznout a proximální nehtový val překlopit zpět do výchozí anatomické pozice jako kožní lalok. Tato operace je vyhrazena pouze erudovanému operatérovi pro možnou nekrózu laloku, pro riziko rozvoje osteomyelitidy a interfalangeální artritidy [4, 34].
Podle doporučení European Nail Society by měly všechny chirurgické metody léčby zarůstajících nehtů zachovat funkci a estetický vzhled nehtového aparátu a zároveň by měla použitá chirurgická metoda vykazovat nejmenší riziko recidivy onemocnění po provedeném výkonu 5. Po totální ablaci nehtové ploténky se procento recidivy onemocnění pohybuje v rozmezí 64–70 %, po provedené parciální ablaci nehtové ploténky je toto riziko dokonce 73%. Recidiva onemocnění po chirurgické terapii je dána ponecháním germinativního epitelu nehtové matrix in situ, což vede k tvorbě nového nehtu s rozvojem opětovných potíží. Po opakovaných ablacích, následkem dlouhodobých zánětlivých změn, pozorujeme vytvoření exostózy na dorzální straně nehtového výběžku, která pak brání volnému odrůstání nehtové ploténky. Nehtová ploténka je tak postupně nadzvedávána a odlučována od nehtového lůžka, dochází k novým zánětlivým změnám a opětovnému zarůstání nehtu. Tomuto lze zabránit včasnou resekcí exostózy [65]. Zvýšené riziko recidivy onemocnění po provedené totální ablaci nehtové ploténky a výskyt kostních změn typu exostózy hovoří proti paušálnímu provádění totální ablace nehtové ploténky u zarůstajících nehtů.
Riziko recidivy onemocnění ve skupině chirurgických výkonů redukujících nehtovou matrix je signifikantně nižší. U Emmertovy operace je riziko recidivy onemocnění 25%, u Hanekeho operace je riziko recidivy onemocnění 5% [6, 18, 29, 34, 67, 68].
Preventivní opatření
Mezi preventivní opatření patří edukace správného stříhání nehtových plotének, kdy pacientům zdůrazňujeme rovné stříhání nehtové ploténky s přerůstáním okraje nehtové ploténky přes distální falangu o 1–2 mm. Důležitá je volba obuvi s volnou špicí, která zabrání tlaku obuvi na nehtový aparát. Korekce anatomické abnormality nohou či prstů je nezbytnou podmínkou úspěšné léčby onemocnění.
Vlastní soubor léčených pacientů: materiál, metodika a výsledky, hodnocení
Chirurgická léčba je indikována u pacientů ve druhém a třetím stadiu onemocnění, využíváme nehtovou matrix redukující operaci podle Hanekeho, která byla popsána výše. V letech 2010–2011 jsme provedli celkem 66 operací podle Hanekeho pro hypertrofické stadium zarůstání nehtové ploténky halluxů dolních končetin. V souboru bylo 42 mužů a 24 žen, průměrný věk operovaných mužů byl 21 let, žen 26 let. Nejvíce nemocných bylo ve věku do 24 let (muži 87 %, ženy 60 %). O recidivu onemocnění se jednalo u 48,5 % pacientů (tj. u 24 mužů a 8 žen). Nejčastěji postiženou nehtovou ploténkou byla nehtová ploténka fibulárního okraje levého halluxu, a to u 41 z 66 pacientů (tj. 62,1%). Pacienti našeho souboru byli sledováni 1 rok po operaci a recidiva onemocnění po operačním výkonu byla zaznamenána u 2 z 66 pacientů, tj. ve 3,03 %. V našem souboru léčených pacientů pro zarůstání nehtové ploténky halluxů dolních končetin jsme zvolili operační metodu ze skupiny nehtovou matrix redukujících výkonů pro nízké riziko recidivy, které bylo opakovaně prokázáno v literatuře [6, 18, 29, 34, 67, 68]. Riziko recidivy onemocnění po Hanekeho operaci v souboru námi léčených pacientů bylo 3,03%. Operace je bezpečná, zachovává funkci a také estetický vzhled nehtového aparátu, vykazuje nízké riziko recidivy onemocnění po výkonu a podle našich zkušeností by měla být metodou první volby v léčbě druhého a třetího stadia zarůstajících nehtů.
Subunguální glomus tumory
Historie
Glomus tumor je relativně vzácným benigním nádorem měkkých tkání (1–2 %), jehož původem jsou glomové buňky glomového tělíska [6, 10, 23, 32]. Poprvé byl glomus tumor popsán v roce 1812 Woodem [21, 22, 23]. Woodova pozorování s přesným popisem onemocnění v subunguální lokalizaci byla zapomenuta a poté byl glomus tumor znovu objeven v roce 1922, kdy Barré popsal klinický nález subunguálního glomus tumoru, jeho symptomy a doporučil účinný terapeutický postup – exstirpaci nádoru [46, 54]. Termín glomus tumor pochází z roku 1924, kdy Masson jako první na světě publikoval histologickou strukturu glomus tumoru a správně určil neuromyoarteriální původ glomového tělíska [55].
Definice a epidemiologie
Glomus tumory patří do heterogenní skupiny benigních nádorů, které jsou charakterizovány nádorovým bujením glomových buněk. Skupina glomus tumorů se dělí na dvě základní podskupiny [10]:
- a) Solitární glomus tumor – v užším slova smyslu se také označuje jako subunguální glomus tumor. Touto variantou se zabývá naše sdělení.
- b) Glomangiomy – tyto nádory jsou mnohočetné, přítomné u novorozenců a dětí v kterékoliv lokalizaci na těle. Tato podskupina tvoří 10–20 % všech glomus tumorů.
Subunguální glomus tumor je vzácným benigním nádorem nehtového aparátu. Onemocnění postihuje jedince kteréhokoliv věku, častěji jsou postiženy ženy ve druhém až čtvrtém deceniu (83 %). Nejčastěji se nádor vyskytuje v subunguální lokalizaci na horních (až 80 %) a dolních končetinách (25,6–37 %) [37, 46, 54]. Glomus tumor se může vyskytovat kdekoliv na těle [9, 10]. Popsány jsou lokalizace glomus tumoru v mediastinu, plicích, trachei, kostech [45, 46, 53], žaludku, čípku dělohy a vagině, což nepřímo prokazuje původ glomových buněk z hladkých svalových buněk. Nádor je většinou solitární, vzácně se mohou vyskytovat mnohočetné glomus tumory. Mnohočetné glomus tumory vídáme především u dětí a jsou spojeny s autosomálně dominantním typem dědičnosti [55]. Některé z forem glomus tumorů jsou kongenitální, popsány jsou také familiární formy glomus tumorů [2, 10, 21, 23].
Anatomicko-histologická korelace
Glomus tumor pochází z glomových buněk glomových tělísek (anastomosis arteriovenosa glomeriformis), která jsou zodpovědna za regulaci průtoku krve. Kožní glomové tělísko je uloženo v retikulární vrstvě dermis kdekoliv na těle. Nejvíce glomových tělísek je obsaženo na akrálních partiích těla, zejména v oblasti nehtových lůžek distálních falang, kde jejich koncentrace dosahuje hodnoty 93–501 glomových tělísek na cm2 [6, 9, 32, 46]. Glomové tělísko je oválného tvaru, velikosti cca 350 µm a každé je obaleno vazivovou membránou. Glomové tělísko obsahuje aferentní arteriolu a eferentní venulu (Sucquetův-Hoyerův kanál) bez přítomnosti kapilární sítě. Takto vzniklá arteriovenózní anastomóza, označována jako Hoyerova-Grosserova anastomóza (zkrat), je vystlána uvnitř endoteliemi a zevně obklopena 2–3 koncentrickými vrstvami myoepiteloidních buněk, které se nazývají glomovými buňkami. Tyto glomové buňky, specializované buňky hladkého svalu kuboidního tvaru, jsou hojně inervovány jak myelinizovanými, tak také nemyelinizovanými cholinergními nervy [9]. Funkčně slouží glomové tělísko k termoregulaci, kdy inervovanými glomovými buňkami vznikají kontrakce a relaxace glomového tělíska. Kontrakce a relaxace glomového tělíska se přenáší na arteriovenózní anastomózu, dochází k regulaci průtoku krve tělískem a tím sekundárně k ovlivnění termoregulace [9, 10, 46, 54].
Etiopatogeneze
Příčina nádorového bujení glomových buněk není známa. Solitární subunguální glomus tumor častěji vzniká v terénu akutního traumatu a/nebo po opakovaných mikrotraumatech nehtového aparátu [46, 54]. Na druhé straně existují skupiny pacientů, u kterých není popsána žádná vazba na trauma nehtového aparátu. V těchto případech nádor vzniká na podkladě intrinzních faktorů, jako je dědičnost a další, ještě ne zcela známé faktory. Mnohočetné subunguální glomus tumory jsou vzácnou vrozenou variantou glomus tumoru s autozomálně dominantním typem dědičnosti. Je rovněž popsána asociace subunguálních glomus tumorů s von Recklinghausenovou neurofibromatózou (NF-1) [55].
Klinický obraz
Typické klinické příznaky subunguálního glomus tumoru se sdružují do triády:
- I. paroxysmální bolestivost končetiny,
- II. intolerance chladu s rozvojem paroxysmálního záchvatu bolestivosti končetiny,
- III. prudká bolestivost v místě lokalizace nádoru, která se zesiluje palpací tumoru [46, 54]. Tyto symptomy mohou předcházet i sedm let, než je stanovena správná diagnóza. V anamnéze většina pacientů uvádí trauma či omrzliny nehtového aparátu, pacienti popisují paroxysmální záchvaty bolesti postižené končetiny, analyzují možné spouštěcí mechanismy (trauma, chlad) a dále udávají naprostou neúčinnost zvolené terapie. Pacienti jsou nezřídka léčeni pod diagnózou syndromu karpálního tunelu, kauzalgie či jiných onemocnění, která jsou dále rozvedena v diferenciální diagnostice.
Při klinickém vyšetření je subunguální glomus tumor patrný jako purpurová makula či papulka pod nehtovou ploténkou, kterou může tumor deformovat. Při palpaci může ložisko problednout (Haynesův fenomén) a pacient pociťuje ostrou bolestivost v místě lokalizace tumoru (Loveho test) [46, 54]. Paroxysmální bolest je vyvolána tlakem nehtové ploténky na tumorózní tkáň či změnou teploty ve smyslu ochlazení. Tento paroxysmální záchvat bolesti může trvat několik minut až hodin. Typické pro glomus tumor je vymizení záchvatu paroxysmální bolestivosti končetiny po přiložení turniketu proximálně od tumorózní léze (Hildrethovo znamení) [46, 54]. Jako raritní je v literatuře také popsána varianta subunguálního glomus tumoru, která nečinila svému nositeli žádné bolestivé vjemy [46, 54].
Diagnostika a diferenciální diagnostika
Pečlivé klinické vyšetření a analýza klinických příznaků vede v 50–78 % ke správné diagnóze [46, 54]. V diferenciální diagnostice bychom měli vyloučit ostatní subunguální tumory: angioleiomyom [7], leiomyom, Kaposiho sarkom, pyogenní granulom, keratoakantom, spinocelulární karcinom, bazocelulární karcinom, metastázy nádorů do subunguálního prostoru, subunguální exostózu, epidermální cystu a gangliom. Nikdy bychom neměli opomenout v diferenciální diagnostice akrolentiginózní melanom [38]. Také je vhodné vyloučit dnu a kalcinózu [63].
Při diagnostických pochybách využíváme metody podporující diagnózu subunguálního glomus tumoru. Provádíme chladový provokační test či tlakový test (Loveho test) a analyzujeme výskyt paroxysmálního záchvatu bolestivosti končetiny. Laboratorní stanovení hladiny kyseliny močové a hladiny iontů kalcia odliší dnu a kalcinózu. Dále můžeme využít širokou paletu zobrazovacích technik. Rentgenové vyšetření distální falangy může prokázat ve 22–60 % přítomnost erozivní plochy, která je dána přímým tlakem tumoru na kostní struktury distální falangy [2, 21, 22]. Bohatá vaskularizace subunguálních glomus tumorů dovoluje jejich zobrazení angiografickým vyšetřením s aplikací kontrastní látky do cévního řečiště. Angiografické metody se pro svou semiinvazivitu rutinně nevyužívají [46]. Další zobrazovací metodou, kterou diagnostikujeme subunguální glomus tumory větší než 3 mm, je ultrazvuková sonografie. Glomus tumory se jeví jako hypodenzní ložiska v subunguální lokalizaci. Nevýhodou této metody je 75% senzitivita, která je výrazně ovlivněna zkušenostmi vyšetřujícího personálu a přítomností akustického stínu nehtové ploténky [14].
Zlatým standardem v diagnostice subunguálních tumorů je diagnostika magnetickou rezonancí (MRI). Využití MRI v diagnostice subunguálního glomus tumoru pochází z posledního desetiletí 20. století z francouzských pracovišť [11, 20, 23, 33, 50] a umožňuje neinvazivní vyšetření nehtového aparátu s přesnou lokalizací tumorózního procesu nehtového aparátu již od velikosti 1–2 mm. Výhodou MRI vyšetření je možnost rozlišení tkáně, ze které tumor vznikl, na základě T1 a T2 relaxačních časů [11, 20, 23, 50]. Můžeme odlišit struktury glomus tumoru, angiomu nehtového lůžka, myxoidní cysty, subunguální exostózy, fibromu či akrolentiginózního melanomu. V případě pochybností lze upřesnit diagnostiku subunguálních tumorů intraarteriální aplikací gadolinia (kontrastní MRI) [11, 20, 23, 33, 50, 64].
Histologie
Histologické vyšetření zůstává nadále hlavním vyšetřením, které potvrdí diagnózu glomus tumoru. Mikroskopický nález je většinou zcela typický, v histologickém obraze vidíme nejčastěji solidní tumor nehtového lůžka, velikosti průměru 1 cm, dobře ohraničený vazivovou membránou. V histologickém obraze prokazujeme množství vaskulárních prostor vystlaných endoteliemi, které jsou obklopeny dvěma až třemi vrstvami kuboidních glomových buněk. Glomové buňky mají velké oválné až okrouhlé bazofilní jádro a úzký lem eozinofilní cytoplasmy. Nádor také obsahuje myelinizovaná a nemyelinizovaná nervová zakončení. Histologický obraz glomus tumoru je typický, imunohistochemická metoda prokáže původ glomových buněk: pozitivní α-SMA (specific muscle actin) a vimentin, negativní desmin, S-100 protein a HMB 45 [24, 54, 63]. Lokalizace tumoru v hluboké dermis, perivaskulární distribuce glomových buněk a jejich cytomorfologický a imunohistochemický profil jsou klíčovými znaky v histologické diagnostice. Experimentálně lze v histologické diagnostice užít metody elektronové mikroskopie [55].
Terapie
Jedinou účinnou léčbou subunguálního glomus tumoru je radikální exstirpace tumoru (obr. 6). Rekurence klinických symptomů po chirurgickém výkonu jsou popisovány ve 12–24 % [22]. Příčinou těchto rekurencí je neprovedení radikální exstirpace tumoru in toto. Alternativně a zcela experimentálně lze subunguální glomus tumor odstranit elektrokoagulací, vaporizačním laserem nebo lokální radioterapií [35, 54, 59, 60, 63].
Obr. 6. Glomus tumor A: pacientka po proximální, příčné ablaci nehtové ploténky s obnažením subunguálního prostoru s glomus tumorem nehtového lůžka B: stav po excizi glomus tumoru C: histologický obraz glomus tumoru, barvení hematoxylin- eozin (HE) D: histologický obraz glomus tumoru, histochemické vyšetření, barvení α-SMA 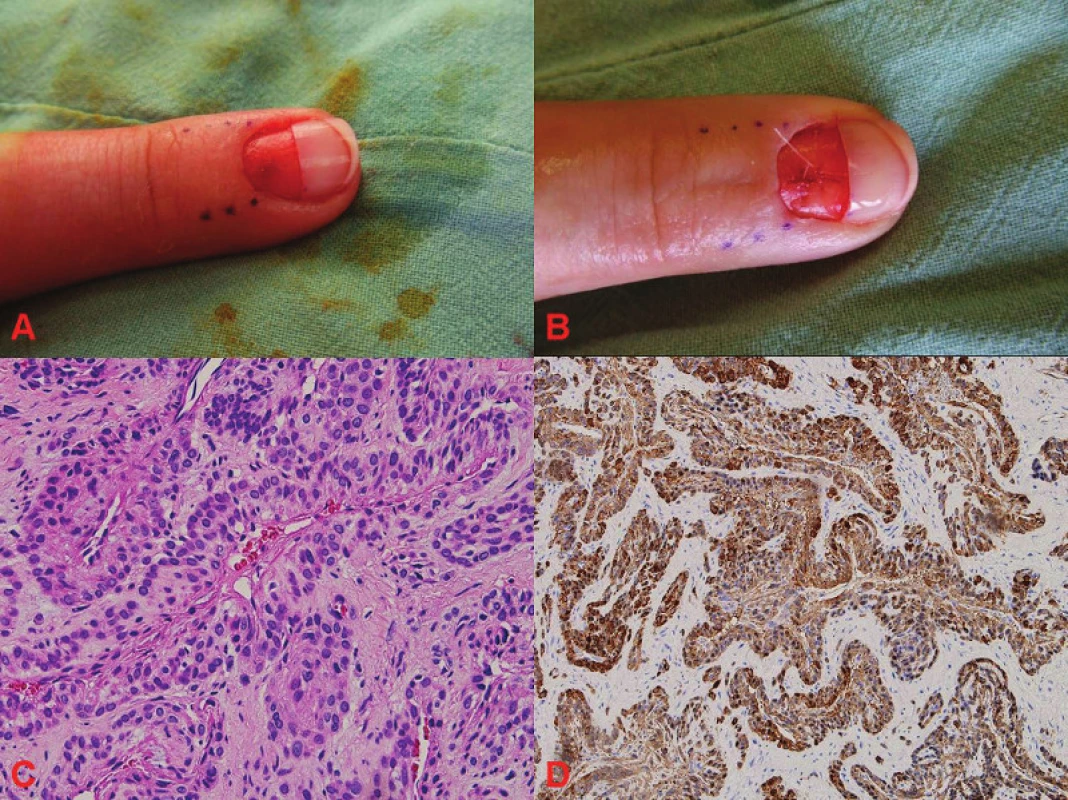
Vlastní soubor léčených pacientů: materiál, metodika a výsledky
Od roku 2002 do roku 2012 jsme diagnostikovali a chirurgicky exstirpovali tři subunguální glomus tumory. Před operačním výkonem jsme provedli u všech pacientů klinické vyšetření, chladový provokační test, Loveho test a rentgenové vyšetření distální falangy postiženého prstu končetiny. Diagnóza byla u všech pacientů potvrzena histologickým vyšetřením. V souboru byli dva muži, ve věku 50 let, respektive 45 let, a jedna žena ve věku 32 let. Průměrná doba potíží trvající ke stanovení správné diagnózy byla 11 let. U všech pacientů jsme provedli transunguální exstirpaci tumoru po předchozí ablaci nehtové ploténky. Léze se po radikální exstirpaci tumoru zhojily bez komplikací, po operačním výkonu jsou pacienti bez příznaků a bez známek recidivy onemocnění. Nehtová ploténka, která byla odstraněna totální ablací, dorostla a nevykazuje žádné známky dystrofie.
Subunguální exostóza
Subunguální exostóza je definována jako solitární, benigní nádor vycházející z kostní struktury distální falangy prstů. Poprvé byla popsána v roce 1847 Dupuytrenem na palci nohy, v roce 1857 byla Hutchinsonem popsána subunguální exostóza prstů ruky [1]. Mechanismus vzniku subunguální exostózy není znám, faktory ovlivňující vznik onemocnění zahrnují především chronicku mechanickou traumatizaci distální falangy prstů. Onemocnění postihuje 2krát častěji adolescentní ženy, postižen je v 77 % případů palec u nohy [5, 6, 48].
Subunguální exostóza se projevuje na tlak bolestivým, tuhým zduřením postranního nehtového valu s deformitou nehtové ploténky (parciální onycholýza). Diagnóza je dána klinickým nálezem doplněným rentgenovým průkazem exostózy. V diferenciální diagnostice je nutno vyloučit pyogenní granulom, vulgární verruku, keratoakantom, spinocelulární karcinom, fibrom, subunguální melanom a osteochondrom. Léčba je chirurgická, po eventuálním snesení nehtové ploténky je subunguální exostóza radikálně excidována, od kostní struktury falangy je vyštípnuta kostními kleštěmi. Histologie excidátu potvrdí diagnózu přítomností trabekulární kosti s fibrózně-chrupavčitou membránou na povrchu. Vzniklý defekt můžeme sešít (monofilament 3/0 nebo 4/0), nebo jej dohojit per secundam intentionem s dobrým kosmetickým efektem. Recidivy subungální exostózy jsou po radikálním odstranění popisovány v 11 % [1, 5, 6, 17].
Operovali jsme 20letého baletního tanečníka pro bolestivou subunguální exostózu mediálně-distální oblasti levého halluxu. Jednalo se o tuhou, polokulovitou papulu průměru 1 cm, která deformovala nehtovou ploténku. Rentgenové vyšetření kostního skeletu distální falangy prokázalo přítomnost exostózy. Provedli jsme parciální ablaci nehtové ploténky v rozsahu nad subunguální exostózou, následovala radikální excize exostózy a sešití vzniklého defektu monofilamentem 3/0. Histologické vyšetření potvrdilo diagnózu subunguální exostózy. Po operačním výkonu došlo ke zhojení ad integrum, bez deformity nehtové ploténky a bez recidivy onemocnění (obr. 7).
Myxoidní cysta
Myxoidní cysta byla poprvé popsána Hidem v roce 1883, jedná se o časté onemocnění postihující zejména ženy středního věku [10, 17, 18]. Příčina vzniku není známá, diskutuje se o traumatických vlivech vzniku cysty, která je kanálkem spojena s distálním interfalangeálním kloubem, který vykazuje známky osteoartritidy. Na dorzální ploše zadního nehtového valu distálního článku prstu ruky, vzácně na prstech nohou, vzniká v prostoru mezi zadním nehtovým valem a distálním interfalangeálním kloubem obvykle solitární, ohraničený, měkký, často průhledný cystický útvar až 1 cm velký, někdy bolestivý. Útvar tlačí na nehtovou matrix za vzniku longitudinální brázdy nehtové ploténky. Obsah cysty je vazký a bohatý na hyaluronovou kyselinu. Histologicky zjišťujeme myxoidní degeneraci vaziva [66]. Z léčebných konzervativních metod můžeme cystu vypustit punkcí, aplikovat intralezionálně kortikosteroidy, nebo se pokusit o léčbu kryalizací. Lékem volby zůstává radikální exstirpace cysty s histologickým vyšetřením.
Operovali jsme 25letou pacientku s typickým klinickým obrazem myxoidní cysty v oblasti zadního nehtového valu prostředníčku pravé ruky. Provedli jsme horizontální exstirpaci útvaru se suturou vzniklého defektu monofilamentem 3/0. Histologie potvrdila klinickou diagnózu myxoidní cysty. Po provedeném operačním výkonu jsme pacientku sledovali dva roky, nedošlo k recidivě onemocnění (viz obr. 7).
Obr. 7. Myxoidní cysta a subunguální exostóza A: pacientka s myxoidní cystou před operací B: pacientka po operaci myxoidní cysty C: pacient se subunguální exostózou před operací D: pacient po operaci subunguální exostózy 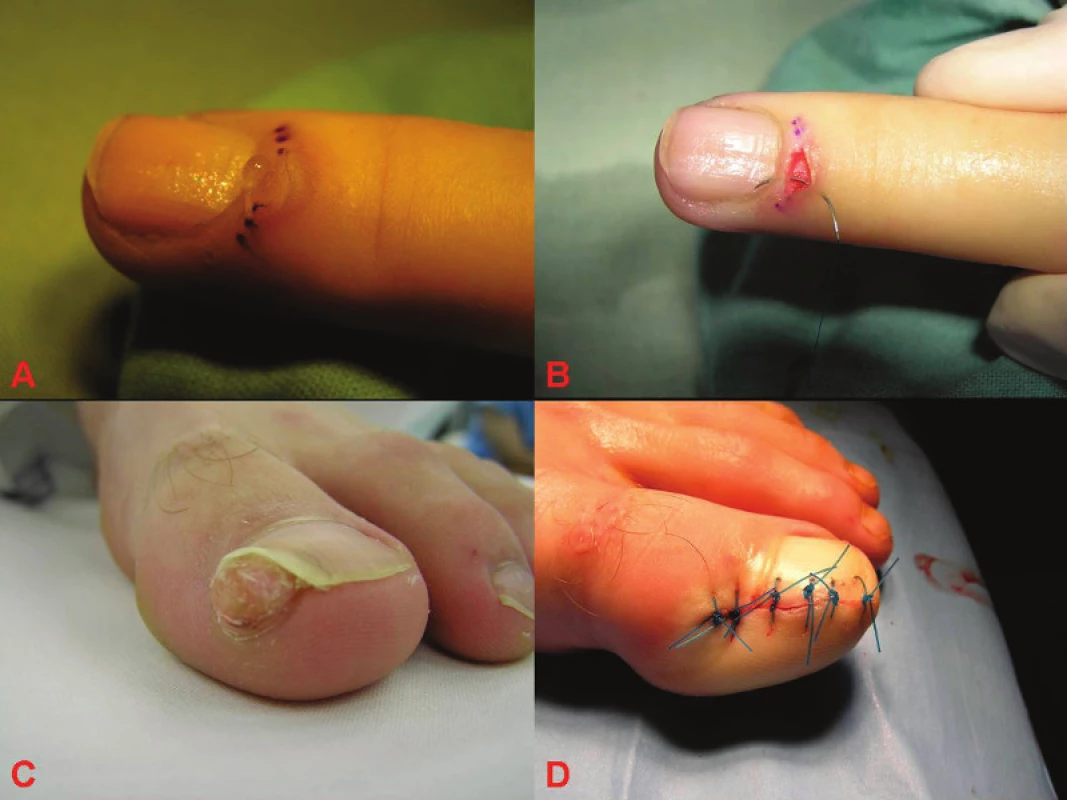
Subunguální keratoakantom
Subunguální keratoakantom je vzácným benigním nádorem nehtového aparátu, do dnešních dnů jsou v literatuře popsány necelé čtyři desítky případů. Jedná se o bolestivý, rychle rostoucí (4–8 týdnů) hyperkeratotický tumor subunguálního prostoru terminální falangy, poprvé popsaný Fischerem v roce 1961, asociovaný s erozí kostního skeletu distální falangy. Vyskytuje se převážně na prstech rukou u mužů v 5. deceniu a nejeví tendenci ke spontánnímu zhojení tak, jak je tomu u keratoakantomů na volné kůži [16, 49, 58]. Etiologie onemocnění není známa, zvažuje se role dehtu, minerálních olejů, drátěnek (trauma) či virové etiologie lidskými papilomaviry (HPV) [19]. V diferenciální diagnostice je nutno vyloučit především virové bradavice a spinocelulární karcinom. Diagnóza subunguálního keratoakantomu je dána typickou anamnézou rychle rostoucího, bolestivého nádoru subunguálního prostoru prstů ruky, klinickým obrazem (po odloučení nehtové ploténky se objeví hrbol krytý krustou nebo exulcerovaný). Rentgenové vyšetření distální falangy prstů může prokázat ostře ohraničenou čepičkovitou erozi kostní struktury postižené falangy. Histologické vyšetření s typickým histologickým obrazem potvrdí diagnózu subunguálního keratoakantomu. Lékem volby je radikální excize nádoru po předchozí totální ablaci nehtové ploténky [19].
Námi operovaný 72letý pacient s histologicky ověřeným subunguálním keratoakantomem, který bolestivě vyrostl v průběhu jednoho měsíce v subunguálním prostoru palce pravé ruky, na rentgenovém snímku bez eroze kostní struktury distální falangy, byl řešen radikální excizí nádoru po předchozí ablaci nehtové ploténky. Po operačním výkonu došlo ke zhojení ad integrum, bez deformity nehtové ploténky a bez recidivy onemocnění (obr. 8).
Obr. 8. Keratoakantom A: pacient s projevem subunguálního keratoakantomu B: odstranění nehtové ploténky a vizualizace rozsahu keratoakantomu C: pacient po radikální excizi keratoakantomu D: pacient za 6 měsíců po operaci 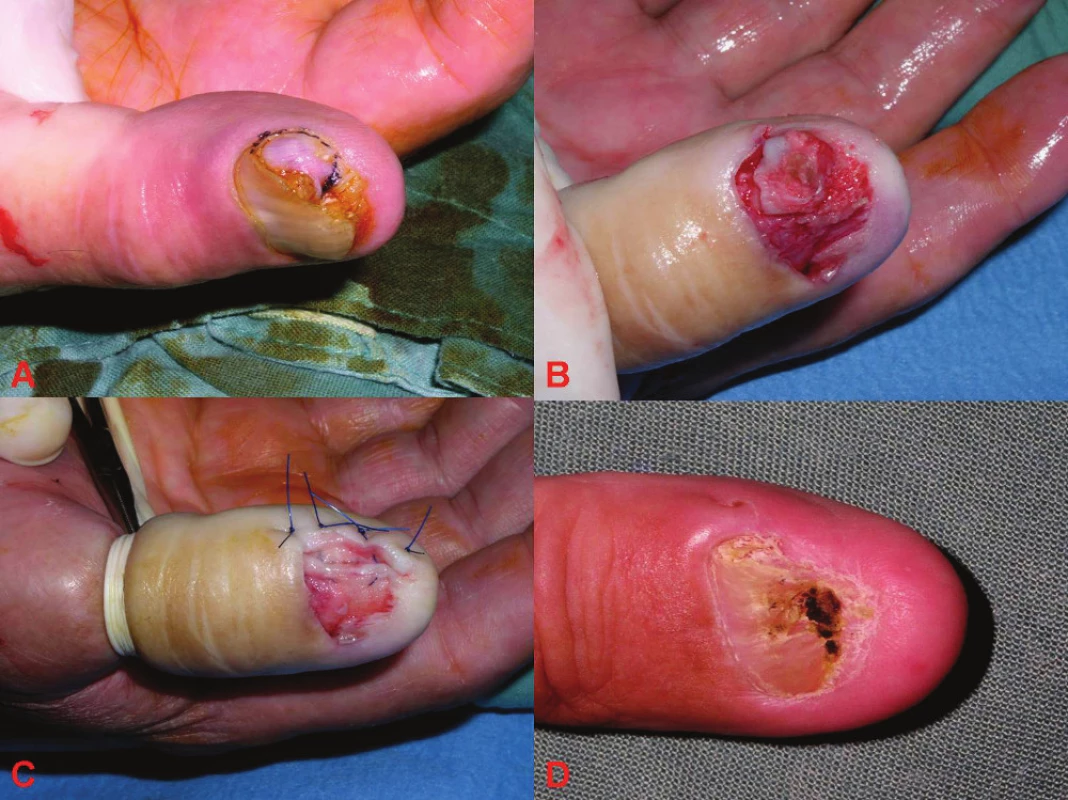
Subunguální melanom
Subunguální melanom postihuje obě pohlaví stejně, predilekční lokalizací jsou v 75 % případů palce nohou a rukou. Stanovení diagnózy subunguálního melanomu je často obtížné, 10–15 % případů tvoří amelanotické formy, ale i při přítomnosti pigmentu je zejména v počátečním stadiu obtížné odlišení od subunguálního hematomu [38]. Ložisko hematomu je striktně vázáno na oblast nehtové ploténky a postupně s růstem nehtu odrůstá a mizí (obr. 9). Jakmile pigmentace subunguálního melanomu přerůstá ze subunguálního prostoru na nehtové valy (Hutchinsonovo znamení), je diagnóza melanomu jednoznačná. Subunguální melanom může někdy imitovat zarůstající nehet a pacient dochází na opakovaná chirurgická ošetření, než je stanovena diagnóza melanomu [38]. Při diagnostických rozpacích je na místě včasná probatorní biopsie. Histologický nález bývá podobný nálezu u superficiálně se šířícího melanomu. Jednotlivé melanomové buňky a nádorová hnízda infiltrují všechny úrovně epidermis a postupně se šíří do koria. Nádorové buňky mají tendenci k pronikání podél vývodů potních žláz hluboko do koria a podkoží [38]. Rozsah chirurgického výkonu při subunguálním postižení je závislý na lokalizaci a rozsahu ložiska. V podstatě není možné dosáhnout ani jednocentimetrového lemu zdravé tkáně bez odstranění posledního článku prstu (viz obr. 9). Ve většině případů je nutné přistoupit k amputaci distálního článku postiženého prstu [38]. Při lokalizaci na palci se provádějí amputace v interfalangeálním kloubu, u ostatních prstů v distálním interfalangeálním kloubu. Při rozsáhlém postižení prstu je vhodné provést amputaci celého prstu v metakarpofalangeálním kloubu [4, 5, 6]. Vhodné je rovněž provedení peroperačního mapování a biopsie sentinelové uzliny.
Obr. 9. Subunguální hematom a subunguální melanom A: subunguální hematom B: subunguální melanom C: peroperační snímek diagnostické excize subunguálního melanomu D: stav po provedené diagnostické excizi subunguálního melanomu, po které následovala amputace prstu 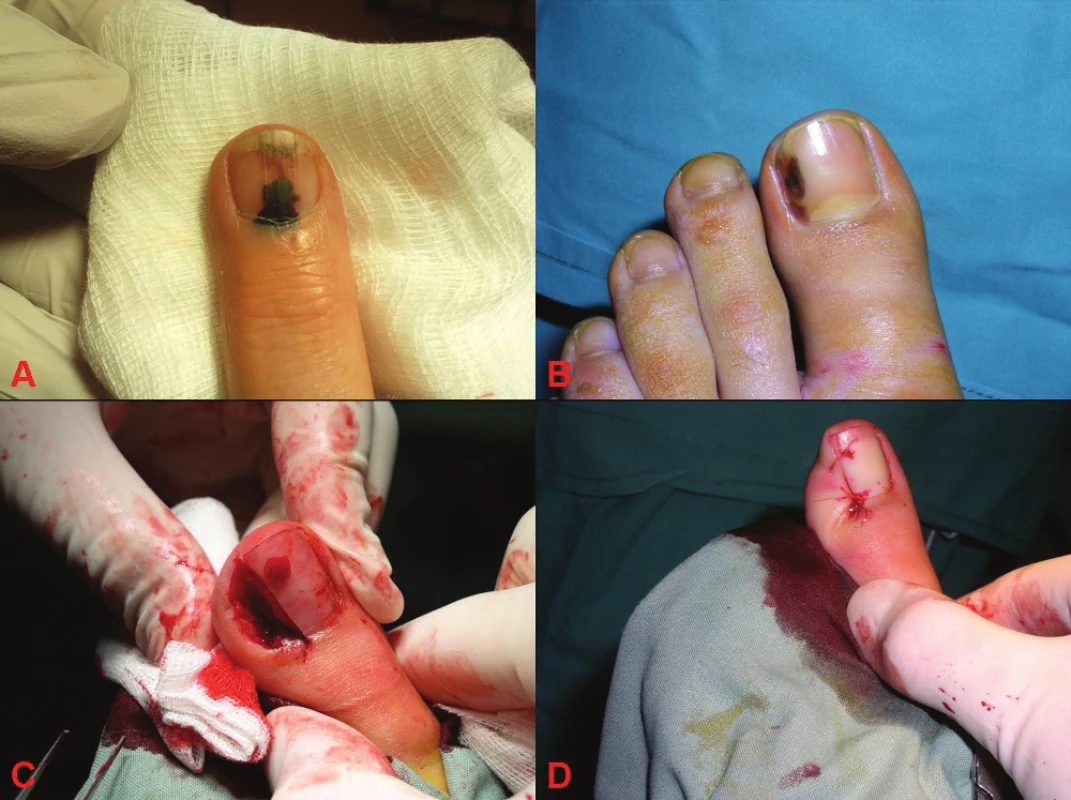
ZÁVĚR
Chirurgie nehtového aparátu je delikátní oblastí dermatochirurgie vyžadující důkladnou znalost stavby a funkce nehtového aparátu. V České republice je nehtová chirurgie neprávem opomíjenou disciplínou. Dermatologům se nehtová chirurgie jeví obtížná, pro plastické chirurgy není nehtová chirurgie dostatečně atraktivní a pro všeobecné chirurgy se jedná o marginální problematiku. Hlavními indikacemi chirurgického výkonu nehtového aparátu jsou zejména pigmentové projevy, subunguální tumory a deformity nehtových plotének. Přístup k subunguálním projevům je možný po odstranění korespondující oblasti nehtové ploténky, poté lze biopsií získat materiál k histologickému vyšetření a ke stanovení přesné diagnózy. Prováděné biopsie v oblasti nehtového lůžka by měly být provedeny striktně podélně, zatímco biopsie nehtové matrix příčně. Po stanovení přesné diagnózy onemocnění nehtového aparátu je nejčastěji volena radikální excize se zachováním vzhledu i funkce nehtového aparátu.
Na našem pracovišti operujeme v lokální anestezii děti od 5 let věku a dospělé pacienty; mladší a nespolupracující pacienty operujeme v celkové anestezii. Neprovádíme operační výkon v prvním trimestru gravidity, u pacientů s poruchou prokrvení akrálních partií končetin (ischemická choroba končetin, endangiitis obliterans, diabetes mellitus, kolagenózy, chronický flebo/lymfedém), u imunosuprese jakékoli etiologie a při alergii na lokální anestetikum 30. Ke všeobecným komplikacím chirurgických výkonů nehtového aparátu patří ischémie z nadměrně komprimujícího krytí, bolestivost, otok, krvácení, hematom, infekce v místě výkonu, nežádoucí účinky lokální anestezie a recidiva onemocnění, pokud není provedena excize in toto. Obávanou komplikací je rozvoj ireverzibilní nehtové dystrofie. Jejímu vzniku můžeme předejít co nejšetrnějším operováním (zásady fyziologického operování podle Buriana) a co nejcitlivějším přístupem k nehtové matrix [30]. Chirurgie nehtového aparátu vyžaduje týmovou transdisciplinární spolupráci, členem operačního týmu je dermatolog, plastický chirurg, odborník v zobrazovacích metodách (rentgen, ultrazvuk, magnetická rezonance) a anesteziolog při operacích v celkové anestezii. Jen komplexním přístupem k uvedené problematice, s hlubokými znalostmi anatomie, histologie, fyziologie nehtového aparátu, s širokou diferenciální diagnostikou onemocnění nehtového aparátu a znalostí chirurgických technik, lze úspěšně pomoci našim pacientům.
Do redakce došlo dne 24. 6. 2013.
Kontaktní adresa:
MUDr. Radek Litvik
Kožní oddělení
Fakultní nemocnice Ostrava
17. listopadu 1790
708 52 Ostrava-Poruba
e-mail: radek.litvik@fno.cz
Zdroje
1. AGGARWAL, K., GUPTA, S., JAIN, VK., MITAL, A., GUPTA, S. Subungual exostosis. Indian J. Dermatol. Venereol. Leprol., 2008, 74, 2, p. 173–174.
2. ALI NOOR, M., MASBAH, O. Synchronous glomus tumors in a distal digit: a case report. J. Hand Surg., 1997, 22, 3, p. 508–510.
3. ARENBERGER, P., ŠTORK, J. Keratinizovaná adnexa. In Štork, J. et al. Dermatovenerologie. Praha : Galén, 2008, s. 8.
4. BANKS, A. S., DOWNEY, M. S., MARTIN, D. E., MILLER, S. J. McGlamry’s comprehensive textbook of foot and ankle surgery – volume I. 3rd ed. Lippincott Williams and Wilkins. 2001, p. 1278
5. BARAN, R. Common – sense advice for the treatment of selected nail disorders. JEADV, 2001, 15, 2, p. 97–102.
6. BARAN, R., DE BERKER, D., DAWBER, R. Manual of Nail Disease and Surgery. 2nd ed. London: Blackwell Science Ltd. 1997, p. 93
7. BARAN, R., REQUENA, L., DRAPÉ, JL. Subungual angioleiomyoma masquerading as a glomus tumour. Br. J. Dermatol., 2000, 142, 6, p. 1239–1241.
8. BARAN, R., FOX, L., ROBERT, C. Nail toxicity of targeted anticancer therapies. In ROBERT, C., SIBAUD, V. Cutaneous side effects induced by targeted anticancer therapies. Editions Privat. 1st Ed. 2011, p. 117–124.
9. BELANGER, S. M., WEAVER, T. D. Subungual glomus tumor of the hallux. Cutis, 1993, 52, 1, p. 50–53.
10. BOLOGNIA, J. L., JORIZZO, J. L., RAPINI, R. P. Dermatology – volume II. Mosby. 1st Ed. 2003, p. 1817–1842.
11. BOUDGHENE, F. P., GOUNY, P., TASSART, M. et al. Subungual glomus tumor: combined use of MRI and three – dimensional contrast MR angiography. J. Magn. Reson. Imaging, 1998, 8, 6, p. 1326–1328.
12. BOUREZANE, Y., THALAMY, B. Ingrown toenail and indinavir case-control study demonstrates strong relationship. AIDS, 1999, 13, 15, p. 2181–2182.
13. BURGE, S., COLVER, G., LESTER, R. Simple Skin Surgery. Bleckwell Science Ltd. 2nd Ed. 1996, p. 90
14. CHEN, S. H., CHEN, Y. L., CHENG, M. H., YEOW, K. M., CHEN, H. C., WEI, F. C. The use of ultrasonography in preoperative localization of digital glomus tumors. Plast. Reconstr. Surg., 2003, 112, 1, p. 115–119.
15. CONNOLLY, A. A. P., MEYER, L. C., TATE, J. J. T. Local anaesthetic agents in surgery for ingrown toenail. Br. J. Surg., 1994, 81, 3, p. 425–426.
16. CONNOLLY, M., NARAYAN, S., OXLEY, J., DE BERKER, DAR. Immunohistochemical staining for the differentiation of subungual keratoacanthoma from subungual squamous cell carcinoma. Clin. Exp. Dermatol., 2008, 33, 5, p. 625–628.
17. DE BERKER, D., BARAN, R., DAWBER, R. Handbook of Diseases of the Nails and their Management. Blackwell Science Ltd. 1st Ed. 1995, p. 177.
18. DE BERKER, D., LAWRENCE, C. Ganglion of the distal interphalangeal joint (myxoid cyst): therapy by identification and repair of the leak of joint fluid. Arch. Dermatol., 2001, 137, 5, p. 607–610.
19. DOBSON, C. M., AZURDIA, R. M., KING, C. M. Squamous cell carcinoma arising in a psoriatic nail bed: case report with discussion of diagnostic difficulties and therapeutic options. Br. J. Dermatol., 2002, 147, 1, p. 144–149.
20. DRAPÉ, J. L., IDY–PERETTI, I., GOETTMANN, S. et al. Subungual glomus tumors: evaluation with MR imaging. Radiology, 1995, 195, 2, p. 507–515.
21. EKIN, A., ÖZKAN, M., KABAKLIOGLU, T. Subungual glomus tumours: a different approach to diagnosis and treatment. J. Hand Surg., 1997, 22, 2, p. 228–229.
22. GARMAN, M. E., ORENGO, I. F., NETSCHER, D., SCHWARTZ, M. R., ROSEN, T. On glomus tumors, warts, and razors. Dermatol. Surg., 2003, 29, 2, p. 192–194.
23. GOETTMANN, S., DRAPÉ, J. L., IDY–PERETTI, I., et al. Magnetic resonance imaging: a new tool in the diagnosis of tumours of the nail apparatus. Br. J. Dermatol., 1994, 130, 6, p. 701–710.
24. HANDA, U., PALTA, A., MOHAN, H., PUNIA, R. P. Aspiration cytology of glomus tumor. Acta Cytol., 2001, 45, 6, p. 1073–1076.
25. HANEKE, E., BARAN, R. Subunguale tumoren. Z. Hautkr., 1981, 57, 5, p. 355–362.
26. HANEKE, E. Nail surgery. Eur. J. Dermatol., 2000, 10, 3, p. 237–241.
27. HANEKE, E. Nail surgery. J. Cutan. Aesthet. Surg., 2011, 4, 3, p. 163–164.
28. HANEKE, E. Advanced Nail Surgery. J. Cutan. Aesthet. Surg., 2011, 4, 3, p. 167–175.
29. HANEKE, E. Contraversies in the Treatment of Ingrown Nails. Dermatol. Res. Pract., 2012, p. 1–12.
30. HANEKE, E., BARAN, R. Nail Surgery. In HARAHAP, M. Complications of dermatologic Surgery. Springer. 1st ed. 1993, p. 84–91.
31. HEGYI, E., HEGYI, V. Dermatovenerologická propedeutika. 1. vyd. Bratislava: Medicina correctiva, 1997. 314 s.
32. HSU, CH. J., WANG, D. Y. Glomus tumors. Mid. Taiwan J. Med., 2002, 7, p. 222–227.
33. IDY–PERETTI, I., CERMAKOVA, E., DION, E., REYGAGNE, P. Subungual glomus tumor: diagnosis based on high–resolution MR images. Am. J. Roentgenol., 1992,159, 6, p. 1351.
34. JATŠOVÁ, E., MARDEŠIČOVÁ, L. Možnosti terapie unguis incarnatus. Trendy v medicíně, 2002, 4, 5, p. 102–105.
35. KAHLE, B., DREPPER, E. Sklerosierungstherapie bei multiplen glomangiomen. Phlebol, 1995, 24, p. 52–54.
36. KING, B. Pain at first dressing change after toenail avulsion. The experience of nurses, patients and observer: 1. J. Wound Care, 2003, 12, 1, p. 5–10.
37. KOTI, M., BHATTACHARRYYA, R., EWEN, S. W. B., MAFFULLI, N. Subungual glomus tumor of the hallux. Acta Orthop. Belg., 2001, 67, 3, p. 297–299.
38. KRAJSOVÁ, I. Melanom. 1. vyd. Praha: Maxdorf, 2006. 332 s.
39. KRTIČKA, F. Epistolae chirurgicae. Rozhl. Chir., 1999, 78, 7, s. 364–366.
40. KWON, S. H., CHOI, J. W., HONG, J. S., BYUN, S. Y., PARK, K. C., YOUN, S. W., HUH, C. H. Gefitinib-Induced Paronychia: Response to Autologous Platelet-Rich Plasma. Arch. Dermatol., 2012, 148, 12, p. 1399–1402.
41. LIM, I. J., PHO, R. W. H., TOCK, E. P. C. Atypical extraungual manifestation of a subungual glomus tumour. Br. J. Plast. Surg., 1999, 52, 4, p. 327–328.
42. LITVIK, R. Surgical treatment of the ingrown toenail. JEADV, 2003, 17, Suppl. 3, p. 267–268.
43. LITVIK, R., KEMPNY, T., VANTUCHOVA, Y. Treatment of ingrowing toenail using phenol. JEADV, 2004, 18, Suppl. 1, p. 69.
44. LITVIK, R., VANTUCHOVA, Y. What’s new in the treatment of the ingrown toenail? JEADV, 2004, 18, Suppl. 1, p. 69.
45. MALEY, E. D., MAC DONALD, CH. J. Bilateral subungual glomus tumors. Plast. Reconstr. Surg., 1975, 55, 4, p. 488–489.
46. MOOJEN, T. M., HOUPT, P. Glomus tumors of the hand in the Netherlands: analysis of 107 patients. Eur. J. Plast. Surg., 2000, 23, p. 224–226.
47. NAZARI, S. A simple and practical method in treatment of ingrown nails: splinting by flexible tube. JADV 2006, 20, 10, p. 1302–1306.
48. NOWILLO, K. S., SIMPSON, R. L. Subungual exostosis of the finger with nail plate induction. Hand, (NY), 2010, 5, 2, p. 203–205.
49. OLIWIECKI, S., PEACHEY, R. D. G., BRADFIELD, J. W. B., ELLIS, J., LOVELL, C. R. Subungual keratoacanthoma – a report of four cases and review of the literature. Clin. Exp. Dermatol, 1994, 19, 3, p. 230–235.
50. OPDENAKKER, G., GELIN, G., PALMERS, Y. MR imaging of a subungual glomus tumor. Am. J. Roentgenol., 1999, 172, 1, p. 250–251.
51. PETRES, J., ROMPEL, R., ROBINS, P. Dermatologic Surgery. Springer, 1st Ed. 1996, p. 522.
52. RAMMELT, S., GRASS, R., ZWIPP, H. Zur Behandlung des eingewachsenen Zehennagels. Chirurg, 2003, 74, p. 239–243.
53. ROBINSON, J. C., KILPATRICK, S. E., KELLY, D. L. Intraosseous glomus tumor of the spine. J. Neurosurg., 1996, 85, 2, p. 344–347.
54. ROHRICH, R. J., HOCHSTEIN, L. M., MILLWEE, R. H. Subungual glomus tumors: an algorithmic approach. Ann. Plast. Surg., 1994, 33, 3, p. 300–304.
55. SAWADA, S., HONDA, M., KAMIDE, R., NIIMURA, M. Three cases of subungual glomus tumors with von Recklinghausen neurofibromatosis. J. Am. Acad. Dermatol., 1995, 32, 2, p. 227–228.
56. SCHULTE, K. W., NEUMANN, N. J., RUZICKA, T. Surgical Pearl: Nail splinting by flexible tube–A new noninvasive treatment for ingrown toenails. J. Am. Acad. Dermatol., 1998, 39, 4, p. 629–630.
57. SIBAUD, V., DALENCE, F., MOUREY, L., CHEVREAU, C. Paronychia and pyogenic granuloma induced by new anticancer mTOR inhibitors. Acta Derm. Venereol., 2011, 91, 5, p. 584–585.
58. SINHA, A., MARSCH, R. LANGTRY, J. Spontaneous regression of subungual keratoacanthoma with reossification of underlying distal lytic phalynx. Clin. Exp. Dermatol, 2005, 30, 1, p. 20–22.
59. TADA, H., HIRAYMA, T., TAKEMITSU, Y. Prevention of postoperative nail deformity after subungual glomus resection. J. Hand Surg. Am., 1994, 19A, 3, p. 500–503.
60. TAKATA, H., IKUTA, Y., ISHIDA, O., KIMORI, K. Treatment of subungual glomus tumor. Hand Surg., 2001, 6, 1, p. 25–27.
61. TOSTI, A., PIRACCINI, BM., D’ANTUONO, A., MARZADURI, S., BETTOLI, V. Paronychia associated with antiretroviral therapy. Br. J. Dermatol., 1999, 140, 6, p. 1165–1168.
62. TÖRÖK, L. Kožní projevy při chorobách vnitřních orgánů. 1. vyd.. Heidelberg-Leipzig: J. A. Barth Verlag, Hüthig GmbH, 1998. 228 s.
63. TSUNEYOSHI, M., ENJOJI, M. Glomus tumor. Cancer, 1982, 50, 8, p. 1601–1607.
64. VAN RUYSSEVELT, CHEA., VRANCKX, P. Subungual glomus tumor: emphasis on MR angiography. Am. J. Roentgenol., 2004, 182, 1, p. 263–264.
65. VOKOUN, Z. Chirurgické léčení zarůstajícího nehtu. Čs. Derm., 1992, 67, 1–2, s. 51–54.
66. VOSMÍK, F. Myxoidní digitální cysta. In ŠTORK, J. et al. Dermatovenerologie. Praha: Galén, 2008, s. 376.
67. ZUBER, T. J. Ingrown Toenail Removal. Am. Fam. Physician, 2002, 65, 12, p. 2547–2550.
68. ZUBER, T. J., PFENNINGER, J. L. Management of ingrown toenail. Am. Fam. Physician, 1995, 52, 1, p. 181–190.
Štítky
Dermatologie Dětská dermatologie
Článek Odborné akce v roce 2013
Článek vyšel v časopiseČesko-slovenská dermatologie
Nejčtenější tento týden
2013 Číslo 4- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
- Condylomata accuminata a jejich prevence i léčba
- Proces hojení ran krok za krokem a co ho může zkomplikovat
- Miniinvazivní léčba pilonidálního sinu: laserová a podtlaková terapie jako šetrná a účinná modalita
- Význam lokální oxygenoterapie a ozonoterapie pro léčbu nehojivých ran
-
Všechny články tohoto čísla
- Chirurgie nehtového aparátu: úvod do problematiky, přehled operačních technik a naše zkušenosti u vybraných onemocnění nehtového aparátu
- Doškolování lékařů – kontrolní test
- Využitie UVA 1 žiarenia v liečbe dermatóz
- Zriedkavá forma Tinea capitis profunda spôsobená Trichophyton tonsurans u dietata
- Klinický případ: Svědivé papuly na hrudi
- Dermatochirurgie a její zásadní postavení v oboru dermatovenerologie
- Psychosociální aspekty života pacientů s psoriázou v České republice
- Odborné akce v roce 2013
- Kontaktné alergeny v pracovnom a životnom prostredí
- Česko-slovenská dermatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Chirurgie nehtového aparátu: úvod do problematiky, přehled operačních technik a naše zkušenosti u vybraných onemocnění nehtového aparátu
- Klinický případ: Svědivé papuly na hrudi
- Dermatochirurgie a její zásadní postavení v oboru dermatovenerologie
- Zriedkavá forma Tinea capitis profunda spôsobená Trichophyton tonsurans u dietata
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



