-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Dlouhodobé sledování pacientů se sympatickou oftalmií z diagnosticko léčebného pohledu. Literární přehled.
Autoři: J. Krásný 1; T. Eckchlager 2; K. Smetana 3; J. Šach 4; H. Šubrtová 5
Působiště autorů: Oční klinika FN Královské Vinohrady a 3. LF UK, Praha, Přednosta: prof. MUDr. P. Kuchynka, CSc. 1; Dětská onkologická klinika FN Motol a 2. LF UK, Praha, Přednosta: prof. MUDr. J. Starý, DrSc. 2; Ústav hematologie a krevní transfuze, Ředitel: prof. MUDr. P. Cetkovský, Ph. D. 3; Ústav patologie, FN Královské Vinohrady a 3. LF UK, Praha, Přednosta: prof. MUDr. R. Matěj, Ph. D. 4; Hematologická klinika FN Královské Vinohrady a 3. LF UK, Praha, Přednosta: prof. MUDr. T. Kozák, Ph. D, MBA 5
Vyšlo v časopise: Čes. a slov. Oftal., 75, 2019, No. 5, p. 235-248
Kategorie: Souborná práce
doi: https://doi.org/10.31348/2019/5/1Souhrn
Cíl: Zhodnotit možnosti diagnosticko-léčebného postupů u sympatické oftalmie (SO) ve srovnání s literárními podklady.
Teoretický podklad: SO je oční zánět autoimunitní povahy, charakterizovaný disbalancí subpopulací lymfocytů v rámci IV. typu přecitlivělosti.
Metodika: Do souboru vyšetření SO zahrnující humorální a buněčnou imunitu byl zařazen nukleolární test (NT), hodnotící aktuální stav biosyntetické aktivace lymfocytů v organismu podle morfologie jadérka dané aktivitou transkripce RNA. Kromě klasického histologického vyšetření byla jednou provedena i imunohistochemická verifikace SO pro stanovení subpopulací lymfocytů v enukleovaném bulbu.
Materiál: V rámci dvou studií v letech 1979 až 1994 a 1999 až 2017 bylo sledováno a léčeno celkově 5 pacientů mužského pohlaví se SO, která vznikla čtyřikrát po perforačním poranění a jednou po lensektomii s vitrektomií. Věk vzniku SO se pohyboval mezi 4 až 24 let (průměr 12 let). SO vznikla za 10 dnů až 3 měsíce (průměr 1,7 měsíce) po inzultu. U všech se objevil relaps onemocnění v rozmezí 3 měsíců až 38 let (průměr 15 let). Další dva pacienti s SO byli jen konsiliárně vyšetřeni, 16letý chlapec pro relaps SO po extrakci katarakty a 71-letá žena pro SO vzniklou po lensektomii s vitrektomii. Současně byla vyšetřena a porovnána skupina 19 nemocných s jinými typy uveitid. U 16 nemocných (z toho u 13 mužů a chlapců) fakoantigenní uveitidy vznikly po úrazech (perforace a kontuze). U dalších třech pacientů (mladé ženy) se po enukleaci dolorózního bulbu s uveitidou II. či. III. typu přecitlivělosti zklidnila sekundární uveitida na druhém oku bez změny celkové imunosupresivní terapie a ovlivnění NT.
Výsledky: Z komplexu provedených imunologických vyšetření byly prokázány změny u SO v hodnotách aktivních lymfocytů periferní krve. U SO byl počet aktivních lymfocytů zvýšen na rozdíl od fakoantigenních uveitid. Mezi oběma skupinami uveitid byl zjištěn u NT statisticky významný rozdíl (p = 0,0134). Diagnózy byly histologicky verifikovány (5 bulbů s SO a 7 bulbů s uveitidami nesoucitné etiologie), což bylo pro diagnostickou rozvahu zásadní. Imunohistochemické vyšetření potvrdilo přítomnost jednotlivých subpopulací T-lymfocytů, makrofágů a také B-lymfocytů. Základem imunosupresivní léčby v počátku byla kombinace prednisonu a azathioprinu, později účinnou terapii představoval cyklosporin.
Závěr: NT upozorňuje na aktuální zvýšenou aktivaci lymfocytů bez rozdílu na zastoupení subpopulací a jejich absolutní počet v mechanismu uveitidy u IV. typu přecitlivělosti. Imunosupresivní terapie tuto aktivaci zásadně ovlivňuje poklesem hodnot, především u SO, ale i uveitid dalších typů přecitlivělosti. Imunohistochemické vyšetření prokazuje různé zastoupení jednotlivých typů lymfocytů podle stadia SO.
Klíčová slova:
sympatická oftalmie – fakoantigenní uveitida – funkční aktivita lymfocytů – imunosupresivní terapie – transkripce RNA
Úvod
Soucitné onemocnění - ophthalmia sympatica (SO) je bilaterální difúzní granulomatózní uveitida. Po poranění uveální tkáně v rámci úrazu, vlastního operačního výkonu či následkem dalších léčebných postupů vzniká zánět na oku tzv. sympatizujícím podle akademika Kurze (exciting and initiating eye – podle anglosaské literatury) a v časovém odstupu se objeví uveitida i na dosud zdravém oku, tzv. sympatizovaném (sympatizing eye) [47]. Do jeho charakteristického obrazu patří špekovité precipitáty na endotelu (Obrázek 1B) a žlutavě-bílé nodulární léze cévnatky označované jako Dalenovy-Fuchsovy (F-D) noduly (Obrázek 1C) [14], jejichž četnost se pohybuje v 25 % až 35 % [51]. SO patří svým mechanismem mezi choroby IV. typu přecitlivělosti, tzv. reakce zprostředkovaná buňkami (CMI - Cell Mediated Immune Response). Senzibilizovaný lymfocyt po setkání s antigenem (uvažuje se o nejméně třech) začne produkovat mediátory, interleukiny. Tyto nízkomolekulární peptidy působí na další lymfocyty či buňky schopné předávání informací pro příslušnou imunitní reakci. Mezi nimi zvlášť důležitou roli hrají dva faktory, a to inhibující makrofágy a aktivující makrofágy. Ty potom atakují cévní stěnu a spolu s různými subpopulacemi lymfocytů včetně NK (Natural Killers - přirození zabíječi) buněk pronikajících do uveálního parenchymu (Obrázek 1A) spolu s dalšími buňkami imunitní reakce. V další fázi následuje vytváření obrovských epiteloidních buněk a inhibice granulocytů. Stimulace lymfocytů pod vlivem interleukinů vede v konečné fázi k poškození nitroočních tkání, hlavně uvey a sítnice, a to lymfotoxinem nebo kontaktní cytolýzou [34,47]. Lymfotoxin představuje jeden z cytokinů: TNF-beta s nekrotizujícím efektem potlačující růst buněk, zároveň s protizánětlivým efektem a kontaktní cytolýza je potom nespecifickou imunitní odpovědí přítomných NK buněk vedoucí osmotické lýze cílových buněk [26].
Obr. 1. Schéma IV. typu přecitlivělosti (A), pacient č. 2.: špekovité precipitáty na endotelu rohovky (B), Fuchsovy-Dalenovy noduly v cévnatce (C), remise S.O. s artefakii a Express shuntem (D) 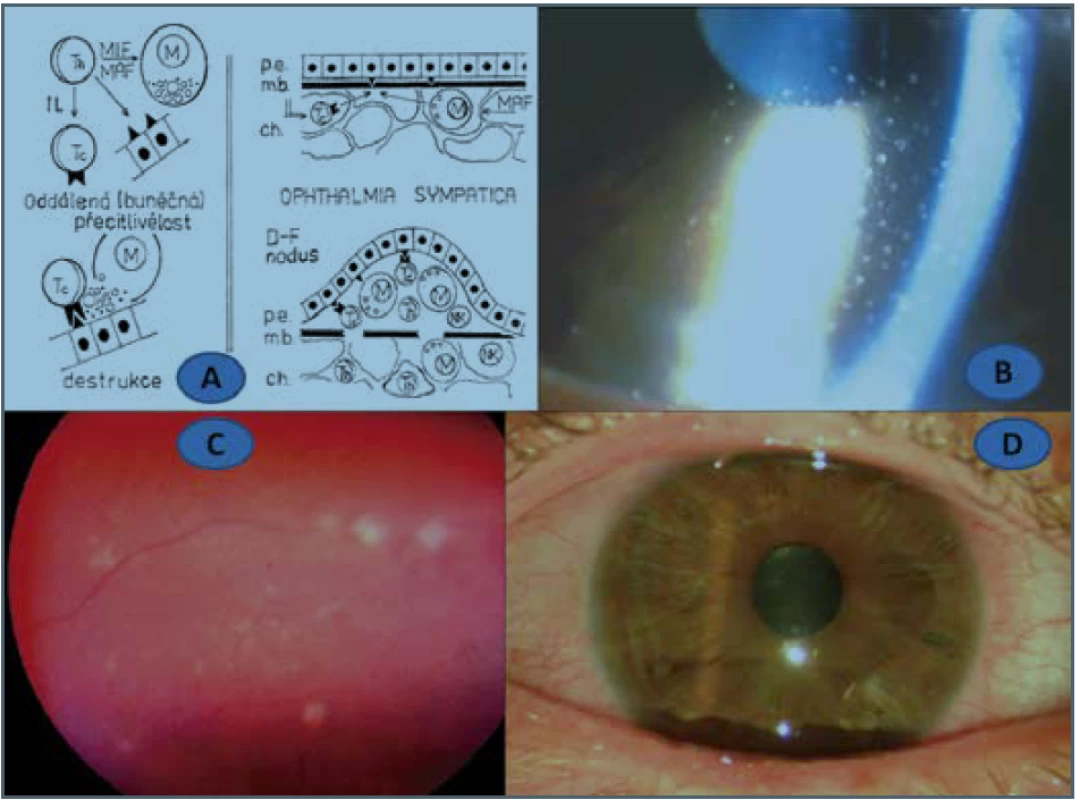
Dlouhodobé sledování SO spolu s rozborem literárních údajů nám umožnilo posoudit vývoj léčebných postupů, ale především se zamyslet nad možností laboratorního sledování imunopatologického charakteru této choroby při definování podstaty zánětlivého procesu v oku.
Metodika
Pro sledování dynamiky SO jsme zařadili široké spektrum laboratorních vyšetření z periferní krve, podmíněné danou dobou. Ve spektru humorální imunity jsme hodnotili imunoglobuliny IgA, IgM, IgG a cirkulující imunokomplexy PEG. Buněčnou imunitu jsme posuzovali společně s krevním obrazem, původně používané E-rozety (souhrnný počet T-lymfocytů) či imunoregulační index (poměr absolutního počtu helperů k cytotoxickým T-lymfocytů v periferní krvi) byly nahrazeny jednotlivými subpopulacemi lymfocytů (CD3, CD4, CD8, CD20, CD56, atd.). Do autoprotilátek jsme zařadili ty, které mají vztah uveitid k celkovým autoimunitním chorobám (ANA, ANCA, anti ds-DNA, ENA) a ze sérologie to bylo ASLO. Samostatně jsme posuzovali nukleolární test (NT), který představuje metodiku umožňující hodnotit aktuální stav biosyntetické aktivace lymfocytů na základě morfologie jadérka. Ke znázornění nukleolů v lymfocytech jsme použili cytologické barvení nátěrů periferní krve 0,05% toluidinovou modří při pH 5 pro demonstraci RNA podle prof. K. Smetany [67,68,69,71,72]. Lymfocyty lze podle funkčně dominantního typu jadérka dělit na tři typy (Obrázek 2):
- Nejpočetněji jsou zastoupeny lymfocyty s prstenčitým nukleolem (R – z anglického ring), který se znázorňuje v podobě tmavého prstýnku v jádře. Obsahuje ribonukleo-proteinové struktury pouze v periferii jadérka, hovoří se o „klidovém jadérku“. Buňky mají nízkou úroveň syntézy r-RNA, ale jsou schopny další aktivace, mohou obsahovat mikronukleoly.
- Aktivované lymfocyty (A) s „aktivovaným jadérkem“, viditelným jako kompaktní homogenní oválek v jádře s relativně uniformní distribucí RNA, které se vyznačují vysokou transkripcí RNA. Jedná se o buňky produkující interleukiny, které ovlivňují buňky schopné imunitních reakcí, nebo buňky časné fáze blastické transformace.
- Lymfocyty pouze s mikronukleoly (M) mají jadérka, které se jeví jako tmavé body v jádře lymfocytů. Mikronukleoly (inaktivní nukleoly) jsou nukleoly menší než 1,2 µm a jeví se jako malé kulaté partikule ribonukleo-proteinů. Jedná se o terminální stádium vývoje lymfocytů, které již není schopné další aktivace a jejich počet je ovlivněn zvýšeným obratem lymfocytů. Ve světelném mikroskopu inversně při zvětšení 800x se počítá podíl aktivovaných lymfocytů a buněk s mikronukleoly z celkového počtu 100 vyhledaných lymfocytů, kde zbytek tvoří neaktivní lymfocyty s prstenčitým jádrem, což se vyjadřuje v procentech (číselný údaj je uváděný v textu za znaky tří typů lymfocytů). Mezi druhým a dvanáctým rokem života se referenční hodnoty nukleolárního testu pohybují u aktivovaných lymfocytů mezi 4 – 7 % a lymfocytů s mikronukleoly mezi 8 – 14 %. Tyto hodnoty v pozdějším věku pak mírně klesají.
Obr. 2. Schéma nukleolárního testu (NT) A – aktivované lymfocyty R – lymfocyty s prstenčitým nukleolem, M – lymfocyty pouze s mikronukleoly, zvětšení (1000x) z hlediska znázornění 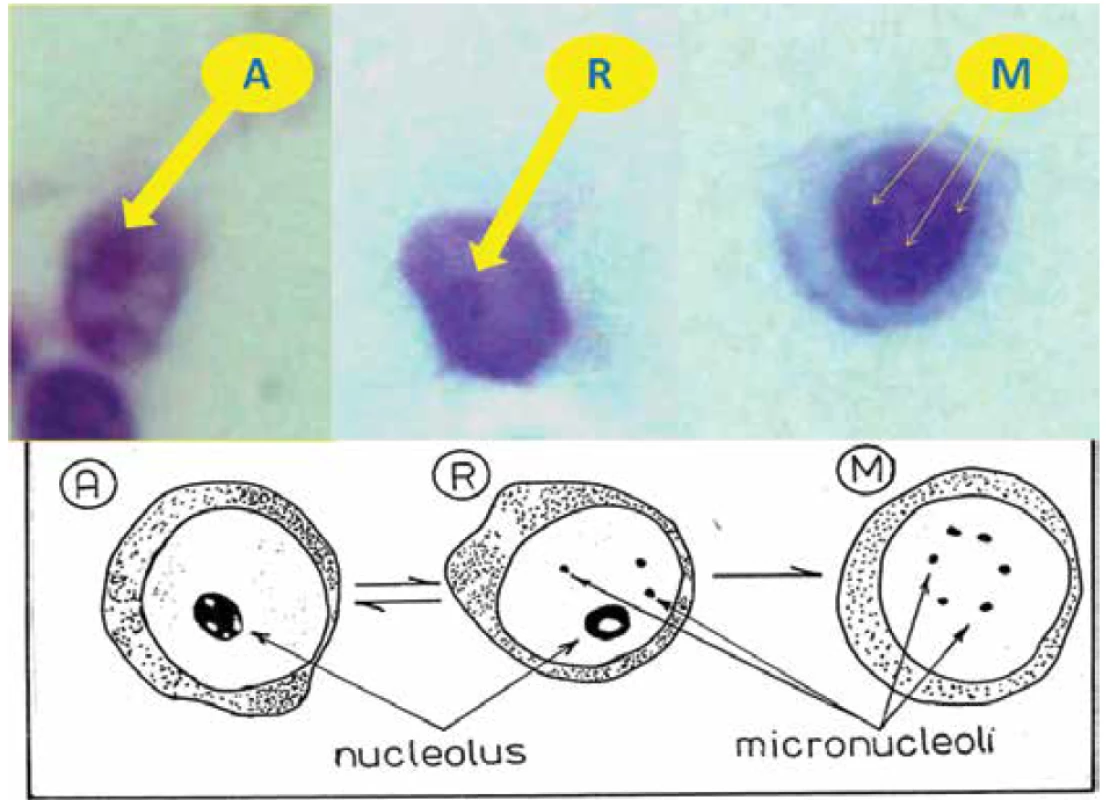
Imunohistochemie je novodobá metoda používaná v histologii, která na principu vazby antigen protilátka, může identifikovat jakoukoliv substanci s antigenními vlastnostmi v histologických řezech, např. rozliší subpopulace lymfocytů. Metoda se skládá ze tří základních fází:
- aplikace primární protilátky (vzniká imunokomplex),
- aplikace sekundární protilátky (vytvoření enzymatické aktivity vzniklých imunokomplexů)
- podání detekčního systému (barevné znázornění antigenu v řezu) [63].
Vlastní sestava
Pozorování SO probíhalo v období třiceti pěti let ve dvou časových obdobích. Tabulka 1 uvádí časové faktory vývoje a průběhu pěti pacientů se SO, formy celkové imunosuprese, komplikace a klinický nález na konci studie. Tabulka 2 rozebírá především NT v časových souvislostech, HLA typizaci a základní imunologické parametry buněčné imunity a podle možností v dané době u SO. Tabulka 3 uvádí hodnoty NT spolu s etiologií a léčbou u 16 poúrazových fakoantigenních uveitid.
Tab. 1. Časové faktory SO, celková imunosuprese, komplikace a klinický nález SO na konci studie 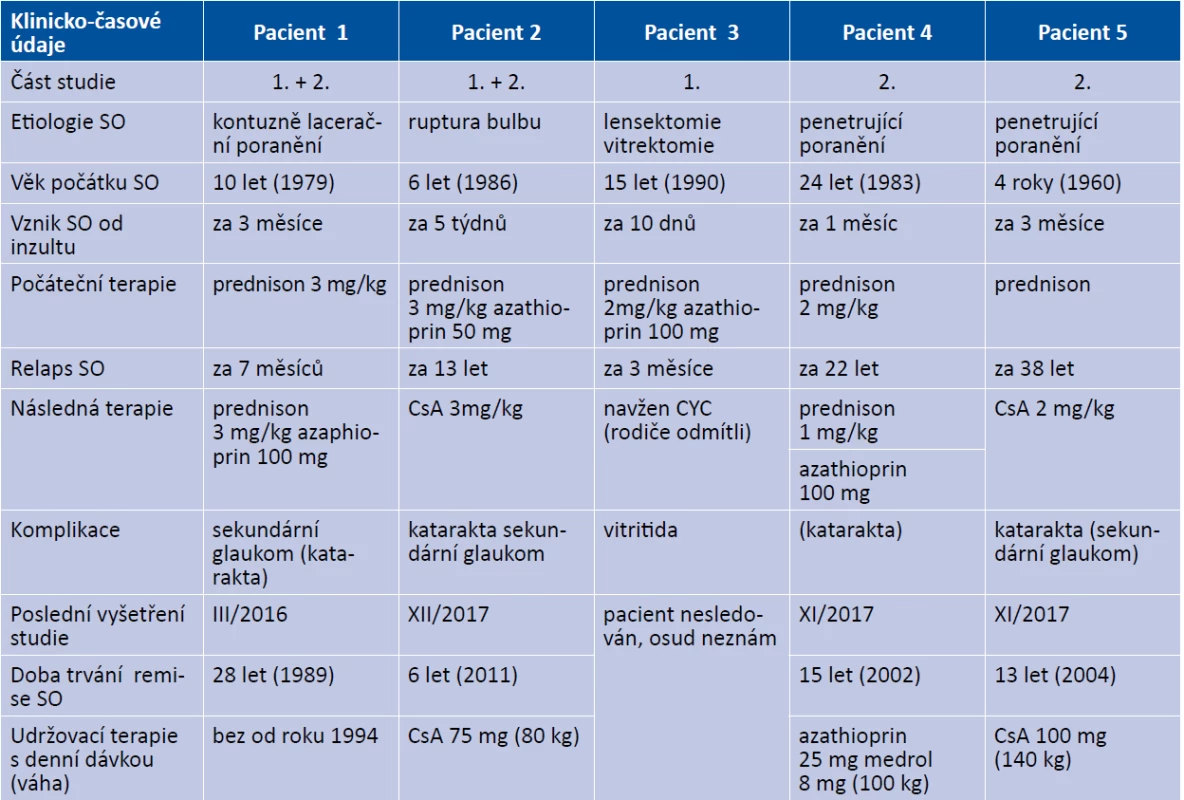
Tab. 2. Laboratorní hodnocení S.O.: NT v časových souvislostech, HLA typizace a základní imunologické parametry buněčné imunity 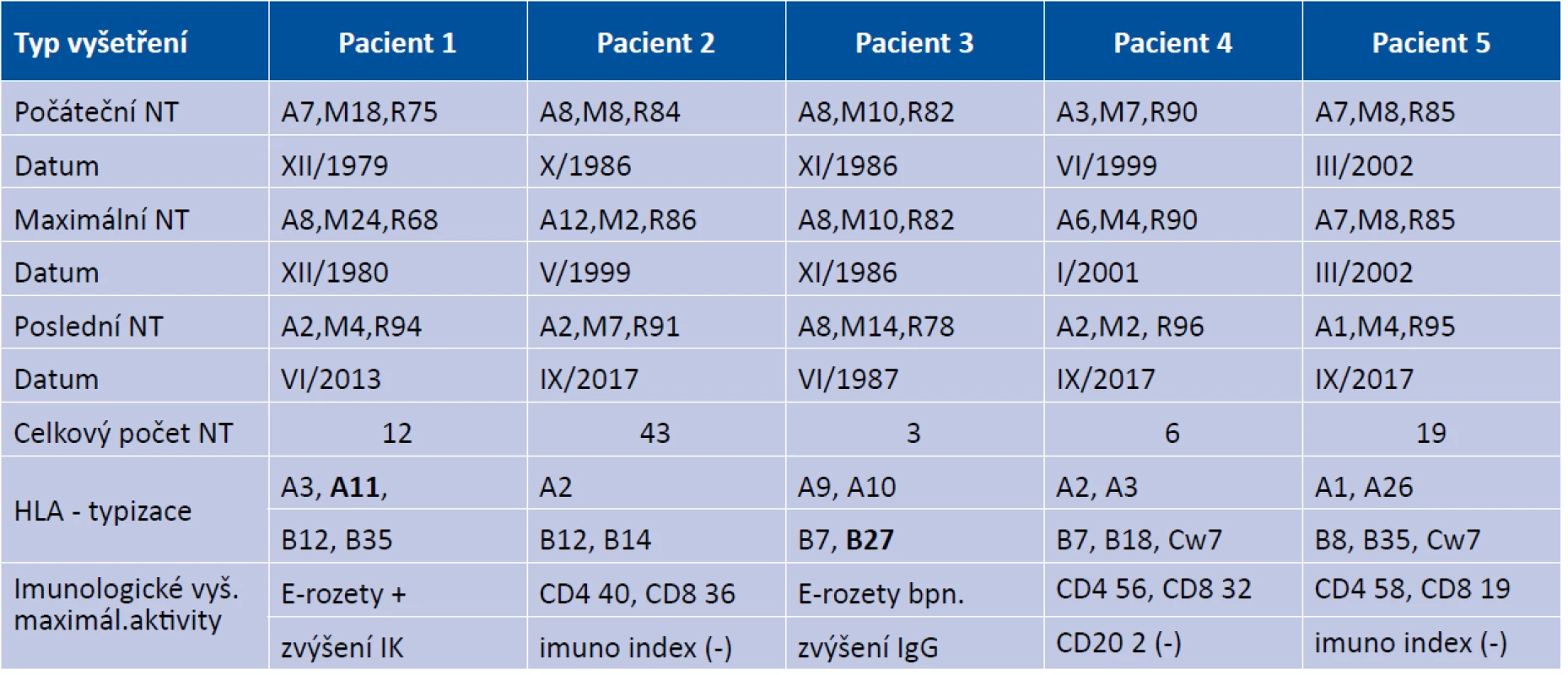
Tab. 3. Hodnoty NT, etiologie a léčba poúrazových uvetid 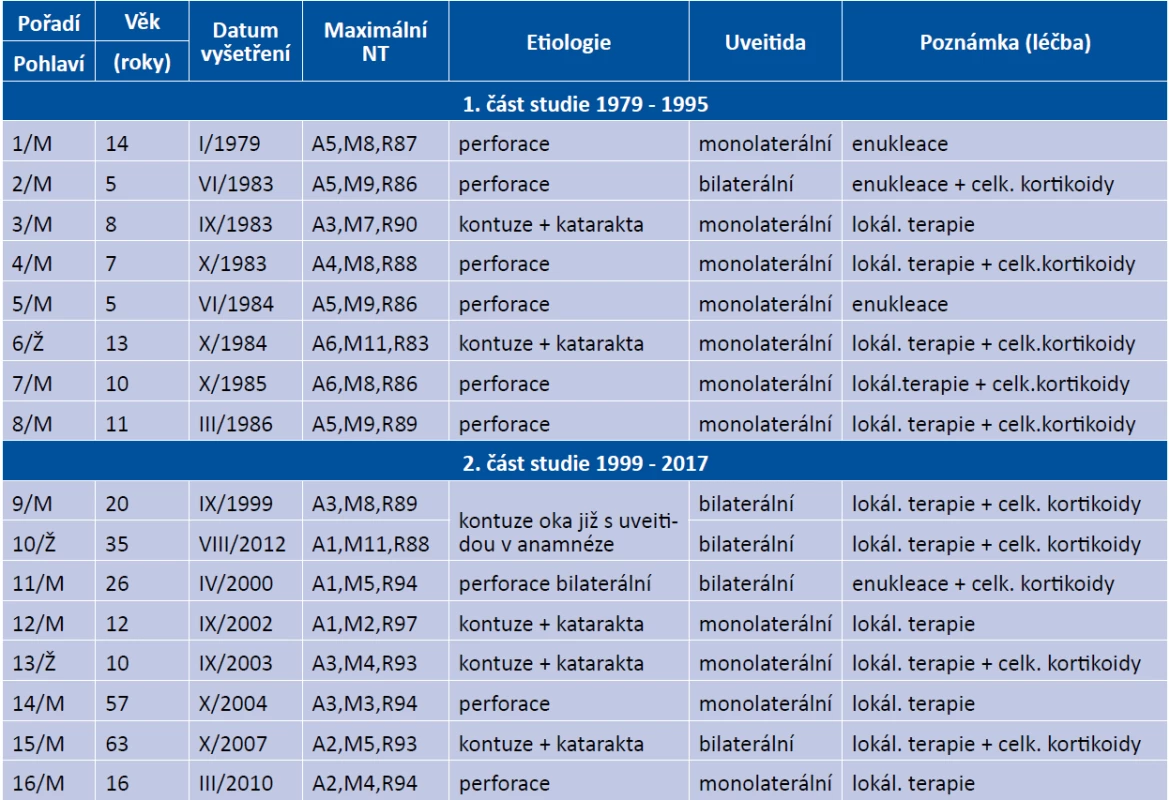
1. část studie byla součástí výzkumného projektu IGA 1152-3 (1992 –1994) [46] v letech 1979 – 1994, zahrnovala sledování a léčbu 3 chlapců s SO ve věku 6 – 15 let (Tabulka 1). Zároveň jsme provedli konsiliární vyšetření u další 16letého nemocného se SO. Laboratorní hodnoty jsme také srovnávali se skupinou 6 postižených (5 – 14 let, průměr 9,1 let) s posttraumatickými uveitidami nezánětlivé etiologie – fakoantigenními (fakoanafylaktickými) a jejich léčbou (Tabulka 3).
2. část studie probíhala od roku 1999 do 2017, kde se pozorování týkalo 2 nových dospělých pacientů s SO a 2 převzatých pacientů nyní dospělých z první části studie a s laboratorním hodnocením u 10 převážně dospělých pacientů (12 – 63 let, průměr 28,4 let) s poúrazovými uveitidami, ale také následně exacerbovanými uveitidami neúrazové etiologie u tří mladých žen, včetně léčebných postupů (Tabulka 3). Součástí bylo konsiliární vyšetření enukleovaného bulbu u 71leté ženy i po stránce imunohistochemické.
Hodnocení pěti nemocných se SO (Tabulka 1) probíhalo u čtyř chlapců a jednoho mladého muže (průměrný věk 12 let). Příčinou bylo perforující poranění či kontuzně-lacerační poranění, kdy SO vznikla v průměru 2 měsíce po inzultu, z toho důvodem enukleace sympatizovaného oka byl vznik zánětu na sympatizujícím oku u 3 z nich. Jen jednou SO se vyvinula na druhém oku až 1 týden po enukleaci slepého a iritovaného oka (pacient 2 a ázek 1BC). Příčinou vzniku SO 10 dnů po lensektomii s vitrektomií pro kongenitální kataraktu s perzistencí a. hyaloidea u chlapce s M. Down (pacient 3). U toto nemocného se objevil relaps choroby po počátečním zklidňování zánětu po již 3 měsících při snižující se imunosupresi. Navržené nasazení cyklofosfamidu (CYC) rodiče odmítli a přešli na jiné pracoviště. Další osud nemocného nám není znám.
Šestnáctiletého pacienta jsme jen konziliárně vyšetřili v listopadu 1986, byl bez imunosupresivní terapie. SO vlevo se vyvinula v šesti letech po korneo-sklerálním poranění vpravo. Histologická verifikace enukleovaného bulbu není dostupná. 3 roky po vzniku SO byla mimo území tehdejšího Československa provedena extrakce katarakty vlevo. 7 let po operaci katarakty byl levý bulbus hypotonický a zornice byla fixována k sekundární blanité kataraktě s fenestrem a sklivec byl zkalen (Obrázek 3A). Zraková ostrost (ZO) vlevo 1,5/50, do blízka Jaeger (J). č. 13 s afakickou korekcí. NT prokázal výraznou aktivitu: A11, M7, R82. Nasazen byl prednison 2 mg/kg a azathioprin 2x50 mg denně. ZO vlevo se stabilizovala na 2-3/50. Další osud nemocného neznáme.
Obr. 3. Klinický obraz předního segmentu sympatizovaného oka: 16letý konzultovaný pacient (A), pacient č. 3 (B), pacient č. 5 (D), pacient č. 6 (C) 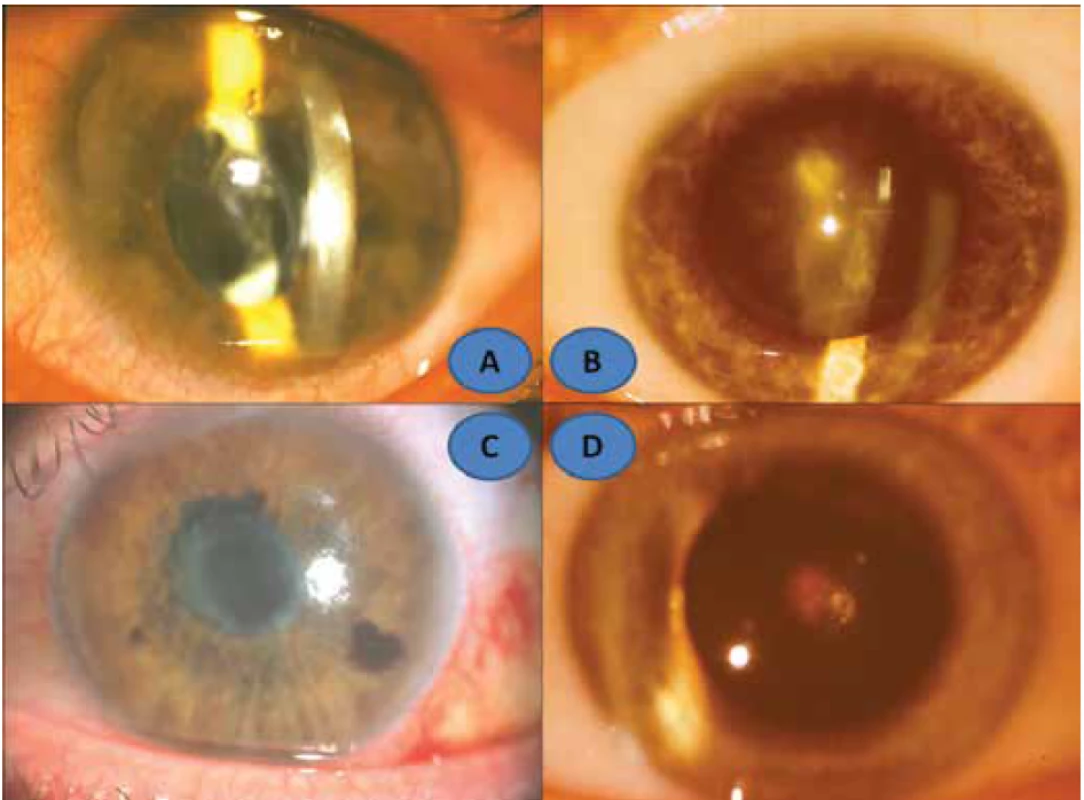
Relaps této autoimunitní choroby se po vysazení imunosuprese projevil ze sledované skupiny u tří z pěti nemocných v rozmezí několika měsíců až několika desítek let. Nejdelší období remise představovalo 38 let po vzniku SO u tehdy 4-letého chlapce, kdy enukleace byla provedena na jiném pracovišti v roce 1964 po projevu SO na druhém oku (verifikace SO byla provedena na našem pracovišti). U pacienta s Downovým syndromem při snižování nárazové dávky imunosuprese se projevil relaps SO vitritidou (Obrázek 3B) a u mladého může s projevem SO při udržovací dávce imunosuprese o 20 mg Prednisonu ob den. U toho pacienta 4 předcházelo dva roky zpět mírné zvýšení aktivity zánětu (náznak flare a ojedinělé buňky na endotelu v podobě Lüsseho linie), které bylo řešeno jen aplikací triamcinolonu 40 mg (Kenalog, Léčiva) parabulbárně. Komplikací u všech pacientů na sympatizovaném oku byla katarakta a třikrát sekundární glaukom. Komplikovaná katarakta se v počátku vyvíjela v podobě zadní subkapsulární voštinovité formy také v důsledku celkové kortikosteroidní terapie. V této podobě zůstala u pacienta 1 a 4 bez významného ovlivnění vidění. U dalších dvou nemocných katarakta postupně progredovala: pacient 2 a pacient 5 (Obrázek 3C). Muselo být přistoupeno k operačnímu řešení pro ZO vpravo 0,05, resp. 0,02. Rozvoj tak výrazného poklesu vidění bylo ovlivněno čekáním na naprosté klinické i laboratorní zklidnění SO, což umožnilo fakoemulsifikační techniku s implantací zadněkomorové nitrooční čočky (PC IOL) při peroperačním imunosupresním zajištění Solu-Medrolem a zvýšenou dávkou cyklosporinu A (CsA) v roce 2005, resp. 2003. Sekundární glaukom se projevil u 3 postižných. Konzervativní léčbou se podařilo jej normalizovat dvakrát (pacient 1 a 5). Jen u pacienta 2 nebyla tato léčba efektivní, a tak v roce 2011 byl kompenzován pomocí glaukomového implantátu Express 100 (Alcon), což následně umožnilo vysazení lokálních antiglaukomatik (Obrázek 1D). Nejdelší doba remise tří desítky let je u pacienta 1, který je dlouhodobě bez udržovací imunosuprese, na kontroly sám přestal docházet a zůstal jen telefonický kontakt. U dvou dalších sledovaných zůstala udržovací léčba o dávce CsA méně než 1mg denně. Jednalo se o jedince, kteří se podrobili operačnímu řešení komplikací. U obou se v pooperačním období přes zvýšenou dávku CsA se projevila přechodná aktivita na předním segmentu oka bez sklivcové reakce. U pacienta 4, který se v roce 2014 podrobil amputaci nohy pro poúrazovou flegmónu v roce 2014, jsme změnili před touto operací imunosupresi. Nahradili jsme prednison s azathioprinem za CsA. V pooperačním období se objevila přechodně jen Lüsseho linie buněk na endotelu rohovky bez flare v přední komoře, bez progrese katarakty (Obrázek 3D). Po necelém roce jsme se museli udržovací imunosupresi CsA pro jeho trvalou nesnášenlivost (nausea) zaměnit na původní léčbu.
Posuzovali jsme 16 fakoantigenních (fakoanafylaktických) převážně jednostranných uveitid (Tabulka 2) po perforačním poranění nebo méně často po kontuzích s rychle nastupující intumescentní kataraktou. Byla zde jasná převaha mužské populace v poměru 13 : 3 k ženám. Jen dvakrát byl odhalen oboustranný zánětlivý proces (pacient 2 a 15) po jednostranném perforačním poranění. Kontuze oka s nitroočním zánětem v anamnéze vyvolalo sekundární dráždění i na druhém dosud zdravém oku také dvakrát (pacient 9 a 10). Enukleace byla určována podle klinického stavu oka a jeho prognózy. Celková imunosuprese kortikoidy byla vždy indikována u oboustranných procesů, ale i u výrazných klinických projevů jednostranné nastupující uveitidy.
Dvě mladé ženy byly zařazeny s pauciartikulární formou juvenilní idiopatické artritidy (JIA) s ANA+ v předškolním věku, kdy oboustranná uveitida předcházela kloubní projevy. Kloubní i oční proces se postupně podařilo celkovou imunosupresivní terapií: prednison, později azathioprin i methotrexat (MTX) až k využití CsA a CYC stabilizovat. Později ve věku 16, resp. 23 let se projevil jednostranně sekundární glaukom, který přešel přes veškerou léčebnou snahu v dolorózní formu na slepnoucím bulbu. Tato změna vyvolala sekundární dráždění na druhém oku s již původní dlouhodobou remisí uveitidy v rámci JIA. Po enukleaci slepého oka ve věku 30, resp. 26 let druhostranné uveitické dráždění ustoupilo při stejné terapii jako před mutilujícím výkonem a vidění se stabilizovalo na ZO 0,5 – 0,66 s korekcí. Třetí pacientku jsme sledovali od šesti let (1998 – 2006) pro oboustrannou iridocyklitidu s vaskulitidou sítnice a s centrální neparazitární granulomatózní chorioretinitidou zasahující do oblasti zrakového nervu vlevo. Pro přetrvávající mírnou aktivitu uveitidy vpravo jsme prozatímně řešení komplikované katarakty nedoporučili a v lednu 2006 jsme převedli pacientku z prednisonu na CsA. Rodiče se rozhodli sami vyhledat léčebnou péči na jiném pracovišti, kde byla provedena lensektomie s vitrektomií vpravo. Ve věku 13 let zde opakovaně intravitreálně aplikovali bevacizumab (Avastin, Genentech). V květnu 2007 se vrátila pro oboustrannou exacerbaci panuveitidy bez celkové léčby do naší léčebné péče po jednoročním přerušení. Vpravo byla hypotonie a ZO světlocit s nepřesnou projekcí (Obrázek 4A). Vlevo byl v přední komoře flare se sekluzí zornice ke zkalené čočce a ZO 0,05 nat. (Obrázek 4B) Opětovně jsme zahájili imunosupresivní léčbu CsA s cílem stabilizovat zánět vlevo a zachránit pravé oko. V květnu 2008 jsme přistoupili k enukleaci pro trvalou zánětlivou aktivitu vpravo při mírném zánětlivém dráždění i vlevo. V říjnu 2010 následovala operace katarakty vlevo s implantací PC IOL, imusupresivní zajištění představovala kombinace Solu-Medrolu a CsA. Následné uvolnění sekluze a YAG kapsulotomii jsme zajistili v říjnu 2013 tacrolimem (Prograf, Astellas Pharma) za CsA. V listopadu 2017 byl zánět stále v remisi při udržovací terapii CsA 1mg/kg/den. ZO vlevo 0,15 s -3,0, ZO do blízka J.č. 6 nat. byla podmíněna změnami na očním pozadí (úroveň vstupního ZO z roku 1998).
Obr. 4. Klinický nález fakoantigenní uveitidy u 14leté dívky: vpravo (A),vlevo (B), histologický nález: fibrotizované řasnaté tělísko s gliózou amované sítnice, zvětšení 100x, HE (C), glióza sítnice a fibrotizace cévnatky, zvětšení 400x, HE (D) 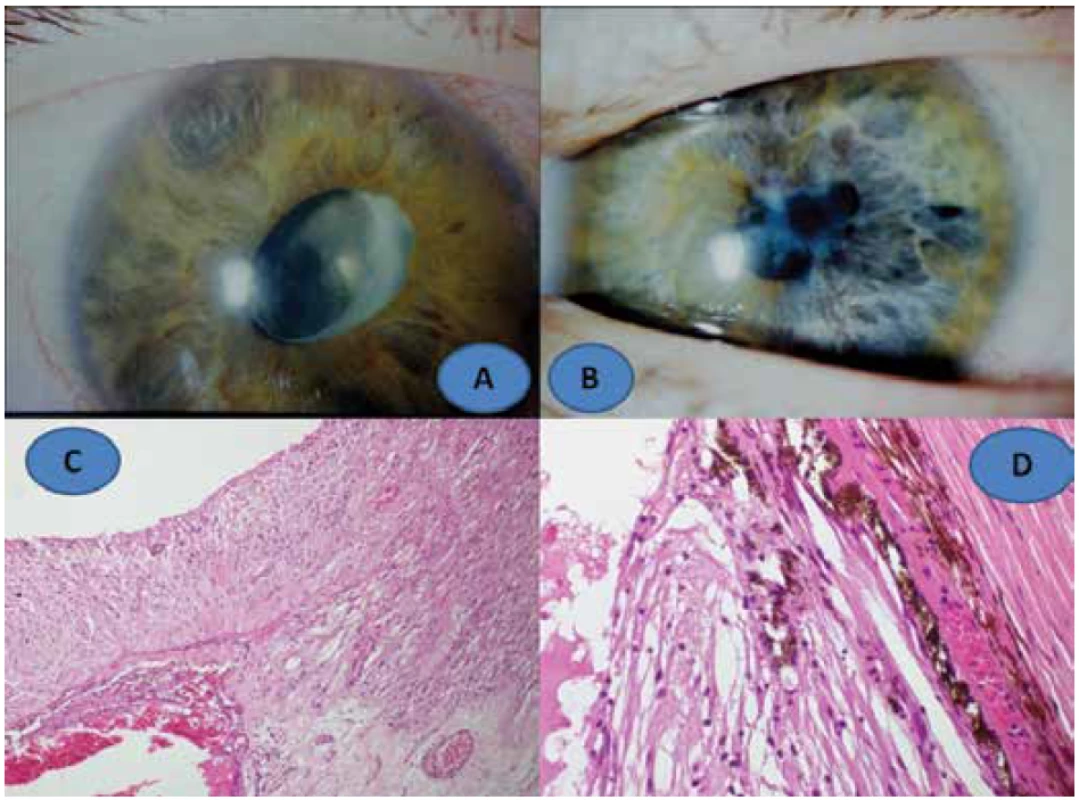
Výsledky
Celkově byl NT použit 87x u pacientů se SO a cca 60x u pacientů nesoucitné etiologie uveitid (byli zařazeni jen nemocní s nejméně 2x provedeným NT). Tabulka 2 uvádí výsledky NT u SO v počátku sledování, její nejvyšší hodnotu a poslední vyšetření v rámci studie. U všech 3 dětských pacientů při počátečním odhalení SO a u dospělého při relapsu bez imunopresivní léčby (pacient 5) byl vždy NT zvýšen. Zatímco u pacienta 4 v rámci udržovací imunosuprese byl v počátku test v normě, teprve relaps SO přes tuto mírnou imunosupresi vyvolal jeho patologické zvýšení. Nejvyšší maximální hodnoty NT se projevily při relapsu onemocnění u pacienta 2 a primárně u konzultovaného 16letého pacienta vždy bez celkové imunosuprese. Až v průběhu útočné celkové imusupresivní terapie hodnoty NT vždy postupně klesaly, jak prokázalo i poslední vyšetření u 4 z nich. Potvrdil to i přechodný pokles NT u pacienta 3 na hodnotu NT: A5, M16, R79 s jeho následným zvýšením při snaze o snížení imunosuprese. Hodnoty subpopulace T-lymfocytů CD4 v periferní krvi byly v době maximální aktivity NT snížené u dvou nemocných a zvýšené u dvou dalších pacientů (v rámci hodnocení E-rozet). Pouze jednou byl počet CD4 zvýšený a CD8 snížený (pacient 6). Sledování subpopulací lymfocytů či jejich analogie dané dobou vyšetření (imunoregulační index) v průběhu SO neprokázalo signifikantní hodnoty. Vyšetření humorální imunity a autoprotilátek bylo vždy negativní.
Ve všech případech nebyla u fakoantigenní (fakoanafylaktické) uveitidy odhalena patologická hodnota NT (Tabulka 3), kdy těsně pod hraničními hodnotami byl NT dvakrát (pacient 6 a 7). Uveitický proces byl vždy lokální i ev. celkovou léčbou kortikoidy definitivně utlumen na hodnoty NT v rozmezí: A2-3, M5-7, R91-94. Tato dynamika procesu svědčila pro minimální přítomnost lymfocytární aktivity u tohoto typu nitroočního zánětu. Minimální NT aktivita souvisela s imunosupresivní léčbou u dvou nemocných JIA uveitidou, která byla pod referenčními hodnotami, při terapii CsA a MTX byl NT: A1, M6, R93 a při kombinaci Medrolu s CYC vykázal NT: A0, M7, R93. Vliv imunosuprese prokázala i změna terapie u 14leté dívky po lensektomii s aplikací bevacizumabu – před a po nasazení CsA NT poklesl z A5, M5, R90 na A1, M7, R92 a při převodu udržovací léčebné dávky CsA na zajišťovací léčbu tacrolimem klesl NT z A2, M3, R95 na A0, M4, R96. Provedli jsme statistické hodnocení srovnávající maximální hodnoty NT v době nejvyšší klinické aktivity SO a akutních fakoantigenních uveitid (jen hodnoty pacientů bez jakékoliv imunosupresivní terapie). Dvojstupňový T-test prokázal signifikantní rozdíly u aktivních lymfocytů na statistické hladině významnosti (p = 0,0134), přestože nebylo možno pominout chybu malých čísel. Hodnocení lymfocytů s mikronukleoly (p = 0,5426) a prstenčitých inaktivních lymfocytů (p = 0,1333) nebylo statisticky významné.
Histologická verifikace sedmi enukleovaných bulbů, která nepotvrdila SO, byla zásadní u 14-leté pacientky po aplikaci bevacizumabu. Verifikovány byly především jizevnaté změny, a to atrofické a fibrotizované řasnaté tělísko a nepravidelně stočená odchlípená sítnice (Obrázek 4C) s gliózou a pozánětlivou atrofií a fibrotizací cévnatky (Obrázek 4D). U této uveitidy bylo vzhledem předcházejícímu typu operace možno předpokládat spoluúčast II. typu cytotoxického mechanismu přecitlivělosti. Tento obraz jizevnatých změn bez floridně probíhajícího granulomatózního zánětu byl odhalen v enukleovaných bulbech obou mladých žen s JIA uveitidou. Lze předpokládat, že se jednalo o III. imunokomplexový mechanismus přecitlivělosti charakteristický pro JIA, nikoliv o IV. typ přecitlivělosti.
Histologická verifikace konsiliárně vyšetřeného bulbu u 71leté ženy, kdy SO vznikla po vitrektomii provedená pro vitreoretinální proliferaci, potvrdila toto onemocnění. Sítnice s chronickým totálním odchlípením, zcela dezorganizovaná a těžce glioticky změněná. V navazujících subretinálních proliferacích a i v samotné uveální tkáni byly ložiskové zánětlivé infiltráty tvořené převážně lymfocyty a makrofágy (Obrázek 5A) s výrazně převažujícími T-lymfocyty (Obrázek 5B). Imunohistochemicky (Obrázek 5 dole) byly pozitivní subpopulace CD3, ale i CD4 s CD8. Minoritní část infiltrátu byla tvořena B-lymfocyty CD20. Poměrně hojná byla v infiltrátu účast makrofágů pozitivní na protilátky CD68, které ohraničily Fuchs-Dalenovy noduly.
Obr. 5. Histologický nález sympatické oftalmie (SO) – zbytnělá uvea s infiltrátem lymfocytů a makrofágů (A), zvětšení 100x, HE, detail lymfocytárního infiltrátu cévnatky (B), zvětšení 600x, HE. Dole imuno histochemická verifikace SO. Fuchs-Dalenův nodul ohraničený CD68, dále CD3 a CD20, zvětšení 400x 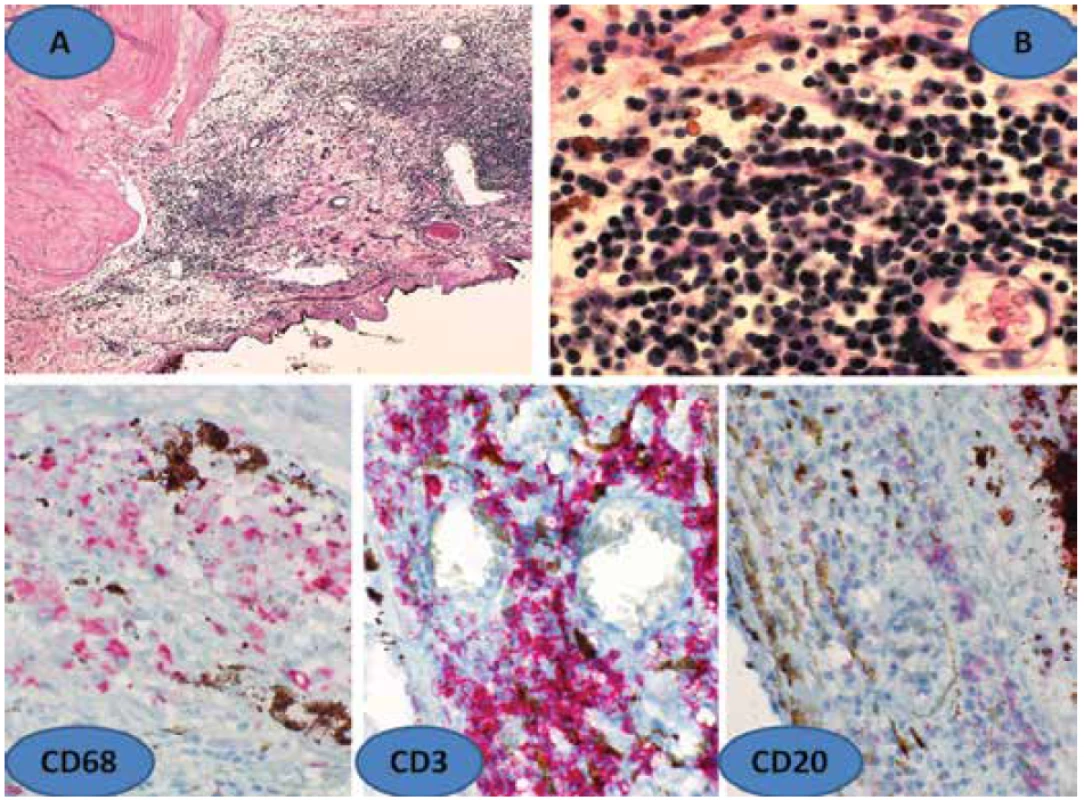
Závěr
NT upozorňuje na aktuální zvýšenou aktivaci lymfocytů bez rozdílu na zastoupení subpopulací a jejich absolutní počet v mechanismu uveitidy u IV. typu přecitlivělosti. Imunosupresivní terapie tuto aktivaci zásadně ovlivňuje poklesem hodnot, především u SO, ale i uveitid dalších typů přecitlivělosti. Imunohistochemické vyšetření prokazuje různé zastoupení jednotlivých typů lymfocytů podle stádia SO.
Diskuse
Nukleolární test byl zařazen do bodovacího systému hematologických vyšetření Všeobecné zdravotní pojišťovny pod kódem 91467 a stále je platný. Toto vyšetření se dříve využívalo u patologických stavů, kde se spolupodílí pozdní buněčná přecitlivělost. Reakce štěpu proti hostiteli po transplantaci kostní dřeně [30] a ve vztahu k rejekci ledvinových štěpů [44] byla provázena zvýšením počtu aktivovaných lymfocytů. Tato fakta byla důvodem našeho zařazení do škály laboratorních imunologických vyšetření u našich pacientů s SO. Jedná se o vyšetření spojené se jménem českého hematologa profesora K. Smetany, kdy v průběhu šedesátých a sedmdesátých let minulého století byla stanovena jeho přesná pravidla [67,68,71]. Chronická lymfocytární leukémie při pokročilých stádiích byla provázená vzestupem počtu aktivních nukleolů a následná chemoterapie jejich počet snížila [73], jak potvrzovala ultrastruktura nukleolů [70], což je paralelou poklesu aktivních lymfocytů u SO při imunosupresivní terapii našich nemocných i při udržovacích dávkách těchto léků, což bylo potvrzeno i u dalších léků [21]. Zvýšení počtu aktivních jadérek bylo prokázáno u systémového onemocnění pojivové tkáně [44] v souvislost kloubní aktivitou u JIA a revmatoidní artritidy u dospělých [77]. U našich nemocných, kdy byla uveitida spojena s JIA se při pouze oční symptomatologii zvýšená aktivita nukleolů v lymfocytech neprojevila i vzhledem k imunosupresi. Vzestup nukleolů v lymfocytech periferní krve byl prokázán u likvidátorů havárie jaderné elektrárny v Černobylu jako cytogenetický radiační efekt [32]. V současné době využití NT u autoimunitních chorob a nádorů krve je překonáno díky průtokovému cytometru rozpoznávající jednotlivé subpopulace lymfocytů v periferní krvi. Navíc proliferační markery Ki67 (MiB1) rozpoznají probíhající buněčný cyklus buněk ve fázi mitózy a přípravy na ni. Přesto NT může přinést nové poznatky, také v oblasti dalších uveitid.
Sympatická oftalmie v Československé oftalmologii se poprvé objevuje v rozmezí let 1927 – 1932, k autorům šesti článků lze přiřadit významné oftalmology: např. prof. Záboje Brucknera: Ophtalmia sympathica in luetico po perforovaném plazivém vředu [10] či prof. Václava Vejdovského: Sympathická ophtalmie po operaci šedého zákalu [80]. Po 2. světové válce byla snaha léčit SO pomocí penicilinu, která se v té době považovala za kauzální [19]. První imunosupresivní léčba toho onemocnění byla u nás popsána v roce 1958 pomocí adrenokortikotropního hormonu (ACTH) a prednisonu [38]. V případě 17-leté dívky proběhla léčba výše uvedenou imunosupresí a bez enukleace poraněného oka [39]. Studie čtyř pacientů řešila vždy stav poraněného oka při vyvolání SO enukleací. Autor zastával infekčně-alergickou teorii vzniku SO, proto byli pacienti celkově léčeni prednisonem a antibiotiky [57]. Relaps SO byl vyvolán snahou o uvolnění sekluze zornice korepraxí (pomocí fotokoagulační techniky) [35]. Včasná a účinná imunosupresivní terapie v kombinaci azathioprinu a prednisonu umožnila zachránit bulbus a provést rekonstrukční operaci u 17letého pacienta [74]. Poslední dosud publikovaná studie se už zabývá otázkou SO jako následek pars plana vitrektomie u dvou nemocných ze čtyř sledovaných, kdy bez enukleace byl léčebně zvolen prednison či v kombinaci s MTX či CsA [75].
Vzhledem k tomu, že od této poslední studie uplynulo 13 let a SO se stále těší velké pozornosti oftalmologů v současnosti (PubMed), zařadili jsme i literární rozbor.
Historický pohled na sympatickou oftalmii. Předpokládá se, že se o SO učilo již v době Hippocrata. První písemnou zprávu zaznamenal již 1000 let před naším letopočtem Konstatius Cephalis: „Postižené oko často předává své utrpení druhému“ [20]. Klinický obraz SO byl poprvé knižně popsán řecky v 16 století: „Po poranění pravého oka bylo následně postiženo těžce i levé oko“ [8]. Vlastní název soucitného onemocnění použil poprvé MacKenzie již v 19. století [52]. Na začátku 20. století byla vyslovena Puseyem domněnka o hypersenzitivním charakteru onemocnění [60]. O teorii vzniku SO se zajímali dva historicky známí oftalmologové; prof. Fuchs popsal nodulární infiltraci uveálního traktu [25] a prof. Elschnig za příčinu onemocnění považoval antigenní vlastnost uveálního pigmentu [22].
Etiologie sympatické oftalmie. Americká studie SO z let 1913 – 1978 o 105 pacientech, kde převládali muži v 67 %, byla podmíněna především jako pooperační komplikace tehdejších intrakapsulárních extrakcí katarakt v 28 %, přesto v etiologii celkově převládaly penetrující úrazy v 53 %, zároveň SO byla popsána i u těžkých kontuzí oka [51]. V novější indické studii z let přelomu 20. a 21. století bylo zastoupení mužů obdobné v 62 % ze 130 pacientů se SO a její etiologie byla ve ¾ poúrazová [78], což odpovídá pozorování z 80. let minulého století [13]. Souhrnný pohled na české a slovenské studie z let 1958 – 2017 uvádí 89 % mužů a 73 % úrazů z 19 sledovaných. Roční incidence SO na konci minulého století klesla na 0,03/100.000 obyvatel [41]. Nebezpečí vzniku SO po penetrujícím úrazu se pohybuje mezi 0,1 až 0,3 %, zatímco u oční chirurgie celkově je to pouze 0,02 % [56]. Na konci minulého století byla SO popsána po operacích katarakt ojediněle, a to v počátcích implantací nitroočních čoček [79]. Daleko závažnější riziko představují vitrektomie s incidencí od 0,06 % [28] do 0,97 % [32]; především to jsou v současnosti reoperace s četností 0,125 % [3] a u retinální chirurgie v 0,37 % [33]. Nejpočetnější a nejnovější soubor 175 nemocných s SO z Commonwelthu uvádí jen 16 případů SO po vitrektomiích (9 %), a to z celkového počtu 41.365 těchto operací, což znamená, že riziko je už pouze 0,038 % [80]. Po vitrektomiích byla SO zaznamenána i dvakrát u nás [75]. U výkonu bez porušení korneosklerálního obalu oka rovněž stále trvá nebezpečí vniku SO. Vznikla při YAG cykloterapii glaukomu [4,50], kdy incidence SO z 5,8 % v devadesátých letech 20. st. [49] poklesla na 0,03 až 0,17 % [4] v tomto století. SO může vzniknout také po brachyterapii melanomu [1,24] či protonové léčbě [8] a jeho resekci [29]. Navíc tento nádor může vznik SO svým růstem iniciovat [51,56]. Raritní bylo pozorování vzniku SO po aplikaci plomby u extraokulární operace sítnice [58]. SO vznikla po perforaci vředu rohovky, a to vyvolaného poleptáním [65], ale i po jiných podnětech [51]. Nově byla SO zaznamenána po anti-VEGF terapii, a to vlivem intravitreální aplikace bevacizumabu [9,66].
Časový faktor vzniku sympatické oftalmie. Závažnost SO spočívá ve faktu, že může vzniknout i řadu let po poranění oka [14,54,51]; literárně je udáváno rozmezí 5 dnů až 66 let [14]. Již dříve byly popsány ojedinělé případy SO (2 %) s potvrzenou histologickou verifikací projevující se již krátce po enukleaci [16,51]. Potvrdila to i pozdější studie v 5 až 7 % [14]. Tuto skutečnost jsme odhalili u jednoho nemocného. Nejčastějšími a inciálními příznaky SO je pokles vidění v 89 % spojený s bolestivostí v 29 % a zákaly ve sklivci v 24 % [78], dále ciliární injekce a fotofobie [76].
Laboratorní verifikace sympatické oftalmie. Onemocnění je uváděno jako bilateralní granulomatózní uveitida, charakterizovaná výrazným podílem T-lymfocytů v zánětlivém infiltrátu cévnatky spolu s makrofágy [14,63], která jsou pro histologickou diagnózu rozhodující. Odpovídá to teorii IV. typu přecitlivělosti, kdy SO sloužila jako její model v 80. letech 20. století [34]. Imunohistochemické studie v dalších letech odhalily nové skutečnosti, neboť D-F noduly obsahují T-lymfocyty, hlavně CD4 (helpery) a CD8 (supresory či cytotoxické buňky) v poměru 3 : 1 až 4 : 1 (později se poměr obrací). NK buňky jsou difúzně v celé cévnatce. Přítomno je také malé množství B-lymfocytů již v akutní fázi [11,14]. Navíc byly odhaleny B-lymfocyty ve zvýšeném počtu v D-F nodulech u dvou ze čtyř enukleovaných bulbech [5]. Později bylo odhaleno, že počet makrofágů a B-lymfocytů může být vyšší než T-lymfocytů v rozdílných fázích SO [6] ve finální fázi SO, kdy B-lymfocyty reaktivují T-lymfocyty [17]. Podrobnější detekce ukázala, že v první fázi SO jsou obsahem granulomu D-F nodulů M1 makrofágy (CD68, CD 163) než jiné T-lymfocyty. PCR (polymerázová řetězová reakce) metodikou byly detekovány pouze v nodulech specifické cytokiny (IL-7, IL18, IL-20, CCL19 a CXL11) [27]. Vzhledem k pozitivitě NT u krevních nádorů s významným zastoupením B-lymfocytům [73] vyplývá, že pro aktivitu NT u SO není rozhodující, zda se jedná o T - či B - lymfocyty a jejich absolutní hodnoty, ale zásadní je celková biologická aktivita všech lymfocytů. Rozbor informací v několika desetiletích na informačním portále PubMed, ani několik zásadních studií o SO ve svých závěrech a podrobných diskusích v posledních letech [3,16,17] nepřinesly informace o možnosti monitorování SO při hodnocení subpopulací lymfocytů v periferní krvi. Hladiny T-lymfocytů jsou popisovány jako proměnlivé [23,56] či pokles subpopulace CD4 a z toho vyplývající změnu v imunoregulačním indexu [54]. Potvrdil to jeho pokles při vyšetření u dvou našich pacientů. V periferní krvi byl prokázán pokles T-lymfocytů v korelaci s jejich zvýšením v uveální tkáni [37]. Všechna tato vyšetření hladin lymfocytů v periferní krvi nemají dynamický charakter, protože SO nemá systémové projevy. V obraze SD-OCT se D-F noduly projeví hyperreflexní lézí v RPE s narušením přechodu vnitřních a zevních vrstev vláken [53].
Patogeneze soucitného onemocnění. Také se uvažuje, že se v etiologii vzniku onemocnění uplatňuje histokompatibilní kód postižených. Byla zjištěna vyšší incidence antigenu A11 [14,62], který jsme potvrdili u jednoho nemocného. Také antigen B27 může mít určitý význam [62], potvrzený u dalšího našeho pacienta. Z dalších predisponujících antigenů jsou to B40 a DR4/ DRw53 či DQw3 [14], později byly u bělošské populace stanoveny další antigeny HLA-DRB1 a DRQA1 [42]. Při hledání etiologické příčiny SO byl odhalen přímý vztah s Vogt-Koynagi-Haradovou (VHK) chorobou charakterizované uveo-meningoencefalitidou a uveo-kutánním syndromem. Obě onemocnění provází podobná oboustranná granulomatózní uvetida s extenzivní infiltrací cévnatky, podmíněné T-lymfocytární reakcí na uveálně retinální antigen [60], charakterizované jako autoimunitní onemocnění s imunologickou dysregulací [2] a společnými některé HLA antigeny, a to DR4 a DRW53 [12]. VKH choroba se v počátcích projevuje poklesem T-lymfocytů, především subpopulací CD4, ale i CD8 [49], což jsme potvrdili poklesem celkových T-lymfocytů u dvou chlapců [48]. V pozdějších stadiích onemocnění dochází k vyrovnání T-lymfocytů až k jejich vzestupu [12,48,49]. Z toho vyplývá, že sledování hladin T-lymfocytů v periferní krvi u VHK choroby umožňuje její monitorování, na rozdíl od SO. Exaktní experimentální model SO ještě neexistuje, ale u opic se podařilo vyvolat uveitidu s D-F noduly antigeny IRBP a S-A [54]. Nové experimentální autoimunitní uveitidy na zvířecích modelech prokázaly vliv cytokinové dysregulace a mitochondriálního oxidativního stresu. Právě u SO se uvažuje o vlivu fotoreceptorového mitochondiálního poškození [55], uvažuje se zde i o vlivu TNF - alfa, vedoucí k apoptóze fotoreceptorů [17]. Přepokládá se autoimunitní reakce proti původně sekvestrovanému retinálnímu antigenu (S-Ag) nebo inter-fotoreceptorovému retinoid-binding proteinu (IRDP) či rhodopsinu [16]. Byla hodnocena i celulární imunita, např. blastická aktivita nebo lymfocytární transformace [23]. Novou strategii léčby by mohla přestavovat syntetická příprava microRNA. Identifikace změny hladiny microRNA při její expresi profiluje možnost nového pohledu na patogenezi SO, protože u této choroby bylo odhaleno několik specifických microRNA, které je použito jako regulační medium aktivace lymfocytů Obě metodiky, a to americká [36] a česká [67,68,71] se věnují změnám aktivace lymfocytů. Americká metodika studie využívá molekulárně genetickou analýzu založenou na PCR [36], zatímco česká metodika prof. Smetany [67,68,71] je práce morfologická za pomocí mikroskopických laboratorních vyšetření. Souvisí spolu nepřímo, ale existuje určitá korelace. Jedná se o ověření stavu transkripce RNA v jádrech lymfocytů ovlivňující jejich biologickou aktivitu.
Terapie sympatické oftalmie. Při léčbě SO, ať už s enukleací sympatizujícího oka či bez něj, se uplatňuje celková imunosupresivní terapie, která je ze všech uveitid ekonomicky nejnáročnější [45]. Kromě kortikosteroidů ve vysokých dávkách, které stále tvoří základ terapie [14,23,54,56,75], jsme uplatňovali hlavně v počátku. Později byla zařazena další imunosupresiva a cytostatika: azathioprin, CYC, MTX, merkaptopurin [14,23] či vysoko dávkovaný chlorambucil [59], a to v kombinaci s mycophenolatem u refrakterních SO [17]. Především se využívá CsA [14,56], s kterým jsme sami nejčastěji léčili SO v posledním desetiletí. Nově se objevila možnost terapie SO pomocí biologické léčby adalimumabem s cílem ovlivnit cytokinové mechanismy a TNF (tumor necrosis faktor) [40] i jako doplňující terapii u její refraktorní formy [30]. Doplnění systémové terapie SO je intravitrealní aplikace afliberceptu k odstranění choriodální neovaskulární membrány [64] a dexamethazonu k útlumu cystoidního edému [81]. Stále platí, že jedinou prevencí SO druhého oka je včasná enukleace iritovaného slepého poraněného bulbu, ale zde není jednotný názor [3,13]. Velké studie uvádí enukleace u SO, a to ve 100 % (n = 105) [51], resp. v 28 % (n = 130) [78]. České a slovenské studie uvádí souhrnně enukleaci v 68 %. Po očních úrazech je eviscerace bulbu doporučena před enukleacemi jen v případech s nízkým rizikem SO [3,82], neboť hrozbou je nedostatečné odstranění uveální tkáně zůstávající v emisariích [3]. Pozdější enukleace po aktivaci SO nemá na její průběh vliv [14,56].
Diferenciální diagnóza sympatické oftalmie. V našem regionu je nutno uvažovat především o fakoantigenní uveitidě, která představuje soubor onemocnění s rozdílnými klinickými příznaky, patologickými mechanismy a histologickými verifikacemi [18,76]. Proto se rozlišovalo několik typů uveitid vyvolaných čočkovými hmotami [54]: fakotoxická negranulomatózní přední uveitida, granulomatózní uveitida vyvolaná čočkovými hmotami, nespecifická infiltrace s makrofágovou reakcí na čočkové hmoty, fakoanafylaktická endoftalmitida neinfekční etiologie. V literatuře se také vžil termín fakoanafylaktická uveitida [12]. Důvodem tohoto diferenciálně diagnostického pohledu je mechanismus vzniku (úraz a pooperační stav) a podobnost počátečních klinických stadií onemocnění. U SO se jedná převážně o T-lymfocytární reakci ve všech částech uveální tkáně v rámci oddálené buněčné přecitlivělosti, zatímco u fakoantigenní uveitidy se jedná o reakci na čočkový antigen v rámci cytotoxické či imunokomplexové hypersensitivity [18,54] za účasti účasti Arthusovy reakce B-lymfocyty [12]. Přesto nejvýznamnější vliv v mechanismu fakoantigenní (fakoanafylaktické) uveitidy mají makrofágy [18]. Zánětlivá granulomatózní reakce je soustředěna převážně okolo poškozené čočky [16]. Absolutní odlišení SO od fakoantigenní uveitidy umožňuje pouze přesná histologická verifikace (u slepých bulbů), tak jak byla provedena u našich nemocných. Několikrát jsme zaznamenali oboustranné uveální dráždění po jednostranných úrazech, což by mohlo odpovídat cytotoxické či imunokomplexové přecitlivělosti.
Prognóza sympatické oftalmie. SO je velice závažné onemocnění očí se špatnou prognózou vidění, pro které má zásadní vliv včasná diagnóza a dostatečná terapie [14]. Pro dobrou prognózu vidění sympatizovaného oka se považovala včasná enukleace sympatizujícího oka [51], což stále platí pro slepé a dlouhodobě iritované oči. Relaps onemocnění je velice pravděpodobný, přestože řada pacientů bez příznaků tohoto zánětu bývá řadu let [14]. Sami jsme zaznamenali relaps SO, který následoval až po 38 letech klidového stavu. V kontrastu dalšího pacienta byla trvalá remise onemocnění na konci studie 32 let. Vidění mohou zásadně ovlivňovat komplikace: katarakta, glaukom a edém makuly. Pro zachování remise SO je nutná dlouhodobá imunosupresivní terapie [14]. U všech tří dosud námi sledovaných nemocných s SO stále ponecháváme udržovací dávky imunosupresiv.
Předneseno na 52. sjezdu Čs. oftalmol. společnosti v Ústí/Labem v červnu 1989, na Slovensko-českých hematologických dnech laboratornej hematologie a transfuziologie v Trenčanských Teplicích v září 2001, na 17. sjezdu České oftalmol. společnosti v Praze v říjnu 2009, na 19. Vejdovském olomouckém dni v březnu 2018, na 58th Annual Meeting of EOPS – Glasgow, květen 2018 a následně na 14. sympoziu Detskej oftalmológie v Bratislavě v květnu 2019
Věnováno památce prof. MUDr. H. Lomíčkové, DrSc. ke stoletému výročí jejího narození, spoluzakladatelce moderní české pedooftalmologie.
Děkujeme za histologickou verifikaci soucitného onemocnění in memoriam významným očním patologům: as. MUDr. F. Kloučkovi, CSc. (pacient 1 a 2), prof. MUDr. J. Stejskalovi, DrSc. a spolupracovníkům (pacient 4 a verifikace nesoucitných pacientů 1. studie) a prof. MUDr. F. Vrabcovi, DrSc. (pacient 5 a 6). Dále děkujeme MUDr. J. Pražákovi, CSc. z ÚHKT (Ústav hematologie a krevní transfuze v Praze) za stanovení HLA typizace
První část studie byla podpořena projektem IGA 1152-3
Autoři práce prohlašují, že vznik a téma odborného sdělení a jeho zveřejnění není ve střetu zájmů a není podpořeno žádnou farmaceutickou firmou.
Do redakce doručeno dne: 5. 9. 2019
Do tisku přijato dne: 30. 10. 2019
MUDr. Jan Krásný
Oční klinika FNKV
Šrobárova 50
100 34 Praha 10
Zdroje
1. Ahmad N., Salvi S., Rudle PA. et al.: Sympahtetic ophthalmia after ruthenium plaque brachytherapy. Br J Ophtalmol, 91; 2007 : 399–401.
2. Al-Halafi A., Dhibi HA., Hamade IH. et al.: The association of systematic disorders with Vogt-Koyanagi-Harada and sympathetic ophthalmia. Graefes Arch Clin Exp Ophthalmol, 249; 2011 : 1229–1233.
3. Arevalo JF., Garcia RA., Al-Dhibi HA. et al.: Update on sympathetic ophthalmia Middle East Afr J. Ophthalmol, 19; 2012 : 13–21.
4. Aujla JS., Lee GA., Vincent, SJ. et al.: Incidence of hypotony and sympathetic ophthalmia following transscleral cyclophotocoagulation for glaucoma and a report of risk factors. Clin Experiment Ophthalmol, 41; 2013 : 761–772.
5. Auw-Haedrich C., Loeffler KU., Witschel H.: Sympathetic ophthalmia: an immunohistochemistry study of four cases. Ger J Ophthalmol, 5; 1996 : 98–103.
6. Aziz HA., Flynn HW., Young RC. et al.: Sympathetic ophthalmia: clinicopathologic correlation in a consecutive case series. Retina, 35, 2015 : 1696–1703.
7. Bartisch G.: ОFTALMOLOGIA (Augendienst). Stockel, Dressden, 1583, p. 205.
8. Brour J., Desjardins L., Lehoang P. et al.: Sympathetic ophthalmia after proton beam irradiation for choriodal melanoma. Ocul Immunol Inflamm, 20; 2012 : 273–6.
9. Brouzas D., Koutsandrea C., Moschos M. et al.: Massive choriodal hemorrhagae after intravitreal administration of bevacizumab (Avastin) for AMD followed by controlateral symphatetic ophthalmia. Clin Ophthalmol, 3; 2009 : 457–9.
10. Bruckner Z.: Ophtalmia sympathica in luetico po perforovaném plazivém vředu. Oftalmologický Sborník, 2; 1928 : 393 – 424.
11. Chan CC., Beneza D., Rodrigues MM. et al.: Immunohistochemistry and elektron microscopy of chorioidal infiltrates and Dalen-Fuchs nodules in sympathetic ophthalmia. Ophthalmology. 92; 1985 : 580–590.
12. Chan CC.: Relationships between sympathetic ophtalmia, phacoanaphylactic endophtalmitis and Vogt-Koyanagi-Harada disease. Ophthalmology, 95; l988 : 619 –624.
13. Chan CC., Roberge RG., Whitcup SP. et al.: 32 Case of sympathetic ophthalmia. A retrospective study at the National Eye Institute, Bethesda, Md., from 1982 to 1992. Arch Ophtalmol, 113; 1995 : 597–600.
14. Chan CC., Roberge FG.: Sympathetic Ophthalmia. In Pepose JS, Holland GJ, Wilhelmus KR.: Ocular Infection & Immunity, Mosby, New York, 1996, pp. 723–733. 15.Chang GC., Young LH.: Sympathetic ophtalmia. Semin Ophtalmol, 26; 2011 : 316–320.
16. Chen S., Aronow ME., Wang C. et al.: Classical pathology of sympathetic ophthalmia presented in a unique case. Open Ophthamol, 8; 2014 : 32–38.
17. Chu XK., Chan CC.: Sympathetic ophthalmia: to the twenty-first century and beyond. J Ophthalmol Inflamm Infect, 3; 2013 : 49–56.
18. Cousin CW., Kraus-Mackiw E.: Lens-associated uveitis. In Pepose JS, Holland GJ, Wilhelmus KR: Ocular Infection & Immunity, Mosby, New York, 1996, pp. 507–528.
19. Dienstbier E.: Konečná zpráva o výsledku léčby sympatické oftalmie penicilinem. Cs Oftal, 4; 1948 : 408–411.
20. Duke-Elder S (ed.): Text Book of Ophthalmology, Vol. IX. Disease of the uveal tract., Mosby, St.Louis, 1954, pp. 558–593.
21. Eckschlager T., Kasal P., Smetana K.: Některé možnosti využití nukleolárního testu v klinické diagnostice. Prakt Lek, 60; l980 : 667–68.
22. Elschnig A.: Die antigena Wirkung des Augenpigmentes. Albrecht von Graefes Arch Ophthalmol, 76; 1910 : 509.
23. Friedlaender MH.: Alergy and Immunology of the Eye, Raven Press, NewYork, 1993, pp. 206–212.
24. Fries PD., Char DH., Craford JB., et al.: Sympathetic ophthalmia complicating helium ion irradiation of a choriodal melanoma. Arch Ophthalmol, l05; l987 : 1561–64.
25. Fuchs E.: Über sympathisierende Entzündung zuerst bermerkungeen über seröse traumatische Iritis. Albrecht von Graefes Arch Ophthalmol, 61; 1905 : 365.
26. Fučíková T.: Imunologie. Vnitřní lékařství, Sv.V. Galén, Praha, 2002, 58 s.
27. Furusato E, Shen DF, Cao X, et al.: Inflammatory Cytokine and Chemokine Expression in Sympathetic Ophthalmia. Histol Histpatol, 26; 2011 : 1145 51.
28. Gass J.: Sympathetic ophthalmia after vitrectomy. Am J Ophthal, 93; l982 : 552–58.
29. Garcia-Arumi J., Montolio GM., Morral M. et al.: Sympathetic ophthalmia after surgical resection of iridociliary melanoma. Graefes Arch Clin Exp Ophthalmol, 244; 2006 : 1353–1356.
30. Hiyama T., Harada Y., Kiuchi Y.: Effective treatment of refractory sympathetic ophthalmia with glaucoma using adalimumab. Am J Ophthalmol Case Rep, 14; 2019 : 1–4.
31. Hrabánek J., Lukášová M., Smetana K.: Monitorování aktivních lymfocytů v periferní krvi pacientů po transplantaci kostní dřeně. Cas Lek Ces, 133; 1994 : 80–2.
32. Ibragimova NV., Tugolukova LV., Kravtsov V. et al.: The number of nucleoli in peripheral blood lymphocytes of the Chernobyl accident liquidator. Tsitologia, 43; 2001 : 941 43.
33. Inouye S., Ideta H., Ishikova H., et al.: Sympathetic ophthalmia following vitrectomy and /or retinal detachment surgery. Acta Soc Ophthalmol, 92; l988 : 372–376.
34. Jakobiec FA., Lefkowitch J., Knowles II. DM.: B - and T-lymphocytes in ocular diseases. Ophthalmology, 91; 1984 : 635 654.
35. John J., Iserle J.: Korepraxe fotokoagulací a sympatická oftalmie. Cesk Slov Oftalmol, 33; 1977 : 377–82.
36. Kaneko Y., Wu GS., Saraswathy S. et al.: Immunopathologic processes in sympathetic ophthalmia as signified by microRNA profiling. Invest Ophthalmol Vis, Sci, 53; 2012 : 4197–204.
37. Kaplan H., Waldrep JC., Chan WC. et al.: Human sympathetic ophthalmia immunologic analysis of the vitreous et uvea. Arch Ophthalmol, 104; l986 : 240–4.
38 Karel I., Krejčí L.: Naše dosavadní zkušenosti při léčbě sympatické oftalmie. Cesk Slov Oftalmol, 14; 1958 : 468–471.
39. Kavka J.: K prevenci a léčbě soucitného onemocnění. Cesk Slov Oftalmol, 23; 1967 : 212–4.
40. Kim JB., Jeroudi A., Angels-Han ST. et al.: Adalimumab for pediatric sympathetic ophthalmia. JAMA Ophthalmol, 132; 2014 : 1022–24.
41. Kilmartin DJ., Dick AD., Forrester JV.: Prospective surveillance of sympathetic ophthalmia in the UK and republic of Ireland. Brit J Ophthalmol, 84; 2000 : 259–263.
42. Klimartin DJ., Wilson D., Liversidge J. et al.: Immunogenetics and clinical phenotype of sympathetic ophthalmia in British and Irish patients. Br J Ophthalmol, 85; 2001 : 281–286.
43. Korčáková L., Reneltová J., Hašková V.: Možnost diagnostiky při transplantaci ledvin podle morfologie nukleolů cirkulujících lymfocytů, Cas Lek Ces, 114; 1975 : 616–618.
44. Korčáková L., Pekárek J., Rovenský J. et al.: Lymphocyte nucleolar activation as a marker of autoimmune disorders. Immunology 31; 1976 : 803–805.
45. Krásná J., Mezerová V., Krásný J.: Hodnocení efektivnosti léčby neinfekčních uveitid. Cesk Slov Oftalmol, 69; 2013 : 110–116.
46. Krásný J.: Závěrečná zpráva IGA 1152-3: Komplexní hodnocení péče o děti s imunopatologickým onemocněním oka, 1992–1994.
47. Krásný J.: Uvea. In Kolín J, a kol.: Oftalmologie praktického lékaře. Karolinum, Praha, 1994, s. 9–111.
48. Krásný J., Honzová S.: Vogt-Koyanagi-Harada syndrom u dětí. Cesk Slov Oftalmol, 51; 1995 : 156–165.
49. Kyoichi O., Shinji K., Keiji O. et al.: Surface markers of periferal blood lymphocytes in Vogt-Koyanagi-Harada diseases. J Clin Lab Immunol, 17, 1985 : 49–52.
50. Lam S., Tessler HH., Lam BL. et al.: High incidence of sympathetic ophthalmia after contakt and noncontact neodymiumYAG-cyclotherapy. Ophthalmology, 99; l992 : 1818–2.
51. Lubin JR., Albert DM., Weinstein M.: Sixty-five years of sympathetic ophthalmia. A clinicopathologic review of 105 cases 1913-1978. Ophthalmology, 87; l980 : 109–121.
52. MacKenzie W.: A practical treatment on the diseases of the eye. 3rd ed. Longman, London, 1840: pp. 523–534.
53. Muakkassa NW., Witkin AJ.: Spectral-domain optical coherence tomography of sympathetic ophthalmia with Dalen-Fuchs nodules. Ophthal Surg Lasers Imaging Retina. 45; 2014 : 610–612.
54. Müller-Hermelink HK., Kraus W.: Recent topic in the pathology of uveitis. In Kraus-Mackiw E, O´Connor GR: Uveitis, Pathophysiology and Therapy, Thieme-Stratton Inc., New York, l986, pp. 155–203.
55. Nguyen AM., Rao NA.: Oxidative photoreceptor cell damage in autoimmune uveitis. J Ophthalmol Inflamm Infect, 1; 2011 : 7–13.
56. Nussenblatt RB., Palestine AG.: Uveitis, Fundamentals and Clinical Practice, YBMP, New York, l989, pp. 257 273.
57. Oláh Z.: Príspevok k patologii sympatickej oftalmie. Cesk Slov Oftalmol, 23; 1967 : 35–40.
58. Parvaresh MM., Falavarjani KG.: Presumed sympathetic ophthalmia after scleral bucking surgery. Retin Cases Brief Rep, 4; 2013 : 331–333.
59. Patel SS., Dodds EM., Echandi LV. et al.: Long-term, drug-free remission of sympathetic ophthalmia with high-dose, short-term chlorambucil therapy. Ophthalmology, 121; 2014 : 596–602.
60. Pusey B.: Cytotoxin and sympathetic ophthalmia. Arch Ophthalmol, 32; 1903: p. 334.
61. Rao NA.: Mechanisms of imflammatory response in sympathetic ophthalmia and VKH syndrome. Eye, 11; 1997 : 213–216.
62. Reynard M., Shulman IA., Azen, SP. et al.: Histocompatibility antigens in sympathetic ophthalmia. Am J Ophthalmol, 95; l983 : 216–221.
63. Roberts F., Chee KT.: Lee´s Ophtalmic Histopathology, 3th ed., Springer-Verlang, London, 2014, 466 pp.
64. Saatci AO., Ayhan Z., Ipek SC. et al.: Intravitreal Aflibercept as an adjunct to systemic therapy in a case chorioidel neovascular membrane associated with sympathetic ophthalmia. Turk J Ophthalmol, 48; 2018 : 208–11.
65. Shen J., Fang W., Jin XH. et al.: Sympathetic ophthalmia caused by a severe ocular chemical burn: a case report and literature review. Int J Clin Exp Med, 8; 2015 : 2974–8.
66. Sisk RA., Davis JL., Dubovy SROV., et al.: Symphatetic ophthalmia following vitrectomy for endophtalmitis after intravitreal bevacizumab. Ocul Immunol Inflamm, 16; 2008 : 236–238.
67. Smetana K.: Poznámky k vyšetřovaní nukleolů v lymfocytech. Imunol Zpravodaj, 7; l976 : 399–419.
68. Smetana K.: A futher contribution on the question of the incidence of nucleoli in the nuclei of mature lymphocytes in man. Folia Biol (Praha), 7; 1961 : 268–274.
69. Smetana K., Freireich, EJ., Busch H.: Chromatin structures in ring-shaped nucleoli of human lymphocytes. Exptl Cell Res, 52; 1968 : 112-128.
70. Smetana K., Gyorkey F., Gyorkey P. et al.: Comparative studies on the ultrastructure of nucleoli in human lymphosarcoma cells and leukemic lymphocytes. Cancer Research, 30; 1970 : 1149–55.
71. Smetana K., Lejnar J., Potměšil M.: A futher contribution to the demonstration of RNA and nucleoli of blood cells in smear preparations. Folia Haemat, 91; 1969 : 4–9.
72. Smetana K., Lejnar J., Sálková J.: Studies on nucleoli in rossetting T and B lymphocytes of the human peripheral blood. Folia Haematol Int Klin Morphol Blutforsch, 107; 1980 : 720–7.
73. Smetana K., Rosa L., Šubrtová H. et al.: Futher studies on satellite nucleoli of lymphocytes in patients suffering from B chronic lymphatic leukaemia. Int J Tissue React, 16; 1994 : 181–185.
74. Sváčová H., Izák M., Timová S. et al.: Sympatická oftalmia. Cesk Slov Oftalmol, 40, 1990 : 218–222.
75. Svozílková P., Říhová .E, Brichová M. et al.: Sympatická oftalmie. Cesk Slov Oftalmol, 62; 2006 : 218–223.
76. Svozílková P.: Sympatická oftalmie. In Říhová E, a kol.. Uveitidy, Praha, Grada, 2009, s. 59–60.
77. Štepán J., Smetana K., Smolíková M. et al.: Lymphocyte nucleoli in the peripheral blood and knee joint effusions in patients with rheumatoid arthritis. Z Rheumatol, 37; 1978 : 40–4.
78. Tan XL., Seen S., Dutta-Majumder P. et al.: Anylysis of 130 cases of sympathetic ophthalmia – a retrospective multicenter case series. Ocul Imunol Inflamm, 12; 2018 : 1–8.
79. Toriyama K., Miyajima Y., Lijima F.: Two cases of sympathetic ophthalmia following in intraocular lens Implantation Folia Ophthalmol, 40; l989 : 32–5.
80. Tyagi M., Agarwal K., Reddy Pappuru RR. et al.: Sympathetic ophthalmia after vitreoretinal surgeries: incidence, clinical presentations and outcomes of rare disease. Semin Ophthalmol, 32; 2019 : 157–62.
81. Vejdovský V.: Sympathická ophtalmie po operaci šedého zákalu. Oftalmologický Sborník, 7; 1932 : 109 – 111.
82. Wocker L., Januschowski K.: Steroid implant in treatment of sympathetic ophthalmia: intravitreal implant of dexamethasone in cystoid macular edema in the context of sympathetic ophthalmia. Ophthalmologe, 116; 2019 : 380–3.
83. Zheng C., Wu AY.: Enucleation versus evisceration in ocular trauma: a retrospective review and study of current literature. Orbit, 32; 2013 : 356–61.
Štítky
Oftalmologie
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
2019 Číslo 5- Stillova choroba: vzácné a závažné systémové onemocnění
- Familiární středomořská horečka
- První schválený léčivý přípravek pro terapii Leberovy hereditární optické neuropatie dostupný rovněž v ČR
- Diagnostický algoritmus při podezření na syndrom periodické horečky
- Možnosti využití přípravku Desodrop v terapii a prevenci oftalmologických onemocnění
-
Všechny články tohoto čísla
- Dlouhodobé sledování pacientů se sympatickou oftalmií z diagnosticko léčebného pohledu. Literární přehled.
- Drúzy zrakového nervu a hemodynamika
- Senzitivita a specificita spektrálního OCT u pacientů s počínajícím glaukomovým onemocněním.
- Nanolaser v chirurgii katarakty a jeho vplyv na endotel rohovky
- Molekulárně genetická příčina achromatopsie u dvou pacientů českého původu
- Intravitreálna liečba endogénnej endoftalmitídy pri urosepse – Kazuistika
- Vodiace psy sa cvičia na Slovensku už 25 rokov
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Molekulárně genetická příčina achromatopsie u dvou pacientů českého původu
- Intravitreálna liečba endogénnej endoftalmitídy pri urosepse – Kazuistika
- Senzitivita a specificita spektrálního OCT u pacientů s počínajícím glaukomovým onemocněním.
- Dlouhodobé sledování pacientů se sympatickou oftalmií z diagnosticko léčebného pohledu. Literární přehled.
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




