-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Funkční magnetická rezonance u vybraných očních onemocnění
Functional Magnetic Resonance Imaging in Selected Eye Diseases
In the study, an actual overview of eye’s examinations by means of functional magnetic resonance focused on selected eye’s diseases is presented. Special attention is paid to hypertension glaucomas, normotension glaucoma, age-related macular degeneration, and peeling of the epimacular membrane and the internal limiting membrane. The authors point out the decreased activity of the visual cortex in diseases in which the damage of retinal ganglion cells occurs.
Key words:
functional magnetic resonance imaging, glaucomas, age-related macular degeneration, peeling of the epimacular membrane, and peeling the internal limiting membrane
Autoři: J. Lešták 1,2,3; Jaroslav Tintěra 1
Působiště autorů: Klinika JL, s. r. o., Praha 1; Fakulta biomedicínského inženýrství ČVUT, Praha 2; Lékařská fakulta Karlovy univerzity, Hradec Králové 3
Vyšlo v časopise: Čes. a slov. Oftal., 71, 2015, No. 3, p. 127-133
Kategorie: Původní práce
Souhrn
V práci je podán aktuální přehled vyšetření funkční magnetickou rezonancí na zrakové paradigma zaměřený na vybraná oční onemocnění. Zvláštní důraz je kladen na hypertenzní glaukomy, normotenzní glaukom, věkem podmíněnou makulární degeneraci a peeling epimakulární membrány a membrány limitans interna.
Autoři poukazují na sníženou aktivitu zrakové kůry u nemocí, kde dochází k poškození gangliových buněk sítnice.Klíčová slova:
funkční magnetická rezonance, glaukomy, věkem podmíněná makulární degenerace, peeling epimakulární membrány a membrány limitans internaÚvod
Funkční vyšetřování mozku včetně zrakové kůry je poměrně novou vyšetřovací metodou. V literatuře je jen několik prací zabývajících se funkční magnetickou rezonancí (fMR) zrakové kůry u závažných onemocnění oka s postižením gangliových buněk sítnice, u nichž nelze vyloučit druhotnou alteraci gangliových buněk zrakového centra transsynaptickou (transneuronální) degenerací.
Cílem našich prací bylo vyšetřit pomocí fMR nemocné s glaukomem, exsudativní, věkem podmíněnou makulární degenerací (VPMD) a nemocné po chirurgickém odstranění epimakulární membrány (EMM) spolu s membránou limitans interna (MLI).
VPMD a glaukomy jsou závažná progresivní onemocnění, která jsou nejčastější příčinou ztráty zrakových funkcí u starších dospělých ve vyspělém světě.
Přestože diagnostika a léčba obou nemocí v posledních letech velmi pokročila, mají tyto choroby vzhledem k ireverzibilitě i vážné sociální dopady. Ty vyplývají ze skutečnosti prodlužování lidského věku, a tím i přibývání takto nemocných lidí. S jejich nárůstem je zatěžován nejen systém sociálního pojištění, ale s přísunem nových drahých léčebných metod i systém zdravotního pojištění. Stavy po odstranění EMM a MLI u lamelárních děr a pseudoděr makuly se staly s rozvojem vitreoretinální a speciální makulární chirurgie, častým předmětem diskuse o přínosu a nedostatcích odstranění MLI v makulární chirurgii.
To jsou hlavní důvody, proč je i tato práce zaměřena na uvedené diagnostické skupiny.
2. Definice glaukomů a věkem podmíněné makulární degenerace
2.1 Glaukomy se stále definují jako chronická progresivní neuropatie s exkavací a atrofií terče zrakového nervu a následnými změnami v zorném poli. Tato formulace nevystihuje současné znalosti a je nutno ji korigovat. V modernějším pojetí lze glaukomy definovat jako onemocnění, kde se progresivní ztráta gangliových buněk sítnice a jejich axonů projevuje změnami v zorném poli s atrofií a exkavací terče zrakového nervu. Avšak ani tato definice, zdůrazňující poškození gangliových buněk sítnice před jejími axony není úplná, protože neukazuje současně na poškození gangliových buněk podkorových a korových ústředí v mozku. Současné definice neodlišují hyper - (HTG) a normo-tenzní glaukomy (NTG).
NTG ve srovnání s HTG je odlišný v několika aspektech: kromě výše nitroočního tlaku jsou to změny v zorném poli, které poškozují u NTG více centrální část a mají hlubší defekty citlivosti [1, 27, 28], vlákna jsou u NTG více poškozena v centrální části sítnice a poškození mají fokální charakter [38], exkavace bývá širší a hlubší [9, 31], dále se u nemocných s NTG vyskytují vazospazmy [10], noční systémové hypotenze, redukce pulzní oční amplitudy a fluktuace očního perfuzního tlaku [31, 33, 37], úzké retinální vény, a dokonce zhoršené hemoreologické vlastnosti krve [11, 12, 39] a další.
2.2 Věkem podmíněná makulární degenerace (VPMD) je onemocnění, kde poškození chorioidálních cév a Bruchovy membrány je podmíněno věkem, genetickými a zevními faktory. Lipoidní infiltrace a degenerace kolagenu a elastické tkáně poškozují především bohatě vaskularizovanou makulu. U exsudativní formy VPMD vede cévnatkové kapilární poškození ke zvýšení intrakapilárního tlaku a následné proliferaci neovaskularizací, které penetrují přes defekty v Bruchově membráně pod pigmentový epitel, případně dále, mezi pigmentový epitel a fotoreceptory neuroretiny, a vyvolává exsudaci a krvácení a odchlípení pigmentového epitelu neuroretiny. Všechny tyto procesy vedou nejen k primárnímu zničení pigmentového epitelu a fotoreceptorů, ale také k sekundárnímu poškození bipolárních a gangliových buněk [20].
3. Možnosti vyšetření korových zrakových center pomocí funkční magnetické rezonance (fMR)
Funkční zobrazování mozkové aktivity pomocí magnetické rezonance je relativně novou metodou. Oproti pozitronové emisní tomografii (PET), která byla již o několik let dříve využívána při perfuzních a funkčních studiích mozkové aktivity, má fMR hned několik výhod: lepší časové rozlišení (doba měření obrazu může být i výrazně kratší než 1 s), lepší prostorové rozlišení (velikost základního voxelu matice může být jen několik mm3) a také možnost opakovat několik funkčních měření u stejného subjektu bez jakékoliv invazivnosti. Metoda nevyužívá ionizující záření, ani žádnou externě podanou kontrastní látku a tato skutečnost činí tuto elegantní metodu i přes některé praktické problémy (jako např. relativně nízký poměr signál/šum) velmi atraktivní. Pomocí nepřeberného množství testovacích úloh (tzv. paradigmat) lze studovat téměř libovolné mozkové funkce, provádět časové či srovnávací studie na skupinách vybraných subjektů (např. pacienti versus zdraví dobrovolníci), a to za výhodných etických i ekonomických podmínek.
Mechanismus, umožňující vyšetřování funkční aktivity mozkových center magnetickou rezonancí, je založen na rozdílu lokálního krevního zásobení, tedy na změnách toku a objemu mozkových cév (Cerebral Blood Flow – CBF, Cerebral Blood Volume – CBV) a v krevní oxygenaci. Při aktivaci mozkových buněk dochází ke spuštění hemodynamického procesu, který musí vést k uspokojení zvýšené energetické spotřeby aktivovaných neuronů. Jinými slovy, v místě neuronální aktivity musí dojít ke změně v metabolismu glukózy a tím také ke zvýšené spotřebě kyslíku. Kyslík je distribuován pomocí krevního hemoglobinu. Zvýšení dodávky kyslíku je zajištěno procesem, který je nazýván neurovaskulární vazba (coupling). Aktivita neuronů přenese informaci na přilehlé endoteliální buňky arteriol, a vyvolanou následnou vazodilatací se zvýšeným průtokem krve. Neurovaskulární vazba vede k lokálnímu zvýšení krevního průtoku (zvýšení CBF), lokálnímu zvýšení krevního objemu (zvýšení CBV) a k vyšší lokální koncentraci oxyhemoglobinu (oproti klidovému stavu).
Dynamiku celého procesu lze popsat následujícím způsobem: Krátce po začátku aktivace (řádově několik stovek ms) nastane lokální pokles oxyhemoglobinu (oxy-Hb) v místě aktivace, díky okamžité zvýšené poptávce po kyslíku nárůstem metabolismu glukózy [7]. Následně, během zhruba 3–7 s, ale dojde k lokálnímu zvýšení krevního průtoku (zvýšení CBF a CBV) a tím také k relativnímu nárůstu oxyhemoglobinu v poměru k deoxyhemoglobinu (deoxy-Hb) v blízkosti aktivních neuronů. Fyziologické zvýšení zásobení kyslíkem nejen kompenzuje zvýšenou spotřebu, ale je natolik „předimenzováno“, že v aktivované oblasti dojde ke změně poměru koncentrace mezi oxy-Hb a deoxy-Hb ve prospěch oxy-Hb. Doposud není zcela známo, proč dochází k disproporci mezi zvýšením CBF (a tím i zvýšením koncentrace oxy-Hb) a spotřebou kyslíku metabolismem glukózy. Podle jedné teorie má „předimenzovaný“ průtok chladící efekt, podle jiné má za cíl rychlé odplavení metabolických produktů. Celou kaskádu dějů, které provázejí aktivaci mozkových buněk, schematicky ukazuje obr. 1.
Obr. 1. Schéma neuro-vaskulární vazby: při zvýšení neuronální aktivity dojde tímto mechanismem k lokálnímu zvýšení krevního průtoku 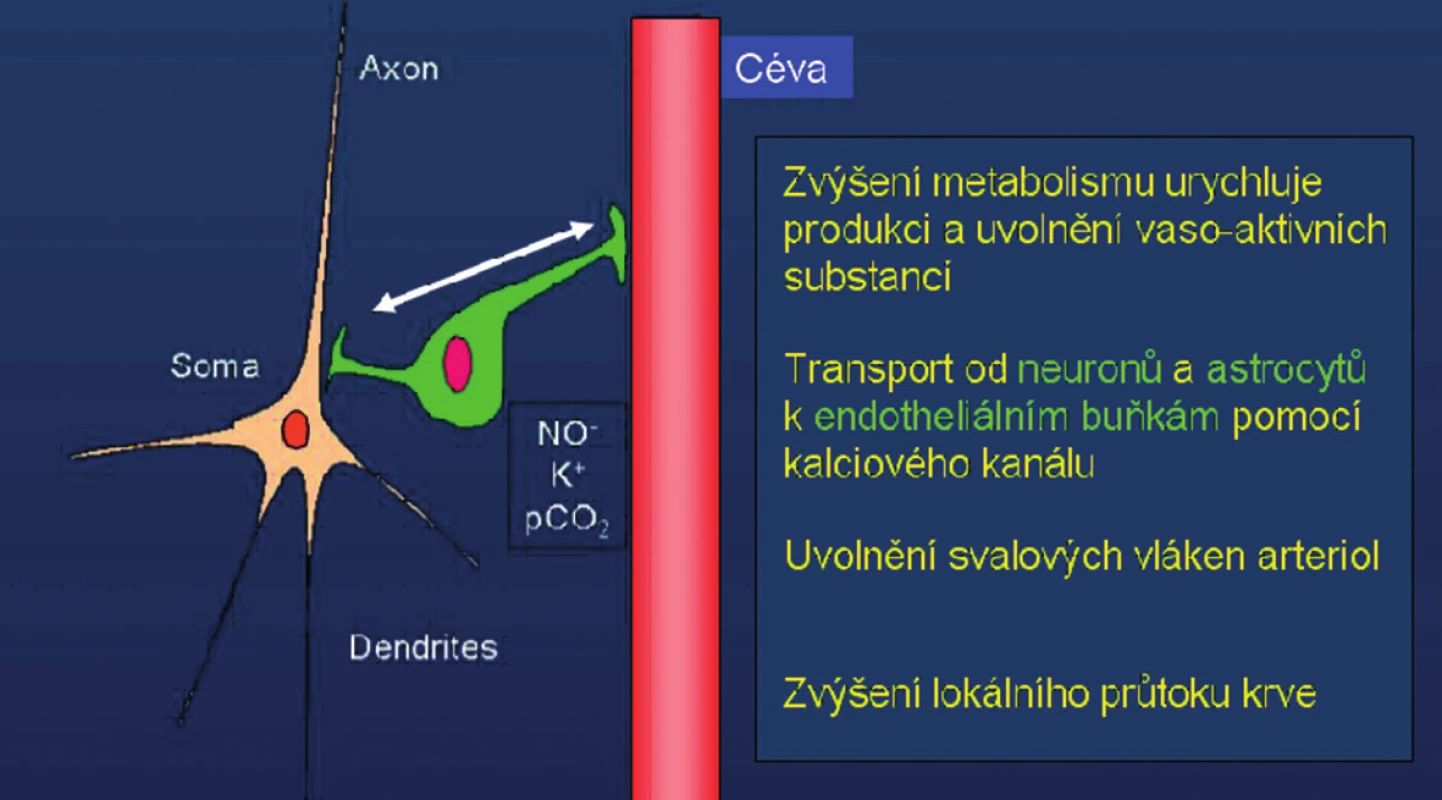
3.1 BOLD efekt
I když z hlediska logiky fyziologických procesů není projev změny oxygenace primární, jeho souvislost s charakterem MR signálu sehrál v historii fMR určitě nejdůležitější roli a i dnes je tento efekt v praxi nejčastěji využíván.
Téměř veškerý kyslík v krvi je vázán k hemoglobinu. Na jednu molekulu hemoglobinu mohou být navázány až čtyři molekuly kyslíku. Odkysličený hemoglobin (deoxy-Hb) má sloučeniny železa se čtyřmi nespárovanými elektrony, které tvoří značný magnetický moment. Důsledkem je paramagnetické chování deoxy-Hb na rozdíl od okysličeného hemoglobinu (oxy-Hb), který nemá žádný magnetický moment a je diamagnetický. Rozdíl v magnetických vlastnostech látek je vyjádřen rozdílnou susceptibilitou. Plně odkysličená krev má susceptibilitu o 0,2 ppm vyšší než plně okysličená krev [5, 41, 42].
Mapování subtilních změn magnetického pole v důsledku oxygenace krve [42] ukazují lineární souvislost mezi susceptibilitou a oxygenací krve, měřenou při 1,5 Tesla. Relativní rozdíl v susceptibilitě paramagnetického deoxy-Hb a okolní tkáně tvoří lokální nehomogenity magnetického pole, které mohou způsobit pokles signálu MR. Situace je schematicky ukázána na obr. 2.
Obr. 2. Schéma rozdílu v susceptibilitě diamagnetického oxy-Hb a paramagnetického deoxy-Hb. Tento rozdíl vyvolává lokální nehomogenitu magnetického pole, která vede k poklesu MR signálu. Změny v rovnovážném poměru koncentrací oxy-Hb a deoxy-Hb řídí změny signálu při měření tohoto tzv. BOLD efektu 
Poprvé byla možnost studovat změny v oxygenaci krve pomocí MR ověřena ve velmi vysokém poli (7 a 8,4 Tesla) a při vysokém rozlišení (65 mm) na hlodavcích [29] a efekt byl nazván „Blood Oxygen Level Dependent“ (BOLD) kontrast. Tyto studie ukázaly, že venózní signál v obraze MR dobře koresponduje se stupněm oxygenace vdechované směsi a tedy také vaskulární oxygenaci. První úspěšné zobrazení aktivity lidského mozku ukázali Belliveau a spol. pomocí optické stimulace a intravenózní aplikací bolu paramagnetické kontrastní látky (GD-DTPA) [2].
3.2 Metodika vyšetření fMR
Všechna měření funkčního MR zobrazování byla provedena na systému Philips Achieva TX SERIES s magnetickým polem 3 Tesla. Ke skenování byla použita 6kanálová hlavová SENSE RF cívka, později 32kanálová hlavová SENSE RF cívka. Optická stimulace při měření fMR byla realizována pomocí komerčního stimulačního systému Eloquence (In Vivo, Německo).
Pro měření fMR metodou BOLD byla použita sekvence gradientního echa EPI s následujícími parametry: TE = 30 ms, TR = 3 s, sklápěcí úhel 90°. Měřený objem obsahoval 39 navazujících vrstev s tloušťkou 2 mm a velikost měřeného voxelu (prostorové rozlišení) byla 2 × 2 × 2 mm3 (FOV = 208 × 208 mm2, matice 104 × 104, rekonstrukční matice 128 × 128, SENSE faktor 1,8). Během snímání fMR byla subjektům promítána alternace černobílé nebo žlutomodré šachovnice (obr. 3). Velikost stimulačního pole byla 25,8 x 16,2 stupňů. Alternace obrazu byla s frekvencí 2 Hz. Během klidové fáze byl subjektu promítán statický zaměřovací kříž, umístěný do středu vizuálního pole. Každé měření tvořilo blokové schéma s 5 intervaly aktivní fáze o délce 30 s (10 dynamických skenů) a 5 klidovými intervaly o stejné délce trvání. Celkově tedy každé měření obsahovalo 100 dynamik a trvalo 5 minut.
Získaná data byla zpracována pomocí softwaru SPM8 a obecného lineárního modelu (GLM).
Během pre-procesu byly údaje pohybově korigovány (realignment) a korigovány na časový posun jednotlivých řezů (slice timing), poté vyhlazeny Gaussovým filtrem s FWHM 6 x 6 x 6 mm a nakonec normalizovány do standardního prostoru MNI_152. Pro statistické vyhodnocení na úrovni jednotlivých subjektů byl použit GLM s modelovou funkcí danou konvolucí tzv. kanonické funkce hemodynamické odpovědi (HRF – hemodynamic response function) s průběhem použitého blokové schématu stimulace. Výsledné statistické mapy byly prahovány na úrovni statistické významnosti p = 0,05 s korekcí na mnohočetná pozorováni FWE (Family Wise Error).
Výsledky
4.1 Normální hodnoty fMR a oční dominance
Při separátní stimulaci každého oka jsme u zdravých osob během vyšetření fMR zaznamenali různou aktivitu zrakových ústředí v mozku. To vedlo k postulování hypotézy, zda interokulární variabilita není spojena s oční dominancí.
Proto jsme vyšetřili 20 očí deseti zdravých osob (osm žen průměrného věku 50,2 let a dva muži průměrného věku 59 let). U všech osob jsme vyšetřili směrovou (hole-in-the-hand and pointing-a-finger test) i senzorickou dominanci (Worth dot test and fogging test). Vyšetření fMR jsme provedli podle výše uvedené metodiky černo-bílou šachovnicí velikosti 25,8 x 16,2 stupně.
U všech osob jsme zjistili různou interokulární fMR aktivitu. Rozdíl nebyl statisticky významný (p = 0,85) a činil 2,2 %. S tímto nálezem nekorelovala ani směrová a ani senzorická oční dominance [25].
Rozbor uvedených výsledků vedl k otázce, zda při oční dominanci nemůže hrát roli i velikost obrazu zobrazeného na sítnici. Vyšetřili jsme stejnou skupinu osob jako v předchozím experimentu, ale tentokrát jsme ke stimulaci použili dvě různě velká vizuální pole (25,8 x 16,2 a 2 x 2 stupně).
U všech osob jsme zjistili různou interokulární variabilitu, avšak větší diferenci jsme zaznamenali u menšího pole. Směrová a ani senzorická dominance nekorelovala s rozsahem aktivace fMR a nezaznamenali jsme ani směrovou lateralitu po separátní stimulaci každého oka [24].
4.2 Funkční MR u hypertenzních a normotenzních glaukomů
O poškození, které ovlivňuje pouze axony gangliových buněk sítnice u HTG, máme pochybnosti od roku 1987, kdy jsme současně měřili pattern elektroretinogram (PERG)a pattern zrakové vyvolané odpovědi (pattern visual evoked potential – PVEP. Měření bylo provedeno u dvacetiletého zdravého muže, nejdříve při nitroočním tlaku 15 mmHg. Následně jsme pomocí sukčního pohárku zvýšili nitrooční tlak na 40 mm Hg a vyšetření opakovali. K našemu překvapení došlo k blokádě přenosu elektrických změn napětí na úrovni gangliových buněk sítnice, zatímco ze zrakového ústředí jsme sejmuli téměř nezměněnou PVEP odpověď. Na základě tohoto zjištění jsme dospěli k závěru, že počáteční změny nebudou na úrovni axonů gangliových buněk, ale samotných buněk [22].
Z důvodu téměř nezměněných zrakových vyvolaných odpovědí ve druhém pokusu jsme vyslovili podezření, že se u HTG zapojí do patogenetického procesu nejen gangliové buňky sítnice, ale i zraková dráha a korová zraková centra. V období kolem roku 1987 byly pro zobrazení mozku k dispozici jen přístroje CT a SPECT. Ani jedno vyšetření nebylo schopno prokázat poškození na úrovni samotných buněk. Proto jsme pomocí pozitronové emisní tomografie, v roce 2002, vyšetřili nemocného s hypertenzním glaukomem obou očí. Prokázali jsme u něj deficit v náplni fluoro-deoxy-glukózy (FDG) v oblasti zrakové kůry a tím i poškození korových buněk zrakového centra [23].
Protože se jednalo o finančně náročné vyšetření a vyšetření zatěžující nemocné radioaktivitou, nepokračovali jsme dále s touto diagnostickou metodou. V roce 2010 jsme přešli na vyšetření pomocí fMR. Podnětem byly výsledky PERG a PVEP, která ukázala, že u vyvinutých HTG s defekty zorných polí se elektrické odpovědi zrakové dráhy liší od odpovědí u NTG. Pomocí PERG a PVEP jsme vyšetřili 80 očí 40 pacientů. Třicet z nich mělo HTG třech různých typů: deset pacientů mělo primární prostý glaukom s otevřeným úhlem (POAG), deset pacientů pigmentový glaukom (PG), deset pseudoexfoliativní glaukom (PEXG) a deset normotenzní glaukom (NTG). Výsledky strukturálních a psychofyziologických vyšetření jsme porovnali se skupinou 40 očí, 20 zdravých osob, přibližně stejného věku a refrakce.
Pomocí PERG a PVEP jsme zjistili, že u hypertenzních glaukomů různé etiologie (POAG, PG, PEXG), dochází k poškození celé zrakové dráhy (od sítnicových gangliových buněk až do zrakových korových ústředí v mozku). Nemocní s PG měly z této skupiny největší poškození zrakové dráhy. U NTG byly odpovědi sítnicových gangliových buněk normální, ale signifikantní změny byly prokázány ve zrakové dráze [17]. Na základě těchto výsledků jsme konstatovali, že korové buňky zrakového ústředí u HTG mohou být na rozdíl od NTG poškozeny.
Pozoruhodné výsledky přinesla strukturální vyšetření periferní části zrakové dráhy. K posouzení velikosti corpus geniculatum laterale (CGL) u HTG a NTG jsme vyšetřili (Philips Achieva TX series release 3.2.1.1) skupinu 9 pacientů s HTG a 9 pacientů s NTG. Diagnóza byla stanovena na základě komplexního oftalmologického vyšetření, které bylo doplněno o vyšetření zorného pole fast threshold programem. Součet citlivostí v homolaterálních polovinách zorných polí (v rozsahu 0 to 22 stupňů) byl porovnán s velikostí druhostranného CGL. Výsledky měření jsme porovnali se skupinou 9 zdravých osob a výsledky jsme podrobili statistické analýze Wilcoxonovým testem a Spearman’s rank korelačním koeficientem. Zjistili jsme redukci CGL jak u HTG, tak NTG (p = 0,0000). Redukce CGL nebyla statisticky závislá na pokročilosti změn v zorných polích u HTG pro pravé poloviny zorných polí (RH VF) a levého CGL r = 0,3255, p = 0,3926 a levých polovin zorných polí (LHVF) a pravého CGL r = 0,0033, p = 0,9934.
Podobně, u NTG, jsme nezjistili statisticky významný rozdíl mezi RH VF a levým CGL (r = 0,0496, p = 0,1745) a mezi LHVF a pravým CGL (r = 0,5399, p = 0,1335 [22].
Abychom potvrdili hypotézu, založenou na předcházejících PERG a PVEP vyšetřeních, že korové buňky zrakového ústředí mohou být u HTG na rozdíl od NTG poškozeny, provedli jsme pomocí fMR vyšetření zrakových korových center mozku.
První práce byla zaměřena na rozsah aktivací fMR u hypertenzních glaukomů s cílem zjistit, zda existuje u HTG korelace mezi pokročilostí onemocnění a rozsahem aktivace.
Vyšetřili jsme devět nemocných s různě pokročilými změnami pomocí metody BOLD a stimulací černo-bílou šachovnici (obr. 3).
Obr. 3. Šachovnicové pole černo-bílé stimulace (a) a žluto-modré stimulace (b). Během stimulace dochází k alternaci šachovnicového pole s jeho inverzí o frekvenci 2 Hz 
Komplexní oftalmologické vyšetření bylo doplněno o vyšetření zorného pole glaukomovým fast threshold programem. Součet citlivostí v homolaterálních polovinách zorných polí (v rozsahu 0 a 22 stupňů) byl porovnán s fMR aktivitou druhostranné hemisféry.
Výsledky jsme porovnali se skupinou osmi zdravých osob. Získaná data ukázala, pomocí non-parametric Spearman’s rank korelace, středně silnou závislost mezi změnami v zorných polích a aktivacemi fMR. Pro pravé poloviny zorných a polí a levou hemisféru byl r = 0,667 (p < 0,05), pro levé poloviny zorných polí a pravou hemisféru byl r = 0,767 (p < 0,016).
V této práci výsledky potvrdily, že s pokročilostí změn v zorných polích se snižuje i aktivita fMR [16, 21, 23].
V další práci jsme stejnou metodikou vyšetřili osm nemocných NTG (počínajícího až středního stadia) a výsledky jsme porovnali se skupinou osmi zdravých osob.
Podobně jako v předchozí práci, jsme postupovali i při vyhodnocení výsledků (non-parametric Spearman’s rank korelace). Korelační koeficient ukázal na slabou nepřímou korelaci mezi změnami v zorných polích a aktivitou fMR. Vztah mezi součtem citlivostí pravých polovin zorných polí a aktivitou kontralaterálního okcipitálního laloku byl r = - 0,270 (p = 0,558) a levých polovin a kontralaterálního okcipitálního laloku byl r = - 0,071 (p = 0,879).
Vztah mezi změnami v zorných polích a aktivitou fMR nebyl prokázán. Výsledky ukázaly, že se NTG patogeneticky chovají jinak než HTG [18, 21, 23].
Protože u HTG dochází k poškození všech typů gangliových buněk sítnice, je zřejmé, že u nemocných HTG musí být i porucha barvocitu. Tento fakt je známý již od roku 1883, kdy byl prokázán Bullem [6] a následně potvrzen i dalšími autory, kteří defekt specifikovali do žluto-modré oblasti [8, 35, 36] a s pokročilostí HTG prokázali progresi [13].
V další práci jsme se proto snažili zjistit, zda se při použití různé stimulace mění aktivita fMR a jako paradigma jsme použili jak černo-bílou, tak žluto-modrou stimulaci, která dosud v žádné citované práci nebyla použita.
Vyšetřili jsme osm nemocných HTG (různých stadií) a jejich výsledky jsme porovnali s výsledky osmi zdravými osobami.
Výsledky byly překvapivé. Zjistili jsme, že rozdíl v počtu aktivovaných voxelů byl u nemocných HTG při použití černo-bílé versus žluto-modré stimulace 59%. U kontrolní skupiny jen 2%.
Zatímco u HTG byl rozdíl mezi černo-bílou a modro-žlutou stimulací statisticky signifikantní 1606 voxelů (p = 0,039), u kontrolní skupiny nebyl zjištěn rozdíl (p = 0,18).
Prokázali jsme tedy, že u HTG dochází k většímu poklesu aktivity fMR při použití barevných paradigmat než černo-bílých [21, 23, 34].
Pokud by HTG byly patogeneticky stejnou skupinou jako NTG, pak by byl i nález fMR po barevné stimulaci podobný.
Pro potvrzení této domněnky jsme vyšetřili osm pacientů s NTG a výsledky jsme porovnali s výsledky osmi zdravých osob. Průměrný počet aktivovaných voxelů po černo-bílé stimulaci byl u nemocných NTG 7 626. U osob kontrolní skupiny 7 462. Průměrný počet aktivovaných voxelů po modro-žluté stimulaci byl u NTG 5 650, u kontrolní skupiny pak 6 353. Tento rozdíl nebyl statisticky významný.
Průměrná hodnota rozdílu v počtu aktivovaných voxelů mezi černo-bílou a modro-žlutou stimulací byla 6% u nemocných NTG. U zdravých osob byl tento rozdíl roven 2 % [19, 21, 23, 34].
I tímto experimentem jsme demonstrovali, že se HTG patogeneticky chová jinak než NTG.
4.3 Změny fMR u věkem podmíněné makulární degenerace
Boucard a spol. zkoumali za pomoci MR šedou hmotu zrakové kůry mozku u nemocných glaukomem a VPMD. Závěr jejich práce byl, že dlouhodobá sítnicová patologie, získaná v pozdějším životě, je spojená s redukcí hustoty šedé hmoty okcipitálního kortexu [3].
Tento závěr je v souladu s našimi výsledky o hypertenzním glaukomu. Nemohli jsme ale najít korelát mezi poškozením zrakových korových buněk a VPMD. U VPMD, která je charakterizována primárním poškozením pigmentového epitelu a fotoreceptorů sítnice, je poškození gangliových buněk sítnice, především u exsudativní formy VPMD sekundární a transsynaptickou degenerací, lze předpokládat asociaci mezi poškozením gangliových buněk sítnice s alterací gangliových buněk zrakové kůry.
Poškození pigmentového epitelu a fotoreceptorů sítnice u VPMD, ale i samotných gangliových buněk sítnice popsali Kim a spol. a Medeiros a Curcio [14, 29].
V naši práci jsme se snažili najít vztah mezi pokročilostí vlhké formy VPMD a aktivitou zrakového centra. Do souboru jsme zařadili deset pacientů s různě pokročilou oboustrannou exsudativní formou VPMD (9 žen a jeden muž) průměrného věku 74,7 let. Žádný ze souboru neměl jiné oční a ani neurologické onemocnění. Funkční MR jsme provedli za pomoci stimulace černo-bílou šachovnicí o velikosti 25,8 x 16,2 stupňů. Vyšetření, vzhledem k výrazné alteraci centrální zrakové ostrosti, jsme provedli najednou na obou očích. Nálezy jsme porovnali s výsledky devíti zdravých osob průměrného věku 54,1 let. Abychom mohli porovnat výsledky obou skupin, adjustovali jsme výsledky zdravé skupiny na průměrný věk první skupiny.
Výsledky jsme zpracovali pomocí Mann-Whitney U testu. Porovnáním obou skupin jsme zjistili statisticky signifikantní rozdíl mezi oběma skupinami (p = 0,0247). Práci jsme uzavřeli, že nemocní s VPMD mají nižší aktivitu fMR než zdravá populace [20].
4.4 Změny fMR po peelingu u symptomatické lamelární makulární díry a makulární pseudodíry
Při odstraňování epiretinální membrány (ERM) s membránou limitans interna (MLI) u lamelárních makulární děr a makulárních pseudoděr sítnice nelze zabránit přímému poškození nejen axonů gangliových buněk sítnice [15], ale i samotných Mullerových buněk (MB), neboť MLI je jejich součástí. MB mají obrovskou metabolickou aktivitu a kromě jiného přeměňují i excitotoxický glutamát na netoxický glutamin. Nahromadění glutamátu v poškozené sítnici může vést k apoptóze gangliových buněk sítnice [4].
Cílem naši práce bylo zjistit, zda odstranění ERM nebo MLI u makulární díry a pseudodíry může vést ke snížení odpovědi fMR na světelnou stimulaci. Do studie jsme zařadili 20 očí deseti pacientů (7 žen a 3 muži) průměrného věku 75,1 let, kterým byla (mezi lednem 2009 až říjnem 2009) provedena pars plana vitrektomie s peelingem MLI na jednom oku. Pacienti neměli žádné jiné oční a ani neurologické onemocnění. Všem byla za čtyři roky provedena fMR při stimulaci černo-bílou šachovnicí (obr. 3) velikosti 25,8 x 16,2 stupně každého oka separátně a obou očí současně. Ke statistickému zpracování jsme použili párový t-test. U všech nemocných jsme zjistili pokles fMR aktivity po stimulaci operovaného oka. Analýza ukázala statisticky významný rozdíl mezi operovaným a neoperovaným okem (p = 0,0049). Výsledky prokázaly, že po odstranění ERM a MLI vede po určité době k poklesu fMR aktivity [27].
Snížení aktivity fMR zrakového centra po odstranění MLI lze vysvětlit poškozením sítnicových gangliových buněk (a to buď přímo peroperačním poškozením jejich axonů, nebo nepřímo poškozením Mullerových buněk sítnice) a následným poškozením korových gangliových buněk cestou transneuronální (transynaptickou) degenerací.
Závěr
V našich pracích jsme prokázali vztah mezi poškozením gangliových buněk sítnice a aktivitou fMR zrakové kůry mozku u HTG, exsudativní VPMD a po odstranění EMM a MLI u lamelární díry a pseudodíry makuly.
Naopak u NTG, kde gangliové buňky sítnice nejeví známky poškození, jsou i hodnoty fMR bez alterace.
Nižší aktivity fMR po odstranění EMM a MLI na operovaném oku nebyly dosud popsány a jsou určitým varováním před nadměrným radikalizmem při těchto operacích.
Velký význam má i zjištění poškození zrakového ústředí mozku u nemocných VPMD, kde se celosvětově léčba soustředila jen na léčbu zevních vrstev sítnice.
Vedoucí lékař prim. MUDr. Ján Lešták, CSc., FEBO, MBA, LLA, DBA, FAOG
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmu a není podpořeno žádnou farmaceutickou firmou.
Prim. MUDr. Ján Lešták, CSc., FEBO, MBA, LLA, DBA, FAOG
V Hůrkách 1296/10
158 00 Praha 5
e-mail: lestak@seznam.cz
Do redakce doručeno dne 17. 2. 2015
Do tisku přijato dne 10. 4. 2015
Zdroje
1. Araie M., Yamagami J., Suziki Y.: Visual field defects in normal-tension and high-tension glaucoma. Ophthalmology, 100; 1993 : 1808–1814.
2. Belliveau JW., Kennedy DN., McKinstry RC., Buchbinder BR., Weiskoff RM., Cohen MS., Vevea JM., Brady TJ., Rosen BR.: Functional mapping of the human visual cortex by magnetic resonance imaging. Science, 254; 1991 : 716–719.
3. Boucard CC., Hernowo AT., Maguire RP., Jansonius NM., Roerdink JB., Hooymans JM., Cornelissen FW.: Changes in cortical grey matter density associated with longstanding retinal visual field defects. Brain, 132; 2009 : 1898–1906.
4. Bringmann A., Reichenbach A.: Role of Müller cells in retinal degenerations. Front Biosci, 1; 2001 : 6: E72–92.
5. Brooks RA., DiChiro G.: Magnetic resonance imaging of stationary blood: a review, Med Phys, 14; 1987 : 903–913.
6. Bull O.: Bemerkungen über Farbensinn unter verschiedenen physiologischen und pathologischen Verhältnissen. Albrecht von Graefes Arch Ophthalmol, 29; 1883 : 71–116.
7. Buxton R., Frank L.: A model for the coupling between cerebral blood flow and oxygen metabolism during neural stimulation. J Cereb blood Flow Metab, 14; 1997 : 365–372.
8. Drance SM., Lakowski R., Schulzer M., Douglas GR.: Acquired color visionchanges in glaucoma. Use of 100-hue test and Pickford anomaloscope as predictors of glaucomatous field change. Arch Ophthalmol, 99; 1981 : 829–831.
9. Eid TE., Spaeth GL., Moster MR., Augburger JJ.: Quantitative differences between the optic nerve head and peripapillary retina in low-tension glaucoma and high-tension primary open-angle glaucoma. Am J Ophthalmol, 124; 1997 : 805–813.
10. Flammer J., Prünte C.: Ocular vasospasm. 1: Functional circulatory disorders in the visual system, a working hypothesis. Klin Monbl Augenheilkd, 198; 1991 : 411–412.
11. Chang M., Yoo C., Kim SW., Kim YY.: Retinal vessel diameter, retinal nerve fiber layer thickness, and intraocular pressure in Korean patients with normal-tension glaucoma. Am J Ophthalmol, 151; 2011 : 100–105.
12. Cheng HC., Chan CM., Yeh SI., Yu JH., Liu DZ.: The hemorrheological mechanisms in normal tension glaucoma. Curr Eye Res, 36; 2011 : 647–653.
13. Jonas JB., Zäch FM.: Color vision defects in chronic open angle glaucoma. Fortschr Ophthalmol, 87; 1990 : 255–259.
14. Kim SY., Sadda S., Humayun MS., de Juan E., Melia BM., Green WR.: Morphometric analysis of the macula in eyes with geographic atrophy due to age-related macular degeneration. Retina, 22; 2002 : 464–470.
15. Lesnik Oberstein SY., Lewis GP., Chapin EA., Fisher SK.: Ganglion cell neuritis in human idiopathic epiretinal membranes. Br J Ophthalmol, 92; 2008 : 981–985.
16. Lešták J., Tintěra J., Kynčl M., Svatá Z., Obenberger J., Saifrtová A.: Changes in the Visual Cortex in Patients with High-Tension Glaucoma. J Clinic Exp Ophthalmol, 2011; S4 doi: 10.4172/2155-9570.S4-002.
17. Lešták J., Nutterová E., Pitrová Š., Krejčová H., Bartošová L., Forgáčová V.: High tension versus normal tension glaucoma. A comparison of structural and functional examinations. J Clinic Exp Ophthalmol, 2012; S:5, http://dx.doi.org/10.4172/2155-9570.S5-006.
18. Lešták J., Tintěra J., Ettler L., Nutterová E., Rozsíval P.: Changes in the Visual Cortex in Patients with Normotensive Glaucoma. J Clinic Exp Ophthalmol, 2012; S:4 http://dx.doi.org/10.4172/2155-9570.S4-008.
19. Lešták J., Tintěra J., Svatá Z., Ettler L., Rozsíval P.: Brain Activations in fMRI induced by Color Stimulation in Patients with Normotensive Glaucoma. J Clin Exp Ophthalmol, 3;2012 : 8 http://dx.doi.org/10.4172/2155-9570.1000250.
20. Lešták J., Tintěra J., Karel I., Svatá Z., Rozsíval P.: FMRI in Patients with Wet Form of Age-Related Macular Degeneration. Neuro-Ophthalmology, 37; 2013 : 192–197.
21. Lešták J., Tintěra J., Kynčl M., Svatá Z., Rozsíval P.: High Tension Glaucoma and Normal Tension Glaucoma in Brain MRI. J Clin Exp Ophthalmol, 4; 2013 : 4. http://dx.doi.org/10.4172/2155-9570. 1000291.
22. Lešták J., Kynčl M., Svatá Z., Rozsíval P.: Lateral Geniculate Nucleus in Hypertensive and Normotensive Glaucoma. J Clin Exp Ophthalmol, 4; 2013 : 269. doi:10.4172/2155-9570.1000269.
23. Lestak J., Tintera J., Svata Z., Ettler L., Rozsival P.: Glaucoma and CNS. Comparison of fMRI results in high tension and normal tension glaucoma. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub, 158; 2014 : 144–153.
24. Lestak J., Tintera J., Rozsival P.: Ocular dominance and FMRI activation in response to various stimuli. International Journal of Scientific Research, 3; 2014 : 505–507.
25. Lestak J., Tintera J. Rozsival P.: FMRI and ocular dominance. Inter J Scient Res, 3; 2014 : 293–296.
26. Lešták J., Tintěra J., Kalvoda J., Svatá Z., Kalvodová B., Karel I., Rozsíval P.: FMRI after internal limiting membrane peeling for symptomatic lamellar macular hole and macular pseudohole surgery. International Journal of Applied Research, 4; 2014 : 379–382.
27. Lestak J., Nutterova E., Bartosova L., Rozsival P.: The Visual Field in Normal tension and Hypertension Glaucoma. International Journal of Scientific Research, 3; 2014 : 49–51.
28. Lester M., De Feo F., Douglas GR.: Visual field loss morphology in high-and normal-tension glaucoma. J Ophthalmol, 2012; 327326. Epub 2012: Feb 8.
29. Medeiros NE., Curcio CA.: Preservation of ganglion cell layer neurons in age-related macular degeneration. Invest Ophthalmol Vis Sci, 42; 2001 : 795–803.
30. Ogawa S., Lee TM., Nayak AS, Glynn P.: Oxygenation-sensitive contrast in magnetic resonance imaging of rodent brain at high magnetic field, Magn Reson Med, 14; 1990 : 68–78.
31. Okuno T., Sugiyama T., Kojima S., Nakajima M., Ikeda T.: Diurnal variation in microcirculation of ocular fundus and visual field change in normal-tension glaucoma. Eye (Lon), 18; 2004 : 697–702.
32. Park HY., Jeon SH., Park CK.: Enhanced depth imaging detects lamina cribrosa thickness differences in normal tension glaucoma and primary open-angle glaucoma. Ophthalmology, 119; 2012 : 10–20.
33. Plange N., Remky A., Arend O.: Colour Doppler imaging and fluorecein filling defects of the optic disc in normal tension glaucoma. Br J Ophthalmol, 87; 2003 : 731–736.
34. Saifrtová A., Lešták J., Tintěra J., Svatá Z., Ettler L., Rozsíval P., Veselá-Florová Z.: Colour vision defect in patients with high-tension glaucoma. J Clin Exp Ophthalmol, 3;2012 : 9 http://dx.doi.org/10.4172/2155-9570.1000252
35. Sample PA., Weinreb RN., Boynton RM.: Acquired dyschromatopsia in glaucoma. Surv Ophthalmol, 131;1986 : 54–64.
36. Sample PA., Boynton RM., Weinreb RN.: Isolating the color vision loss in primary open-angle glaucoma. Am J Ophthalmol, 106; 1988 : 686–691.
37. Schwenn O., Troost R., Vogel A., Grus F., Beck S., Pfeiffer N.: Ocular pulse amplitude in patients with open angle glaucoma, normal tension glaucoma, and ocular hypertension. Br J Ophthalmol, 86; 2002 : 981–984.
38. Shin IH., Kang SY., Hong S., Kim SK., Seong GJ., Ma KT., Kim CY.: Comparison of OCT and HRT findings among normal tension glaucoma, and high tension glaucoma. Korean J Ophthalmol, 22; 2008 : 236–241.
39. Sung KR., Lee S., Park SB., Choi J., Kim ST., Yun SC., Kang SY., Cho JW., Kook MS.: Twenty-four hour perfusion pressure fluctuation and risk of normal-tension glaucoma progression. Invest Ophthalmol Vis Sci, 50; 2009 : 5266–5274.
40. Thonginnetra O., Greenstein VC., Chu D., Liebmann JM., Ritch R., Hood DC.: Normal versus high tension glaucoma: a comparison of functional and structural defects. J Glaucoma, 19; 2010 : 151–157.
41. Thulborn KR., Waterton JC., Matthews PM. et al.: Oxygenation dependence of the transverse relaxation time of water protons in whole blood at high field, Biochem Biophys Acta, 714; 1982 : 265–270.
42. Weisskoff RM., Kühne S.: MRI susceptometry: image-based measurements of absolute susceptibility of MR contrast agents and human blood, Magn Reson Med, 24; 1992 : 375–383.
Štítky
Oftalmologie
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
2015 Číslo 3- Stillova choroba: vzácné a závažné systémové onemocnění
- Familiární středomořská horečka
- Léčba chronické blefaritidy vyžaduje dlouhodobou péči
- První schválený léčivý přípravek pro terapii Leberovy hereditární optické neuropatie dostupný rovněž v ČR
- Konjunktivitida a původce Corynebacterium macginleyi – kazuistika
-
Všechny články tohoto čísla
- Funkční magnetická rezonance u vybraných očních onemocnění
- Stereotaktická rádiochirurgia (LINAC) uveálnych melanómov; postradiačné komplikácie
- Vnitřně fotosenzitivní gangliové buňky sítnice
- Exenterácia očnice pre malígny melanóm choroidey v štádiu T4; možnosti epitetického riešenia
- Corneal cross-linking v liečbe keratokónusu – výsledky a komplikácie v dvojročnom sledovaní
- Chirurgické řešení idiopatické makulární díry 25-gauge pars plana vitrektomií s peelingem vnitřní limitující membrány asistované briliantovou modří a plynovou tamponádou
- Multifokálna viteliformná retinálna lézia
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Vnitřně fotosenzitivní gangliové buňky sítnice
- Funkční magnetická rezonance u vybraných očních onemocnění
- Chirurgické řešení idiopatické makulární díry 25-gauge pars plana vitrektomií s peelingem vnitřní limitující membrány asistované briliantovou modří a plynovou tamponádou
- Exenterácia očnice pre malígny melanóm choroidey v štádiu T4; možnosti epitetického riešenia
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



