-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Kolagen v kombinaci s kyselou formou karboxymethylcelulosy v podobě netkané textilie jako moderní krycí prostředek pro terapii ran – formulace, příprava a hodnocení
Collagen in combination with the acid form of carboxymethylcellulose in the form of a nonwoven textile as a modern wound dressing – formulation, preparation and evaluation
The acid form of carboxymethylcellulose (HCMC) is less known than its sodium salt (NaCMC). However, it is commonly used as a sorbent for chromatographic columns and has a number of valuable properties for its use in wound care. As a wound dressing in the form of hydrofibers, it is already commercially available on our market. Collagen, the most abundant protein in the human body, fulfils both a building and a physiological function in the body, also has an irreplaceable place in the treatment of wounds. It is important in the process of wound healing and is used in wound therapy in various forms. It exhibits very good film-forming properties as well, but the collagen-based films themselves have weaker mechanical resistance, which limits their successful application to a wound. Therefore, the effort is to combine collagen with other materials in order to ensure better mechanical and application properties even in the wet state. The aim of this experiment was to create a wound dressing by combining a collagen film with HCMC in the form of a nonwoven textile. The resulting dressing had satisfactory organoleptic, physicochemical (pH, absorbency) and application properties for its use in wound therapy. The textile HCMC formed a mechanical support for collagen, which enabled its saving during the dressing preparation and partly served as an absorbent layer.
Autoři: Kateřina Tenorová; Ruta Masteiková; Jana Jarábková; David Vetchý; Jurga Bernatonien
Vyšlo v časopise: Čes. slov. Farm., 2020; 69, 163-171
Kategorie: Původní práce
Souhrn
Kyselá forma karboxymethylcelulosy (HCMC) je oproti její sodné soli (NaCMC) méně známá. Je však běžně využívána jako sorbent pro chromatografické kolony a má řadu cenných vlastností pro uplatnění v péči o rány. Jako krytí ve formě hydrokoloidních vláken je již komerčně dostupná na našem trhu. Své nezastupitelné místo v léčbě ran má i kolagen, nejhojněji zastoupený protein lidského těla, plnící v organismu jak stavební, tak i fyziologickou funkci. Je důležitý v procesu hojení ran a v terapii ran je využíván v různých formách. Má i velmi dobré filmotvorné vlastnosti, avšak samotné kolagenové filmy mají slabší mechanickou odolnost, což by pro případnou aplikaci na ránu nebylo vyhovující. Proto je snaha kolagen kombinovat s jinými materiály za účelem zajištění lepších mechanických a aplikačních vlastností i ve vlhkém stavu. Cílem tohoto experimentu bylo vytvořit krycí prostředek na rány, a to kombinací kolagenového filmu s HCMC ve formě netkané textilie. Vzniklé krytí mělo vyhovující organoleptické, fyzikálně-chemické (pH, nasákavost) a aplikační vlastnosti pro uplatnění v terapii ran. Textilní HCMC tvořila mechanickou oporu pro kolagen, čímž umožnila jeho úsporu při přípravě krytí a částečně sloužila i jako absorpční vrstva.
Klíčová slova:
wound dressing – collagen – acid form of carboxymethylcellulose – hydrofibers – films – wound therapy
Úvod
Fakt, že moderní krycí prostředky na rány jsou založeny na tzv. principu vlhkého hojení, je všeobecně známý1, 2). Udržení vlhkého prostředí v ráně podporuje její správnou regeneraci a urychluje tím proces hojení3–5). Požadavky na moderní krycí prostředky však nejsou jen udržení vlhkého prostředí v ráně, ale jedná se o komplexní záležitost. Ideální krytí by mělo zároveň poskytovat optimální pH i teplotu pro správné hojení rány, být schopné absorbovat nadměrné množství exsudátu, zvyšovat epidermální migraci, podporovat angioneogenezi i syntézu pojivové tkáně, umožnit proudění plynů mezi ránou a okolním prostředím, poskytovat mechanickou ochranu i bariéru proti bakteriální infekci, nepřilnout na ránu a být snadno odstranitelné, být sterilní, netoxické a nealergenní, umožnit sledování rány, být přizpůsobivé a lehce tvarovatelné, snížit potřebu výměny krytí a prodloužit časový interval aplikace, být snadno dostupné ve zdravotnických zařízeních v požadovaném množství a různých velikostech, a v neposlední řadě být také nákladově efektivní3, 4, 6–9). K výrobě moderních krycích prostředků jsou využívány jak syntetické, tak i přírodní materiály, které se v současné době dostávají do popředí ve všech odvětvích, včetně oblasti péče o rány a jsou předmětem mnoha výzkumů a studií7, 10–12). Právě přírodní materiály a jejich deriváty vykazují příznivé vlastnosti pro hojení ran vzhledem k jejich biokompatibilitě, podobnosti s extracelulární matricí (ECM) či nižší pravděpodobností výskytu imunologických reakcí, jako je tomu v případě materiálů syntetických10, 13, 14). Další výhodou je jejich biodegradovatelnost a ekologičnost, na což je v dnešní době upírána čím dál větší pozornost. Snahou je využívat pro tyto účely i odpadní materiály vznikající při zpracování různých známých surovin přírodního původu15, 16). Již běžně jsou v klinické péči o rány využívány krycí prostředky na bázi alginátů17), chitosanu18), kolagenu19) a celulosových derivátů20). Zkoumány jsou však i další látky s potenciálním uplatněním pro terapii ran, a to například sericin21), hedvábný fibroin22) a mnoho dalších. Zároveň je však tendence stávající materiály modifikovat a kombinovat – ať už navzájem, nebo i se syntetickými polymery s cílem vyvinout nové prostředky na rány, které by se svými vlastnostmi blížily výše popsanému ideálnímu krytí10).
Celulosa a především její deriváty nabízejí řadu cenných vlastností uplatnitelných právě pro ošetřování ran23). Používá se jak přírodní celulosa (bavlna), regenerovaná celulosa (viskóza), tak i dva celulosové deriváty, a to oxidovaná celulosa (oxycelulosa) a karboxymethylcelulosa20).
Karboxymethylcelulosa (CMC) je etherový derivát celulosy se širokou škálou uplatnění24). Je hojně využívána jako emulgátor, stabilizátor, zahušťovadlo, protispékavá a gelotvorná látka v širokém spektru odvětví, jako jsou medicína, farmaceutický, kosmetický, textilní, potravinářský, chemický, ropný, keramický i papírenský průmysl25, 26). V medicíně a farmacii se uplatňuje zejména jako gelotvorná látka; je používána např. do očních kapek vzhledem ke svým viskoelastickým a mukoadhezivním vlastnostem. Ve farmaceutické technologii slouží jako pojivo a rozvolňovadlo (kroskarmelosa) v tabletách či jako látka zvyšující viskozitu využívaná pro stabilizaci suspenzí a emulzí27, 28). V neposlední řadě je i významným materiálem v krycích prostředcích na rány29), kde může být využita v různých typech krytí – ať už se jedná o hydrokoloidy, hydrokoloidní vlákna, či hydrogely20). Usušením koloidních roztoků je možné připravit z CMC i krytí filmová, která zatím na trhu dostupná nejsou a jedná se zejména o experimentální práce na toto téma30, 31). Karboxymethylcelulosa je využívána nejčastěji ve formě své sodné soli (NaCMC), existuje i jako sůl vápenatá (CaCMC) a jako kyselá forma (HCMC), která je však méně známá20, 32). HCMC se běžně používá jako sorbent pro chromatografické kolony. Zajímavostí je, že má vhodné vlastnosti pro uplatnění v péči o rány a jako krytí HCel® HT je již dostupná na našem trhu. Typově se jedná o hydrokoloidní vlákna, avšak od těch klasických (NaCMC) se liší tím, že bobtnají postupně, jak dochází v ráně k výměně iontů (přechod HCMC v NaCMC). Jedná se o pH modulující krytí, eliminující působení některých bakterií. Výhodou je nedráždivost a samozřejmě zlepšení a urychlení hojení. Ačkoliv jsou klasická hydrokoloidní vlákna určena primárně pro silně až středně secernující rány, HCel® HT je vhodný i pro slabě exsudující rány v kombinaci s navlhčením fyziologickým roztokem20).
Dalším významným biopolymerem nacházejícím uplatnění v potravinářství, medicíně, kosmetice, farmacii i tkáňovém inženýrství je kolagen33, 34). Kolagen má řadu výhodných vlastností z hlediska jeho možného využití pro terapii ran – ať už se jedná o jeho nízkou cytotoxicitu, antigenicitu, dráždivost a především dobrou kompatibilitu s lidským organismem35, 36). Jako hlavní strukturální protein pojivových tkání (kosti, vazy, šlachy, chrupavky, rohovky či cévní stěny) plní v lidském těle převážně mechanickou funkci, důležitou roli však zastává i v pokožce a tkáních, kde plní fyziologickou úlohu v procesu hojení ran a reparace tkání36, 37). Molekula kolagenu je tvořena třemi polypeptidovými řetězci, jež jsou uspořádané do spirálovité (helikální) struktury, tzv. superšroubovice. Každý řetězec je tvořen tisíci aminokyselinami se základní sekvencí glycin-X-Y, kdy pozice X a Y obsahují ze všech aminokyselin nejčastěji prolin nebo hydroxyprolin37, 38). V lidském těle existuje až 29 typů kolagenu; nejčastěji zastoupenými jsou kolageny typu I, III, IV, V a VII, z nichž typ I a III hraje zásadní roli v procesu hojení ran36, 38, 39). Uměle dodaný kolagen v krycích prostředcích na rány na bázi kolagenu slouží jako obětní substrát pro enzymy (matricové metaloproteinázy, MMPs), kterých je u chronických ran nadbytek a degradují nově vznikající kolagen v zánětlivé fázi hojení rány19, 39, 40). Ten může být do rány dodán v různých formách – ať už se jedná o gel, prášek či krytí ve formě polštářku39). Kolagen má však i velmi dobré filmotvorné vlastnosti, jichž je využíváno především v potravinářském průmyslu41). V terapii ran prozatím kolagenové filmy využití nenacházejí, neboť vzniklé kolagenové filmy mají slabé mechanické vlastnosti, což je z hlediska případné aplikace na ránu nevyhovující. Je však snaha kolagen různě modifikovat např. zesíťováním, popřípadě ho kombinovat s dalšími materiály s cílem zlepšení jeho mechanických vlastností 11, 41, 42).
Vzhledem k výše popsaným skutečnostem se nabízí možnost kombinace kolagenu v podobě filmu s textilní HCMC, která je sama o sobě osvědčeným krycím prostředkem s dobrými absorpčními vlastnosti, s cílem zlepšit mechanické vlastnosti výsledného krytí a zajistit optimální aplikační vlastnosti na ránu, a to i ve vlhkém stavu, což bylo i předmětem našeho experimentu.
Pokusná část
Materiál
Pro přípravu kolagenového krytí na rány kombinovaného s textilní podobou kyselé formy karboxymethylcelulosy (HCMC) byly použité dva druhy kolagenu ve formě gelu, a to koňský a prasečí kolagen, oba původem ze šlach, dodané firmou Collado, s.r.o., Brno, Česká republika. Kyselou formu karboxymethylcelulosy ve formě netkané textilie se stupněm substituce (DS) 0,378 dodala firma Holzbecher Medical, s. r. o. barevna a bělidlo Zlíč, Česká Skalice, Česká republika. Použitá změkčovadla – glycerol 85% a makrogol 300, stejně jako další pomocná látka – ethanol 96%, byly dodány firmou Fagron a.s., Olomouc, Česká republika. K testování připravených krycích prostředků na rány posloužil lékopisný (ČL 2017) fyziologický tlumivý roztok o pH 7,2 (FTR 7,2), k jehož přípravě byly použité běžně komerčně dostupné suroviny lékopisné kvality. Čištěná voda lékopisné kvality byla připravena pomocí přístroje Rodem 4.
Metodika
Stanovení koncentrace kolagenového gelu
Výchozí surovinou byl koňský a prasečí kolagen, dodané ve formě viskózního gelu neznámé koncentrace. Ke stanovení sušiny (% obsahu) kolagenu v gelu byl použit halogenový analyzátor vlhkosti (Excellence Plus HX 204, Mettler Toledo, Švýcarsko), kde sušení probíhalo za následujících podmínek: standardní program sušení, teplota sušení 105 °C, kritérium pro vypnutí 1 mg/50 s. Kolagenový gel byl nejprve řádně zhomogenizován, poté bylo odebráno množství cca 1 g, které bylo umístěno na vytárovanou váhu analyzátoru a bylo spuštěno měření. Výstupem byla hodnota % MC (moisture content), z níž byl odečtením od 100 zjištěn obsah kolagenové sušiny, čili % koncentrace kolagenu v gelu. Pro oba dva kolageny byla sušina stanovena celkem 6krát a ze získaných hodnot byl vypočten aritmetický průměr.
Příprava krycích prostředků z kolagenu a HCMC
Připravované krytí na rány bylo tvořeno kolagenovým filmem v první vrstvě, na nějž byla přiložena vrstva druhá, kterou tvořila kyselá forma karboxymethylcelulosy (HCMC) ve formě netkané textilie. Krytí bylo připraveno metodou odpaření rozpouštědla a jednotlivé vzorky se lišily druhem použitého kolagenu (koňský nebo bovinní) a typem použitého změkčovadla (glycerol 85% a makrogol 300) a jeho poměrem vůči kolagenu (1 : 1; 1 : 1,5; 1 : 2). Množství použitého kolagenu bylo u všech vzorků stejné (3 mg/cm2) a vycházelo z našich předchozích zkušeností. Disperze kolagenu byla odlévána na hranaté polystyrenové Petriho misky o rozměrech 12 × 12 cm, na něž byla přiložena textilní HCMC jako svrchní vrstva. Připravované a testované vzorky včetně jejich složení jsou uvedeny v tabulce 1.
Tab. 1. Označení a složení jednotlivých vzorků 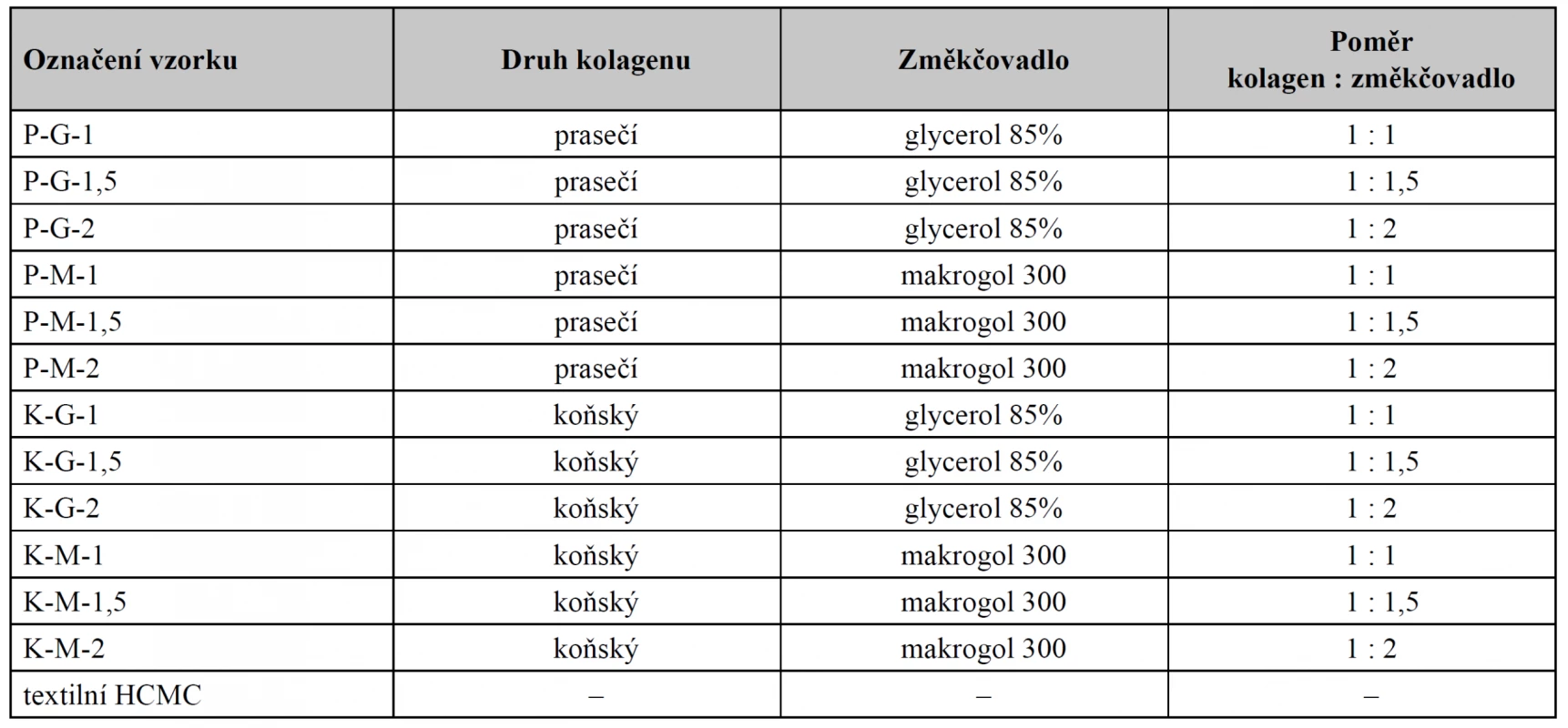
Vlastní příprava krytí probíhala tak, že byla nejprve vytvořena 1% disperze kolagenu s daným poměrem změkčovadla a předem stanoveným potřebným množstvím ethanolu 96%, která byla zhomogenizována na přístroji Cito-Unguator 2000 (Sophis a.s., Česká republika) s využitím programu „Emulze“. Ta byla následně vylita na Petriho misky a na povrch byla umístěna textilní HCMC tak, aby respektovala tvar misky a byla rovnoměrně rozložena na kolagenové vrstvě. Sušení poté probíhalo při teplotě místnosti. Důkladně usušené vzorky byly organolepticky hodnoceny a následně uchovávány ve vzduchotěsných obalech.
Hodnocení připravených krytí na rány
Organoleptické a mikroskopické hodnocení
Organoleptické hodnocení připravených krytí bylo prováděno během celé jejich přípravy. Kontrolována byla odlévaná disperze kolagenu, a to především její homogenita a možná přítomnost bublinek. Hotové a dostatečně usušené vzorky byly hodnoceny z hlediska jejich vzhledu, pevnosti, změny tvaru a schopnosti manipulace s nimi, a to jak v suchém, tak i ve vlhkém stavu. Mikroskopické hodnocení bylo provedené na optickém mikroskopu (SMZ 1500, Nikon, Japonsko), kde byly pořízeny fotografie krytí za pomocí softwaru Elements (Nikon, Japonsko).
Měření tloušťky
Tloušťka byla měřena s využitím digitálního tloušťkoměru Elcometer 456 (Gamin, Česká republika). Každé připravené krytí (3 ks od každého typu) bylo umístěno na nerezovou desku a sondou tloušťkoměru bylo naměřeno celkem 27 hodnot tloušťky (3 × 9) na různých místech krytí. Z naměřených hodnot byla spočítána průměrná tloušťka a směrodatná odchylka.
Hmotnostní stejnoměrnost
Jelikož ČL 2017 nedefinuje podmínky pro hodnocení krycích prostředků na rány včetně hodnocení jejich hmotnostní stejnoměrnosti, byla pro naše účely použita lékopisná zkouška uvedená v ČL 2017 v kapitole 2.9.5. Hmotnostní stejnoměrnost pevných jednodávkových lékových forem. Od každého typu krytí bylo vybráno 20 náhodných vzorků (vystřižené čtverečky o rozměrech 25 × 25 mm), které byly zváženy na analytických vahách. Z těchto hodnot byl následně spočítán aritmetický průměr a hranice maximální a minimální povolené odchylky, která činí pro tablety v rozmezí hmotnosti 80–250 mg 7,5 %. Dle ČL 2017 se mohou nejvýše dvě hmotnosti lišit od povolené odchylky, přičemž žádná se nesmí lišit o více než její dvojnásobek43).
Stanovení stupně nasákavosti (bobtnavosti) krytí
Hodnocení schopnosti krytí bobtnat, a pohlcovat tak exsudát z rány, bylo provedeno jako stanovení stupně nasákavosti Sn. K tomu byl použit umělý model rány, jehož cílem je imitovat exsudující ránu a byl využíván již v našich předchozích experimentech44). Je tvořený Petriho miskou s průměrem dna 10 cm, v níž je umístěna savá houbička po celé její ploše směřující svým hrubým povrchem nahoru, což má za cíl napodobit nerovnoměrný povrch rány. Houbička v misce je zalita 20 ml média – FTR 7,2 a zakryta víčkem, aby nedocházelo k odpařování média. Vzorek o rozměrech 2,5 × 2,5 cm byl nejprve zvážen v suchém stavu na analytických vahách a poté umístěn na ránu (houbičku), a to kolagenem směrem do rány. Ve stanovených časových intervalech – 15 min, 1 h, 5 h, 8 h a 24 h byl pomocí pinzety oddělen od modelu rány. Následovalo jeho zvážení na analytických vahách. Ze získaných hodnot hmotností vzorku za sucha a za mokra v daném intervalu byl spočítán stupeň nasákavosti Sn (g/g), a to dle následujícího vzorce:
Sn = (mm – ms)/ms,
kde mm je hmotnost nasáklého vzorku a ms hmotnost vzorku suchého.
Povrchové pH krytí po navlhčení kapkou vody
K měření povrchového pH po navlhčení kapkou vody byl použit pH metr (pH 3210, Wissenschaftlich-Technische Werkstätten GmbH, Německo) a kontaktní skleněná elektroda (FlaTrode, Hamilton Company, USA). Na vzorek o rozměru 2,5 × 2,5 cm byla ze střičky kápnuta kapka čerstvě převařené čištěné vody. Po nasáknutí vzorku bylo změřené povrchové pH na kolagenové straně krytí.
pH vodného výluhu
Pro měření pH výluhu byly použity čtverečky krytí o rozměrech 2,5 × 2,5 cm. Jednotlivé vzorky byly nejprve zváženy, umístěny do kádinek a zality čerstvě převařenou čištěnou vodou pokojové teploty, jejíž hmotnost byla v poměru 1 : 100 vůči hmotnosti daného vzorku. Měření pH vodného výluhu bylo provedeno za pomocí pH metru (pH 3210, Wissenschaftlich-Technische Werkstätten GmbH, Německo) a ponorné elektrody (SenTix 41, Wissenschaftlich-Technische Werkstätten GmbH, Německo), a to ve dvou časových intervalech – po 3 a po 24 hodinách.
Změny povrchového pH v čase
Měření povrchového pH krytí a hodnocení jeho změn v čase bylo realizováné za pomocí výše zmíněného umělého modelu rány. Vzorky o rozměrech 2,5 × 2,5 cm byly umístěny na model, a to tak, že vrstva kolagenu směřovala na houbičku (do rány). Po uplynutí stanovených časových intervalů – 15 minut, 1 h, 5 h, 8 h a 24 h byl vzorek z modelu rány odstraněn, umístěn na prázdnou Petriho misku a bylo změřeno jeho povrchové pH na kolagenové straně za pomocí kontaktní elektrody.
Výsledky a diskuze
Kolagenové krytí s kyselou formou karboxymethylcelulosy ve formě netkané textilie, která tvořila opornou vrstvu pro kolagenový film, bylo připraveno metodou odpaření rozpouštědla. Ačkoliv má kolagen velmi dobré filmotvorné vlastnosti, především po navlhčení mají kolagenové filmy minimální mechanickou odolnost, což je z hlediska potencionální aplikace na ránu nevyhovující a nepřijatelné. Z toho důvodu je snaha kolagen kombinovat s jinými materiály45, 46), s cílem zajistit dostatečnou pevnost, pružnost a mechanickou odolnost přípravku jako takového11, 41, 42). Z hlediska organoleptických vlastností se námi zvolená kombinace kolagenu s HCMC jeví jako žádoucí pro aplikaci na rány, neboť vykazuje dobré vlastnosti a manipulaci i po navlhčení a krytí je zároveň soudržné na kolagenové vrstvě po 24 hodinách, čehož jsme chtěli docílit. Textilní HCMC vlastní kolagenový film nejen mechanicky podporuje a vede k úspoře použitého kolagenu, který sám o sobě není levným materiálem, ale zároveň funguje i jako hydrokoloidní krytí se schopnostní bobtnat a pojmout exsudát (obr. 1).
Obr. 1. Mikroskopický vzhled krytí při 10násobném přiblížení (vlevo) – struktura krytí v suchém stavu, vzhled krytí ve vlhkém stavu po 24 hodinách po umístění na umělý model rány (vpravo) 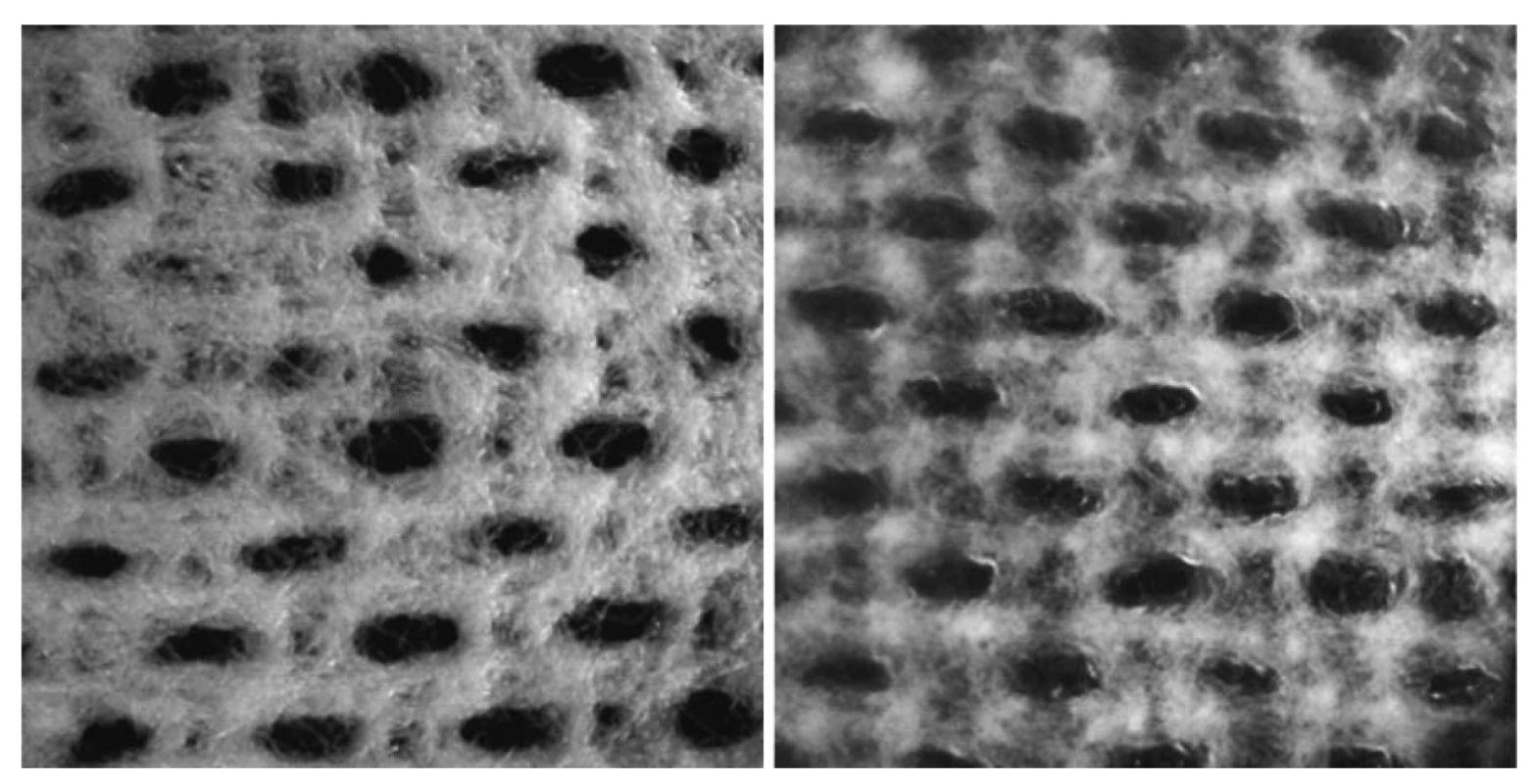
Odlévané disperze obou typů kolagenu byly viskózní, homogenní a bělavého zabarvení s tím, že druh použitého změkčovadla nijak neovlivňoval jejich vzhled a vlastnosti. Důležitou roli hrál při tvorbě disperze 96% ethanol, který sloužil k naředění disperze a k případnému odstranění nežádoucích bublinek vzniklých homogenizací. Připravená a řádně usušená krytí na rány byla z hlediska kolagenové vrstvy homogenní, hladká, lesklá, průhledná a mezi jednotlivými druhy kolagenu nebyly patrné žádné rozdílné organoleptické vlastnosti. Vzorky s makrogolem však při pohmatu působily pevněji, vyšší poměr změkčovadla vůči kolagenu způsobil, že vzorky byly při pohmatu měkčí a poddajnější jak v případě glycerolu, tak i makrogolu. Vrstva textilní HCMC byla ve všech případech stejná, na ohmat drsná a tvořila mechanickou oporu vzniklého krytí. Ve vlhkém stavu byly všechny vzorky pevné, dobře se s nimi manipulovalo, a to i po 24 hodinách na umělém modelu rány. Z kolagenové strany působily mírně lepivým dojmem, který se zvětšoval v průběhu času. Nebyly zřejmé žádné významné rozdíly organoleptických vlastností v rámci druhu použitého kolagenu, změkčovadel či jejich poměrů. Vzhled připraveného krytí na rány přibližuje obrázek 2.
Obr. 2. Vzhled připraveného krytí na rány (vlevo) – usušený vzorek o rozměrech cca 12 × 12 cm, vzorek o rozměru 2,5 × 2,5 cm ve vlhkém stavu na umělém modelu rány po 24 hodinách (vpravo) 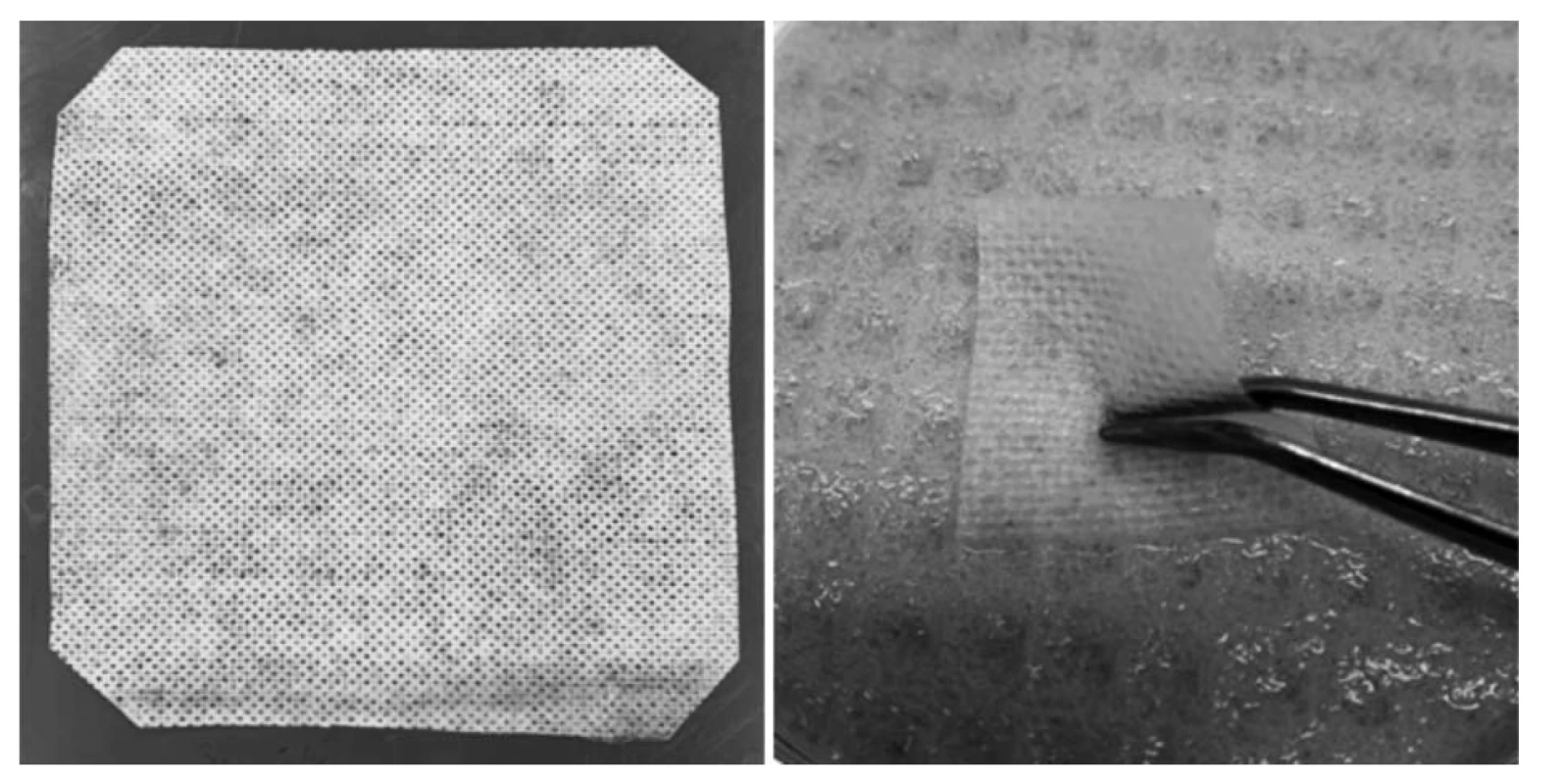
Všechny typy připraveného krytí vyhovovaly námi aplikované zkoušce hmotnostní stejnoměrnosti dle ČL 2017. Průměrné hmotnosti jednotlivých vzorků včetně povolené odchylky a maximální/minimálních hmotnostní přibližuje tabulka 2. V tabulce je také uvedena průměrná tloušťka jednotlivých vzorků. Největší naměřená tloušťka byla obecně vždy u filmů s poměrem změkčovadla 1 : 2 a s makrogolem jako změkčovadlem. Filmy z prasečího kolagenu byly silnější než filmy z kolagenu koňského, ačkoliv v průměru vážily méně. Samotná textilie logicky dosahovala nejmenší tloušťky i hmotnosti.
Tab. 2. Tloušťka a hodnocení hmotnostní stejnoměrnosti jednotlivých vzorků 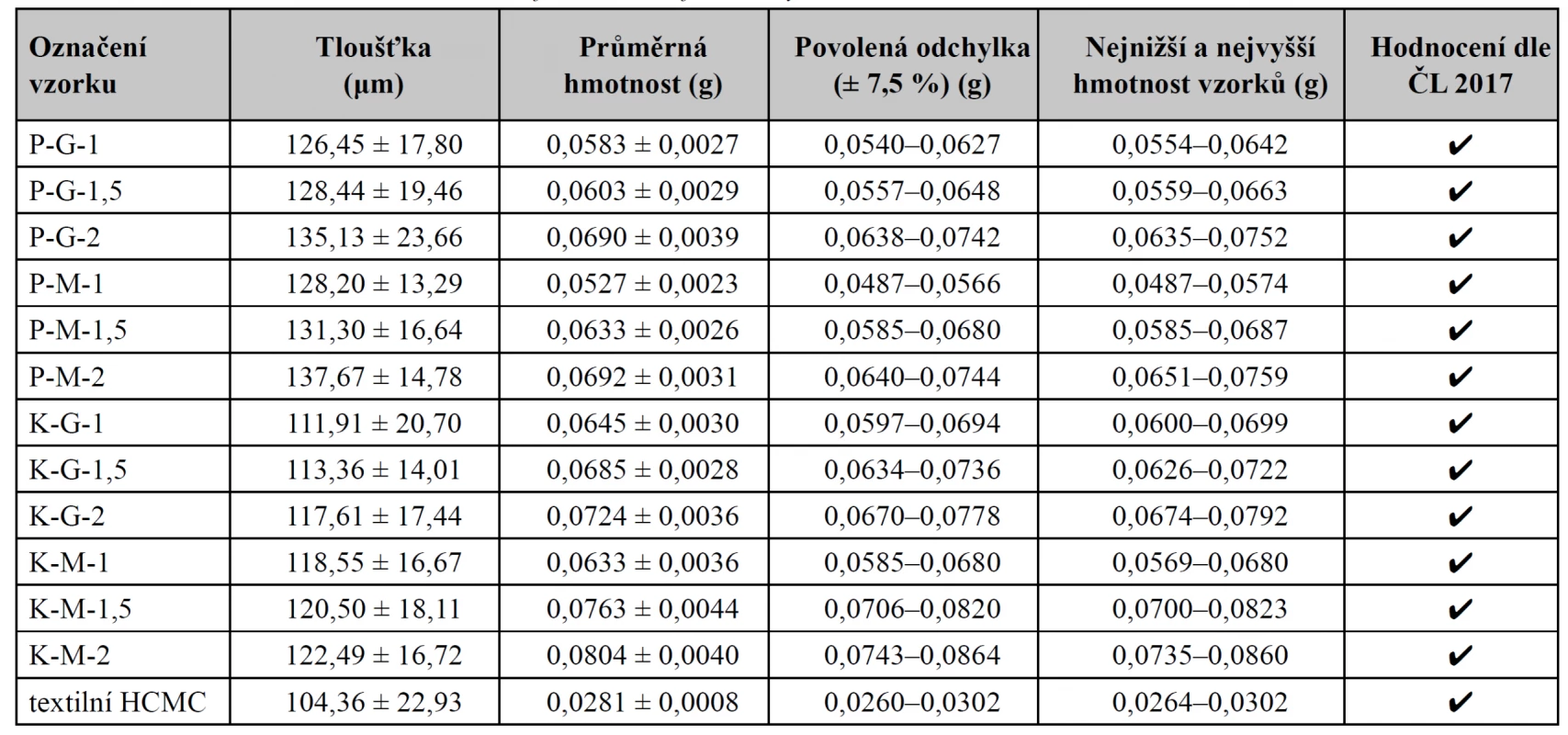
Hodnocení absorpčních vlastností krycích prostředků patří k jedné ze základních charakteristik jejich vlastností z hlediska aplikace na ránu. Moderní krytí mají za cíl zajistit optimální vlhkost v ráně, což vede k jejímu správnému hojení44). Konkrétní požadavky se liší od zamýšleného použití a především druhu rány – některé rány jsou silně exsudující, jiné rány jsou suché, a tudíž potřebují spíše hydratovat a z minimálního množství exsudátu zajistit vlhké prostředí1). V našem případě sloužil pro porovnání schopnosti absorpce stupeň nasákavosti Sn. U hydrokoloidních vláken (samotná textilní HCMC) se vzhledem k jejich charakteristice očekává poměrně vysoká schopnost absorpce exsudátu, což potvrzuje i obrázek 3. Je patrné, že samotná textilie dosahovala až 3krát vyšší nasákavosti než v kombinaci s oběma kolageny. V případě kombinace textilie s kolagenem dosahovala nasákavost těchto vzorků průměrných hodnot s tím, že můžeme konstatovat, že oproti koňskému kolagenu má prasečí kolagen vyšší absorpční vlastnosti, které se zvyšují i v rámci času. U koňského kolagenu se sice schopnost nasáknout FTR 7,2 v čase zvyšuje, ale ne tak výrazně jako u kolagenu prasečího. Co se týče změkčovadla, filmy s makrogolem jsou nasákavější než s glycerolem a svoji roli hraje i poměr změkčovadla – čím vyšší poměr změkčovadla, tím nižší nasákavost. To je dáno hydroskopickým charakterem obou těchto látek, kvůli kterému krytí obsahuje určité procento vlhkosti, avšak tím se snižuje schopnost pojmout další kapalinu.
Obr. 3. Změny nasákavosti krytí a textilie v průběhu času 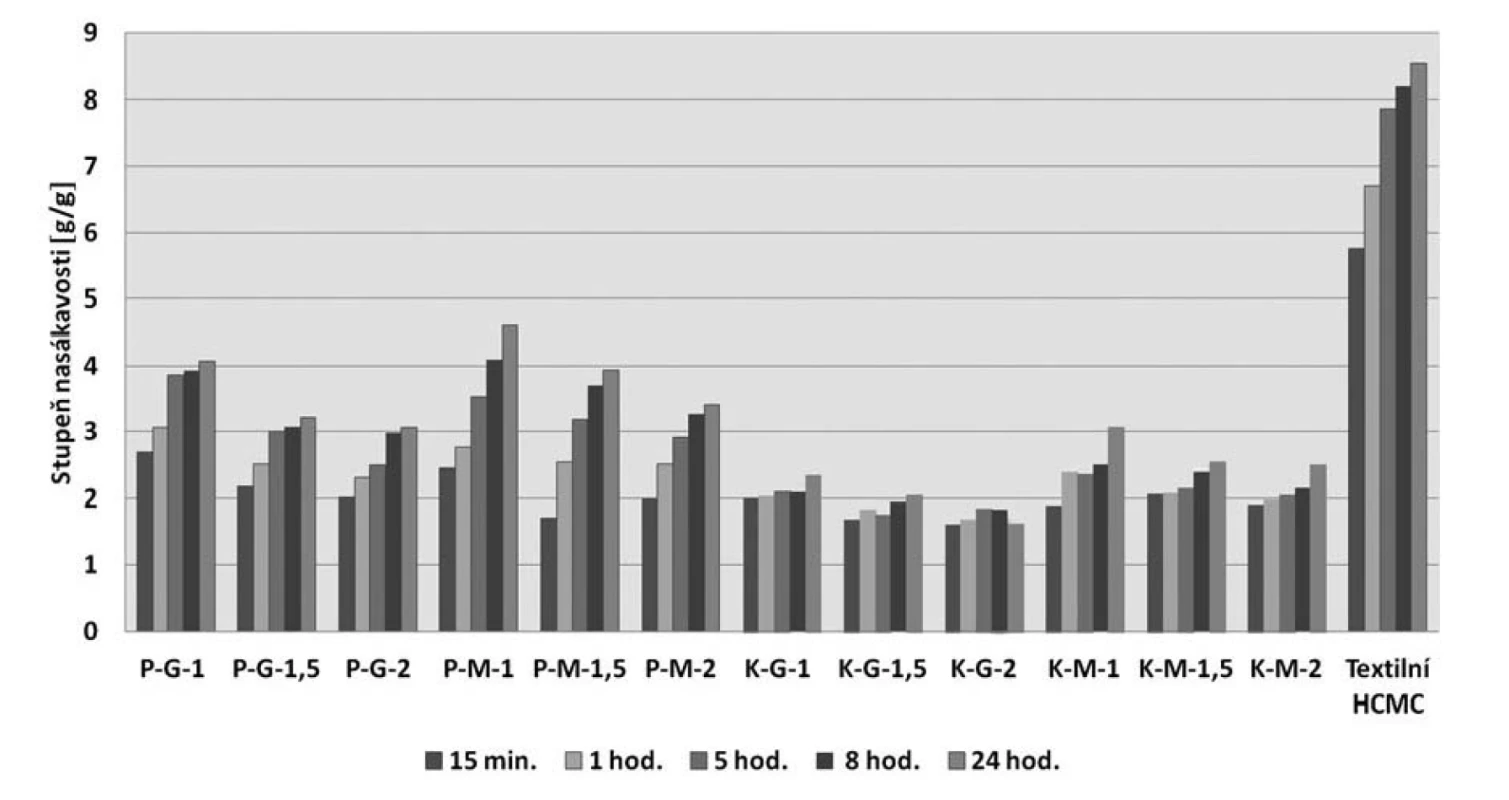
Stanovení hodnot pH, a především hodnocení jeho změn v čase, řadíme k významnému testování aplikačních vlastností krycích prostředků na rány. Bylo prokázáno, že chronické nehojící se rány jsou charakteristické zásaditým pH, které je spojené s vyšší aktivitou MMPs, popř. s výskytem bakteriální infekce. Naopak mírně kyselé prostředí vede k inhibici MMPs, proliferaci fibroblastů, epitelizaci, angioneogenezi a potlačuje výskyt mikroorganismů4, 47). Z tohoto důvodu je důležité znát, zda je krycí prostředek na rány schopný pH modulovat a udržet jeho hodnoty v kyselé oblasti. Tabulka 3 shrnuje hodnocení povrchového pH po navlhčení kapkou vody a pH vodného výluhu všech vzorků včetně textilie. Všechny hodnoty leží v kyselé oblasti, u vzorků s makrogolem jsou nižší než u krytí s glycerolem. U stanovení pH výluhu v podstatě není zásadní rozdíl mezi hodnotami pH po 3 a 24 hodinách. O tom, zda je krytí schopné udržet pH v kyselé oblasti po jeho aplikaci v určitém časovém intervalu, vypovídá více hodnocení změn pH v čase na obrázku 4. Všechny vzorky jsou schopné i po 24 hodinách na modelu rány s FTR 7,2 udržet pH v mírně kyselé oblasti, tudíž je můžeme považovat za pH modulující krytí. V případě textilie a prasečího kolagenu se v rámci 24hodinového intervalu pH zvyšovalo mírně, zatímco u vzorků s koňským kolagenem lze pozorovat výraznější nárůst pH v intervalu 24 hodin.
Tab. 3. Hodnocení pH po navlhčení kapkou vody a pH vodného výluhu 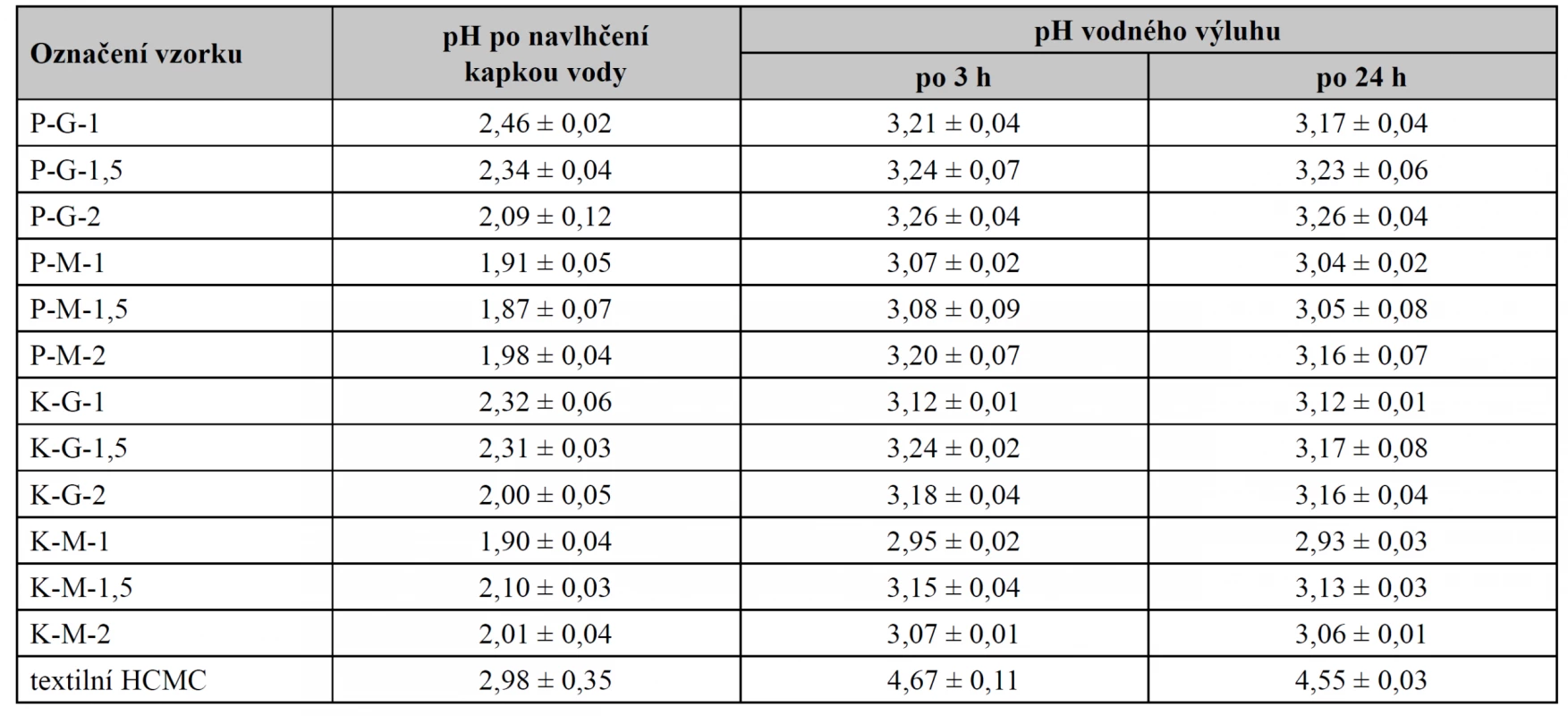
Obr. 4. Změny povrchového pH krytí a textilie v průběhu času ve FTR 7,2 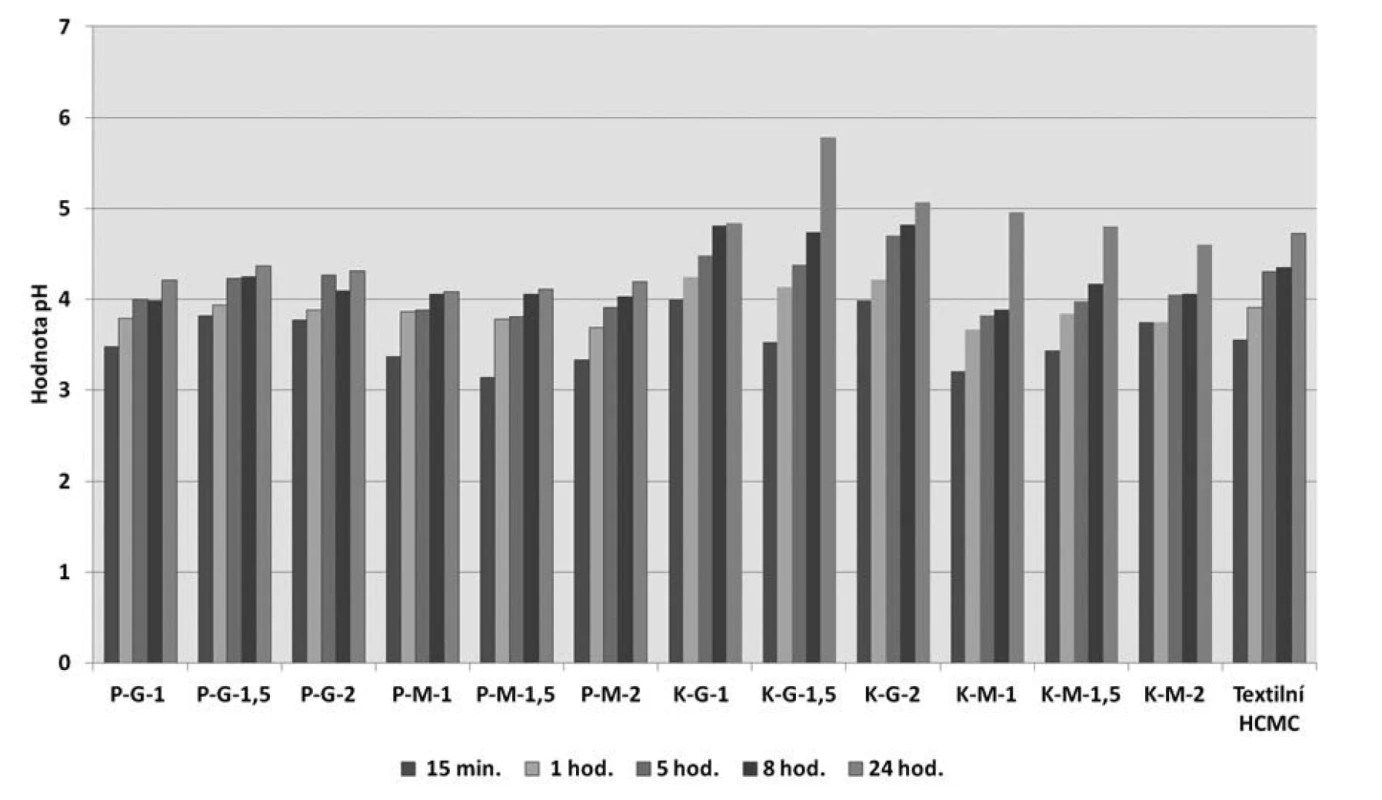
Závěr
Z výše uvedených skutečností a provedeného experimentu vyplývá, že námi zvolená kombinace kolagenového filmu a HCMC ve formě netkané textilie se jeví jako vhodná pro zamýšlenou aplikaci na rány. Všechny připravené vzorky měly dobré organoleptické vlastnosti i ve vlhkém stavu po 24 hodinách na umělém modelu rány. Krytí bylo schopné udržet pH v kyselé oblasti a zároveň pohlcovat přiměřené množství exsudátu v ráně. Rozdíl v použitých změkčovadlech a jejich poměrech nemá zásadní vliv na testované vlastnosti krytí, avšak druh použitého kolagenu je ovlivňuje. Vzorky s koňským kolagenem mají nižší absorpční vlastnosti a menší schopnost udržet pH v rámci 24hodinového intervalu než vzorky s kolagenem prasečím.
Práce vznikla za podpory IGA VFU Brno, Česká republika pod číslem (304/2019/FaF).
Střet zájmů: žádný.
PharmDr. Kateřina Tenorová () • R. Masteiková • J. Jarábková •
D. Vetchý
Masarykova univerzita, Farmaceutická fakulta
Ústav farmaceutické technologie
Palackého třída 1946/1, 612 00 Brno
e-mail: K.Tenorova@seznam.cz
J. Bernatonienė
Akademie medicíny, Litevská univerzita zdravotnických věd
Farmaceutická fakulta, Katedra technologie léků a sociální farmacie
Kaunas, Litva
Zdroje
1. Peate I., Glencross W. Wound Care at a Glance. Oxford: Wiley-Blackwell 2015.
2. Rajendran S. Advanced Textiles for Wound Care (The Textile Institute Book Series), 2nd ed. Woodhead Publishing 2018.
3. Boateng J. S., Matthews K. H., Stevens H. N. E., Eccleston G. M. Wound healing dressings and drug delivery systems: a review. J. Pharm. Sci. 2008; 97(8), 2892–2923.
4. Dhivyaa S., Padmab V. V., Santhinia E. Wound dressings – a review. BioMedicine 2015; 5(4), 24–28.
5. Sweeney I. R., Miraftab M., Collyer G. A critical review of modern and emerging absorbent dressings used to treat exuding wounds. Int. Wound J. 2012; 9(6), 601–612.
6. Bell D., Hyam D. Choosing an appropriate dressing for chronic wounds. Prescriber 2007; 18(11), 65–70.
7. Okur M. E., Karantas I. D., et al. Recent trends on wound management: New therapeutic choices based on polymeric carriers. Asian J. Pharm. Sci. 2020.
8. Yao K., Bae L., Yew W. P. Post-operative wound management. Aust. Fam. Physician 2013; 42(12), 867–870.
9. Naude L. Exudate management: Putting the patient first. Prof. Nurs. Today 2008; 12(5), 29–32.
10. Mogoșanu G. D., Grumezescu A. M. Natural and synthetic polymers for wounds and burns dressing. Int. J. Pharm. 2014; 463(2), 127–136.
11. Gaspar-Pintiliescu A., Stanciuc A. M., Craciunescu O. Natural composite dressings based on collagen, gelatin and plant bioactive compounds for wound healing: A review. Int. J. Biol. Macromol. 2019; 138, 854–865.
12. Paul E. J., Padmapriya B. A pragmatic review on the property, role and significance of polymers in treating diabetic foot ulcer. Mater. Today: Proceedings 2020; 23, 91–99.
13. Naseri-Nosar M., Ziora Z. M. Wound dressings from naturally-occurring polymers: A review on homopolysaccharide-based composites. Carbohydr. Polym. 2018; 189, 379–398.
14. Calori I. R., Braga G., De Jesus P. C. C., Bi H., Tedesco A. C. Polymer scaffolds as drug delivery systems. Eur. Polym. 2020; 129, 109621.
15. Li X., Ma M., Ahn D. U., Huang X. Preparation and characterization of novel eggshell membrane-chitosan blend films for potential wound-care dressing: From waste to medicinal products. Int. J. Biol. Macromol. 2019; 123, 477–484.
16. Jaganathan G., Manivannan K., Lakshmanan S., Sithique M. A. Fabrication and characterization of Artocarpus heterophyllus waste derived lignin added chitosan biocomposites for wound dressing application. Sustain. Chem. Pharm. 2018; 10, 27–32.
17. Varaprasad K., Jayaramudu T., Kanikireddy V., Toro C., Sadiku E. R. Alginate-based composite materials for wound dressing application: A mini review. Carbohydr. Polym. 2020; 236, 116025.
18. Hamedi H., Moradi S., Hudson S. M., Tonelli A. E. Chitosan based hydrogels and their applications for drug delivery in wound dressings: A review. Carbohydr. Polym. 2018; 199, 445–460.
19. Fleck C. A., Simman R. Modern Collagen Wound Dressings: Function and Purpose. J. Am. Col. Certif. Wound Spec. 2010; 2(3), 50–54.
20. Sopuch T., Drahovzalová R., Rýdl J. et al. Celulózové materiály v ošetřování ran. Hojení ran 2013; 7(2), 14–20.
21. Bakhsheshi-Rad H. R., Ismail A. F., Aziz M., Akbari M., Hadisi Z., Omidi M., Chen X. Development of the PVA/CS nanofibers containing silk protein sericin as a wound dressing: In vitro and in vivo assessment. Int. J. Biol. Macromol. 2020; 149, 513–521.
22. Farokhi M., Mottaghitalab F., Fatahi Y., Khademhosseini A., Kaplan D. L. Overview of Silk Fibroin Use in Wound Dressings. Trends Biotechnol. 2018; 36(9), 907–922.
23. Gupta B., Agarwal R., Alam M. S. Textile-based smart wound dressings. Indian J. Fibre Text. Res. 2010; 35, 174–187.
24. Benchabane A. Carboxymethyl Cellulose: Rheological and Pipe Flow Properties. RAPSCI 2018; 5(5), 95–103.
25. Tufan M., Uraz E., Tosun C., Gercel H. Synthesis and characterization of carboxymethyl cellulose film from pistachio shells. Int. J. Adv. Sci. Eng. Tech. 2016; 4(1), 153–155.
26. Sunardi N., Febriani M., Junaidi A. B. Preparation of carboxymethylcellulose produced from purun tikus (Eleocharis dulcis). AIP Conference Proceedings 2017; 1868, 1–8.
27. Kulikowska A., Wasiak I., Ciach T. Carboxymethyl cellulose oxidation to form aldehyde groups. Biomed. Eng. 2013; 4(2), 11–18.
28. Araújo D. M. L., Galera P. D. Ocular lubricants: what is the best choice? Ciência Rural. 2016; 46(11), 2055–2063.
29. Stephen-Haynes J., Callaghan R., Stephens C. Evaluating the performance of a new carboxymethylcellulose dressing in the community setting. Br. J. Nurs. 2017; 26(6), S36–S41.
30. Ramli N. A., Wong T. W. Sodium carboxymethylcellulose scaffolds and their physicochemical effects on partial thickness wound healing. Int. J. Pharm. 2011; 403(1–2), 73–82.
31. Vinklárková L., Masteiková R., Vetchý D., Doležel P., Bernatoniené J. Formulation of novel layered sodium carboxymethylcellulose film wound dressings with ibuprofen for alleviating wound pain. BioMed Res. Int. 2015; 2015, 1–11.
32. Lopez C. G., Rogers S. E., Colby R. H., Graham P., Cabral J. T. Structure of sodium carboxymethylcellulose aqueous solutions: A SANS and rheology study. J. Polym. Sci. B Polym. Phys. 2015; 53(7), 492–501.
33. Liu X., Zheng Ch., Luo X., Wang X., Jiang H. Recent advances of collagen-based biomaterials: Multi-hierarchical structure, modification and biomedical applications. Mater. Sci. Eng. C. 2019; 99, 1509–1522.
34. Brett D. A review of collagen and collagen-based wound dressings. Wounds 2008; 20(12), 347–356.
35. Salvatore L., Gallo N., Natali M. L., et al. Marine collagen and its derivatives: Versatile and sustainable bio-resources for healthcare. Mater. Sci. Eng. 2020; 113, 110963.
36. Romero-Ortuno R., Kenny R. A., McManus R. Collagens and elastin genetic variations and their potential role in aging-related diseases and longevity in humans. Exp. Gerontol. 2020; 129, 110781.
37. Kirkness M. W. H., Lehmann K., Forde N. R. Mechanics and structural stability of the collagen triple helix. Curr. Opin. Chem. Biol. 2019; 53, 98–105.
38. Abou Nell E. A., Bozec L., Knowles J. C., Syed O., Mudera V., Day R., Hyun J. K. Collagen – Emerging collagen based therapies hit the patient. Adv. Drug Deliv. Rev. 2013; 65(4), 429–456.
39. Hochstein A. O., Bhatia A. Collagen: its role in wound healing. Podiatry management 2014; 8, 103–110.
40. Harding K. G., Rangaraj A., Leaper D. Role of collagen in wound management. Wounds 2011; 7(2), 54–60.
41. Yang H., Guo X., Chen X., Shu Z. Preparation and characterization of collagen food packaging film. J. Chem. Pharm. Res. 2014; 6(6), 740–745.
42. Chen X., Zhou L., Xu H., et al. The structure and properties of natural sheep casing and artificial films prepared from natural collagen with various crosslinking treatments. Int. J. Biol. Macromol. 2019; 135, 959–968.
43. Český lékopis 2017. Praha: Grada Publishing 2017; 4904 s.
44. Masteiková R., Vinklárková L., Muselík J., Vetchý D., Bernatoniené J., Sopuch T. Vliv stupně substituce na nasákavost kyselé formy karboxymethylcelulosy v podobě netkané textilie. Čes. slov. Farm. 2013; 62(2), 89–94.
45. Ocak B. Development of the mechanical and barrier properties of collagen hydrolysate/carboxymethyl cellulose films by using SiO2 nanoparticles. PAJES 2019; 25(3), 320–324.
46. Tenorová K., Masteiková R., Kovárová N., Kostelanská K., Přikryl J., Vetchý D., Bernatoniené J. Příprava a hodnocení dvouvrstvých filmů na bázi kolagenu a karboxymethylcelulosy za účelem terapie ran. Čes. slov. Farm. 2019; 68, 229–236.
47. Metcalf D. G., Haalboom M., Bowler P. G., Gamerith C., Sigl E., Heinzle A., Burnet M. W. M. Elevated wound fluid pH correlates with increased risk of wound infection. Wound Medicine 2019; 26(1), 1–5.
Štítky
Farmacie Farmakologie
Článek vyšel v časopiseČeská a slovenská farmacie
Nejčtenější tento týden
- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Ukažte mi, jak kašlete, a já vám řeknu, co vám je
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
-
Všechny články tohoto čísla
- Vakcíny z pohledu farmaceuta
- Kolagen v kombinaci s kyselou formou karboxymethylcelulosy v podobě netkané textilie jako moderní krycí prostředek pro terapii ran – formulace, příprava a hodnocení
- Aplikácia inhalačných liekov z pohľadu lekárnika
- Současné stanovení amoxicilinu a klavulanátu draselného v kombinovaných lékových formách: přenos postupu z HPLC na UPLC
- Složení mastných kyselin v Centaurea cyanus (L.)
- Česká a slovenská farmacie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Vakcíny z pohledu farmaceuta
- Aplikácia inhalačných liekov z pohľadu lekárnika
- Kolagen v kombinaci s kyselou formou karboxymethylcelulosy v podobě netkané textilie jako moderní krycí prostředek pro terapii ran – formulace, příprava a hodnocení
- Složení mastných kyselin v Centaurea cyanus (L.)
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



