-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Možnosti léčby plazmou u pacientů s hereditární formou trombotické trombocytopenické purpury
Autoři: Z. Čermáková 1,2; M. Kořístka 1,3; B. Kořístková 4; R. Hrdličková 1; T. Šuláková 5; J. Furková 1; P. Kovářová 1
Působiště autorů: Fakultní nemocnice Ostrava, Krevní centrum 1; Univerzita Karlova v Praze, 1. lékařská fakulta, I. interní klinika VFN 2; Ostravská univerzita Ostrava, Fakulta zdravotnických studií, Katedra vyšetřovacích metod 3; Fakultní nemocnice Ostrava, Ústav klinické farmakologie 4; Fakultní nemocnice Ostrava, Klinika dětského lékařství 5
Vyšlo v časopise: Čas. Lék. čes. 2009; 148: 493-496
Kategorie: Původní práce
Souhrn
Východisko.
U trombotické trombocytopenické (TTP) purpury je léčba výměnnými plazmaferézami metodou volby.Metody a výsledky.
Pacienti s TTP jsou opakovaně léčeni vysokými dávkami dárcovské plazmy, klinický i laboratorní efekt této léčby je ve většině případů úspěšný. Výměnné plazmaferézy výrazně snížily mortalitu pacientů s TTP. Léčba plazmou nabízí různé alternativy – infuze plazmy či výměnnou plazmaferézu – a dále alternativy v podání jednotlivých typů plazmy. Plazma bez kryoproteinu (K-plazma) byla zavedena jako modifikace podání čerstvě zmrazené plazmy (ČZP), avšak mnohé studie nepotvrzují její výhodu v porovnání s ČZP. Karanténovaná ČZP je nejčastěji používaným typem plazmy při léčbě TTP, je opakovaně vyšetřována na negativitu HIV, HBV, HCV a syfilis. V České republice není rozšířeno podávání plazmy protivirově ošetřené, což je solvent-detergentní plazma, plazma ošetřená metylenovou modří, psoralenem či riboflavinem. Autoři uvádějí jednotlivé možnosti léčby pacientů s TTP a prezentují své zkušenosti v rámci souboru sedmi pacientů s hereditární formou TTP.Závěry.
U pěti pacientů jsou efektivní výměnné léčebné plazmaferézy. V empiricky nastavených intervalech je u těchto pacientů hrazeno 1,5 plazmatického volumu čerstvě zmrazenou karanténovanou plazmou, u dvou pacientek, které jsou v péči dětské kliniky, je léčba realizována infuzemi čerstvě zmrazené karanténované plazmy v intervalu 2 týdny.Klíčová slova:
trombotická trombocytopenická purpura, výměnná plazmaferéza, čerstvě zmrazená karanténovaná plazma.ÚVOD
Trombotická trombocytopenická purpura (TTP) je závažné, život ohrožující onemocnění, které je charakterizováno pentádou laboratorních a klinických příznaků: mikroangiopatická hemolytická anémie s výskytem schistocytů v periferním krevním nátěru, horečka, trombocytopenie, renální a neurologické abnormality, při čemž ne vždy se musí vyskytovat všechny příznaky (1). Etiopatogeneticky se na rozvoji onemocnění podílí deficit metaloproteázy ADAMTS13 (adisintegrin-like and metalloprotease with thrombospondin type 1 repeats 13), která je zodpovědná za proteolytické štěpení multimerů von Willebrandova faktoru (vWF). Neštěpící se multimery se váží na destičky, způsobují jejich intravaskulární agregaci a tvorbu trombů, které jsou deponovány v mikrocirkulaci pacientů (2, 3). TTP se může vyskytovat v několika formách. Hereditární forma TTP, která je velmi vzácná (2–3 % pacientů) (4), je podmíněna genetickou mutací genu pro ADAMTS13. U pacientů s touto formou onemocnění je hladina ADAMTS13 snížena na 3–5 % normálních hodnot, přičemž hodnoty proteázy kolem 10 % jsou dostačující pro štěpení multimerů (5, 6). U sekundárních forem TTP jsou za sníženou hladinu metaloproteázy zodpovědné protilátky proti ADAMTS13. Před zavedením výměnných plazmaferéz do léčby TTP se mortalita tohoto onemocnění pohybovala kolem 90 % (7). Výměnné plazmaferézy, eventuálně infuze čerstvě zmrazené plazmy (ČZP) ve většině případů navodí remisi onemocnění tím, že dodají chybějící metaloproteázu, která rozštěpí přítomné multimery. Pokud je provedena plazmaferéza, resp. série plazmaferéz, jsou navíc odstraněny přítomné protilátky (8).
Možnosti léčby jednotlivými druhy plazmy
Karanténovaná ČZP
Karanténovaná ČZP je plazma, vyrobená z plné krve jednoho dárce, anebo odebraná od jednoho dárce separátorem. Bezprostředně (do 6 hodin) po odběru je šokově zmrazena na teplotu -30 °C tak, aby byly v maximálně možné míře uchovány koagulační faktory. Takto může být plazma skladována až 36 měsíců. Během prvního půl roku povinného skladování je dárce, jehož plazma je uložena v karanténě, znovu vyšetřen na přítomnost, resp. nepřítomnost známek virového onemocnění. Povinně se vyšetřuje HIV, HBV, HCV a syfilis. Tato strategie snižuje nebezpečí, že je dárce odebírán v období tzv. diagnostického okna, kdy je virová nálož nízká a nedochází k sérokonverzi. Karanténovaná plazma je nejčastěji používaným typem plazmového transfuzního přípravku v České republice.
K-plazma (karanténovaná)
K-plazma je plazma zbavená kryoproteinu. Vyrábí se na transfuzních odděleních běžně dostupnými technikami a ve srovnání s ČZP obsahuje méně fibrinogenu, faktoru VIII, faktoru XIII a vWF. Právě snížený obsah vWF, hlavně těch molekul, které nesou velké multimery, vedlo k úvahám o preferenci tohoto typu plazmy k léčbě pacientů s TTP (9). Nicméně pozdější práce prokázaly, že pro nastolení remise onemocnění je významná hladina vWF štěpící metaloproteázy, která je přítomna v obou typech plazmy. Není proto důvod upřednostňovat podání K-plazmy před FFP (10).
Rutinní užití obou výše uvedených typů plazmy v léčbě TTP není bez komplikací. Pacientům je během jedné procedury vyměněno 1–1,5 plazmatického volumu, což představuje u 70 kg pacienta zhruba 3000 ml plazmy. Navíc je mnohdy nutno plazmaferézy provádět několik dní za sebou do dosažení remise. Aplikace velkých objemů plazmy s sebou nese riziko přenosu patogenů i výskyt nežádoucích reakcí, zejména středních až těžkých alergických reakcí a TRALI (11, 12).
Protivirově ošetřená plazma
Do této skupiny patří plazma ošetřená solvent-detergentem, plazma ošetřená metylenovou modří a plazma ošetřená psoralenem, anebo riboflavinem.
Plazma, ošetřená solvent-detergentem (SD-plazma)
Solvent-detergentem ošetřená plazma je bio-farmaceutický přípravek, který se vyrábí z poolu 100–1600 jednotek dárcovské plazmy. Solvent (tri-n-butyl phosphate) – detergent (Triton® X-100) ničí lipidové obaly virů (HIV, HBV, HCV), méně efektivně redukuje například parvovirus B19 či HAV, což jsou viry bez lipidových obalů. Poolování jednotlivých dárcovských jednotek plazmy může vést k neutralizaci protilátek a alergenů v plazmě, následně pak k významnému snížení výskytu TRALI a závažných alergických reakcí (13). Většina evropské SD plazmy se vyrábí ve frakcionačních závodech Octapharmy (Octapharma, Lachen, Švýcarsko) a je distribuována pod názvem Octaplas (14). Mnohé klinické studie potvrzují efektivní využití Octaplasu v léčbě pacientů s TTP (15, 16).
Plazma, ošetřená metylenovou modří a fotoinaktivována
Metylenová modř je barvivo fenothiazinu. Po expozici viditelným světlem generuje superoxidy, peroxid vodíku a hydroxylové radikály, které ničí virové nukleové kyseliny (17, 18). Systém je účinný pro lipidové obaly virů, méně účinný pro inaktivaci virů bez lipidových obalů (19). Nicméně, klinický efekt plazmy ošetřené metylenovou modří v porovnání s karanténovanou ČZP je menší (20).
Plazma, inaktivovaná psoralenem (systém INTERCEPT)
Plazma, inaktivovaná riboflavinem (systém MIRASOL® PRT)
Oba systémy jsou určeny pro patogenní in-house inaktivaci, tedy pro inaktivaci na transfuzních odděleních. INTERCEPT je vyráběn firmou Cerus (Cerus, USA). Pro patogenní inaktivaci využívá amotosalen-HCl (S-59) v kombinaci s ultrafialovým světlem (UVA) (21, 22). Jeho použití je schváleno pro inaktivaci patogenů v dárcovských trombocytech i plazmě. Ve vztahu k vhodnosti léčby TTP existuje dosud pouze jedna malá studie, srovnávající léčbu pacientů s TTP plazmou, ošetřenou Interceptem a karanténovanou ČZP (23). MIRASOL®PRT je vyráběn firmou CaridianBCT, Inc. (USA). Pro patogenní inaktivaci využívá riboflavin v kombinaci s UVA. Tento systém je však zatím schválen pouze pro inaktivaci patogenů v dárcovských trombocytech, inaktivace plazmy je ve stadiu preklinických zkoušek (14).
SOUBOR NEMOCNÝCH A POUŽITÉ METODY
V Krevním centru FN Ostrava je soubor sedmi pacientů s vzácnou hereditární formou TTP, chronicky léčených výměnnými plazmaferézami anebo infuzemi ČZP (tab. 1). Interval mezi jednotlivými výkony je stanoven empiricky dle počtu trombocytů, které klesají pod hodnoty pro pacienty vlastní, dlouhodobě sledované; s poklesem počtu trombocytů pod tyto hodnoty dochází k vzestupu laktát-dehydrogenázy. Intervaly plazmaferéz se pohybují mezi 3–7 týdny. V rámci jednoho výkonu je vyměněno 1,5 plazmatického objemu. Výměnné plazmaferézy jsou prováděny na separátorech Fresenius ComTec 204 (Fresenius GmbH, Německo). Pacientům je podávána karanténovaná ČZP; během jednoho výkonu je vyměněno 1,5 plazmatického objemu. Pacienti užívají před výkonem perorální antihistaminika, během výkonu je podáván bolus Solu-Medrolu. Přesto dochází k výskytu středních až závažných alergických reakcí. U tří pacientů (v tabulce 1 pod čísly 1, 2, 4) byly zaznamenány lehké až střední reakce s alergickým exantémem na horní polovině těla a s dechovými obtížemi. U dvou pacientů (v tabulce 1 pod čísly 3 a 6) došlo k těžké alergické reakci. Pacientky pod číslem 6 a 7 jsou v péči dětské kliniky FN Ostrava, je jim podávána v pravidelných intervalech (2 týdny) infuze karanténované plazmy v dávce 10 ml/kg. Dosud jsme pozorovali výskyt jedné alergické reakce u pacientky s číslem 6.
Tab. 1. Soubor pacientů s vrozenou formou TTP 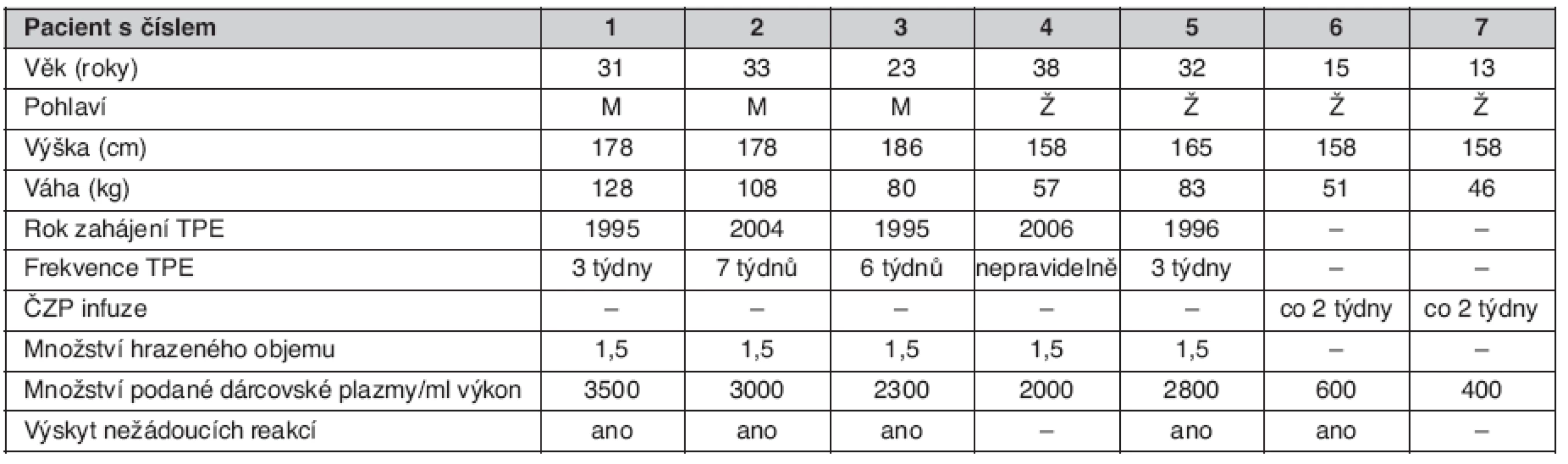
Diskuze
Ve FN Ostrava jsou léčeni pacienti s vzácnou hereditární formou trombotické trombocytopenické purpury. Všichni tito pacienti měli příznaky již v dětském období, u čtyř pacientů (1, 3, 5 a 6) se symptomy projevovaly jako relabující hemolyticko-uremický syndrom, u pacienta s číslem 2 byla první ataka ve 2 letech hodnocena jako idiopatická trombocytopenická purpura (ITP), pacientka s číslem 4 měla první ataku ve 13 letech; tato byla hodnocena jako ITP a anémie. Léčba výměnnými plazmaferézami u těchto pacientů je efektivní (24). Pacienti v našem souboru reagují na léčbu úpravou laboratorních hodnot sledovaných parametrů, především laktát-dehydrogenázy a počtu trombocytů. Nicméně léčba karanténovanou ČZP má svá úskalí, zejména v možnosti přenosu virových onemocnění a výskytu nežádoucích reakcí – alergických reakcí a TRALI. Přípravek Octaplas, který je dle závěrů mnoha zahraničních studií vhodnější a bezpečnější alternativou, je v České republice zatím nedostupný. U pacientů se závažnými alergickými reakcemi v anamnéze však předpokládáme, že budeme muset tento přípravek do budoucna zajistit.
Závěr
Karanténovaná čerstvě zmrazená plazma pro léčbu pacientů s trombotickou trombocytopenickou purpurou je léčbou dostupnou a účinnou. Dostupnost přípravku Octaplas, který je v mnoha zahraničních studiích prezentován jako bezpečnější a efektivnější přípravek, je v České republice v současné době obtížná a vzhledem k velkým objemům měněné plazmy také finančně náročná.
Zkratky
ADAMTS13 – a disintegrin-like and metalloprotease with thrombospondin type 1 repeats13
ČZP – čerstvě zmrazená plazma
FFP – fresh frozen plasma
HAV – hepatitis A virus
HBV – hepatitis B virus
HCV – hepatitis C virus
HIV – human immunodeficiency virus
ITP – idiopatická trombocytopenická purpura
K-plazma – plazma, zbavená kryoproteinu
MB – methylen blue
SD – solvent-detergent
PRT – Pathogen Reduction Technology
TRALI – transfusion-related acute lung injury
TPE – therapeutic plasma exchange
TTP – trombotická trombocytopenická purpura
vWF – von Willebrand factor
Adresa pro korespondenci:
MUDr. Zuzana Čermáková, Ph.D.
Krevní centrum FN
17. listopadu 1790, 708 52 Ostrava
fax: +420596 916 379, e-mail: zuzana.cermakova@fnspo.cz
Zdroje
1. Mannucci P, Peyvandi F. TTP and ADAMTS13: When Testing is Appropriate? Hematology Am Soc Hematol Educ Program 2007; 1 : 121–126.
2. Moake JL, Rudy CK, Troll JH, et al. Unusually large plasma factor VIII: von Willebrand factor multimers in chronic relapsing thrombotic thrombopenic purpura: N Engl J Med. 1982; 307: 1432–1435.
3. Moake JL, Turner NA, Stathopoulos NA, Nolasco LH, Hellums JD. Involvement of large plasma von Willebrand factor (vWF) multimers and unussually large vWF forms derived from endothelial cells in shear stress-induced platelet aggregation. J Clin Invest 1986; 78 : 1456–1461.
4. Levy GG, Nichols WC, Lian EC, Foroud T, McClintick JN, Mc Gee BM, Yang AY, Siemieniak DR, Stark KR, Gruppo R, Sarode R, Shurin SB, Chandrasekaran V, Stabler SP, Sabio H, Bouhassira EE, Upshaw JD Jr, Ginsburd D, Tsai HM. Mutations in a member of the ADAMTS gene family cause thrombotic thrombocytopenic purpura. Nature 2001; 413 : 488–494.
5. Furlan M, Lämmle B. Aetiology and pathogenesis of thrombotic thrombocytopenic purpura and haemolytic uraemic syndrome: the role of von Willebrand factor – cleaving protease. Best Pract Res Clin Haematol 2001; 14 : 437–454.
6. Barbot J, Costa E, Guerra M, et al. Ten years of prophylactic treatment with fresh-frozen plasma in a child with chronic relapsing thrombotic thrombocytopenic purpura as a result of congenital deficiency of vonWillenbrand factor-cleaving protease. Br J Haematol 2001; 113 : 649–651.
7. Amorosi EL, Ultmann JE. Thrombotic thrombocytopenic purpura: report of 16 cases and review of the literature. Medicine 1966; 45 : 139–159.
8. Rock G. The management of thrombotic thrombocytopenic purpura in 2005. Semin Thromb Hemost 2005; 31 : 709–716.
9. Rock G, Shumak KH, Sutton DM, BuskardNA, Nair, RC. Cryosupernatant as replacement fluid for plasma exchange in thrombotic thrombocytopenic purpura. Members of the Canadian Apheresis Group. Br J Haematol 1996; 94 : 383–386.
10. Zeigler ZR, Shadduck RK, Gryn JF, Rintels PB, George JN, Besa EC, Bidensteiner D, Silver B, Kramer RE. Cryoprecipitate poor plasma does not improve early response in primary adult thrombotic thrombocytopenic purpura (TTP). North American TTP GrouP. J Clin Apher 2001; 16 : 19–22.
11. Mintz PD, Neff A, MacKenzie M, Goodnough LT, Hillyer Ch, Kessler C, McCrae K, Menitove JE, Skikne BS, Damon L, Lopez-Plaza I, Rouault Ch, CrookstonKP, Benjamin, RJ, George J, Lin JS, Corash L, Conlan MG. A randomized controlled Phase III trial of therapeutic plasma exchange with fresh-frozen plasma (FFP) prepared with amotosalen and ultraviolet A light compared to untreated FFP in thrombotic thrombocytopenic purpura. Transfusion 2006; 46 : 1693–1704.
12. Helltern, P. Fresh-frozen plasma, pathogen-reduced single-donor plasma or bio-pharmaceutical plasma. Transf and Aph J 2008; 39 : 69–74.
13. Andreu G. Transfusion-associated circulatory overload and transfusion-related acute lung injury: diagnosis, pathophysiology, management and prevention. Vox Sang 2009; 4 : 63–71.
14. Solheim BG, Seghatchan J. Update on pathogen reduction technology for therapeutic plasma: an overview. Transf and Aph Sci 2006; 35 : 83–90.
15. Pereira A. Efficacy of different plasma sources in threatment of thrombotic thrombocytopenic purpura. Vox Sang 2009, 4 : 111–117. ISBT Science Series (2009).
16. Hellestern P. Haubelt H. Manufacture and composition of fresh frozen plasma and virus inactivated therapeutic plasma preparations: correlation between composition and therapeutic efficacy. Thromb Res 2002; 31: S3–S8.
17. Hellestern P. Solvent/detergent-treated plasma: composition, efficacy and safety. Curr Opin Hematol 2004; 11 : 346–350.
18. Chapman J. Virus inactivation of plasma by methylene blue photoinactivation: approaches and toxicology. Transfus Today 1994; 20 : 2–4.
19. Mohr H, Lambrecht B, Selz A. Photodynamic virus inactivation of blood components. Immunol Invest 1995; 24 : 73–85.
20. Williamson LM, Cardigan R, Prowse Ch. Methylene blue-treated fresh-frozen plasma:what is its contribution to blood safety? Transf 2003; 436 : 1322–1329.
21. del Río-Garma J, Alvarez-Larrán A, Martínez C, Muncunill J, Castellá D, de la Rubia J, Zamora C, Corral M, Viejo A, Peňa F, Rodríguez-Vincente P, Contrera, E, Arbona C, Ramírez C, Garcia-Erce J,A, Alegre A, Mateo J, Pereira, A. Methylene blue-photoinactivated plasma versus quarantine fresh frozen plasma in thrombotic thrombocytopenic puprura: a multicentric, prospective cohort study. Br J Haematol 2008; 143 : 39–45.
22. Janetzko K, Lin L, Eichler H, Mayaudon V, Flamen J, Klüter H. Implementation of the INTERCEPT Blood System for Platelets into routine blood bank manufacturing procedures: evaluation of apheresis platelets. Vox Sang 2004; 86 : 239–245.
23. Mintz PD, Neff A, MacKenzie M, Goodnough LT, Hillyer C, Kessler C, McCrae K, Menitove JE, Skikne BS, Damon LI, Lopez-Plaza I, Rouault C, Crooston KP, Benjamin RJ, George J, Lin.JS Corash L, Conlan MG. A randomized, controlled Phase III trial of therapeutic plasma exhange with fresh-frozen plasma (FFP) prepared with amotosalen and ultraviolet A light compared to untreated FFP in thrombotic thrombocytopenic purpura. Transf 2006; 46 : 1693–1704.
24. Čermáková Z, Hrdličková R, Šuláková T, Kořístka M, Kovářova P, Hrachovinová I. Thrombotic thrombocytopenic purpura: Incidence of congenital form of disease in North Moravia (Region Moravia-Silesia). Prague Medical Report 2009; v tisku.
Štítky
Adiktologie Alergologie a imunologie Anesteziologie a resuscitace Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská dermatologie Dětská gastroenterologie Dětská gynekologie Dětská chirurgie Dětská kardiologie Dětská nefrologie Dětská neurologie Dětská onkologie Dětská otorinolaryngologie Dětská pneumologie Dětská psychiatrie Dětská radiologie Dětská revmatologie Dětská urologie Diabetologie Endokrinologie Farmacie Farmakologie Fyzioterapie Gastroenterologie a hepatologie Genetika Geriatrie a gerontologie Gynekologie a porodnictví Hematologie a transfuzní lékařství Hygiena a epidemiologie Hyperbarická medicína Chirurgie cévní Chirurgie hrudní Chirurgie plastická Chirurgie všeobecná Infekční lékařství Intenzivní medicína Kardiochirurgie Kardiologie Logopedie Mikrobiologie Nefrologie Neonatologie Neurochirurgie Neurologie Nukleární medicína Nutriční terapeut Obezitologie Oftalmologie Onkologie Ortodoncie Ortopedie Otorinolaryngologie Patologie Pediatrie Pneumologie a ftizeologie Popáleninová medicína Posudkové lékařství Praktické lékařství pro děti a dorost Protetika Psychologie Radiodiagnostika Radioterapie Rehabilitační a fyzikální medicína Reprodukční medicína Revmatologie Sestra Sexuologie Soudní lékařství Stomatologie Tělovýchovné lékařství Toxikologie Traumatologie Urgentní medicína Urologie Laboratoř Domácí péče Foniatrie Algeziologie Zdravotnictví Dentální hygienistka Student medicíny
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
-
Všechny články tohoto čísla
- Specializační vzdělávání lékařů v České republice
- Personalizovaná medicína – genomická fáze Proč a zač
- Nízko-molekulárne heparíny a ich neantitrombotické účinky na hojenie rán
- Spolek lékařů českých
- Kompliance v psychiatrii
- Možnosti léčby plazmou u pacientů s hereditární formou trombotické trombocytopenické purpury
- Podávání intravenózního železa v bezkrevní medicíně
- Oceněné vědecké práce za rok 2008
- Pomoc manželkám mužů závislých na alkoholu
- Historie a současnost registrace vrozených vad v České republice
- Popis a funkce lipidových raftů
- Průkaz lipidových raftů na buněčné membráně
- Žírné buňky v nádoru
- Výuka humanitních věd na lékařských fakultách v České republice IX. sympozium lékařských fakult ČR Praha, 18. února 2009
- VIII. setkání dětských alergologů a klinických imunologůKrahulčí u Telče, 19.–21. června 2009
- XX. kongres ČLS JEP pro lékaře v praxi s mezinárodní účastí Brno, 21. října 2009
- Regionální pracovní den pro management klinických laboratoří Olomouc, 10. září 2009
- Helsinská deklarace Světové lékařské asociace (WMA)
- Laureáti Nobelovy ceny
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Podávání intravenózního železa v bezkrevní medicíně
- Helsinská deklarace Světové lékařské asociace (WMA)
- Nízko-molekulárne heparíny a ich neantitrombotické účinky na hojenie rán
- Kompliance v psychiatrii
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



