-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Je dosažení nedetekovatelné minimální zbytkové nemoci optimálním cílem léčby CLL?
Venetoklax či jeho kombinace s anti-CD20 protilátkami obnovily význam minimální reziduální nemoci (MRN) v léčbě CLL, když studie MURANO ukázala, že dosažení nedetekovatelné MRN (uMRN) na konci této léčby je spojené s prodloužením přežití bez progrese (PFS) a celkového přežití (OS). Nové práce se zaměřují na hledání optimální kombinované léčby s venetoklaxem v léčbě CLL. Příznivých výsledků je dosahováno při jeho podávání spolu s obinutuzumabem a ibrutinibem. Studie CAPTIVATE v současné době hodnotí režim venetoklax + ibrutinib v 1. linii léčby mladších nemocných s CLL i pokračující terapii dle dosažení uMRN.
Význam MRN při léčbě CLL v éře chemoimunoterapie a v éře cílené léčby
Názor na význam minimální reziduální nemoci (MRN) u chronické lymfocytární leukémie (CLL) se neustále mění a přizpůsobuje novým poznatkům. V éře chemoimunoterapie byla MRN klíčovým ukazatelem přežití bez progrese (PFS).
Studie CLL1 porovnávala režimy chemoterapie R-CLB (rituximab + chlorambucil) a G-CLB (obinutuzumab + chlorambucil) v 1. linii léčby CLL u starších nemocných. U pacientů léčených G-CLB bylo dosažení nedetekovatelné MRN (uMRN) spojeno s významně delším PFS.1 Dosažení uMRN bylo využito k optimalizaci chemoimunoterapie.
V irské studii CTRIAL-IE byla u pacientů s CLL po 4 cyklech léčby režimem FCR (fludarabin + cyklofosfamid + rituximab) při dosažení kompletní remise s negativitou MRN terapie ukončena, ostatní pacienti pokračovali ještě 2 cykly chemoimunoterapie. PFS bylo u pacientů s dosažením uMRN po 4 cyklech a u těch, kteří dosáhli uMRN až po 6 cyklech, srovnatelné.2 To je důležité zjištění vzhledem k toxicitě léčby a možnosti jejího dřívějšího ukončení.
Poté přišla éra cílené terapie, kdy kontinuální terapie inhibitory Brutonových kináz (BTKi) v 1. linii léčby CLL přinesla dlouhodobou účinnost i bez nutnosti dosažení negativity MRN, což dokládají například výsledky 8letého PFS a celkového přežití (OS) s ibrutinibem v porovnání s chlorambucilem ve studii RESONATE 2.3
Ibrutinib prokázal přínos také u relabující/refrakterní CLL (R/R CLL), i když prodloužení PFS nebylo v porovnání s kombinací rituximab + idelalisib tak výrazné jako v 1. linii.4 Jednou z nevýhod kontinuální terapie je ovšem výskyt nežádoucích účinků, které často vedou k předčasnému ukončení léčby. Vysazení ibrutinibu z důvodu toxicity bylo v české studii během 34 měsíců sledování zjištěno u 22,5 % pacientů s R/R CLL.4
Jaké důkazy máme o významu MRN v éře cílené léčby kinázovými inhibitory?
Průkopníkem v léčbě CLL s předem stanovenou délkou podávání bez cytostatik je venetoklax.
Data ze studie MURANO u pacientů s R/R CLL ukazují, že i v případě velmi nepříznivých prognostických ukazatelů, jakými jsou del(17p13.1), del(11q22.3), trisomie 12, del(13q14), je možné dosahovat hlubokých remisí. Nedetekovatelné MRN bylo při léčbě venetoklaxem + rituximabem dosaženo u 46,2–77,5 % pacientů s těmito mutacemi, u ostatních bylo uMRN dosaženo v 91,7 % případů.5 Délka PSF významně korelovala s hloubkou remise. Nedetekovatelná MRN na konci kombinované terapie byla spojená s významně delším PFS: 18měsíční PFS činilo 90,3 % u pacientů s uMRN, 64,4 % u pacientů s nízkou pozitivitou MRN a 8,33 % u nemocných s vysokou pozitivitou MRN.5
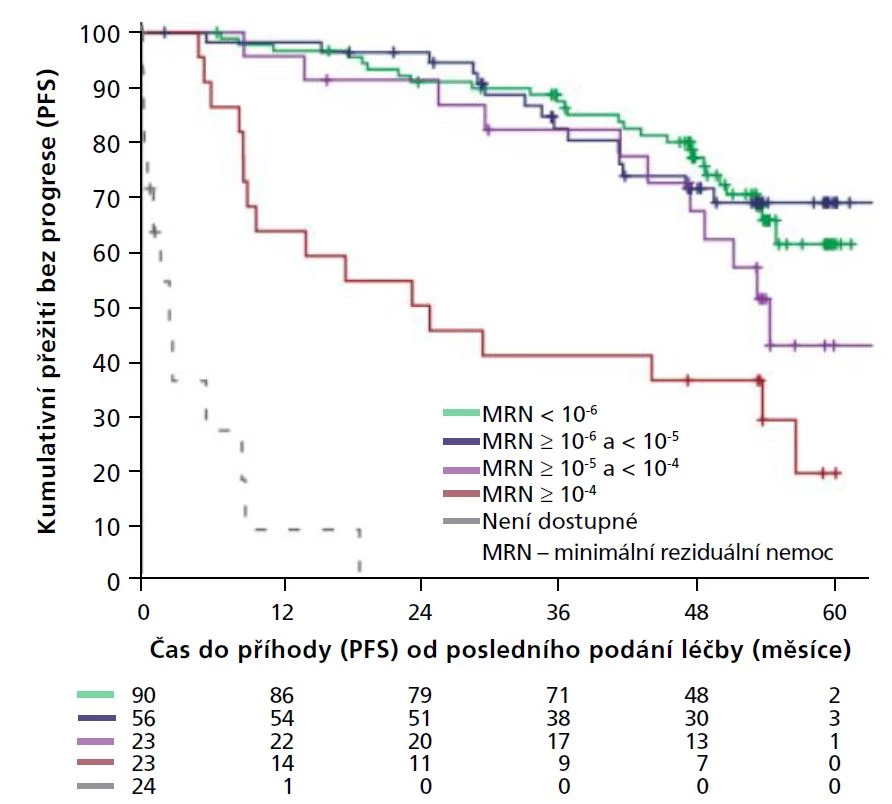
Dosažení uMRN v 1. linii léčby CLL venetoklaxem + obinutuzumabem hodnotila studie CLL14. Využila k tomu vyšetření periferní krve pomocí sekvenování nové generace (NGS).6 Stav MRN na konci léčby koreloval s PFS. Bylo zjištěno, že pozitivita MRN (≥ 10–4) je spojena s vyšší expresí genu ABCB1 (MDR1) a dosažení uMRN (< 10–6) s genem BCL2L11 (BIM).6
Obr. PFS dle MRN u pacientů s CLL léčených v 1. linii venetoklaxem + obinutuzumabem ve studii CLL146
MRN při kombinované léčbě s venetoklaxem – pohled do budoucnosti
Na hledání optimálního režimu s venetoklaxem v 1. linii léčby CLL se zaměřila studie CLL13.7 Randomizovala 926 pacientů s CLL v dobrém výkonnostním stavu (s vyloučením nemocných s del(17p)/mutací TP53) do 4 ramen: s chemoimunoterapií (CIT) zahrnující FCR nebo BR (bendamustin + rituximab) v 6 cyklech, s venetoklaxem podávaným ve 12 cyklech, a to v kombinaci s rituximabem (VenR) v 6 cyklech nebo s obinutuzumabem (VenG) v 6 cyklech nebo s obinutuzumabem v 6 cyklech + ibrutinibem ve 12 cyklech (při přetrvávající MRN až v 36 cyklech). Primární sledované parametry zahrnovaly podíl pacientů s uMRN (< 10–4) v periferní krvi po 15 měsících (VenG vs. CIT) a PFS (VenG + ibrutinib vs. CIT). Výsledky ukázaly, že významně lepších výsledků je dosaženo při kombinaci venetoklaxu s obinutuzumabem. Podíl pacientů s uMRN činil po 15 měsících 92,2 % ve skupině VenG + ibrutinib, 86,5 % s VenG, 57 % s VenR a 52 % s CIT.7
Do studie fáze III GLOW byli zařazeni pacienti s CLL vyššího věku nebo s komorbiditami. V 1. linii dostávali venetoklax v kombinaci s ibrutinibem nebo chlorambucil s obinutuzumabem (G-CLB). Na konci léčby byla pomocí NGS zjištěna uMRN v periferní krvi u 54,7 % pacientů s venetoklaxem + ibrutinibem v porovnání s 39 % s G-CLB.8 Negativita MRN v kostní dřeni činila v těchto terapeutických skupinách 51,9 vs. 17,1 %. I střední hloubka odpovědi na venetoklax + ibrutinib byla spojená s častějším přetrváváním odpovědi než u CIT. Vliv na dosažení a dynamiku uMRN má přítomnost mutace IGHV. Pacienti s touto mutací dosáhli uMRN méně často (na konci léčby ve 40,6 % oproti 59,7 % u pacientů bez mutace IGHV), ale dosažená odpověď u nich přetrvávala déle (na konci sledování mělo uMRN 43,8 % pacientů s mutací IGHV oproti 35,8 % bez ní).8 Tato práce ukázala významně delší PFS při léčbě kombinací venetoklax + ibrutinib bez ohledu na stav MRN na konci léčby. Pacienti s venetoklaxem + ibrutinibem s uMRN i s MRN ≥ 10–4 na konci léčby měli delší PFS než pacienti s G-CLB s uMRN.9
Režim venetoklax + ibrutinib v 1. linii léčby mladších nemocných (< 70 let) s CLL je hodnocen v registrační studii CAPTIVATE. Po 12 cyklech terapie jsou pacienti randomizováni k dalšímu podávání ibrutinibu nebo placeba, pokud u nich bylo dosaženo uMRN, a to za dvojitě zaslepených podmínek a po stratifikaci dle mutace IGHV, nebo k dalšímu podávání ibrutinibu + venetoklaxu či samotného ibrutinibu, pokud uMRN dosaženo nebylo; v tomto rameni za otevřených podmínek.10 Dosažené výsledky v kohortě s uMRN jsou tak příznivé, že na závěr ukazující významné rozdíly po podávání ibrutinibu nebo placeba bude třeba čekat déle. Pacienti, kteří po 12 cyklech léčby venetoklaxem + ibrutinibem dosáhli uMRN, mají při pokračující léčbě ibrutinibem 100% roční přežití bez progrese (DFS), při pokračujícím podávání placeba činí roční DFS 95,3 %.10
Závěr
Chemoimunoterapie umožnila v léčbě CLL dosáhnout hlubokých remisí, což vedlo k významnému prodloužení PFS pacientů. Význam dosažení negativity MRN přechodně zpochybnilo zavedení kontinuální cílené léčby inhibitory BCRi. Venetoklax či jeho kombinace s anti-CD20 protilátkami význam MRN opět obnovil, když bylo zjištěno, že dosažení nedetekovatelné MRN na konci této léčby je spojené s prodloužením PFS a OS. Dosažení uMRN je žádoucím výsledkem terapie CLL, ale definitivní úloha MRN zatím nebyla určena. Podle MRN není v současné době možné řídit délku terapie CLL cílenými inhibitory ani určit, kdy zahájit další linii léčby.
MUDr. Martin Šimkovič, Ph.D.
IV. interní hematologická klinika LF UK a FN Hradec KrálovéLiteratura:
1. Goede V, Fischer K, Busch R et al. Obinutuzumab plus chlorambucil in patients with CLL and coexisting conditions. N Engl J Med 2014; 370 (12): 1101–1110.
2. Appleby N, O'Brien D, Quinn FM et al. Risk adjusted therapy in chronic lymphocytic leukemia: a phase II cancer trials Ireland (CTRIAL-IE [ICORG 07-01]) study of fludarabine, cyclophosphamide, and rituximab therapy evaluating response adapted, abbreviated frontline therapy with FCR in non-del(17p) CLL. Leuk Lymphoma 2018; 59 (6): 1338–1347.
3. Barr PM, Owen C, Robak T et al. Up to 8-year follow-up from RESONATE-2: first-line ibrutinib treatment for patients with chronic lymphocytic leukemia. Blood Adv 2022 Jun 14; 6 (11): 3440–3450.
4. Špaček M, Smolej L, Šimkovič M et al.; Czech CLL Study Group. Idelalisib plus rituximab versus ibrutinib in the treatment of relapsed/refractory chronic lymphocytic leukaemia: a real-world analysis from the Chronic Lymphocytic Leukemia Patients Registry (CLLEAR). Br J Haematol 2023 Mar 27, doi: 10.1111/bjh.18736.
5. Kater AP, Wu JQ, Kipps T et al. Venetoclax plus rituximab in relapsed chronic lymphocytic leukemia: 4-year results and evaluation of impact of genomic complexity and gene mutations from the MURANO phase III study. J Clin Oncol 2020; 38 (34): 4042–4054.
6. Al-Sawaf O, Zhang C, Jin HY et al. Transcriptomic profiles and 5-year results from the randomized CLL14 study of venetoclax plus obinutuzumab versus chlorambucil plus obinutuzumab in chronic lymphocytic leukemia. Nat Commun 2023 Apr 18; 14 (1): 2147.
7. Eichhorst B, Niemann CU, Kater AP et al; GCLLSG, the HOVON and Nordic CLL Study Groups, the SAKK, the Israeli CLL Association, and Cancer Trials Ireland. First-line venetoclax combinations in chronic lymphocytic leukemia. N Engl J Med 2023 May 11; 388 (19): 1739–1754.
8. Kater AP, Owen C, Moreno C et al. Fixed-duration ibrutinib-venetoclax in patients with chronic lymphocytic leukemia and comorbidities. NEJM Evid 2022; 1 (7), doi: 10.1056/EVIDoa2200006.
9. Niemann C. New results from the phase 3 GLOW study of fixed-duration treatment with IMBRUVICA® (ibrutinib) plus venetoclax demonstrate robust efficacy and sustained response in older, unfit patients with previously untreated chronic lymphocytic leukemia. ASH 2022.
10. Wierda WG, Barr PM, Siddiqi T. Fixed-duration (FD) ibrutinib (I) + venetoclax (V) for first-line (1L) treatment (Tx) of chronic lymphocytic leukemia (CLL)/small lymphocytic lymphoma (SLL): three-year follow-up from the FD cohort of the phase 2 CAPTIVATE study. J Clin Oncol 2022; 40 (16_suppl.): 7519.Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




