-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaMetastazektomie při 2. linii paliativní chemoterapie metastatického kolorektálního karcinomu – kazuistika
21. 4. 2020
ÚVOD
Kolorektální karcinom je jednou z nejčastějších onkologických diagnóz v České republice – nachází se na 2. místě hned za karcinomem prostaty u mužů a karcinomem prsu u žen. Léčba kolorektálního karcinomu zahrnuje široké spektrum modalit: terapii chirurgickou, systémovou (chemoterapii a biologickou terapii), radioterapii a intervenční radiologii.
V následující kazuistice bych chtěla vyzdvihnout význam multimodální léčby a také důležitost prediktivní patologie při výběru terapie. Zásadními faktory prediktivní patologie při léčbě kolorektálního karcinomu IV. stadia patří především lokalizace a RAS status. U následující pacientky se jedná o kombinaci pravostranné lokalizace a wild type RAS statusu.POPIS PŘÍPADU
55leté pacientce byl v květnu 2018 diagnostikován pravostranný kolorektální karcinom, pro který byla na začátku června téhož roku operována. Byla provedena pravostranná hemikolektomie, histologicky byl nález uzavřen jako adenokarcinom colon ascendens pT3 pN2b M0, RAS wild type.
InzercePacientka byla v regionálním onkologickém centru (ROC) indikována k podávání 6měsíční adjuvantní chemoterapie, avšak pro astenii byl zvolen režim FUFA de Grammont. Vzhledem ke zlepšení stavu byla chemoterapie od 6. cyklu změněna na mFOLFOX, přičemž hematotoxicita vedla ke snížení dávky oxaliplatiny a následně musela být ze stejného důvodu adjuvantní chemoterapie po 11. cyklu ukončena (prosinec 2018).
Velmi brzy po ukončení adjuvantní léčby však došlo k recidivě onemocnění. Na restagingovém CT v dubnu 2019 byly popsány celkem 4 metastatické léze na játrech, které byly potvrzeny i na MRI provedeném o měsíc později. Pacientka byla referována na vyšším pracovišti k resekci jaterních metastáz, ovšem dle onkoboardu nebyl nález k metastazektomii indikovaný. Pro neoperabilitu nálezu bylo doporučeno zahájit paliativní chemoterapii a v případě regrese onemocnění opět posoudit chirurgické řešení.
Pacientka zahájila v červnu 2019 na spádovém pracovišti 1. linii paliativní chemoterapie v režimu FOLFOX a následně byla předána na naše pracoviště k podávání biologické léčby. Vzhledem k pravostranné lokalizaci tumoru byla indikována k léčbě bevacizumabem. Terapie byla tolerována téměř bez obtíží, až na epizodu neutropenie stupně 4 před podáním posledního cyklu.
V srpnu 2019 bylo provedeno CT vyšetření ke zhodnocení efektu léčby, kde byla popsána velikostní progrese jaterních metastáz, dále bylo CT bez nálezu jiných nových ložisek. Jako 2. linii paliativní terapie jsme zvolili režim FOLFIRI + anti-EGFR protilátku panitumumab. Pro neutropenii stupně 4 při posledním cyklu předchozí linie léčby jsme pacientku nově zajistili G-CSF preparáty. Dále byl průběh léčby neproblematický, bez dalších epizod neutropenie.
Obr. CT jaterních metastáz – před 1. a 2. linií paliativní léčby (duben a srpen 2019)
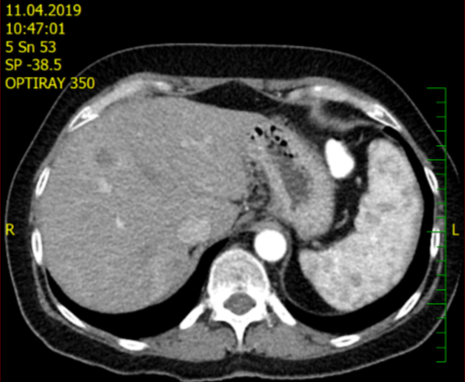
Efekt terapie byl znovu hodnocen v prosinci 2019, kdy byl nález na CT uzavřen jako stabilizace onemocnění. Vzhledem k vysoké agresivitě tumoru a otazné délce efektu léčby do budoucna jsem se rozhodla pacientku znovu referovat k jaterní metastazektomii na jiném pracovišti, i přes nesplnění původní podmínky zmenšení nálezu. Pacientka byla schválena k operačnímu výkonu a v únoru 2020 byla provedena kompletní resekce všech 4 jaterních metastáz.
Pacientka je nyní zbavena všech aktivních ložisek choroby, a proto byla dále indikována k 6měsíční pseudoadjuvantní chemoterapii kapecitabinem. Tento režim jsme vybrali s ohledem na fakt, že kombinace s oxaliplatinou při podávání 1. linie vedla k progresi onemocnění. Přínos irinotekanu v adjuvantní terapii nebyl prokázán, naopak u něj byla popsána vysoká – dokonce i letální – toxicita (1). Perioperační podávání anti-EGFR léčby po jaterní metastazektomii taktéž nepřineslo žádný benefit (2). První cyklus terapie kapecitabinem pacientka zahájila v březnu 2020.
DISKUZE A ZÁVĚR
V rámci tohoto případu bylo u pacientky několik zásadních aspektů, které mohly léčbu zkomplikovat.
Prvním aspektem byl stav nemocné po resekčním výkonu, kdy byla pro astenii hraničně únosná k zahájení adjuvantní chemoterapie. Proto je velmi důležitá podpůrná léčba a také management nežádoucích účinků, což v tomto případě zlepšilo stav pacientky natolik, aby mohla podstupovat systémovou terapii a byla později v dostatečné kondici k operačnímu výkonu.
Dalším aspektem byly charakteristiky tumoru, tedy pravostranná lokalizace a wild type RAS status, které mohly způsobit rozpor při výběru paliativní chemoterapie. Pro 1. linii byla zvolena biologická léčba s ohledem na lokalizaci tumoru. Po rychlé progresi onemocnění jsme zvolili režim FOLFIRI + panitumumab s cílem zmenšení choroby před zvažovanou metastazektomií (3) navzdory tomu, že některé publikace zastávají názor, že pravostranné kolorektální karcinomy jsou vůči anti-EGFR terapii často rezistentní (4).
Posledním aspektem, který v úspěchu onkologické léčby této pacientky hrál roli, je subjektivita při rozhodování o operabilitě (5). Efekt léčby a množství vyčerpaných terapeutických možností mohou hrát zásadní roli při náhledu na pacienta v různých okamžicích jeho onemocnění. Proto je zásadní nepovažovat status neoperability za definitivní ortel. U kolorektálního karcinomu byl prokázán zásadní efekt resekce nádorových ložisek i při generalizovaném onemocnění. Celkové přežití (OS) bylo prodlouženo ve srovnání s chorobou neresekovanou z 30,8 na 51,3 měsíce (6). Zda byla resekce provedena po 1., či po 2. linii paliativní chemoterapie, nemělo na výsledné OS žádný vliv (7).
Nyní je pacientka na adjuvantní terapii a i při nepříznivém scénáři, tedy relapsu onemocnění, máme opět v záloze léčebné možnosti, které bychom v případě pokračování samotné systémové léčby pravděpodobně brzy vyčerpali do nuly.
MUDr. Kateřina Šašková
Onkologická klinika 2. LF UK a FN Motol v Praze
Literatura:
- Saltz L. B., Niedzwiecki D., Hollis D. et al. Irinotecan fluorouracil plus leucovorin is not superior to fluorouracil plus leucovorin alone as adjuvant treatment for stage III colon cancer: results of CALGB 89803. J Clin Oncol 2007; 25 (23): 3456–3461, doi: 10.1200/JCO.2007.11.2144.
- Bridgewater J. A., Pugh S. A., Maishman T. et al. Systemic chemotherapy with or without cetuximab in patients with resectable colorectal liver metastasis (New EPOC): long-term results of a multicentre, randomised, controlled, phase 3 trial. Lancet Oncol 2020; 21 (3): 398–411, doi: 10.1016/S1470-2045(19)30798-3.
- Carrato A., Abad A., Massuti B. et al. First-line panitumumab plus FOLFOX4 or FOLFIRI in colorectal cancer with multiple or unresectable liver metastases: a randomised, phase II trial (PLANET-TTD). Eur J Cancer 2017; 81 : 191–202, doi: 10.1016/j.ejca.2017.04.024.
- Petruželka L a kol. Kolorektální karcinom. Farmakon Press, Praha, 2018.
- Broc G., Gana K., Denost Q., Quintard B. Decision-making in rectal and colorectal cancer: systematic review and qualitative analysis of surgeons' preferences. Psychol Health Med 2017; 22 (4): 434–448, doi: 10.1080/13548506.2016.1220598.
- Modest D. P., Denecke T., Pratschke J. et al. Surgical treatment options following chemotherapy plus cetuximab or bevacizumab in metastatic colorectal cancer-central evaluation of FIRE-3. Eur J Cancer 2018; 88 : 77–86, doi: 10.1016/j.ejca.2017.10.028.
- Adam R., Yi B., Innominato P. F. et al. Resection of colorectal liver metastases after second-line chemotherapy: is it worthwhile? A LiverMetSurvey analysis of 6415 patients. Eur J Cancer 2017; 78 : 7–15, doi: 10.1016/j.ejca.2017.03.009.
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Štítky
Onkologie Radioterapie
Nejnovější kurzy
Autoři: MUDr. Karolína Svobodová
Přejít do kurzů
Nejčtenější tento týden Celý článekPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




