-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Neurotoxicita jako nežádoucí účinek Nivolumabu
9. 12. 2019
Aneta Kyllarová, Mária Hanišová, Jindřich Kopecký Klinika onkologie a radioterapie FN Hradec Králové
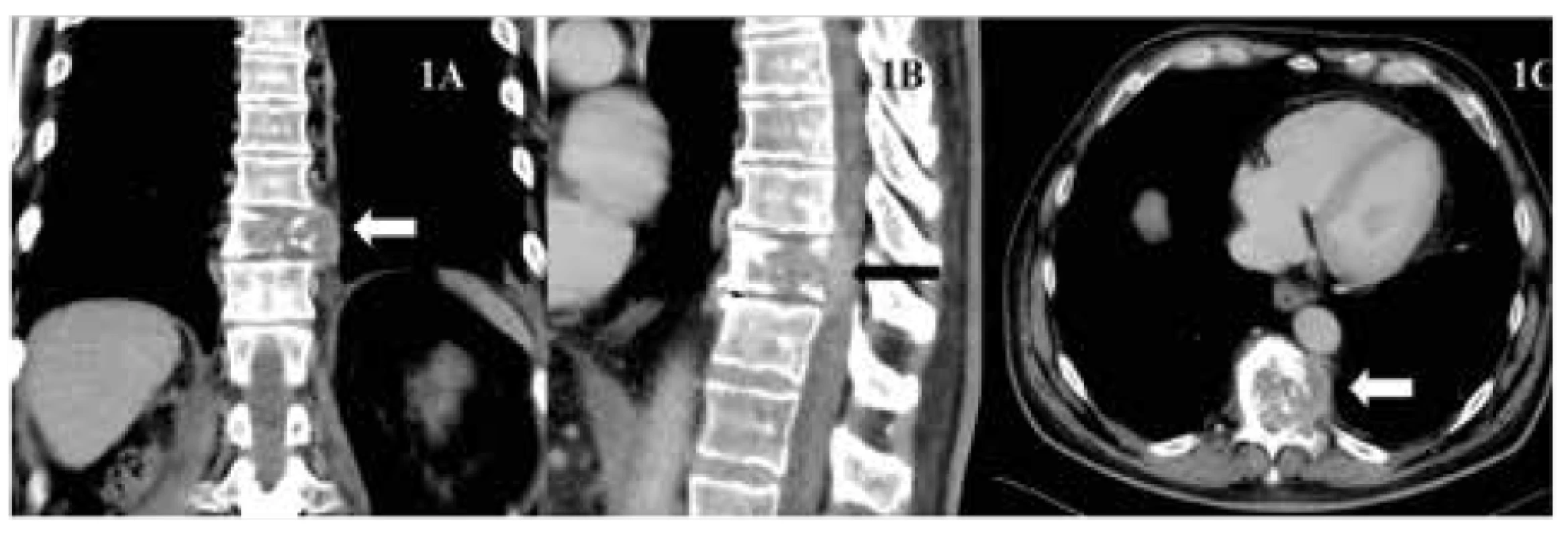
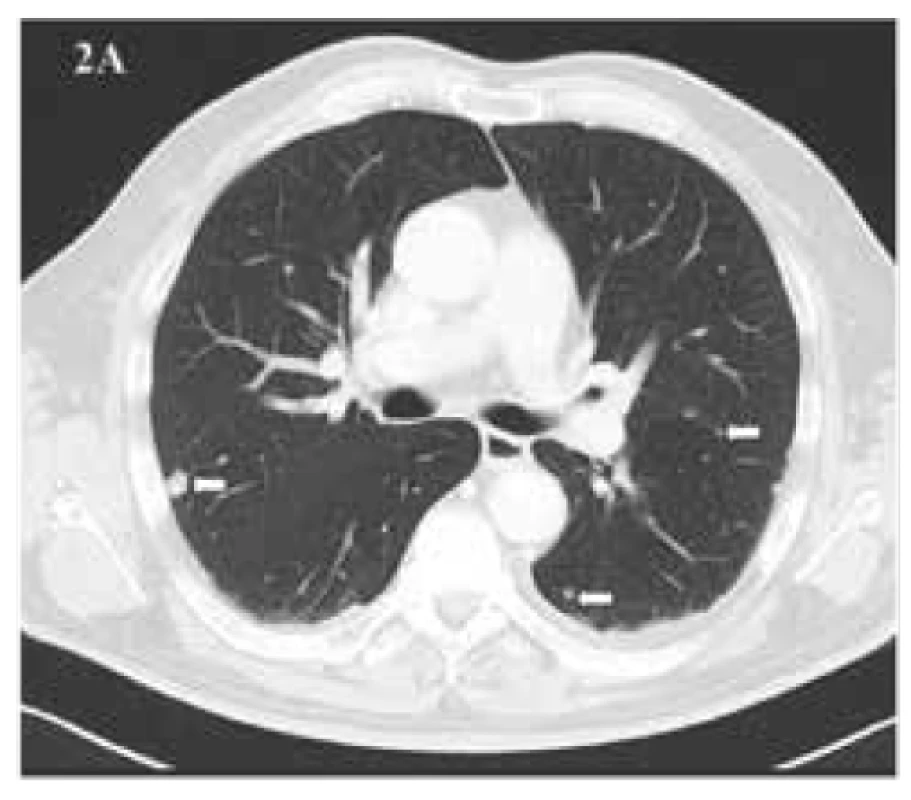
63letý pacient podstoupil v prosinci roku 2015 cytoredukční výkon pro tumor ledviny vpravo s radiologicky potvrzenou generalizací do skeletu v oblasti 11. hrudního obratle a mnohočetně do plic (obr. 1, 2). Histologicky byl verifikován světlobuněčný karcinom grade 3 až 4 s okrsky sarkomatoidní diferenciace.
InzerceOd prosince 2015 do dubna 2016 byl pacient léčen v rámci 1. linie sunitinibem, v dávce 50 mg denně v režimu 4+2. Pro horší toleranci (nevolnosti, anorexii) bylo schéma léčby změněno na 2+1. Současně s cílenou terapií byl pacient léčen od února 2016 denosumabem. Již v rámci prvního restagingového vyšetření v dubnu 2016 byla popsána progrese jak velikosti, tak i počtu metastatických ložisek v plicích.
Pro progredující bolesti v oblasti zad byla opakovaně upravována analgetická medikace s nutností podávání opiátů a následně i aplikací analgetické radioterapie na oblast Th 9–12 v celkové dávce 20 Gy za hospitalizace. Tato hospitalizace byla komplikována průjmy, kdy byla opakovaně vyloučena jakákoliv infekční etiologie s dobrou odpovědí na antidiaroika a probiotika.
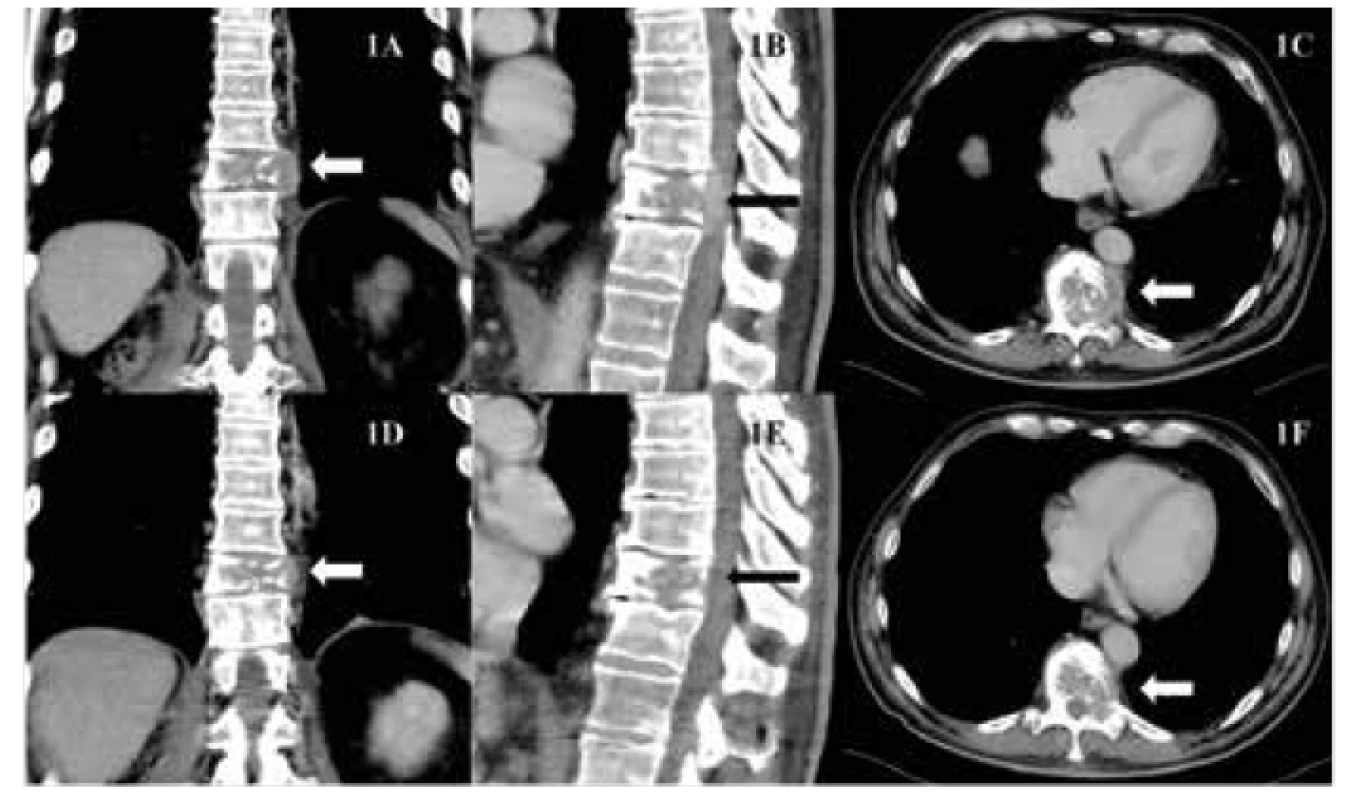
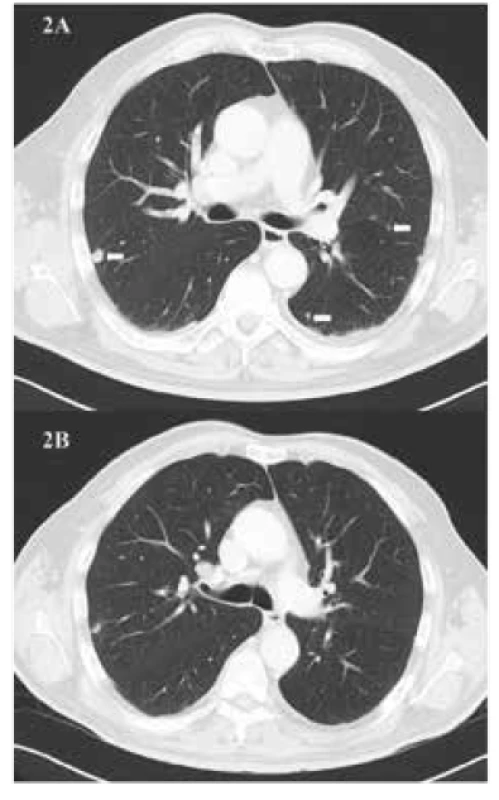
Od května 2016 byl pacient léčen v rámci specifického léčebného programu nivolumabem v dávce 300 mg každé dva týdny. Pacient absolvoval všech šest dávek nivolumabu bez jakýchkoliv klinických či laboratorních známek imunitně podmíněných nežádoucích účinků. Během léčby naopak došlo k postupnému zmírnění bolestí zad, což umožnilo redukci dávek opiátů. Na kontrolním CT vyšetření, provedeném po aplikaci 6. dávky nivolumabu v červenci 2016, byla nově popsána fraktura obratového těla Th 11 s regresí velikosti měkotkáňové expanze do durálního vaku a parciální regrese velikosti plicních ložisek (obr. 3, 4).
14 dní po podání poslední dávky nivolumabu byl pacient vyšetřován pro postupně progredující nespecifické obtíže, jako motání hlavy, neklid a občasné nekontrolovatelné pohyby. Kontrolní laboratorní výsledky nevykazovaly jakékoliv anomálie. Z chronické medikace pacient v době objevení se obtíží užíval pouze transdermální fentanyl. V rámci restagingu bylo doděláno i CT hlavy, které neprokázalo ložiskové postižení mozku. Klinický stav pacienta byl neurologem uzavřen jako stav generalizované dyskineze typu chorey.
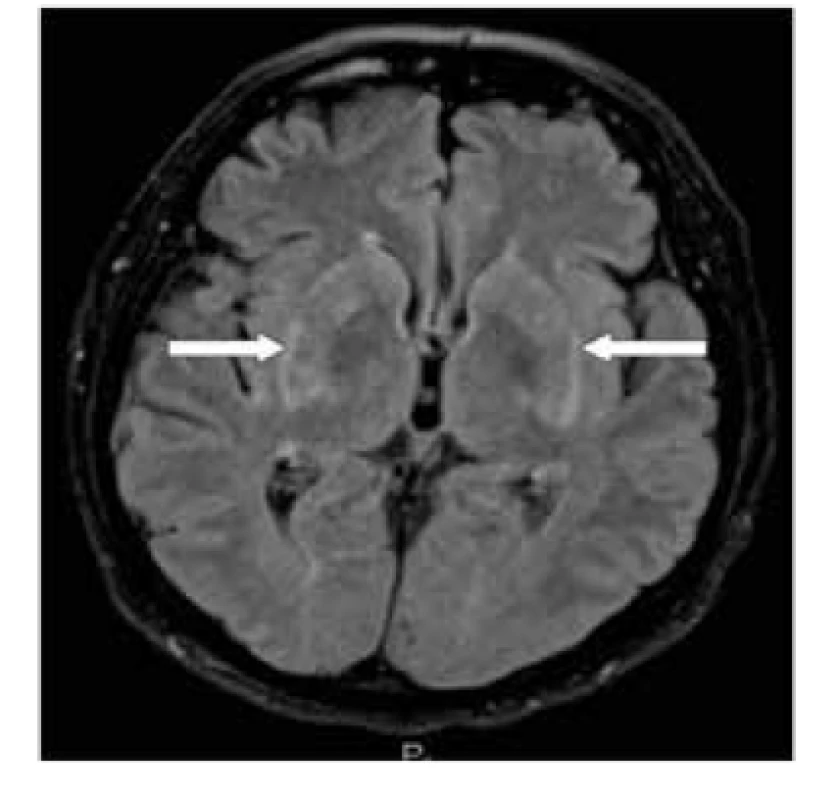
Vzhledem k podezření na možnou souvislost s toxicitou nivolumabu byl pacient hospitalizován k dovyšetření etiologie těchto neuropsychických změn. Provedená magnetická rezonance mozku vyloučila možnost metastatického postižení mozku, čerstvé ischémie či přítomnosti abscesů. Popsán byl pouze patologicky zvýšený signál v oblasti bazálních ganglií bilaterálně, nevylučující možnost toxického postižení (obr. 5). Dalšími vyšetřeními pak byla vyloučena infekční či autoimunitní příčina v séru. Vyšetření mozkomíšního moku vyloučilo virovou i bakteriální infekci, včetně přítomnosti nádorových buněk. Specifické neuroimunologické vyšetření (Topelex) likvoru prokázalo pouze pozitivitu paraneoplastického antigenu Ma2 v IgG třídě a vyšší zastoupení lymfocytů, z nichž většinu tvořily CD4+ T lymfocyty.
V souladu s doporučeními managementu nežádoucích účinků byl pacient hospitalizován a byla zahájena léčba vysokodávkovaným kortikosteroidem (Solu-Medrol) v dávce 2 mg na kilogram a den. Během léčby kortikosteroidy byl rovněž podáván Cotrimoxazol jako prevence možných infekčních komplikací. Navzdory této léčbě došlo k další progresi neurologických obtíží, ke kterým se nově přidaly i paranoické halucinace se suicidálními myšlenkami. Ve spolupráci s psychiatry a neurology byla opakovaně upravována antipsychotická medikace. Efektivní byla až kombinace clonazepamu, haloperidolu, olanzapinu a tisercinu.
Vzhledem k neúčinnosti kortikoterapie byla imunosupresivní léčba eskalována podáním infliximabu v dávce 5 mg/kg 19. 08. 2017. I tato léčba však byla bez výraznějšího efektu.
Pacient i rodina trvali na dimisi. S pacientem a rodinou byla opakovaně probrána situace a doporučeno setrvání v nemocnici. Dle psychiatrického konzilia byl pacient shledán schopným podpisu negativního reverzu. 23. 08. 2017, navzdory našemu doporučení, byl pacient propuštěn z nemocnice. Aplikace antipsychotické medikace a terapie kortikoidy byla zajištěna cestou domácí hospicové péče. U pacienta bylo plánováno podání další dávky infilximabu, ke kterému se však pacient i přes opakované výzvy již nedostavil.
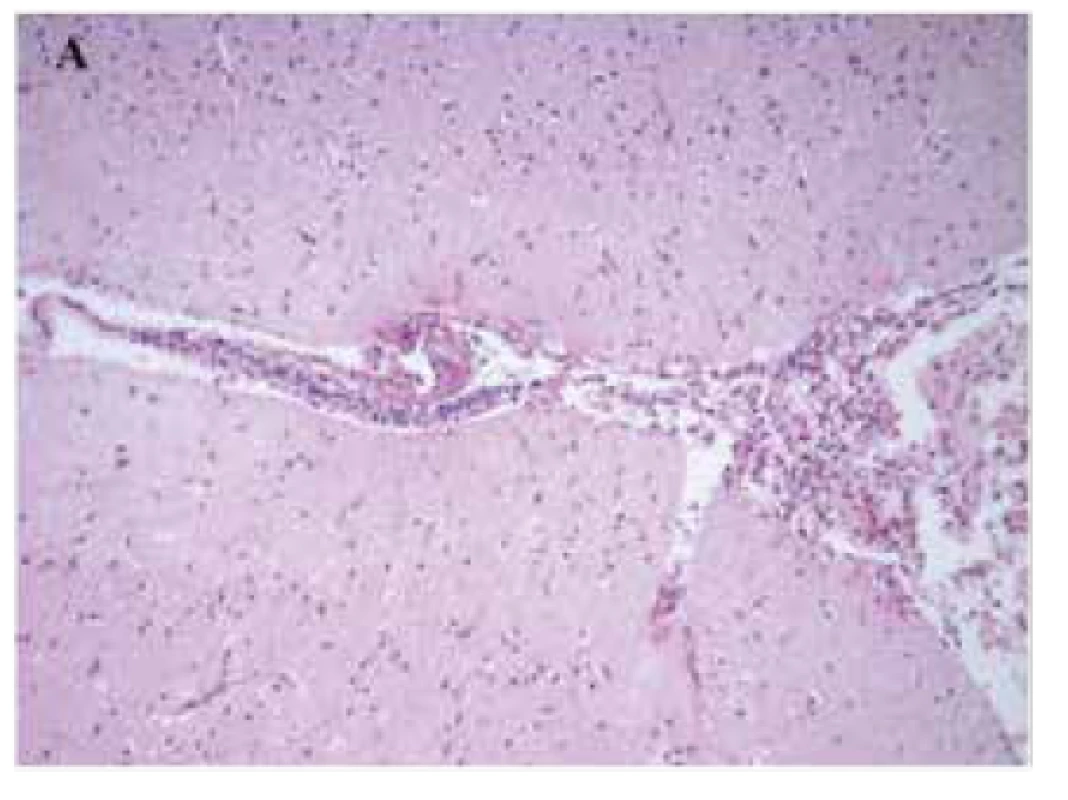
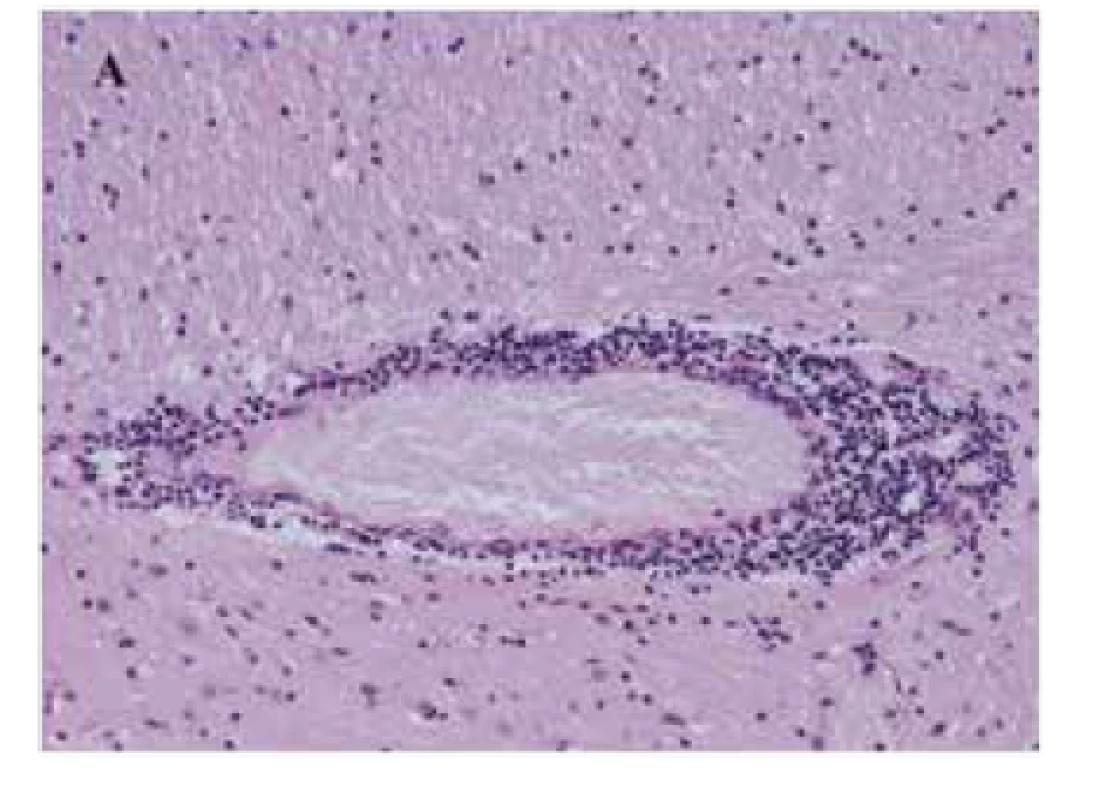
Za tři týdny od dimise byl pacient akutně přijat do nemocnice pro soporózní stav a febrilie. V laboratoři nebyly mimo zvýšených známek zánětu nalezeny žádné abnormality. Vzhledem ke klinickému obrazu urosepse byl pacient empiricky zajištěn antibiotiky a byla zahájená parenterální hydratace. Po dvou dnech podpůrné terapie pacient částečně nabyl vědomí, současně však opět progredovala chorea a agresivita s nutností opětovného nasazení antipsychotické terapie. I přes podpůrnou terapii došlo u pacienta postupně k deterioraci vědomí a rozvoji bronchopneumonie. Čtyři dny po přijetí do nemocnice pacient umírá pod obrazem bronchopneumonie. V rámci pitevního vyšetření byla verifikována nekróza v oblasti Th11 bez známek aktivního tumoru a dále nebyla detekována již žádná metastatická ložiska v plicích. Vzhledem k podezření na aseptickou meningitidu byl excesivně vyšetřen mozek pacienta, který byl bez makroskopických pozoruhodností. Histologické vyšetření prokázalo nevýraznou fokální lymfocytární meningitidu v celém vyšetřovaném rozsahu (obr. 6) a mnohočetné perivaskulární lymfocytární infiltráty, s maximem v oblasti bazálních ganglií (obr. 7). Tento výsledek byl v souladu se závěrem z magnetické rezonance provedené měsíc před smrtí. Imunohistochemicky byly vyšetřeny povrchové markery T lymfocytů CD4 a CD8, jednak z oblasti baze frontálního laloku a jednak z oblasti bazálních ganglií. Poměr CD4 ku CD8 T lymfocytům, který je při aseptické meningitidě typicky okolo 3 : 1, byl však v obou řezech nezvykle nízký, přibližně 1 : 1 (obr. 8).
I přes terapeutický přínos imunoterapie v léčbě karcinomu ledviny je vzhledem k možnému výskytu nežádoucích účinků nutná obezřetnost, a to i k méně častým vedlejším účinkům, jako je například neurotoxicita. Tato kazuistika poukazuje také na důležitost spolupráce při řešení nežádoucích účinků nejen s pacientem, ale i jeho rodinou.
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Štítky
Dětská onkologie Onkologie
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání