-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaInovativní farmakoterapie obstrukční HCM v reálné české praxi – kazuistika
7. 8. 2024
Na základě případu pacientky z naší klinické praxe sdílíme své první pilotní zkušenosti s léčbou hypertrofické kardiomyopatie novou farmakoterapeutickou modalitou – mavakamtenem.
Úvod
Hypertrofická kardiomyopatie (HCM) je relativně časté onemocnění s celosvětovou distribucí a odhadovanou prevalencí 1/200–500 (1). Je definována přítomností hypertrofie levé komory (LK) > 15 mm v jakémkoliv segmentu LK, nesouvisející s jiným srdečním, metabolickým ani systémovým onemocněním schopným produkovat podobný rozsah hypertrofie.
HCM může být zděděna jako autosomálně dominantní porucha s proměnlivou penetrancí, která je spojená s variantami v genech kódujících proteiny srdeční sarkomery, nebo s neidentifikovaným genetickým pozadím.
InzerceHCM je u většiny pacientů asociovaná s přítomností nitrokomorové obstrukce, ať už klidové či provokované. Přítomnost obstrukce výtokového traktu levé komory (LVOTO), tj. subaortální obstrukce, je nejčastějším patofyziologickým mechanismem vedoucím k rozvoji příznaků srdečního selhání a vzniku funkční mitrální regurgitace (MiR) (2).
Identifikace a kvantifikace LVOTO pomocí klidové nebo zátěžové echokardiografie je klíčová pro další terapeutický management, který má v ideálním případě vést k odstranění nebo alespoň zmírnění LVOTO. Terapeutické možnosti symptomatických pacientů s obstrukční hypertrofickou kardiomyopatií (HOCM) lze rozdělit mezi dva přístupy:
- Invazivní metody, spočívající v provedení septální redukční terapie (SRT) ať už pomocí alkoholové septální ablace (ASA) nebo chirurgické myektomie.
- Farmakoterapie, jež se v našich podmínkách donedávna opírala o betablokátory nebo kalciové blokátory (verapamil, diltiazem).
Oba terapeutické přístupy mohou být účinné v redukci LVOTO a symptomů pacienta, jedná se však o léčbu nespecifickou.
Průlomem ve farmakoterapii HOCM byl proto objev léků ze skupiny inhibitorů myozinu, jež cílí na primární patofyziologii onemocnění. Prvním lékem z této skupiny je mavakamten, který byl v červnu 2023 zaregistrován Evropskou lékovou agenturou (EMA) pro léčbu symptomatických pacientů s HOCM.
Popis případu
69letá pacientka byla praktickým lékařem odeslána na naše pracoviště k provedení echokardiografického vyšetření z důvodu progredující námahové dušnosti a palpitací. Pacientka měla v anamnéze arteriální hypertenzi dobře kontrolovanou monoterapií sartanem, léčila se s hypotyreózou a hyperlipoproteinémií. Již v roce 2016 měla provedené koronarografické vyšetření v rámci diferenciální diagnostiky námahové dušnosti. Koronarogram byl negativní, echokardiografii provedenou v té době v rajonní kardiologické ambulanci se nám nepodařilo dohledat, kardiologicky dispenzarizovaná ale nebyla. Rodinná anamnéza stran výskytu kardiovaskulárních onemocnění či náhlého úmrtí byla negativní.
Provedené echokardiografické vyšetření zobrazilo nedilatovanou LK s asymetrickou septální hypertrofií s maximem tloušťky septa 18 mm. Byl přítomný systolický dopředný pohyb předního cípu mitrální chlopně (SAM) s turbulencí toku ve výtokovém traktu LK a sekundární asymetrickou mitrální insuficiencí do dilatované levé síně (viz video 1). Při dopplerovském vyšetření byl měřený klidový obstrukční gradient v LVOT 32 mmHg (viz obr. 1), který po provokačním Valsalvově manévru stoupal na 81–106 mmHg (viz obr. 2). LK byla hyperkontraktilní s EF LK > 65 %, s poruchou diastolické funkce I. stupně. U pacientky bylo indikováno doplnění magnetické rezonance (MRI) srdce s následnou konzultací ve specializované ambulanci pro kardiomyopatie.
Video 1 SAM a MiR
Abyste mohli shlédnout toto video, musíte povolit cookies.
Obr. 1 Klidový gradient LVOTO
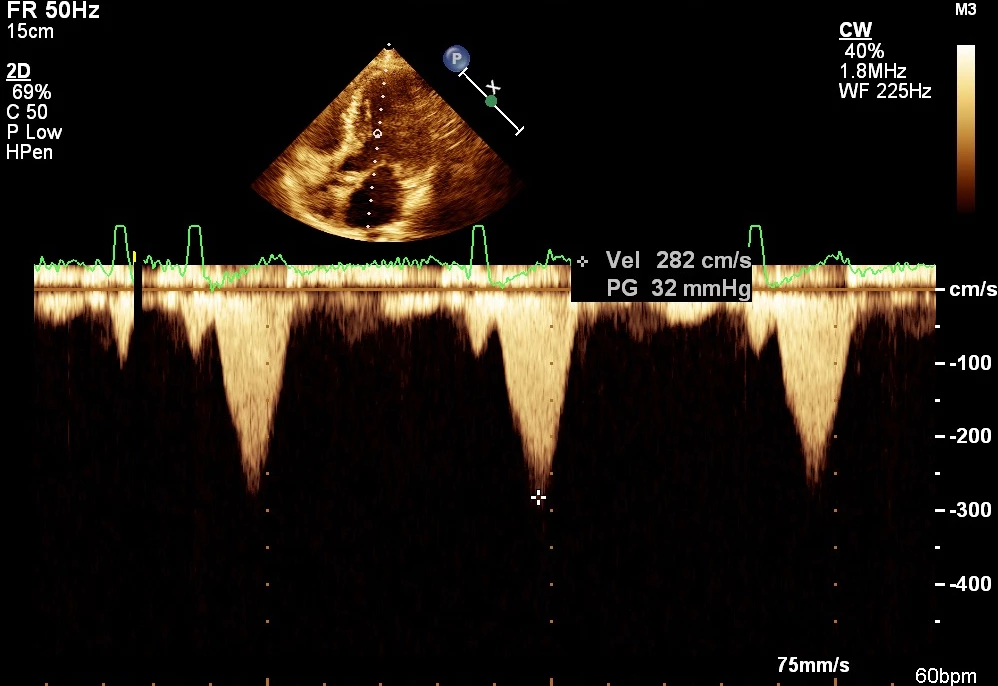
Obr. 2 Gradient LVOTO po Valsalvově manévru

MRI vyšetření potvrdilo přítomnost těžké asymetrické hypertrofie stěn LK s maximem ve středním segmentu inferosepta s tloušťkou myokardu 18–19 mm, LK byla nedilatovaná (naopak s nižším EDVi 49 ml/m2) s ejekční frakcí (EF LK) 64 %; rovněž byl patrný SAM s turbulencí toku v LVOT (viz video 2 a 3). V pozdních postkontrastních skenech nebylo přítomné pozdní sycení LK (LGE – late gadolinium enhancement) (viz obr. 3–5), kalkulovaná hodnota extracelulárního objemu byla normální (ECV 25 %).
Video 2 MRI A3CH
Abyste mohli shlédnout toto video, musíte povolit cookies.
Video 3 MRI A4CH
Abyste mohli shlédnout toto video, musíte povolit cookies.
Obr. 3 MRI PSIR A3CH
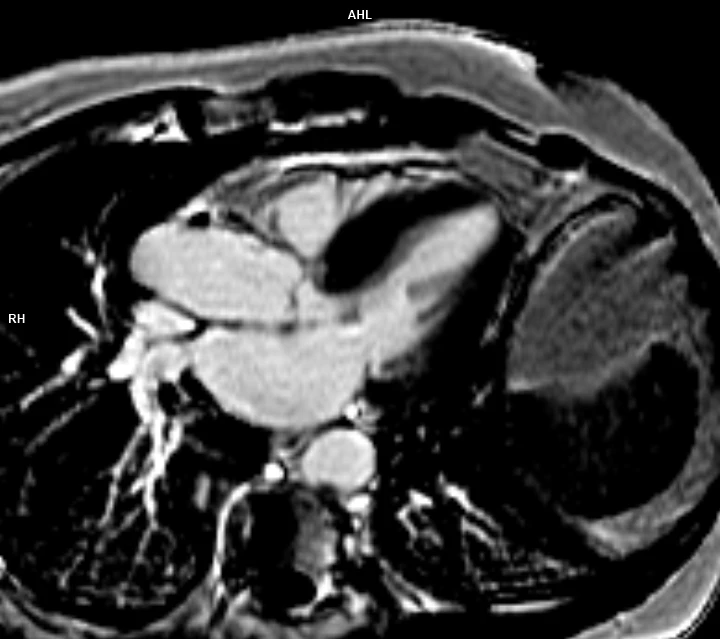
Obr. 4 MRI PSIR A4CH
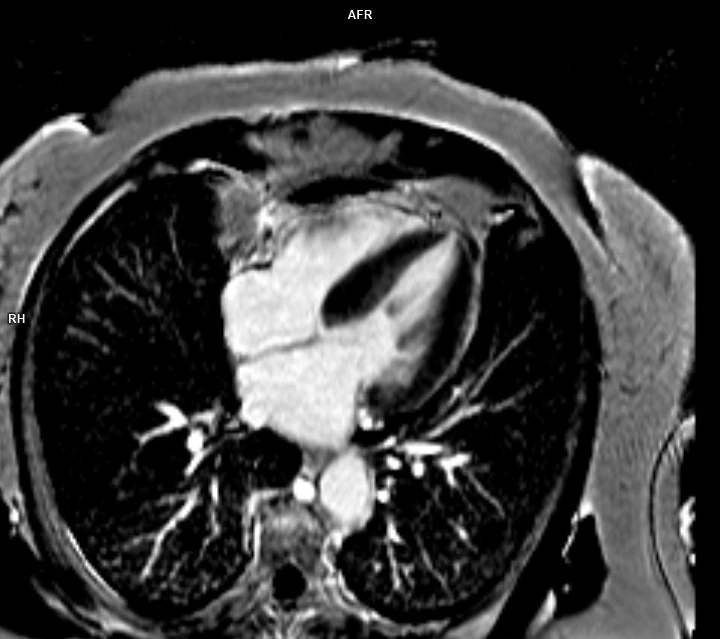
Obr. 5 MRI PSIR SA
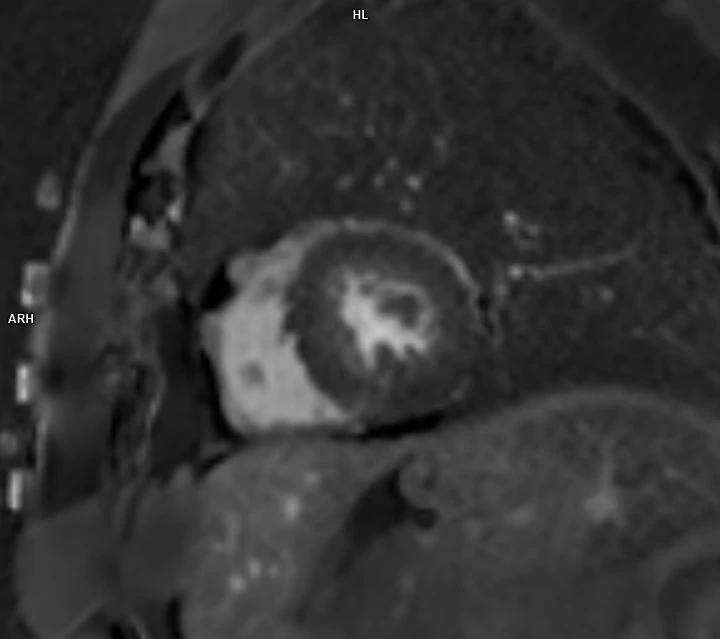
Při ambulantním vyšetření si pacientka stěžovala na progredující námahovou dušnost, obzvlášť zhoršenou v posledním půlroce, odpovídající funkční třídě NYHA III; dále si stěžovala na závratě ve vazbě na námahu a občasné palpitace. Negovala bolesti na hrudi, neprodělala synkopu. Při objektivním vyšetření byl nápadný systolický ejekční šelest v prekordiu, jinak byl klinický nález normální, TK 119/70 mmHg, na klidovém EKG (obr. 6) byla tepová frekvence (TF), sklon srdeční osy doleva, levý přední hemiblok a patrná voltážová kritéria pro hypertrofii LK. Při holterovském EKG monitorování byl přítomný sinusový rytmus s průměrnou TF 69/min, s málo četnými supraventrikulárními extrasystolami (SVES) a izolovanými komorovými extrasystolami (KES) dvojí morfologie, jež celkově tvořily 5 % záznamu, ale nebyly zachyceny nesetrvalé komorové tachykardie (nsKT). Laboratorně byla zvýšená hladina NT-proBNP na 673 ng/l, jinak byl laboratorní nález normální.
Obr. 6 Klidové EKG
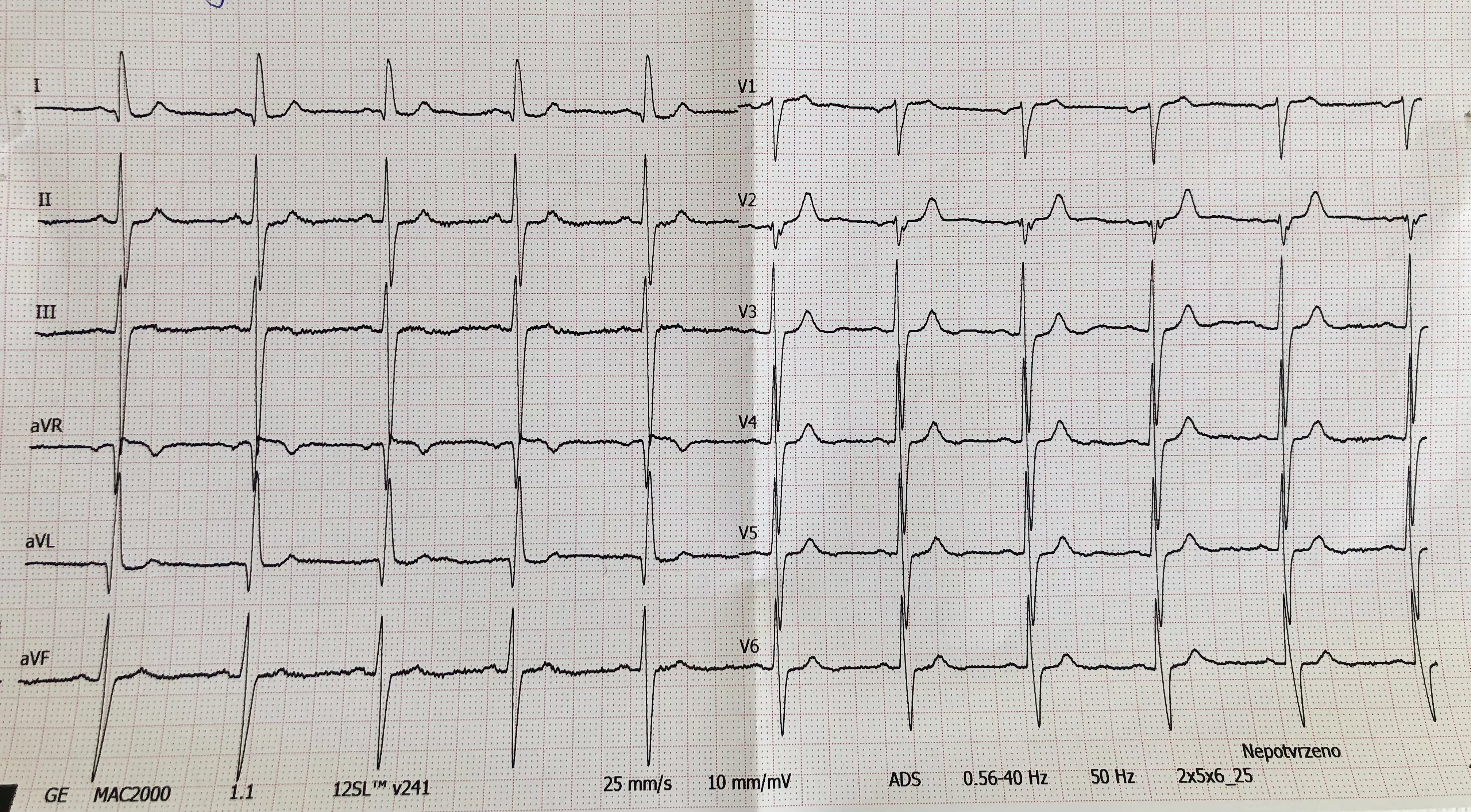
U pacientky byla iniciálně zahájená terapie betablokátorem (metoprolol 25 mg denně) a současně snížena dávka sartanu pro sklon k hypotenzi, s plánovanou klinickou kontrolou a kontrolním EKG Holterem za 3 měsíce. Rovněž bylo doporučeno screeningové kardiologické vyšetření prvostupňových příbuzných.
Po 3 měsících léčby při ambulantní kontrole byly symptomy pacientky ovlivněny jen minimálně. Zaznamenala sice redukci palpitací, ale přetrvávala limitující námahová dušnost a závratě při zátěži. Klinické potíže nadále odpovídaly funkční třídě NYHA III. Na klidovém EKG byla TF 58/min, měřený TK 90/60 mmHg. Při kontrolním holterovském monitorování došlo k redukci četnosti SVES i KES (oboje cca 1 % záznamu), průměrná TF činila 60/min. Vzhledem k hypotenzi nebylo možné dál navyšovat dávku betablokátoru a pacientce byla nabídnuta možnost konzultace stran provedení septální redukční terapie pomocí alkoholové septální ablace nebo farmakoterapie mavakamtenem. Pacientka vzhledem k obavám z možných komplikací invazivního výkonu preferovala farmakoterapii.
Na základě aktuálních doporučení zdravotní pojišťovna schválila úhradu léčby mavakamtenem v režimu § 16. Bylo indikované genetické vyšetření ve vztahu k diagnóze HCM a současně k provedení genotypizace kvůli určení fenotypu izoenzymu CYP2C19 cytochromu P450, které je nutné pro vedení léčby. Má za cíl identifikovat případné pomalé metabolizátory a vyhnout se možným nežádoucím efektům kumulativní dávky léčiva.
Vzhledem k absenci výsledku fenotypizace CYP2C19 k datu zahájení léčby jsme dle doporučení zahájili terapii iniciální dávkou mavakamtenu 2,5 mg denně přidaného ke stávající terapii metoprololem.
Při klinické kontrole a echokardiografickém vyšetření po 4 týdnech léčby byla EF LK normální (65 %), byl patrný pokles, respektive vymizení klidového obstrukčního gradientu v LVOT, provokovaný gradient LVOTO po Valsalvově manévru dosahoval maximálně 29 mmHg (viz obr. 7). Současně již nebyl patrný SAM a došlo k významné redukci mitrální insuficience (viz video 4 a 5). Subjektivně pacientka uváděla zmírnění dechových potíží, léčbu tolerovala velmi dobře, nezaznamenala žádné nežádoucí účinky.
Obr. 7 ECHO kontrola – provokovaný gradient po Valsalvově manévru
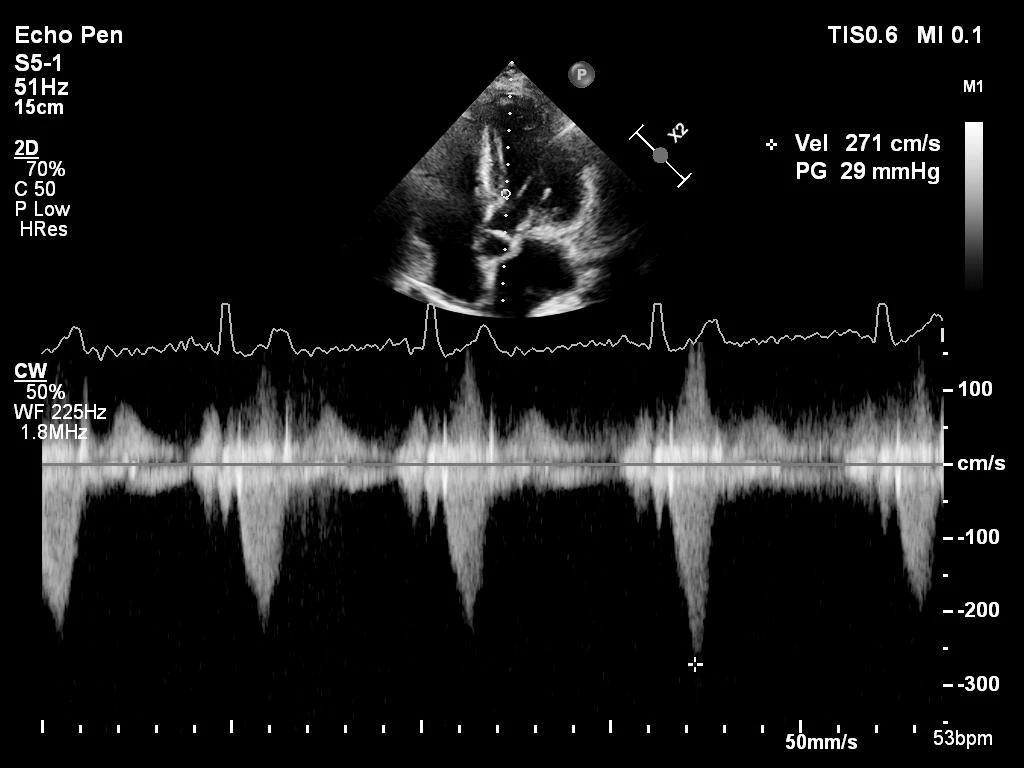
Video 4 ECHO A3CH – vymizení SAM a MiR
Abyste mohli shlédnout toto video, musíte povolit cookies.
Video 5 ECHO A4CH – vymizení SAM a LVOTO
Abyste mohli shlédnout toto video, musíte povolit cookies.
Dle doporučení jsme vzhledem k redukci obstrukčního gradientu pokračovali v udržovací dávce mavakamtenu 2,5 mg denně. Při klinické a echokardiografické kontrole po 8 týdnech léčby byla pacientka nadále bez detekovatelného klidového gradientu LVOTO a byl detekovaný pouze provokovaný zátěžový gradient v LVOT s hodnotou kolem 30 mmHg, EF LK byla normální. Laboratorně došlo k poklesu hodnot NT-proBNP o více než 2/3 (na 185 ng/l z původních 673 ng/l); klinicky redukce potíží odpovídala funkční třídě NYHA I–II.
Závěr
U pacientky se symptomatickou HOCM na terapii mavakamtenem prokazatelně došlo k vymizení klidového obstrukčního gradientu ve výtokovém traktu LK, vymizení funkční mitrální regurgitace a výrazné redukci provokovaného obstrukčního gradientu v LVOT což klinicky vedlo k ústupu subjektivních obtíží, zlepšení kvality života a zlepšení funkčního stavu.
Ve vztahu k novým terapeutickým možnostem je identifikace nemocných s LVOTO klíčová. Zejména u symptomatických pacientů je proto nutné po přítomnosti obstrukce aktivně pátrat pečlivým echokardiografickým vyšetřením v klidu, při provokačních manévrech i provedením zátěžového echokardiografického vyšetření. Rutinní dostupnost a proveditelnost zobrazovacích metod, funkčních testů a genetického vyšetření představuje nutnou součást komplexní péče o pacienta s HCM. Je také důležitým předpokladem pro volbu adekvátní terapeutické strategii ke zmírnění či odstranění obstrukce, a to jak ve vztahu k farmakoterapii, tak i při plánovaní septální redukční terapie u vybraných skupin pacientů.
Mavakamten je novou terapeutickou možností pro symptomatické pacienty s LVOTO, kteří nereagují na léčbu 1. linii nebo ji netolerují, případně jako alternativa k provedení septální redukční terapie.
MUDr. Júlia Borová
Komplexní kardiovaskulární centrum Nemocnice AGEL Třinec-PodlesíLiteratura:
1. Maron BJ, Desai MY, Nishimura RA et al. Diagnosis and evaluation of hypertrophic cardiomyopathy: JACC state-of-the-art review. JACC 2022; 79 (4): 372–389.
2. Maron MS, Olivotto I, Zenovich AG et al. Hypertrophic cardiomyopathy is predominantly a disease of left ventricular outflow obstruction. Circulation 2006; 114 (21): 2232–2239.
3. Charron P, Elliott PM, Gimeno JR et al. The Cardiomyopathy Registry of the EURObservational Research Programme of the European Society of Cardiology: baseline data and contemporary management of adult patients with cardiomyopathies. Eur Heart J 2018; 39 : 1784–1793.
4. Olivotto I, Oreziak A, Barriales-Villa R et al. Mavacamten for treatment of symptomatic obstructive hypertrophic cardiomyopathy (EXPLORER-HCM): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2020; 396 (10253): 759–769.
5. Desai MY, Wolski K, Owens A et al. Study design and rationale of VALOR-HCM: evaluation of mavacamten in adults with symptomatic obstructive hypertrophic cardiomyopathy who are eligible for septal reduction therapy. Am Heart J 2021; 239 : 80–89.
6. Arbelo E, Protonotarios A, Gimeno JR et al.; ESC Scientific Document Group. 2023 ESC Guidelines for the management of cardiomyopathies. Eur Heart J 2023; 44 (37): 3503–3626.3500-CZ-2400061
Zkrácenou informaci o přípravku naleznete zde.
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Štítky
Interní lékařství Kardiologie
Nejnovější kurzy
Autoři: doc. MUDr. David Zemánek, Ph.D., MUDr. Anna Chaloupka, Ph.D.
Přejít do kurzů
Nejčtenější tento týden Celý článekPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




