-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Přínosy versus rizika kombinované hormonální antikoncepce
Datum publikace: 20. 2. 2017
Anotace
Kombinovaná hormonální kontracepce (CC) je vysoce účinnou reverzibilní metodou ochrany před otěhotněním. V současnosti používané nízkodávkované preparáty si udržují vysokou spolehlivost při minimálních zdravotních rizicích. Přetrvává pouze riziko kardiovaskulárních komplikací závislé na dávce estrogenu a typu progestinu.
CC je spojena s neantikoncepčními pozitivními efekty (kontrola menstruačního cyklu, léčba hyperandrogenismu, léčba ovariálních cyst, dysmenorey, kongestivní pelipatie, …). Při dodržování pravidel pro předepisování CC převažuje přínos nad riziky užívání.
Úvod
Kombinovaná hormonální antikoncepce (CC) je dominantní antikoncepční metodou. Její rozšíření je v nepřímé úměře k počtu vyžádaných přerušení těhotenství. Kombinovaná hormonální antikoncepce má jako každý lék svá rizika, ale při respektování všech kontraindikací její antikoncepční i neantikoncepční účinky převažují případná rizika, která spočívají zejména v tromboembolické nemoci.
Nežádoucí účinky kombinované hormonální antikoncepce
Častější nežádoucí účinky CC jsou charakteru diskomfortu bez dlouhodobého ohrožení zdraví ženy. Patří sem bolesti hlavy, napětí v prsou, zvětšení prsou, nervozita, podrážděnost a zvýšení hmotnosti. Za nejčastější mechanismus jejich vzniku je považována retence tekutin.
Mezi vzácné komplikace jsou někdy řazeny migrény, změny libida, kožní změny, změny nálady, emoční labilita, zvracení a nesnášenlivost kontaktních čoček.
Velmi vzácnými, ale potenciálně smrtícími komplikacemi jsou tromboembolická nemoc, arteriální komplikace ve smyslu infarktu myokardu nebo cévní mozkové příhody, hypertenze, tumor jater a cholestatická žloutenka. Varovnými příznaky těchto stavů jsou dyspnoe a bolest na hrudi, silná bolest hlavy, poruchy vidění, nejasné bolesti břicha a bolesti dolních končetin.
Mezi nejčastější komplikace užívání hormonální antikoncepce vedoucí k přerušení jejího užívání patří nepravidelnosti menstruačního cyklu zejména ve smyslu krvácení a přibírání na váze.
Pro nepravidelnosti cyklu platí, že je vhodné vyčkat minimálně tři cykly, zda nedojde k úpravě. Promptní změny preparátů po jednom cyklu nepřináší řešení. Po třech cyklech doporučují někteří autoři při přetrvávajícím špinění podávat nesteroidní antirevmatika, ale častější praxí je změna preparátu CC. Nejčastěji je doporučováno zvýšit dávku ethinylestradiolu (EE). Speciálně pro switchers je doporučována kombifázická konstrukce CC.
Možný nežádoucí hmotnostní přírůstek uvádí jako hlavní nevýhodu CC 73 % žen. Dosud známé efekty sexuálních steroidů na metabolismus shrnuje ve své práci z roku 1992 Karlsson:
- stimulace renin-angiotensinového systému a tím zvýšená retence tekutin,
- změny v metabolismu sacharidů,
- snížená sekrece sérového cholecystokininu; pokles hladiny cholecystokininu v séru vede ke zvýšení chuti k jídlu a dalším změnám na úrovni centrálního nervového systému, jež vedou ke zvýšení příjmu tekutin.
Nejčastěji uváděné změny tělesné hmotnosti ve studiích porovnávajících uživatelky nízko - a velmi nízkodávkované CC jsou 0,5–2 kg za 6–12 měsíců. Se snižováním dávky steroidů v pilulce klesá i uváděný průměrný hmotnostní přírůstek ve studiích z 2 na 0,3–0,8 kg/rok. U 74 % žen setrvá hmotnost, 12 % ztratí více než 2 kg a 14 % totéž přibere. Pokud se jedná o retenci tekutin, je vhodné snížit dávku EE nebo použít preparát s antimineralokortikoidním progestinem, nejlépe drospirenonem. Vyšší váhové změny bývají dány spíše změnou životního stylu spojenou s nasazením antikoncepce, a tak často bývá důležité dříve vyšetřit změnu stravovacích režimů pacientky než kompletní metabolický profil.
Vliv na glukózovou toleranci je minimální. Nebylo prokázáno zvýšení rizika tvorby žlučových kamenů, ale během prvních měsíců se zvyšuje riziko klinické manifestace konkrementů již přítomných.
Relativní riziko (RR) výskytu Crohnovy choroby mírně stoupá u uživatelek CC s RR 1,4 (95% CI: 1,1–1,9), naproti tomu u ulcerózní kolitidy není tato závislost významná – s RR 1,3 (95% CI: 0,9–1,8). Ale tato asociace je slabá a chybí kauzální vysvětlení.
Nebylo prokázáno spojení mezi CC a vaginálním fluorem, choreou a benigní intrakraniální hypertenzí (pseudotumor cerebri), infekčními a zánětlivými onemocněními.
Hypertenze
Na vzniku hypertenze po podání kombinovaných kontraceptiv se podílí několik mechanismů: zvýšená syntéza angiotenzinu ve stimulovaných játrech (obr. 1), snížení syntézy dopaminu v hypotalamu a přímé působení progestinů na cévní stěnu. Téměř u poloviny žen dojde po podání CC ke zvýšení systolického i diastolického tlaku. Průměrná změna se pohybuje mezi 1 a 2 mm Hg. Maximálně u 2,5 % žen překročí hodnoty tlaku normu. Kontroly krevního tlaku jsou již zaběhnutou rutinou. Objevení hypertenze po nasazení COC je indikací k jejímu vysazení, nikoli k léčbě této nově vzniklé hypertenze.
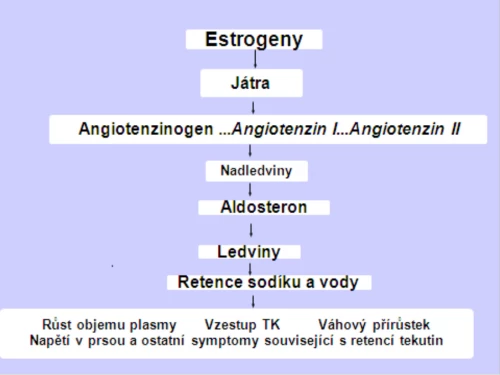
Obrázek 1: Mechanismus elevace tlaku krve u uživatelek CC
Edukační materiál SÚKL
V únoru 2014 byli všichni gynekologové obesláni dopisem od držitelů rozhodnutí o registraci (míněno CC) s názvem „Kombinovaná hormonální antikoncepce: věnujte pozornost rozdílům v riziku tromboembolie mezi přípravky, významu individuálních rizikových faktorů a známkám a příznakům tohoto stavu“.
Dopis zcela bez odkazů na odborné zdroje uvádí, že:
- míra rizika žilní tromboembolie (VTE) je u nízkodávkovaných přípravků CC (ethinylestradiol < 50 μg) malá,
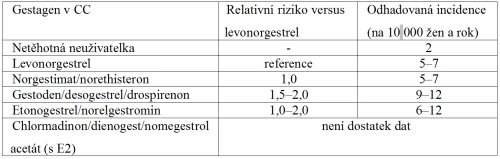
- existují pádné důkazy o rozdílech mezi jednotlivými přípravky CC z hlediska rizika VTE v závislosti na typu gestagenu, nejnižší riziko je spojeno s přípravky s levonorgestrelem, norethisteronem a norgestimatem (tab. 1),
Tabulka 1: Riziko VTE v CC
- při předepisování CC je třeba zvážit individuální aktuální rizikové faktory dané ženy, zejména pro VTE, a rozdíl rizika VTE mezi jednotlivými přípravky,
- není třeba, aby žena, která užívá CC bez problémů, její užívání ukončila,
- neexistují důkazy o rozdílech mezi nízkodávkovými přípravky CC z hlediska arteriální tromboembolie (ATE),
- přínosy spojené s užíváním CC u většiny žen zdaleka převyšují riziko závažných nežádoucích účinků, pozornost je třeba věnovat individuálním rizikovým faktorům a známkám a projevům VTE a ATE.
Dopis je doplněn o edukační materiál pro pacientky a lékaře, který lze stáhnout na stránkách http://www.sukl.cz/leciva/edukacni-materialy-k-bezpecnemu-pouzivani-lecivych-pripravku-2. V materiálech pro lékaře překvapivě laickým jazykem vyjmenovává známé absolutní i relativní kontraindikace CC. Bohužel zcela chybí specifikace pojmu vysoká hladina lipidů.
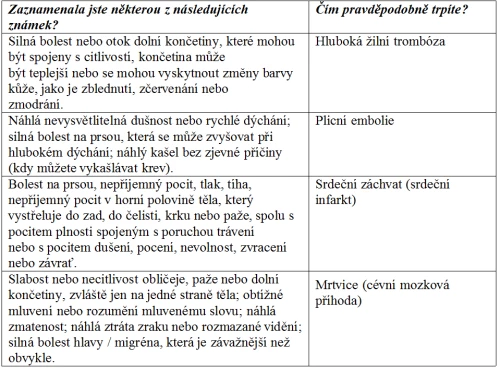
Jako praktický se jeví materiál pro pacientky a zejména tabulka časných příznaků VTE a ATE (tab. 2).
Tabulka 2: Příznaky VTE a ATE – popis klinické symptomatologie pro uživatelky CC
Kombinovaná hormonální antikoncepce a tromboembolická nemoc
Výše uvedený edukační materiál jen opakuje známá fakta, která i samotná EMEA uvádí již v roce 2001. Relativní riziko tromboembolické nemoci u uživatelek CC je 2–4. Je nutno toto riziko brát v úvahu přesto, že pouze 1–2 % těchto příhod končí fatálně. Pečlivě odebraná anamnéza může odhalit ženy ve vyšším riziku VTE (anamnéza VTE v 1. a 2. linii, body mass index nad 30).
U žen s pozitivní rodinnou anamnézou TEN je vhodné vyšetření vrozených trombofilií:
- leidenská mutace (mutace faktoru V),
- mutace protrombinu (mutace faktoru II 20210A),
- deficity inhibitorů koagulační kaskády – protein C, protein S, antitrombin III,
- hyperhomocysteinémie,
- hyperlipoproteinémie (a).
Nález deficitu AT III, proteinu C, proteinu S, homozygotní formy leidenské mutace, homozygotní formy mutace protrombinu F II nebo hyperhomocysteinémie (doprovázející například Marfanův syndrom) je absolutní kontraindikací CC.
Nález heterozygotní formy leidenské mutace, mutace protrombinu a hyperlipoproteinémie (a) je relativní kontraindikací CC.
Kvůli 4–8% výskytu v populaci v heterozygotní formě je nejčastější kontraindikací podávání CC a kofaktorem tromboembolické nemoci APC rezistence (leidenská mutace), která zvyšuje relativní riziko na 35, tedy z 0,8/100 000 na 30/100 000 žen ročně.
Často vyšetřovaná mutace MTHFR, která má v heterozygotní formě prevalenci 40 %, není většinou odborníků považována za rizikovou pro VTE, a její nález bez osobní anamnézy VTE tedy není kontraindikací CC.
Pouhé dodržování pravidel o nutnosti vysazení CC při akutním výskytu dalšího trombofilního rizika přinese výrazné zvýšení bezpečnosti. Nejvyšší riziko VTE je sledováno v prvních 6 měsících užívání CC. Studie prokázala, že u žen v riziku (imobilizace pro zlomeniny, chirurgické operace) byl výskyt TEN 17krát vyšší než u žen bez patrného rizika (idiopatické TEN).
Od roku 1960, kdy bylo poprvé zvýšené riziko VTE při CC zjištěno, došlo v CC k výrazným změnám: snížení dávky EE, diferenciace v použitém progestinu a jeho dávce. Při mnohdy bouřlivé a farmaceutickým marketingem ovlivněné diskusi je naprosto nezbytné si uvědomit, že relativní riziko VTE v těhotenství je 5,5–6 , tedy vždy vyšší než při kterékoli dostupné CC.
Jednou z cest, jak snížit riziko VTE při užívání CC, je snižování dávky EE. Dávky nižší než 50 μg nesou nižší riziko než v 70. letech používané vyšší dávky. Většina studií neprokázala již další snižování rizika při poklesu dávky EE pod 35 μg.
Riziko VTE je významně ovlivněno užitým progestinem. V roce 1995 byly publikovány tři studie prokazující vyšší riziko při užití progestinů 3. generace oproti generaci 2. Jick prokázal kohortovou analýzou relativní riziko 1,9 a analýzou případů a kontrol 2,3 pro progestiny 3. generace proti 2. generaci. V roce 2001 EMEA uzavírá diskusi reanalýzou, ze které vyplývá, že riziko při 3. generaci je 1,5–2krát vyšší, incidence se tedy zvýší z 20/100 000 na 30–40/100 000.
Pro nejúčinnější z antiandrogenních progestinů – cyproteronacetát 2 mg – v kombinaci s 35 μg EE zjistili Vasilakis-Scarmozza a Jick ve srovnání s 30 μg EE a levonorgestrelem riziko 3,9krát vyšší, tedy incidenci TEN 78/100 000. Kombinace EE s cyproteronacetátem byla proto recentně vyhrazena jen pro léčbu kožních hyperandrogenních příznaků.
Metaanalýza B. H. Stagemanové vybrala z 3 110 publikací 26 studií, v nichž byla incidence VTE u neuživatelek 1,9–3,7 na 10 000 žen ročně. Užívání CC obecně přineslo relativní riziko 3,5 (CI 2,9–4,3). Relativní riziko CC s 30–35 μg EE v kombinaci s gestodenem, desogestrelem, cyproteronacetátem nebo drospirenonem bylo obdobné a o 50–80 % vyšší než pro kombinaci s levonorgestrelem (tab. 3). Přímá úměra rizika VTE k dávce EE byla zjištěna pro kombinaci s gestodenem, desogestrelem a levonorgestrelem.
Tabulka 3: Metaanalýza rizika VTE dle generace progestinu v CC – relativní riziko

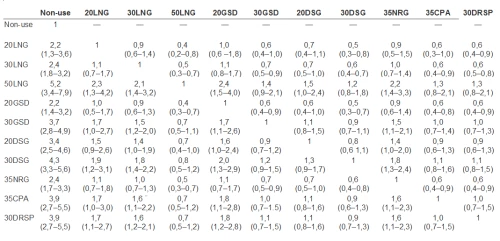
Zajímavé je, že tato publikace svým způsobem rehabilituje výše zmíněný cyproteronacetát (tab. 4).
Tabulka 4: Metaanalýza RR VTE pro jednotlivé přípravky CC (20LNG = 20 μg EE + levonorgestrel; 30LNG = 30 μg EE + levonorgestrel; 50LNG = 50 μg EE + levonorgestrel; 20GSD = 20 μg EE + gestoden; 30GSD = 30 μg EE + gestoden; 20DSG = 20 μg EE + desogestrel; 30DSG = 30 μg EE + desogestrel; 35NRG = 35 μg EE + norgestimat; 35CPA = 35 μg EE + cyproteronacetát; 30DRSP = 30 μg EE + drospirenon)
Kombinovaná hormonální antikoncepce a arteriální tromboembolie
Relativní riziko infarktu myokardu je pro uživatelky CC 2–3,2. Prakticky není zvýšeno u žen do 35 let. Nicméně v kombinaci s kouřením se situace razantně mění, u kuřaček pod 35 let je relativní riziko 10, nad 35 let 120. Zavedení progestinů 3. generace do praxe vedlo díky snížení rizika infarktu myokardu k rozšíření preskripce CC i do rizikových skupin žen. Na 7. kongresu ESC Jespersen předběžně uzavřel rozsáhlou diskusi na toto téma doporučením preferovat u žen s rizikem TEN progestiny 2. generace, u žen v riziku infarktu myokardu pak progestiny 3. generace.
Ateroskleróza je přímo spojena s poruchou metabolismu lipidů. Estrogeny snižují hladiny LDL cholesterolu cestou stimulace exprese LDL receptorů v játrech. Zároveň se zvyšuje hladina HDL a slabě i hladina VLDL. Progesteron zvyšuje hladinu LDL. Kombinace estrogenů a gestagenů v CHC je k lipidovému metabolismu neutrální.
Riziko krvácivé cévní mozkové příhody (CMP) se nezvyšuje, mírně narůstá riziko ischemické CMP s RR 0,89–2,99. V kombinaci s arteriální hypertenzí či kouřením však riziko významně stoupá na RR 3,1–7,2, respektive 10,7. Závislost byla pozorována na dávce EE, nikoli typu gestagenu. Dle některých studií migrenózní bolesti hlavy zvyšují riziko CMP dvakrát a v kombinaci s CC 6krát.
Karcinom prsu a hrdla děložního
Doba užívání nízkodávkované antikoncepce je relativně krátká pro zjištění možné závislosti rozvoje karcinomu prsu a užívání CC. Studie proliferace prsní tkáně ukazují rozdíl mezi nuliparami a ženami, které již rodily. U nulipar zvyšuje CC proliferaci prsní tkáně ve srovnání s neuživatelkami i se ženami, které již rodily. Není zcela jasně prokázána souvislost mezi stimulací proliferace a kancerogenezí. Závěry Collaborative Group on Hormonal Factors in Breast Cancer opřené o reanalýzu 54 studií s 53 297 ženami s karcinomem prsu a 100 239 kontrolami jsou považovány za závazné. Relativní riziko uživatelek CC je nízké – 1,24 (CI 95 %: 1,15–1,33), po vysazení klesá během 10 let na 1,16, respektive 1,07 a jeho míra závisí na věku užívání. Karcinomy prsu u uživatelek jsou méně pokročilé. Vyšší riziko vykazují ženy, které začaly antikoncepci užívat před svým 20. rokem. Ve studii Women’s CARE nebyl prokázán vliv nízkodávkované antikoncepce na riziko karcinomu prsu. Nízkodávkovaná antikoncepce nezvyšuje riziko karcinomu prsu ani u nositelek mutací BRCA 1 a BRCA 2.
Současná CC není schopna ovlivnit benigní léze prsu ani mastodynie, jak bylo uváděno u starších preparátů. Stejně tak absolutní většina epidemiologických studií nenachází vztah mezi užíváním CC a karcinomem prsu. Hodnoty relativního rizika se pohybují mezi 1,0 a 2,0 a nejsou statisticky významné.
Nižší prevalence užívání bariérové kontracepce v kombinaci s častějším výskytem ektopie jsou teoretickým podkladem zvýšení výskytu karcinomu hrdla děložního u uživatelek CC s RR 1,2–3,5. Nicméně po očištění od dalších rizikových faktorů (kouření, koitarché, počet sexuálních partnerů) není toto riziko výrazné.
Neantikoncepční přínosy kombinované hormonální antikoncepce
Indikací k podání CC je nejen její antikoncepční účinek, ale také tak zvané neantikoncepční terapeutické účinky.
Tabulka 5: Přínosy a rizika CC
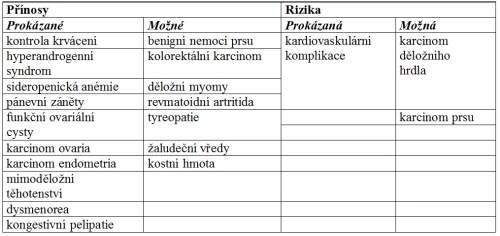
Kombinovaná hormonální antikoncepce:
- je indikována v léčbě poruch menstruačního cyklu ve smyslu plus i minus;
- snižuje riziko opakování mimoděložního těhotenství;
- snižuje riziko pánevních zánětů, snad změnou prostupnosti cervikálního hlenu s RR 0,2–0,3 navzdory prokázané vyšší prevalenci (RR 1,5–3) chlamydiové infekce;
- snižuje riziko tvorby ovariálních cyst, pravděpodobně potlačením folikulogeneze s RR 0,5.
Některé studie naznačují pozitivní vliv užívání COC na tyreopatie, revmatoidní arthritidu a žaludeční vředy, ale klinický význam těchto izolovaných dat je diskutabilní.
Hyperandrogenní syndrom
Při užití nízkodávkovaných preparátů se slabě androgenními progestiny nebo antiandrogeny je CC lékem volby pro syndrom polycystických ovarií (PCOS). Diagnostické kritérium pro PCOS je chronická anovulace nebo porucha menstruačního cyklu (oligomenorea, sekundární amenorea) provázená hyperandrogenémií po vyloučení jiných možných příčin nadbytku androgenů s podpůrnými kritérii poměru LH : FSH větším než 2 a sonografickým nálezem polycystických ovarií.
Pro léčbu akné jsou vhodné preparáty s antiandrogenním progestinem, speciálně pro tuto léčbu registrované.
Existuje několik mechanismů, kterými může CC působit:
- vazba gestagenu na androgenní receptor,
- změna vazebné kapacity pro androgeny,
- ovlivnění produkce SHBG v játrech,
- vytěsnění androgenů z vazby na SHBG,
- ovlivnění periferního metabolizmu testosteronu inhibicí 5alfa reduktázy,
- ovlivnění nadledvinové produkce androgenů.
Mezi antiandrogenní progestiny patří cyproteronacetát, dienogest, chlormadinonacetát a drospirenon.
Estrogeny jsou schopny indukovat tvorbu SHBG a IGFBP v játrech a tím nepřímo snižovat hladinu volného testosteronu. CC rovněž snižuje produkci androgenů v ovariích celkovou supresí jejich činnosti a pravděpodobně i v nadledvinách. Antiandrogenní progestiny jsou schopny snížit aktivitu 5alfa-reduktázy, která je zodpovědná za periferní konverzi testosteronu na účinnější dihydrotestosteron. Signifikantně nižší hladiny testosteronu je dosaženo při kontinuálním podávání.
Syndrom polycystických ovarií je vedle hyperandrogenismu spojen i s hyperestrogenním stavem. O to významnější je zde obecně uznávaný vliv CC na snížení rizika karcinomu endometria.
Kolorektální, ovariální a endometriální karcinom
Ochranný vliv užívání přípravků kombinované hormonální antikoncepce na riziko vzniku kolorektálního karcinomu byl prokázán několika studiemi. Mechanismus je vysvětlován změnou koncentrace žlučových kyselin nebo přímým ovlivněním cestou estrogenních receptorů, prokázaných ve sliznici střeva.
Fernandez v metaanalýze dat z osmi case-control studií stanovil relativní riziko rozvoje kolorektálního karcinomu pro ženy, které užívaly přípravky COC – 0,81 (95% CI: 0,69–0,94), ze čtyř kohortových studií odhadl relativní riziko na 0,84 (95% CI: 0,72–0,97). Souhrnné kombinované relativní riziko ze všech studií bylo 0,82 (95% CI: 0,74–0,92). Délka užívání hormonální antikoncepce není spojena s dalším snížením rizika vzniku kolorektálního karcinomu, silnější ochrana přetrvává do 10 let od vysazení (RR = 0,46; 95% CI: 0,3–0,71).
Teoretický předpoklad ochrany před nádory ovaria a endometria, vycházející z výrazného snížení proliferační aktivity těchto tkání v průběhu užívání COC, byl potvrzen mnoha studiemi případů a kontrol a několika observačními studiemi. U obou je snížení rizika úměrné délce užívání. Pro ovariální karcinom se RR pohybuje mezi 0,3 a 0,7. Schlesselmanova metaanalýza ukazuje snížení rizika karcinomu endometria rostoucí s délkou užívání od 1 do 12 let o 23–70 %.
Riziko karcinomu endometria při užívání COC kratším než 1 rok není změněno, užívání delší než l rok je spojeno s RR 0,4. Totéž platí pro karcinom ovaria s RR 0,5.
Závěr
Cílená volba dávky ethinylestradiolu a gestagenní složky je základem pro možnost úplného využití antikoncepčního a neantikoncepčního potenciálu CC u dané pacientky. Každý originální preparát s sebou přináší prohloubení možnosti individuálního výběru antikoncepční metody. Při hodnocení relativních kontraindikací je vždy nutno kalkulovat s možností nežádoucího otěhotnění, které je, odhlédneme-li od etické stránky věci, svými hormonálními změnami výrazně nebezpečnější než kterýkoli ze soudobých antikoncepčních preparátů.
Přes převahu přínosu CC nad jejími riziky je zcela namístě opatrnost, řádné odebrání anamnézy a odhalení případných rizikových faktorů, které v koincidenci s CC nadměrně zvyšují její rizika.
Tabulka 6: Kontraindikace kombinované hormonální antikoncepce (liší se dle autorů)
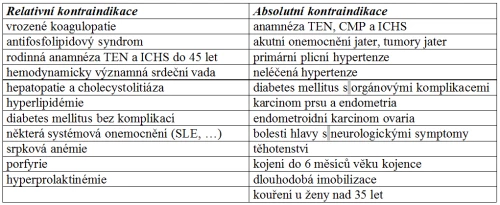
-
Stageman B. H., de Bastos M., Rosendaal F. R. et al. Different combined oral contraceptives and the risk of venous trombosis: systematic review and network meta-analysis. BMJ 2013, 347: I5298; doi: 10.1136
-
Jick H., Jick S. S., Gurewid V. et al.: Risk of idiopathic cardiovascular death and nonfatal venous thromboembolism in women using oral contraceptive with different progestagen components. Lancet, 1995, 346 (8990), p. 1589–93
-
Vasilakis-Scarmozza C., Jick H.: Risk of venous tromboembolism with cyproterone or levonorgestrel contraceptives. Lancet, 2001, 358 (9291), p. 1427–9
-
WHO Collaborative Study of Cardiovascular Disease and Steroid Hormone Contraception: Acute myocardial infarction and combined oral contraceptives: results of an international multicentre case-control study. Lancet, 1997, 349, p. 102–9
-
Thorogood, M.: Stroke and steroid hormonal contraception. Contraception, 1998, 53 Suppl I, S19–25
-
Spinillo A., Gorini G., Piazzi G. et al.: The impact of oral contraception on chlamydial infection among patients with pelvic inflamatory disease. Contrraception, 1996, 54, p. 163–8
-
Vessey M., Metcalfe A., Wells C. et al.: Ovarian neoplasms, functional ovarian cysts and oral contraceptives, BMJ, 1987, 294, p. 1518–20
-
Rabe, T., Kowald, A., Ortmann, J. et. al.: Inhibition of skin 5alfa-reductase by oral contraceptive progestin in vitro. Gynecol Endocrinol, 2000, 14, p. 223–30
-
Fernandez E., la Vecchia C., Franceschi S. et al.: Oral contraceptive use and risk of colorectal cancer. Epidemiology, 1998, 9, p. 295–300
-
Gross T. P., Schlesselman J. J.: The estimated effect of oral contraceptive use on the cumulative risk of epitelial ovarian cancer. Obstet Gynecol, 1994, 83, p. 419–24
-
Schlesselman J. J.: Oral contraceptives and neoplasia of the uterine corpus. Contraception, 1991, 43, p. 557–79
Kurz je již bez kreditace, vhodný k edukaci
Byl pro Vás kurz přínosný? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



