-
Medical journals
- Career
Bolesti při pokročilých gynekologických malignitách a jejich léčba
Authors: Pavla Navrátilová
Authors‘ workplace: Klinika radiační onkologie, Masarykův onkologický ústav a LF MU, přednosta prof. MUDr. Pavel Šlampa, CSc.
Published in: Prakt Gyn 2013; 17(1): 47-52
Category: Oncogynecology: Review Article
Overview
Pacientky s pokročilou gynekologickou malignitou trpí často vážnými komplikacemi vyvolanými nádorovou infiltrací a tlakem na okolní pánevní tkáně a orgány, postižením lymfatických cest a později i komplikacemi ze vzdálených metastáz. Jedním z nejčastějších příznaků pak bývá bolest, zejména chronického charakteru. Zhodnocení a základní léčbu bolesti by měl znát každý lékař jakékoliv specializace. Článek se zabývá praktickými zásadami terapie a možnostmi ovlivnění bolesti při gynekologických malignitách. Zvláštní pozornost je věnována také paliativní radioterapii.
Klíčová slova:
bolest – gynekologická malignita – analgetika – paliativní radioterapieÚvod
V České republice byla za rok 2010 incidence karcinomu děložního čípku 18,5/100 000 žen, karcinomu dělohy 34,8/100 000 a karcinomu ovaria 20,6/100 000 žen [1].I přes zavedený screeningový program jsou stále ještě diagnostikovány pacientky v pokročilých, inoperabilních stadiích nemoci, nebo v některých případech do těchto stadií dospějí i přes úvodní radikální onkologickou léčbu.
Lokálně pokročilé gynekologické nádory způsobují potíže vyplývající z lokální destrukce zdravých tkání a orgánů přímo v pánvi. Jedná se o bolestivé syndromy, komplikace charakteru obstrukce močových cest, ileózního stavu při střevní obstrukci, krvácení při infiltraci orgánů, ascites při implantačních metastázích karcinomu ovaria či lymfedémy dolních končetin při postižení lymfatických cest, útlaku krevních cév, cévní trombózy. Mohou se také objevit příznaky ze vzdálených metastáz, jako dyspnoe a kašel při metastatickém onemocnění plic, bolesti v pravém podžebří a úporný singultus při metastatickém postižení jater nebo dyspepsie při ascitu [2].
Léčba bolesti
Rozpoznání etiologie bolesti – klíč k její léčbě
Základním pilířem léčby bolesti je farmakoterapie. Abychom k bolesti a její terapii správně přistupovali, musíme si uvědomit rozdílnou etiologii bolesti a s ní související rozdílné přístupy k léčbě (tab. 1) [3,4].
Table 1. Přehled typů bolesti, jejich subjektivní charakteristika, mechanizmus vzniku, zdroje a terapeutická ovlivnitelnost 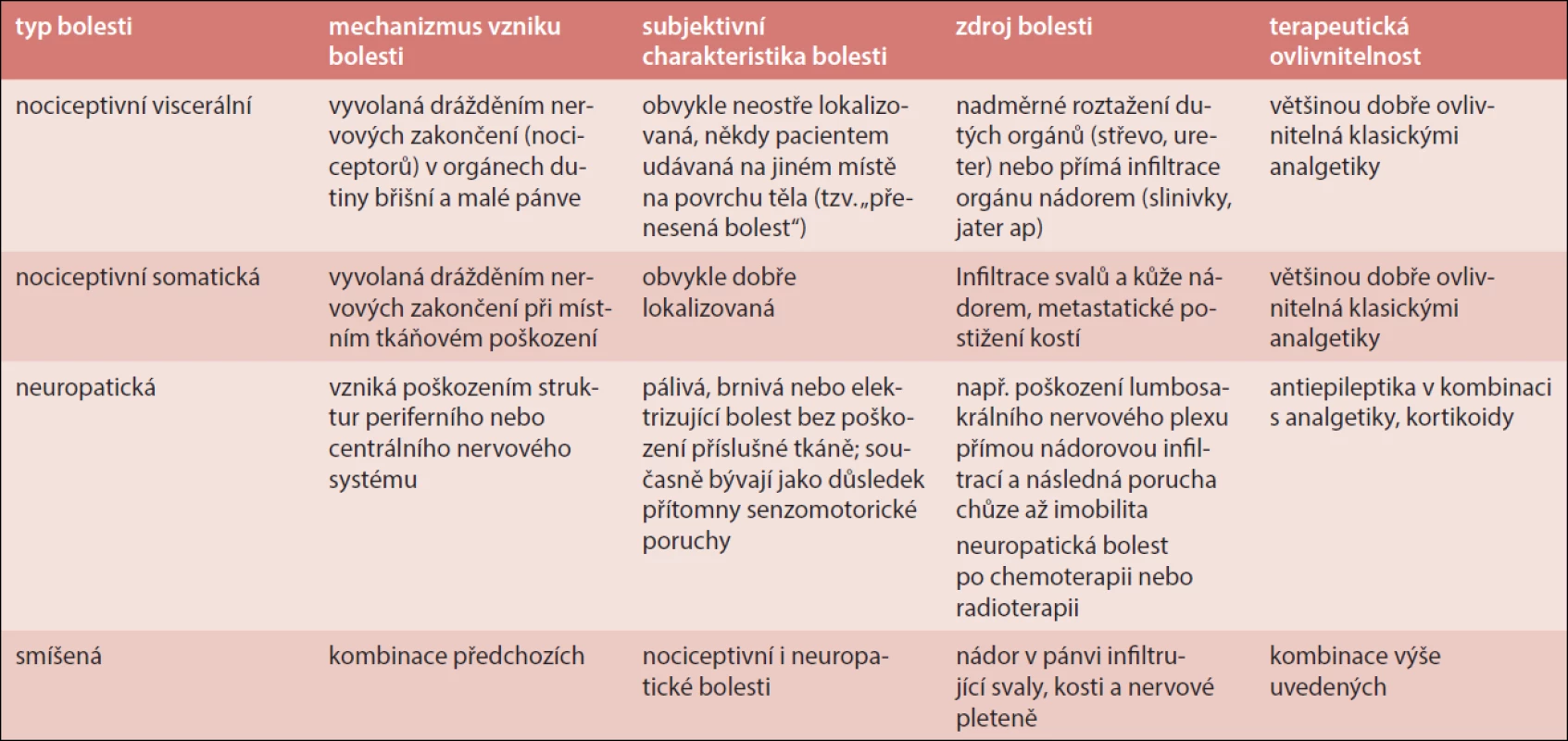
Pro vytvoření představy o etiologii bolesti je stěžejním bodem anamnéza. Při zjišťování anamnézy bolesti pokládáme pacientce tyto otázky:
- kde to bolí (lokalita)
- jak moc to bolí (intenzita)
- jaká bolest je (pocitový charakter bolesti)
- jak dlouho trvá (časový charakter bolesti – chronická, akutní)
- zdali je trvalá nebo epizodická
- zdali existují úlevové polohy, nebo naopak momenty prohlubujících bolest (pohyb, kašel, defekace)
Následuje pečlivé fyzikální vyšetření, a teprve poté můžeme s pacientkou diskutovat o možnostech léčby bolesti, zvažovat vedlejší nežádoucí účinky a zátěž, kterou může léčba přinášet.
Farmakoterapeutický management
Terapie bolesti pokročilých gynekologických malignit se řídí obecnými zásadami léčby bolesti. I zde se uplatňuje klasický 3stupňový žebříček bolesti WHO (schéma), s postupnou titrací analgetik od nejslabších po nejsilnější, od nízkých dávek k vyšším. Při silných bolestech se uplatňuje metoda tzv. výtahu, s přechodem z I. stupně analgetik ihned na silné opioidy (s vynecháním II. stupně – slabých opioidů).
Schéma. Klasický 3stupňový žebříček bolesti dle WHO 
Pacientka indikovaná pro charakter a míru bolestí k podávání silných opioidů musí být vždy současně vybavena tzv. záchrannou medikací – tzn. analgetiky užívanými při průlomové bolesti, a to v adekvátní účinné dávce. Záchrannou medikací mohou být jak neopioidní, tak i opioidní analgetika s rychlým nástupem účinku (příklady v tab. 2) [3,4].
Table 2. Příklady a charakteristika analgetik užívaných při průlomové bolesti (záchranná medikace) 
Hlavní nevýhodou neopioidních analgetik a slabých opioidů je jejich stropový efekt, tj. skutečnost, že při překročení maximální doporučené denní dávky již nedochází ke zvyšování analgetického účinku, nýbrž pouze k zesilování účinků nežádoucích.
Oproti tomu, opioidní analgetika nemají stropový efekt. Současně bylo zjištěno, že neexistuje vztah mezi základní a záchrannou medikací. Ve většině případů obvyklá dávka záchranné medikace odpovídá 10–20 % celkové denní dávky. Zásadou je opět opatrná titrace léku.
Monitorování nežádoucích účinků opioidů
Velmi důležité je, krom analgetického efektu, pečlivě sledovat také nežádoucí účinky opioidů, snažit se o jejich prevenci a neustálé přehodnocování s ohledem na stav, potřeby a přání pacientky. Nežádoucí účinky mohou být obzvláště zvýrazněny při kumulaci aktivních metabolitů opioidů (především morfinu), například při renální insuficienci. V těchto případech dáváme přednost fentanylu a buprenorfinu – látkám, jejichž metabolizmus je na funkci ledvin nezávislý a jejichž dávku není třeba redukovat.
Mezi nejčastější nežádoucí účinky opioidů patří zácpa, nevolnost, sucho v ústech, únava a ospalost [4]. Zatímco nevolnost je přechodného charakteru a po několika dnech podávání opiátů vymizí, zácpa je problém chronický. Oběma potížím se dá vyvarovat pečlivým poučením pacientky a vybavením symptomatickou medikací: prokinetiky (např. metoklopramid), antiemetiky (např. thietylperazon) a laxativy. Mezi časté chyby patří vysazení opioidu pro nevolnost a zvracení ihned po jeho nasazení bez podpůrné medikace a označení stavu za intoleranci daného léku. Současně se vyvíjejí stále nové lékové formy, které by tyto nežádoucí účinky opioidů minimalizovaly. Příkladem může být nový přípravek Targin®, registrovaný v loňském roce v ČR, který řeší problém chronické zácpy při podávání opioidů bez nutnosti užívání laxativ. Zahrnuje v sobě fixní kombinaci opioidu – oxykodonu a antagonisty opioidních receptorů ve střevě – naloxonu, který tímto mechanizmem snižuje výskyt zácpy.
Nutno dodat, že lékaři nejvíce obávaný útlum dechového centra je velmi vzácný a rozvíjí se současně s celkovou sedací pacienta. Vyšší riziko je u pacientů s těžkou poruchou ventilačních funkcí (např. CHOPN), při rychlém navyšování dávky (více než o 50 % denně), při bolusovém nitrožilním podání silných opioidů nebo při současném podávání sedativních léků (benzodiazepiny, antipsychotika). Rovněž riziko rozvoje obávané psychické závislosti je velmi nízké (okolo 1 %). Výjimkou jsou pacienti s drogovou anamnézou nebo pacienti s psychiatrickým onemocněním [4].
Pokud se zvoleným opioidem nedaří bolest zmírnit a další navyšování dávky není možné vzhledem k závažným nežádoucím účinkům (zmatenost, útlum, zvracení, zácpa a další) nebo se podařilo bolest zmírnit, ale léčba již působí závažné nežádoucí účinky, které se nám nedaří podpůrnou léčbou zvládnout, přichází na řadu rotace opioidů (tzn. změna druhu podávaného opioidu). Vychází se z celkové denní dávky původního opioidu (součet pravidelných a záchranných dávek za 24 hodin) a pomocí tabulky ekvianalgetických dávek (tab. 3) [3,5] lze vypočítat dávku nového opioidu. Pokud je důvodem rotace nedostatečně tlumená bolest v kombinaci s nežádoucími účinky, pak lze podat plnou vypočítanou ekvianalgetickou dávku. Pokud jsou však důvodem rotace pouze nezvladatelné nežádoucí účinky a analgetizace je dostatečná, doporučuje se vypočítanou ekvianalgetickou dávku snížit až o 50 %.
Table 3. Ekvianalgetické dávky opioidů (podle pokynů pro farmakoterapii nádorové bolesti 2009) 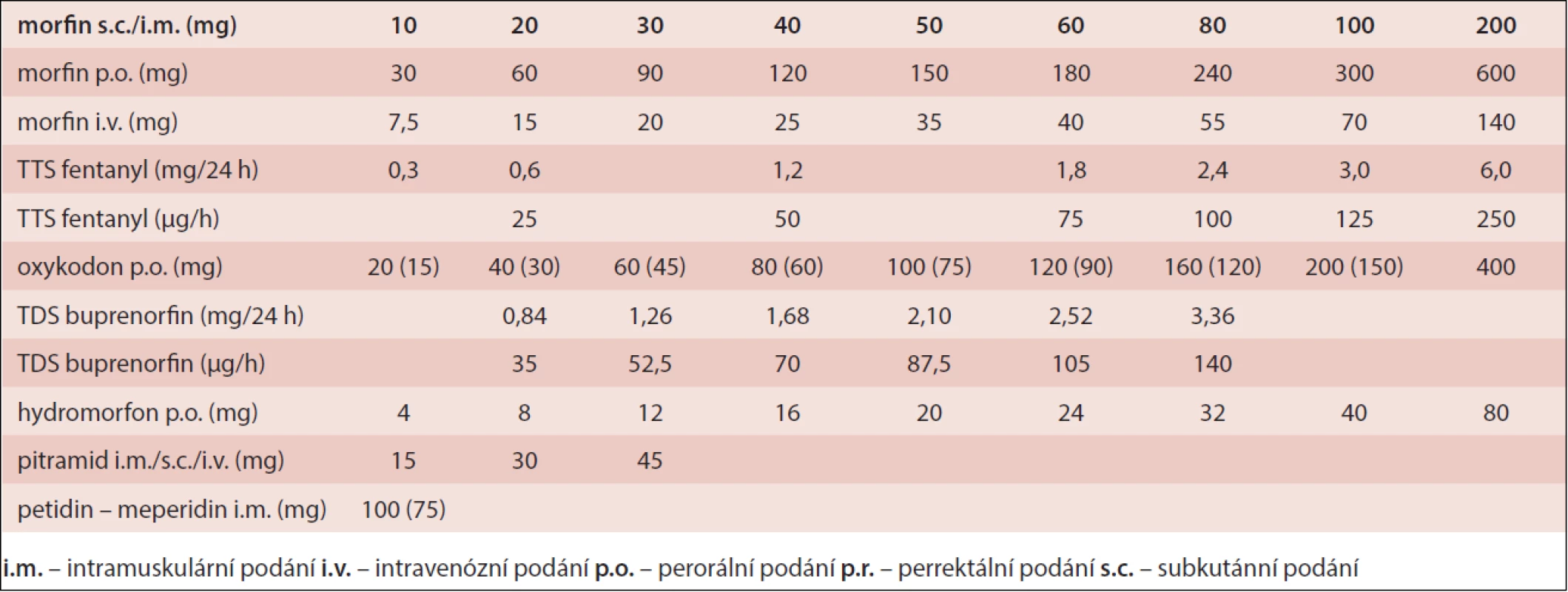
Přepočet je pouze orientační a je nutné myslet na interindividuální rozdíly ve vnímavosti pacientů na opioidy [3,4].
Koanalgetika
Samostatnou kapitolou v léčbě bolesti jsou koanalgetika. Jedná se o léky, které se primárně uplatňují v jiných indikacích, než je bolest. Většinou se přidávají k analgetikům ke zvládnutí tišení bolesti, v některých případech se užívají i samostatně jako léky první volby (např. antiepileptika u neuropatické bolesti). Patří sem široká paleta lékových skupin, od antidepresiv, antiepileptik přes ketamin, bisfosfonáty, myorelaxancia až po kortikoidy.
Kortikoidy
Poslední léková skupina – kortikoidy – působí analgeticky, antiflogisticky a důležitý je i jejich účinek antiedematózní (redukce otoku v okolí nádoru). Nejčastěji užívaným kortikoidem je dexametazon v koanalgetické 1 denní dávce 4–8 mg a prednizon v dávce 5–20 mg. Vyšší dávky se užívají při plexopatiích, syndromu míšní komprese a podobně. Jako prevence gastrointestinální toxicity se kombinují s inhibitory protonové pumpy. Při nasazení kortikoidů je nutno si předem ujasnit důvody pro jejich nasazení a určit si symptomy, které budou hodnoceny jako ukazatele odezvy na léčbu (nemusí se jednat pouze o bolest, ale také současně o ovlivnění chuti k jídlu, nevolnosti, dyspnoe, a podobně). Pokud symptomy neodpovídají na léčbu, pak by kortikoterapie měla být ukončena (5–7denní terapeutický test). Léčba by se měla řídit dle klinického stavu pacientky a po diskusi s ní. Měla by být užita nejnižší účinná dávka, kterou bychom se měli vždy snažit nalézt. U pacientek, které mohou profitovat z kortikoterapie v posledních týdnech svého života, není nutné přikládat takovou váhu vedlejším nežádoucím účinkům, naopak u pacientek s dlouhodobou prognózou je jejich monitorování nezbytné.
Antiepileptika (antikonvulziva), antidepresiva
Další, často užívanou skupinou koanalgetik jsou antiepileptika – antikonvulziva. Konkrétně gabapentin a pregabalin. Jsou indikována zejména pro terapii neuropatické bolesti, ať už nádorové nebo poléčebné etiologie (polyneuropatie po chemoterapii, plexopatie po radioterapii). Dobrý efekt u neuropatické bolesti zaznamenávají i tricyklická antidepresiva, například amitryptilin. Pro tuto medikaci vždy platí zahájení nízkou dávkou (nejčastěji na noc) a pomalá titrace (navyšování dávky) léku. Pokud se efekt nedostaví, vysadit neúčinný preparát a titrovat nový.
Invazivní anesteziologické postupy
Systémovým podáváním analgetik a koanalgetik dle analgetického žebříčku WHO lze dosáhnout dostatečného zmírnění bolestí u 80–90 % onkologicky nemocných. U zbývající části pacientů však samotné systémové podání nestačí. Jednou z možných strategií řešení těchto situací je užití invazivních anesteziologických postupů. Jejich společným principem je přechodné nebo trvalé přerušení převodu bolestivých stimulů na úrovni periferního nebo centrálního nervového systému aplikací různých chemických látek do blízkosti příslušných nervových struktur. Těmito specifickými invazivními postupy se zabývají specializované ambulance léčby bolesti [3,4], jejichž přehled je dostupný na internetu [6].
Paliativní radioterapie pánve
Při bolestivých stavech způsobených lokálně pokročilým nádorem v oblasti pánve může být užitečná také paliativní radioterapie pánve [7–13]. V některých případech může dojít ke zmenšení nádorové masy, a tím k uvolnění nádorové obstrukce. Neméně důležitý je účinek analgetický a hemostyptický.
Radioterapii dělíme na zevní – teleradioterapii [13] a vnitřní – brachyterapii, při níž se pomocí aplikátoru umístí zdroj záření do těsné blízkosti nádoru (např. intravaginálně).
Při brachyterapii je aplikována vysoká dávka s prudkým spádem do okolí, a tím se snižuje radiační zátěž okolních zdravých orgánů. Většinou se volí jednoduché techniky ozařování, krátká frakcionační schémata s vyšší jednotlivou dávkou na frakci, vždy s ohledem na celkový klinický stav pacientky a potíže, které jsou nádorem vyvolány.
Analgetický efekt radioterapie nastupuje většinou v průběhu 2 týdnů. S tímto faktem úzce souvisí již výše zmiňovaný klinický stav a prognóza pacientky. Pokud předpokládáme délku života v měsících, provedení radioterapie jistě svůj smysl má. Jakmile však délku života počítáme ve dnech, maximálně několika týdnech, v tu chvíli se radioterapie stává pro pacientku pouze zátěží, neefektivní léčebnou metodou, jejíhož efektu se pacientka často ani nedožije.
Po radioterapii může dojít k úplné nebo částečné úlevě od bolesti se snížením dávek podávaných analgetik, a tím i úlevě od vedlejších nežádoucích účinků. Délka trvání analgetické odezvy je velmi individuální, v literatuře se udává široké rozmezí 4 měsíců až 1 roku.
Paliativní radioterapie má nejen efekt analgetický, ale také hemostyptický. Při krvácení volíme vyšší jednorázovou hemostyptickou dávku. Efekt se dostaví s odstupem dnů až týdnů, nikoliv ihned, jak je tomu např. u operačního zákroku při ligaci či embolizaci cévy. Naopak, těsně po ozáření může dojít ke zhoršení samotného krvácení a mohou se přidat průvodní jevy z poradiační iritace nejbližších zdravých orgánů, jako je močový měchýř, močové cesty a kličky tenkého střeva. Projeví se přechodným častějším močením a dysuriemi. Podráždění střev se projeví řidší stolicí až průjmem, tenezmy, eventuálně se může objevit i nauzea. Všechny tyto příznaky jsou velice dobře zvládnutelné podpůrnou medikací, kterou jsou pacientky profylakticky vybaveny a o jejím užití podrobně edukovány.
Závěr
Zásadní je komplexní pohled na bolest, její příčiny a důsledky (somato-psycho-spirito-sociální), znalost možných způsobů léčby bolesti a patřičně jich v praxi využívat.
V dnešní době při současných možnostech léčby by již pacientky neměly trpět bolestí. V opačném případě se jedná o pacientky špatně léčené.
Doručeno do redakce dne 27. ledna 2013
Přijato po recenzi dne 7. února 2013
MUDr. Pavla Navrátilová
pavla.navratilova@mou.cz
Klinika radiační onkologie
Masarykův onkologický ústav a LF MU, Brno
www.mou.cz
Sources
1. Epidemiologie zhoubných nádorů v České republice. Dostupné z WWW: <http://www.svod.cz> .
2. Booth S, Bruera E, Tate T (eds). Paliative care consultations in gynaeoncology. University Press Oxford: Oxford 2004. ISBN 019–852806-X.
3. Sláma O, Adam Z, Ševčík P. Onkologická bolest a její léčba. Kap. 18.3. In: Souček M, Špinar J, Vorlíček J (eds) et al. Vnitřní lékařství: Vol. 2 : 1515–1519.
4. Sláma O, Kabelka L, Vorlíček J (eds) et al. Paliativní medicína pro praxi. Galén: Praha 2007. ISBN 978–80–7262–505–5.
5. Vyzula R (ed) et al. Modrá kniha České onkologické společnosti. 15. vyd. (platné od 1. 8. 2012). Brno: Česká onkologická společnost ČLS JEP: 185(tab. 4). ISBN 978–80–904989–0–7. Dostupné z WWW: <http://www.linkos.cz/informace-pro-praxi/modra-kniha/ 30-farmakoterapie-nadorove-bolesti/>.
6. Dostupné z WWW: <http://www.linkos.cz/lecba-bolesti-2/mapa--pracovist-pro-lecbu-bolesti/>.
7. Princ D, Garčicová J, Šlampa P et al. Radiační onkologie v praxi. 3. vyd. Masarykův onkologický ústav: Brno 2011. ISBN 978–80–86793–19–1.
8. Spanos WJ jr, Clery M, Perez CA et al. Late effect of multiple daily fraction palliation schedule for advanced pelvic malignancies (RTOG 8502). Int J Radiat Oncol Biol Phys 1994; 29(5): 961–967.
9. Spanos WJ jr, Pajak TJ, Emami B et al. Radiation palliation of cervical cancer. J Natl Cancer Inst Monogr 1996 (21): 127–130.
10. Kraiphibul P, Srisupundit S, Kiatgumjaikajorn S, Pairachvet V. The experience in using whole pelvic irradiation in management of massive bleeding from carcinoma of the uterine cervix. J Med Assoc Thai 1993; 76(Suppl 1): 78–81.
11. Tan HS. Use of high dose rate gammamed brachytherapy in the palliative treatment of gynaecological cancer. Ann Acad Med Singapore 1994; 23(2): 231–234.
12. Corn BW, Lanciano RM, Boente M et al. Recurrent ovarian cancer. Effective radiotherapeutic palliation after chemotherapy failure. Cancer 1994; 74(11): 2979–2983.
12. Gelblum D, Mychalczak B, Almadrones L et al. Palliative benefit of external-beam radiation in the management of platinum refractory epithelial ovarian carcinoma. Gynecol Oncol 1998; 69(1): 36–41.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inPractical Gynecology

2013 Issue 1-
All articles in this issue
- PROJEKT 35: možná cesta ke zlepšení přežití žen ve věku do 35 let postižených karcinomem prsu
- Význam správného odběru rodinné anamnézy u onkologicky nemocných
- Behaviorální determinanty osteoporózy: je třeba edukovat ženy v prevenci osteoporózy?
- Problematika rozsáhlého porodního poranění a komplikace s ním spojené
- Epigenetika v individualizované péči o ženy se zhoubným nádorem
- Indikace mamografie, ultrasonografie a vyšetření prsu magnetickou rezonancí u mladých žen
- Souběh těhotenství, kojení a karcinom prsu
- Vývoj epidemiologie zhoubných nádorů prsu u žen dle nových dat Národního onkologického registru ČR a dalších datových zdrojů
- Antiangiogenní léčba karcinomu ovaria
- Bolesti při pokročilých gynekologických malignitách a jejich léčba
- Molekulární cytogenetika v diagnostice genetických abnormalit u karcinomu děložního hrdla
- Screening tyreopatií v těhotenství
- Negynekologické kontraindikace „office“ hysteroskopie prováděné v ambulanci
- Vliv některých anestetik a sedativ na sexuální halucinace pacienta: podceňované forenzní riziko pro lékaře
- Raritní komplikace děložní myomatózy: kazuistiky
- Practical Gynecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Vliv některých anestetik a sedativ na sexuální halucinace pacienta: podceňované forenzní riziko pro lékaře
- Problematika rozsáhlého porodního poranění a komplikace s ním spojené
- Raritní komplikace děložní myomatózy: kazuistiky
- Indikace mamografie, ultrasonografie a vyšetření prsu magnetickou rezonancí u mladých žen
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

