Priebeh ochorenia u pacientov s diferencovaným mikrokarcinómom štítnej žľazy pri použití rôznych liečebných postupov
Authors:
Marianna Grigerová 1,2; Martin Griger 3; Emília Mojtová 1,2; Ján Podoba 1,2
Authors‘ workplace:
Klinika endokrinológie LF SZU, Bratislava, Slovenská republika
1; Onkologický ústav svätej Alžbety, s. r. o, Bratislava, Slovenská republika
2; EuroPainClinics Bratislava, Slovenská republika
3
Published in:
Vnitř Lék 2016; 62(Suppl 3): 17-21
Category:
Original Contributions
Overview
Liečba nízkorizikových štádií diferencovaného karcinómu štítnej žľazy patrí v súčasnosti ku kontroverzným oblastiam manažmentu tyreoidálnych nádorov. Významné svetové odborné spoločnosti a renomované pracoviská pokladajú lobektómiu za dostatočný terapeutický výkon pri papilárnom mikrokarcinóme v štádiu pT1a cN0cM0. Napriek tomu pretrvávajú aj iné názory a liečebné postupy, ktoré väčšinou vedú k zbytočnému nadliečovaniu pacientov, a tým k zhoršenej kvalite ich života. V našej práci sme zisťovali priebeh choroby u pacientov s diferencovaným mikrokarcinómom štítnej žľazy pri použití rôznych liečebných postupov: lobektómia, totálna tyreoidektómia, totálna tyreoidektómia s profylaktickou lymfadenektómiou centrálneho kompartmentu a totálna tyreoidektómia s následnou liečbou rádiojódom. Popri výbornej prognóze sme nezistili žiadne klinicky významné rozdiely v priebehu ochorenia. Vyplýva z toho, že lobektómia je dostatočným terapeutickým výkonom pri diferencovanom mikrokarcinóme štítnej žľazy bez dokázaných metastáz.
Kľúčové slová:
diferencovaný mikrokarcinóm štítnej žľazy – manažment – nadliečenie – priebeh choroby
Úvod
Mikrokarcinómy (nádory ≤ 10 mm, pT1a) tvoria asi 30 % diagnostikovaných diferencovaných karcinómov štítnej žľazy a sú hlavným dôvodom vzostupu incidencie karcinómu štítnej žľazy v posledných desaťročiach. V ich manažmente zostáva stále viacero kontroverzií. Väčšinou ide o náhodne zistené nádory pri histologickom vyšetrení žľazy po jej chirurgickom odstránení alebo menej často sa odhalia pri ultrazvukovom vyšetrení. Vo väčšine prípadov (78–99 %) ide o papilárne mikrokarcinómy (mikro-PTC) [1–3].
Vzhľadom na fakt, že úmrtnosť na toto ochorenie je veľmi zriedkavá, snahou liečby je redukovať vznik lokálnej recidívy a vzdialených metastáz pri minimálnom iatrogénnom poškodení pacienta.
Implementácia poznatkov medicíny založenej na dôkazoch do praxe priniesla významné zmeny v manažmente týchto pacientov. Mnohé štúdie dokázali nízku agresivitu mikro-PTC, a preto sa upustilo od komplexnej onkologickej liečby tohto ochorenia. V súčasnosti väčšina významných svetových odborných spoločností a renomovaných pracovísk pokladá lobektómiu za dostatočný terapeutický výkon pri mikro-PTC bez klinicky dokázaných metastáz, v štádiu pT1a cN0cM0. Totálna tyreoidektómia (TTE) sa odporúča u pacientov s mikro-PTC pri multifokalite postihujúcej oba laloky žľazy, u pacientov s predchádzajúcim ožiarením krku, pri dokázaných uzlinových alebo vzdialených metastázach a pri familiárnom non-medulárnom karcinóme štítnej žľazy [4]. Štandardné postupy Americkej tyreoidologickej spoločnosti (ATA) najnovšie dokonca pripúšťajú u pacientov s cytologicky potvrdeným mikro-PC bez agresívnych čŕt a bez klinických metastáz alebo lokálnej invázie iba aktívne sledovanie pacienta [5]. Napriek tomu, že moderné odporúčania endokrinologických spoločností (Európska tyreoidálna spoločnosť – ETA a ATA) sú pomerne jednoznačné, nestretli sa všade so súhlasom. Aj na Slovensku sa stále možno stretnúť s pretrvávaním starších a už prekonaných liečebných postupov, s nejednotnosťou terapeutických postupov a zbytočným nadliečovaním pacientov.
Cieľ práce
Cieľom našej práce bolo zistiť priebeh ochorenia u pacientov s histologicky dokázaným diferencovaným mikrokarcinómom štítnej žľazy v štádiu pT1aN0 alebo Nx pri použití rôznych liečebných postupov: lobektómia, TTE, TTE s profylaktickou lymfadenektómiou centrálneho kompartmentu (CK) a TTE s následnou liečbou rádiojódom (RI).
Vyšetrení a metódy
Retrospektívne sme analyzovali súbor 296 pacientov (248 žien a 48 mužov) s diferencovaným mikrokarcinómom štítnej žľazy sledovaných v endokrinologických ambulanciách Onkologického ústavu sv. Alžbety (OUSA) od roku 2000 do júna roku 2016. 16 pacientov malo folikulárny mikrokarcinóm, všetci ostatní mali mikro-PTC.
Zisťovali sme, ako ovplyvnil zvolený terapeutický postup prognózu pacienta. Pacienti boli operovaní na rôznych chirurgických pracoviskách z celého Slovenska (15 pracovísk s často vykonávanými operáciami štítnej žľazy a 5 pracovísk s príležitostnými výkonmi na štítnej žľaze). O rozsahu operácie a ďalšej liečbe RI rozhodovali väčšinou lokálni lekári (chirurgovia a endokrinológovia). Do našej starostlivosti sa pacienti dostali až po histologickom určení diagnózy diferencovaného mikrokarcinómu.
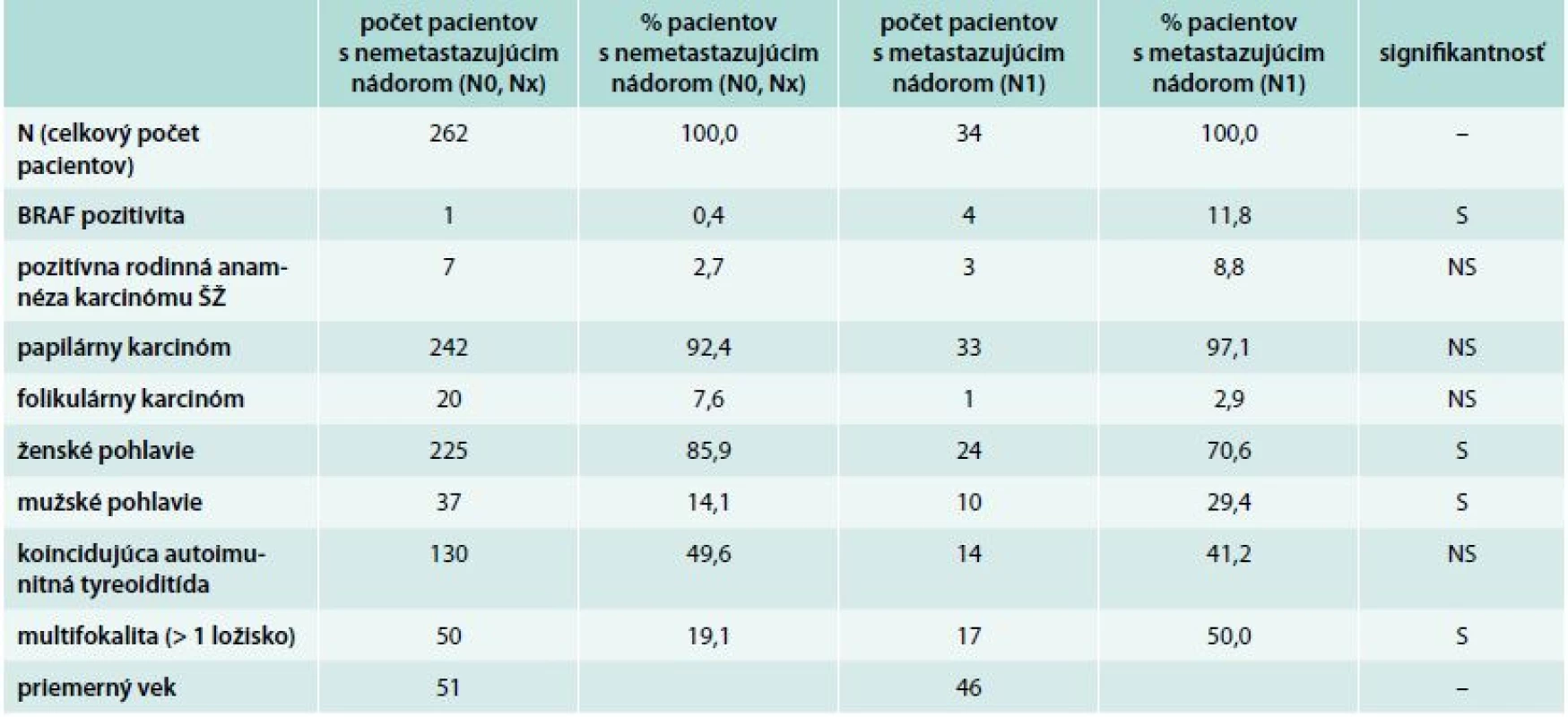
Štatistickú významnosť zistených rozdielov (tab. 1) sme vyhodnotili metódou podľa Newcombe [6] v kalkulátore http://vassarstats.net.
Výsledky
Celkovo sme zistili veľmi dobrú prognózu ochorenia. Iba u 6 pacientov (2 %) z celého súboru ochorenie perzistuje. U 4 z nich ide len o minimálnu laboratórnu perzistenciu (vzostup stimulovanej hladiny tyreoglobulínu) bez klinicky manifestných a zobrazovacími metódami odhalených metastáz. U 2 (0,7 %) sú metastázy prítomné aj klinicky.
Z celého súboru pacientov s tyreoidálnym mikrokarcinómom (296 pacientov) sa u 264 (89 %) v čase diagnózy nádoru nezistili metastázy. 228 pacientov bolo v štádiu pT1aNx, tj. nemali profylakticky exstirpované a histologicky vyšetrené lymfatické uzliny CK a 36 pacientov v štádiu pT1aN0, tj. mali negatívny histologický nález pri profylaktickej disekcii CK.
Iba 20 pacientov (7 %) z celého súboru malo vykonanú v súčasnosti odporúčanú lobektómiu, 2 pacienti mali ponechanú celú štítnu žľazu in situ (nádor bol resekovaný v cyste ductus thyreoglossus). Ostatní pacienti mali realizovanú TTE. U žiadneho pacienta s lobektómiou, ani u pacientov s ponechanou štítnou žľazou sme nepozorovali perzistenciu ani recidívu ochorenia. Lobektómia bola teda dostatočným chirurgickým výkonom.
Celkovo bola vykonaná profylaktická disekcia CK u 52 pacientov bez klinicky zjavných metastáz (cN0). U 16 (31 %) bol histologický nález na lymfatických uzlinách pozitívny v zmysle uzlinových mikrometastáz (pN1a). Napriek liečbe RI ochorenie perzistuje u jedného z týchto pacientov (6 %). Z 228 pacientov bez histologického vyšetrenia uzlín CK (v štádiu pNx) perzistuje ochorenie u 2 (0,9 %). Pacienti s realizovanou disekciou CK nemali teda lepšiu prognózu.
88 pacientov (34 %) bez potvrdených uzlinových metastáz (N0 alebo Nx) absolvovalo liečbu RI s priemernou kumulatívnou dávkou 237 mCi na pacienta. 176 (66 %) pacienti liečbu RI nedostali. V prvej skupine pacientov liečených RI sme v 1–16-ročnom sledovaní nezistili lokálnu recidívu ochorenia, ani vznik uzlinových metastáz na krku. V druhej väčšej skupine bez liečby RI sa dokázali metastázy u 2 pacientov (1 %) po 6 a 12 rokoch sledovania. Obaja nemali vykonanú profylaktickú disekciu CK. Súčasne to znamená, že u 99 % pacientov v štádiu pT1aNx alebo N0 bez liečby RI sme v dlhodobom sledovaní nezistili recidívu (graf 1).

Uzlinové metastázy sa dokázali celkovo u 34 pacientov (11 %) celého súboru. U 13 z nich (4,4 %) boli metastázy diagnostikované sonograficky pred operáciou štítnej žľazy. U 11 sa manifestovali hmatnou krčnou lymfadenopatiou a u 2 sa zistili náhodne pri USG vyšetrení. U 3 pacientov (1 %) sa zistilo metastatické postihnutie lymfatických uzlín pri pooperačnom USG vyšetrení, tj. išlo o nepoznané metastázy pred operáciou. Všetky tieto metastázy boli lokalizované v laterálnom krčnom kompartmente (pT1aN1bMx). Tento typ karcinómu je vysoko rizikový a logicky vyžaduje komplexnú štandardnú liečbu (vrátane liečby RI) a prísne sledovanie. V našom súbore 296 pacientov sa mikrokarcinóm manifestoval uzlinovými metastázami iba v 5,4 % (tab. 2).
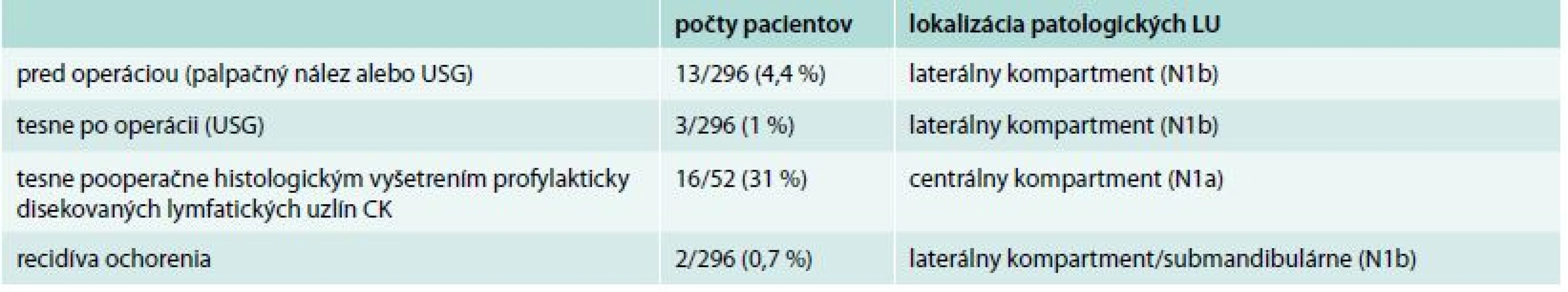
U 16 pacientov sa zistili metastázy tesne pooperačne histologickým vyšetrením profylakticky disekovaných lymfatických uzlín CK (pT1aN1a), tab. 2. Iba u 1 z týchto pacientov ochorenie perzistuje. Ide o pacienta s multifokálnym nádorom, ktorý bol liečený TTE a RI.
U 2 pacientov (obaja iniciálne T1aNxM0) sa zistili uzlinové metastázy v priebehu sledovania ochorenia (6 a 12 rokov od stanovenia diagnózy karcinómu). U jedného sa metastázy diagnostikovali ultrasonografickým vyšetrením krku v lymfatických uzlinách laterálneho kompartmentu. U druhého odhalila patologické lymfatické uzliny v submandibulárnej oblasti scintigrafia, ktorá bola indikovaná na základe merateľnej hladiny tyreoglobulínu. U oboch týchto pacientov bola iniciále vykonaná totálna tyreoidektómia bez adjuvantnej liečby RI. U oboch ochorenie stále perzistuje. Recidívu sme teda zaznamenali u 0,7 % pacientov celého súboru, resp. u 0,8 % pacientov bez dokázaných metastáz. Všetci ostatní pacienti iniciálne bez metastáz (99 %) dosiahli remisiu ochorenia (tab. 2).
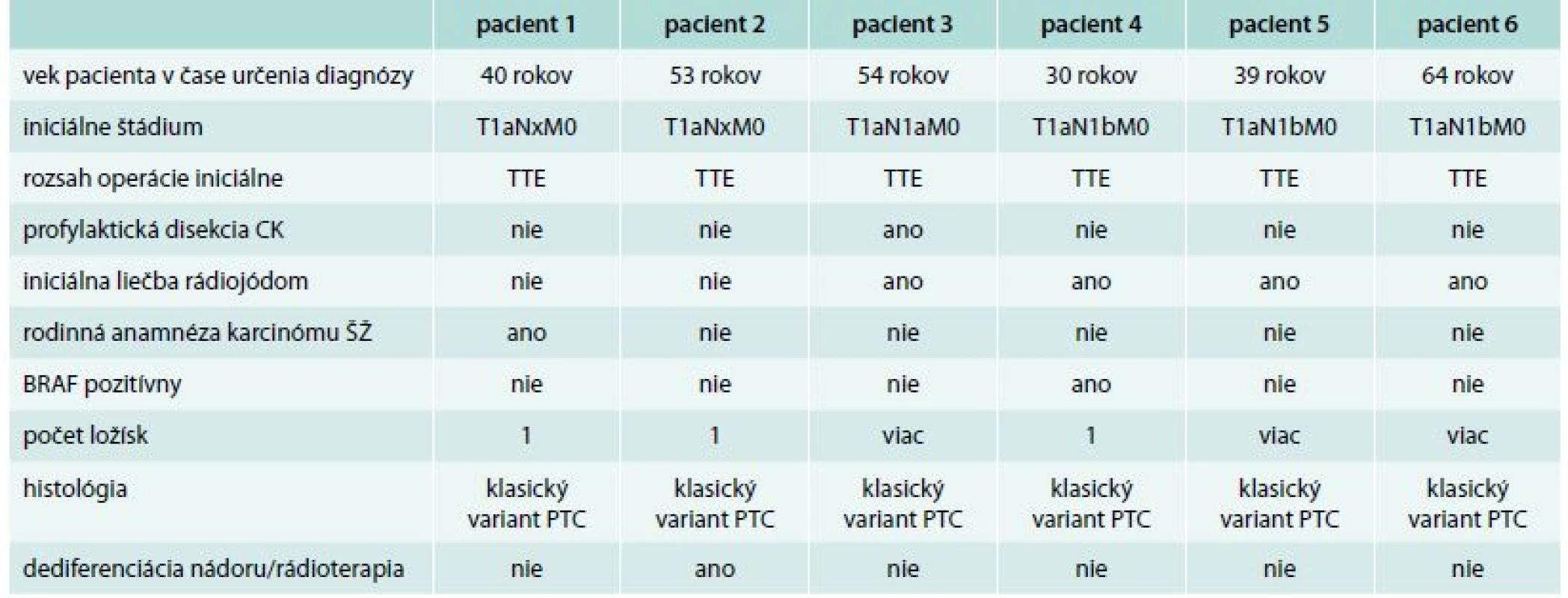
Ľahkú laboratórnu perzistenciu so zvýšenou hladinou tyreoglobulínu bez detekovateľných metastáz sme zaznamenali u 4 pacientov. 1 pacient bol iniciálne v štádiu T1aN1aM0, 2 pacienti T1aN1bM0 a 1 pacient T1aN1bM1 (prítomné boli pľúcne metastázy). Všetci mali iniciálne vykonanú TTE a boli liečení RI. U 2 pacientov (0,7 %) sú metastázy dokázateľné zobrazovacími vyšetreniami (tab. 3).
U pacientov s metastazujúcim nádorom sme zistili častejší výskyt pozitívnej rodinnej anamnézy karcinómu štítnej žľazy (8,8 % vs 2,7 %) a BRAF mutácie (11,8 % vs 0,4 %). Častejšie u nich išlo o multifokálny nádor (50 % vs 19 %) a častejšie boli postihnutí muži (29 % vs 14 %). V tejto skupine mali pacienti nižší priemerný vek v čase stanovenia diagnózy (46 vs 51 rokov). Štatisticky významné sú iba rozdiely v prítomnosti mutácie BRAF a v multifokalite (tab. 1).
Diskusia
Mikro-PTC sa v súčasnosti pomerne často a náhodne zisťujú pri histologickom vyšetrení resekátov štítnej žľazy po operáciách z neonkologickej indikácie. Vzhľadom k tomu, že ide o neočakávaný nález, chirurgovia nemajú dôvod vykonávať profylaktickú lymfadenektómiu CK. Vzniká otázka, ako postupovať u pacienta po lobektómii (menej často po tyreoidektómii) s náhodným nálezom mikrokarcinómu, keď nie je istota, či pacient nemá uzlinové mikrometastázy v CK. Náhodne zistený mikro-PTC bez dokázaných uzlinových metastáz v súčasnosti väčšina autorov pokladá za ochorenie s výbornou prognózou nevyžadujúce intenzívnu komplexnú liečbu ako väčšie tyreoidálne karcinómy.
Avšak aj mikro-PTC môže byť zriedkavo sprevádzaný metastázami do lymfatických uzlín alebo výnimočne do vzdialených orgánov. Tieto metastazujúce nádory sa správajú agresívne a vyžadujú si adekvátnu liečbu. Klinicky sa manifestujú práve lymfadenopatiou. Veľká väčšina mikrokarcinómov sa však zistí náhodne a takéto agresívne správanie nemá. Práve na tieto je zameraná naša práca a úvaha.
Sugitani et al z Cancer Institute Hospital v Tokyu vo svojej práci z roku 2010 uvádzajú, že počas 5 rokov sledovania 230 pacientov s papilárnym mikrokarcinómom bez chirurgickej liečby došlo k nárastu tumoru iba u 7 %. Len u 1 % sa zistili nové metastázy, ktoré boli úspešne liečené [7]. Roku 2014 publikovali Ito et al výsledky 10-ročného aktívneho sledovania chirurgicky neliečených 1 235 pacientov s cytologicky dokázaným mikro-PTC. V 8 % došlo k nárastu nádoru o ≥ 3 mm. U 3,8 % pacientov sa diagnostikovali nové metastázy, taktiež úspešne liečené. Progresia nádoru bola najväčšia u mladších (≤ 40 rokov) a najmenšia u starších pacientov (≥ 60 rokov). Preto autori považujú starších pacientov so subklinickým mikro-PTC za najvhodnejších kandidátov iba na observáciu. Avšak aj u mladších pacientov je možné s chirurgickou liečbou vyčkať až do prechodu nádoru do klinického štádia [8]. Japonskí autori Oda et al vo svojej práci z roku 2016 porovnávali súbor 1 179 pacientov s mikro-PTC iba aktívne sledovaných so skupinou 974 pacientov liečených chirurgicky. Na základe faktu, že onkologické výsledky boli u oboch skupín rovnako výborné, avšak druhá skupina mala viac komplikácii chirurgickej liečby (paréza n. laryngeus recurrens, hypoparatyreóza, krvácanie, jazva, potreba substitúcie levotyroxínom), preferujú u mikrokarcinómov bez dokázaných metastáz aktívne sledovanie pred chirurgickou liečbou [9]. Tento názor zastáva u pacientov v štádiu pT1a cN0cM0 aj Japonská spoločnosť tyreoidálnych chirurgov a Japonská spoločnosť endokrinných chirurgov [10].
V našej práci sme v zhode s najnovšími poznatkami potvrdili výbornú prognózu pacientov s diferencovaným mikrokarcinómom štítnej žľazy, najmä však s náhodne zisteným mikro-PTC. U 31 % pacientov, u ktorých sa vykonala profylaktická disekcia CK, sa dokázali uzlinové mikrometastázy. Rovnaký výskyt možno preto očakávať v celom ostatnom súbore, kde sa tento profylaktický výkon neuskutočnil (štádium pT1aNx). Napriek tomu, že väčšina týchto pacientov liečbu RI nedostala, počas 1–15-ročného sledovania sme okrem 2 z nich (1 %) nezistili progresiu uzlinových mikrometastáz. Vyplýva z toho, že uzlinové mikrometastázy v CK zďaleka nemajú taký význam ako klinicky manifestné uzlinové metastázy, ktoré sa zistia perioperačne sonograficky. K podobnému záveru dospel aj kolektív autorov z Japonska. Vo svojom súbore zistili postihnutie lymfatických uzlín pri profylaktickej disekcii CK až u 66 % pacientov (z celkového počtu 235 pacientov), avšak klinická recidíva bola u tejto skupiny iba v 0,4 % (pacienti neboli liečení RI). Rovnako nízku recidívu 0,65 % zistili aj u pacientov bez profylaktickej disekcie CK [11]. Tieto zistenia potvrdzujú, že profylaktická disekcia CK nezlepšuje prognózu pacientov s mikro-PTC. Preto ju v tejto indikácii neodporúča vykonať ETA [4] ani ATA [5].
Liečbu RI absolvovalo celkovo 34 % pacientov nášho súboru s asymptomatickým mikro-PTC. Išlo skôr o pacientov s dávnejšie diagnostikovaným nádorom. Nepotvrdili sme jej prínos pre prognózu pacienta. Na neopodstatnení tejto liečby u danej skupiny pacientov sa zhodujú všetky svetové odborné spoločnosti [4,5,10].
Rizikovými faktormi metastazovania boli v našom súbore nižší vek, BRAF pozitivita, pozitívna rodinná anamnéza karcinómu štítnej žľazy, multifokalita nádoru, mužské pohlavie. U týchto pacientov odporúčame prísnejšie sledovanie. Nižší vek (< 40 rokov) považujú na základe svojich zistení za nezávislý prediktor progresie mikro-PTC aj Ito et al [8]. Väčšie PTC progredujú naopak častejšie vo vyššom veku [12]. Pozitívnu koreláciu BRAF mutácie s recidívou mikro-PTC publikoval Chen [13]. Aj iní autori potvrdili väčší sklon k metastazovaniu u multifokálnych mikro-PTC [1,14].
Záver
V našom súbore pacienti s mikro-PTC bez liečby RI mali rovnako priaznivý priebeh ochorenia ako pacienti, ktorí RI dostali. Aj keď u významného podielu mikrokarcinómov možno predpokladať uzlinové mikrometastázy v CK, tieto sa u pacientov bez liečby RI v ďalšom sledovaní klinicky nemanifestovali. Preto považujeme v súlade so súčasnými odporúčanými postupmi [4,5] lobektómiu za dostatočnú liečbu pacientov s diferencovaným mikrokarcinómom štítnej žľazy bez prítomných uzlov na kontralaterálnej strane a bez klinicky zjavnej lymfadenopatie (negatívny predoperačný ultrasonografický a peroperačný makroskopický a palpačný nález na uzlinách, cN0). Pre pacienta určite nie je irelevantné, či sa vykoná lobektómia alebo totálna tyreoidektómia, ktorá nie je prínosom. Podmienkou však musí byť, aby endokrinológ predoperačne, aj pri neonkologickej indikácii, dôkladne ultrasonograficky vyšetril aj druhý lalok štítnej žľazy a zameral sa aj na vyšetrenie lymfatických uzlín a aby chirurg peroperačne dôsledne vyšetril aspexiou a palpáciou pretracheálne a paratracheálne lymfatické uzliny (CK). Pacienti po lobektómii s mikro-PTC by mali byť sledovaní skúseným endokrinológom. Vzhľadom na súčasné možnosti ultrasonografickej a laboratórnej diagnostiky možno ojedinelých pacientov s menej priaznivým priebehom zavčasu podchytiť a efektívne liečiť. Malý podiel pacientov s mikro-PTC, ktorý sa manifestuje uzlinovými metastázami, samozrejme vyžaduje komplexnú liečbu, ktorú predstavuje TTE s disekciou CK a postihnutého laterálneho komparmentu, liečba RI a hormonálna supresívna terapia.
MUDr. Marianna Grigerová
marianna@griger.net
Klinika endokrinológie LF SZU, Bratislava, Slovenská republika
www.new.szu.sk
Onkologický ústav svätej Alžbety , s.r.o., Bratislava, Slovenská republika
www.ousa.sk
Doručeno do redakce 30. 8. 2016
Přijato po recenzi 15. 9. 2016
Sources
1. Baudin E, Travagli JP, Ropers J et al. Microcarcinoma of the thyroid gland. Cancer 1998; 83(3): 553–559.
2. Lee J, Rhee Y, Lee S et al. Frequent, Aggressive Behaviors of Thyroid Microcarcinomas in Korean Patients. Endocr J 2006; 53(5): 627–632.
3. Rodriguez JM, Moreno A, Parrilla P et al. Papillary thyroid microcarcinoma: clinical study and prognosis. Eur J Surg. 1997; 163(4): 255–259.
4. Pacini F, Schlumberger M, Dralle H et al. [European Thyroid Cancer Taskforce]. European consensus for the management of patients with differentiated thyroid carcinoma of the follicular epithelium. Eur J Endocrinol 2006; 154(6): 787–803. Erratum in Eur J Endocrinol 2006; 155(2): 385.
5. Haugen BR, Alexander EK, Bible KC et al. 2015 American Thyroid Association Management Guidelines for Adult Patients with Thyroid Nodules and Differentiated Thyroid Cancer: The American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. Thyroid 2016; 26(1): 1–133. Dostupné z DOI: <http://dx.doi.org/10.1089/thy.2015.0020>.
6. Newcombe RG. Interval estimation for the difference between independent proportions: comparison of eleven methods. Stat Med 1998; 17(8): 873–890. Erratum in Stat Med 1999; 18(10): 1293.
7. Sugitani I, Toda K, Yamada K et al. Three Distinctly Different Kinds of Papillary Thyroid Microcarcinoma should be Recognized: Our Treatment Strategies and Outcomes. World J Surg 2010; 34(6): 1222–1231.
8. Ito Y, Miyauchi A, Kihara M et al. Patient Age Is Significantly Related to the Progression of Papillary Microcarcinoma of the Thyroid Under Observation. Thyroid 2014; 24(1): 27–34. Dostupné z DOI: <http://dx.doi.org/10.1089/thy.2013.0367>.
9. Oda H, Miyauchi A, Ito Y et al. Incidences of Unfavorable Events in the Management of Low-Risk Papillary Microcarcinoma of the Thyroid by Active Surveillance Versus Immediate Surgery. Thyroid 2016; 26(1): 150–155. Dostupné z DOI: <http://dx.doi.org/10.1089/thy.2015.0313>.
10. Takami H, Ito Y, Okamoto T et al. Therapeutic Strategy for Differentiated Thyroid Carcinoma in Japan Based on a Newly Established Guideline Managed by Japanese Society of Thyroid Surgeons and Japanese Association of Endocrine Surgeons. World J Surg 2010; 35(1): 111–121. Dostupné z DOI: <http://dx.doi.org/10.1007/s00268–010–0832–6>.
11. Wada N, Duh QY, Sugino K et al. Lymph Node Metastasis From 259 Papillary Thyroid Microcarcinomas: Frequency, Pattern of Occurrence and Recurrence, and Optimal Strategy for Neck Dissection. Ann Surg 2003; 237(3): 399–407.
12. Ito Y, Kudo T, Kobayashi K et al. Prognostic Factors for Recurrence of Papillary Thyroid Carcinoma in the Lymph Nodes, Lung, and Bone: Analysis of 5,768 Patients with Average 10-year Follow-up. World J Surg 2012; 36(6): 1274–1278. Dostupné z DOI: <http://dx.doi.org/10.1007/s00268–012–1423–5>.
13. Chen Y, Sadow PM, Suh H et al. BRAFV600E Is Correlated with Recurrence of Papillary Thyroid Microcarcinoma: A Systematic Review, Multi-Institutional Primary Data Analysis, and Meta-Analysis. Thyroid 2016; 26(2): 248–255. Dostupné z DOI: <http://dx.doi.org/10.1089/thy.2015.0391>.
14. Pyo JS, Sohn JH, Kng G. Detection of Tumor Multifocality Is Important for Prediction of Tumor Recurrence in Papillary Thyroid Microcarcinoma: A Retrospective Study and Meta-Analysis. J Pathol Transl Med 2016; 50(4): 278–286. Dostupné z DOI: <http://dx.doi.org/10.4132/jptm.2016.03.29>.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2016 Issue Suppl 3
Most read in this issue
- Vrozená adrenální hyperplazie v dospělosti
- Mnohočetná endokrinní neoplazie I (Wermerův syndrom) – formy klinické manifestace: 5 kazuistik
- Vitamin D a autoimunitní tyreopatie
- Centrální poruchy funkce štítné žlázy
