-
Medical journals
- Career
Úloha variací genu ABCB4 v etiologii idiopatické cholelitiázy dětského věku
Authors: J. Bronský 1; M. Hřebíček 2; T. Jirásek 3; J. Šperl 4; L. Dvořáková 2; V. Šmajstrla 5; J. Horák 6; M. Jirsa 7; J. Nevoral 1
Authors‘ workplace: Pediatrická klinika UK 2. LF a FN Motol, Praha přednosta prof. MUDr. J. Lebl, CSc. 1; Ústav dědičných metabolických poruch UK 1. LF a VFN, Praha přednosta prof. MUDr. M. Elleder, DrSc. 2; Ústav patologie UK 3. LF a FNKV, Praha přednosta prof. MUDr. V. Mandys, CSc. 3; Klinika hepatogastroenterologie IKEM, Praha přednosta prof. MUDr. J. Špičák, CSc. 4; Privátní zdravotnické zařízení Bormed, Ostrava 5; 1. interní klinika UK 3. LF a FNKV, Praha přednosta prof. MUDr. J. Horák, CSc. 6; Pracoviště experimentální medicíny IKEM, Praha přednosta prof. MUDr. L. Červenka, CSc. 7
Published in: Čes-slov Pediat 2009; 64 (7-8): 337-343.
Category: Original Papers
Overview
Úvod a cíle:
Syndrom nízkofosfolipidové cholelitiázy (LPAC) je definován jako symptomatická cholelitiáza asociovaná s mutacemi v genu ABCB4, který kóduje fosfolipidovou pumpu na kanalikulárním pólu hepatocytu. Na syndrom by mělo být pomýšleno u nemocných splňujících alespoň jedno z následujících malých kritérií: (a) začátek symptomů ve věku do 40 let, (b) opakované obtíže i po cholecystektomii, (c) intrahepatální hyperechogenní ložiska topograficky odpovídající tukovým depozitům podél lumen intrahepatálního žlučového stromu, (d) intrahepatální sludge, (e) mikrolitiáza, (f) rodinná anamnéza cholelitiázy u příbuzných v přímé linii, nebo (g) anamnéza těhotenské intrahepatální cholestázy. V naší studii jsme zkoumali podíl mutací v ABCB4 na etiologii dětské idiopatické cholelitiázy.Pacienti a metody:
Mutační analýzu ABCB4 jsme provedli u 26 vybraných dětských pacientů s idiopatickou cholesterolovou cholelitiázou s rodinnou anamnézou žlučových kamenů či cholestázy a v pěti rodinách mladých žen se suspektní nízkofosfolipidovou cholelitiázou.Výsledky:
U žádného z vyšetřených dětí jsme nenalezli prokazatelně patogenní variantu ABCB4. Naopak u žádného z 15 zachycených heterozygotů pro patogenní mutaci v ABCB4 se cholelitiáza nevyvinula v dětském věku.Závěry:
Klinická kritéria syndromu LPAC nemohou být použita u dětských pacientů, neboť idiopatická cholelitiáza bez cholestázy či známek postižení jater zjevně není v dětském věku asociovaná s mutacemi v genu ABCB4.Klíčová slova:
idiopatická cholelitiáza, MDR3, ABCB4Úvod
Syndrom nízkofosfolipidové cholelitiázy (Low phospholipid-associated cholelithiasis, LPAC, synonymum Gallbladder disease 1, OMIM #600803) je definován jako symptomatická recidivující cholelitiáza asociovaná s mutacemi v genu ABCB4 (Gen ID: 5244), který kóduje exportní pumpu MDR3 pro fosfolipidy lokalizovanou v kanalikulární membráně hepatocytu [1, 2].
Na syndrom by mělo být pomýšleno v případě anamnézy symptomatické cholelitiázy splňující alespoň jedno z následujících malých kritérií:
- (a) začátek symptomů ve věku pod 40 let,
- (b) opakované obtíže i po cholecystektomii,
- (c) intrahepatální hyperechogenní ložiska topograficky odpovídající tukovým depozitům podél lumen intrahepatálního žlučového stromu,
- (d) intrahepatální sludge,
- (e) mikrolitiáza,
- (f) rodinná anamnéza cholelitiázy u příbuzných v přímé linii, nebo
- (g) anamnéza těhotenské intrahepatální cholestázy [3].
Syndromem LPAC trpí méně než 5 % všech pacientů s cholelitiázou. Při analýze žluči od pacientů s LPAC bývá ve žluči zjištěno větší množství krystalů monohydrátu cholesterolu, nízká koncentrace fosfolipidů, vysoký poměr cholesterol/fosfolipidy a vysoký saturační index cholesterolu. Lokalizace mutací v konzervované oblasti genu ABCB4 a jejich typ (nulové mutace však nebyly nikdy nalezeny v obou alelách ABCB4 u téhož pacienta) poukazují na významný podíl genu ABCB4 v patogenezi syndromu LPAC a vysvětlují fenotypové projevy a změny ve složení žlučových lipidů na podkladě parciálního deficitu proteinu MDR3 (ABCB4).
Kromě LPAC mohou mutace v genu ABCB4, které snižují, ale zcela neblokují funkci proteinu MDR3, způsobovat řadu mírnějších forem familiární intrahepatální cholestázy 3. typu (PFIC3, OMIM #602347) spojené s mírně progresivním nebo neprogresivním jaterním postižením. Mírně progresivní formy onemocnění vedou ke konečnému stadiu jaterního onemocnění mezi druhou a pátou dekádou života. Mírnější forma deficitu MDR3 se projevuje též jako anikterická cholestáza s různým stupněm jaterní fibrózy v dospělosti a byla popsána teprve nedávno [4].
Některé práce [5, 6, 7] prokázaly, že těhotenská intrahepatální cholestáza (ICP) je u podskupiny nemocných s touto chorobou rovněž asociována s mutacemi v genu ABCB4. Navíc byl pozorován vztah mezi cholestázou indukovanou kontraceptivy (CIC) a mutacemi v genu ABCB4: Ganné-Carrié et al. [8] popsali 17letou dívku s asymptomatickou cholelitiázou a jaterní cirhózou na podkladě PFIC3, která se projevila užíváním kontraceptiv s obsahem 30 µg ethinylestradiolu a 150 µg levonorgesterolu. Další výskyt cholelitiázy u pacientky užívající orální kontraceptiva popsali Rosmorduc et al. [1]. Naopak Lang et al. [9] nenalezli mutaci v genu ABCB4 u 5 pacientů s CIC bez cholelitiázy.
V naší studii jsme se zaměřili na podíl mutací v genu ABCB4 na etiologii idiopatické cholelitiázy v dětském věku, která je na rozdíl od idiopatické cholelitiázy dospělých a s výjimkou novorozeneckého období vzácná [10, 11], a na fenotyp heterozygotů v rodinách se syndromem LPAC.
Pacienti a metody
Dětští pacienti s cholelitiázou
Celkem bylo vyšetřeno 76 dětí, které byly hospitalizovány na Pediatrické klinice Fakultní nemocnice v Motole v letech 1995–2004. U 22 z nich byla cholelitiáza asociována s jiným primárním onemocněním, jako např. Downův syndrom, Gaucherova nemoc, cystická fibróza, hemolytická anémie, idiopatický střevní zánět nebo imunodeficit. Dále byli vyloučeni pacienti na dlouhodobé parenterální výživě, pacienti léčení cefalosporiny nebo furosemidem a pacienti s anamnézou infekčního onemocnění jater, dyslipidemií či obezitou (BMI >27), u kterých nemusela být cholelitiáza primární chorobou. Celkem bylo takto vyloučeno 13 nemocných. U zbylých 41 dětí se velmi pravděpodobně jednalo o idiopatickou cholelitiázu. U těchto dětí nebyly identifikovány žádné rizikové faktory, které přispívají k cholelitiáze dospělých.
Pro analýzu mutací v genu ABCB4 bylo vybráno 26 nemocných (14 chlapců a 12 dívek) s idiopatickou cholelitiázou s pozitivní rodinnou anamnézou ICP, cholestázy či žlučových kamenů. Tito pacienti splňovali velké kritérium a malá kritéria (a) a (f) podle definice Rosmorduca a Poupona [3]. Všichni tito pacienti byli nepříbuzní běloši českého původu. Dvanáct nemocných (6 chlapců a 6 dívek) podstoupilo cholecystektomii. U žádného z nich nedošlo k recidivě cholelitiázy po operačním výkonu. V současnosti jsou všichni nemocní bez obtíží a nejeví žádné známky jaterní choroby.
Studie byla schválena etickou komisí Fakultní nemocnice v Motole a oba rodiče pacienta nebo pacient osobně (ve věku nad 15 let) podepsali informovaný souhlas před odběrem krve.
Pacienti s podezřením na LPAC
Mutační analýzu ABCB4 jsme provedli u pěti dospělých mladých žen – probandek se symptomatickou cholelitiázou s nástupem obtíží do 40 let věku, intrahepatální cholestázou v osobní anamnéze a rodinnou anamnézou cholelitiázy u příbuzných v přímé linii. Žádná neměla hyperechogenní ložiska v jaterní tkáni ani prokázaný intrahepatální sludge (přítomnost mikrolitiázy v duodenální žluči nebyla vyšetřována). I přesto všechny pacientky splňovaly výše uvedená kritéria podle Rosmorduca a Poupona [3]. Bližší klinická charakteristika pacientek je popsána v tabulce 1.
Table 1. Charakteristika žen s podezřením na nízkofosfolipidovou cholelitiázu. 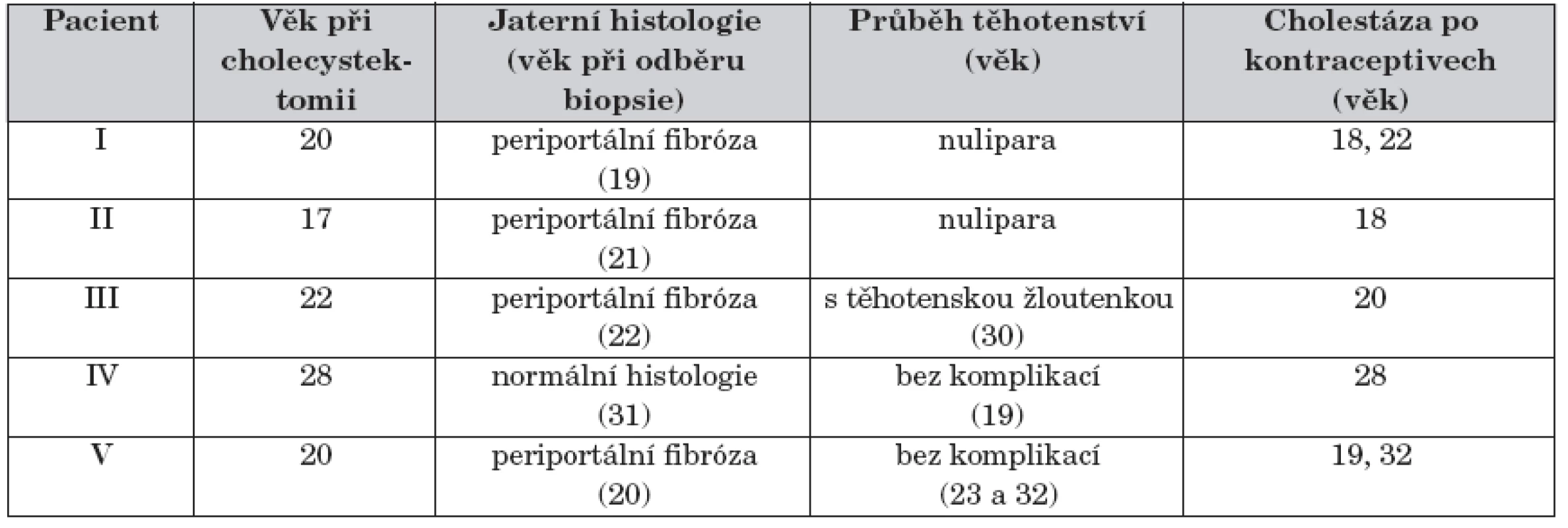
Vyšetření všech pěti probandek a jejich rodinných příslušníků bylo schváleno etickou komisí Institutu klinické a experimentální medicíny a Fakultní Thomayerovy nemocnice v Praze. Všichni vyšetření podepsali informovaný souhlas před odběrem krevních vzorků pro extrakci DNA.
Imunohistologie
Pro imunohistochemickou analýzu jsme použili 5 µm silné parafínové řezy tkáňových vzorků fixovaných formalinem od pacientů č. 2 a 3. Vzorky byly odparafinovány a ošetřeny roztokem Dako® Target Retrieval Solution (Dako Cytomation, Glostrup, Dánsko) ve vodní lázni při 99 °C po dobu 40 minut. Následně byly inkubovány s primární myší anti-MDR3 monoklonální protilátkou (klon P3II-26) od firmy Kamiya (Seattle, WA) naředěnou v poměru 1 : 30 roztokem ChemMate™ Antibody Diluent (Dako Cytomation, Glostrup, Dánsko). K vizualizaci řezů byl použit kit Histofine® (Exbio, Praha). Na všechny řezy byl aplikován chromogen 3,3-diaminobenzidin (Liquid DAB+Substrate, Dako Cytomation, Glostrup, Dánsko). Poté byly řezy obarveny Mayerovým hematoxylinem.
Jako pozitivní kontrola byla použita normální jaterní tkáň dospělého člověka získaná při resekci solitární jaterní metastázy kolorektálního adenokarcinomu. Jako negativní kontrolu jsme použili řezy jaterní tkáně inkubované bez primární protilátky.
Mutační analýza
Pomocí PCR bylo z genomové DNA amplifikováno 27 fragmentů pokrývajících celou protein kódující oblast genu ABCB4 a části přilehlých intronových sekvencí. Na 5´ - koncích primerů byly sekvence standardních primerů T7 nebo RP nehybridizující s genomovou DNA, které byly využity pro přímé sekvenování PCR produktů. Sekvence primerů jsou na vyžádání k dispozici u korespondujícího autora. Sekvence purifikovaných PCR produktů byla analyzována na automatických sekvenátorech DNA (AlfExpress, Pharmacia, Uppsala, Švédsko a ABI-PRISM 3100-Avant, Applied Biosystems, Foster City, CA). Jako referenční sekvence genomové DNA a cDNA byly použity sekvence Ensembl Acc. No. ENSG00000005471 a GenBank Acc. No. NM_018849.2. Sekvence byly číslovány tak, že adeninu v iniciačním ATG kodónu bylo přiřazeno číslo 1.
Přítomnost mutací nalezených při sekvenování DNA byla nezávisle potvrzena vyšetřením polymorfismu délky restrikčních fragmentů (PCR/RFLP) získaných štěpením příslušného PCR produktu restrikčními enzymy rozpoznávajícími buď mutovanou, nebo wild-type sekvenci. U vybraných pacientů byla v genu ABCB4 také vyšetřena přítomnost delecí/duplikací metodou multiplex ligation-dependent probe amplification (MLPA) s využitím soupravy SALSA MLPA KIT P109 ABCB4 (MRC-Holland, Amsterdam, Holandsko), která byla použita podle instrukcí v manuálu výrobce.
Statistické vyhodnocení
Statistické vyhodnocení bylo provedno pomocí softwarového balíku R (http://www.R-project.org).
Výsledky
Dětští pacienti s cholelitiázou
Analýza exonů kódujících protein a oblastí na přechodu intron/exon genu ABCB4 neodhalila žádné zjevně patogenní mutace. Byla však detekována přítomnost řady známých variant v kódujících (viz tab. 2) a intronových sekvencích (c.1357-40G>A (rs31675); c.2065+55A>G, (rs1017054); c.2199+72T>C (rs31668); c.2199+72C>T (rs31667); c.2478+40A>G, (rs7788404); a c.3508-16C>T (rs31653)). Žádná z těchto variant nebyla popsána v souvislosti s hepatobiliárním onemocněním vyjma varianty c.1954A>G nalezené v heterozygocii u pacientů č. 4, 8 a 26.
Varianta c.1954A>G nebyla přítomna častěji (3/52, alelická frekvence 0,058) než odpovídá výskytu v obecné české populaci (alelická frekvence 0,090; 27 heterozygotů ze 150 kontrol, viz též tab. 2).
Table 2. Frekvence variací v kódující sekvenci ABCB4 u dětských pacientů s idiopatickou cholelitiázou a v obecných populacích. 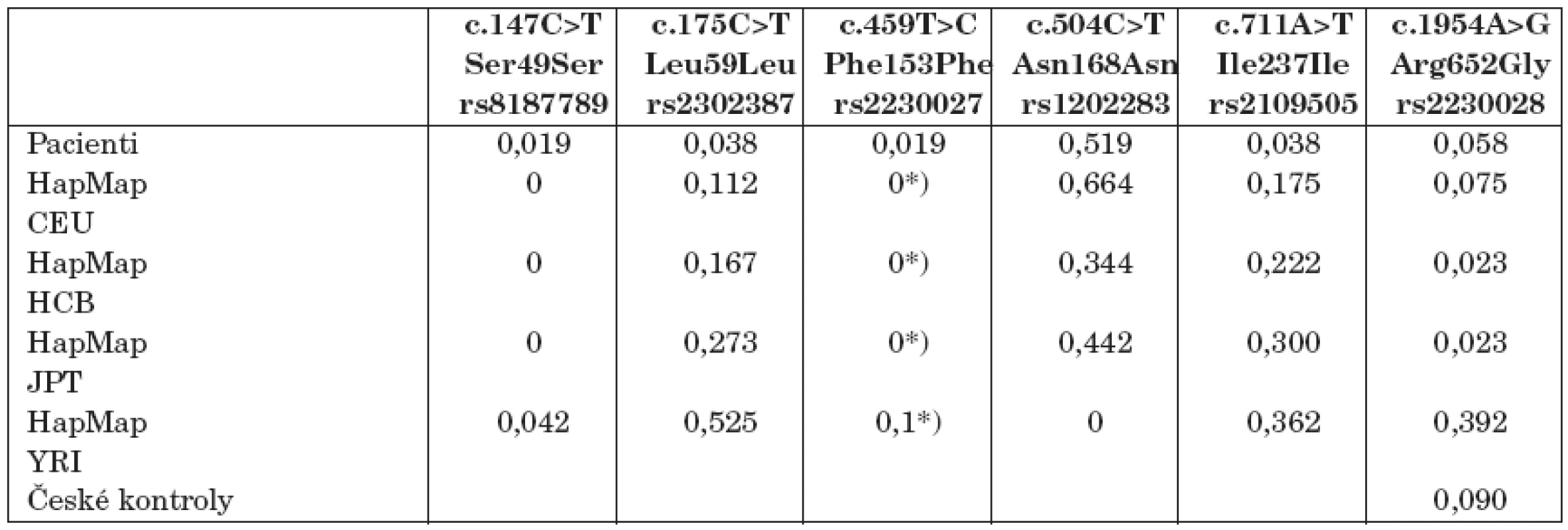
Frekvence genotypů v populačních vzorcích evropské (CEU), čínské (HCB), japonské (JPT) a africké (YRI) populace převzaty z databáze HapMap: www.hapmap.org. Frekvence označené *) v obdobných populačních vzorcích převzaty z databáze Environmental Genome Project (NIEHS ES15478 project): http://www.niehs. nih.gov/research/supported/programs/egp/. Rodiny s podezřením na syndrom LPAC
Histologie jaterní tkáně prokázala u probandek 1–3 změny typické pro syndrom LPAC: portální nebo periportální fibrózu, marginální duktální proliferaci a mírnou až středně intenzivní přítomnost zánětlivých buněk. U obou probandek č. II a III byl protein MDR3 v kanalikulární membráně hepatocytů exprimován (obr. 1). U probandky č. I nemohlo být imunohistochemické vyšetření MDR3 provedeno pro nedostatečné množství jaterní tkáně získané biopsií. Probandky IV a V nebyly vyšetřeny, neboť jejich bioptické vzorky nebyly k dispozici.
Image 1. ImunohistologieMDR3 v jaterní tkáni probandek II a III. Šipkami je označeno pozitivní imunobarvení proteinu MDR3, který je přítomen v kanalikulární membráně hepatocytů. Původní zvětšení 400x. Fig. 1. Immunohistology of MDR3 in liver tissue of the female probands II and III. The arrows indicate positive immunostaining of MDR3 protein which is present in the hepatocyte canalicular membrane. Original magnification 400-fold. 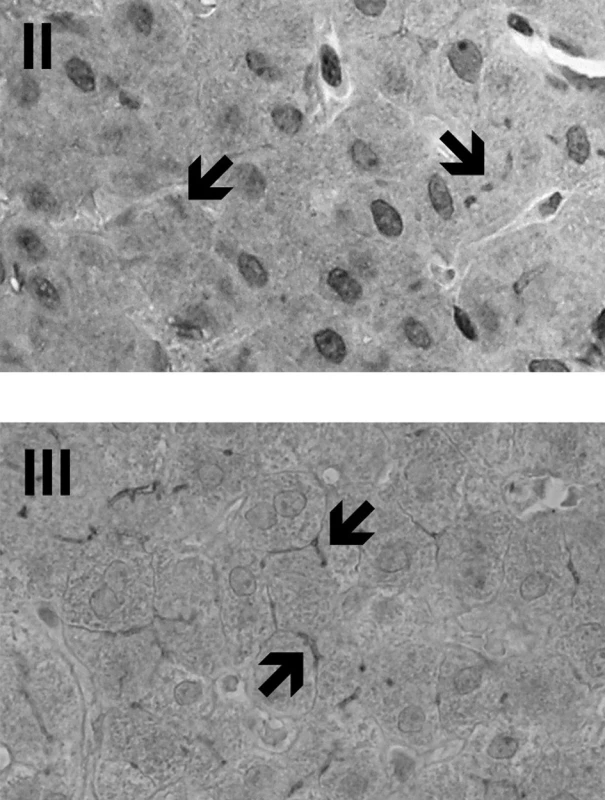
U dvou z pěti probandek byla prokázána nonsense mutace v heterozygotní konfiguraci, dvě probandky byly heterozygoty pro missense mutaci c.523A>G (p.Thr175Ala) a jedna probandka byla složeným heterozygotem pro tuto mutaci a současně pro mutaci vedoucí k posunu čtecího rámce (frameshift) p.Gln458ArgfsX7 (obr. 2). Variantu c.523A>G jsme nalezli u 30 % (3/10) alel u pacientů s LPAC, ale jen 2,7 % kontrolních alel v české populaci neslo v pozici 523 guanin (8/300, 8 heterozygotů ze 150 kontrol, odd sratio = 26,6, 95% interval spolehlivosti 3,9–182,7, p <0,00001). I když počet vyšetřených nemocných byl poměrně nízký, je možné považovat variantu p.Thr175Ala za alelu predisponující ke zvýšenému výskytu hepatobiliárních chorob. Všechny 3 nulové mutace jsou podle nám dostupných informací nové.
Image 2. Rodokmeny rodin se syndromem LPAC. Fenotyp LPAC je označen hvězdou na pozadí, probandky č. I–V jsou označeny šipkami. Bratr otce probandky I (F2-1) žádné projevy syndromu LPAC ve věku 53 let neuvádí. Děd probandky I z otcovy strany (F1-1) cholelitiázu sice vyvinul, avšak až po 40. roce věku. Rovněž otec probandky III (F1-1) udává první biliární koliku kolem 60. roku věku. Děti (F3-1 a F3-2) probandky III jsou pětiletá dvojčata bez známek LPAC. DNA sestry probandky IV (F2-1), která splňovala klinická kritéria pro syndrom LPAC, byla analyzována, avšak žádnou mutaci v ABCB4 jsme nenalezli. Vysvětlení, proč se u této pacientky vyvinula cholelitiáza před 40. rokemvěku, neznáme. 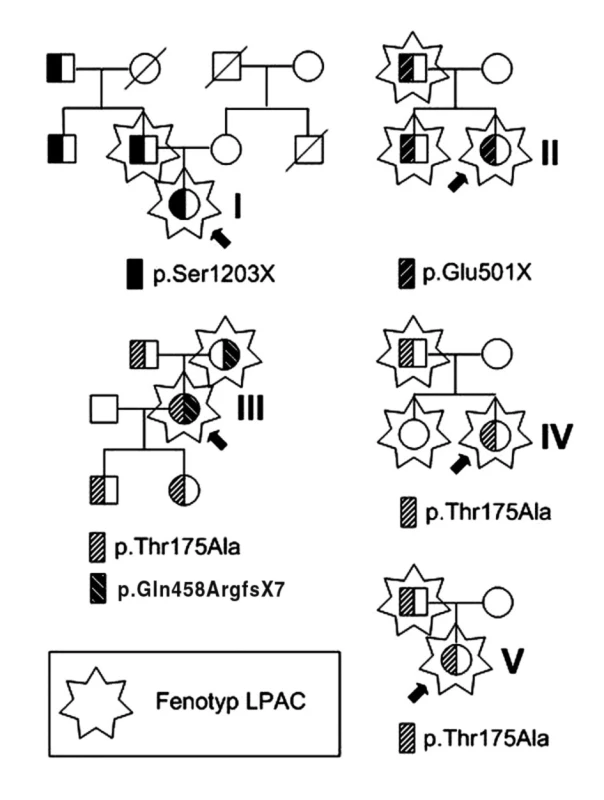
U žádné nemocné s LPAC nebyly metodou multiplex ligation-dependent probe amplification v genu ABCB4 nalezeny ani delece, ani duplikace. Ostatní členové jejich rodin proto nebyli touto technikou vyšetřeni.
K zodpovězení otázky míry segregace fenotypu s genotypem v rodinách probandů jsme provedli vyšetření rodinných příslušníků. Jak ukazují rodokmeny znázorňující segregaci genotypu a fenotypu v postižených rodinách na obrázku 2, jsou rodiče probandů I, II, IV a V nesoucí stejnou mutaci v genu ABCB4 na jedné z alel symptomatičtí. To podporuje hypotézu, že jak nulové mutace nalezené v rodinách I a II, tak missense mutace p.Thr175Ala nalezená v rodině IV a V, jsou pravděpodobně dostačující v heterozygotní konfiguraci k tomu, aby vyvolaly fenotyp LPAC. Nelze však vyloučit, že penetrance není úplná a je ovlivněna zatím neznámými modifikujícími faktory.
Diskuse
Výsledky naší studie neprokázaly žádnou jednoznačně patogenní variantu v ABCB4 u 26 vybraných dětských pacientů s idiopatickou cholesterolovou cholelitiázou a rodinnou anamnézou cholelitiázy u příbuzných v přímé linii. Jedinou potenciálně patogenní mutací nalezenou u dětí s idiopatickou cholelitiázou byla variace c.1954A>G (p.Arg652Gly). Tato nukleotidová záměna je běžná v evropské kavkazské i v africké populaci (viz tab. 2), ale byla také popsána u pacienta s nízkou koncentrací žlučových fosfolipidů. Předpokládá se, že p.Arg652Gly by mohla být podmíněná mutace, která vede ke klinickým projevům pouze za určitých okolností jako je těhotenství nebo v kombinaci s jinou mutací [12]. Naopak ve studii Meiera et al. [13] nebyla pozorována žádná korelace genotypu c.1954A|G s mírou exprese proteinu MDR3. To však nevylučuje vliv aminokyselinové záměny na funkci proteinu. Naše zjištění, že genotyp c.1954A|G nebyl u pediatrických pacientů s idiopatickou cholelitiázou ani častější ani významně méně častý než v obecné populaci, svědčí pro malý význam této variace v etiologii dětské idiopatické cholelitiázy.
Varianta c.523A>G zjištěná u tří probandek s LPAC nebyla nalezena u žádného z 26 dětských nemocných s idiopatickou cholelitiázou. Alela c.523G byla již dříve uváděna v souvislosti s cholestatickým onemocněním [1], ačkoliv je též nalézána v běžné bělošské populaci s frekvencí 0,025–0,032 [9, 14, 15]. Threonin v pozici 175 je vysoce konzervovaný v motivu Thr-Arg-Leu-Thr, který je nezbytný pro adenosin trifosfatázovou aktivitu proteinu. Zatímco funkční důsledky substituce threoninu v pozici 175 nepolární aminokyselinou s hydrofobním postranním řetězcem nebyly v proteinu MDR3 studovány, byly studovány u jeho blízkého homologu P-glykoproteinu (MDR1/ABCB1) u kvasnic [16]. Substituce p.Thr169Ile vedla ke ztrátě substráty indukované ATPázové aktivity. Proto je substituci p.Thr175Ala možno považovat za patogenní mutaci s neúplnou penetrancí.
Vzhledem k uvedeným výsledkům a dále vzhledem k tomu, že ani u jednoho z 15 heterozygotních nosičů mutace v ABCB4 v rodinách probandek s molekulárně potvrzenou diagnózou syndromu LPAC ani u žádného heterozygota zachyceného v dříve publikovaných studiích [1, 2, 4, 17, 18, 19] se v dětství nevyvinula symptomatická cholelitiáza bez přítomnosti známek PFIC, máme za to, že mutace v genu ABCB4 se u dětí s idiopatickou cholelitiázou významně nepodílejí na etiologii této choroby.
Nejpravděpodobnější vysvětlení pozorování, že syndrom LPAC se manifestuje nejdříve v období střední adolescence, spočívá ve změně složení žlučových lipidů během druhé životní dekády. Hlavním důvodem raritního výskytu cholelitiázy v dětství ve srovnání s dospělostí je patrně nízká koncentrace cholesterolu ve žluči [20]. Děti mají snížený poměr cholesterol/žlučové kyseliny [21]. Z tohoto důvodu nedochází ani při snížené sekreci fosfolipidů při částečném deficitu MDR3 k nasycení žluči cholesterolem. Zvýšení cholesterolového saturačního indexu v časné dospělosti [21] spolu se sníženou sekrecí lecithinu u nosičů mutací v ABCB4 posouvá rovnováhu k hraničním hodnotám. Klinická manifestace LPAC může být následně vyvolána malým množstvím exogenních hormonů obsažených v kontraceptivech nebo jiných hormonálních preparátech, které inhibují sekreci žlučových kyselin [22], tím dále snižují sekreci fosfolipidů [23] a mohou tak působit jako faktor podporující krystalizaci cholesterolu z přesycené žluči, tvorbu intrahepatálního sludge a žlučových konkrementů.
Závěr
Závěrem je možno konstatovat, že klinická kritéria syndromu LPAC vyvolaného mutacemi v ABCB4 nemohou být používána u dětských nemocných s idiopatickou cholelitiázou, neboť prevalence mutací v genu ABCB4 je u nich nízká. Navíc, u nosičů patogenních mutací v ABCB4 dochází k manifestaci syndromu LPAC nejdříve v období od střední adolescence. Mutační analýza genu ABCB4 u dětských nemocných s idiopatickou cholelitiázou bez známek chronického poškození jater s cholestázou proto není diagnosticky přínosná.
Seznam zkratek
ABC – ATP-binding cassette;
BSEP – bile salt export pump;
CIC – kontraceptivy indukovaná intrahepatální cholestáza;
ICP – těhotenská intrahepatální cholestáza;
MDR3 – multidrug resistance protein 3;
LPAC – nízkofosfolipidová cholelitiáza;
PFIC – progresivní familiární intrahepatální cholestáza.
Studie byla podpořena grantem IGA MZ NR/9079-3.
Došlo: 26. 2. 2009
Přijato: 29. 5. 2009
Doc. MUDr. Mgr. Milan Jirsa, CSc.
Laboratoř experimentální hepatologie
Pracoviště experimentální medicíny
Institut klinické a experimentální medicíny
Vídeňská 1958/9
140 21 Praha 4
e-mail: milan.jirsa@ikem.cz
Sources
1. Rosmorduc O, Hermelin B, Poupon R. MDR3 gene defect in adults with symptomatic intrahepatic and gallbladder cholesterol cholelithiasis. Gastroenterology 2001;120 : 1459–1467.
2. Rosmorduc O, Hermelin B, Boelle PY, et al. ABCB4 gene mutation-associated cholelithiasis in adults. Gastroenterology 2003;125 : 452–459.
3. Rosmorduc O, Poupon R. Low phospholipid associated cholelithiasis: association with mutation in the MDR3/ABCB4 gene. Orphanet. J. Rare Dis. 2007;2 : 29.
4. Ziol M, Barbu V, Rosmorduc O, et al. ABCB4 heterozygous gene mutations associated with fibrosing cholestatic liver disease in adults. Gastroenterology 2008;135 : 131–141.
5. Floreani A, Carderi I, Paternoster D, et al. Intrahepatic cholestasis of pregnancy: three novel MDR3 gene mutations. Aliment. Pharmacol. Ther. 2006;23 : 1649–1653.
6. Schneider G, Paus TC, Kullak-Ublick GA, et al. Linkage between a new splicing site mutation in the MDR3 alias ABCB4 gene and intrahepatic cholestasis of pregnancy. Hepatology 2007;45 : 150–158.
7. Floreani A, Carderi I, Paternoster D, et al. Hepatobiliary phospholipid transporter ABCB4, MDR3 gene variants in a large cohort of Italian women with intrahepatic cholestasis of pregnancy. Dig. Liver Dis. 2008;40 : 366–370.
8. Ganné-Carrié N, Baussan C, Grando V, et al. Progressive familial intrahepatic cholestasis type 3 revealed by oral contraceptive pills. J. Hepatol. 2003;38 : 693–694.
9. Lang C, Meier Y, Stieger B, et al. Mutations and polymorphisms in the bile salt export pump and the multidrug resistance protein 3 associated with drug-induced liver injury. Pharmacogenet. Genomics 2007;17 : 47–60.
10. Volf V, Vondráková L, Votruba M, et al. Cholelitiáza v dětském věku. Čes.-slov. Pediat. 2003;58 : 637–641.
11. Vaňatka R. Cholelitiáza u novorodencov – bežný nález. Čes.-slov. Pediat. 2008;63 : 248–255.
12. Jacquemin E, Cresteil D, Manouvrier S, et al. Heterozygous non-sense mutation of the MDR3 gene in familial intrahepatic cholestasis of pregnancy. Lancet 1999;353 : 210–211.
13. Meier Y, Pauli-Magnus C, Zanger UM, et al. Interindividual variability of canalicular ATP-binding-cassette (ABC)-transporter expression in human liver. Hepatology 2006;44 : 62–74.
14. Pauli-Magnus C, Kerb R, Fattinger K, et al. BSEP and MDR3 haplotype structure in healthy Caucasians, primary biliary cirrhosis and primary sclerosing cholangitis. Hepatology 2004;39 : 779–791.
15. Pauli-Magnus C, Lang T, Meier Y, et al. Sequence analysis of bile salt export pump (ABCB11) and multidrug resistance p-glycoprotein 3 (ABCB4, MDR3) in patients with intrahepatic cholestasis of pregnancy. Pharmacogenetics 2004;14 : 91–102.
16. Kwan T, Gros P. Mutational analysis of the P-glycoprotein first intracellular loop and flanking transmembrane domains. Biochemistry 1998;37 : 3337–3350.
17. Gendrot C, Bacq Y, Brechot MC, et al. A second heterozygous MDR3 nonsense mutation associated with intrahepatic cholestasis of pregnancy. J. Med. Genet. 2003;40: e32.
18. Lucena JF, Herrero JI, Quiroga J, et al. A multidrug resistance 3 gene mutation causing cholelithiasis, cholestasis of pregnancy, and adulthood biliary cirrhosis. Gastroenterology 2003;124 : 1037–1042.
19. Gotthardt D, Runz H, Keitel V, et al. A mutation in the canalicular phospholipid transporter gene, ABCB4, is associated with cholestasis, ductopenia, and cirrhosis in adults. Hepatology 2008;48 : 1157–1166.
20. Niessen KH, Theisen M. Why do children rarely have gallstones? Examinations of the lithoindices and the bile acid pattern in infants and children in health and disease. Monatsschr. Kinderheilkd. 1980;128 : 551–557.
21. Heubi JE, Soloway RD, Balistreri WF. Biliary lipid composition in healthy and diseased infants, children, and young adults. Gastroenterology 1982;82 : 1295–1299.
22. Stieger B, Fattinger K, Madon J, et al. Drug - and estrogen-induced cholestasis through inhibition of the hepatocellular bile salt export pump (Bsep) of rat liver. Gastroenterology 2000;118 : 422–430.
23. Oude Elferink RP, Ottenhoff R, van Wijland M, et al. Regulation of biliary lipid secretion by mdr2 P-glycoprotein in the mouse. J. Clin. Invest. 1995;95 : 31–38.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2009 Issue 7-8-
All articles in this issue
- Komplikace varicely u dětí
- Úloha variací genu ABCB4 v etiologii idiopatické cholelitiázy dětského věku
- Vitamín D – nový pohľad na starý vitamín
- Terapeutické přístupy v léčbě novorozenecké anémie z nezralosti
- Intrauterinní růstová retardace a její vliv na další vývoj extrémně nezralých novorozenců
- Prenatální život z pohledu etiky
- Etický kontext tzv. „baby- boxů“
- Lázně pro děti – léčba nebo rekreace?
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Terapeutické přístupy v léčbě novorozenecké anémie z nezralosti
- Intrauterinní růstová retardace a její vliv na další vývoj extrémně nezralých novorozenců
- Vitamín D – nový pohľad na starý vitamín
- Komplikace varicely u dětí
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

