-
Medical journals
- Career
Kontaktní dermatitidy – část II:
epikutánní testy v současné praxi
Authors: A. Machovcová 1,2
Authors‘ workplace: Dermatovenerologické oddělení FN Motol, Praha primářka MUDr. Alena Machovcová, Ph. D, MBA 1; Klinika pracovního lékařství 1. LF UK a VFN, Praha přednostka prof. MUDr. Daniela Pelclová, CSc. 2
Published in: Čes-slov Derm, 91, 2016, No. 5, p. 207-221
Category: Reviews (Continuing Medical Education)
Overview
Epikutánní testy (ET) jsou standardní vyšetřovací metodou ke zjištění kontaktní senzibilizace. V přehledu jsou uvedeny současné poznatky o aplikaci ET, jejich indikace, výběr alergenů (standardizované, nestandardizované), typy testů, odečítání, komplikace a hodnocení klinické relevance. Autorka se podrobněji věnuje problematice častých kontaktních alergenů, mezi které patří soli kovů (nikl, kobalt, chrom) a složky kosmetických přípravků (vonné látky, konzervační látky). Z aktuálních kontaktních alergenů jsou zmíněné parafenylendiamin a textilní barvy.
Klíčová slova:
kontaktní dermatitidy – epikutánní testy – nejčastější kontaktní alergenyÚVOD
Epikutánní testy (ET) jsou standardní vyšetřovací metodou k průkazu kontaktní senzibilizace (KS) u dětí i dospělých. Mají dlouholetou historii (od roku 1895) a dosud nebyly nahrazeny spolehlivější laboratorní metodou. Princip metody spočívá v expozici malého okrsku kůže podezřívanému alergenu. U senzibilizované osoby se při dodržení standardního postupu podaří vyvolat pozitivní reakci. In vivo jde o vizualizaci efektorové fáze senzibilizační reakce. Úspěšnost vyšetření je závislá na řadě faktorů (volba alergenů, vhodná koncentrace, místo aplikace, doba odečítání, klinická relevance) [6, 29, 42, 45, 46, 60–62, 66, 99].
INDIKACE EPIKUTÁNNÍCH TESTŮ
ET jsou indikovány u pacientů všech věkových skupin, včetně dětí pro akutně nebo chronicky probíhající dermatitidy a dermatózy, které nereagují na standardní léčbu nebo se i přes intenzivní léčbu zhoršují. K testům jsou indikovány projevy na kůži nebo sliznicích, u kterých je třeba KS vyloučit [6, 29, 42, 45, 60–62, 66, 99].
ALERGENY K EPIKUTÁNNÍM TESTŮM
Evropská základní sada (EZS) kontaktních alergenů je doporučena European Environmental and Contact Dermatitis Research Group (EECDRG) a obsahuje standardizované, nejčastěji se vyskytující kontaktní alergeny v evropských zemích (obr. 1). Seznam kontaktních alergenů a jejich koncentrace se průběžně mění a doplňuje podle výsledků multicentrických studií. Regionálně/kontinentálně se základní sady mohou lišit, nicméně celosvětově obsahují soli kovů (chrom, nikl, kobalt), antioxidanty a akcelerátory vulkanizace, formaldehyd, součásti zevních léčiv a kosmetiky (vonné látky, konzervační látky), pryskyřice aj. To umožňuje srovnávání mezi jednotlivými zeměmi a regiony. Podle národních zvyklostí lze základní sadu rozšířit o další alergeny. Frekvence senzibilizace na alergeny EZS je odlišná podle testované populace v různých studiích [6, 29, 42, 45, 60–62, 66, 99]. Aktuálně používaná EZS kontaktních alergenů obsahuje 30 standardizovaných alergenů (tab. 1) [42]. Alergeny jsou chemicky jasně definované, čisté a bez příměsí. Většina z nich je jednodruhová (obsahuje jednu chemickou látku/sloučeninu). Některé testy obsahují směs tzv. mix alergenů, která se často i v reálných podmínkách vyskytuje pohromadě (např. směs parfémů), nebo se mixy používají ke zvýšení záchytu senzibilizace (např. parabeny mix, merkaptobenzothiazol mix apod.) [6, 29, 42, 45, 60–62, 66, 99].
Image 1. Uzavřené epikutánní testy – evropská základní sada a atopické epikutánní testy 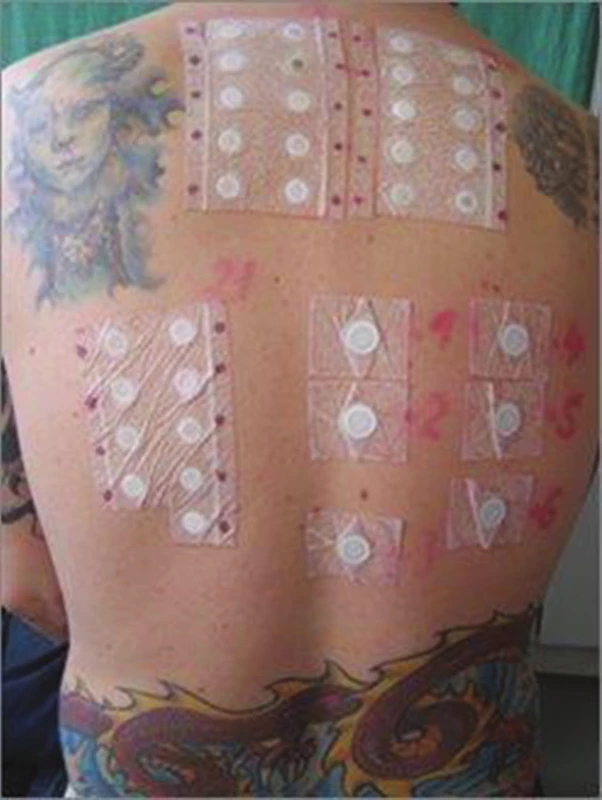
Table 1. Evropská základní sada 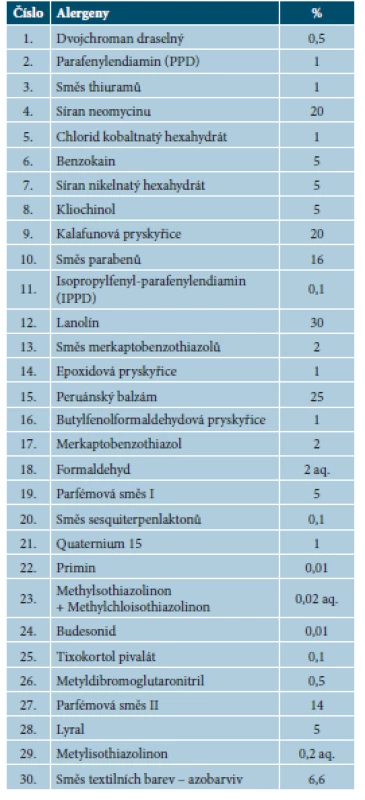
aq. – voda Ostatní alergeny jsou ve vazelíně. VÝBĚR ALERGENŮ
Kromě EZS je možné si objednat speciální sady standardizovaných alergenů. K dispozici jsou sady zaměřené na určitou profesi (např. kadeřníci, obráběči kovů, pekaři apod.), na určité specifické podezřívané alergeny (např. sady lékové, sady zubních alergenů, kosmetických alergenů, chemikálií pryže, fotokontaktních alergenů apod.). K testování lze použít sady kontaktní alergenů od firem Chemotechnique Diagnostics (www.chemotechnique.se), AllergEASE (www.smartpracticecanada.com) nebo tzv. T.R.U.E testy (www.smartpracticecanada.com). T.R.U.E test (Thin-layer Rapid Use Epicutaneous test) je speciální testovací systém, u kterého je přesně stanovené množství alergenu (v miligramech na cm2) vpravené do hydrofilního gelu a je rovnoměrně rozložené na celou plochu testovací komůrky. Předností je snadná manipulace s testy, jejich rychlá aplikace, standardní množství a rozložení testovaného alergenu po celé ploše komůrky u všech testovaných osob (obr. 2). Jsou dostupné pouze pro 35 alergenů a sada není identická s EZS [6, 29, 42, 45, 60–62, 66, 99].
Image 2. Epikutánní testy T.R.U.E 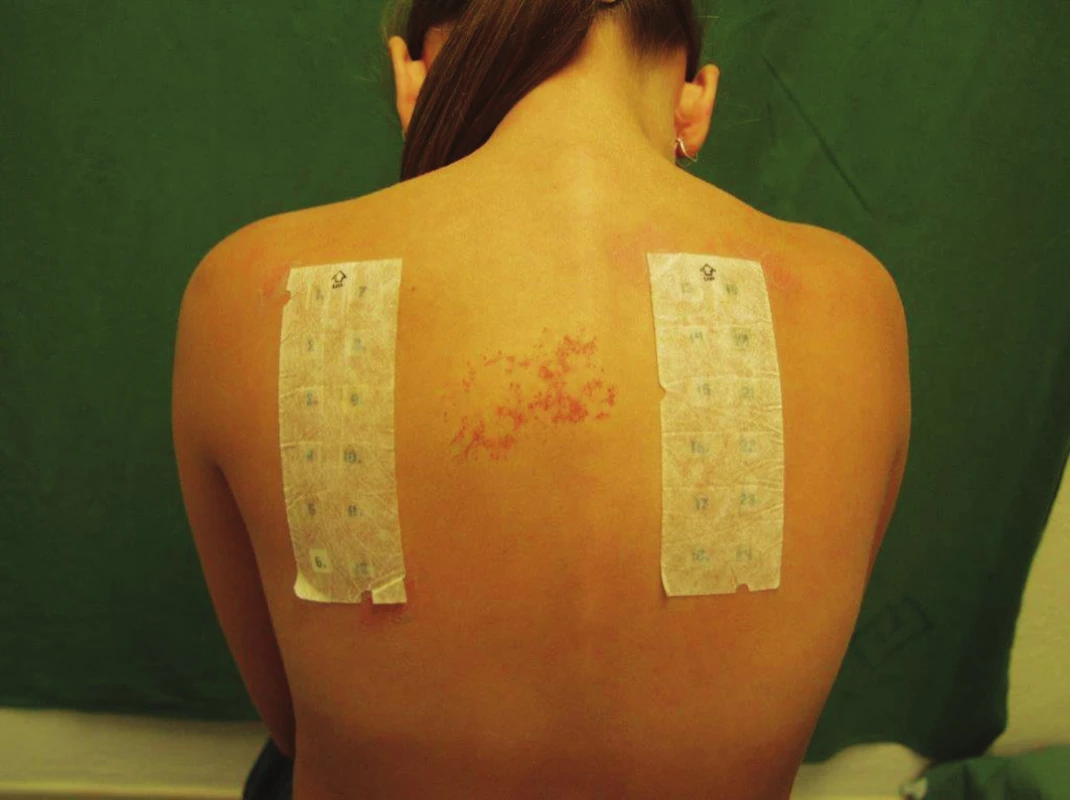
Nestandardizované alergeny
Testování donesených vzorků (včetně kosmetických přípravků) od pacientů se provádí, pokud není dostupný standardizovaný komerčně vyráběný alergen. Tyto látky, většinou z pracoviště pacienta, se připravují individuálně pro každého pacienta těsně před aplikací testů. Příslušné koncentrace a vhodné vehikulum jsou u mnohých alergenů uvedené v alergologických tabulkách. Jinak je nutno vycházet z chemické struktury testované látky, eventuálně použít titrovaný způsob testování. Toto lze uskutečnit pouze ve specializovaných dermatoalergologických ambulancích. Spektrum testovaných látek vyplyne z anamnézy pacienta [42, 54, 89]. Pokud je k dispozici standardizovaný alergen, měl by se použít přednostně. Látky neznámého složení se zásadně netestují [6, 29, 42, 45, 60–62, 66, 89, 99].
Kosmetické přípravky, které na kůži zůstávají delší dobu, tzv. „leave on“ kosmetika (např. pěstící a dekorativní kosmetika, protektivní krémy, emoliencia, zevní externa apod.) se neředí, testuje se hotový přípravek tak, jak byl vyrobený (tzn. „jak je“ – „as is“). Při pozitivním testu se doporučuje otestovat jednotlivé substance podle složení. Negativní výsledek testu se vzorkem kosmetiky zcela nevylučuje kontaktní alergii na některou její složku (např. koncentrace v produktu je příliš nízká), při přetrvávajícím podezření na KS je vhodné doplnit otevřený test opakovaným užitím (tzv. ROAT – repeated open application test, viz dále). Kosmetika, která se po několika minutách opláchne vodou, tzv. „rinse off“ kosmetika (např. tekutá mýdla, šampony, mycí gely apod.), se před testováním ředí. Vhodná koncentrace je mezi 5–10 % ve vodě. Pevné látky (papír, textil, pryž, kovové předměty, prach apod.) se neupravují (je možné je rozdrtit na malé částečky), testují se beze změny, jak jsou, případně se zakápnou vodou nebo jiným rozpouštědlem. Ponechávají se v kontaktu s kůží o den déle, tj. 72 hodin. Při jejich odečtech mohou vznikat některé specifické obrazy (viz dále). Z rostlin se testují (pokud není k dispozici standardizovaný alergen) jednotlivé části rostliny (list, květ, stonek, kořen) v kapce vody a v etanolu. Části rostlin musí být čerstvé a lehce rozmačkané [42, 99].
TYPY EPIKUTÁNNICH TESTŮ
Uzavřený epikutánní test
Uzavřené ET se provádí obvykle na klinicky zdravé kůži horní poloviny zad po odmaštění kůže éterem nebo alkoholem (usnadní průnik alergenu a adhezi testovací náplasti). U všech pacientů se aplikuje celá EZS. Optimální množství alergenů ve vazelíně je mezi 20 mg až 35 mg v závislosti na velikosti testovací komůrky. Pro vodné roztoky alergenů se doporučuje 15–20 µl [42, 45, 62, 66, 99]. Alergeny se aplikují na testovací náplasti (např. Curatest, Finn Chamber on Scanpor, Al-test, IQ Chamber a další), kdy jednotlivé pruhy obsahují 10 komůrek (o průměru 8–10 mm) na hypoalergenní (akrylátové) testovací náplasti [42, 45, 62, 66, 99]. Den nalepení se označuje jako den 0 (D0). Náplasti přikládáme ve svislých nebo vodorovných pruzích. První řadu testů klademe cca 10 cm pod poslední krční obratel a místa nad páteří vynecháváme. Místo aplikovaných alergenů si barevně na zádech označíme (viz obr. 1, 2).
Testování dětské populace
ET se u dětí považují za bezpečné vyšetření a indikace jsou obdobné jako u dospělých [17, 28, 53, 60, 62, 66]. Přesto existují určitá omezení při testování dětí [28]:
- U velmi malých dětí s omezenou plochou zad se EZS rozdělí a aplikuje se ve dvou sezeních.
- U hyperaktivních dětí, u kterých je vyšší riziko spadnutí náplastí, je vhodné testovací náplasti fixovat další náplastí. Spadlé testy rodiče nemají znovu přilepovat.
- Rodiče dětí je nutné detailně informovat o testovací proceduře a o opatřeních k zajištění optimálních podmínek testování.
Odečítací dny a hodnotící škála jsou shodné s dospělou populací. Při podezření na KS na parafenylendiamin z dočasné tetováže černou henou odborné společnosti některých zemí (např. německá) doporučují použít k testování nižší koncentraci parafenylendiaminu (pod 1 %) nebo zkrátit aplikační dobu na 24 hodin [6]. Při podezření na silnou reakci je vhodné provést otevřený test (viz dále). Cílem je vyvarovat se silné pozitivní reakce a možné senzibilizace z testů [42].
MODIFIKACE ET A JINÉ DIAGNOSTICKÉ TESTY
Otevřený test se používá k testování ne zcela přesně definovaných substancí nebo donesených přípravků od pacientů (např. laky na nehty apod.). Zkoušený přípravek se aplikuje na paži nebo záda (horní plochu) 2krát denně 2 dny, nesmí se omýt a nezakrývá se náplastí. Odečet se provádí během prvních 30–60 minut (vyloučení časné reakce), další odečty jsou za 48, 72 a/nebo 96 hodin. Negativní otevřený test umožňuje provedení uzavřeného testu [29, 30, 42, 62].
Polootevřený test (semi-open test) popsal Goossens v roce 2007 [29]. Jedná se o modifikaci otevřeného testu, je vhodný pro testování většího množství výrobků (většinou kosmetických) s možným iritačním potenciálem. Umožní vyvarovat se falešně pozitivních/negativních nebo iritačních reakcí (např. laky na nehty, šampony, detergenty, farmaceutické přípravky apod.). Malé množství (1–2 μl) přípravku se aplikuje vatovou štětičkou na malou plochu kůže (1 cm2), nechá se odpařit. Po 30–60 minutách se hodnotí případná časná reakce (většinou charakteru kopřivkového pupenu), poté se místa se vzorky zakryjí běžnou náplastí. Další odečty následují stejným způsobem jako u uzavřeného ET [29, 30, 42].
Otevřený opakovaný test užitím (ROAT – repeated open application test) byl poprvé popsán v roce 1986. Jedná se o expoziční test, který je v některých případech jako jediný schopný potvrdit KS. Podezřívaný přípravek (cca 0,1 ml) se 2krát denně aplikuje na volární plochu předloktí blízko loketní jamky (plocha asi 5 x 5 cm). Případné reakce se hodnotí nejdříve za týden. Někdy se aplikace přípravku musí provádět déle (až 21 dnů). Provádí se u kosmetických výrobků, ve kterých některé alergeny mohou být v nízké koncentraci. První známky pozitivní reakce mají charakter folikulární reakce [29, 30, 42, 62, 66, 99].
Fotosenzibilizační ET se používá k diagnostice fotoalergické kontaktní dermatitidy. Dvě identické sady podezřívaných alergenů se aplikují na záda (nebo na paže), po 2 dnech okluze (D2 po 48 hodinách) se obě sady náplastí sejmou a odečtou. Poté se jedna sada testů ozáří UVA zářením v dávce 5 J/cm2 (druhá se před ozářením zakryje). Následují minimálně další 2 odečty testů (D3, D4) a vzájemné porovnávání ozářené a neozářené sady. K hodnocení se používá stejná škála jako u klasických ET (viz dále). Pozitivní reakce pouze v ozářených polích potvrzují fotokontaktní senzibilizaci, pozitivní reakce v obou polích (neozářené i ozářené) svědčí pro prostou KS [26, 42].
Atopické epikutánní testy spočívají v aplikaci alergenu proteinové povahy do uzavřené komůrky na 48 hodin (viz obr. 1). Výsledky atopických epikutánních testů (APT) se hodnotí za 48 a 72 hodin od aplikace. Technika APT není dosud standardizovaná, standardizovaných alergenů k APT je minimum, často se používají k testům alergeny určené k prick-testům (nestandardizované). Senzitivita APT pro aeroalergeny je nižší (18–66 %) a specificita APT je vyšší (64–91 %) v porovnání s prick-testy a sérovými hladinami celkových IgE protilátek. Mechanismus APT není identický s prick-testy nebo klasickými ET. Pozitivní APT na aeroalergeny (obr. 3) jsou často u pacientů s projevy na obličeji charakteru airborne dermatitidy. Vyloučení alergenů následně může vést ke zklidnění AD [32, 62, 70].
Image 3. Pozitivní reakce v atopických epikutánních testech 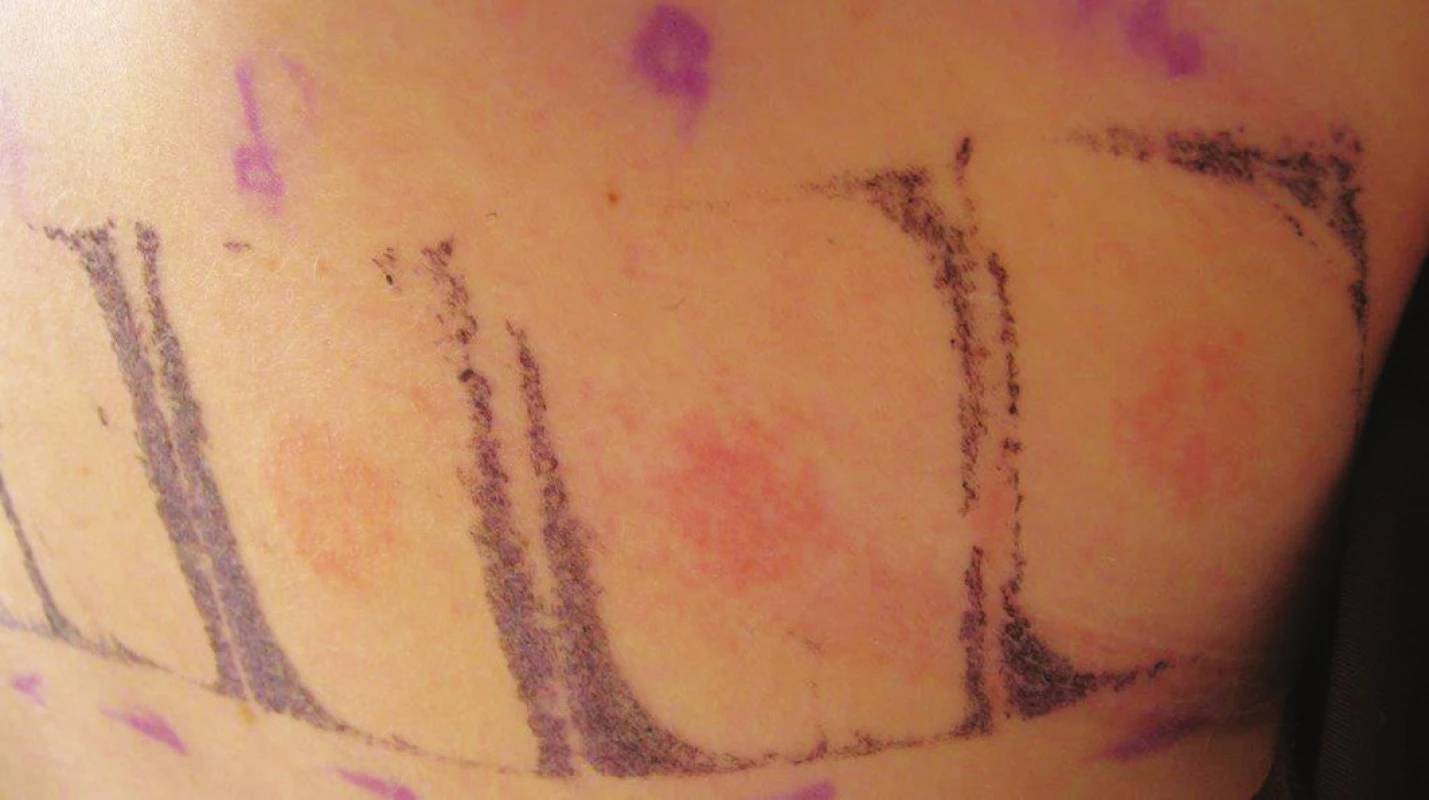
Prick-prick testy jsou modifikací klasických prick-testů. Provádí se k testování čerstvých potravin. Jsou možné 2 způsoby provedení – buď se běžnou lancetou nejprve „píchne“ do čerstvé potraviny a poté se malé množství potraviny stejnou lancetou aplikuje do kůže. Druhý způsob je aplikace do kůže přes čerstvou potravinu položenou na kůži, poté se potravina z kůže odstraní. Odečty se provádějí po 30 minutách a poté jako u uzavřených ET [25, 30, 32].
Test vetřením – podezřívaná nativní neupravená substance se jemně vtírá 8–10 tahy do zdravé kůže předloktí. U senzibilizovaných osob se reakce objevuje do 30 minut ve formě folikulárně vázaných posléze splývajících urtik, pozdější odečty za 24, 48, 72 hodin jsou nezbytné [32, 42, 45, 66, 99].
SAFT (skin application food test) – přibližně 1 ml potraviny v tekutém stavu nebo malý kousek tuhé potraviny (cca 4 cm2) se na gáze přiloží na kůži a fixuje náplastí, maximální doba okluze je 30 minut s pravidelnými odečty po 10 minutách a poté jako u uzavřených ET (obr. 4). Je možné použít testovací náplast k uzavřeným testům [25, 30, 32, 62].
Image 4. Pozitivní kožní test s potravinami (SAFT) 
Odečítání ET
Náplasti s alergeny EZS se ponechávají v kontaktu s kůží (podle mezinárodního konsenzu) po dobu 2 dnů, tj. 48 hodin, poté se sundávají a hodnotí se vzniklé reakce (den 2 – D2). Testy se hodnotí pouhým zrakem, popř. za použití lupy, odečítající lékař ani pacient se nesmí dotýkat testované lokality (přenos stop alergenů mezi sebou). Hodnocení testů se provádí minimálně dvakrát, první odečet následuje po sejmutí náplastí po 48 hodinách (D2), po odeznění erytémové reakce vyvolané tahem náplasti při jejím snímání. Další odečty následují po 72 hodinách (den 3 – D3) a/nebo 96 hodinách (den 4 – D 4) a D7 (po týdnu) od nalepení testů. Za pozitivní se považují reakce po 72 hodinách (D3), popř. později vzniklé. Odečet mezi 5.–10. dnem od aplikace testů je nezbytný u některých alergenů (kortikosteroidy, aminoglykosidová antibiotika, stomatologické materiály). 7–30 % případů KS není zachyceno v důsledku krátké doby odečítání [6, 42, 45, 61, 62, 66, 89, 99].
Praktické aspekty epikutánních testů
Ochlupení na zádech je nutné v předstihu oholit. Před aplikací náplastí s alergeny se kůže zad jemně odmastí etanolem nebo směsí etanolu s éterem. Náplasti se přikládají na kůži jemným tlakem, který vytlačí vzduch a zajistí dokonalé přilnutí náplastí ke kůži. Pořadí jednotlivých kontaktních alergenů je konstantní. Místo aplikace testů se následně označí speciálním fixem. Po sejmutí náplastí nesmí být zbytky alergenů odstraněny z kůže. Pro dosažení správného výsledku je důležité podrobné poučení pacientů (není dovoleno testovanou lokalitu osprchovat, na kůži v oblasti testů se nesmí sahat, není vhodné cvičení nebo aktivity spojené se zapocením atd.). [42, 45, 61, 62, 66, 89, 99].
Interpretace pozitivních reakcí v epikutánních testech
Doporučená mezinárodní hodnotící škála je uvedená v tabulce 2 [42, 62].
Table 2. Hodnotící škála 
(upraveno podle [42, 62]) Alergické reakce
Pozitivní reakce (+, ++, +++) při druhém (D3) a dalších odečtech (D4, D7) se hodnotí jako alergická reakce (obr. 5). Nejasné reakce (? +) se považují za klinicky relevantní v individuálních případech. Vyžadují další vyšetřování (opakování ET s různými koncentracemi, ROAT test, apod.) (42, 45, 62, 66, 99).
Image 5. Alergické reakce v epikutánních testech (sestupně +++ silná, ++ střední, + mírná intenzita) 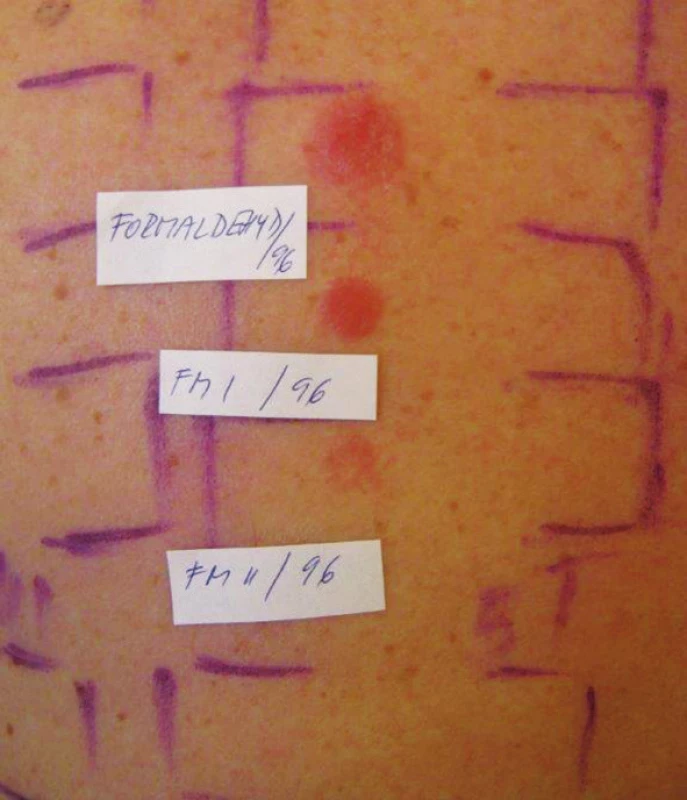
Iritační reakce
Iritační reakce v ET mohou mít různou morfologii. Klasická iritační reakce má monomorfní vzhled, je ohraničená na místo aplikace a maxima dosahuje první odečítací den (D2). Během dalších hodnocení reakce zeslabuje (tzv. „decrescendo“ fenomén) nebo zcela vymizí. Příčinami bývají nevhodná koncentrace, zvýšená dráždivost kůže a další faktory. Některé iritační reakce mají charakteristický obraz: Mýdlový (šamponový) efekt (obr. 6) vyvolávají mýdla, mycí, čisticí prostředky, detergenty a alkalické látky i v dostatečném ředění při prvním odečtu (D2). Monomorfní erytém se při dalších odečtech mění v jemné řasení kůže a posléze vymizí. Okrajový („edge“, „ring-shaped“) fenomén pozorujeme D2 a další odečítací dny (D3, D4, D7) kompletně vymizí. Na okraji testovacího pole je patrný erytém, eventuálně papulky, centrum je bez erytému. Reakci vyvolává akumulace látky (obvykle v tekutém vehikulu) na okrajích testovacího pole. Tuto neobvyklou morfologii může mít pozitivní alergická reakce na testované kortikosteroidy. Vzhledem k vazokonstrikčnímu efektu těchto léků může být při hodnocení za 48 hodin (D2) centrum bledé a pouze v okraji testovacího pole patrný erytém a eventuálně papulky (obr. 7). Folikulárně vázanou purpuru (dřívější termín flyktény) vyvolávají typicky některé alergeny, zejména chlorid kobaltnatý (až u 5 % testovaných osob), dále textilní barviva a další alergeny [45]. Považuje se za toxickou reakci při transadnexálním průniku alergenu do epidermis [45]. Pustulózní reakce se nevyskytuje v ET často. Objevuje se u pacientů s atopickou diatézou po solích kovů (soli niklu, mědi, chromu, zlata) – obrázek 8. Může jít o zesílenou odpověď způsobenou chemotaxí neutrofilních leukocytů. Pustula může překrývat alergickou reakci, proto v nejasných případech je třeba testy zopakovat s nižší koncentrací alergenu [45, 66, 99].
Image 7. Alergická reakce „edge“ charakteru 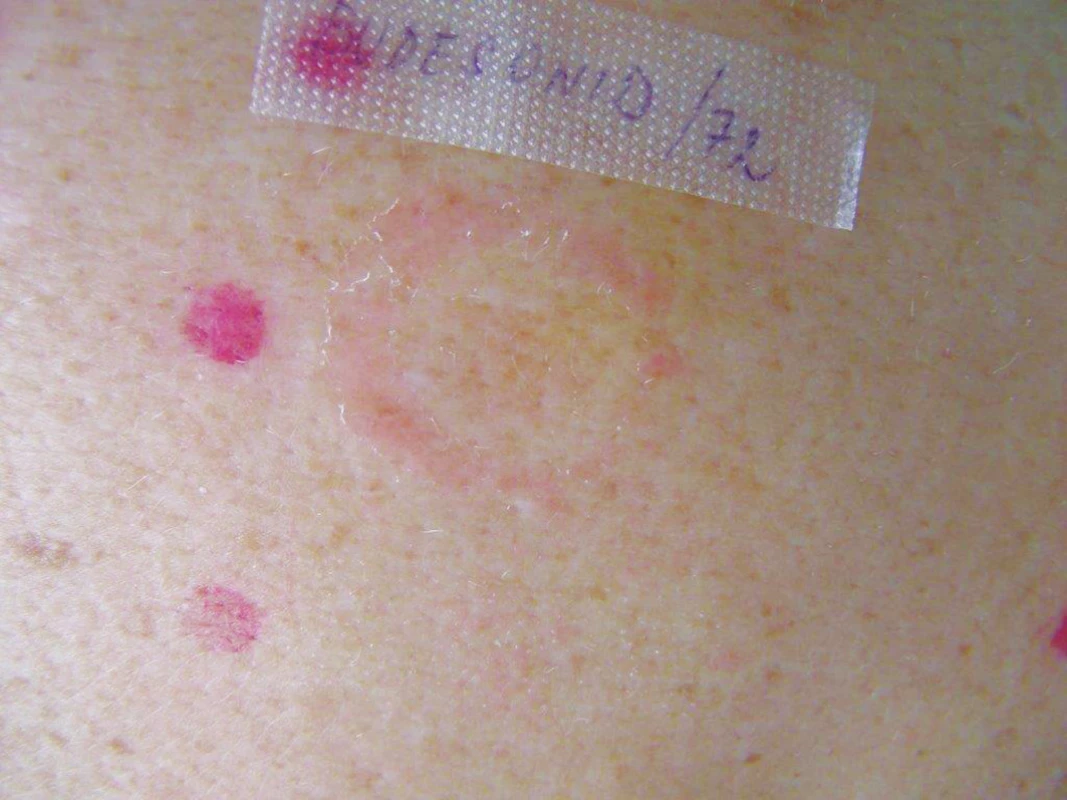
Image 8. Pozitivní reakce s mokváním a pustulami 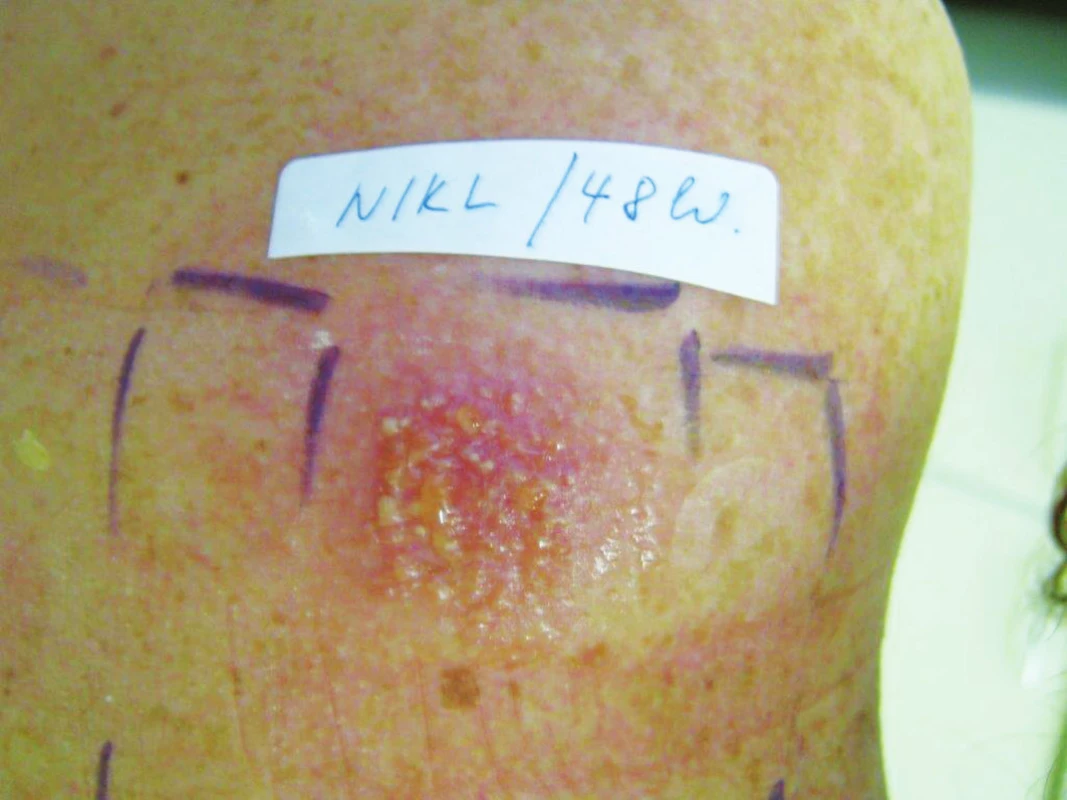
Další časté reakce vznikající při epikutánních testech nepatří mezi alergické ani iritační reakce. Vyskytnout se mohou tlaková/tahová reakce, které vznikají při testování pevných látek, občas se vyskytují drobné eroze nebo puchýř (obr. 9, 10). U pacientů s plastickým dermografismem se přechodně objevuje urtikariální reakce. Nekrózu vyvolá chybné ředění a nesprávná testovací koncentrace. Kausticky působí silné kyseliny, zásady, nebo jiné koncentrované chemikálie. Před aplikací látek, které nejsou součástí komerčně dodávaných testů, proto musí být k dispozici informace o jejich složení. Látky neznámého složení se nesmí testovat. Nekróza se hojí se sekundární jizvou, u mladších osob často keloidního charakteru. Jedná se o chybně provedený test a jde o poškození pacienta. Pigmentace v místě pozitivních reakcí vzniknou při nerespektování doporučení pacientem a opalování ještě nezhojených pozitivních reakcí. Hyperpigmentace mohou přetrvávat týdny a obvykle dobře reagují na lokální kortikosteroidy. Depigmentaci v místě ET vyvolává např. hydrochinon [45, 66, 99].
Image 9. Tlaková reakce po sejmutí testovacích náplastí 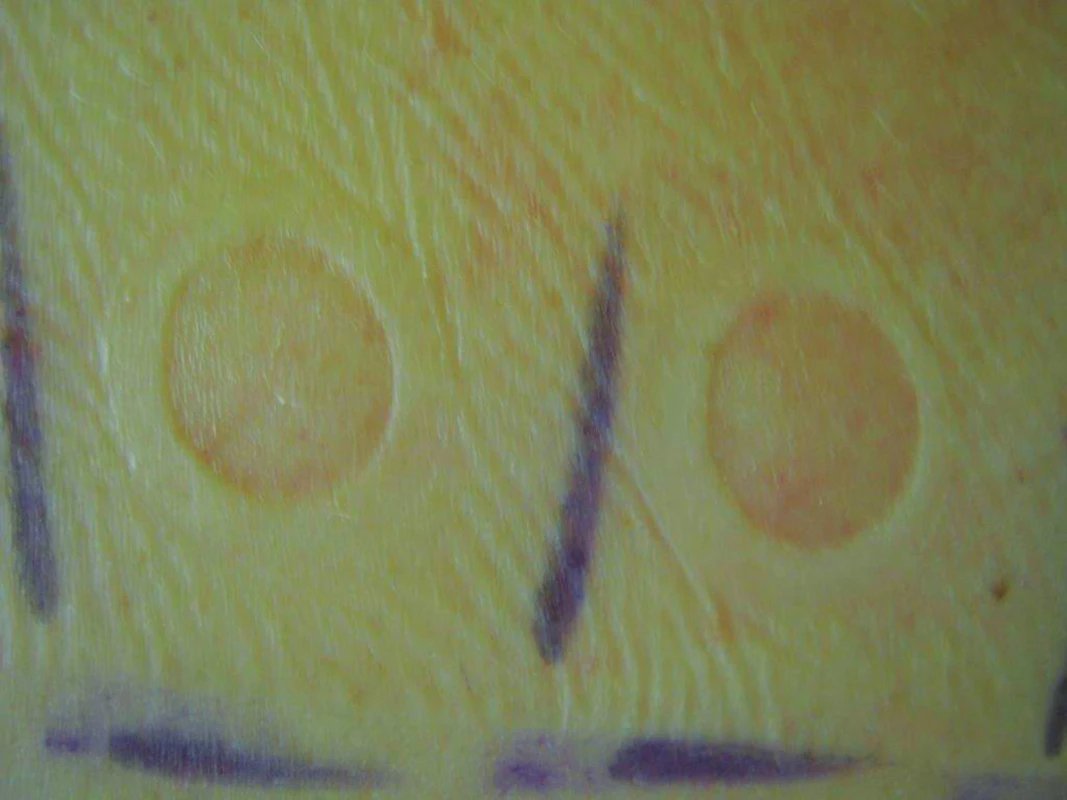
Image 10. Tahová reakce charakteru puchýře u okraje testovací náplasti 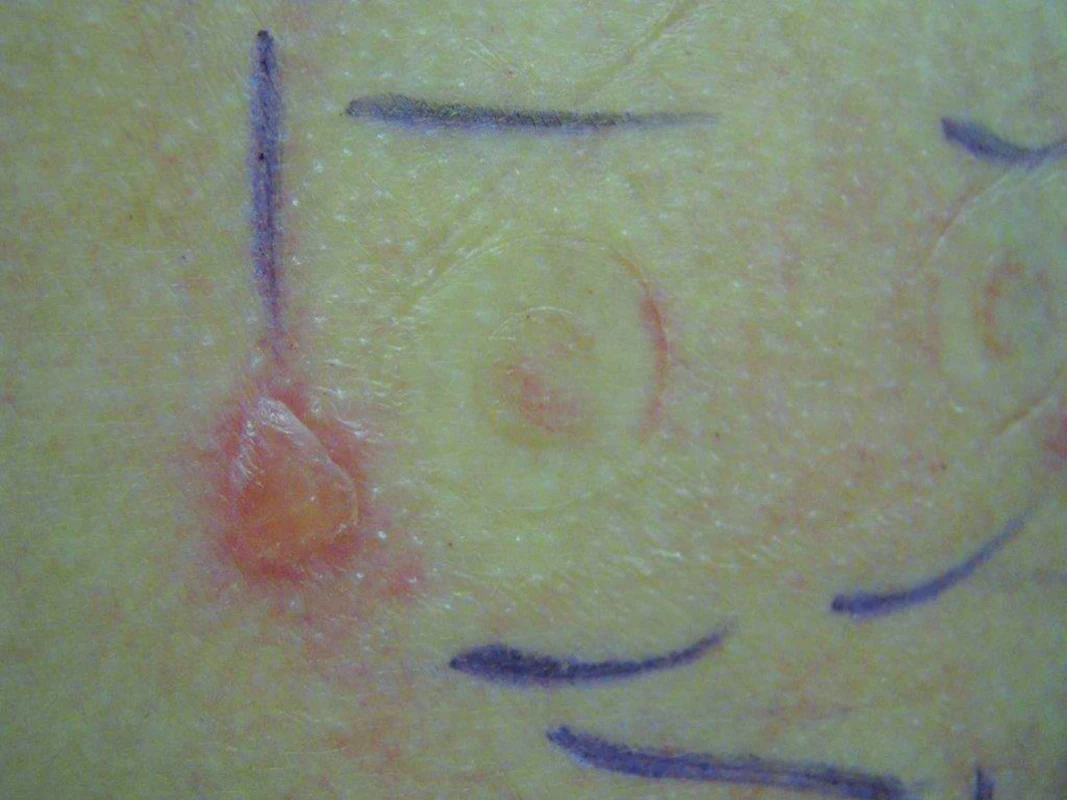
Kontraindikace epikutánních testů
ET jsou kontraindikovány u akutních nebo chronických dermatóz v místě aplikace testů. Opálená kůže může vést k falešně negativním reakcím (imunosupresivní účinky UV záření) a slabé reakce lze přehlédnout. Vhodný časový odstup k testování je nejméně 4–6 týdnů [42, 45, 61, 66, 99].
Aplikované léky (celkové nebo lokální) s imunosupresivními (cyklosporin A, azatrioprin, kortikosteroidy) nebo imunomodulačními účinky (pimecrolimus, tacrolimus) mohou ovlivnit výsledky a vést k falešně negativním výsledkům. Prednison v dávce 20 mg významně oslaboval pozitivní reakce na soli niklu [45], pro ostatní imunosupresivní léky chybí dostatek informací. Lokálními kortikosteroidy se kůže nemá ošetřovat nejméně 7–10 dnů před aplikací testů. Vliv podávaných antihistaminik na výsledek ET je nejistý a v klinických studiích výsledky zůstávají kontroverzní [45, 62, 66]. V jedné studii se prokázal inhibiční vliv loratadinu na reakci v ET [45]. Vhodnější je všechna antihistaminika vysadit dostatečně před testováním (doba vysazení se řídí poločasem vylučování daného antihistaminika) a po celou dobu testování. Pro topické imunomodulátory (pimecrolimus, tacrolimus) chybí dostatek klinických studií [45, 66, 99]. Pacienti s akutními onemocněními, s celkovými závažnými onemocněními (solidní nádory, malignity krve), s poruchou funkce T lymfocytů (např. se sarkoidózou apod.), těhotné a kojící ženy se obvykle netestují [42, 62].
Komplikace epikutánních testů
Anafylaktoidní nebo anafylaktická reakce je naštěstí vzácná komplikace ET. Obvykle se objevuje do 30 minut po aplikaci testů s antibiotiky (např. penicilinem, gentamycinem, bacitracinem, neomycinem apod.), bílkovinou latexu nebo epoxidovou pryskyřicí u silně senzibilizovaných jedinců. „Ektopické vzplanutí“ (tzv. flare up reakce) je oživení původní dermatitidy v průběhu testování. Spolu s pozitivní reakcí v ET se oživí ložiska v místě původního působení alergenu. Reakce je vhodná k edukaci pacientů s důrazem na důsledné vyloučení kontaktu s alergenem. Přetrvávání pozitivní reakce (až 4 týdny od aplikace ET) je typické pro soli zlata nebo rtuti. U ostatních alergenů nově vzniklá pozitivní reakce v delším časovém odstupu znamená iatrogenně vyvolanou aktivní senzibilizaci. Je proto důležité po závěrečném hodnocení testovanou lokalitu důkladně osprchovat a pozitivní reakce ošetřit lokálními kortikosteroidy. Syndrom podrážděné kůže („excited-skin“ syndrom, „angry back“ syndrom) byl poprvé popsán v roce 1975. Velký počet pozitivních reakcí, které mohou splývat, se nepovažuje za relevantní, ET nelze vyhodnotit (obr. 11). Testovanou lokalitu je nutné nejprve zklidnit a pacienty je nutné s časovým odstupem (min. 2 měsíce) znovu přetestovat [66]. Aktivní senzibilizace z ET je vzácná. Jde o testy indukovanou (navozenou) senzibilizaci. Objevuje se minimálně 10–14 dnů od aplikace ET (např. u PPD). Vyvolá jí většinou vysoká koncentrace testovací substance, méně významnými faktory jsou velké množství použitého alergenu a doba kontaktu kůže s alergeny. Aktivní senzibilizace je na alergeny EZS při použití standardizovaných alergenů a dodržení standardního postupu vzácná [42, 45, 61, 62, 66, 89, 99].
Image 11. Syndrom rozhněvaných zad 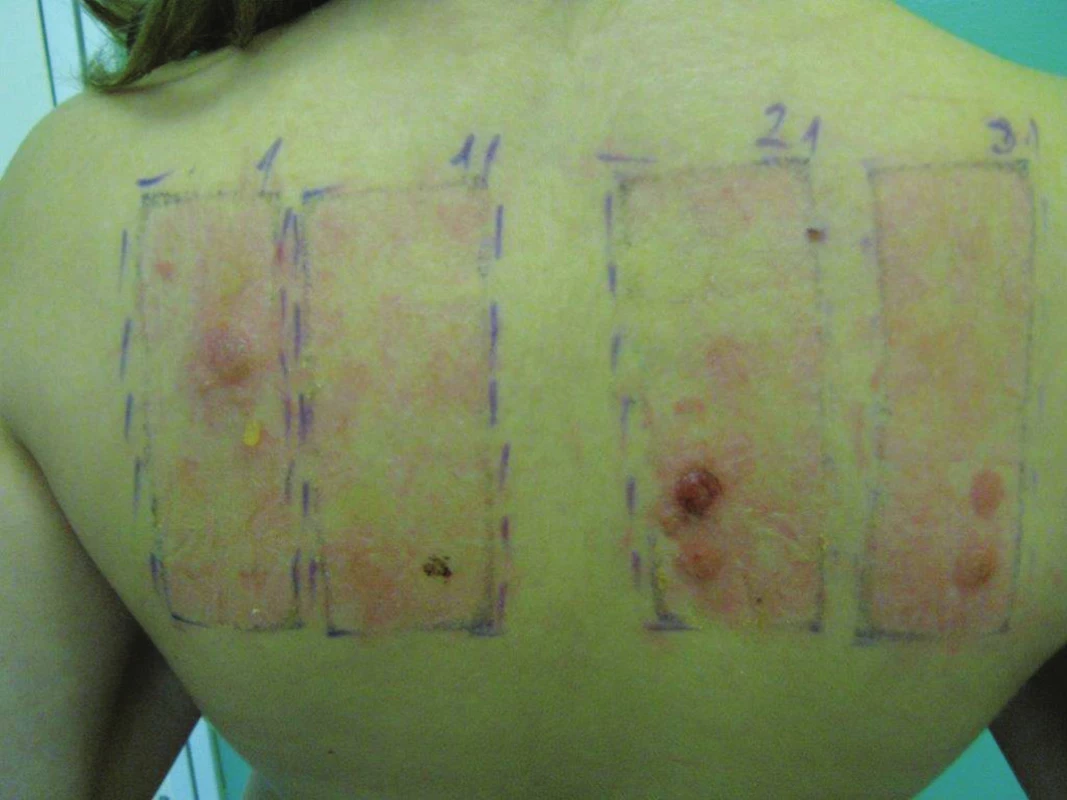
Fenomény kontaktní senzibilizace
Přecitlivělost může být monovalentní (na jeden alergen), může se objevit senzibilizace oligovalentní (na několik alergenů), méně často senzibilizace polyvalentní (na řadu alergenů) (obr. 12). Skupinová přecitlivělost se vyskytuje na látky chemicky příbuzné, sdružená alergie na alergeny vyskytující se současně [89].
Image 12. Polyvalentní kontaktní senzibilizace 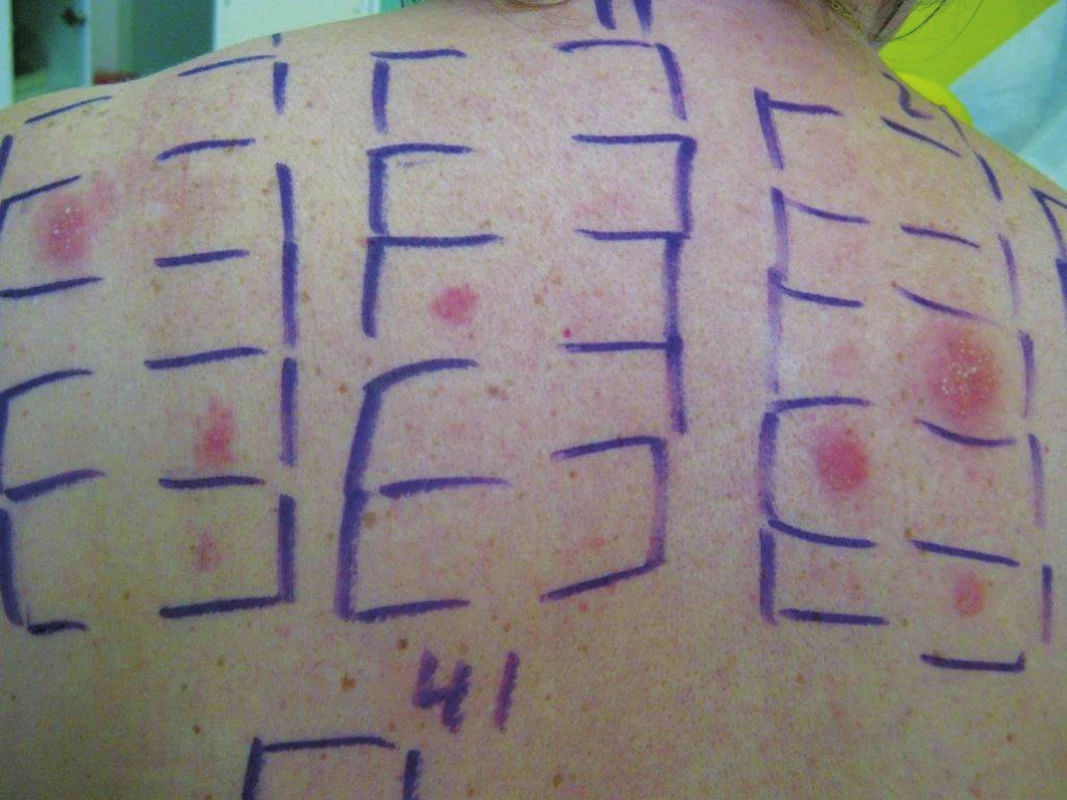
Klinická relevance
Klinická relevance (KR) dává do souvislosti zjištěné pozitivní alergeny a potíže pacienta. Jde o nejsložitější část vyšetření, která je závislá na zkušenostech a odborných znalostech vyšetřujícího lékaře.
- Aktuální (současná) KR – zjištěný pozitivní alergen je současně příčinou aktuálních problémů pacienta. Jedná se o primární příčinu onemocnění nebo zhoršující faktor (superalergizace) u jiné dermatózy.
- Minulá (historická) KR – zjištěná pozitivní reakce vyjadřuje senzibilizaci proběhlou v minulosti, pacient mívá potíže, o kterých ví, avšak zjištěná senzibilizace se nevztahuje k aktuálním problémům pacienta.
- Latentní senzibilizace – zjištěný alergen nevysvětluje udávané klinické projevy pacienta. U pacienta proběhla senzibilizace na daný alergen, avšak pacient zatím nemá klinické potíže. Může se jednat o falešně pozitivní reakci (viz dále).
- Bez klinické relevance – souvislost mezi zjištěným pozitivním alergenem a potížemi pacienta se nepodařilo zjistit. Pacienta je třeba dále sledovat [42, 45, 61, 62, 66, 99].
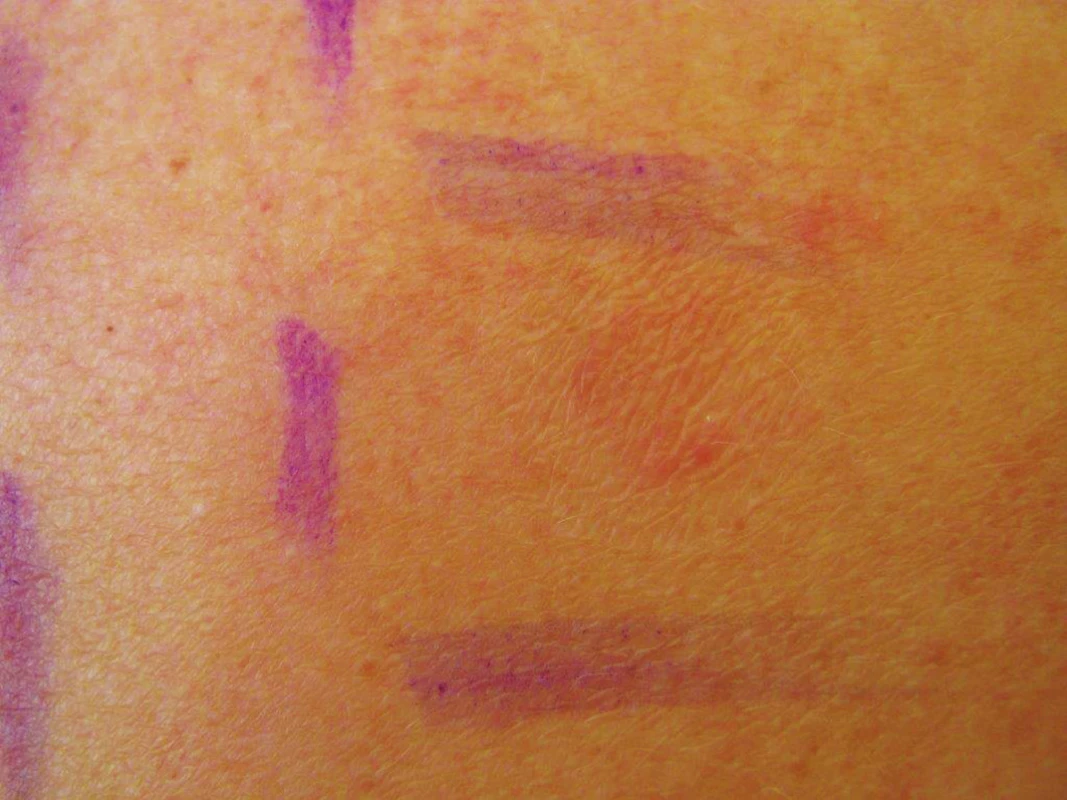
Falešně pozitivní reakce se mohou objevit i přes dodržení standardního vyšetřovacího postupu. Pozitivní reakce bez klinické relevance mívá řadu příčin (např. vysoká koncentrace nestandardizovaného alergenu, kontaminovaná nebo nečistá substance, podráždění kůže po použitém vehikulu, zbarvení kůže barevným alergenem, neznalost nebo nezkušenost odečítajícího lékaře, apod.) [42, 45, 66, 99].
Falešně negativní reakce – navzdory existující KS je výsledek ET negativní. Příčinami jsou většinou nedodržení standardního postupu vyšetření: nedostatečná okluze, krátká doba kontaktu alergenu s kůží, nedostatečná penetrace alergenu do kůže, nízká koncentrace alergenu (při ředění donesených kosmetických a hygienických přípravků), malé množství alergenu (např. odpaření alergenu v tekutém vehikulu, oxidace alergenu apod.), nedodržení standardního postupu pro vyhodnocení testů (např. pozitivní reakce na neomycin až v D7). Při krátké době trvání onemocnění může být pozitivní reakce omezená na místo primárního kontaktu. V těchto případech bývá diagnostický tzv. blízký test, kdy se ET s podezřívaným alergenem aplikuje do blízkosti primárního ložiska, většinou na předloktí – pokud jsou projevy lokalizované na rukou [42, 45, 62, 66, 89, 99].
NEJČASTĚJŠÍ KONTAKTNÍ ALERGENY
Nejčastěji zjišťovanými kontaktními alergeny jsou soli kovů (nikl, kobalt, chrom), součásti kosmetických a farmaceutických výrobků, parafenylendiamin [9, 15, 52, 61, 90].
Nikl
Nikl je dlouhodobě celosvětově nejčastějším kontaktním alergenem dětí i dospělých. Počet senzibilizovaných i přes řadu opatření stále stoupá. V roce 2008 v USA byl nikl nazván „alergenem roku“, KS u žen mezi 18.–50. rokem dosáhla 24 %, u mužů 4 % [36, 76]. V Evropě je situace obdobná, KS v testované populaci byla zjištěná po roce 2000 v Dánsku u 16,8 % testovaných osob, v Německu u 17,3 %, ve Velké Británii u 18,6 %, v Itálii u 25,6 %. Rozdíly v KS byly zaznamenány i regionálně (střední Evropa 19,7 %, jižní Evropa 24,4 % testovaných) [73]. V České republice (ČR) byla KS na soli niklu zjištěná v letech 1995–2003 ve výši 13,8 % (muži 4,7 %, ženy 19 %) [52], v letech 2004 až 2012 stoupla na 17,3 % (muži 6,3 %, ženy 21,7 %) [9].
Zdrojů niklu je v populaci velké množství, obsahuje ho řada předmětů běžného denního kontaktu, např. bižuterie a šperky včetně zlata [58, 76], kovové součásti oblečení, brýlové obruby. Je uvolňován z kovových součástí mobilních telefonů [41, 101], tabletů a počítačů [4, 38, 40]. Dalšími zdroji niklu jsou stomatologické a ortopedické aparáty [44], hračky, alkalické baterie apod. [76]. Jako příměs se vyskytuje s ostatními kovy v pracích prášcích, tekutých mýdlech a dalších přípravcích pro domácnost [3, 76]. Zdrojem niklu je také celá řada potravin (např. listová zelenina, ovesné vločky, luštěniny, ořechy, kakao atd.), které je vhodné omezit u silně senzibilizovaných osob [76]. V poslední době byly popsány příklady KS na soli niklu obsažené v make-upech, kosmetických tužkách, očních stínech [88, 98], uvolňované při kontaktu s elektronickými cigaretami [56] nebo do ovzduší při manipulaci a balení stíracích losů [20].
Zastavit, popř. snížit dramaticky narůstající počty senzibilizovaných osob vedl Evropskou unii (EU) ke snaze omezit množství niklu v předmětech z běžného kovu. První Direktiva EU regulující množství niklu v kovových předmětech (EU Communities Directive 94/27/EC) byla přijata v roce 1994. Jejímu příznivému vlivu se přisuzuje pokles senzibilizace v Německu z 36,1 % (v roce 1994) na 25,8 % (v roce 2001) u žen mladších 31 let [73, 75]. V následujících letech (2002–2009) již k poklesu nedošlo. Vysvětlením byla nedostatečná kontrola obsahu niklu v běžných kovových předmětech na evropském trhu včetně mobilních telefonů [75, 81, 101]. Revize Direktivy EU (v roce 2004) změnila maximální množství obsaženého niklu v kovových předmětech (0,05 %) na maximální množství uvolňování niklu, které bylo stanovené na < 0,2 µg/cm2/týden (Commission Directive 2004/96/EC) [75, 77]. Poté byl znovu v Německu zaznamenán pokles KS na nikl u žen ve všech věkových kategoriích, ve věkové skupině 1–17 let z 17,3 % (2005–2006) na 11,6 % (2011–2012), ve věkové skupině 18–30 let z 26,4 % na 19,8 %, ve věkové kategorii 31–44 let z 36,2 % na 31,1 % [75]. Obdobná situace byla popsána v Itálii, kde u žen do 26 let KS postupně klesala z 38,3 % (1996–1998) na 31,9 % (2002–2004) a dále na 28,3 % (2005–2007). V letech 2008-2009 zůstala na 29 %. Naopak vzestup byl zaznamenán u žen starších 36 let [67]. I přes pozitivní klesající trend v některých evropských zemích je KS na soli niklu zejména u žen stále vysoká, u nás má stoupající tendenci [9, 52] a bude zřejmě vyžadovat další regulace [47]. Pozitivně testovaným pacientům je k dispozici rychlý a levný orientační test na přítomnost solí niklu v kovových předmětech (obr. 13) [79].
Image 13. Pozitivní test na přítomnost solí niklu v patentu 
Kobalt
Kobalt je silný senzibilizátor a častá příčina AKD. Často se vyskytuje sdružená přecitlivělost se solemi niklu a/nebo kobaltu. Tradičními zdroji jsou kovové součásti oděvů a předměty z běžného kovu (včetně mobilních telefonů, laptopů), ortopedické a dentální materiály [47, 59]. Profesionálně jsou solím kobaltu exponováni pracovníci některých profesí (např. obráběči kovů, výrobci keramiky, stavební dělníci apod.) [89]. Soli kobaltu se uvolňují z řady kožených výrobků (obuvi, sedacích souprav, kožených oděvů, z volantu a ostatních kožených součástí automobilů apod.) [82, 85]. Systémová kontaktní dermatitida na soli kobaltu byla popsána po kovovém implantátu obsahujícím kobalt [102].
Soli kobaltu v ČR byly pozitivní v letech 1997–2001 u 5,2 % [52], v jiné publikaci byly soli kobaltu pozitivní v letech 1995–2003 u 5,4 % testovaných (muži 3,8 %, ženy 6,3 %), v letech 2004–2012 stoupla KS na 8,3 % (muži 5,7 %, ženy 9,3 %) [9]. V Evropě se pohybovala KS na soli kobaltu podle různých publikací mezi 5,2–7,8 % [15, 90, 93], v USA byla mezi 7,4–11,0 % [15]. Regionální rozdíly v KS na soli kobaltu byly zjištěny v rozmezí mezi 6,2 % testovaných (data z Velké Británie) až 8,8 % testovaných ze severovýchodního regionu Evropy) [90, 93]. V Itálii stoupala KS na soli kobaltu u mužů do 26 let z 2,7 % (1996–1998) na 7,3 % (1999–2001) a 9,6 % (2002–2004) a mírně klesla na 6,6 % (2005–2007) [67].
Stanovení klinické relevance u pozitivní reakce na soli kobaltu není snadné, lze jí prokázat asi u 25 % pacientů [82, 85]. Regulace EU množství kobaltu v kožených předmětech je připravená, ale zatím nebyla schválená. K dispozici je orientační test ke zjištění solí kobaltu v předmětech (tzv. Cobalt spot test) [57].
Chrom
Šestimocné soli chromu díky své výborné penetrační schopnosti do kůže mají vysoký senzibilizační potenciál. Regulace EU (2003/53/EC) platná od roku 2005 vedla k poklesu profesionální senzibilizace na soli chromu u stavebních dělníků. Od roku 1981 se přidává do cementu síran železnatý. Tím se snížil obsah ve vodě rozpustných šestimocných iontů chromu pod 2 ppm a KS na chrom se z profesionálního problému změnila na spotřebitelský problém [7, 73]. Tradičními zdroji chromu jsou kovové předměty, mobilní telefony, dentální a ortopedické implantáty, barvy a antikoroziva [7, 44]. V dekorativní kosmetice je použití chromu zakázáno od roku 1976, nelze však vyloučit výskyt ve stopových množstvích (jako příměs nebo nečistota), která u senzibilizovaných osob mohou vyvolat kožní reakci [7]. V současné době jsou hlavními zdroji chromu kůže a kožené výrobky, kterým soli chromu zaručují měkkost, pružnost, trvanlivost. Chrom obsahuje 95 % kožených výrobků [7, 83]. Nová regulace EU se týká obsahu chromu v kůži a kožených výrobcích [84]. V roce 2003 bylo sníženo množství šestimocného chromu v ochranných rukavicích pod 10 ppm (EN 420 : 2003) a v roce 2009 byl povolený limit snížený pod 3 ppm (EN 420 : 2009). Německo jako první země EU v roce 2010 uvedlo do praxe opatření pro limit obsahu solí chromu (< 3 ppm) pro všechny kožené výrobky, které přicházejí do dlouhodobého kontaktu s kůží. Takzvané „chrom–free“ výrobky i přesto mohou obsahovat soli chromu a vyvolávat AKD [86]. Stejný limit pro všechny země EU platí od roku 2014 (EU Commission Regulation No. 301/2014) a pro všechny kožené výrobky přicházející na trhy EU nabyla účinnosti od května 2015 [7, 84].
KS na soli chromu v Evropě mírně klesla, z 5,3 % (2002–2003) na 4,2 % (2007–2009 [75], v Německu se KS pohybuje v rozmezí 2,4–5,9 % [90]. V Itálii poklesla KS na soli chrómu u žen z 10,2 % (1996–1998) na 4,6 % (2008–2010), u mužů z 11,3 % (1996–1998) na 5,9 % (2008–2010) [67]. V ČR dosáhla KS v letech 1995–2003 4,3 % (u mužů 5,8 %, u žen 3,4 %), v letech 2004–2012 stoupla na 5,4 % (u mužů 6,4 %, u žen 4,7 %) [9]. Mimo EU je KS na soli chromu podstatně vyšší, v Asii se uvádí KS na chrom ve výši 15,4 % (2009), v USA dokonce 16,1 % (2012) [7].
Fragrance (vonné látky)
Fragrance (vonné látky) jsou příčinou 30–45 % alergických reakcí na kosmetické přípravky [63, 103]. Kromě kosmetických výrobků se parfemace přidává také do výrobků pro domácnost a průmyslových výrobků. Používá se více než 3000 chemických látek různého původu (syntetického, přírodního, živočišného, rostlinného). Projevy se vyskytují nejčastěji na obličeji, krku nebo v podpaží [12, 18, 34].
V EZS se testují dvě směsi vonných látek (fragrance mix – FM I, FM II) a hydroxyisohexyl-3 cyclohexen-karboxaldehyd (HIIT, komerčně Lyral). Směs alergenů FM I obsahuje 8 vonných složek – extrakt lišejníku Evernia prunastri (oak moss absolute), eugenol, isoeugenol, hydroxycitronellal, skořicový alkohol, skořicový aldehyd, skořicový alfa-amylaldehyd a geraniol. Směs FM II obsahuje 6 vonných látek (HIIT, citral, farnesol, citronellol, hexylcinnamal, kumarin) a do EZS byla zařazena v roce 2005 [21, 22, 63, 71]. FM I zachytí přibližně 70–80 % KS na vonné látky [21, 22, 96]. Další přibližně třetinu senzibilizovaných pacientů zachytí FM II [21, 22, 71, 87]. Přibližně 15 % kontaktních alergií na vonné složky EZS nezachytí [11, 21, 22].
U nás KS na FM I byla zjištěná v prvním sledovaném období (1995–2003) ve výši 5,6 % (muži 4,3 %, ženy 6,3 %), ve druhém období (2004–2012) mírně klesla na 5,4 % (muži 4,8 %, ženy 5,6 %). FM II se v ČR testuje od roku 2008 a KS byla zjištěna u 2,7 % testovaných osob (muži 2,5 %, ženy 2,7 %). HIIT (testován také od roku 2008) byl pozitivní u 1,3 % testovaných (muži 0,9 %, ženy 1,5 %) [9]. V Německu podle posledních údajů dosáhla KS na FM I 8,1 %, FM II 5,4 % a na HIIT 2,3 % [18]. V Evropě se KS pohybuje u FM I mezi 4,8–7,7 %, na FM II 1,8 až 5,5 % a na HIIT 0,5–2,7 % [90]. V USA se KS na FM I pohybuje mezi 7,4–11 % na FM I [15].
Podle Direktivy EU (EU Directive 2003/15/E) se musí vonné látky povinně uvádět ve složení výrobků (jako parfum, aroma nebo fragrance). Dvacet šest vonných substancí musí být uvedeno ve složení jmenovitě, pokud je použitá koncentrace v přípravcích ulpívajících na kůži („leave-on“) vyšší než 10 ppm (0,001%) a 100 ppm (0,01%) v přípravcích, které se z kůže oplachují („rinse-off“) [34]. Obdobné opatření se týká detergentů, kde je nutné uvést 26 vonných komponent, pokud je jejich použitá koncentrace vyšší než 100 ppm (Regulation EC 684/2004) [34].
Peruánský balzám
Peruánský balzám (PB) je dalším typickým kosmetickým alergenem v EZS. Jde o alergen přírodní povahy, pocházející ze stromu Myroloxon balsamum var. pereirae. Surový PB byl zakázán v kosmetických přípravcích v roce 1982. Extrakcí nebo destilací se získávají jednotlivé složky, které se považují za méně alergogenní a mohou se používat nadále. Avšak složení pryskyřice se regionálně liší. Na rozdíl od vonných substancí se PB nemusí uvádět ve složení výrobku [63]. Kromě kosmetických přípravků se PB používá jako přísada do nealkoholických nápojů nebo jako koření (skořice, hřebíček, vanilka, kari apod.) do potravin. Ačkoliv efekt dietních opatření při prokázané KS na PB zůstává sporný, pozitivní účinek se může dostavit u pacientů, u nichž běžná opatření nevedla ke zlepšení projevů [69, 87].
PB senzibilizoval v ČR v letech 1995–2003 7,4 % testovaných osob (muži 6,5 %, ženy 7,5 %), v letech 2004–2012 6,1 % testovaných (muži 6,7 %, ženy 5,9 %) [9]. V USA se KS se pohybuje mezi 10,6–13,7 % [15], v Evropě je KS na PB nižší, pohybuje mezi 5,4–9,0 % [15, 90], v Německu dosáhla podle posledních údajů 7,0 % [18].
Isothiazolinony
Isothiazolinony jsou organické sloučeniny, které se pro své baktericidní a fungicidní vlastnosti používají jako konzervační látky. V EU byly povolené 2 biocidy pro použití v kosmetice, methylchloroisothiazolinon (MCI) a methylisothiazolinon (MI). Směs MCI/MI v poměru 3 : 1 (Kathon CG) byla zavedená v 80. letech 20. století a široce se používala jako účinný širokospektrý konzervační prostředek [10]. To vedlo k epidemii AKD v Evropě, zjištěná KS se pohybovala mezi 3–8 % [35]. Došlo proto k postupnému snižování povolené koncentrace v kosmetických přípravcích (ze 100 ppm na 15 ppm) a od 16. dubna 2016 je použití MCI/MI v kosmetických přípravcích typu „leave-on“ zcela zakázáno [2]. V průmyslových kapalinách (např. lepidla, detergenty, oleje, malířské barvy, apod.) se stále používá v koncentracích mezi 15–50 ppm [36]. Pro nárůst KS na směs MCI/MI se od roku 2005 začal používat v kosmetických a průmyslových přípravcích výhradně nehalogenovaný derivát MI, jehož konzervační vlastnosti jsou nižší. Používané koncentrace proto byly vyšší než 100 ppm, a to ve všech typech kosmetických výrobků a řadě průmyslových výrobků [92]. Předpokládalo se, že se jedná o bezpečnou koncentraci [24]. S masivním používáním celosvětově prudce stoupla KS na MI [5]. Aktuálně je koncentrace ve všech kosmetických přípravcích omezená na 100 ppm, v průmyslových výrobcích (např. malířské barvy) a domácích přípravcích (přípravky na ošetřování kožených výrobků, aviváže apod.) limit není stanovený [2, 94]. Pryžové rukavice nechrání před penetrací MI [19]. Z malířských barev se uvolňuje řadu týdnů (déle než 6 týdnů) a může být příčinou relapsů onemocnění [1, 49, 50]. MI byl nazván alergenem 21. století, alergenem roku 2013 v USA [91, 92] a KS na MI druhou epidemií na isothiasolinony [2, 23, 27, 78]. Kromě AKD ekzémového vzhledu (obr. 14, 15) vyvolává i kontaktní dermatitidu charakteru lymfomatoidní dermatitidy, vzhledu erytema exsudativum multiforme, vyvolává airborne typ KD a systémovou KD (inhalací výparů) u senzibilizovaných osob včetně dětí, často zaměňovanou za recidivu atopické dermatitidy nebo lékový exantém [1, 39, 64, 97].
Image 14. Alergická kontaktní dermatitida na isothiazolinony v deodorantu 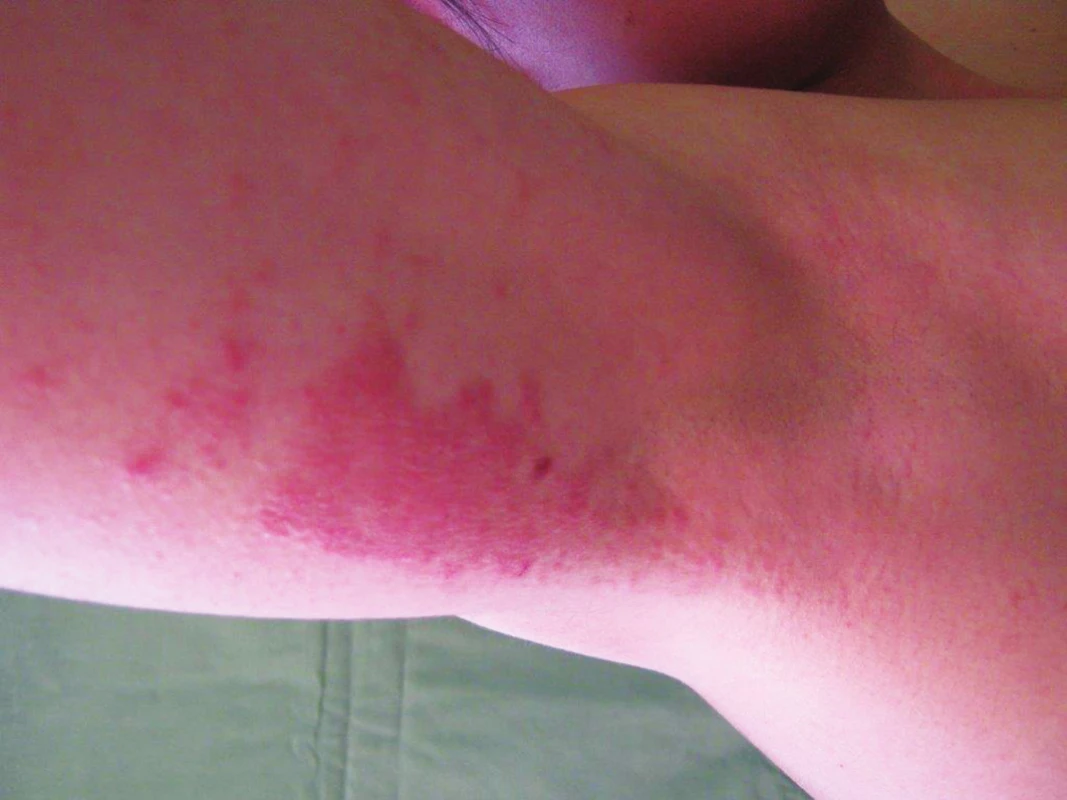
Image 15. Pozitivní epikutánní testy na isothiazolinony 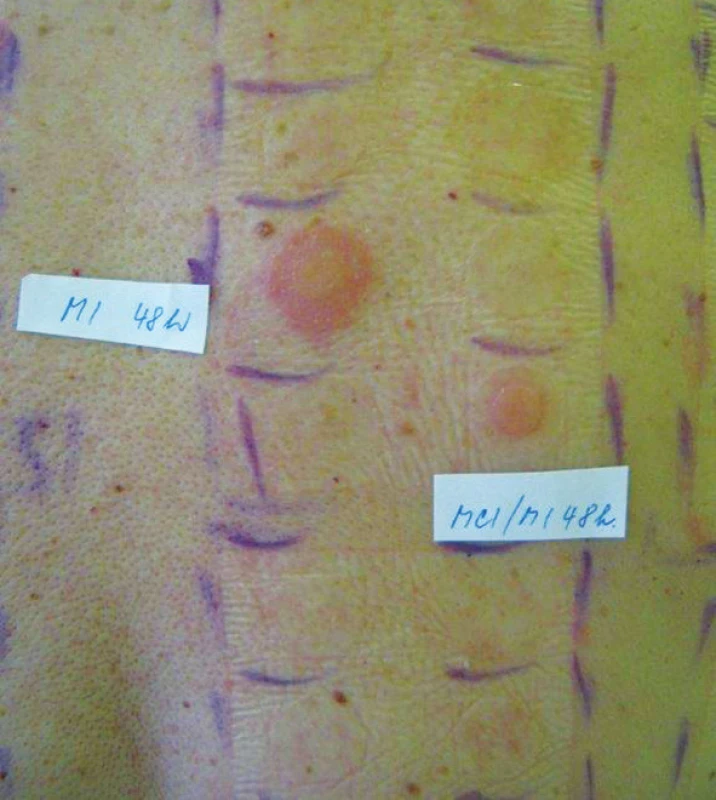
V EZS se testují MCI/MI, MI byl zařazen do EZS v roce 2013 (0,2 % ve vodě) [8]. V ČR dosahovala KS na MCI/MI v letech 1995–2003 1,4 % (muži 1,3 %, ženy 1,6 %), ve II. sledovaném období stoupla na 2,9 % testovaných (muži 3,0 %, ženy 2,9 %) [9]. Výsledky pro MI v ČR nebyly dosud publikovány. V Německu se KS na MCI/MI pohybuje mezi 2,1–4,1 % [90], na MI 1,5 % [74]. V USA se uvádí KS mezi 2,2–3,1 % [15]. U 67 % senzibilizovaných na MI se současně vyskytuje pozitivní reakce na MCI/MI [49, 74]. V Evropě je KS na MCI/MI pozitivní u 1,3–2,6 % testovaných [15]. V Dánsku senzibilizace na MI stoupla z 4,8 % (2011) na 6,5 % (2013) [51], ve Velké Británii stoupla KS na MCI/M z 4,3 % (2010) na 8,3 % (2013), u MI z 1,7 % (2010) na 11,1 % (2013) [43] a podobné údaje jsou i v ostatních zemích [2, 18, 23, 27, 35, 49, 50, 64, 100].
Methyldibromoglutaronitril
Konzervační látka methyldibromoglutaronitril (MDBGN) používaná v kombinaci s fenoxyetanolem (v poměru 1 : 4 pod názvem Euxyl K 400) byla uvedená na evropský trh v letech 1983–1985. MDBGN měl být alternativou MCI/MI [78]. Z uvedené směsi je významnějším alergenem MDBGN, fenoxyetanol senzibilizuje zřídka [89]. Široké používání vedlo ke strmému vzestupu senzibilizace, např. v Dánsku z 2,9 % (1998 až 2000) na 6,1 % (2001–2005). Tento vzestup byl označen jako další epidemie kontaktní alergie na konzervační látky (po formaldehydu a směsi MCI/MI), která vrcholila na konci 90. let 20. století a na začátku 21. století [78]. Direktiva EU snížila koncentraci MDBGN ve všech typech kosmetických přípravků na 0,1 %. V roce 2005 byl MDBGN nejprve zakázán v „leave-on“ kosmetice (Commission Directive 2003/83/E) a následně (2008) v „rinse-off“ přípravcích [92, 103].
V ČR byla KS zjištěná u 1,1 % testovaných (muži 1,3 %, ženy 1,0 %), data jsou k dispozici od roku 2007 [9]. V Německu se KS pohybuje mezi 2,3–4,5 % [18, 74], v Evropě mezi 0,1 % a 5,6 % [90], v USA byl test pozitivní u 5,8 % testovaných osob (2005–2006) [78].
Formaldehyd a konzervanty uvolňující formaldehyd
Formaldehyd se užívá jako konzervační látka v řadě oblastí (kosmetické a průmyslové výrobky, přípravky pro domácnost, dezinfekční prostředky, barvy a laky, řezné kapaliny a další výrobky). Používá se v několika formách (volný formaldehyd, konzervační látky uvolňující formaldehyd, formaldehydové pryskyřice) a všechny formy mohou vyvolat KS [89]. Konzervační látky uvolňující formaldehyd ve vodném prostředí nahradily vlastní formaldehyd v řadě kosmetických a průmyslových produktů, protože jejich senzibilizační potenciál je nižší než u vlastního formaldehydu. Patří k nim Quaternium 15 (obchodní název Dowicil 200), imidazolidinylurea (Germal 115), diazolidinylurea (Germal II), 2brom-2nitro-propanol (Bronopol), 1,3-dimethylol-5,5-dimethylhydantoin (DMDM-hydantoin) [13, 78]. EZS kromě formaldehydu zahrnuje Quaternium 15, ostatní konzervanty odštěpující formaldehyd jsou součásti speciálních sad. KS na formaldehyd pochází většinou z jiných zdrojů (profesionální expozice), u senzibilizovaných osob může dojít k recidivě projevů po použití kosmetických přípravků s obsahem konzervantů uvolňujících formaldehyd [13, 89]. Souběžná pozitivita na formaldehyd a formaldehyd uvolňující konzervanty se uvádí od 15 % do 50 % [74].
V ČR KS na formaldehyd byla pozitivní v letech 1995 až 2003 u 3,4 % testovaných (muži 2,7 %, ženy 3,8 %), v letech 2004–2012 klesla na 1,8 % testovaných osob (muži 2,1 %, ženy 1,7 %). Na Quaternium-15 byla KS zachycena v prvním období u 0,5 % testovaných (muži 0,3 %, ženy 0,7 %), ve druhém sledovaném období u 0,8 % osob (muži 0,7 %, ženy 0,9 %) [9]. V Evropě formaldehyd senzibilizoval mezi 2–3 % testovaných, v USA mezi 8–9 % [13, 14, 33]. V Německu byla v letech 2006–2011 zjištěná KS na vlastní formaldehyd ve výši 1,1 %, na Quaternium 15 ve výši 0,6 % [18]. Pro vyšší výskyt falešně negativních reakcí v ET byla koncentrace formaldehydu v EZS zvýšená na 2,0 % a používá se od roku 2014 [65].
Parafenylendiamin
Pro svůj silný senzibilizační potenciál je parafenylendiamin (PPD) od 30. let 20. století součástí EZS kontaktních alergenů [80]. Původně se používal k barvení textilu a kůže, nyní se používá k barvení vlasů. Pravidelně si barví vlasy více než 30 % žen a více než 10 % mužů starších 40 let, některé zdroje uvádějí i čísla podstatně vyšší [31]. PPD se smí v omezeném množství přidávat pouze do vlasových barev, maximální povolená koncentrace je 2 % PPD (v EU), v USA limit není stanovený. PPD se nesmí používat pro barvy na obočí, řasy nebo k přímé aplikaci na kůži [16]. Po obarvení kštice s barvou obsahující PPD se ekzémové projevy vyskytují spíše na vlasové hranici, na šíji a na obličeji, kde je často doprovází masivní edém kolem očí, ve kštici často mokvají. Aktuálním zdrojem senzibilizace u dětí a dospívajících je dočasná tetováž černou henou, která se stala oblíbenou atrakcí během dovolených, zejména mimo EU (obr. 16). Obsahuje PPD v různé koncentraci (až 27,2 %) [16]. Vysoká koncentrace PPD, dlouhotrvající kontakt s kůží bez následné neutralizace a oplachu vede k silné senzibilizaci a následným bouřlivým závažným alergickým reakcím při dalším kontaktu s PPD i při ET (obr. 17).
Image 16. Alergická reakce na parafynelendiamin po dočasné tetováži černou henou 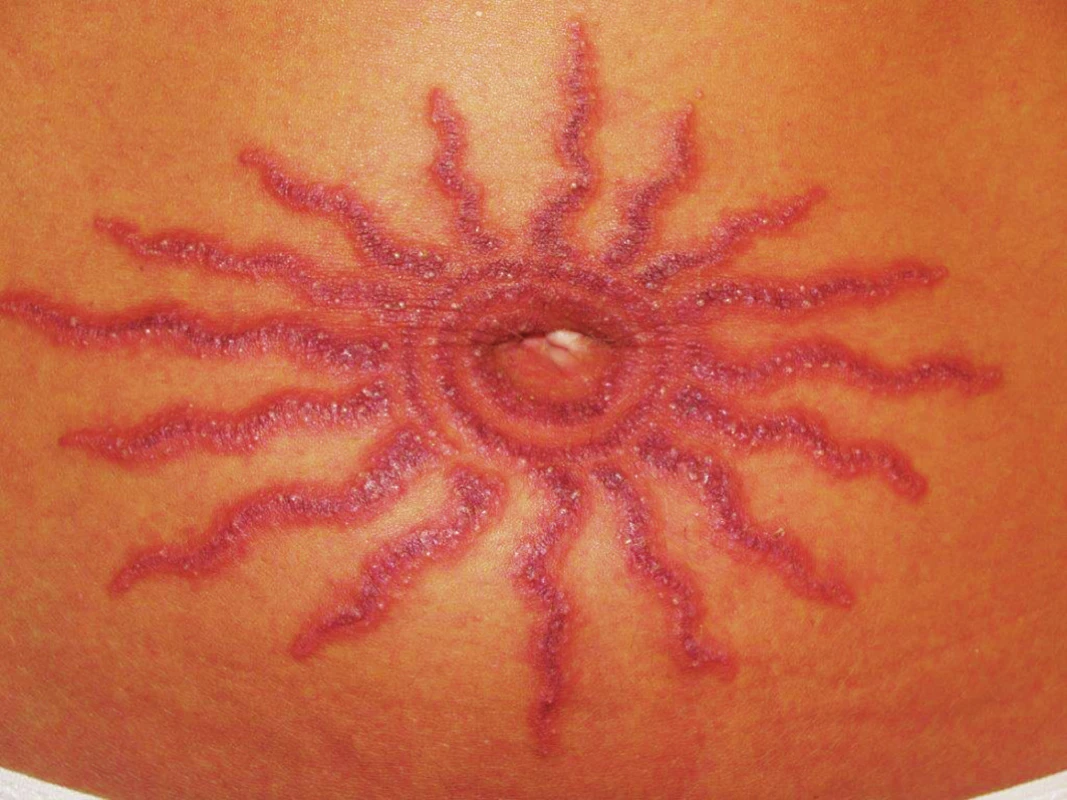
Image 17. Silně pozitivní reakce v epikutánním testu na parafenylendiamin a thiuram mix 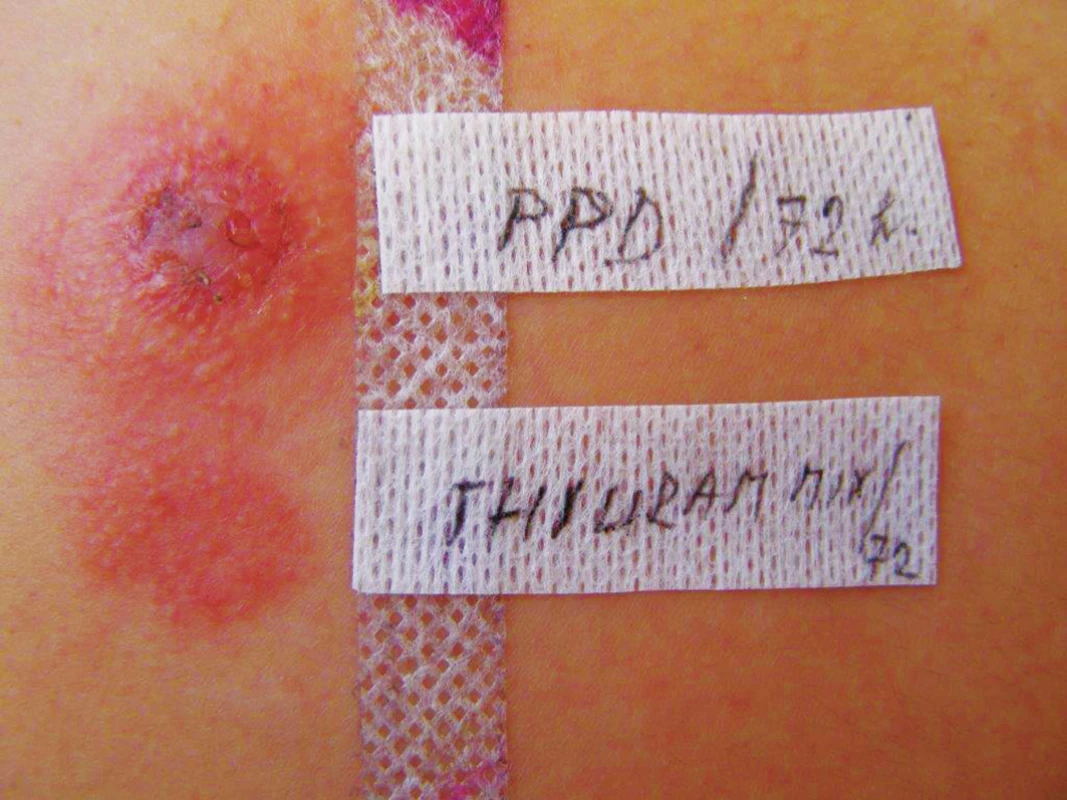
Ve světě se průměrná prevalence senzibilizace na PPD udává v Asii 4,3 %, v Evropě 4 % a 6,2 % v Severní Americe [72, 80]. KS na PPD v Evropě se pohybuje v širokém rozmezí od 1,0 % do 20,3 %, v USA od 3,0 % do 14 % [15, 16, 31, 80, 90]. V ČR byla zjištěná KS na PPD v prvním sledovaném období (1995–2003) u 1,9 % testovaných osob (muži 1,7 %, ženy 2,1 %), v druhém období (2004 až 2012) 2,7 % testovaných (muži 1,4 %, ženy 3,2 %) [9].
Textilní barvy
Směs 8 textilních barev (6,6% ve vazelíně) byla nově zařazena do EZS kontaktních alergenů [37]. V multicentrické studii [68] byla zjištěna KS ve výši 3,7 % (v rozmezí 2,1–6,9 %). U 53 % testovaných byla současně zjištěna pozitivní reakce na PPD. U 1/3 pozitivně testovaných je reakce klinicky relevantní. Disperzní barvy se používají k barvení syntetických vláken (polyester, acetát, nylon apod.), ze kterých se snadno uvolňují a patří k častým alergenům [48]. Méně často senzibilizují ustalovače nebo fixátory tkanin. Nejčastějšími alergeny jsou 4 azobarviva – disperzní modrá 124 a 106, disperzní žlutá 3, disperzní oranžová 3. Kromě ekzémových projevů (80 %) se mohou vyskytnout lichenoidní (5 %), dyshidrotické (3 %), psoriaziformní (2,7 %), numulární (2 %) projevy, purpura (3 %) nebo projevy imitují mycosis fungoides. Jsou obvykle lokalizovány v místech těsného kontaktu oděvu s kůží [48, 95]. Data z ČR nebyla zatím publikována, prevalence KS ve světě se uvádí 0,4–6,7 % [48]. V USA se udává KS u 45,5 % testovaných s klinickou relevancí mezi 42–78 %, u cíleně testované populace je pozitivních až 100 % testovaných s klinickou relevancí 75–100 % [55].
ZÁVĚR
Epikutánní testy jsou vyšetřovací metodou, která je náročná pro pacienta i vyšetřujícího lékaře. Z pohledu pacienta je vyšetření zdlouhavé a omezující. Od vyšetřujícího lékaře vyžaduje klinickou zkušenost, hluboké znalosti, které si musí neustále doplňovat, protože se stále objevují nové alergeny. Najít vyvolávající alergen, vztah k aktuálním potížím pacienta nemusí být vždy jednoduché. Přesto, pokud se příčinný alergen podaří identifikovat a pacient spolupracuje a pochopí podstatu onemocnění, dochází ke zhojení pacienta.
Do redakce došlo dne 14. 9. 2016.
Adresa pro korespondenci:
Prim. MUDr. Alena Machovcová, Ph.D., MBA
Dermatovenerologické oddělení FN Motol
V Úvalu 84,
150 06 Praha 5
e-mail: alena.machovcova@fnmotol.cz
Sources
1. AERTS, O., CATTAERT, N., LAMBERT, J., GOOSSENS, A. Airborne and systemic dermatitis, mimicking atopic dermatitis, caused by methylisothiazolinone in a young child. Contact Dermatitis, 2013, 68, p. 250–251.
2. AERTS, O., MEERT, H., GOOSSENS, A. et al. Methylisothiasolinone in selected consumer products in Belgium: Adding fuel to the fire? Contact Dermatitis, 2015, 73, p. 142–149.
3. BASKETTER, D. A., ANGELINI, G., INGBER, A. et al. Nickel, chromium and cobalt in consumer products: revisiting safe levels in the new millenium. Contact Dermatitis, 2003, 49, p. 1–7.
4. BERK, D. R., BAYLISS, S. J. Cellular Phone and Cellular Phone Accessory Dermatitis Due to Nickel Allergy: Report of Five Cases. Pediatric Dermatology, 2011, 28, p. 327–331.
5. BOYAPATI, A., TAM, M., TATE, B. et al. Allergic contact dermatitis to methylisothiazolinone: Exposure from baby wipes causing hand dermatitis. Australasian Journal of Dermatology, 2013, 54, p. 264–267.
6. BRASCH, J., BECKER, D., ABERER, W. et al. Guideline contact dermatitis: S1-Guidelines of the German Contact Allergy Group (DKG) of the German Dermatology Society (DDG), the Information Network of Dermatological Clinics (IVDK), the German Society for Allergology and Clinical Immunology (DGAKI), the Working Group for Occupational and Environmental Dermatology (ABD) of the DDG, the Medical Association of German Allergologists (AeDA), the Professional Association of German Dermatologists (BVDD) and the DDG. Allergo J. Int., 2014, 23, 4, p. 126–138.
7. BREGNBAK, D., JOHANSEN, J. D., JELLESEN, M. S. et al. Chromium allergy and dermatitis: prevalence and main findings. Contact Dermatitis, 2015, 73, p. 261–280.
8. BRUZE, M., ENGFELDT, M., GONCALO, M. et al. Recommendation to include methylisothiazolinone in the European baseline patch test series – on behalf of the European Society of Contact Dermatitis and the European Environmental and Contact Dermatitis Research Group. Contact Dermatitis, 2013, 69, 5, p. 263–270.
9. DASTYCHOVÁ, E., DOBEŠOVÁ, J., HORAŽĎOVSKÝ, J. et al. Vývoj kontaktní přecitlivělosti na alergeny evropské základní sady v České republice v průběhu let. Čes.-slov. Derm., 2014, 89, 3, p. 93–148.
10. DE GROOT, A. C., HERXHEIMER, A. Isothiasolinone preservative: cause of a continuing epidemic of cosmetic dermatitis. Lancet, 1989, 1, p. 314–316.
11. DE GROOT, A. C., VAN DER KLEY, A. M., BRUYNZEEL, D. P. et al. Frequency of false-negative reactions to the fragrance mix. Contact Dermatitis, 1993, 28, 3, p. 139–140.
12. DE GROOT, A. C., FROSCH, P. J. Adverse reactions to fragrances. A clinical review. Contact Dermatitis, 1997, 36, p. 57–86.
13. DE GROOT, A. C., COENRAADS, P. J. Twenty-five years quaternium-15 in the European baseline series: does it deserve its place there? Contact Dermatitis, 2010, 62, p. 210–220.
14. DE GROOT, A. C., VEENSTRA, M. Formaldehyde-releasers in cosmetics in the USA and in Europe. Contact Dermatitis, 2010, 62, p. 221–224.
15. DE GROOT, A. C., MAIBACH, H. I. Frequency of sensitization to common allergens: comparison between Europe and the USA. Contact Dermatitis, 2010, 62, p. 325–329.
16. DE GROOT, A. C. Side-effects of henna and semi-permanent ‘black henna’ tattoos: a full review. Contact Dermatitis, 2013, 69, p. 1–25.
17. DE WAARD-VAN DER SPEK, F. B., ORANJE, A. P. Patch Test in Children with Suspected Allergic Contact Dermatitis: A Prospective Study and Review of the Literature. Dermatology, 2009, 218, p. 119–125.
18. DINKLOH, A., WORM, M., GEIER, J. et al. Contact sensitization in patients with suspected cosmetic intolerance: results of the IVDK 2006–2011. J. Eur. Acad. Dermatol. Venereol., 2015, 29, p. 1071–1081.
19. ESPASANDÍN-ARIAS, M., GOOSSENS, A. Natural rubber gloves might not protect against skin penetration of methylisothiazolinone. Contact Dermatitis, 2014, 70, p. 249–251.
20. FRÉLING, E., POREAUX, C., VALOIS, A. et al. Occupational contact dermatitis caused by nickel in scratchcards. Contact Dermatitis, 2015, 73, p. 371–372.
21. FROSCH, P. J., PIRKER, C., RASTOGI, S. C. et al. Patch testing with a new fragrance mix detects additional patients sensitive to perfumes and missed by the current fragrance mix. Contact Dermatitis, 2005, 52, 4, p. 207–215.
22. FROSCH, P. J., JOHANSEN, J. D., SCHUTTELAAR, M.-L. et al. Patch test results with fragrance markers of the baseline series – analysis of the European Surveillance System on Contact Allergies (ESSCA) network 2009–2012. Contact Dermatitis, 2015, 73, p. 163–171.
23. GAMEIRO, A., COUTINHO, I., RAMOS, L. et al. Methylisothiazolinone: second ‚epidemic‘ of isothiazolinone sensitization. Contact Dermatitis, 2014, 70, 4, p. 242–243.
24. GARCÍA-GAVIN, J., VANSINA, S., KERRE, S. et al. Methylisothiasolinone, an emerging allergen in cosmetics? Contact Dermatitis, 2010, 63, p. 96–101.
25. GIMENEZ-ARNAU, A., MAURER, M., DE LA CUADRA, J. et al. Immediate Contact Skin Reactions, an Update of Contact Urticaria, Contact Urticaria Syndrome and Protein Contact Dermatitis – „A Never Ending Story“. Eur. J. Dermatol., 2010, 20, 5, p. 552–562.
26. GONÇALO, M., FERGUSON, J., BONEVALLE, A. et al. Photopatch testing: recommendations for a European photopatch test baseline series. Contact Dermatitis, 2013, 68, p. 239–243.
27. GONÇALO, M., GOSSENNS, A. Whilst Rome burns: the epidemic of contact allergy to methylisothiasolinone. Contact Dermatitis, 2013, 68, p. 257–258.
28. GOOSSENS, A., MORREN, M. Contact Allergy in Children. In Frosch, P. J., Menne, T., Lepoittevin, J.-P., (Eds). Contact Dermatitis. 4th ed., Berlin: Springer-Verlag, 2006, p. 811–830.
29. GOOSSENS, A. Art and science of patch testing. Indian J. Dermatol. Venereol. Leprol., 2007, 73, p. 289–291.
30. GOOSSENS, A. Alternatives to patch tests. Ann. Dermatol. Venereol., 2009, 136, p. 623–625.
31. HAMANN, D., YAZAR, K., HAMANN, C. R. et al. p-Phenylenediamine and other allergens in hair dye products in the United States: a consumer exposure study. Contact Dermatitis, 2014, 70, p. 213–218.
32. HANNUKSELA, M. Protein Contact Dermatitis. In Frosch, P. J., Menné, T., Lepoittevin, J.-P. (Eds). Contact Dermatitis. 4th ed., Berlin: Springer-Verlag, 2006, p. 345–348.
33. HAUKSSON, I., PONTÉN, A., ISAKSSON, M. et al. Formaldehyde in cosmetics in patch tested dermatitis patients with and without contact allergy to formaldehyde. Contact Dermatitis, 2015, 74, p. 145–151.
34. HEISTERBERG, M. V., MENNÉ, T., JOHANSEN, J. D. Contact allergy to the 26 specific fragrance ingredients to be declared on cosmetic products in accordance with the EU cosmetics directive. Contact Dermatitis, 2011, 65, p. 266–275.
35. HOSTEING, S., MEYER, N., WATON, J. et al. Outbreak of contact sensitization to methylisothiazolinone: an analysis of French data from the REVIDAL-GERDA network. Contact Dermatitis, 2014, 70, p. 262–269.
36. HSU, J. W., MATIZ, C., JACOB, S. E. Nickel Allergy: Localized, Id, and Systemic Manifestations in Children. Pediatr. Dermatol., 2011, 28, 3, p. 276–280.
37. ISAKSSON, M., RYBERG, K., GOOSSENS, A. et al. Recommendation to include a textile dye mix in the European baseline series. Contact Dermatitis, 2015, 73, p. 15–20.
38. JACOB, S. E., ADMANI, S. Allergic Contact Dermatitis to a Laptop Computer in a Child. Pediatric Dermatology, 2014, 31, p. 345–346.
39. JENSEN, J. M., HARDE, V., BRASCH, J. Airborne contact dermatitis to methylchloroisothiasolinone/methylisothiasolinone in a boy. Contact Dermatitis, 2006, 55, p. 311.
40. JENSEN, P., JELLESEN, M. S., MØLLER, P. et al. Nickel may be released from laptop computers. Contact Dermatitis, 2012, 67, p. 384–385.
41. JENSEN, P., JOHANSEN, U. B., JOHANSEN, J. D. et al. Nickel may be released from iPhone® 5. Contact Dermatitis, 2013, 68, p. 255–256.
42. JOHANSEN, J. D., AALTO-KORTE, K., AGNER, T. et al. European Society of Contact Dermatitis guideline for diagnostic patch testing – recommendations on best practice. Contact Dermatitis, 2015, 73, p. 195–221.
43. JOHNSTON, G. A. et al. The rise in prevalence of contact allergy to methylisothiazolinone in the British Isles. Contact Dermatitis, 2014, 70, s. 238–240.
44. KETTELARIJ, J. A. B., LIDÉN, C., AXÉN, E. et al. Cobalt, nickel and chromium release from dental tools and alloys. Contact Dermatitis, 2004, 70, p. 3–10.
45. LACHAPELLE, J. M., MAIBACH, H. I. Patch Testing and Prick Testing. A Practical Guide. 2nd ed. Berlin, Springer-Verlag, 2009, 195 s. ISBN 978-3-540-92805-8.
46. LACHAPELLE, J. M. Giant Steps in Patch Testing. Phoenix, USA, SmartPractice Phoenix, 2010, 169 s. ISBN 978-0-9773571-2-3.
47. LIDÉN, C. Nickel allergy following EU regulation – more action is needed. Br. J. Dermatol., 2013,169, p. 733.
48. LISI, P., STINGENI, L., CRISTAUDO, A. et al. Clinical and epidemiological features of textile contact dermatitis: an Italian multicentre study. Contact Dermatitis, 2014, 70, p. 344–350.
49. LUNDOV, M. D., KRONGAARD, T., MENNÉ, T. L. et al. Methylisothiazolinone contact allergy: a review. Br. J. Dermatology, 2011,165, p. 1178–1182.
50. LUNDOV, M. D., OPSTRUP, M. S., JOHANSEN, J. D. Methylisothiazolinone contact allergy – a growing epidemic. Contact Dermatitis, 2013, 69, p. 271–275.
51. MADSEN, J. T., ANDERSEN, K. E. Further evidence of the methylisothiazolinone epidemic. Contact Dermatitis, 2014, 70, 4, p. 246–247.
52. MACHOVCOVÁ, A., DASTYCHOVÁ, E., KOŠŤÁLOVÁ, D. et al. Common contact sensitizers in the Czech Republic. Patch test results in 12,058 patients with suspected contact dermatitis. Contact Dermatitis, 2005, 53, 3, p. 162–166.
53. MACHOVCOVÁ, A. Contact Dermatitis in Children. In Young Suck, R. O., (Ed). Contact Dermatitis. Rijeka: InTech, 2011, p. 141–156.
54. MACHOVCOVÁ, A. Profesionální kožní nemoci z povolání. In Pelclová, D. a kol. Nemoci z povolání a intoxikace. Praha: Karolinum, 2014, p. 41–48.
55. MALINAUSKIENE, L., BRUZE, M., RYBERG, K. et al. Contact allergy from disperse dyes in textiles-a review. Contact Dermatitis, 2013, 68, p. 65–75.
56. MARIDET, C., ATGE, B., AMICI, J.-M. et al. The electronic cigarette: the new source of nickel contact allergy of the 21st century? Contact Dermatitis, 2015, 73, p. 49–50.
57. MIDANDER, K., JULANDER, A., SKARE, L. et al. The cobalt spot test – further insights into its performance and use. Contact Dermatitis, 2013, 69, p. 280–287.
58. MIDANDER, K., KETTELARIJ, J., JULANDER, A. et al. Nickel release from white gold. Contact Dermatitis, 2014, 71, p. 109–111.
59. MIDANDER, K., HURTIG, A., BORG TORNBERG, A. et al. Allergy risks with laptop computers – nickel and cobalt release. Contact Dermatitis, 2016, 74, p. 353–359.
60. MOUSTAFA, M., HOLDEN, C. R., ATHAVALE, P. et al. Patch testing is a useful investigation in children with eczema. Contact Dermatitis, 2011, 65, p. 208–212.
61. MOWAD, C. M., MARKS, J. G. Jr. Allergic Contact Dermatitis. In Bolognia, J. L., Jorizzo, J. L., Schaffer, J. V. Dermatology. 3rd ed., Vol. I, USA: Elsevier Saunders: 2012, p. 233–248.
62. MOWAD, CM., ANDERSON, B., SCHEINMAN, P. et al. Allergic contact dermatitis: Patient diagnosis and evaluation. J. Am. Acad. Dermatol., 2016, 74, 6, p. 1029–1040.
63. NARDELLI, A., CARBONEZ, A., DRIEGHE, J. et al. Results of patch testing with fragrance mix 1, fragrance mix 2, and their ingredients, and Myroxylon pereirae and colophonium, over a 21-year period. Contact Dermatitis, 2013, 68, p. 307–313.
64. PATEL, A. N., WOOTTON, C. I., ENGLISH, J. S. Methylisothiazolinone allergy in the paediatric population: the epidemic begins? Br. J. Dermatol., 2014, 170, 5, p. 1200–1201.
65. PONTÉN, A., GOOSSENS, A., BRUZE, M. Recommendation to include formaldehyde 2.0% aqua in the European baseline patch test series. Contact Dermatitis, 2013, 69, p. 372–374.
66. RIETSCHEL, R. L., FOWLER, J. F. Jr. Fisher’s Contact Dermatitis. 6th ed., Hamilton: BC Decker Inc, 2008, 862 s. ISBN 978-1-55009-378-0.
67. RUI, F., BOVENZI, M., PRODI, A. et al. Nickel, chromium and cobalt sensitization in a patch test population in north-eastern Italy (1996–2010). Contact Dermatitis, 2013, 68, p. 23–31.
68. RYBERG, K., AGNER, T., ANDERSEN, K. E. et al. Patch testing with a textile dye mix – a multicentre study. Contact Dermatitis, 2014, 71, p. 215–223.
69. SALAM, T. N., FOWLER, J. F. Jr. Balsam-related systemic contact dermatitis. J. Am. Acad. Dermatol., 2001, 45, p. 377–381.
70. SCHNUCH, A., UTER, W., REICH, K. Allergic contact dermatitis and atopic eczema. In Ring, J., Przybilla, B., Ruzicka, T., (Eds.). Handbook of Atopic Eczema. 2nd ed., Berlin: Springer-Verlag, 2006, p. 178–201.
71. SCHNUCH, A., UTER, W., GEIER, J. et al. Sensitization to 26 fragrances to be labelled according to current European regulation. Contact Dermatitis, 2007, 57, p. 1–10.
72. SCHNUCH, A., LESSMANN, H., FROSCH, P. J. et al. Para-phenylenediamine: the profile of an important allergen. Results of the IVDK. Br. J. Dermatol., 2008, 159, p. 379–386.
73. SCHNUCH, A., WOLTER, J., GEIER, J. et al. Nickel allergy is still frequent in young German females – probably due to insufficient protection from nickel-releasing objects. Contact Dermatitis, 2011, 64, p. 142–150.
74. SCHNUCH, A., LESSMANN, H., GEIER, J. et al. Contact allergy to preservatives. Analysis of IVDK data 1996–2009. Contact Dermatitis, 2011, 64, p. 1316–1325.
75. SCHNUCH, A., SCHWITULLA, J. Decrease in nickel allergy in women after the second EU nickel directive. Contact Dermatitis, 2013, 69, p. 253–256.
76. SCHRAM, S. E., WARSHAW, E. M., LAUMANN, A. Nickel hypersensitivity: a clinical review and call to action. Int. J. Dermatol., 2010, 49, p. 115–125.
77. THYSSEN, J. P., JOHANSEN, J. D. Mobile phones are now covered by the European Union Nickel Directive. Contact Dermatitis, 2009, 61, p. 56–57.
78. THYSSEN, J. P., ENGKILDE, K., LUNDOV, M. D. et al. Temporal trends of preservative allergy in Denmark (1985–2008). Contact Dermatitis, 2010, 62, p. 102–108.
79. THYSSEN, J. P., SKARE, L., LUNDGREN, L. et al. Sensitivity and specificity of the nickel spot (dimethylglyoxime) test. Contact Dermatitis, 2010, 62, 279–288.
80. THYSSEN, J. P., MENNÉ, T., JOHANSEN, J. D. The increase in p-phenylenediamine allergy in Denmark is not explained by an increase in contact allergy to para group chemicals. Contact Dermatitis, 2011, 64, p. 158–184.
81. THYSSEN, J. P., UTER, W., MCFADDEN, J. et al. The EU Nickel Directive revisited-future steps towards better protection against nickel allergy. Contact Dermatitis, 2011, 64, p. 121–125.
82. THYSSEN, J. P., MENNÉ, T., LIDÉN, C. et al. Cobalt release from implantants and consumer items and characteristics of cobalt sensitized patients with dermatitis. Contact Dermatitis, 2012, 66, 3, p. 113–122.
83. THYSSEN, J. P., STRANDESEN, M., POULSEN, P. B. et al. Chromium in leather footwear-risk assessment of chromium allergy and dermatitis. Contact Dermatitis, 2012, 66, p. 279–285.
84. THYSSEN, J. P., JOHANSEN, J. D. Hexavalent chromium in leader is now regulated in European Union member states to limit chromium allergy and dermatitis. Contact Dermatitis, 2013, 70, p. 1–2.
85. THYSSEN, J. P., JOHANSEN, J. D., JELLESEN, M. S. et al. Consumer leather exposure: an unrecognized cause of cobalt sensitization. Contact Dermatitis, 2013, 69, p. 276–279.
86. THYSSEN, J. P., JELLESEN, M. S., MØLLER, P. et al. Allergic chromium dermatitis from wearing ‘chromium-free’ footwear. Contact Dermatitis, 2014, 70, p. 185–187.
87. TOMAR, J., JAIN, V. K., AGGARWAL, K. et al. Contact allergies to cosmetics: testing with 52 cosmetic ingredients and personal products. J. Dermatol., 2005, 32, p. 951–955.
88. TRAVASSOS, A. R., BRUZE, M., DAHLIN, J. et al. Allergic contact dermatitis caused by nickel in a green eye pencil. Contact Dermatitis, 2011, 65, p. 307–308.
89. URBANČEK, S., DASTYCHOVÁ, E., BUCHVALD, D. et al. Kontaktné alergeny v pracovnom a životnom prostředí. 2. upravené vydání, Banská Bystrica: Press Group, 2013, 304 s. ISBN 80-969307-5-3.
90. UTER, W., RAMSCH, C., ABERER, W. et al. The European baseline series in 10 European Countries 2005/2006 – results of the European Surveillance System on Contact Allergies (ESSCA). Contact Dermatitis, 2009, 61, p. 31–38.
91. UTER, W., GEFELLER, O., GEIER, J. et al. Methylchloroisothiazolinone/ methylisothiazolinone contact sensitization: diverging trends in subgroups of IVDK patients in a period of 19 years. Contact Dermatitis, 2012, 67, p. 125–129.
92. UTER, W., YAZAR, K., KRATZ, E.-M. et al. Coupled exposure to ingredients of cosmetic products: II. Preservatives. Contact Dermatitis, 2013, 70, p. 219–226.
93. UTER, W., GEFELLER, O., GEIER, J. et al. Contact sensitization to cobalt – multifactorial analysis of risk factors based on long-term data of the Information Network of Departments of Dermatology. Contact Dermatitis, 2014, 71, p. 326–337.
94. VANDEVENNE, A., VANDEN BROECKE, K., GOOSSENS, A. Sofa dermatitis caused by methylisothiazolinone in a leather-care product. Contact Dermatitis, 2014, 71, p. 111–113.
95. VALLADARES-NARGANES, L. M., SANCHEZ-SAMBUCETY, P., RUIZ-GONZALEZ, I. et al. Lymphomatoid dermatitis caused by contact with textile dyes. Contact Dermatitis, 2013, 68, p. 62–64.
96. VAN OOSTEN, E. J., SCHUTTELAAR, M.-L.A., COENRAADS, P. J. Clinical relevance of positive patch test reactions to the 26 EU-labelled fragrances. Contact Dermatitis, 2009, 61, p. 217–223.
97. VAN STEENKISTE, E., GOOSSENS, A., MEERT, H. et al. Airborne-induced lymphomatoid contact dermatitis caused by methylisothiazolinone. Contact Dermatitis, 2015, 72, p. 237–240.
98. VERHULST, L., PERSSON, L., ZIMERSON, E. et al. Palpebral eczematous dermatitis caused by nickel in an eye pencil. Contact Dermatitis, 2014, 70, p. 247–249.
99. WAHLBERG, J. E., LINDGERG, M. Patch testing. In Frosch, P. J., Menné, T., Lepoittevin, J.-P., (Eds.). Contact Dermatitis, 4th ed., Berlin: Springer-Verlag, 2006, p. 366–390.
100. WARBURTON, K. L., WILKINSON, M. Contact allergy to methylisothiazolinone: Has there been any change? Experience of a UK centre. Contact Dermatitis, 2015, 72, p. 398–400.
101. WÖHRL, S., JANDL, T., STINGL, G. et al. Mobile telephone as new source for nickel dermatitis. Contact Dermatitis, 2008, 56, p. 113.
102. WONG, C. C., NIXON, R. L. Systemic allergic dermatitis caused by cobalt and cobalt toxicity from a metal on a metal hip replacement. Contact Dermatitis, 2014, 71, p. 113–114.
103. YAZAR, K., JOHNSSON, S., LIND, M. L. et al. Preservatives and fragrances in selected consumer-available cosmetics and detergents. Contact Dermatitis, 2011, 64, p. 265–272.
Labels
Dermatology & STDs Paediatric dermatology & STDs
Article was published inCzech-Slovak Dermatology

2016 Issue 5
Most read in this issue-
Kontaktní dermatitidy – část II:
epikutánní testy v současné praxi - Atypický fibroxantom – popis případu
- Případ méně obvyklé mykózy
- Analýza pacientů se středně těžkou až těžkou psoriázou před zahájením biologické léčby v České republice – údaje z registru BIOREP 2005–2016
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career