-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
VLIV VSTUPNÍ CENTRÁLNÍ RETINÁLNÍ TLOUŠŤKY NA VÝSLEDEK LÉČBY DIABETICKÉHO MAKULÁRNÍHO EDÉMU AFLIBERCEPTEM – ZKUŠENOSTI Z BĚŽNÉ KLINICKÉ PRAXE V ČESKÉ REPUBLICE
Autoři: J. Němčanský 1; A. Stepanov 2; M. Veith 3; M. Koubek 1; A. Kopecký 1; S. Němčanská 1; D. Beran 2; J. Studnička 2
Působiště autorů: Oční klinika Fakultní nemocnice Ostrava a Lékařské fakulty, Ostravské univerzity 1; Oční klinika Fakultní nemocnice v Hradci Králové a Lékařské fakulty Univerzity Karlovy v Hradci Králové 2; Oční klinika Fakultní nemocnice Královské Vinohrady a 3. Lékařské fakulty Univerzity Karlovy, Praha 3
Vyšlo v časopise: Čes. a slov. Oftal., 78, 2022, No. 2, p. 64-70
Kategorie: Původní práce
doi: https://doi.org/10.31348/2022/9Souhrn
Cíle: Prezentovat roční výsledky léčby afliberceptem u pacientů s diabetickým makulárním edémem (DME) a porovnat léčebnou odezvu u nemocných s rozdílnou vstupní centrální retinální tloušťkou (CRT).
Materiál a metody: Jedná se o multicentrickou, retrospektivní, observační studii série případů. Pacienti s DME byli léčeni ve fixním režimu (5x injekcí s odstupem 1 měsíce a poté injekce ve 2měsíčních intervalech). Doba sledování byla 12 měsíců. Byl zhodnocen vývoj nejlepší korigované zrakové ostrosti (NKZO) a CRT. Měření byla prováděna před zahájením léčby a dále v období po 4, 6, 8, 10 a 12 měsících.
Výsledky: Terapeuticky naivní skupina se skládala z 82 očí 79 pacientů. Celkový soubor pacientů byl rozdělen na 3 skupiny podle vstupních hodnot CRT. První skupinu tvořilo 28 očí se vstupní CRT < 450 μm (34,1 %), do druhé skupiny bylo zařazeno 25 očí s CRT v rozmezí 450–550 μm (30,5 %) a třetí skupina se skládala z 29 očí se vstupní CRT > 550 μm (35,4 %). Průměrná vstupní NKZO a SO byla v první skupině 66 ±7,1 písmen ETDRS optotypů, poté 70 ±7 písmen, 69,6 ±7,3 písmen a 71,3 ±7 písmen na kontrole po 4, 8 a 12 měsících. Průměrná vstupní hodnota CRT a SO byla v první skupině 379 ±48,6 μm, poté 337,1 ±76,5 μm, 320,2 ±74,1 μm a 315,1 ±62,2 μm po 4, 8 a 12 měsících. Průměrná vstupní NKZO a SO ve druhé skupině byla 64,1 ±9,7 písmen ETDRS, poté 66,9 ±10 písmen, 70 ±9,9 písmen a 70,5 ±11,5 písmen po 4, 8 a 12 měsících. Průměrná vstupní hodnota CRT a SO ve druhé skupině byla 497,4 ±76,4 μm a poté 376,5 ±106,1 μm, 360,8 ±70 μm a 351,3 ±91,3 μm ve 4, 8 a 12 měsících. V třetí skupině byla průměrná vstupní hodnota NKZO a SO 59,7 ±10,4 písmen ETDRS a poté 65 ±10,6 písmen, 64,8 ±9,6 písmen a 67 ±10 písmen po 4, 8 a 12 měsících. Průměrná vstupní hodnota CRT a SO ve třetí skupině byla 639,4 ±79,6 μm a poté 396,7 ±147,1 μm, 416,9 ±139,8 μm a 368,5 ±109,9 μm ve 4, 8 a 12 měsících. Všechny tyto změny byly statisticky významné (p < 0,05).
Závěr: Léčba afliberceptem ve fixním režimu u nemocných s DME v prvním roce léčby vede ke statisticky významnému zlepšení NKZO a poklesu CRT. Pacienti s větší vstupní CRT, která byla doprovázena horší vstupní NKZO, prokázali nejlepší anatomické a funkční výsledky roční léčby afliberceptem.
Klíčová slova:
aflibercept – diabetický makulární edém – anti-VEGF terapie – běžná praxe
ÚVOD
Diabetická retinopatie a diabetický makulární edém (DME) patří mezi nejčastější příčiny těžké ztráty zraku u nemocných v produktivním věku a vzhledem k četnosti diabetu v populaci se jedná o chorobu s významným dopadem na zdraví populace [1–4]. Po dlouhá desetiletí patřilo mezi zlatý standard léčby DME ošetření sítnice laserovou fotokoagulací [5,6]. Přes pokroky v konstrukci laserů však tento typ léčby většinou pouze stabilizuje zrakové funkce [7]. Léčebný efekt u DME byl prokázán také u intravitreálně aplikovaných steroidů [8], ale teprve s rozvojem protilátek proti vaskulárnímu endoteliálnímu růstovému faktoru (anti-VEGF) došlo k výrazné změně paradigmatu léčby u DME a nemocní dosahují zlepšení vidění [9]. Dnes tvoří anti-VEGF aplikované do sklivce léky první volby u DME a v řadě klinických studií byl prokázán jejich významný účinek jak na nejlepší korigovanou zrakovou ostrost (NKZO), tak na centrální retinální tloušťku (CRT). Jedná se především o léky schválené pro nitrooční podávání – ranibizumab (Lucentis; Genentech USA Inc, San Francisco, CA, USA) [10,11] a aflibercept (Eylea; Regeneron Pharmaceutical Inc, Tarrytown, NY, USA a Bayer Healthcare, Berlín, Německo) [12]. Bevacizumab (Avastin; Genentech USA Inc, San Francisco, CA, USA) i přes to, že se v některých zemích používá pro léčbu sítnicových onemocnění, není schválen pro nitrooční podání [13].
Ranibizumab byl v úvodu používán především ve fixním léčebném režimu v měsíčních intervalech, posléze také v reaktivním režimu pro re nata (PRN) a nejnověji v proaktivním režimu Treat and Extend (T&E). V takových režimech je nutné nemocné léčené ranibizumabem sledovat a léčit v krátkých, často měsíčních intervalech. V takovém případě existuje riziko zhoršení compliance pacientů a dále to přináší vysoké sociálně-ekonomické náklady na systémy zdravotní péče a společnost [14]. Jako hlavní problém v průběhu léčby byly označeny měsíční klinické návštěvy, ke kterým většina pacientů potřebovala doprovázející osobu [15].
Aflibercept kromě blokování všech izoforem VEGF blokuje také placentární růstový faktor, navíc jeho struktura předurčuje k vyšší afinitě k VEGF a také dlouhodobějšímu účinku jak in vitro [16], tak in vivo [17]. I díky tomu má aflibercept potenciál velmi dobré efektivity při zachování únosné zátěže pro nemocné i ošetřující již ve fixním dávkovacímu režimu, kdy jsou původně 1měsíční léčebné intervaly po nasycovací dávce po 5 měsících prodlouženy na 2 měsíce.
Cílem této retrospektivní studie bylo zjistit u dosud neléčených anti-VEGF preparáty (tzv. naivních) nemocných s DME rozdělených podle vstupních hodnot CRT do třech skupin vývoj NKZO a CRT. Intravitreální léčba afliberceptem probíhala ve fixním režimu po dobu 12 měsíců.
MATERIÁL A METODIKA
Jedná se o multicentrickou, retrospektivní, observační studii série případů zahrnující pacienty z běžné klinické praxe z Fakultní nemocnice Ostrava, Fakultní nemocnice Hradec Králové a Fakultní nemocnice Královské Vinohrady, Praha, kteří byli sledováni v období od března 2016 do srpna 2019.
Celkem 82 terapeuticky naivních očí 79 pacientů bylo zařazeno do studie (u třech pacientů byly léčeny obě oči). Základní charakteristiky souboru jsou uvedeny v Tabulce 1. Jednalo se o nemocné s onemocněním diabetes mellitus 1. nebo 2. typu s prokázaným dosud neléčeným DME. Vstupní kritéria k zařazení do studie zahrnovala NKZO v rozmezí 40–80 písmen ETDRS (Early Treatment Diabetic Retinopathy Study) optotypů na postiženém oku, tedy 20/32–20/200 na Snellenových optotypech a hodnotu CRT ≥ 300 μm. Nemocní měli hladinu HbA1c do 70 mmol/mol, hladinu celkového cholesterolu do 4,8 mmol/l. Dalšími kritérii pro zařazení byly: aplikace afliberceptu v proaktivním fixním režimu, tj. začátek léčby aplikací pěti dávek v měsíčním intervalu následovanými dalšími dávkami každé dva měsíce během 12měsíčního sledování. Byla tolerována jedna výjimka z dávkovacího režimu, tj. minimální počet injekcí byl 7. Vyloučeni byli pacienti s jinými možnými příčinami snížení NKZO (např. progrese katarakty, jiné patologie předního nebo zadního segmentu oka apod.). Mezi další vylučující kritéria patřila následující: stav po iktu, dekompenzovaná hypertenze s krevním tlakem nad 140/90 mmHg, diabetická nefropatie s hladinou sérového kreatininu nad 180 μmol/l, trvání DME déle než 2 roky a vysoce riziková forma proliferativní diabetické retinopatie (PDR).
Tab. 1. Vstupní charakteristiky souboru pacientů 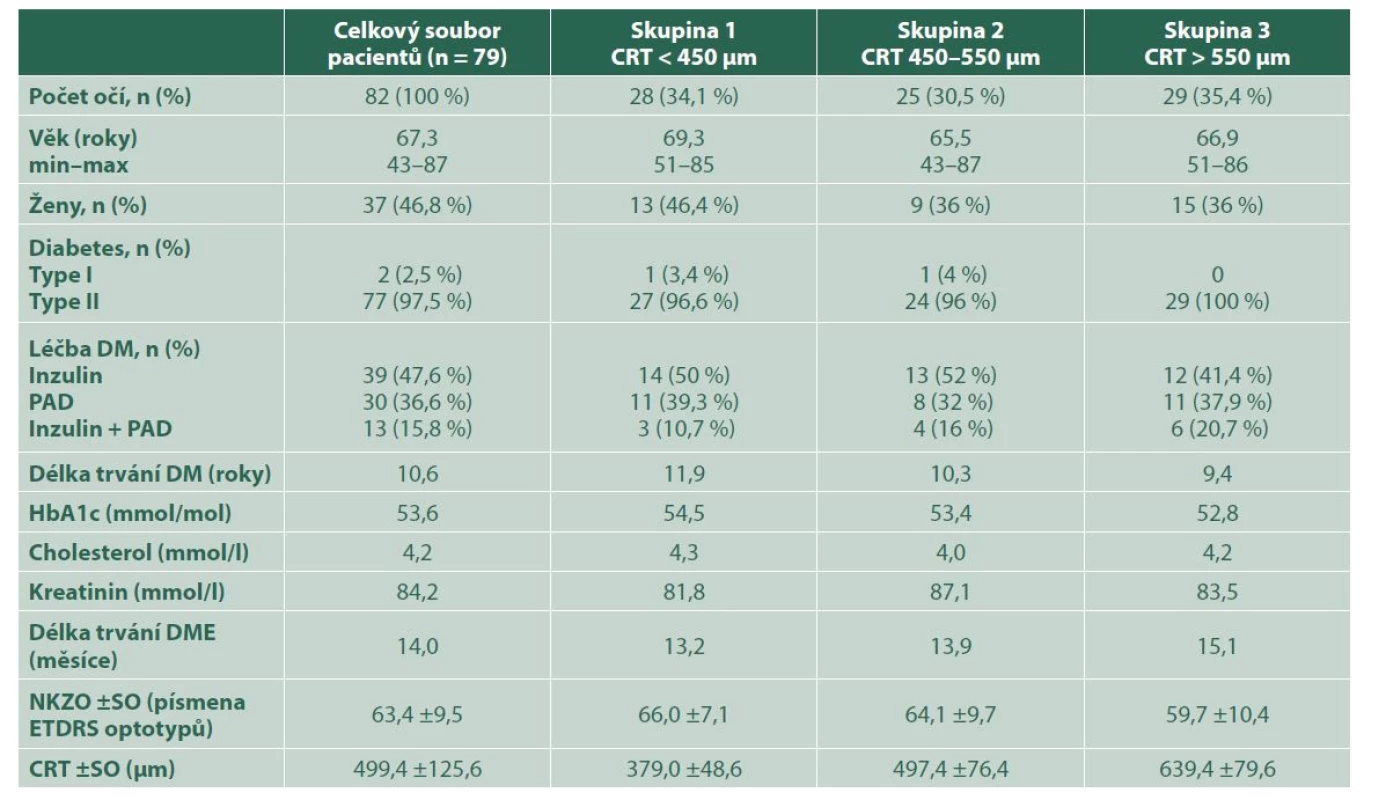
CRT – centrální retinální tloušťka, DME – diabetický makulární edém, NKZO – nejlepší korigovaná zraková ostrost, DM – diabetes mellitus, SO – směrodatná odchylka Celkový soubor pacientů byl rozdělen na 3 skupiny podle vstupních hodnot CRT. První skupinu tvořilo 28 očí se vstupní CRT < 450 μm (34,1 %), do druhé skupiny bylo zařazeno 25 očí s CRT v rozmezí 450–550 μm (30,5 %) a třetí skupina se skládala z 29 očí se vstupní CRT > 550 μm (35,4 %). Průměrný věk pacientů v celém souboru byl 67,3 let (rozmezí 43–87), první skupina pacientů měla průměrný věk 69,3 let (rozmezí 51–85), z nichž bylo 13 žen (46,4 %), pacientům ve druhé skupině bylo průměrně 65,5 let (v rozmezí 43–87), z nichž bylo 9 žen (36 %). Průměrný věk u pacientů ve třetí skupině byl 66,9 let (rozmezí 51–86), 15 z nich bylo žen (51,7 %). Všichni pacienti byli léčeni afliberceptem, celkově bylo během ročního sledování aplikováno 7,7 ±1,2 injekcí (minimálně 7), z toho byl počet aplikací v první skupině 7,8 ±1,5, ve druhé skupině 8,6 ±1,3 a ve třetí skupině byl 7,5 ±0,9.
Intravitreální injekce byly podávány všem pacientům za aseptických podmínek na operačním sále na základě ustanovených standardů zdravotní péče platných na jednotlivých nemocničních pracovištích.
V průběhu sledování bylo u všech pacientů prováděno vyšetření NKZO na ETDRS optotypech, vyšetření na štěrbinové lampě s biomikroskopií fundu v arteficiální mydriáze po aplikaci 0,5 % tropikamidu a optická koherenční tomografie (OCT) za pomoci OCT Cirrus 4000 (ZEISS, Oberkochen, Německo). Ve Fakultní nemocnici v Ostravě byla vyšetření prováděna na zařízení Spectralis OCT (Heidelberg Engineering GmbH, Heidelberg, Německo) pomocí automatické analýzy tloušťky sítnice. CRT byla definována jako vzdálenost mezi vnitřní limitující membránou a RPE ve fovee. Hodnoty CRT měřené pomocí Spectralis OCT byly poté přepočítány pomocí vzorce publikovaného Krebsem a kol. [18], aby bylo možné výsledky vyšetření ze zařízení Cirrus a Spectralis vzájemně posoudit. Tato vyšetření byla provedena před zahájením léčby a v 4, 6, 8, 10 a 12 měsíci.
Všichni pacienti před podáním intravitreální injekce podepsali informovaný souhlas. Protokol studie dodržoval zásady Helsinské deklarace.
Statistická analýza
Statistická analýza byla provedena pomocí softwaru IBM SPSS Statistics 23. Kvantitativní údaje jsou shrnuty pomocí průměru a rozmezí. Data NKZO a CRT byla zpracována za pomoci Kolmogorov-Smirnovova testu normality, přičemž hypotéza rovnosti byla zamítnuta. Změna NKZO a CRT měřená vstupně a v době 4, 6, 8, 10 a 12 měsíců byla hodnocena pomocí Friedmanova testu. Následující vícenásobné srovnání bylo provedeno párovým Wilcoxonovým testem upraveným pomocí Bonferroniho korekce. Statistická významnost byla definována jako p < 0,05.
VÝSLEDKY
Analýza zrakové ostrosti
Vstupní hodnota NKZO a SD byla 63,4 ±9,5 písmen ETDRS optotypů v celkovém souboru, z toho 66 ±7,1 písmen u pacientů v první skupině, 64,1 ±9,7 písmen ve druhé skupině a 59,7 ±10,4 písmen v třetí skupině. Hodnoty NKZO a její změny jsou uvedeny v Grafu 1. NKZO na konci ročního sledování byla 69,7 ±9,9 písmen ETDRS optotypů v celkovém souboru, 71,3 ±7 písmen u pacientů v první skupině, 70,5 ±11,5 písmen ve druhé skupině a 67 ±10 písmen v třetí skupině. Změny ve srovnání s výchozími hodnotami byly statisticky významné ve všech sledovacích obdobích (p < 0,05). Nejvýznamnější změna byla zaznamenána po 6 měsících léčby afliberceptem ve druhé skupině (+7,7 písmen ETDRS optotypů od vstupních hodnot (p < 0,05), (Graf 3). U pacientů v první a třetí skupinách byla nejvýznamnější změna NKZO zaznamenána na kontrole v 10. měsíci sledování (+6,1 a +7,3 písmen ETDRS optotypů od vstupních hodnot, p < 0,05), (Graf 3).
Graf 1. Funkční výsledky léčby u oči s diabetickým makulárním edémem a s různými vstupními hodnotami centrální retinální tloušťky (CRT). Všechny skupiny vykazovaly zlepšení nejlepší korigované zrakové ostrosti od vstupního vyšetření do konce 12měsíčního sledování; avšak skupina s CRT > 550 μm vykazovala největší zisk
NKZO – nejlepší korigovaná zraková ostrost, ETDRS – Early Treatment Diabetic Retinopathy Study, M – měsíc
Na konci roční léčby afliberceptem jsme zaznamenali zisk ≥ 15 písmen ETDRS optotypů u 24,4 % (n = 20) z celkového souboru pacientů, z toho v první skupině byl tento zisk u 21,4 % (n = 6), ve druhé skupině u 32 % (n = 8) a ve třetí skupině u 20,7 % pacientů (n = 6) (p < 0,05).
Anatomické výsledky
Průměrná vstupní hodnota CRT a SD byla 499,4 ±125,6 μm v celkovém souboru, z toho 379 ±48,6 μm u pacientů v první skupině, 497,4 ±76,4 μm ve druhé skupině a 639,4 ±79,6 μm v třetí skupině. Vstupní hodnoty CRT a jejích změna jsou uvedeny v Grafu 2. CRT a SD na konci ročního sledování byla 344,3 ±91,9 μm v celkovém souboru, konkrétně 315,1 ±62,2 μm u pacientů v první skupině, 351,3 ±91,3 μm ve druhé skupině a 368,5 ±109,9 μm ve třetí skupině (p < 0,05). Nejvýznamnější změna byla zaznamenána na kontrole po 6 měsících léčby u pacientu ve třetí skupině, kdy byl pokles CRT –274,2 μm a ve druhé skupině –153,6 μm od vstupních hodnot (Graf 4). V první skupině byla tato změna na kontrole v 10. měsíci –86,3 μm (Graf 4). Pokles CRT ve všech skupinách byl statisticky významný (p < 0,05). Na konci sledovacího období byl stálé přítomen makulární edém u 51,2 % ze všech pacientů (n = 42), z nichž 46,4 % bylo v první skupině (n = 13), 48 % ve druhé skupině (n = 12) a 58,6 % ve třetí skupině (n = 17).
Graf 2. Anatomické výsledky léčby u očí s diabetickým makulárním edémem a s různými vstupními hodnotami centrální retinální tloušťky (CRT). Všechny skupiny vykázaly signifikantní pokles CRT od vstupního vyšetření do konce 12měsíčního sledování
M – měsíc
Graf 3. Průměrná změna počtu písmen ETDRS optotypů od vstupních hodnot u třech skupin pacientů s různými vstupními hodnotami centrální retinální tloušťky během prvního roku léčby afliberceptem
NKZO – nejlepší korigovaná zraková ostrost, ETDRS – Early Treatment Diabetic Retinopathy Study, M – měsíc
Graf 4. Průměrná změna centrální retinální tloušťky (CRT) v mikrometrech od vstupní hodnoty u třech skupin pacientů s různými vstupními hodnotami CRT během prvního roku léčby afliberceptem
M – měsíc
Během sledovacího období nebyly zaznamenány žádné významné oční ani celkové nežádoucí účinky léčby.
DISKUZE
V této retrospektivní studii byly zhodnoceny funkční a anatomické výsledky léčby afliberceptem ve fixním režimu terapeuticky naivních očí s DME v běžné klinické praxi v České republice. Do studie byla zařazena relativně velká kohorta očí (n = 82) a celý soubor byl následně rozdělen do třech skupin v závislosti na vstupních hodnotách CRT.
Porovnání účinnosti a bezpečnosti u očí s DME léčených afliberceptem 2 mg nebo bevacizumabem 1,25 mg nebo ranibizumabem 0,3 mg bylo zjišťováno v rámci protokolu T studie DRCR.net (Diabetic Retinopathy Clinical Research Network) [13]. V naší kohortě pacientů bylo průměrné zlepšení NKZO po roce léčby v celém souboru pacientů o 6,3 písmen ETDRS optotypů, tedy o 7 písmen méně než v rámci protokolu T studie DRCR.net [13]. Takový rozdíl vysvětlujeme lepší vstupní NKZO v našem souboru (o 7,2 písmen), menším počtem aplikaci afliberceptu během roční léčby (o 1,3 injekci méně), použitím doplňující záchranné laserové léčby DME ve studii DRCR. net (bylo ošetřeno celkem 37 % očí) a podmínkami léčby v běžné klinické praxi. Pokles CRT v naši studii o 155,1 μm i přes menší počet aplikaci afliberceptu je srovnatelný s poklesem CRT o 169 μm ve studii DRCR.net.
Zlepšení NKZO po roční léčbě afliberceptem v našem celkovém souboru bylo o 4,4 písmena ETDRS optotypů míň než v rámci studií VISTA-DME a VIVID-DME [12]. Takový rozdíl vysvětlujeme lepší vstupní NKZO v našem souboru (o 4 písmena než ve studii VISTA-DME a o 4,6 písmena než ve studii VIVID-DME), menším počtem aplikací afliberceptu (o 0,7 injekci míň než ve studii VISTA-DME a o 1 injekci míň než ve studii VIVID-DME) a podmínkami léčby v běžné klinické praxi. Pokles CRT na konci ročního sledování v naší studii je srovnatelný s anatomickým výsledkem léčby ve studiích VISTA-DME a VIVID-DME (o 155,1 μm versus o 183,1 a 182,4 μm resp.).
Post hoc analýza studií VIVID-DME a VISTA-DME byla zaměřena na vliv vstupní CRT na výslednou NKZO [19]. Celkový soubor pacientů byl rozdělen na 2 skupiny podle hodnot CRT < 400 μm a ≥ 400 μm. Do skupiny pacientů s < 400 μm léčených v režimu 2 mg afliberceptu každých 8 týdnů bylo zařazeno 78 pacientů s průměrnou vstupní NKZO 63 písmen ETDRS optotypů a průměrnou CRT 337 μm. Po roce léčby bylo zaznamenáno zlepšení NKZO v průměru o 10,5 písmen a pokles CRT o 191,2 μm. Zlepšení NKZO o ≥ 15 písmen ETDRS optotypů bylo prokázáno u 21,8 % pacientů. Skupinu pacientů s CRT ≥ 400 μm tvořilo 208 pacientu, u kterých průměrná vstupní NKZO byla 57,7 písmen ETDRS optotypů, průměrná hodnota CRT byla 551,9 μm. Po roce léčby bylo v této skupině zaznamenáno zlepšení NKZO v průměru o 10,7 písmen a pokles CRT o 188 μm. Zlepšení NKZO o ≥ 15 písmen ETDRS optotypů bylo prokázáno u 36,1 % pacientů. Výsledky roční léčby afliberceptem neměly statistický významný rozdíl mezi skupinami (p = 0,11).
Celkový soubor pacientů v naši práci byl podle vstupních hodnot CRT rozdělen do třech skupin (< 450 μm, 450–550 μm a > 550 μm). Stejně jako Midena a kol. jsme zaznamenali největší zlepšení NKZO po roce léčby afliberceptem ve skupině s vyššími vstupnými hodnotami CRT, nicméně rozdělení do třech skupin považujeme za více přehledné a přínosné než rozdělení do dvou skupin. Na rozdíl od metodiky Mideny je naše dělení i srovnatelné co do počtu pacientů v jednotlivých skupinách.
Výsledky roční léčby DME afliberceptem v běžné klinické praxi publikovali Lukic a kol. z Moorfieldu [20] a Korobelnik a kol., který prezentoval závěry francouzské studie APOLLON [21].
Soubor pacientů ve studii Lukica a kol. tvořilo 99 očí s průměrnou vstupní NKZO 59,7 písmen ETDRS optotypů a průměrnou CRT 431 μm [20]. Po úvodních pěti měsíčních aplikacích afliberceptu bylo pokračováno v režimu léčby PRN. V průběhu sledování bylo podáno v průměru 6,9 injekcí afliberceptu. Po roce léčby bylo zaznamenáno zlepšení NKZO v průměru o 9,9 písmen ETDRS optotypů a pokles CRT o 128 μm. V této práci byla provedena i subanalýza anatomických výsledků léčby, kdy celkový soubor pacientů byl rozdělen na 2 skupiny podle vstupních hodnot: CRT 400–499 μm (73 očí) a ≥ 500 μm (26 očí). Průměrný pokles CRT ve skupině s menší CRT byl na konci ročního sledování 86 μm, ve skupině s větší vstupní CRT byla tato změna o 265 μm.
Menší zlepšení NKZO o 3,6 písmena ETDRS optotypů v naši práci v porovnání s prací Lukica a kol. vysvětlujeme lepší vstupní NKZO v našem souboru (o 3,7 písmena). Rozdělení celkového souboru do třech skupin podle vstupních hodnot CRT nám umožnilo lepší zhodnocení anatomických výsledků léčby než v případě rozdělení do dvou skupin.
Studie APOLLON zahrnovala soubor 77 dosud neléčených očí s DME, kdy průměrná vstupní NKZO byla 62,7 písmen ETDRS optotypů a průměrná CRT byla 439 μm. Stejně jako ve studii Lukica a kol. po úvodních pěti měsíčních aplikacích afliberceptu bylo pokračováno v režimu léčby PRN. V průběhu sledování bylo podáno v průměru 7,6 injekcí afliberceptu. Po roce léčby bylo zaznamenáno zlepšení NKZO v průměru o 8,4 písmen ETDRS optotypů a pokles CRT o 129,5 μm. Zlepšení NKZO o ≥ 15 písmen ETDRS optotypů bylo prokázáno u 35 % pacientů. Výsledky léčby v našem celkovém souboru jsou srovnatelné se studii APOLLON.
Naše studie, podle námi dostupných informací, je první studie hodnotící roční výsledky léčby afliberceptem v běžné klinické praxi u pacientů s DME rozdělených podle vstupních hodnot CRT na tři skupiny z funkčního i z anatomického hlediska. Pacienti s vyšší vstupní CRT, která byla doprovázena horší vstupní NKZO, prokázali nejlepší anatomické a funkční výsledky roční léčby afliberceptem. Takové výsledky lze vysvětlit rezervou pro větší zisk písmen ETDRS optotypů při nejmenších vstupních hodnotách a větší pokles CRT ve skupině s CRT > 550 μm. Mezi silné stránky naší studie patří multicentrický design sběru dat ze tří velkých univerzitních center. Omezení naší studie jsou observační povaha a relativně malá velikost vzorku ve srovnání s většími klinickými studiemi.
ZÁVĚR
Prezentujeme roční výsledky z běžné praxe u dosud neléčených pacientů s DME rozdělených podle vstupní hodnoty CRT na tři skupiny léčených afliberceptem ve fixním režimu. Na základě našich zkušeností pacienti s vyšší vstupní CRT, která byla doprovázena horší vstupní NKZO, prokázali nejlepší anatomické a funkční výsledky roční léčby afliberceptem.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmu a není podpořeno žádnou farmaceutickou firmou. Práce nebyla zadána jinému časopisu ani jinde otištěna.
Do redakce doručeno dne: 5. 11. 2021
Přijato k publikaci dne: 4. 1. 2022
První autor:
MUDr. Jan Němčanský, Ph.D., MBA
Korespondující autor:
MUDr. Alexandr Stěpanov, Ph.D., MBA, FEBO
Oční klinika FN a LF UK v Hradci Králové
Sokolská 581
500 05 Hradec Králové
E-mail: stepanov.doctor@gmail.com
Zdroje
1. Yau JW, Rogers SL, Kawasaki R, et al. Global prevalence and major risk factors of diabetic retinopathy. Diabetes Care. 2012;35(3):556 - 564.
2. Kim EJ, Lin WV, Rodriguez SM, Chen A, Loya A, Weng CY. Treatment of Diabetic Macular Edema. Curr Diab Rep. 2019;19(9):68.
3. Amoaku WM, Ghanchi F, Bailey C, et al. Diabetic retinopathy and diabetic macular oedema pathways and management: UK Consensus Working Group. Eye (Lond). 2020;34(Suppl 1):1-51.
4. Sabanayagam C, Yip W, Ting DS, Tan G, Wong TY. Ten Emerging Trends in the Epidemiology of Diabetic Retinopathy. Ophthalmic Epidemiol. 2016;23(4):209-222.
5. Early Treatment Diabetic Retinopathy Study research group. Photocoagulation for diabetic macular edema. Early Treatment Diabetic Retinopathy Study report number 1. Arch Ophthalmol. 1985;103(12):1796-1806.
6. Early Treatment Diabetic Retinopathy Study Research Group. Treatment techniques and clinical guidelines for photocoagulation of diabetic macular edema. Early Treatment Diabetic Retinopathy Study Report Number 2. Ophthalmology. 1987;94(7):761-774.
7. Nemcansky J, Stepanov A, Nemcanska S, Masek P, Langrova H, Studnicka J. Single session of pattern scanning laser versus multiple sessions of conventional laser for panretinal photocoagulation in diabetic retinopathy: Efficacy, safety and painfulness. PLoS One. 2019;14(7):e0219282.
8. Beck RW, Edwards AR, Aiello LP, et al. Three-year follow-up of a randomized trial comparing focal/grid photocoagulation and intravitreal triamcinolone for diabetic macular edema. Arch Ophthalmol. 2009;127(3):245-251.
9. Schmidt-Erfurth U, Garcia-Arumi J, Bandello F, et al. Guidelines for the Management of Diabetic Macular Edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185-222.
10. Mitchell P, Bandello F, Schmidt-Erfurth U, et al. The RESTORE study: ranibizumab monotherapy or combined with laser versus laser monotherapy for diabetic macular edema. Ophthalmology. 2011;118(4):615-625.
11. Nguyen QD, Brown DM, Marcus DM, et al. Ranibizumab for diabetic macular edema: results from 2 phase III randomized trials: RISE and RIDE. Ophthalmology. 2012;119(4):789-801.
12. Korobelnik JF, Do DV, Schmidt-Erfurth U, et al. Intravitreal aflibercept for diabetic macular edema. Ophthalmology. 2014;121(11):2247-2254.
13. Wells JA, Glassman AR, Ayala AR, et al. Aflibercept, bevacizumab, or ranibizumab for diabetic macular edema. N Engl J Med. 2015;372(13):1193-1203.
14. Martin DF, Maguire MG, Ying GS, et al. Ranibizumab and bevacizumab for neovascular age-related macular degeneration. N Engl J Med. 2011;364(20):1897-1908.
15. Droege KM, Muether PS, Hermann MM, et al. Adherence to ranibizumab treatment for neovascular age-related macular degeneration in real life. Graefes Arch Clin Exp Ophthalmol. 2013;251(5):1281-1284.
16. Papadopoulos N, Martin J, Ruan Q, et al. Binding and neutralization of vascular endothelial growth factor (VEGF) and related ligands by VEGF Trap, ranibizumab and bevacizumab. Angiogenesis. 2012;15(2):171-185.
17. Fauser S, Muether PS. Clinical correlation to differences in ranibizumab and aflibercept vascular endothelial growth factor suppression times. Br J Ophthalmol. 2016;100(11):1494-1498.
18. Krebs I, Smretschnig E, Moussa S, Brannath W, Womastek I, Binder S. Quality and reproducibility of retinal thickness measurements in two spectral-domain optical coherence tomography machines. Invest Ophthalmol Vis Sci. 2011;52(9):6925-6933.
19. Midena E, Gillies M, Katz TA, Metzig C, Lu C, Ogura Y. Impact of Baseline Central Retinal Thickness on Outcomes in the VIVID-DME and VISTA-DME Studies. J Ophthalmol. 2018 : 3640135
20. Lukic M, Williams G, Shalchi Z, et al. Intravitreal aflibercept for diabetic macular oedema: Moorfields’ real-world 12-month visual acuity and anatomical outcomes. Eur J Ophthalmol. 2020;30(3):557-562
21. Korobelnik JF, Daien V, Faure C, et al. Real-world outcomes following 12 months of intravitreal aflibercept monotherapy in patients with diabetic macular edema in France: results from the APOLLON study. Graefes Arch Clin Exp Ophthalmol. 2020;258(3):521-528.
Štítky
Oftalmologie
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
2022 Číslo 2- Stillova choroba: vzácné a závažné systémové onemocnění
- Familiární středomořská horečka
- Diagnostický algoritmus při podezření na syndrom periodické horečky
- Možnosti využití přípravku Desodrop v terapii a prevenci oftalmologických onemocnění
- Selektivní laserová trabekuloplastika nesnižuje nitroční tlak více než argonová laserová trabekuloplastika
-
Všechny články tohoto čísla
- MIKROBIOM A UVEITIDY. PŘEHLED
- INCIDENCE PSEUDOEXFOLIAČNÍHO SYNDROMU A GLAUKOMU V SOUBORU VÍCE NEŽ 14 000 OČÍ PACIENTŮ OPEROVANÝCH PRO KATARAKTU
- VLIV VSTUPNÍ CENTRÁLNÍ RETINÁLNÍ TLOUŠŤKY NA VÝSLEDEK LÉČBY DIABETICKÉHO MAKULÁRNÍHO EDÉMU AFLIBERCEPTEM – ZKUŠENOSTI Z BĚŽNÉ KLINICKÉ PRAXE V ČESKÉ REPUBLICE
- SOUČASNÉ POSTUPY V OPERACI KATARAKTY – SUBJEKTIVNÍ PREFERENCE ČESKÝCH KATARAKTOVÝCH CHIRURGŮ
- INTRAVITREÁLNÍ APLIKACE RANIBIZUMABU U TĚHOTNÉ PACIENTKY S MYOPICKOU CHOROIDÁLNÍ NEOVASKULÁRNÍ MEMBRÁNOU. KAZUISTIKA
- IDIOPATICKÉ SKLÉROCHOROIDÁLNE KALCIFIKÁCIE. KAZUISTIKA
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- INCIDENCE PSEUDOEXFOLIAČNÍHO SYNDROMU A GLAUKOMU V SOUBORU VÍCE NEŽ 14 000 OČÍ PACIENTŮ OPEROVANÝCH PRO KATARAKTU
- SOUČASNÉ POSTUPY V OPERACI KATARAKTY – SUBJEKTIVNÍ PREFERENCE ČESKÝCH KATARAKTOVÝCH CHIRURGŮ
- IDIOPATICKÉ SKLÉROCHOROIDÁLNE KALCIFIKÁCIE. KAZUISTIKA
- MIKROBIOM A UVEITIDY. PŘEHLED
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




