-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
INTRAVITREÁLNÍ APLIKACE RANIBIZUMABU U TĚHOTNÉ PACIENTKY S MYOPICKOU CHOROIDÁLNÍ NEOVASKULÁRNÍ MEMBRÁNOU. KAZUISTIKA
Autoři: M. Penčák; M. Veith
Působiště autorů: Oftalmologická klinika, Fakultní nemocnice Královské Vinohrady a 3. Lékařská fakulta Univerzity Karlovy, Praha
Vyšlo v časopise: Čes. a slov. Oftal., 78, 2022, No. 2, p. 79-83
Kategorie: Kazuistika
doi: https://doi.org/10.31348/2022/11Souhrn
Cíl: Prezentovat případ pacientky s myopickou choroidální neovaskulární membránou (CNV) ve 3. trimestru těhotenství, u které byl podán ranibizumab.
Kazuistika: 34letá pacientka byla odeslána na Oftalmologickou kliniku Fakultní nemocnice Královské Vinohrady v lednu 2020 pro myopickou CNV na pravém oku (OP). Pacientka byla ve 34. týdnu těhotenství. Vstupní nejlepší korigovaná zraková ostrost (NKZO) OP byla 68 písmen ETDRS optotypů. Sférický ekvivalent OP byl -11,5 dioptrií, axiální délka bulbu byla 27,7 mm. Na sítnici OP bylo přítomné pigmentované ložisko CNV s drobnou hemoragií. Provedená optická koherentní tomografie (OCT) OP ukázala hyperreflektivní ložisko v oblasti makuly nad retinálním pigmentovým epitelem, centrální retinální tloušťka (CRT) byla 310 μm. Provedená OCT angiografie prokázala přítomnost klasické CNV v makule OP. O dva týdny později došlo u pacientky k nárůstu hyperreflektivního ložiska a edému v makule OP, CRT byla 329 μm, NKZO byla stabilní. Po domluvě s pacientkou a ošetřujícím gynekologem byla provedena intravitreální aplikace ranibizumabu do OP ve 36. týdnu těhotenství. Na kontrole 3 týdny po aplikaci jsme pozorovali pokles edému na 276 μm a zlepšení NKZO na 78 písmen ETDRS optotypů. Pacientka porodila ve 39. týdnu císařským řezem zdravou holčičku, poporodní adaptace novorozence byla normální. Na dalších kontrolách došlo ke zlepšení NKZO na 83 písmen ETDRS optotypů a makulární edém se kompletně vstřebal. 8 měsíců po první aplikaci ranibizumabu došlo k reaktivaci CNV, NKZO klesla na 72 písmen ETDRS optotypů, v makule byl přítomný edém, CRT byla 309 μm. Byla provedena další aplikace ranibizumabu do OP. U pacientky bylo poté zjištěno těhotenství, dle výpočtu byla pacientka v den 2. aplikace ranibizumabu ve 3. týdnu těhotenství. Po 2. aplikaci došlo k opětovnému zlepšení NZKO na 79 písmen ETDRS, ke vstřebání edému na OCT a poklesu CRT na 264 μm. Těhotenství bylo ukončeno interrupcí na přání pacientky.
Závěr: Intravitreální podání ranibizumabu ve 3. trimestru gravidity vedlo u pacientky s myopickou CNV ke zlepšení NKZO a poklesu edému v makule. Aplikace neměla negativní vliv na průběh těhotenství ani na poporodní adaptaci plodu. Přesto je při podání antiVEGF preparátů u těhotných vždy nutno zvážit případná rizika podání ve vztahu k možnému přínosu. Nezbytné je pečlivé poučení pacientky.
Klíčová slova:
těhotenství – ranibizumab – antiVEGF – myopická choroidální neovaskulární membrána
ÚVOD
Intravitreální podání antiVEGF preparátů prokázalo velmi dobrou účinnost v léčbě onemocnění spojených se vznikem choroidální neovaskulární membrány (CNV) a makulárního edému, jako je vlhká forma věkem podmíněné makulární degenerace [1–4], CNV spojená s patologickou myopií [5–7], sekundární CNV při jiných očních onemocněních [8, 9], makulární edém při diabetické retinopatii nebo okluzi sítnicové žíly [10–12]. Velmi dobré výsledky byly také prokázány při léčbě proliferativní diabetické retinopatie [13]. V současné době jsou v České republice k intravitreálnímu podání schváleny tři přípravky – ranibizumab (Lucentis, Novartis, Basilej, Švýcarsko), brolucizumab (Beovu, Novartis, Basilej, Švýcarsko) a aflibercept (Eylea, Bayer, Leverkusen, Německo). V off-label použití je někdy podáván také bevacizumab (Avastin, Roche Pharma AG, Grenzach-Wyhlen, Německo), který ovšem dle Souhrnu údajů o přípravku (SPC) není určen k intravitreálnímu podání [14]. Provedené klinické studie prokázaly vysokou bezpečnost těchto preparátů [1,5,7,8,10,11]. Nebyla ovšem provedena žádná klinická studie studující bezpečnost intravitreálního podání antiVEGF preparátů u těhotných žen. Informací v této oblasti bylo zatím publikováno velmi málo. Dle SPC by tyto přípravky měly být u těhotných žen použity pouze v případě, že potenciální přínos převáží potenciální riziko pro plod. Cílem naší práce je prezentovat kazuistiku těhotné pacientky, u které byl podán intravitreálně anti - VEGF preparát ranibizumab pro přítomnou CNV při patologické myopii.
KAZUISTIKA
34letá pacientka byla odeslána na Oftalmologickou kliniku Fakultní nemocnice Královské Vinohrady v lednu 2020 pro myopickou CNV na pravém oku (OP). Subjektivně udávala asi 3 měsíce trvající pokles vidění na OP. V době vyšetření byla pacientka ve 34. týdnu těhotenství, gravidita probíhala do té doby fyziologicky. Jednalo se o druhou graviditu pacientky, v minulosti proběhl 1 porod přirozenou cestou. Celkově se pacientka s ničím neléčila, v oční anamnéze byla přítomna vysoká myopie na OP. Vstupní nejlepší korigovaná zraková ostrost (NKZO) na OP byla 68 písmen ETDRS optotypů, na levém oku (OL) 85 písmen ETDRS optotypů. Byla přítomna výrazná asymetrie v refrakci i axiální délce mezi OP a OL. Na OP byl sférický ekvivalent -11,5 dioptrií a axiální délka bulbu byla 27,7 mm, na OL byl sférický ekvivalent -6,5 dioptrií a axiální délka bulbu 25,8 mm. Nález na předním segmentu obou očí byl fyziologický. Na sítnici OP bylo přítomno pigmentované ložisko CNV s drobnou hemoragií (Obrázek 1). V periferii sítnice na OP byla u čísla 12 patrná lattice degenerace s drobnou atrofickou dírou sítnice. Na OL byl nález na sítnici fyziologický. Provedená optická koherentní tomografie (OCT) OP ukázala hyperreflektivní ložisko v oblasti makuly nad retinálním pigmentovým epitelem, centrální retinální tloušťka (CRT) byla 310 μm (Obrázek 2A). Provedená OCT angiografie prokázala přítomnost klasické CNV v makule OP. Nález jsme uzavřeli jako CNV při patologické myopii. Vzhledem k těhotenství pacientky a relativně malému nálezu jsme se rozhodli nález zatím pouze sledovat. Provedli jsme laserovou baráž kolem atrofické díry sítnice na OP a pacientku jsme pozvali na kontrolu za 14 dní.
Obr. 1. Fotografie sítnice pravého oka. Patrná pigmentovaná myopická choroidální neovaskulární membrána s drobnou hemoragií 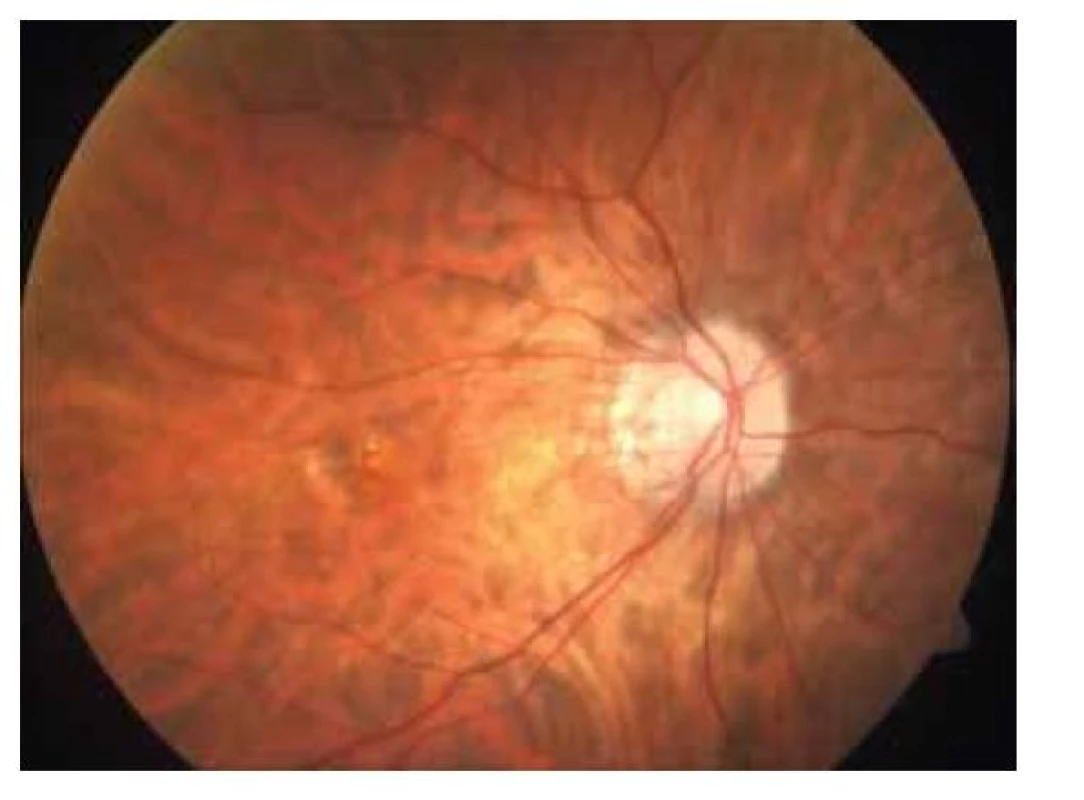
Obr. 2. Optická koherenční tomografie makuly pravého oka.
A) Vstupní nález, patrné hyperreflektivní ložisko v oblasti makuly nad retinálním pigmentovým epitelem, nejlepší korigovaná zraková ostrost (NKZO) 68 písmen ETDRS optotypů, centrální retinální tloušťka (CRT) 310 μm.
B) Nález po 14 dnech od vstupu, patrný nárůst ložiska a edému v makule, NKZO 68 písmen ETDRS optotypů, CRT 329 μm.
C) Nález 3 týdny po aplikaci ranibizumabu, NKZO 78 písmen ETDRS optotypů, CRT 276 μm.
D) Reaktivace myopické neovaskulární membrány, NKZO 72 písmen ETDRS optotypů, CRT 309 μm.
E) Stav po 2. aplikaci ranibizumabu, NKZO 79 písmen ETDRS optotypů, CRT 264 μm.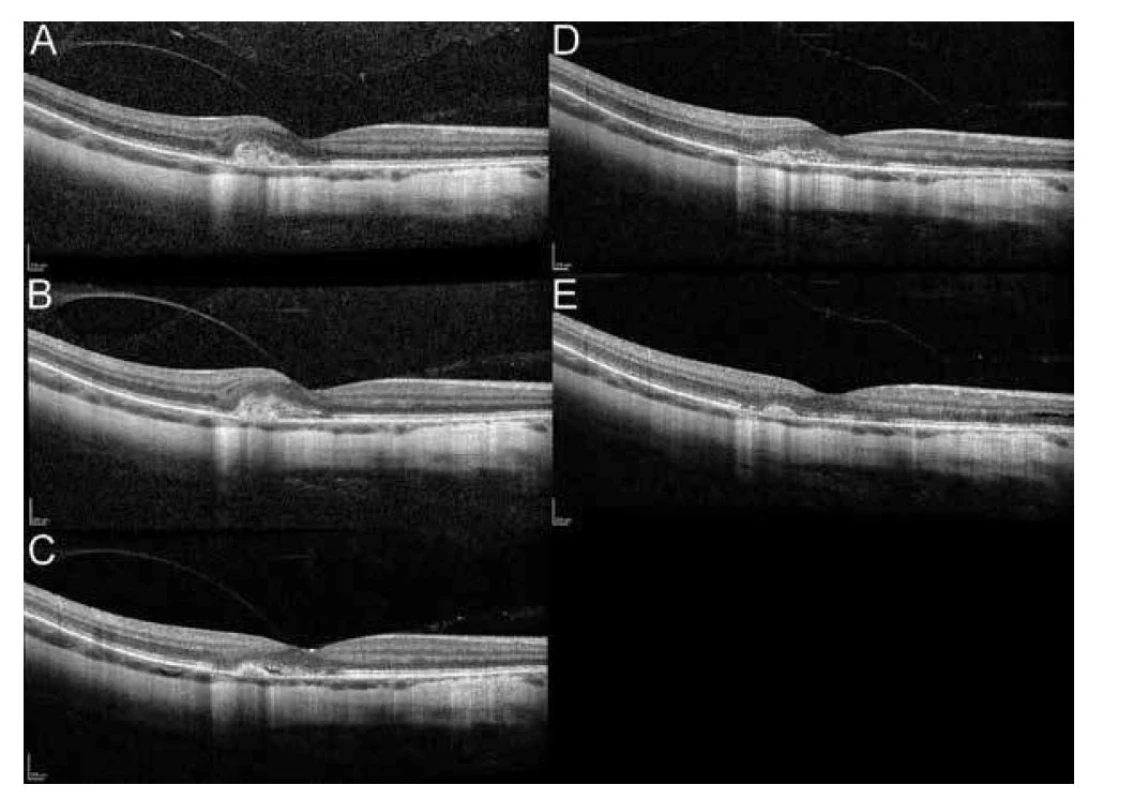
Na kontrole v únoru 2020 byla NKZO stabilní, došlo ovšem k mírnému nárůstu edému a hyperreflektivního ložiska v makule, CRT byla 329 μm (Obrázek 2B). Po domluvě s pacientkou a ošetřujícím gynekologem byla indikována aplikace ranibizumabu do OP. Vzhledem k přítomnosti aktivní CNV v makule bylo také doporučeno vedení porodu císařským řezem (SC) pro riziko krvácení v makule při porodu vedeném přirozenou cestou. Před aplikací byla pacientka poučena o všech rizicích spojených s intravitreální aplikací ranibizumabu pro ni samotnou i pro plod. Pacientka tato rizika akceptovala a podepsala informovaný souhlas s intravitreální aplikací ranibizumabu. Aplikace proběhla ve 36. gestačním týdnu ve standardním režimu naší kliniky bez komplikací.
Na kontrole 3 týdny po aplikaci a týden před plánovanou SC došlo na OP ke zlepšení NKZO na 78 písmen ETDRS optotypů, k poklesu CRT na 276 μm a ke vstřebání hemoragie v makule (Obrázek 2C). Další aplikace ranibizumabu nebyla indikována a pacienta byla pozvána na další kontrolu za 6 týdnů. V mezidobí pacientka porodila SC v týdnu 39+0 zdravou holčičku. Poporodní adaptace novorozence byla normální, Apgar skóre bylo 10-10 - 10. Na kontrole 9 týdnů po aplikaci ranibizumabu došlo k dalšímu zlepšení NKZO na 83 písmen ETDRS optotypů, CRT byla 277 μm. Pacientku jsme dále pravidelně sledovali. V říjnu 2020, 8 měsíců po první aplikaci ranibizumabu došlo k reaktivaci CNV v makule OP a k poklesu NKZO na 72 písmen ETDRS optotypů. Na OCT byl opět patrný edém v makule, CRT byla 309 μm (Obrázek 2D). Byla provedena další aplikace ranibizumabu do OP. U pacientky bylo poté zjištěno těhotenství. Dle výpočtu byla pacientka v den 2. aplikace ranibizumabu ve 3. týdnu těhotenství. Po 2. aplikaci došlo k opětovnému zlepšení NZKO na 79 písmen ETDRS optotypů, ke vstřebání edému na OCT a poklesu CRT na 264 μm (Obrázek 2E). Těhotenství bylo ukončeno interrupcí na přání pacientky. Pacientka je dále sledována na naší klinice.
DISKUZE
Myopická CNV se vyskytuje asi u 5–10 % pacientů s patologickou myopií. Obvykle se jedná o CNV typu 2 – klasickou – menšího rozsahu. Často bývají lokalizovány blízko foveoly a vedou k rychlému poklesu zrakové ostrosti a vzniku metamorfopsií. V diagnostice myopických CNV se uplatňuje OCT, fluorescenční angiografie a OCT angiografie [15,16]. V současné době jsou k léčbě myopické CNV používány s velmi dobrými výsledky antiVEGF preparáty [5–7].
Bylo publikováno několik kazuistických sdělení o podání ranibizumabu u těhotných pacientek [17–20]. U jedné z těchto pacientek došlo po intravitreálním podání ranibizumabu k potratu. Aplikace zde byla provedena v 5. týdnu těhotenství [17]. Bylo popsáno i několik případů potratu po intravitreálním podání bevacizumabu [21 – 23]. Ve všech případech šlo o pacientky v prvním trimestru těhotenství. V tomto období je ovšem zároveň nejvyšší riziko spontánního potratu i u zdravých pacientek [24]. Je tak velmi obtížné určit vliv intravitreálního podání anti - VEGF preparátů na riziko spontánního potratu. U jedné pacientky léčené intravitreálním bevacizumabem došlo k rozvoji preeklampsie a bylo nutno provést akutní SC pro tíseň plodu. Tato pacientka měla ovšem několik rizikových faktorů pro rozvoj preeklampsie. Mezi podáním bevacizumabu a rozvojem preeklampsie u této pacientky navíc uběhlo 26 týdnů [25].
Vaskulární endoteliální růstový faktor (VEGF) hraje významnou roli v růstu placenty a v časné embryogenezi i v pozdějším vývoji plodu [26,27]. Podílí se také na procesu implantace embrya a snížená exprese VEGF může mít vliv na výskyt spontánních potratů v časných fázích těhotenství [28]. Ve studiích se zvířaty nemělo intravitreální podání ranibizumabu vliv na výskyt vývojové toxicity ani teratogenity a nemělo vliv na hmotnost plodu nebo strukturu placenty [29]. Intravitreální podání bevacizumabu vedlo u krys k nižší hmotnosti plodu a placenty při podání v časných a středních fázích březosti [30]. Intravenózní podání bevacizumabu u králíků bylo spojeno s embryotoxicitou i teratogenitou a vedlo ke snížené hmotnosti plodu i gravidní matky [14]. U afliberceptu byla prokázána embryotoxicita při intravenózním i subkutánním podání, ovšem při systémové expozici vysoce přesahující hodnoty pozorované při intravitreálním podání u člověka [31]. U brolucizumabu nebyly dosud reprodukční studie na zvířatech provedeny [32].
U naší pacientky jsme doporučili porod cestou SC pro přítomnost aktivní neovaskulární membrány v makule OP s přítomnou hemoragií. Porod cestou SC bývá u vysoce myopických pacientek obvykle doporučován jako prevence vzniku trhlin a odchlípení sítnice, ačkoliv nikdy nebylo prokázáno, že by porod přirozenou cestou byl spojen s vyšším rizikem odchlípení sítnice [33, 34]. Byly ovšem popsány případy retinálního krvácení po Valsalvově manévru u rodících žen [35]. V literatuře jsme nenašli žádný případ retinálního krvácení vzniklého při porodu přirozenou cestou u pacientky s aktivní CNV.
ZÁVĚR
Intravitreální podání ranibizumabu ve 3. trimestru gravidity vedlo u pacientky s myopickou CNV ke zlepšení NKZO a poklesu edému v makule. Aplikace neměla negativní vliv na průběh těhotenství ani poporodní adaptaci plodu. Přesto je při podání antiVEGF preparátů u těhotných vždy nutno zvážit případná rizika podání ve vztahu k možnému přínosu. Nezbytné je pečlivé poučení pacientky.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmů a není podpořeno žádnou farmaceutickou firmou. Práce nebyla zadána jinému časopisu ani jinde otištěna, s výjimkou kongresových abstrakt a doporučených postupů.
Do redakce doručeno dne: 19. 4. 2021
Přijato k publikaci dne: 3. 12. 2021
MUDr. Martin Penčák
Oftalmologická klinika FNKV a 3. LF UK
Šrobárova 50
100 34 Praha 10
E-mail: pencak@volny.cz
Zdroje
1. Brown DM, Michels M, Kaiser PK, Heier JS, Sy JP, Ianchulev T. Ranibizumab versus verteporfin photodynamic therapy for neovascular age-related macular degeneration: Two-year results of the ANCHOR study. Ophthalmology. 2009;116(1):57-65.e5. doi:10.1016/j. ophtha.2008.10.018
2. Doležalová J, Karel I, Hallová H. Naše dvouleté zkušenosti s léčbou vlhké formy věkem podmíněné makulární degenerace bevacizumabem (Avastin) [Our Two-Years Experience with the Bevacizumab (Avastin) Treatment of the Age Related Macular Degeneration Wet Form]. Cesk Slov Oftalmol. 2010;66(1):10-14. Czech.
3. Klimešová YM, Penčák M, Straňák Z, Lalinská L, Veith M. One-Year Follow-up Outcomes of Treatment of Wet Age-Related Macular Degeneration with Aflibercept. Cesk Slov Oftalmol. 2018;74(2):47 - 52. doi:10.31348/2018/1/1-2-2018
4. Stepanov A, Nemcansky J, Veith M, et al. Two-year results of a combined regimen of aflibercept treatment in three types of choroidal neovascular membrane in the wet form of age-related macular degeneration: Real-life evidence in the Czech Republic. Eur J Ophthalmol. 2020. doi:10.1177/1120672120971190
5. Ikuno Y, Ohno-Matsui K, Wong TY, et al. Intravitreal Aflibercept Injection in Patients with Myopic Choroidal Neovascularization: The MYRROR Study. Ophthalmology. 2015;122(6):1220-1227. doi:10.1016/j.ophtha.2015.01.025
6. Stepanov A, Pencak M, Nemcansky J, et al. Results of Ranibizumab Treatment of the Myopic Choroidal Neovascular Membrane according to the Axial Length of the Eye. J Ophthalmol. 2020. doi:10.1155/2020/3076596
7. Wolf S, Balciuniene VJ, Laganovska G, et al. RADIANCE: A Randomized Controlled Study of Ranibizumab in Patients with Choroidal Neovascularization Secondary to Pathologic Myopia. Ophthalmology. 2014;121(3):682-692.e2. doi:10.1016/j.ophtha.2013.10.023
8. Lai TYY, Staurenghi G, Lanzetta P, et al. Efficacy and safety of ranibizumab for the treatment of choroidal neovascularization due to uncommon cause: twelve-month results of the MINERVA study. Retina. 2018;38(8):1464-1477. doi:10.1097/IAE.0000000000001744
9. Stepanov A, Středová M, Dusová J, Jirásková N, Studnička J. Ranibizumab for the treatment of choroidal neovascularization due to cause other than age related macular degeneration. Cesk Slov Oftalmol. 2019;75(3):138-144. doi:10.31348/2019/3/4
10. Brown DM, Heier JS, Clark WL, et al. Intravitreal Aflibercept Injection for Macular Edema Secondary to Central Retinal Vein Occlusion: 1-Year Results From the Phase 3 COPERNICUS Study. Am J Ophthalmol. 2013;155(3):429-437.e7. doi:10.1016/j.ajo.2012.09.026
11. Korobelnik J-F, Holz FG, Roider J, et al. Intravitreal Aflibercept Injection for Macular Edema Resulting from Central Retinal Vein Occlusion: One-Year Results of the Phase 3 GALILEO Study. Ophthalmology. 2014;121(1):202-208. doi:10.1016/j.ophtha.2013.08.012
12. Lalinská L, Krásný J, Studený P, Veith M. Results of the first 12 months treatment of macular edema complicating BRVO in patients treated with ranibizumab. Cesk Slov Oftalmol. 2018;74(2):62 - 67. doi: 10.31348/2018/1/3-2-2018
13. Writing Committee for the Diabetic Retinopathy Clinical Research Network. Panretinal Photocoagulation vs Intravitreous Ranibizumab for Proliferative Diabetic Retinopathy: A Randomized Clinical Trial. JAMA. 2015;314(20):2137-2146. doi: 10.1001/jama.2015.15217
14. Státní ústav pro kontrolu léčiv. Avastin - Souhrn údajů o přípravku. 2005. Available from: https://www.sukl.cz/modules/medication/ detail.php?code=0028397&tab=texts
15. Neelam K, Cheung CMG, Ohno-Matsui K, Lai TYY, Wong TY. Choroidal neovascularization in pathological myopia. Prog Retin Eye Res. 2012;31(5):495-525. doi: 10.1016/j.preteyeres.2012.04.001
16. Miyata M, Ooto S, Hata M, et al. Detection of Myopic Choroidal Neovascularization Using Optical Coherence Tomography Angiography. Am J Ophthalmol. 2016;165 : 108-114. doi: 10.1016/j. ajo.2016.03.009
17. Akkaya S. Early Miscarriage Occurring Six Days After Intravitreal Ranibizumab Injection. Med Hypothesis Discov Innov Ophthalmol. 2019;8(2):69-72.
18. Fossum P, Couret C, Briend B, Weber M, Lagarce L. Safety of intravitreal injection of ranibizumab in early pregnancy: a series of three cases. Eye (Lond). 2018;32(4):830-832. doi: 10.1038/eye.2017.305
19. Jouve L, Akesbi J, Nordmann JP. Safety and efficacy of ranibizumab for pregnant women in idiopathic choroidal neovascularization. Acta Ophthalmol. 2015;93(7):e597-e598. doi: 10.1111/ aos.12611
20. Sarhianaki A, Katsimpris A, Petropoulos IK, Livieratou A, Theoulakis PE, Katsimpris JM. Intravitreal administration of ranibizumab for idiopathic choroidal neovascularization in a pregnant woman. Klin Monbl Augenheilkd. 2012;229(4):451-453. doi: 10.1055/s-0031 - 1299207
21. Gómez Ledesma I, de Santiago Rodriguez MÁ, Follana Neira I, León Garrigosa F. Neovascular membrane and pregnancy. Treatment with bevacizumab. Arch Soc Esp Oftalmol (English Edition). 2012;87(9):297-300. doi: 10.1016/j.oftal.2011.09.011
22. Kianersi F, Ghanbari H, Naderi Beni Z, Naderi Beni A. Intravitreal vascular endothelial growth factor (VEGF) inhibitor injection in unrecognised early pregnancy. Invest New Drugs. 2016;34(5):650 - 653. doi: 10.1007/s10637-016-0361-8
23. Petrou P, Georgalas I, Giavaras G, Anastasiou E, Ntana Z, Petrou C. Early loss of pregnancy after intravitreal bevacizumab injection. Acta Ophthalmol. 2010;88(4):e136-e136. doi: 10.1111/j.1755 - 3768.2009.01572.x
24. Ammon Avalos L, Galindo C, Li DK. A systematic review to calculate background miscarriage rates using life table analysis. Birth Defects Res A Clin Mol Teratol. 2012;94(6):417-423. doi: 10.1002/ bdra.23014
25. Sullivan L, Kelly SP, Glenn A, Williams CPR, McKibbin M. Intravitreal bevacizumab injection in unrecognised early pregnancy. Eye (Lond). 2014;28(4):492-494. doi: 10.1038/eye.2013.311
26. Hård A-L, Hellström A. On safety, pharmacokinetics and dosage of bevacizumab in ROP treatment – a review. Acta Paediatr. 2011;100(12):1523-1527. doi: 10.1111/j.1651-2227.2011.02445.x
27. Cheung C. Vascular endothelial growth factor: possible role in fetal development and placental function. J Soc Gynecol Investig. 1997;4(4):169-177.
28. Vuorela P, Carpén O, Tulppala M, Halmesmäki E. VEGF, its receptors and the Tie receptors in recurrent miscarriage. Mol Hum Reprod. 2000;6(3):276-282. doi: 10.1093/molehr/6.3.276
29. Státní ústav pro kontrolu léčiv. Lucentis – souhrn údajů o přípravku. 2018. Available from: https://www.sukl.cz/modules/medication/ detail.php?code=0194569&tab=texts.
30. Bamdad S, Bamdad M, Khanlari M, Daneshbod Y, Khademi B. Teratogenic Effects of Intravitreal Injection of Bevacizumab in a Pregnant Rat Model. Iran J Pharm Res. 2017;16(2):670-676.
31. Státní ústav pro kontrolu léčiv. Eylea – souhrn údajů o přípravku. 2020. Available from: https://www.sukl.cz/modules/medication/ detail.php?code=0193696&tab=texts
32. Státní ústav pro kontrolu léčiv. Beovu – souhrn údajů o přípravku. 2021. Available from: https://www.sukl.cz/modules/medication/ detail.php?code=0238813&tab=texts.
33. Landau D, Seelenfreund MH, Tadmor O, Silverstone BZ, Diamant Y. The effect of normal childbirth on eyes with abnormalities predisposing to rhegmatogenous retinal detachment. Graefes Arch Clin Exp Ophthalmol. 1995;233(9):598-600. doi: 10.1007/BF00404712
34. Neri A, Grausbord R, Kremer I, Ovadia J, Treister G. The management of labor in high myopic patients. Eur J Obstet Gynecol Reprod Biol. 1985;19(5):277-279. doi: 10.1016/0028-2243(85)90041-3
35. Eneh A, Almeida D. Valsalva hemorrhagic retinopathy during labour: a case report and literature review. Can J Ophthalmol. 2013;48(6):e145-e147. doi: 10.1016/j.jcjo.2013.05.019
Štítky
Oftalmologie
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
2022 Číslo 2- Stillova choroba: vzácné a závažné systémové onemocnění
- Familiární středomořská horečka
- Diagnostický algoritmus při podezření na syndrom periodické horečky
- Možnosti využití přípravku Desodrop v terapii a prevenci oftalmologických onemocnění
- Selektivní laserová trabekuloplastika nesnižuje nitroční tlak více než argonová laserová trabekuloplastika
-
Všechny články tohoto čísla
- MIKROBIOM A UVEITIDY. PŘEHLED
- INCIDENCE PSEUDOEXFOLIAČNÍHO SYNDROMU A GLAUKOMU V SOUBORU VÍCE NEŽ 14 000 OČÍ PACIENTŮ OPEROVANÝCH PRO KATARAKTU
- VLIV VSTUPNÍ CENTRÁLNÍ RETINÁLNÍ TLOUŠŤKY NA VÝSLEDEK LÉČBY DIABETICKÉHO MAKULÁRNÍHO EDÉMU AFLIBERCEPTEM – ZKUŠENOSTI Z BĚŽNÉ KLINICKÉ PRAXE V ČESKÉ REPUBLICE
- SOUČASNÉ POSTUPY V OPERACI KATARAKTY – SUBJEKTIVNÍ PREFERENCE ČESKÝCH KATARAKTOVÝCH CHIRURGŮ
- INTRAVITREÁLNÍ APLIKACE RANIBIZUMABU U TĚHOTNÉ PACIENTKY S MYOPICKOU CHOROIDÁLNÍ NEOVASKULÁRNÍ MEMBRÁNOU. KAZUISTIKA
- IDIOPATICKÉ SKLÉROCHOROIDÁLNE KALCIFIKÁCIE. KAZUISTIKA
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- INCIDENCE PSEUDOEXFOLIAČNÍHO SYNDROMU A GLAUKOMU V SOUBORU VÍCE NEŽ 14 000 OČÍ PACIENTŮ OPEROVANÝCH PRO KATARAKTU
- SOUČASNÉ POSTUPY V OPERACI KATARAKTY – SUBJEKTIVNÍ PREFERENCE ČESKÝCH KATARAKTOVÝCH CHIRURGŮ
- IDIOPATICKÉ SKLÉROCHOROIDÁLNE KALCIFIKÁCIE. KAZUISTIKA
- MIKROBIOM A UVEITIDY. PŘEHLED
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




