-
Články
- Vzdělávání
- Časopisy
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Volná místa
Doporučené pozice
Reklama- Praxe
Kazuistika pacientky s metastazujícím maligním melanomem s pozitivní mutací V600E léčené kombinací vemurafenibu a kobimetinibu
1. 4. 2019
doc. MUDr. Monika Arenbergerová, Ph.D., MUDr. Alena Fialová, MUDr. Marek Pásek, prof. MUDr. Petr Arenberger, DrSc., MBA
Dermatovenerologická klinika 3. LF UK a FNKV, PrahaMutace BRAF u maligního melanomu
Jednou z klíčových signálních drah u melanomu je MAPK s proteiny RAS, RAF, MEK a ERK. BRAF je jednou ze serin/threoninových kináz v signální cestě MAPK. Mutace BRAF je nejčastější mutací u lidských nádorů (1) a vyskytuje se v 50–60 % případů melanomu (2). Statisticky signifikantní počet mutací BRAF byl objeven u melanomů na intermitentně UV exponované kůži na trupu, u melanomů povrchově se šířících nebo nodulárních u mladších jedinců (3). Doposud bylo identifikováno více než 50 různých typů mutací genu BRAF. 90 % z nich je způsobeno záměnou glutamátu za valin na pozici 600 (mutace V600E) a má za následek 138násobné zvýšení aktivity kinázy BRAF oproti nemutované molekule. Tato mutace vede ke konstitutivní aktivaci signální cesty MAPK a následnému nekontrolovanému buněčnému růstu. Ovlivnění mutace BRAF má obrovský význam v boji proti metastazujícímu malignímu melanomu (MM).
InzerceVemurafenib a kobimetinib v léčbě BRAF-mutovaného MM
Vemurafenib (Zelboraf) je inhibitor mutace BRAF s vysokou vazbou k variantě BRAFV600E. Kobimetinib (Cotellic) pak inhibuje MEK, což je další protein v signální dráze MAPK.
Kombinace vemurafenibu a kobimetinibu byla ověřována v registrační studii fáze III – coBRIM (4). Do této multicentrické randomizované studie bylo zařazeno celkem 495 dosud neléčených pacientů s pokročilým BRAF-mutovaným melanomem, kteří byli randomizováni do ramene s kombinovanou léčbou vemurafenibem 960 mg 2× denně a kobimetinibem 60 mg 1x denně nebo do ramene s monoterapií vemurafenibem 960 mg 2× denně.
Primárním cílem byla doba do progrese onemocnění (PFS). Sekundárními cíli byly celkové přežití, četnost objektivních odpovědí, trvání odpovědi a bezpečnost. Při mediánu sledování 14,2 měsíce bylo v rameni s kombinovanou léčbou dosaženo mediánu PFS 12,3 měsíce oproti 7,2 měsíce v rameni s monoterapií (poměr rizik [HR] 0,58; p < 0,0001).
Při následné analýze bylo dosaženo mediánu celkového přežití (OS) 22,3 měsíce pro kombinaci vs. 17,4 měsíce pro monoterapii (HR 0,70; 95% interval spolehlivosti [CI] 0,55–0,90; p = 0,005). Celkem 70 % pacientů dosáhlo objektivní odpovědi – celkové (CR) nebo částečné (PR) – oproti 50 % v kontrolním rameni a klinického benefitu (CBR) bylo docíleno u 88 % pacientů oproti 77 % v kontrolním rameni.
Nejčastějšími nežádoucími příhodami zaznamenanými při kombinované léčbě u více než 20 % pacientů byly: vyrážka (73 %), diarea (61 %), nauzea (43 %), bolesti kloubů (38 %), únava (37 %), fotosenzitivní reakce (34 %), horečka (29 %), zvýšení ALT / AST / GMT (26 % / 24 % / 22 %), závažná retinopatie (27 %) a zvýšení hodnot kreatinfosfokinázy (35 %).
Popis případu
51letá pacientka byla u nás v dispenzární péči od roku 2016 pro excidovaný maligní melanom na pravé straně krku. Histologicky se jednalo o povrchově se šířící maligní formu, Breslow 2,4 mm, bez ulcerace. Biopsie sentinelové uzliny (SLN) byla provedena zároveň s reexcizí tumoru a histologie v SLN neodhalila metastázu melanomu. Pacientka byla ve stadiu IIA (T3aN0M0). Z osobní anamnézy byla významná dlouhodobá léčba pro hypotyreózu. Otec zemřel na karcinom žlučových cest. Pacientka byla fototypu II s větším množstvím pigmentových névů. Několik z nich bylo excidováno a histologicky uzavřeno jako dysplastický pigmentový névus.
Vzhledem k dlouhodobému pracovnímu pobytu pacientky v zahraničí jsme se o dispenzární prohlídky dělili s dermatoonkologickou ambulancí v Singapuru. Při screeningovém CT vyšetření v lednu 2017 byla zjištěna metastáza v pravé plíci a mnohočetné objemné metastázy jater. Pacientka přitom byla asymptomatická.
V laboratorním odběru byla nalezena následující patologie: ALT 0,87 (˂ 0,73 µkat/l), AST 0,94 (˂ 0,67 µkat/l), CRP 7,1 (˂ 5,0 mg/l) a LDH 5,6 (˂ 4,10 µkat/l). Byla vyšetřena mutace BRAF z primárního tumoru akreditovanou metodou kitem BRAF 600/601 Strip Assay (Vienna Lab Diagnostics GmbH). Ta prokázala mutaci V600E. Pacientka byla zároveň vyšetřena na množství volné nádorové ctDNA (kit Idylla™ ctBRAF Mutation Test, Biocartis), které bylo stanoveno na 1,5 %.
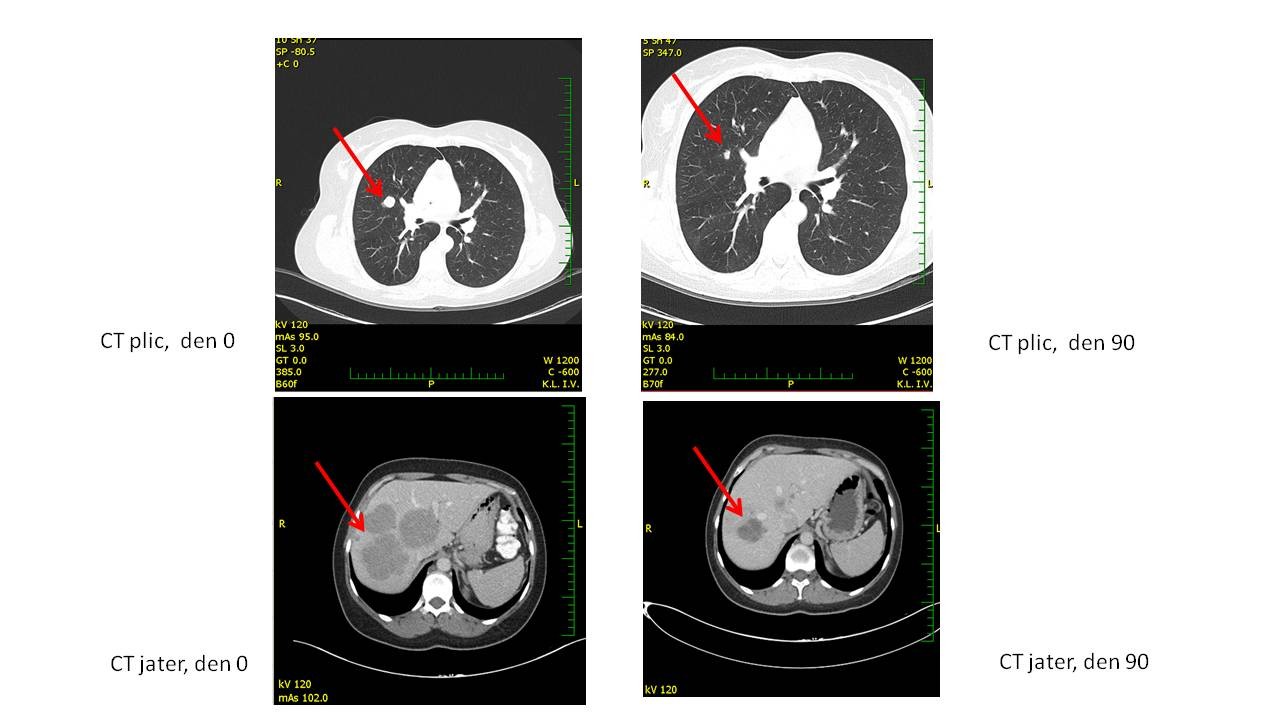
Vzhledem ke generalizovanému metastatickému rozsevu jsme pacientku indikovali k terapii vemurafenibem 960 mg (4 tbl. à 240 mg) 2× denně v kombinaci s kobimetinibem 60 mg (3 tbl. à 20 mg) 1× denně 1.–21. den. Pacientka léčbu tolerovala dobře a po 3 měsících kombinované léčby jsme provedli CT přešetření. Na plicích i v játrech byla pozorována významná regrese metastáz (obr. 1). V laboratorním obrazu došlo k mírné elevaci transamináz – ALT 0,94 (˂ 0,73 µkat/l), AST 1,05 (˂ 0,67 µkat/l) – a výraznému poklesu C-reaktivního proteinu (CRP) na 2,8 (˂ 5,0 mg/l) a LDH na 3,6 (˂ 4,10 µkat/l). Množství volné cirkulující DNA bylo stanoveno na 0,12 %.
Obr. 1
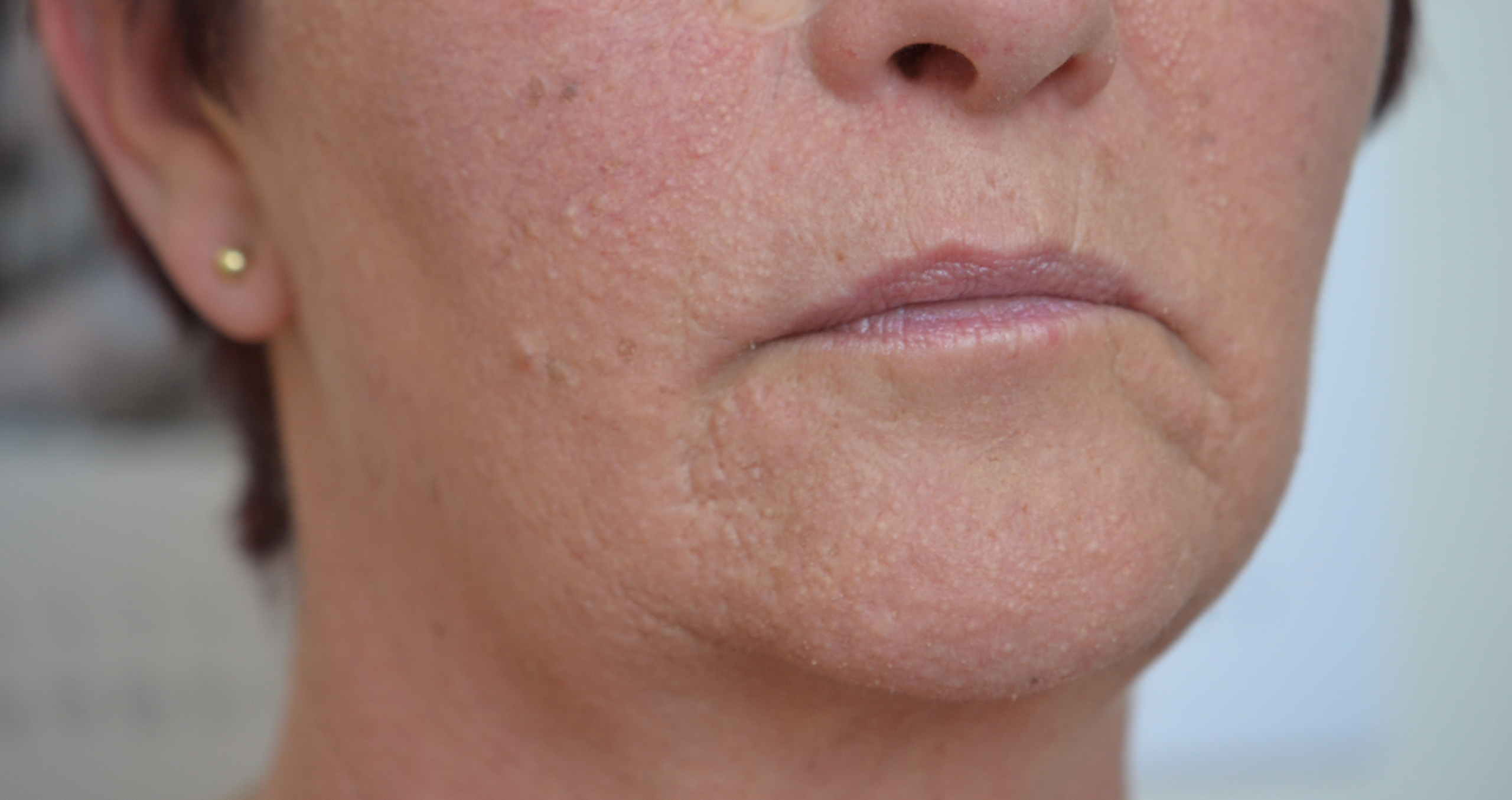
U pacientky se po 1. měsíci terapie objevilo nodulocystické akné v dolní partii obličeje s drobným difuzním rozsevem cyst o velikosti špendlíkové hlavičky (obr. 2). Výsev dobře zareagoval na lokální terapii adapalenem. Jedná se o třetí generaci retinoidů v 0,1% koncentraci s protizánětlivými účinky upravující rohovění kůže.
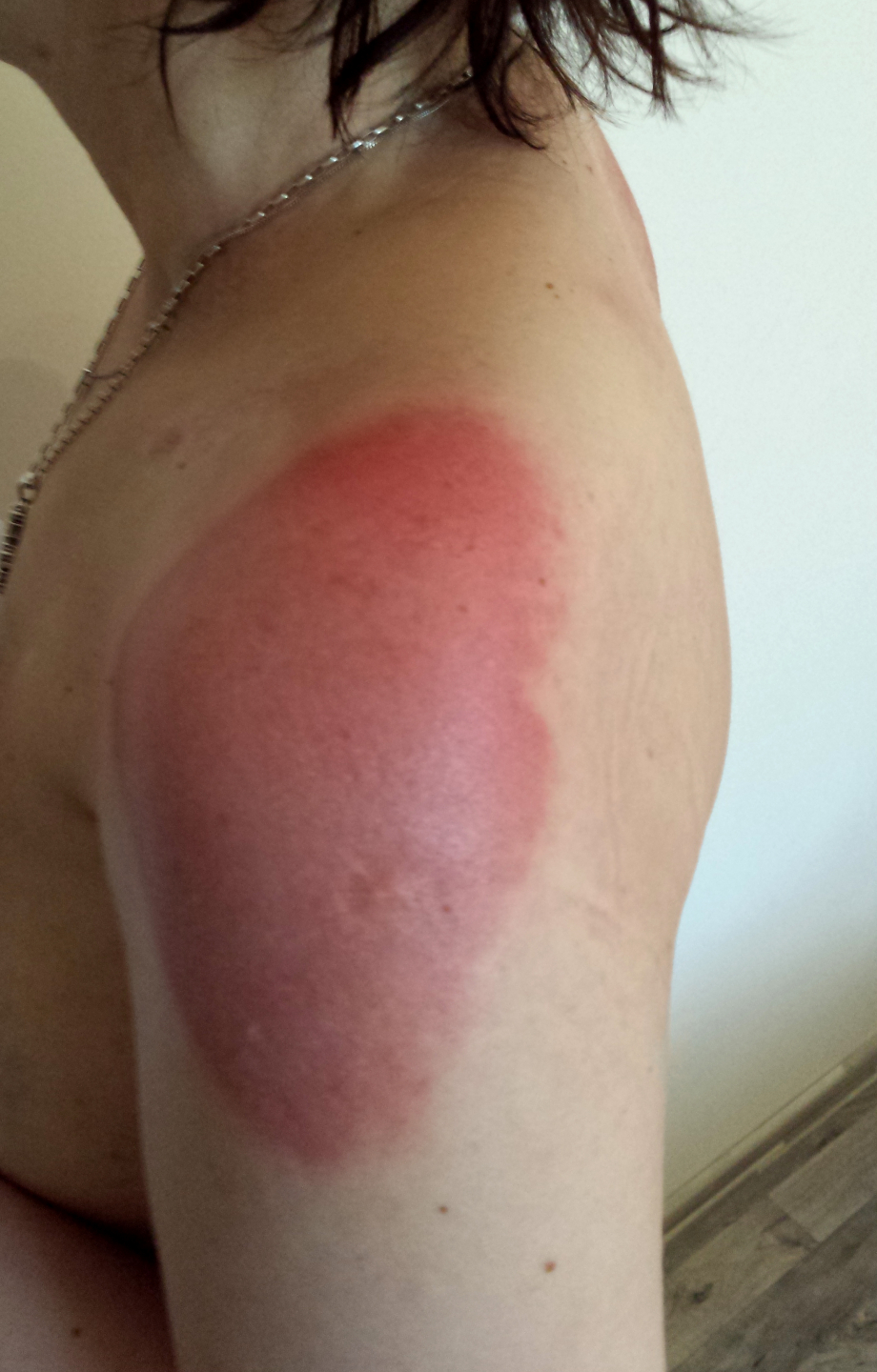
Pacientka byla poučena o nutnosti fotoprotekce. Důsledně se před UV zářením chránila textilem a fotoprotektivními prostředky s SPF 50+. I přes tato opatření došlo ve 4. měsíci k solární dermatitidě na místech odkrytých slunci (tričkové průramky) (obr. 3). Na tato místa byl aplikován lokální kortikosteroid s dobrým efektem.
Obr. 2
Obr. 3
Další restagingová CT vyšetření neodhalila relaps onemocnění a nejlepší léčebnou odpovědí byla významná parciální regrese. Laboratorní vyšetření v průběhu léčby pacientky byla bez významných odchylek. Ve 13. měsíci léčby se objevila progrese choroby ve formě nové metastázy v mediastinu a systémová léčba byla ukončena. Další systémovou protinádorovou léčbu pacientka neabsolvovala. Zemřela v 19. měsíci sledování na progresi onemocnění.
Diskuse
Léčba této pacientky vemurafenibem a kobimetinibem potvrdila výsledky publikovaných studií. Nemocná tolerovala systémovou léčbu po celou dobu tak dobře, že jí umožňovala naplno se věnovat svému náročnému zaměstnání. Z nežádoucích účinků terapie se objevily pouze kožní, které jsme pomocí včas nasazené léčby dostali pod kontrolu. Celkové přežití pacientky bylo kratší než medián OS v klinické studii coBRIM, což může souviset se vstupní velkou nádorovou masou a elevací LDH. I hladina cirkulující volné nádorové DNA byla v průběhu léčby snížená, ale detekovatelná, což je prognosticky horší negativní faktor.
Závěr
Metastazující maligní melanom má špatnou prognózu, nicméně zavedení terapie vemurafenibem vedlo k průlomu v jeho léčbě. Užívání kombinace vemurafenibu a kobimetinibu vede k prodloužení celkové doby přežití a značnému zlepšení kvality života pacientů vzhledem k rapidnímu nástupu účinku a přijatelné toxicitě.
Zdroje:
- Davies H., Bignell G. R., Cox C. et al. Mutations of the BRAF gene in human cancer. Nature 2002; 417 (6892): 949–954.
- Curtin J. A., Busam K., Pinkel D. et al. Somatic activation of KIT in distinct subtypes of melanoma. J Clin Oncol 2006; 24 (26): 4340–4346.
- Maldonado J. L., Fridlyand J., Patel H. et al. Determinants of BRAF mutations in primary melanomas. J Natl Cancer Indy 2003; 95 (24): 1878–1890.
- Ascierto P., McArthur G., Dréno B. et al. Cobimetinib combined with vemurafenib in advanced BRAFV600-mutant melanoma (coBRIM): updated efficacy results from a randomised, double-blind, phase 3 trial. Lancet Oncol 2016; 17 : 1248–1260, doi: 10.1016/S1470-2045(16)30122-X.
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Štítky
Dermatologie Dětská dermatologie Onkologie
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



