-
Medical journals
- Career
Warfarínom indukovaná kožná nekróza: kazuistika a prehľad literatúry
Authors: A. Kreze Jr; J. Koskuba; A. Zadražilová; V. Vomáčka; M. Kosák; A. Zápotocká
Authors‘ workplace: II. interní oddělení FN Bulovka, Praha
Published in: Transfuze Hematol. dnes,15, 2009, No. 3, p. 169-171.
Category: Comprehensive Reports, Original Papers, Case Reports
Overview
Warfarínom indukovaná kožná nekróza je vzácna komplikácia postihujúca kožu a mäkké tkanivá počas perorálnej liečby antikoagulanciami. Práca popisuje klinický priebeh u pacientky, u ktorej sa vyvinula warfarínom indukovaná kožná nekróza a podáva prehľad klinickej manifestácie, diagnózy, liečby a prevencie tejto komplikácie. Podľa našich literárnych zdrojov a vedomostí ide o prvý prípad warfarínom indukovanej kožnej nekrózy popísaný v Českej republike.
Kľúčové slová:
warfarin, nežiadúce účinky, kožná nekrózaÚvod
Perorálna antikoagulačná liečba warfarinom sa extenzívne používa v profylaxii a liečbe tromboembolických stavov. Warfarínom indukovaná kožná nekróza (WISN) je vzácna komplikácia antikoagulačnej liečby u pacientov dostávajúcich warfarin. Spravidla vzniká 3–6 dní od začiatku liečby. Kožná lézia začína parestéziami s erytematóznym začervenaním, progreduje do petéchií a hemoragických búl a môže končiť nekrózou. Spôsobená je hyperkoagulačným stavom, ktorý je navodený deficitom vitamin K-dependentých antikoagulačných faktorov: proteín C a proteín S. Diferenciálna diagnóza WISN zahŕňa purpura fulminans, nekrotizujúcu fascitídu, diseminovanú koagulopatiu, celulitídu a Fournierovu gangrénu. Prezentujeme pacientku, u ktorej sa vyvinula WISN, jej klinické manifestácie, diagnózu a liečbu.
Popis prípadu
72-ročná žena s anamnézou lymfoproliferatívneho ochorenia nízkej malignity z malých B lymfocytov typu SCL/CLL, po liečbe chlorambucilom bez významného efektu, s následnou zmenou terapie na fludarabín (aplikované 2 cykly), bola prijatá na naše oddelenie s diagnózou trombózy povrchovej stehennej žily a predkolenných žíl pravej dolnej končatiny overenou duplexnou sonografiou. Anamnesticky prekonala cholecystektómiu pre cholecystolitiázu a bola polyvalentne alergická. Aktuálne užívala flukonazol 100 mg denne a cotrimoxazol 480 mg trikrát denne (po doporučení hematológom), metoclopramid 3 x 1 tbl denne, alopurinol 100 mg denne, Tanakan 1 tbl ráno a Bellaspon 1 tbl večer. Nezaznamenali sme prítomnosť žiadneho rizika pre vznik WISN (telesná hmotnosť 59 kg, menopauza nastala pred desiatkami rokov).
Bola započatá terapia žilnej trombózy heparínom úvodným bolusom 10 000 U iv s následným pokračovaním dávkou 25 000 U/24 h. Súčasne bol od prvého dňa podaný warfarín v dávke 5 mg denne. Monitorovaním koagulačných parametrov boli získané výsledky uvedené v tabulke 1.
Table 1. Monitorovanie koagulačných. 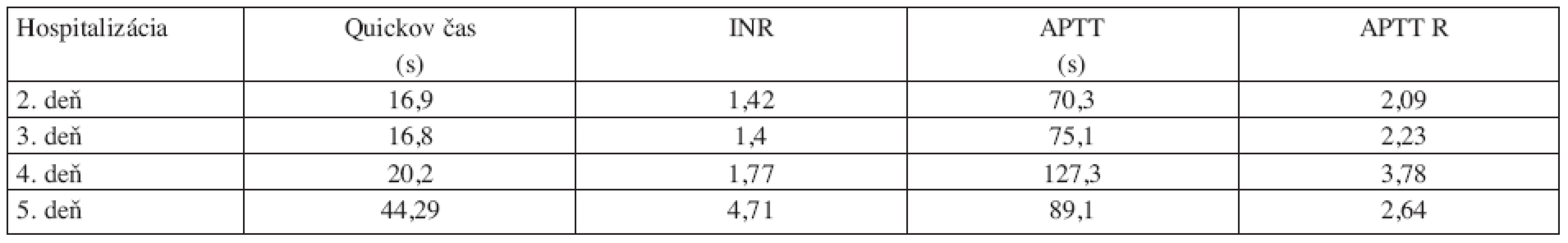
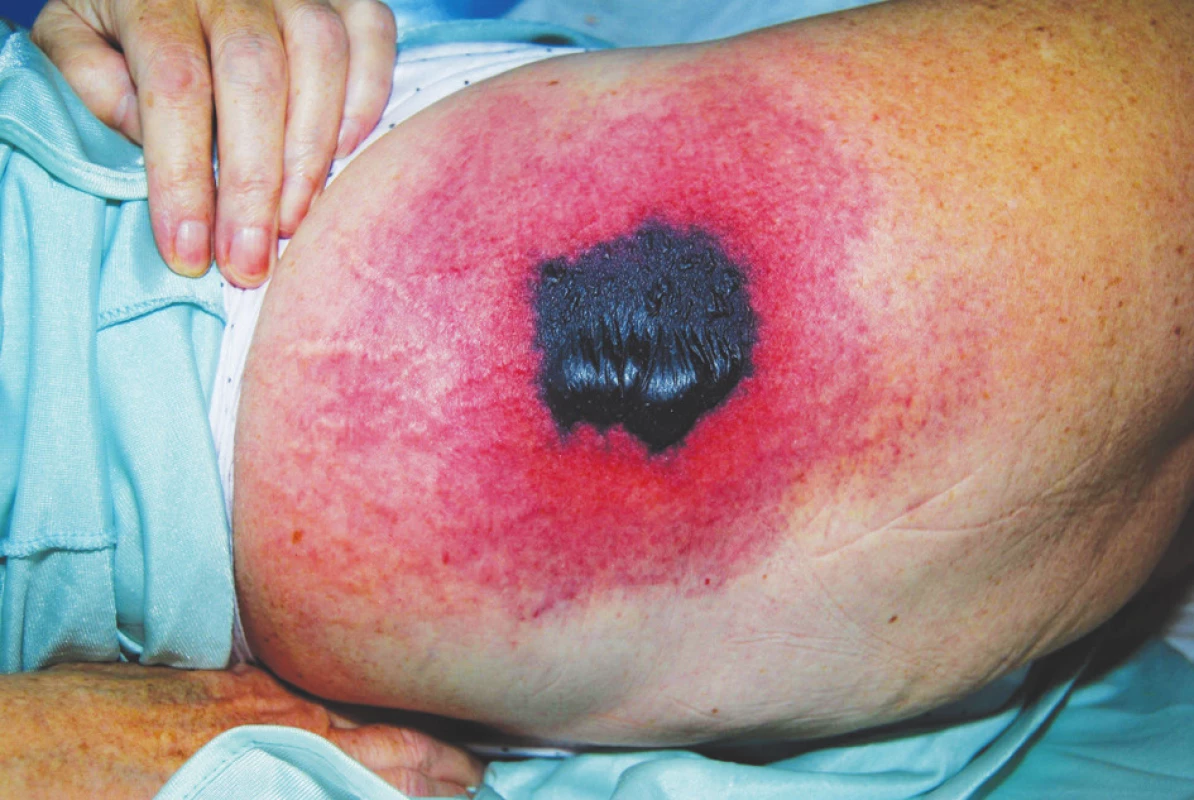
Na piaty deň liečby bol INR 4,71, preto bol heparín vynechaný z terapie a pacientka bola prepustená a doporučená k ambulantnému sledovaniu na dávke 3 mg warfarínu denne. Následný deň sme pacientku hospitalizovali pre bolestivú nekrózu s erytematóznymi hranicami nad pravým bedrovým kĺbom a stehennou oblasťou veľkosti 8 x 8 cm (obr. 1). Nekróza vznikla šiesty deň podávania warfarínu, warfarín sme vynechali z terapie a bola započatá liečba enoxaparínom v dávke 0,6 ml každých 12 hodín podľa telesnej hmotnosti. Nekrotické masy boli chirurgicky odstránené, histológia potvrdila očakávaný nález nekrotického tkaniva s reaktívnou celulizáciou, kultivačný nález bol negatívny. Sekundárnym debridementom boli na 19. deň totálne odstránené nekrotické masy a rana sa hojila dobre a bez komplikácií. Počas liečby nekrózy sme aplikovali spolu dve jednotky plazmy a po chirurgickej intervencii spolu 4 transfúzne jednotky erytrocytov. V lokálnej terapii povidon iodidom a hydrogel alginátom sa následne pokračovalo na chirurgickej ambulancii.Liečba enoxaparínom pokračovala za sledovania v hematologickej ambulancii po dobu 3 mesiacov.
Genetické vyšetrenie
faktor V Leiden: mutácia v heterozygotnej konštitúcii (20210 G > A)
Methylentetrahydrofolát reduktáza:
MTHRF C/T mutácia v heterozygótnej konštitúcii (677 C > T)
MHTRF A/C mutácia v heterozygótnej konštitúcii (1298 A > C)
Faktor II: nedokázaná mutácia
Laboratórne vyšetrenia
kardiolipín IgG 2,28 U/ml (N 0–10 U/ml), IgM 0,91 U/ml (N 0–7 U/ml), antitrombín III 85% (N 81–123 %), Protein C 33 % (N 70–135), Protein S 40 % (N 63–135) homocystein 16,28 μmol/l (N 4,7–10,8).
Vyšetreniami sme vylúčili lupus antikoagulans a deficit antitrombínu III. Zníženie hladín proteínov C a S prikladáme liečbe warfarínom a potvrdili sme spolu 3 heterozygótne mutácie antiprokoagulačných faktorov. Vyššie koncentrácie homocysteinu pričítame mutácii MHTRF, ktorej účasť na protrombogénnom stave je sporná (1, 2, 3). Na kontrolné vyšetrenie hladín proteínov C a S sa pacientka nedostavila, takže definitívne zhodnotenie účasti prípadného deficitu týchto proteínov na stave nebolo možné.
Diskusia
Warfarínom idukovaná kožná nekróza (WISN) bola prvýkrát popísaná Floodom a spoluautormi v roku 1943 (4). Je to vzácna, ale závažná komplikácia antikoagulačnej liečby warfarínom. Celkový počet prípadov sa podľa literárnych prehľadov odhaduje na 300 kazuistík (5). Podobne podľa literatúry sa kožná nekróza po liečbe warfarínom vyskytuje v 0,01 až 0,1 % prípadov (6, 7, 8). WISN postihuje častejšie ženy s pomerom ženy : muži 9 : 1.
Klinický obraz: Výskyt komplikácie sa popisuje najčastejšie u stredne starších obéznych žien dostávajúcich warfarín pre pľúcnu embóliu, hlbokú žilnú trombózu, trombózu myokardiálych a cerebrálnych ciev a pre stavy po operácii kardiálnych chlopní. Väčšina prípadov vzniká medzi 3. až 6. dňom liečby warfarínom. Neskorší začiatok WISN sa môže vyskytnúť od 16. až 56. dňa liečby (9, 10). U žien sú najčastejšie postihnuté miesta: prsníky, gluteálna a stehenná oblasť, brucho, a u mužov penis. Môžu byť postihnuté aj ramená, ruky, prsty, nohy, tvár, nos, očné viečka a kalva (11, 12). Mnohopočetné lézie sa popisujú v 35 % prípadoch a v 20 % prípadoch sú lézie symetrické (13). Bola popísaná aj recidíva kožnej nekrózy v neprítomnosti (resp. po vynechaní) liečby warfarínom (14) a oneskorená diagnóza s dvojnásobným opakovaním stavu v krátkom čase (15).
Pacientove prvotné symptómy sú parestézie, pocit tlaku a chladu s vznikom erytematózneho exantému, následne vznikajú lokálne bolesti, petéchie a subkutánny edém, ktorý môže vytvárať vzhľad „peau dęorange“. Do 24 hodín od prvých príznakov vznikajú v mieste postihnutia kožné hemoragické buly. Definitívnym štádiom je kožný defekt charakteru escharovej nekrózy. Spektrum tkanivového poškodenia siaha od ohraničenej superficiálnej straty tkaniva schopného sa spontánne vygranulovať a vyliečiť, až k rane vyžadujúcej chirurgické ošetrenie a odstránenie nekrotických más s plastickou náhradou tkaniva, v extrémnych prípadoch nekrotického tkaniva je nutná amputácia časti končatín. Histologický nález predstavuje extenzívnu trombózu s mikrovaskulárnym poškodením a fibrínovými depozitami v postkapilárnom venóznom riečišti. V pokožke a subkutánnom tuku sa verifikujú hemorágie a difúzna nekróza. Nález chýbania vaskulárnej a perivaskulárnej inflamácie a absencie arteriolárnej trombózy sa považuje za typický (16).
Patofyziologicky presná etiológia nie je známa. Predpokladaný mechanizmus spočíva vo warfarínom úvodne vyvolanom relatívnom hyperkoagulačnom stave. V prítomnosti warfarínu dochádza k poruche gama karboxylácii reziduí kyseliny glutámovej u koagulačných proteínov, ktoré sa stávajú defektnými. Toto vedie k blokáde syntézy II, VIII, IX, X faktoru a proteinu C a S. Pokles koncentrácie proteínu C je rýchlejší než iných koagulačných proteínov pre jeho kratší biologický poločas (cca 5 hodín) a hemostatická balancia sa dočasne posúva k hyperkoagulačnému stavu. Rizikové faktory sú familiárny deficit proteínu C, proteínu S, faktoru Leiden, antitrombínu III, lupus antikoagulans, mutácia protrombínového génu a génu pre methylentetrahydrofolátovú reduktázu (mutácie C677T a A1298C) a podávanie vysokých dávok warfarínu (1, 17, 18, 19, 20, 21). Prevencia WISN spočíva v antikoagulačnej terapii s heparínom, alebo nízkomolekulárnym heparínom počas 5–7 dní v začiatku podávania warfarínu. Nie sú doporučené úvodné vyššie dávky warfarínu ako 15 mg denne a zvyšovanie dávky o viac ako 1–2 mg denne. Terapiou WISN je vitamín K, čerstvá mrazená plazma, u pacientov s deficitom proteínu C intravenózne podávanie proteínu C, ktorý bol purifikovaný monklonálnymi protilátkami. Ostatné terapeutické intervencie ako sú kortikoidy, dextrán, vazodilatačná liečba, blokáda sympatiku, oxygenoterapia a hypotermia nemali na priebeh WISN vplyv. Pokračujúca liečba spočíva v ošetrovaní nekrotickej rany. Topická terapia môže zahŕňať lokálne antibiotiká, špeciálne obväzy, krytie a hydrogély. Chirurgická liečba je potrebná až v 50 % prípadov, s debridementom nekrotických más, graftingom pokožky až mukokutánnym lalokom k prekrytiu veľkého defektu, extrémne prípady vyžadujú amputáciu končatiny (16, 18). V budúcnosti antikoagulačné stratégie môžu zahrňovať priame inhibítory trombínu a inhibítor faktoru Xa (fondaparinux) (21). Skríning pacientov na deficit proteinu C, S, antitrombínu, Leidenskú mutáciu a MTHFR pred začatím podávania warfarínu môže oneskoriť liečbu a nie je doporučovaný. Výsledky týchto testov však nie sú špecifické ani senzitívne v predikovaní rizika vývoja stavu (18).
Záver
Riziko vzniku tejto vzácnej komplikácie liečby warfarínom môže byť redukované skúseným klinikom pri znalosti rizikových faktorov rýchlym vyslovením podozrenia na WISN. Obmedzenie mortality a morbidity závisí na včasnej intervencii. U plánováného podávania warfarinu sa nedoporučuje štandardne vyšetrovať vrodené genetické trombofilné stavy, resp. len v prípade rodinnej záťaže. Dôležitá je prevencia súčasným podávaním heparínu a používanie nízkych dávok warfarínu (nie viac ako 15 mg denne s denným zvyšovaním dávky o 1–2 mg). U rizikových pacientov sa podanie warfarínu nedoporučuje. Liečba WISN pozostáva v podaní vitamínu K, čerstvej mrazenej plazmy, purifikovaného proteínu C, lokálnej a chirurgickej liečbe. WISN sa vyskytuje u pacientov aj napriek znalostí rizík a dodržaniu liečebných opatrení lege artis. Naostatok, podľa našich vedomostí ide o prvý prípad WISN popísaný v Českej republike.
MUDr. Alexander Kreze Ph.D.
II. interní oddělení FN Bulovka
Budínova 2
180 00 Praha 8–Libeň
Doručeno do redakce: 13. 4. 2009
Přijato: 10. 7. 2009
Sources
1. Byrne JS, Razak A, Patchett S, et al. Warfarin skin necrosis associated protein S deficiency and mutation in the methyltetahydrofollate reductase gene. Clin Exp Dermatol 2004; 29 : 35–36.
2. Varga EA, Sturm AC, Misita CP, et al. Homocysteine and MTHFR mutations. Circulation 2005; 111: e289–e293.
3. Pyeritz RE. Genetic disorders. In: McPee SJ, Papadakis MA, Tierney LM, jr. Current medical diagnosis treatment. 64th ed. New York, McGraw Hill, 2007; 1737–1742.
4. Flood EP, Redish MH, Bociek SJ, et al. Tromboflebitis migrans disseminate: Report of case in which gangrene of breast occured. New York State Jr Med 1943; 43 : 1121–1124.
5. Bhat MH, Bhadada S, Bhansali A. Warfarin-induced skin necrosis: in a patient with craniopharyngioma. Neurosciensces 2006; 11 : 50–52.
6. Gelwix TJ, Beeson MS. Warfarin-induced skin necrosis. Am J Emerg Med 1998; 16 : 541–543.
7. Chan YC, Valenti D, Mansfield AO, et al. Warfarin induced skin necrosis. Br J Surg 2000; 87 : 266–272.
8. Adverse drug reaction advisory commitee (ARDAC): Warfarin-induced skin necrosis. Austral Adverse Drug React Bull 2005; 24.
9. Essex DW, Wynn SS, Jin DK. Late-onset warfarin-induced skin necrosis: case report and review of litarature. Am J Hematol 1998; 57 : 233–237.
10. Scarff CE, Baker CI, Hill P, Foley P. Late onset warfarin necrosis. Case report. Aust J Dermatol 2002; 43 : 202–206.
11. Khalid KK. Warfarin-induced necrosis of the breast: case report. J Postgrad Med 2004; 50 : 268–269.
12. Raifei N, Tabandeh H, Hirschbein M. Warfarin-induced skin necrosis of the eylids. Arch Opthalmol 2007; 125 : 421.
13. Warkentin TT, Whitlock RP, Teoh KH. Warfarin-associated multiple digital necrosis complicating heparin induced trombocytopenia and Raynaud’s phenomen after aortic valve replacement for adenocarcinoma-associated thrombotic endocarditis. Am J Hematol 2004; 75 : 56–62.
14. Humphries JE, Gardner JH, Connelly JE. Warfarin skin necrosis: recurrence in the absence of anticoagulant therapy. Am J Hematol 1991; 37 : 197–200.
15. Jabar HBA. Warfarin-induced skin necrosis: a case report. Clin Appl Tromb Hemost 2006; 12 : 101–104.
16. Beitz JM. Feature: coumadin-induced skin necrosis. Wounds 2002;14 : 217–220.
17. Patel GK, Grey JE, Harding KG. Uncommon causes of ulceration. Br J Med 2006; 332 : 594–596.
18. Van Zandt M. Painful abdominal ecchymotic lesions. Clin J Oncol Nurs 2002; 6 : 363–365.
19. Yang Y, Algazy K. Warfarin-induced skin necrosis in patient with mutation of the prothrombin gene. N Engl J Med 1999; 340 : 753.
20. Kessler P. Trombofilní stavy. Interní med 2006; 9 : 374–379.
21. Jorg I, Fenyvesi T, Harenberg J. Anticoagulant-related skin reaction. Exp Opin Drug Saf 2002; 1 : 278–294.
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today

2009 Issue 3-
All articles in this issue
- Cievny endotelový rastový faktor u osôb s diabetom 2. typu
- Pozitronová emisní tomografie a integrovaná pozitronová emisní tomografie s počítačovou tomografií ve stážování a hodnocení léčebné odpovědi u ne-hodgkinských lymfomů. Část II.: Hodnocení léčebné odpovědi
- Warfarínom indukovaná kožná nekróza: kazuistika a prehľad literatúry
- Činnost nemocniční transfuzní služby v České republice v roce 2008
- Detekce mutace JAK2V617F u myeloproliferativních onemocnění – přehled a vlastní zkušenosti
- Úspěšná léčba časného molekulárního relapsu variantní formy sekundární akutní promyelocytární leukemie oxidem arsenitým
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Detekce mutace JAK2V617F u myeloproliferativních onemocnění – přehled a vlastní zkušenosti
- Úspěšná léčba časného molekulárního relapsu variantní formy sekundární akutní promyelocytární leukemie oxidem arsenitým
- Warfarínom indukovaná kožná nekróza: kazuistika a prehľad literatúry
- Pozitronová emisní tomografie a integrovaná pozitronová emisní tomografie s počítačovou tomografií ve stážování a hodnocení léčebné odpovědi u ne-hodgkinských lymfomů. Část II.: Hodnocení léčebné odpovědi
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career