-
Medical journals
- Career
Komplexní respirační fyzioterapie chronických respiračních onemocnění v dětském věku
Authors: Plešková J.; Irving A.; Stehnová T.; Kobesová A.
Authors‘ workplace: Klinika rehabilitace a tělovýchovného lékařství 2. LF UK a FN Motol, Praha
Published in: Rehabil. fyz. Lék., 30, 2023, No. 2, pp. 105-113.
Category: Review Article
doi: https://doi.org/10.48095/ccrhfl2023105Overview
Respirační fyzioterapie (RFT) je integrální součástí komprehensivní péče o pacienty nejen s primárně respiračním onemocněním. Z dostupné literatury je zřejmé, že poruchy dechu na různých úrovních velmi významně ovlivňují posturální a motorické funkce jedince a je tomu tak i opačně. Různé techniky RFT nemají za cíl ovlivnit pouze očistu dýchacích cest a respirační funkce jako takové, ovlivňují nemocného jedince komplexně. RFT lze v pediatrii využít u širokého spektra diagnóz od respiračních onemocnění přes kardiovaskulární, metabolické a neurologické diagnózy, které ovlivňují dýchání, až po vzácná genetická onemocnění, jako je například cystická fibróza a primární ciliární dyskineze. Péče o pacienty se vzácnými onemocněními je centralizována na velká pracoviště s letitými zkušenostmi, jako je i Fakultní nemocnice v Motole. Text se zaměřuje na komplexní fyzioterapeutickou péči u dětí zejména se vzácnými diagnózami a seznamuje čtenáře nejen s klinickými, ale i recentními vědeckými poznatky v této problematice.
Klíčová slova:
cystická fibróza – primární ciliární dyskineze – respirační fyzioterapie
Úvod
Respirační fyzioterapie (RFT) je jednou ze základních složek širšího pojmu plicní rehabilitace. Respirační fyzioterapeuti spolupracují v multidisciplinárním týmu s lékařem, psychologem, nutričním terapeutem, sociálním pracovníkem a dalšími specialisty. Plicní rehabilitace komplexně pečuje o pacienta zejména z hlediska dechového komfortu, zvládání jeho obtíží v pohledu biopsychosociálním, a snaží se tak o využití funkčního zdraví k dosažení maximální možné kvality života. RFT je soubor technik prováděných fyzioterapeutem, který jednotlivé techniky volí dle konkrétního problému daného pacienta.
Metody a přístupy jsou různé dle základního onemocnění, věku pacienta a zejména pak symptomatiky. Jedním ze symptomů, který lze řešit metodami RFT, je dyspnoe [1], tj. dušnost, která vzniká z různých příčin, jako je např. obstrukce horních cest dýchacích (HCD), hyperprodukce bronchiálního sekretu v dolních cestách dýchacích (DCD), nedostatečná mobilita hrudníku, svalové dysbalance, dysfunkce či paréza bránice, bolest, blokády žeber a páteře, jizvy po operacích, viscerální obtíže a další [2–4]. Z toho vyplývá, že pro úspěch terapie je nutné pohlížet na pacienta komplexně a neomezit se v RFT pouze na techniky hygieny dýchacích cest (ACT – airway clearance techniques).
V rámci každodenní klinické praxe na dětské části Kliniky rehabilitace a tělovýchovného lékařství FN Motol se v rámci RFT často setkáváme s pacienty s chronickým respiračním onemocněním, jako je cystická fibróza (CF) či primární ciliární dyskineze (PCD). Přestože se jedná o onemocnění vzácná, díky specializovaným centrům spadajícím pod FN Motol máme možnost s pacienty dlouhodobě pracovat jak ambulantně, tak při hospitalizaci. Z jiných primárně respiračních onemocnění pracujeme s pacienty s plastickou bronchitidou, bronchopulmonální dysplazií a dalšími vzácnými diagnózami.
Čím dál více pozornosti se však dostává také pacientům s jinou primární diagnózou, v rámci které se respirační obtíže objevily až jako sekundární komplikace, případně jako komplikace léčebných postupů. Velkou skupinu tvoří pacienti s neuromuskulárními onemocněními, tj. nejčastěji spinální muskulární atrofie, Duchennova muskulární dystrofie, dětská mozková obrna (DMO), syndrom transverzální léze míšní a další. U těchto pacientů převládá svalová slabost, a tedy neschopnost efektivně očistit plíce od usazeného hlenu a nečistot.
Do této skupiny spadají také pacienti onkologičtí, např. pacienti po proběhlé alogenní transplantaci kostní dřeně v rámci reakce štěpu proti hostiteli (GVHD – graft versus host disease), která se projevuje v plicním parenchymu jako tzv. obliterující bronchiolitida [5]. RFT také využíváme jak u primárních, tak u sekundárních nádorů v oblasti plic a hrudníku.
Sekundárně respirační problematika se často vyskytuje také u pacientů po chirurgických a kardiochirurgických výkonech [6], kde je nutné dbát zejména na rozvíjení hrudního koše, sílu a vytrvalost dechových svalů a velice pečlivé ošetření pooperační jizvy. Obecně jsou tito pacienti náchylní k posturálním odchylkám a vadnému držení těla, zejména v případě asymetrických operačních přístupů. V rámci výkonů v oblasti jícnu a trachey se často setkáváme se vzniklou tracheomalacií, tj. změknutím chrupavek průdušnice, což je velká překážka pro efektivní odhlenění, která zvyšuje riziko opakovaných respiračních infektů.
V neposlední řadě je pozornost věnována také pacientům se systémovým onemocněním. Autoimunitní onemocnění, jako je např. sklerodermie či juvenilní idiopatická artritida, může v rámci extraartikulárních projevů negativně zasáhnout i do dechového komfortu, a to nejčastěji v podobě limitace vitální kapacity plic. Snížení vitální kapacity může mít příčinu zevní, tedy v omezené posunlivosti a protažitelnosti měkkých tkání, ale i příčinu vnitřní – zasažení intersticia plic [7].
Onemocnění, se kterými se respirační fyzioterapeut v rámci pediatrické praxe může setkat, je velké množství. Při volbě postupů RFT je zásadní podrobná znalost patofyziologie jednotlivých stavů a mechanizmus očekávaného účinku jednotlivých terapeutických technik.
Vzhledem k naší dlouholeté multioborové spolupráci s odborníky z centra CF a nyní nově vznikajícího centra pro pacienty s PCD se v následující části článku věnujeme zejména těmto dvěma onemocněním.
Etiologie a patogeneze u onemocnění cystickou fibrózou a primární ciliární dyskinezí
Cystická fibróza je onemocnění způsobené genovou mutací, která vede k poruše transportu chloridových iontů přes buněčnou membránu. V plicích tato porucha způsobuje zvýšení viskozity hlenu, což narušuje základní obranný mechanizmus plic, tzv. mukociliární clearance. Plíce nejsou řádně očišťovány, vazký hlen stagnuje v dýchacích cestách, a vytváří se tak prostředí pro opakované infekce. Chronické bronchopneumonie pak mohou vést k ireverzibilnímu poškození plicního parenchymu. K typickému průběhu CF patří i postižení dalších orgánových soustav, např. gastrointestinální příznaky, zvýšená koncentrace chloridů v potu či neplodnost [8].
Mukociliární clearance je nedostatečná i u PCD, kde genetická mutace způsobuje poruchu struktury či funkce řasinek – vlasovitých organel, které se na procesu mukociliární clearance významně podílí. U pacientů se často vyskytují respirační příznaky v podobě chronických nebo opakujících se akutních infekcí postihujících horní i dolní cesty dýchací. Jelikož řasinky ovlivňují mj. také uložení nepárových orgánů při embryogenezi, u zhruba poloviny pacientů s PCD se vyskytuje abnormální orgánové uložení, např. dextrokardie [9]. Obdobně jako u CF, i v rámci PCD vidíme další přidružené mimoplicní projevy, jako jsou např. časté otitidy či problémy s fertilitou. Ačkoli prozatím chybí data o průměrném věku dožití pacientů s PCD, předpokládá se, že toto onemocnění sice ovlivňuje kvalitu života pacientů a může vést např. až k respiračnímu selhání, nicméně na rozdíl od CF, u které se v současnosti medián přežití pohybuje mezi 40.–50. rokem věku [10], nezkracuje významně délku jejich života [11].
Systém péče
V České republice se od roku 2009 provádí novorozenecký screening cílený na CF [12], díky němuž se tuto nemoc ve většině případů podaří zachytit již krátce po narození. PCD je naopak celosvětově poddiagnostikované onemocnění a často je diagnóza stanovena až v pozdějším věku, zřejmě z důvodu malého povědomí o této nemoci a komplikovaného diagnostického procesu, který vyžaduje sérii nákladných testů [11]. V Evropě je předpokládaná incidence PCD 1 : 10 000 – 1 : 20 000 živě narozených [8]. Pro porovnání, incidence CF se v současnosti odhaduje na 1 : 3 000 – 1 : 6 000 živě narozených [13]. V ČR má diagnózu PCD potvrzenou 163 pacientů (údaj k 21. 1. 2023, [14]). Pacientů s CF je v ČR aktuálně 693, z toho 367 je dětských (údaj z registru CF pacientů z ledna roku 2023). V současné době je snaha o centralizaci těchto pacientů v rámci diagnostických a terapeutických center nabízejících komplexní péči. Mezi centra pro CF se řadí FN Motol, FN Brno, FN Olomouc a FN Hradec Králové. Pacienti s PCD jsou sdružováni zejména v rámci specializovaného pracoviště ve FN Motol, nicméně je snaha úzce spolupracovat s dalšími pracovišti v rámci ČR.
Pro obě zmíněná onemocnění byl ve FN Motol za přispění multidisciplinárního týmu vytvořen tzv. standardní pracovní postup (SOP – standard operating procedure) [15], jenž představuje doporučenou péči o pacienty s CF i PCD vč. fyzioterapeutických kontrol. Ty jsou indikovány minimálně 1× ročně (ideálně jednou za 3 měsíce) v podobě ambulantní a dále při každé hospitalizaci. Pro nově diagnostikované pacienty probíhají na Pediatrické klinice 2. LF UK a FN Motol edukační pobyty, jejichž nedílnou součástí je edukace technik RFT. Důraz je kladen na nácvik inhalační techniky, péče o horní cesty dýchací a provádění jednotlivých technik RFT. Ty jsou voleny dle věku pacienta. U novorozenců a kojenců je využíván respirační handling, u starších pacientů využíváme aktivních ACT a v případě potřeby i manuální a pohybové fyzioterapie. V rámci edukačních pobytů, které trvají většinou 3–4 dny, jsou pacienti kromě RFT seznámeni se specifickými výživovými doporučeními, hygienickými opatřeními a v neposlední řadě je jim poskytnuta konzultace s genetikem a psychologická podpora. Pro rodiny s dítětem s diagnózou CF je zajištěna návštěva sociálního pracovníka z Klubu CF, neziskové organizace pomáhající k lepší informovanosti a kvalitě života pacientů s CF.
Fyzioterapie u pacientů s cystickou fibrózou a primární ciliární dyskinezí
U chronických respiračních onemocnění v dětském věku typu CF a PCD je fyzioterapie jedním ze základních pilířů komprehensivního terapeutického přístupu. S postupující léčbou se zvyšuje kvalita života pacientů a mění se jejich představy a nároky na jeho prožití. U těchto dvou onemocnění je sice stále hlavní příčinou morbidity a mortality plicní onemocnění, přesto v rehabilitaci hraje důležitou roli pohybová fyzioterapie či se s fyzioterapií respirační prolíná.
Ovlivnění respiračních symptomů fyzioterapeutickými přístupy
Pro ovlivnění hlavních respiračních symptomů se využívají techniky RFT. Jejich hlavním cílem je snížení bronchiální obstrukce, zlepšení průchodnosti dýchacích cest a prevence zhoršování funkce plic [1,16]. Technik RFT je velké množství, avšak existuje jen málo evidence, která by dokazovala prioritní využití jedné techniky před druhou [17]. ACT proto musí být přizpůsobeny individuálním potřebám nemocného dítěte [16]. Při předepisování vhodné ACT je zásadní flexibilita a preference pacienta [18].
Na dýchací cesty je třeba se dívat jako na funkční jednotku začínající nosem a končící plicními sklípky. Chceme-li se tedy např. vyhnout přenosu bakteriální infekce z HCD do DCD, je potřeba pravidelně provádět očistu HCD. Obstrukce HCD má zásadní dopad na čich, chuť, spánek, provádění fyzické aktivity, bolest hlavy atd. [19], což se projevuje zejména u pacientů s PCD. K pravidelné očistě lze s efektem využít proplachy HCD běžně dostupnými pomůckami, jako je např. Rhino Horn či Respimer (obr. 1). Samozřejmostí je také správná technika smrkání. Dítě při smrkání musí používat obě ruce, přičemž dotyk prstů je asi 1 cm vedle kořene nosu. Křídla nosu by neměla být stisknuta. Sekret z HCD by měl být odstraňován za pomocí dlouhého výdechu nosem při uzavřených ústech. Nejprve bychom měli smrkat z obou nosních průduchů, pak ještě z každého zvlášť [20]. Při silné obstrukci HCD jsou doporučovány inhalace do HCD speciálním inhalátorem PARI SINUS (obr. 2, [21]), který zajistí díky kompresím a vibračnímu signálu posun inhalační látky do geometricky složitých nosních dutin.
Image 1. Pomůcky Rhino Horn (vlevo) a Respimer (vpravo).
Fig. 1. Rhino Horn (left) and Respimer (right) aids.
Image 2. Inhalátor PARI SINUS2, se svolením převzato z [21].
Fig. 2. PARI SINUS2 inhaler, adapted with permission from PARI SINUS2 [21].![Inhalátor PARI SINUS2, se svolením
převzato z [21].<br>
Fig. 2. PARI SINUS2 inhaler, adapted
with permission from PARI SINUS2 [21].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/b846ffa9124a4541491e408777b06072.jpg)
Očista DCD je založená na výdechových technikách, při kterých dochází ke změně průtoku nebo odporu v DCD.
Techniky respirační fyzioterapie bez pomůcek
Mezi základní techniky, jejichž využití je i přes příchod nových přístrojových postupů stále aktuální, patří autogenní drenáž a aktivní cyklus dechových technik [16]. Jejich nezastupitelnou výhodou je jejich dostupnost. Po správném zaškolení je může pacient provádět zcela samostatně bez pomoci terapeuta a není tak limitován časem ani místem.
Techniky respirační fyzioterapie s pomůckami, přístroji
Respirační postupy, které využívají k očistě dýchacích cest pomůcky, jsou stejně jako u dospělých velmi oblíbené a hojně využívané i u dětí. U pacientů s CF i PCD lze využít jak pomůcky s kontinuálním, tak oscilačním výdechovým přetlakem. Přetlak (PEP – positive expiratory pressure) v DCD zajistí jejich otevření až do konečné fáze výdechu, zabrání předčasnému kolapsu DCD, a umožní tak posun sekrece z periferních do centrálních DCD. Oscilace napomohou k snadnějšímu odlepení hlenu od stěny bronchu, jeho sesbírání a v neposlední řadě ke změně reologie sputa, která je zapotřebí zejména pro transport vazkého hlenu pacientů. Tyto pomůcky jsou většině fyzioterapeutů zabývajících se RFT známé (tab. 1).
Table 1. Pomůcky s kontinuálním a oscilačním výdechovým přetlakem.
Tab. 1. Devices with continuous and oscillating positive expiratory pressure.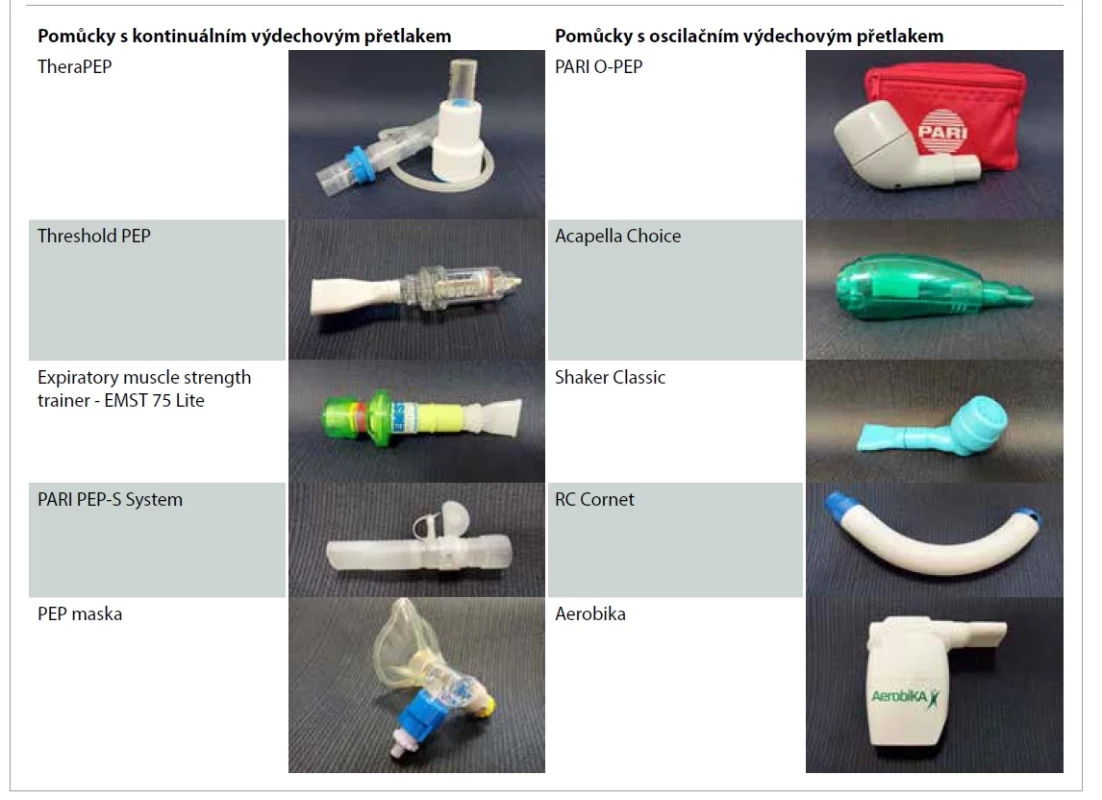
Inovativní přístupy v respirační fyzioterapii
V rámci ACT se nově setkáváme i s přístrojovými metodami pracujícími na základě různých inovativních principů. Jednou z nich je terapie s využitím přístroje Simeox. V ČR je tento přístroj relativní novinkou, od roku 2018 se však postupně dostává do širšího povědomí laické i odborné veřejnosti. Základem technologie je vibrační signál generovaný přístrojem, přenášený do dýchacích cest během výdechu, který je založen na střídání krátkodobého negativního tlaku s atmosférickým tlakem. Tím se odlišuje od ostatních oscilačních pomůcek standardně využívaných v rámci RFT, které jsou založeny převážně na působení mechanického vlnění. Zmíněné střídání tlaků probíhá ve dvou specifických frekvencích 12 a 6 Hz, které byly ověřeny jako účinné pro cílenou změnu viskoelasticity hlenu a jeho posun směrem k centrálním dýchacím cestám. Hlen se tak stává kapalnějším, odlepuje se od stěn dýchacích cest a zároveň je transportován směrem ven [22] (obr. 3).
Image 3. Přístroj Simeox a jeho použití.
Fig. 3. The Simeox device and its use.
Výhoda technologie Simeox také spočívá ve schopnosti zasáhnout až do samotné periferie dýchacích cest [23]. Vzhledem k jeho krátkodobému působení na poli RFT je publikovaných studií týkajících se efektivity terapie s přístrojem Simeox poskrovnu. Z jejich dosavadních výsledků však vyplývá dobrá tolerance přístroje pacienty a jeho vysoká bezpečnost bez výskytu nežádoucích účinků [24]. Studie polských odborníků na skupině pacientů s CF prokázala pozitivní efekt terapie s přístrojem Simeox na parametr MEF 25 (maximální výdechový průtok na 25% vitální kapacity), tedy ukazatel průchodnosti periferních dýchacích cest [23]. Ve FN Motol aktuálně probíhá studie, jejímž úkolem je porovnat efekt terapie standardně používané oscilační přetlakové pomůcky PARI O-PEP s přístrojem Simeox na plicní funkce a rozvíjení hrudníku u pacientů s PCD. Hodnocen bude parametr očišťovací index plic (LCI – lung clearance index) měřený metodou vícedechového vyplavování dusíku z plic (MBW – multiple breath washout). Hodnoceny budou také spirometrické parametry a respirační amplitudy v axilární, mezosternální a xiphosternální oblasti.
Hlavní odlišnosti ve fyzioterapeutických přístupech k pacientům s cystickou fibrózou a primární ciliární dyskinezí
O účinnosti jednotlivých technik RFT u pacientů s PCD zatím není dostatek evidence, doporučení pro fyzioterapii tak vznikají na základě poznatků a klinických zkušeností s pacienty s CF. Přestože tato dvě onemocnění mají podobný klinický obraz, je vždy nutné pamatovat na jejich odlišnou patogenezi.
CF i PCD jsou onemocnění genetická. Na rozdíl od CF, kterou způsobuje mutace jednoho konkrétního genu, je popsáno přes 35 různých genů, jejichž poškození může být příčinou PCD [25]. PCD je tedy geneticky daleko více heterogenní, klinická manifestace symptomů v rámci obou diagnóz se může výrazně lišit, a to jak dominujícími příznaky, tak především jejich závažností, což musí být v rámci terapie vždy zohledněno.
Respirační příznaky jsou u obou nemocí způsobené narušenou mukociliární clearance. U CF je hlavní příčinou respiračních obtíží zvýšená viskozita hlenu, která sekundárně snižuje pohyblivost řasinek. Pacienti s PCD mají sice také více vazký hlen, který je ve svém složení podobný hlenu pacientů s CF [26], řasinková dysfunkce je zde však primární. U pacientů s CF tak může být v raném věku mukociliární clearance částečně zachována, zatímco u PCD tento mechanizmus nefunguje již od narození, a proto se respirační příznaky typicky objevují již u novorozenců, např. jako syndrom dechové tísně [27]. Paradoxně se však v takto nízkém věku setkáváme zpravidla více s pacienty s CF právě díky zavedenému novorozeneckému screeningu. Pro fyzioterapeuty je klinicky nejvýznamnějším rozdílem PCD oproti CF větší míra postižení HCD ve smyslu jejich obstrukce u PCD, často spojená se záněty středouší. V rámci fyzioterapie proto nesmí chybět edukace o metodách hygieny DCD, ale i HCD.
Inhalační léčba – samozřejmá součást respirační fyzioterapie
Pro efektivní zvládnutí očisty dýchacích cest od bronchiální sekrece je důležitá také inhalační léčba. Její správné provedení je taktéž v rukou zkušeného fyzioterapeuta. Správná inhalační technika je závislá na několika faktorech: výběr správného inhalátoru, načasování inhalace během dne (inhalační strategie), výběr inhalační látky a její množství, dechový stereotyp během inhalace, pozice pacienta během inhalace a depozice inhalovaných částic do požadovaného místa. Nejčastěji inhalovanými medikacemi jsou mukolytika mající za cíl různými mechanizmy zředit hlen. Pacienti s chronickým onemocněním dýchacích cest, jako je CF a PCD, provádějí inhalaci mukolytických látek denně (1–3×/den, dle indikace lékaře), aby zajistili pravidelnou a dostatečnou očistu svých dýchacích cest od bronchiálního sekretu. Pro podporu mukociliární clearance se využívá např. hypertonický roztok chloridu sodného (3–7%), který osmoticky přivádí vodu, čímž „ředí“ hlen, a pacient je schopen se ho následně jednodušeji zbavit. Další mukolyticky aktivní látkou je rekombinantní lidská DNáza (rhDNáza – dornáza alfa), která rozpouští DNA uvolňovanou z rozpadlých polymorfonukleárů, což ovlivňuje viskoelasticitu hlenu.
V souvislosti s inhalační léčbou je zapotřebí zmínit ještě další důležitou skupinu léků, a to jsou inhalační antibiotika, která jsou indikována v případě, že se v sekretu z dýchacích cest objeví patogenní mikrobi nebo se objeví známky akutní exacerbace [28].
Ovlivnění fyzické aktivity jedinců
Další základní komponentou, kterou musí mít fyzioterapeut na zřeteli, je pohybová aktivita (PA) nemocného jedince, kterou je potřeba indikovat adekvátně věku a závažnosti onemocnění [17], ideálně ve spolupráci s lékaři z oboru tělovýchovného lékařství. Snižování fyzické zdatnosti jedince je spojeno s poklesem plicních funkcí a parametrů přežití [29]. PA může nemocným pomoci k podpoře očisty dýchacích cest. Za vhodné jsou považovány aktivity jako např. aerobik, basketbal, volejbal, crossfit, kruhový trénink, cyklistika, tanec, fotbal, hokej, intervalový trénink o vysoké intenzitě, pádlování, běh, jogging, orientační běh, squash, plavání, skákání na trampolíně [30]. Záleží vždy na preferencích pacienta a rodiny. Doporučená četnost a trvání pohybových aktivit v jednotlivých věkových obdobích jsou znázorněny v tab. 2 [31].
Table 2. Doporučení pro pohybovou aktivitu u pacientů s cystickou fibrózou v dětském věku, přeloženo a upraveno dle Swisher et al. [31].
Tab. 2. Recommendations for physical activity in patients with cystic fibrosis, translated and adapted from Swisher et al. [31].![Doporučení pro pohybovou aktivitu u pacientů s cystickou fibrózou v dětském věku, přeloženo a upraveno dle
Swisher et al. [31].<br>
Tab. 2. Recommendations for physical activity in patients with cystic fibrosis, translated and adapted from Swisher et al. [31].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/a4dbc1bb1963f3dd95848c4100ffe815.jpg)
PA – pohybová aktivita, TF – tepová frekvence, TF max. – maximální tepová frekvence, RM – repetition maximum Ovlivnění posturálních poruch
Se zlepšujícími se možnostmi léčby a prodlužující se dobou dožití pacientů jdou do popředí i příznaky, které v minulosti byly více upozaděny. Pro fyzioterapii jsou to velmi důležité symptomy muskuloskeletální. Velké množství pacientů s chronickým respiračním onemocněním vykazuje projevy špatné posturální stabilizace, často spojené s bolestmi páteře a posturálními deformitami či odchylkami (hrudní hyperkyfóza, skoliotické držení či skolióza, hyperinflační postavení hrudníku atd.). Některé posturální deformity jsou však reverzibilní, což otevírá okno pro včasné fyzioterapeutické zásahy. Bylo prokázáno, že progredující deformity páteře jsou spojené se zhoršujícími se plicními funkcemi [32]. Stejně tak byla zjištěna korelace mezi množstvím expektorovaného sputa, intenzitou bolestí a deformitami páteře [32]. Proto by se fyzioterapeutická léčba pacienta s chronickým respiračním onemocněním neměla soustředit jen na hygienu dýchacích cest. Z dostupné literatury vyplývá, že posturální odchylky u pacientů s CF mají multifaktoriální podklad [33]. Kromě věku a fyzické zdatnosti pacienta [33] existují další patofyziologické mechanizmy významným způsobem přispívající ke vzniku posturálních a muskuloskeletálních abnormalit. Mezi ně patří změny na úrovni respiračního aparátu (snižování funkce plic, postupná alterace mechaniky dýchání) [34], ale také bolest (schéma 1).
Schéma 1. Vliv abnormální postury na bolest a na plicní funkce, přeloženo a upraveno dle Tattersall et al. [32].
Scheme 1. The effect of abnormal posture on pain and lung function, translated and adapted from Tattersall et al. [32].![Schéma 1. Vliv abnormální postury na bolest a na plicní funkce, přeloženo
a upraveno dle Tattersall et al. [32].<br>
Scheme 1. The effect of abnormal posture on pain and lung function, translated
and adapted from Tattersall et al. [32].](https://pl-master.mdcdn.cz/media/image_pdf/ca7a8210fd64792d0c56b11b64f0db4b.jpg?version=1686074946)
Respirační symptomatika se přímo odráží na pohybovém aparátu nemocného jedince. Pro ovlivnění posturálních dysfunkcí lze využít široké spektrum přístupů a opět je na volbě a znalostech terapeuta, který z nich si vybere. Obecné zásady jsou však stejné. Jako ideální vnímáme v první fázi provést manuální ovlivnění zkrácených, přetížených svalových a vazivových struktur a následně ovlivnit a reedukovat motorické funkce (nejen dechové). Na našem pracovišti k tomuto cíli využíváme zejména prvky Dynamické neuromuskulární stabilizace (DNS) a Vojtovy reflexní lokomoce (VRL). Výhodou využití DNS je možnost po zácviku provádět terapii v domácím prostředí samotným dítětem, k aktivaci motorické reakce při VRL je nutná spoluúčast rodiče. V rámci obou přístupů lze např. dosáhnout aktivace bránice nejen v její respirační, ale také posturální funkci, což má pozitivní dopad nejen na dechové funkce, ale např. i na ovlivnění bolestí páteře [1], velmi častých u pacientů s chronickým kašlem (obr. 4, obr. 5) [32].
Image 4. Hrudník a držení těla pacienta s cystickou fibrózou.
Fig. 4. Chest and posture of a patient with cystic fibrosis.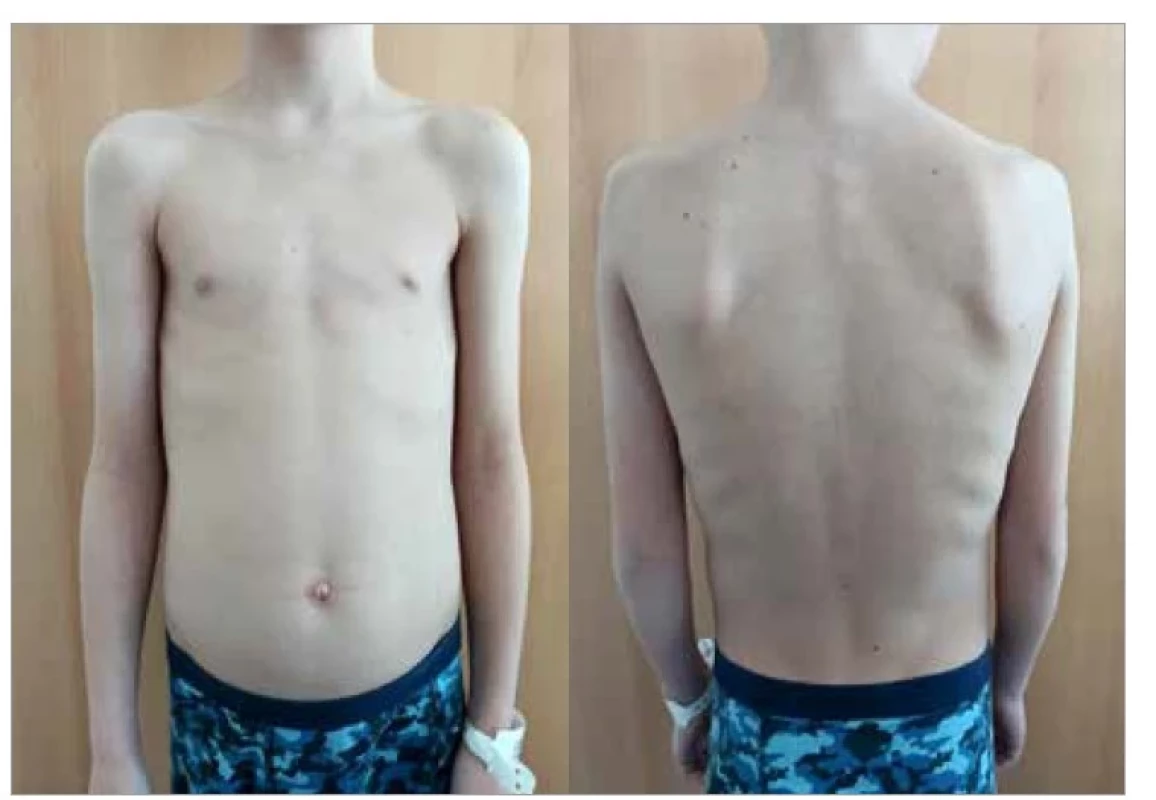
Image 5. Pacient s cystickou fibrózou, kombinace dechového a posturálního tréninku.
Fig. 5. Patient with cystic fibrosis, combination of breathing and postural training.
Vzhledem k tomu, že se ve světě objevují nové terapeutické přístupy, je odbornou společností kladen stále větší důraz na vědecké ověřování účinnosti jednotlivých technik. V rámci Kliniky rehabilitace a tělovýchovného lékařství 2. LF UK a FN Motol byla proto provedena studie hodnotící efekt VRL na plicní funkce u pacientů s CF [35].
Vliv Vojtovy metody na dechové funkce
Přestože byla VRL primárně vyvinuta pro ovlivnění motorických funkcí pacientů s neurologickým deficitem, v dnešní době je tato technika hojně využívána i v jiných medicínských oborech. Její využití v rámci respirační problematiky v praxi poměrně často vídáme, nicméně evidence zkoumající tento aspekt VRL je poměrně málo. Profesor Vojta ve svých pracích popisuje, že ve vztahu k dýchání dochází při VRL ke změně dechové frekvence, dechového objemu, prohloubení kostálního dýchání, rozšíření hrudního koše a zvýšení vitální kapacity [36]. Problematika dechu ve vztahu k VRL byla dále zkoumána jen v několika málo studiích. Italští autoři prověřili bezpečnost provedení VRL u nedonošených jedinců a prokázali pozitivní efekt na saturaci krve kyslíkem SpO2 a zvýšení parciálního tlaku kyslíku PtcO2 [37]. Němečtí autoři po stimulaci VRL zaznamenali pozitivní účinek na dynamickou poddajnost plic a dechovou práci související s objemy plic u kojenců s bronchopulmonální dysplazií [38]. Korejští autoři zkoumali VRL ve vztahu k dechu sledováním motorické reakce bránice u pacientů s DMO a zdravých jedinců. Dospěli k závěru, že při motorické reakci vyvolané VRL stimulací dochází k zvětšení pohybů bránice jak v inspiriu, tak v expiriu [39,40].
Na našem pracovišti proběhla kontrolovaná randomizovaná intervenční cross-over studie, která měla za cíl zhodnotit krátkodobý vliv VRL na dechové funkce u dětských pacientů s CF [35]. Ve studii byl porovnáván účinek 30minutové terapie VRL s „falešnou“ terapií, při které byli pacienti pouze napolohováni do stejných pozic jako při VRL, nicméně nebyla prováděna stimulace reflexních zón [1]. Po VRL stimulaci jsme zjistili statisticky významný pokles globální ventilační nehomogenity (LCI 2,5; p = 0,004), což svědčí pro lepší distribuci vzduchu v periferních dýchacích cestách. Pokles hodnot byl zaznamenán také v regionální ventilační nehomogenitě konduktivních dýchacích cest (Scond*Vt, p = 0,009). Konduktivní dýchací cesty (12.–16. generace bronchiálního větvení) obsahují hladkou svalovinu a jsou vybaveny sympatickými nervovými zakončeními. To by mohlo svědčit pro ovlivnění dechových funkcí prostřednictvím vlivu na autonomní sympatický nervový systém tak, jak hypoteticky naznačoval již prof. Vojta. Pro potvrzení této hypotézy je nutné provést cílené studie. Posledním významně ovlivněným parametrem byla inspirační kapacita, která se po VRL stimulaci signifikantně zvýšila (p = 0,012). Při provádění „falešné“ terapie nedošlo k ovlivnění žádného ze sledovaných parametrů. Deformita trupu a/nebo hrudníku (hodnocena vizuálně při vstupním vyšetření) byla fyzioterapeuty zaznamenána u 76,5 % všech pacientů, přičemž 92,9 % z nich vykazovalo po terapii VRL pokles ventilační nehomogenity [35]. Tyto závěry považujeme za přínosné, neboť dokazují, že skrze ovlivnění motorických funkcí a postury jsme schopni ovlivnit funkci respiračního aparátu jedince.
Závěr
Cílem příspěvku bylo představit systém RFT na dětské části Kliniky rehabilitace a tělovýchovného lékařství 2. LF UK a FN Motol. Článek se věnuje dvěma vzácným chronickým respiračním onemocněním v dětském věku, se kterými přicházíme v naší praxi pravidelně do kontaktu. RFT není omezena pouze na techniky hygieny dýchacích cest, ale po zvládnutí akutních projevů nemoci je nutné fyzioterapií ovlivnit i posturální odchylky a další příznaky nemoci. Pouze tak je možné pacienty do budoucna ochránit od sekundárních komplikací a zvýšit kvalitu jejich života. Fyzioterapeut zastává významné místo v multidisciplinárním týmu, který se o děti s chronickým respiračním onemocněním stará. Limity mohou být v nedostatečném propojení respiračních fyzioterapeutů v rámci ČR a jejich vzájemné komunikaci s místními pneumology. Založení odborné sekce respiračních fyzioterapeutů by usnadnilo vzdělávání fyzioterapeutů, výměnu zkušeností a zkvalitnilo péči o dětské pacienty. Umožnilo by také decentralizaci pacientů, která by výrazně ulevila větším specializovaným zařízením. Vybudování fungující propojené sítě odborníků na dechovou fyzioterapii si klademe jako jeden z hlavních cílů do budoucna.
Doručeno/Submitted: 19. 1. 2023
Přijato/Accepted: 6. 4. 2023
Korespondenční autor:
Mgr. Anna Irving
Klinika rehabilitace a tělovýchovného lékařství
2. LF UK a FN Motol
V Úvalu 84
150 06 Praha 5
e-mail: anna.irving@fnmotol.cz
Sources
1. Kolář P et al. Rehabilitace v klinické praxi. Praha: Galén 2009 : 265–281.
2. Hashmi MF, Modi P, Basit H et al. Dyspnea. StatPearls 2023. [online]. Available from: https://www.ncbi.nlm.nih.gov/books/NBK499965/.
3. Veitch AM, Hughes MJ. Acute abdominal pain and shortness of breath in a female patient. Br J Radiol 2012; 85(1012): 473–475. doi: 10.1259/bjr/21491850.
4. O’Donnell DE, Banzett RB, Carrieri-Kohlman V et al. Pathophysiology of dyspnea in chronic obstructive pulmonary disease: a roundtable. Proc Am Thorac Soc 2007; 4(2): 145–168. doi: 10.1513/pats.200611-159CC.
5. Smith SR, Asher A. Rehabilitation in chronic graft-versus-host disease. Phys Med Rehabil Clin N Am 2017; 28(1):143–151. doi: 10.1016/j.pmr.2016.08.009.
6. Renault JA, Costa-Val R, Rossetti MB. Respiratory physiotherapy in the pulmonary dysfunction after cardiac surgery. Rev Bras Cir Cardiovasc 2008; 23(4): 562–569. doi: 10.1590/s0102-76382008000400018.
7. Yunt ZX, Solomon JJ. Lung disease in rheumatoid arthritis. Rheum Dis Clin North Am 2015; 41(2): 225–236. doi: 10.1016/j.rdc.2014.12.004.
8. Marušiaková L, Ďurdík P, Bacmaňáková I et al. Čo sa môže skrývať za diagnózou atypickej cystickej fibrózy?. Československá Pediatrie 2016; 71(2): 80–86. [online]. Dostupné z: https://www.medvik.cz/link/bmc16014985.
9. Fliegauf M, Benzing T, Omran H. When cilia go bad: cilia defects and ciliopathies. Nat Rev Mol Cell Biol 2007; 8(11): 880–893. doi: 10.1038/nrm2278. Erratum in: Nat Rev Mol Cell Biol 2008; 9(1): 88.
10. Skov M, Hansen CR, Pressler T. Cystic fibrosis – an example of personalized and precision medicine. APMIS 2019; 127(5): 352–360. doi: 10.1111/apm.12915.
11. Schofield LM, Duff A, Brennan C. Airway clearance techniques for primary ciliary dyskinesia; is the cystic fibrosis literature portable? Paediatr Respir 2018; 25 : 73–77. doi: 10.1016/j.prrv.2017.03.011.
12. Skalická V. Terapeutické trendy cystické fibrózy. Pediatr Praxi 2014; 15(6): 340–343.
13. Scotet V, L’Hostis C, Férec C. The changing epidemiology of cystic fibrosis: incidence, survival and impact of the CFTR gene discovery. Genes (Basel) 2020; 11(6): 589. doi: 10.3390/genes11060589.
14. Martinů V. Lékařka PCD centra Pediatrické kliniky FN Motol a 2. LF UK. Ústní sdělení. Praha, 21. 1. 2023.
15. Martinů V, Pohunek P. SOP PCD – ambulantní kontroly a doporučená péče. Řasinky.cz, 2022. [online]. Dostupné z: https://www.rasinky.cz/odb.php.
16. International Physiotherapy Group for Cystic Fibrosis. Physiotherapy for people with cystic fibrosis: from infant to adult. 2019. [online]. Available from: https://www.ecfs.eu/sites/default/files/general-content-files/working-groups/IPG%20CF_Blue%20Booklet_7th%20edition%202019.pdf.
17. Castellani C, Duff AJA, Bell SC et al. ECFS best practice guidelines: the 2018 revision.
J Cyst Fibros 2018; 17(2): 153–178. doi: 10.1016/j.jcf.2018.02.006.
18. Homnick DN. Making airway clearance successful. Paediatr Respir Rev 2007; 8(1): 40–45. doi: 10.1016/j.prrv.2007.02.002.
19. Morrison L, Parrott H (eds) et al. Standards of care and good clinical practice for the physiotherapy management of cystic fibrosis. 2020. [online]. Available from: https://www.cysticfibrosis.org.uk/sites/default/files/2020-12/Standards%20of%20Care%20and%20Good%20Clinical%20Practice%20for%20the%20Physiotherapy%20Management%20of%20Cystic%20Fibrosis%20Fourth%20edition%20December%202020.pdf.
20. Smolíková L. Hygiena horních cest dýchacích – součást léčebné rehabilitace. Pediatr pro Praxi 2002; 6 : 262–267.
21. MR-diagnostic.cz. PARI SINUS2, inhalační přístroj pro nazální použití. [online]. Dostupné z: https://www.mr-diagnostic.cz/pari-sinus2.
22. Philippe G, Morin L, Reynaud-Gaubert M. Safety and efficacy of an innovative airway clearance device versus manual chest physiotherapy techniques for airway secretion clearance: a feasibility study. Europ J Respiratory Med 2020; 1(2): 132–137. doi: 10.31488/ejrm.107.
23. Walicka-Serzysko K, Postek M, Jeneralska N et al. The effects of the addition of a new airway clearance device to chest physiotherapy in children with cystic fibrosis pulmonary exacerbations. J Mother Child 2021; 26(3): 16–24. doi: 10.34763/jmotherandchild.20202403.2013.d-20-00008.
24. Kolek V, Jakubec P, Doleželová J et al. Feasibility and safety evaluation of Simeox airway clearance technique (ACT) in patients with bronchiectasis. Eur Respir J 2020; 54 (Suppl 63): PA601. doi: 10.1183/13993003.congress-2019.PA601.
25. Lucas JS, Alanin MC, Collins S et al. Clinical care of children with primary ciliary dyskinesia. Expert Rev Respir Med 2017; 11(10): 779–790. doi: 10.1080/17476348.2017.1360770.
26. Bush A, Payne D, Pike S et al. Mucus properties in children with primary ciliary dyskinesia: comparison with cystic fibrosis. Chest 2006; 129(1): 118–123. doi: 10.1378/chest.129.1.118.
27. Cohen-Cymberknoh M, Simanovsky N, Hiller N et al. Differences in disease expression between primary ciliary dyskinesia and cystic fibrosis with and without pancreatic insufficiency. Chest 2014; 145(4): 738–744. doi: 10.1378/chest.13-1162.
28. Vávrová V. Cystická fibróza. In: Lebl J, Janda J, Pohunek P et al. Klinická pediatrie. Praha: Galén 2012 : 439–449.
29. Wilkes DL, Schneiderman JE, Nguyen T et al. Exercise and physical activity in children with cystic fibrosis. Paediatr Respir Rev 2009; 10(3): 105–109. doi: 10.1016/j.prrv.2009.04.001.
30. Saynor ZL, Cunningham S, Morrison L et al. Exercise as airway clearance therapy (ExACT) in cystic fibrosis: a UK-based e-Delphi survey of patients, caregivers and health professionals. Thorax 2023; 78(1): 88–91. doi: 10.1136/thorax-2022-219213.
31. Swisher AK, Hebestreit H, Mejia-Downs A et al. Exercise and habitual physical activity for people with cystic fibrosis: expert consensus, evidence-based guide for advising patients. Cardiopulm Phys Ther J 2015; 26(4): 85–98. doi: 10.1097/CPT.0000000000000016.
32. Tattersall R, Walshaw MJ. Posture and cystic fibrosis. J R Soc Med 2003; 96(Suppl 43): 18–22.
33. Cherobin IA, Dalcin PTR, Ziegler B. Association between lung function, physical activity level and postural evaluation variables in adult patients with cystic fibrosis. Clin Respir J 2018; 12(4): 1510–1517. doi: 10.1111/crj.12698.
34. Massery M. Musculoskeletal and neuromuscular interventions: a physical approach to cystic fibrosis. J R Soc Med 2005; 98 (Suppl 45): S55–S66.
35. Pleskova J, Koucky V, Medunova K et al. Reflex zone stimulation reduces ventilation inhomogeneity in cystic fibrosis: a randomised controlled cross-over study. Pediatr Pulmonol 2021; 56(6): 1558–1565. doi: 10.1002/ppul.25350.
36. Vojta V, Peters A. Vojtův princip. Grada Publishing 2010 : 17–19.
37. Giannantonio C, Papacci P, Ciarniello R et al. Chest physiotherapy in preterm infants with lung diseases. Ital J Pediatr 2010; 36 : 65. doi: 10.1186/1824-7288-36-65.
38. Böhme B, Futschik M. Verbesserte Lungenfunktion nach Vojta‐Brustzonen‐Reiz bei bronchopulmonaler Dysplasie. Monatsschrift Kinderheilkunde 1995; 143(12): 1231–1234.
39. Ha S-Y, Sung Y-H. Effects of Vojta method on trunk stability in healthy individuals. J Exerc Rehabil 2016; 12(6): 542–547. doi: 10.12965/jer.1632804.402.
40. Ha S-Y, Sung Y-H. Effects of Vojta approach on diaphragm movement in children with spastic cerebral palsy. J Exerc Rehabil 2018; 14(6): 1005–1009. doi: 10.12965/jer.1836498.249.
Labels
Physiotherapist, university degree Rehabilitation Sports medicine
Article was published inRehabilitation & Physical Medicine

2023 Issue 2-
All articles in this issue
- Bezprostřední vliv Schultzova autogenního tréninku na autonomní nervový systém, hodnocený ukazateli spektrální a časové analýzy variability srdeční frekvence u zdravých probandů
- Terapie Vojtovou reflexní lokomocí není kontraindikována u dětských hematoonkologických a onkologických pacientů
- Proces ergodiagnostiky a jeho vývoj v kontextu aktuálních společenských změn
- Možnosti ovplyvnenie dysmenorey
- Testování motoriky u dětí
- Konzervativní léčba mediálního tibiálního stresového syndromu
- Komplexní respirační fyzioterapie chronických respiračních onemocnění v dětském věku
- Rehabilitation & Physical Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Konzervativní léčba mediálního tibiálního stresového syndromu
- Testování motoriky u dětí
- Terapie Vojtovou reflexní lokomocí není kontraindikována u dětských hematoonkologických a onkologických pacientů
- Proces ergodiagnostiky a jeho vývoj v kontextu aktuálních společenských změn
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

