-
Medical journals
- Career
Aneuryzma pankreatikoduodenální arkády při syndromu ligamentum arcuatum mediale – kazuistika a přehled literatury
Authors: A. Hudák 1; I. Guňka 1; J. Raupach 2; M. Leško 1; A. Krajina 2; Miroslav Lojík 2
Authors‘ workplace: Chirurgická klinika Lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Hradec Králové 1; Radiologická klinika Lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Hradec Králové 2
Published in: Rozhl. Chir., 2021, roč. 100, č. 6, s. 302-306.
Category: Case Report
doi: https://doi.org/10.33699/PIS.2021.100.6.302–306Overview
Úvod: Aneuryzmata viscerálních tepen patří mezi raritně se vyskytující cévní patologie. Obvykle bývají náhodným nálezem při zobrazovacích vyšetřeních. Nejčastějším klinickým projevem jsou nespecifické bolesti břicha a krvácení při jejich ruptuře se závažným klinickým stavem. Aneuryzmata tepen pankreatikoduodenální arkády se vyskytují zejména u pacientů se stenózou nebo uzávěrem truncus coeliacus a kompenzačně rozvinutou kolaterální cirkulací.
Kazuistika: V kazuistice autoři prezentují případ pacientky s náhodně zjištěným aneuryzmatem pankreatikoduodenální arkády, při významné stenóze v odstupu truncus coeliacus, způsobené útlakem ligamentum arcuatum mediale. Průměr výdutě byl 40 mm a endovaskulární terapie nebyla vzhledem k nepříznivým anatomickým poměrům možná. Pacientka byla úspěšně léčena v jedné době kombinovaným chirurgickým výkonem s resekcí aneuryzmatu a současně uvolněním ligamentum arcuatum mediale.
Závěr: U aneuryzmat pankreatikoduodenální arkády není korelace mezi průměrem výdutě a rizikem ruptury. Jejich ruptury mají relativně vysokou morbiditu a mortalitu, a proto
Klíčová slova:
aneuryzma − pankreatikoduodenální arkáda − MALS
ÚVOD
Tepenné aneuryzma definujeme jako permanentní lokalizované rozšíření tepny o více než 50 % předpokládaného průměru normální tepny u daného pacienta [1]. Aneuryzmata viscerálních tepen patří mezi raritně se vyskytující cévní patologie. Viscerální tepny mají široké možnosti kolaterálního oběhu. Jednou ze spojek mezi povodím truncus coeliacus (TC) a horní mezenterickou tepnou (AMS) je pankreatikoduodenální arkáda. Její kaudální část tvoří dolní pankreatikoduodenální arterie odstupující z AMS nebo prvních jejunálních větví AMS. Kraniální část tvoří horní přední a horní zadní pankreatikoduodenální arterie komunikující přes gastroduodenální arterii s TC. Aneuryzmata pankreatikoduodenální arkády (APDA) tvoří okolo 2 % z aneuryzmat viscerálních tepen [2]. První případ APDA byl publikován Fergusonem v roce 1895 [3]. Vznik pravých APDA byl dobře dokumentován jako následek cirkulačních změn při stenóze či uzávěru TC s rozvinutou kolaterální cirkulací [4,5]. Tuto spojitost jako první publikovali Sutton a Lawton v roce 1973 [6]. I když ve většině popsaných případů byly APDA asociované s aterosklerotickými změnami TC, rozvoj APDA může být i následkem stenózy TC zapříčiněné útlakem ligamentum arcuatum mediale [7−9]. APDA se vyskytují u pacientů v širokém věkovém rozmezí s mediánem 60 let, bez významnějšího rozdílu ve výskytu z hlediska pohlaví [10]. Nejčastějším klinickým projevem APDA je ruptura s krvácením, a to nezávisle na velikosti výdutě [11,12]. Většina autorů zabývajících se touto problematikou navrhuje po určení diagnózy časnou léčbu APDA [10,13].
KAZUISTIKA
Prezentujeme případ 51leté ženy, primárně vyšetřené v oblastní nemocnici pro nevolnost, zvracení a bolesti břicha. Při ultrazvukovém vyšetření bylo v oblasti kaudálně pod pankreatem zobrazeno tepenné aneuryzma velikosti 40×30 mm, bez známek ruptury. Dle provedené CT angiografie (CTA) šlo pravděpodobně o změněnou větev odstupující z AMS v rámci pankreatikoduodenální arkády (Obr. 1). S uvedeným nálezem pacientku odeslali do angiocentra Fakultní nemocnice Hradec Králové k další léčbě. Pacientka byla doposud bez závažnějšího předchorobí, neprodělala nitrobřišní infekci ani pankreatitidu. V poslední době byla bez váhového úbytku nebo postprandiálních bolestí, BMI měla 40,7. Úraz břicha anamnesticky negovala. Byla dvakrát těhotná, s nekomplikovanými porody. Při vyšetření na ambulanci cévní chirurgie nebyla přítomna elevace zánětlivých markerů a při klinickém vyšetření už neměla bolesti břicha ani jiné potíže. Angiografické zobrazení prokázalo kritickou stenózu v odstupu TC s obráceným tokem v arteria hepatica communis, která se dominantně plnila přes pankreatikoduodenální ar - kádu z AMS. Stenózu TC způsoboval útlak ligamentum arcuatum mediale (Obr. 1). Angiograficky byla verifikována aneuryzmaticky změněná arteria pancreaticoduodenalis inferior průměru 40 mm odstupující z AMS 25 mm za odstupem z aorty (Obr. 2). Dilatovaný úsek tvořil kaudální část pankreatikoduodenální arkády a podílel se na kolaterálním plnění povodí TC. Endovaskulární ošetření katetrizačním uzávěrem aneuryzmatu s jeho mateřskou tepnou bylo považováno za vysoce rizikové vzhledem k anatomickým poměrům a riziku střevní, případně jaterní ischemie. Chirurgické ošetření nabídlo možnost v jedné době vyřešit APDA i stenózu odstupu TC. Jako operační přístup byla volena příčná laparotomie. Po mobilizaci levého jaterního laloku přes malé omentum byla vypreparována subdiafragmatická aorta s odstupem TC. Přerušením bráničních krúr včetně ligamentum arcuatum mediale byl uvolněn zjevně chronicky zúžený TC. Následně se přes gastrokolické ligamentum infrapankreaticky proniklo k mezenterickým cévám. Po uvolnění horní mezenterické žíly probíhající po přední ploše aneuryzmatu bylo vypreparováno samotné APDA (Obr. 3). Po přerušení tenké přívodné a odvodné větve bylo možné kompletně exstirpovat vak výdutě. Po odstranění výdutě zůstává dobře hmatná pulzace na hepatální arterii. Histologickým nálezem byla stěna vaku pravého aneuryzmatu bez dalších patologických změn. V jinak nekomplikovaném pooperačním průběhu byla přítomna mírná elevace sérové amylázy, s tendencí k poklesu během hospitalizace. Pacientka byla 12. pooperační den propuštěna do ambulantní péče s nastavenou antihypertenzní a dlouhodobou antiagregační terapií 100 mg kyseliny acetylsalicylové denně. Kontrolní CTA vyšetření měsíc po výkonu prokázalo přetrvávající, klinicky asymptomatickou stenózu TC, při dobré průchodnosti mezenterických tepen. V plánu je elektivní endovaskulární dilatace TC se zavedením stentu jako prevence rozvoje dalších aneuryzmat v inkriminované oblasti.
Image 1. CT obraz, aneuryzma pankreatikoduodenální arkády a stenóza odstupu truncus coeliacus
Fig. 1: CT scan, pancreaticoduodenal arcade aneurysm and stenosis of coeliac trunk origin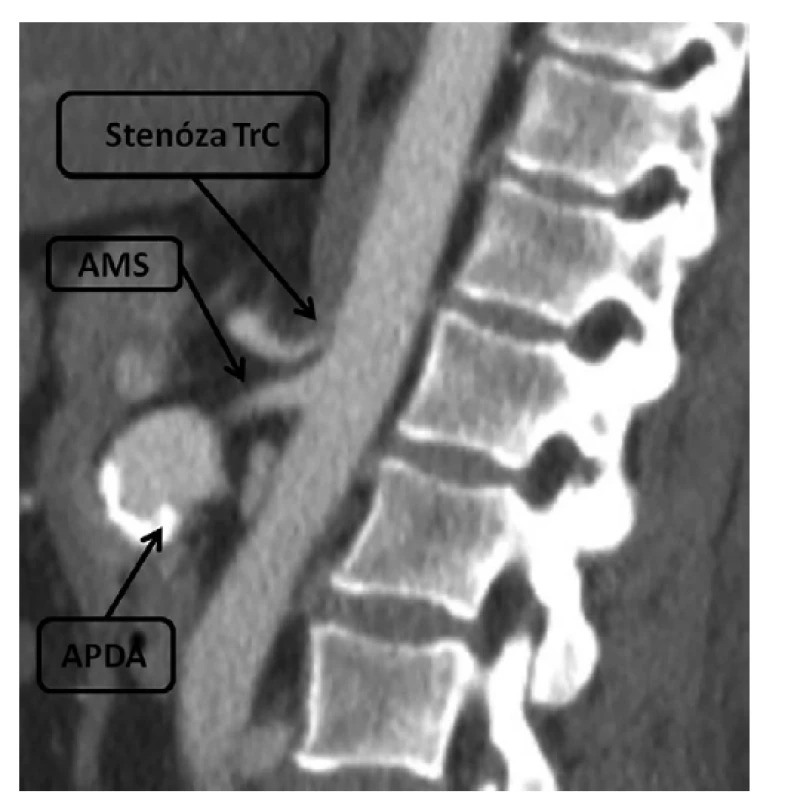
Image 2. Angiografie, horní mezenterická tepna a dolní pankreatikoduodenální tepna
Fig. 2: Angiography, superior mesenteric artery and inferior pancreaticoduodenal artery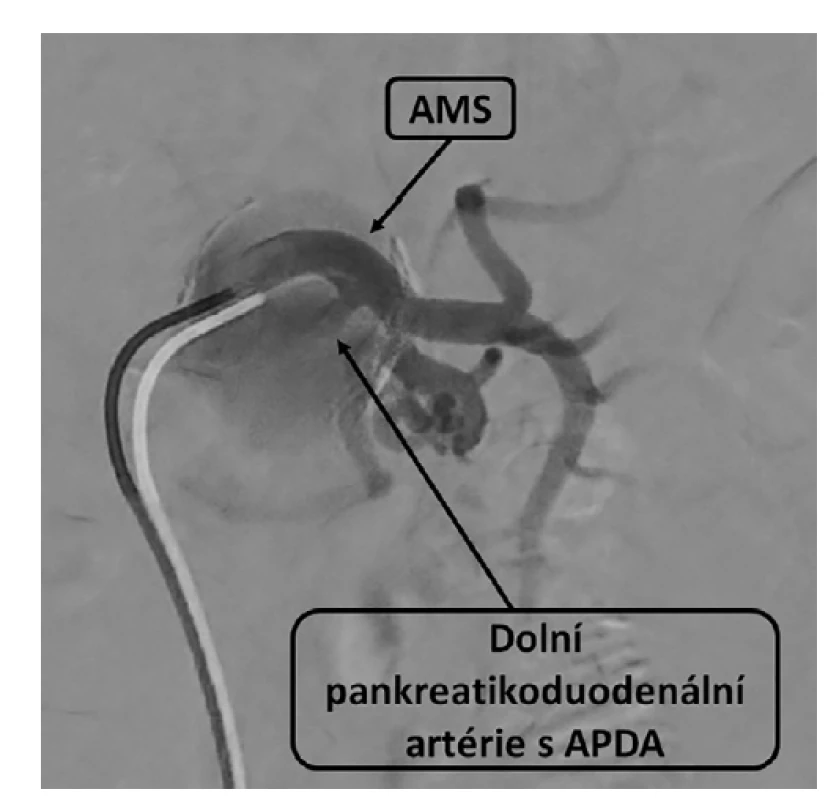
Image 3. Peroperační nález APDA
Fig. 3: Intraoperative finding of APDA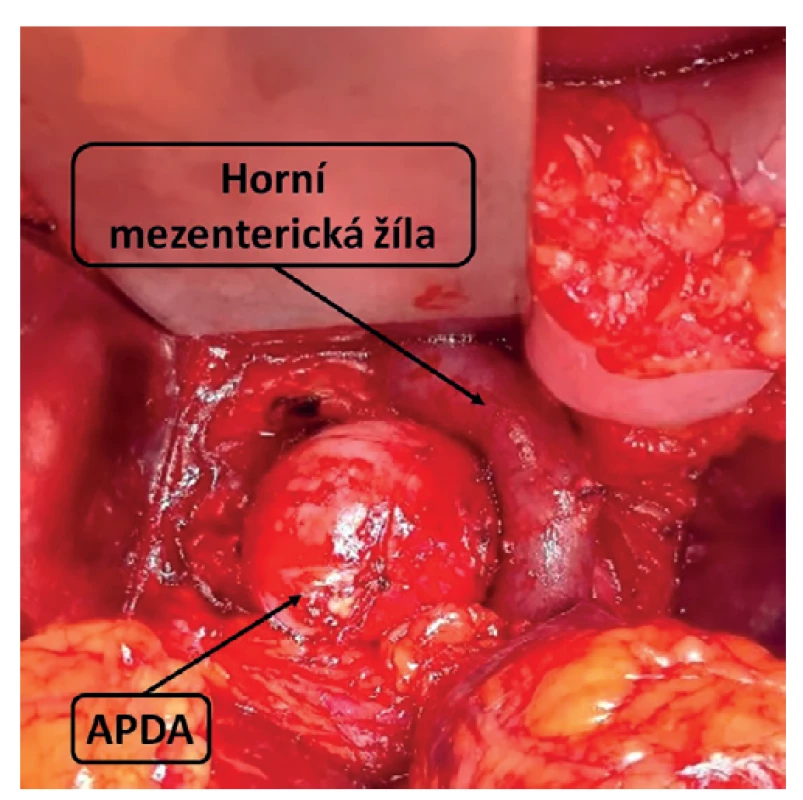
DISKUZE
APDA se vyskytují zejména u pacientů se stenózou nebo uzávěrem TC a kompenzačně rozvinutou kolaterální cirkulací [5]. Dle některých studií je 50−80 % pravých APDA spojeno se stenózou nebo obliterací TC [12,14]. Heo [15] v souboru 37 pacientů se syndromem ligamentum arcuatum mediale (MALS) uvádí vyšší výskyt aneuryzmat viscerálních tepen u pacientů s rozvinutou kolaterální cirkulací oproti těm bez kolaterálního oběhu [15]. Většina pacientů s kompresí TC způsobenou útlakem ligamentum arcuatum mediale nemá ale žádné klinické potíže [16]. Stupeň komprese TC se také může měnit s respiračními pohyby pacienta při vyšetření. Během nádechu se aorta s odstupem TC pohybuje anteriorně a kaudálně. Navíc při inspiriu dochází kaudálním pohybem bránice k relaxaci bráničních krúr a uvolnění tlaku na TC [17]. O klinickém syndromu MALS mluvíme při kombinaci chronických bolestí břicha a radiografické přítomnosti komprese TC [18]. Vzhledem k uvedenému je diagnostika MALS stále obtížná a určit ho jako definitivní příčinu klinických potíží pacienta by se mělo až po vyloučení všech jiných možností. Je však známo, že chronická komprese TC vede ke změnám stěny cévy se zmenšením lumen a sníženému průtoku této tepny. Na kompenzaci sníženého přísunu krve z TC se zvyšuje průtok v kolaterálním systému pankreatikoduodenální arkády zásobené z AMS.
Rozvoj APDA je často klinicky asymptomatický, případně se může projevovat nespecifickými bolestmi břicha a symptomy jako nauzea, zvracení či průjem [12]. U některých pacientů může být APDA symptomatické útlakem AMS nebo obstrukcí žlučových cest [5,19]. Prvním příznakem ale mohou být i bolesti břicha při ruptuře APDA s život ohrožujícím krvácením [10, 20]. V souboru 90 pacientů s APDA, který publikoval Moore, se rupturou projevilo až 62 % výdutí, s mortalitou 21 % [12]. Moore neprokázal korelaci mezi rizikem ruptury a velikosti APDA a v tomto souboru kazuistik praskly i výdutě s průměrem do 1 cm [12]. Při ruptuře APDA směřuje krvácení většinou do retroperitoneálního prostoru [10]. Možná je i propagace krvácení do volné dutiny břišní nebo do gastrointestinálního traktu [20]. Dokumentováno bylo i krvácení do ductus pancreaticus [21].
Základním předpokladem optimální léčby je včasné a komplexní zobrazení viscerálních tepen. Stěžejní zobrazovací a diagnostickou metodou pro viscerální tepny je v současnosti CTA [13]. Umožňuje zobrazit nejen tepenná aneuryzmata, jejich stěnu, přítomnost murálního trombu, známky ruptury a případné krvácení, ale posoudí i průchodnost TC a jeho případnou kompresi okolními strukturami. CTA zobrazí přehledně i břišní orgány a případně posoudí známky ischemie. Angiografické vyšetření je dnes součástí endovaskulární léčby viscerálních výdutí a eventuálně stenóz TC. Angiografické zobrazení posoudí funkčnost kolaterálního oběhu, což je důležitý údaj, který může klinikovi pomoci při volbě léčebného přístupu. Mělo by tak být provedeno pokaždé, když to klinický stav pacienta dovolí [11].
Vzhledem k uváděné vysoké mortalitě a riziku ruptury APDA při jakékoli velikosti doporučuje většina autorů časnou léčbu APDA bez ohledu na jejich průměr [11,20,22]. Také doporučení Evropské společnosti pro cévní chirurgii (ESVS) ohledně mezenterických tepen z roku 2017 uvádí, že u pacientů s asymptomatickým pravým APDA by intervence měla být zvážena bez ohledu na jejich velikost [13].
Z terapeutických možností připadá v úvahu endovaskulární, otevřená chirurgická nebo laparoskopická léčba. Možností jsou i nové hybridní metody [23]. Endovaskulární léčba je dnes pro její nižší morbiditu jednoznačně první volbou jak u akutních, tak především u elektivních výkonů [9,22]. Limitací však může být nevhodná morfologie výdutí nebo nepřístupná anatomická lokalizace. Výhodou endovaskulární léčby je miniinvazivní přístup nezatěžující pacienta laparotomií s kratší dobou hospitalizace a rekonvalescence [24]. Z angio-intervenčních postupů připadají v úvahu embolizace spirálami, uzávěr tekutým embolizačním činidlem či trombinem nebo remodelace tepny s aneuryzmatem za pomocí stentgraftu. Volený výkon je závislý na lokalizaci výdutě a průchodnosti kolaterálního řečiště [24]. Tyto metody nabízejí jasnou výhodu oproti klasické chirurgické léčbě u pacientů po překonané nitrobřišní infekci, pankreatitidě nebo po opakovaných laparotomiích. Mezi komplikace endovaskulární léčby patří distální embolizace s rizikem střevní či jaterní ischemie nebo periprocedurální ruptura aneuryzmatu [24]. Obávanou komplikací endovaskulární léčby APDA je narušení kolaterálního toku do povodí TC s možností jaterní ischemie [20]. Vzhledem k velkým pohybovým exkurzím jsou raritně popsány i dislokace spirál a stentgraftu z viscerálních tepen do retroperitonea [25].
V chirurgické léčbě se může uplatnit prostá ligace, ligace s bypassem nebo aneuryzmorafie se zachováním toku v postižené tepně. První úspěšná resekce APDA byla publikována Van Ouwerkerkem v r. 1951 [26]. APDA jsou často lokalizovány za pankreatem nebo zasahují do jeho parenchymu a jejich peroperační detekce a ošetření může být složité. Byly publikovány případy, kdy si ošetření ruptury APDA vyžadovalo provedení duodenopankreatektomie [11]. Chirurgické metody nabízí dobré dlouhodobé výsledky, redukovanou potřebu dalšího sledování a relativně nízkou mortalitu elektivních výkonů [24].
Navzdory dokumentované kauzální souvislosti stenózy nebo okluze TC a vzniku APDA je v literatuře potřeba revaskularizace TC nebo uvolnění ligamentum arcuatum mediale na základě klinických zkušeností zpochybňována [16,27]. Léčba stenózy nebo okluze TC byla doporučena některými autory hlavně v prevenci rekurence nebo ruptury APDA [10,28]. Brockerem [22] vyhodnocený soubor 93 pacientů s pravým APDA a stenózou nebo okluzí TC patří mezi největší. K ošetření TC došlo v tomto souboru jen u 21 % léčených a při sledování pacientů s neošetřenou stenózou TC nebyla pozorována rekurence APDA [22]. Podobnou zkušenost na menších souborech publikovalo několik dalších autorů [16,27,29]. Sgroi [16] uvádí teorii, že k aneuryzmatické dilataci zde dochází v počátcích rozvoje kolaterální cirkulace a vznik nových aneuryzmat je po jejím plném rozvinutí málo pravděpodobný [16]. Vzhledem k provedenému přehledu literatury Brocker [22] navrhl, že léčba současné stenózy nebo okluze TC by neměla být založena na teoretické možnosti rekurence APDA, ale raději na potřebě intervence k předejití ischemie v povodí TC [22]. Z indikací uvádí případy, kdy je angiografický nález znepokojivý stran možné jaterní nebo duodenální ischemie, dále u pacientů s ischemickými symptomy po prvotní definitivní léčbě APDA nebo u pacientů s přetrvávající vstupní symptomatologií [22]. Jinou zkušenost má Yamana [28], který popisuje případ pacientky s rupturou vícečetných APDA spojených se stenózou TC při MALS. Pacientka byla úspěšně léčena embolizací, ale kontrolní CTA měsíc po intervenci odhalilo rapidní expanzi zbylých APDA. Následná chirurgická revaskularizace v povodí TC vedla k regresi velikosti těchto aneuryzmat [28]. U jiných autorů vedla samotná dekomprese nebo revaskularizace TC ke kompletní angiografické regresi nebo trombóze jinak neošetřené APDA [29,30]. Ojedinělý je popis dvou případů, kdy po úspěšné endovaskulární léčbě ruptur APDA při stenóze TC s MALS došlo během několika dní k rychlému rozvoji aneuryzmat v jiné části povodí pankreatikoduodenální arkády [31]. Pro algickou symptomatologii byla nutná jejich embolizace, nicméně k ošetření stenózy TC nebo MALS autoři nepřistoupili [31].
Stenózu nebo okluzi TC je s ohledem na její etiologii možné řešit několika způsoby. U aterosklerotické stenózy je možné endovaskulární řešení pomocí balon expandibilního stentu [32]. Při selhání endovaskulární intervence je možná chirurgická revaskularizace bypassem z aorty na TC nebo arteria hepatica communis. Při MALS přichází v úvahu otevřené, laparoskopické nebo robotické uvolnění ligamentum arcuatum mediale [33]. Pokud nedojde po chirurgické deliberaci ligamenta k rozšíření stenózy TC, následuje endovaskulární dilatace pomocí balonku či stentu. Samotná endovaskulární dilatace a zavedení stentu při MALS bez chirurgické léčby je kontraindikována vzhledem k riziku zevní komprese až možnosti fraktury stentu s jeho následným uzávěrem [13].
ZÁVĚR
Aneuryzmata pankreatikoduodenální arkády jsou raritní výdutě. Typicky vznikají při změně cirkulačních poměrů při stenóze nebo uzávěru truncus coeliacus. Výdutě v tomto povodí by měly být ošetřeny časně po stanovení diagnózy, protože není korelace mezi jejich velikostí a rizikem ruptury. V léčbě se preferuje primárně endovaskulární přístup. Otázka revaskularizace stenózy nebo okluze truncus coeliacus je nadále diskutována.
Seznam zkratek:
AMS – arteria mesenterica superior
APDA – aneuryzma pankreatikoduodenální arkády
BMI – body mass index
CTA – CT angiografie
TC – truncus coeliacus
MALS – median arcuate ligament syndrome
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Alexander Hudák, PhD.
Chirurgická klinika FNHK a LF UK
Fakultní nemocnice Hradec Králové
Sokolská 581
500 05 Hradec Králové
e-mail: alexander.hudak@fnhk.cz
ORCID ID: 0000-0001-5372-4094
Sources
1. Johnston KW, Rutherford RB, Tilson MD, et al. Suggested standards for reporting on arterial aneurysms. Subcommittee on Reporting Standards for Arterial Aneurysms, Ad Hoc Committee on Reporting Standards, Society for Vascular Surgery and North American Chapter, International Society for Cardiovascular Surgery. J Vasc Surg. 1991;13(3):452−458. doi: S0741521491000794.
2. Stanley JC, Wakefield TW, Graham LM, et al. Clinical importance and management of splanchnic artery aneurysms. J Vasc Surg. 1986;3(5):836−840. doi: 0741 - 5214(86)90059-5.
3. Ferguson F. Aneurysm of superior pancreaticoduodenal artery. Proc N Y Pathol Soc. 1895;24(45):9.
4. Sugiyama K, Takehara Y. Analysis of five cases of splanchnic artery aneurysm associated with coeliac artery stenosis due to compression by the median arcuate ligament. Clin Radiol. 2007;62(7):688−693. doi: 10.1016/j.crad.2007.02.002.
5. Kadir S, Athanasoulis CA, Yune HY, et al. Aneurysms of the pancreaticoduodenal arteries in association with celiac axis occlusion. Cardiovasc Radiol. 1978;1(3):173−177. doi: 10.1007/ bf02552029.
6. Sutton D, Lawton G. Coeliac stenosis or occlusion with aneurysm of the collateral supply. Clin Radiol. 1973;24(1):49−53. doi: 10.1016/s0009-9260(73)80114-x.
7. Ogino H, Sato Y, Banno T, et al. Embolization in a patient with ruptured anterior inferior pancreaticoduodenal arterial aneurysm with median arcuate ligament syndrome. Cardiovasc Intervent Radiol. 2002;25(4):318−319. doi: 10.1007/ s00270-001-0109-4.
8. Suzuki K, Kashimura H, Sato M, et al. Pancreaticoduodenal artery aneurysms associated with celiac axis stenosis due to compression by median arcuate ligament and celiac plexus. J Gastroenterol. 1998;33(3):434−438. doi: 10.1007/ s005350050109.
9. Kalva SP, Athanasoulis CA, Greenfield AJ, et al. Inferior pancreaticoduodenal artery aneurysms in association with celiac axis stenosis or occlusion. Eur J Vasc Endovasc Surg. 2007;33(6):670−675. doi: 10.1016/j. ejvs.2006.12.021.
10. Ducasse E, Roy F, Chevalier J, et al. Aneurysm of the pancreaticoduodenal arteries with a celiac trunk lesion: current management. J Vasc Surg. 2004;39(4):906−911. doi: 10.1016/j. jvs.2003.09.049.
11. de Perrot M, Berney T, Deleaval J, et al. Management of true aneurysms of the pancreaticoduodenal arteries. Ann Surg. 1999;229(3):416−420. doi: 10.1097/00000658-199903000-00016.
12. Moore E, Matthews MR, Minion DJ, et al. Surgical management of peripancreatic arterial aneurysms. J Vasc Surg. 2004;40(2):247−253. doi: 10.1016/j. jvs.2004.03.045.
13. Bjorck M, Koelemay M, Acosta S, et al. Editor‘ s choice − management of the diseases of mesenteric arteries and veins: Clinical Practice Guidelines of the European Society of Vascular Surgery (ESVS). Eur J Vasc Endovasc Surg. 2017;53(4):460−510. doi: 10.1016/j.ejvs.2017.01.010.
14. Mano Y, Takehara Y, Sakaguchi T, et al. Hemodynamic assessment of celiaco-mesenteric anastomosis in patients with pancreaticoduodenal artery aneurysm concomitant with celiac artery occlusion using flow-sensitive four-dimensional magnetic resonance imaging. Eur J Vasc Endovasc Surg. 2013;46(3):321−328. doi: 10.1016/j.ejvs.2013.06.011.
15. Heo S, Kim HJ, Kim B, et al. Clinical impact of collateral circulation in patients with median arcuate ligament syndrome. Diagn Interv Radiol. 2018 Jul;24(4):181−186. doi: 10.5152/dir.2018.17514.
16. Sgroi MD, Kabutey NK, Krishnam M, et al. Pancreaticoduodenal artery aneurysms secondary to median arcuate ligament syndrome may not need celiac artery revascularization or ligament release. Ann Vasc Surg. 2015;29(1):122 e1−7. doi: 10.1016/j.avsg.2014.05.020.
17. Reuter SR, Bernstein EF. The anatomic basis for respiratory variation in median arcuate ligament compression of the celiac artery. Surgery 1973;73(3):381−385. doi:0039-6060(73)90305-X.
18. Jimenez JC, Harlander-Locke M, Dutson EP. Open and laparoscopic treatment of median arcuate ligament syndrome. J Vasc Surg. 2012;56(3):869−873. doi: 10.1016/j.jvs.2012.04.057.
19. Chiou AC, Josephs LG, Menzoian JO. Inferior pancreaticoduodenal artery aneurysm: report of a case and review of the literature. J Vasc Surg. 1993;17(4):784−789. doi: 10.1067/mva.1993.40412.
20. Katsura M, Gushimiyagi M, Takara H, et al. True aneurysm of the pancreaticoduodenal arteries: a single institution experience. J Gastrointest Surg. 2010;14(9):1409−1413. doi: 10.1007/ s11605-010-1257-0.
21. Gangahar DM, Carveth SW, Reese HE, et al. True aneurysm of the pancreaticoduodenal artery: a case report and review of the literature. J Vasc Surg. 1985;2(5):741−742. doi: 0741-5214(85)90049-7.
22. Brocker JA, Maher JL, Smith RW. True pancreaticoduodenal aneurysms with celiac stenosis or occlusion. Am J Surg. 2012;204(5):762−768. doi: 10.1016/j.amjsurg. 2012.03.001.
23. Obara H, Kentaro M, Inoue M, et al. Current management strategies for visceral artery aneurysms: an overview. Surg Today 2020;50(1):38−49. doi: 10.1007/ s00595-019-01898-3.
24. Cordova AC, Sumpio BE. Visceral artery aneurysms and pseudoaneurysms - should they all be managed by endovascular techniques? Ann Vasc Dis. 2013;6(4):687−693. doi: 10.3400/avd. ra.13-00045.
25. Skipworth JR, Morkane C, Raptis DA, et al. Coil migration − a rare complication of endovascular exclusion of visceral artery pseudoaneurysms and aneurysms. Ann R Coll Surg Engl. 2011;93(4):e19−23. doi: 10.1308/003588411X13008844298652.
26. van Ouwerkerk L. Aneurysm of the arteria pancreatico-duodenalis. Arch Chir Neerl. 1951;3(1):11−7.
27. Boll JM, Sharp KW, Garrard CL, et al. Does management of true aneurysms of peripancreatic arteries require repair of associated celiac artery stenosis? J Am Coll Surg. 2017;224(2):199−203. doi: 10.1016/j.jamcollsurg.2016.10.030.
28. Yamana F, Ohata T, Kitahara M, et al. Blood flow modification might prevent secondary rupture of multiple pancreaticoduodenal artery arcade aneurysms associated with celiac axis stenosis. J Vasc Surg Cases Innov Tech. 2020;6(1):41−45. doi: 10.1016/j.jvscit.2019.10.005.
29. Flood K, Nicholson AA. Inferior pancreaticoduodenal artery aneurysms associated with occlusive lesions of the celiac axis: diagnosis, treatment options, outcomes, and review of the literature. Cardiovasc Intervent Radiol. 2013;36(3):578−587. doi: 10.1007/s00270-012-0473-2.
30. Nagano N, Takeuchi Y, Gomi A, et al. A case report of multiple aneurysms of pancreaticoduodenal region with celiac obstruction. [In Japanese] Nihon Geka Gakkai Zasshi. 1997;98(11):968−971.
31. Hasegawa T, Seiji K, Ota H, et al. Rapid development of new aneurysms in the adjacent pancreatic arcade arteries after urgent embolization of pancreaticoduodenal artery aneurysms in cases with celiac stenosis. J Vasc Interv Radiol. 2018;29(9):1306−8 e2. doi: 10.1016/j. jvir.2018.04.003.
32. Tien YW, Kao HL, Wang HP. Celiac artery stenting: a new strategy for patients with pancreaticoduodenal artery aneurysm associated with stenosis of the celiac artery. J Gastroenterol. 2004;39(1):81−85. doi: 10.1007/s00535-003-1251-3.
33. Fernstrum C, Pryor M, Wright GP, et al. Robotic surgery for median arcuate ligament syndrome. JSLS 2020;24(2). doi: 10.4293/JSLS.2020.00014.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2021 Issue 6-
All articles in this issue
- Chirurgie prsu – důležitá součást onkochirurgie
- První zkušenosti s použitím jódových zrn pro lokalizaci nehmatných lézí v mamární chirurgii
- Mukokéla apendixu z perspektivy radiologa
- Význam chirurgické biopsie sentinelové uzliny u pacientek s karcinomem prsu po neoadjuvantní chemoterapii: prospektivní multicentrická studie
- Komentář k článku: Žatecký J., et al. Význam chirurgické biopsie sentinelové uzliny u pacientek s karcinomem prsu po neoadjuvantní chemoterapii: prospektivní multicentrická studie
- Předoperační CT pro plánování pooperační radioterapie karcinomu prsu
- Komentář k článku A. Hlávky a kol. Předoperační CT pro plánování pooperační radioterapie karcinomu prsu
- Úloha radiologa při neoadjuvantní systémové terapii karcinomu prsu
- Fyloidní tumor a jeho malignizace v invazivní duktální karcinom prsu − kazuistika
- Aneuryzma pankreatikoduodenální arkády při syndromu ligamentum arcuatum mediale – kazuistika a přehled literatury
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- První zkušenosti s použitím jódových zrn pro lokalizaci nehmatných lézí v mamární chirurgii
- Mukokéla apendixu z perspektivy radiologa
- Fyloidní tumor a jeho malignizace v invazivní duktální karcinom prsu − kazuistika
- Aneuryzma pankreatikoduodenální arkády při syndromu ligamentum arcuatum mediale – kazuistika a přehled literatury
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

