-
Medical journals
- Career
Mukokéla apendixu z perspektivy radiologa
Authors: V. Válek jr. 1; D. Bartušek 1; M. Svoboda 2; V. Válek 1; V. Procházka 2
Authors‘ workplace: Klinika radiologie a nukleární medicíny Lékařské fakulty Masarykovy Univerzity, Fakultní nemocnice Brno 1; Chirurgická klinika Lékařské fakulty Masarykovy Univerzity, Fakultní nemocnice Brno 2
Published in: Rozhl. Chir., 2021, roč. 100, č. 6, s. 266-270.
Category: Review
doi: https://doi.org/10.33699/PIS.2021.100.6.266–270Overview
Mukokéla apendixu je obstrukční dilatace apendixu, která vzniká v důsledku vyplnění jeho lumen hlenem. Jedná se o vzácný stav, který je u poloviny pacientů asymptomatický. Jeho závažnost závisí na příčině vzniku dilatace apendixu. V malém procentu případů dochází k ruptuře dilatovaného apendixu s rozvojem závažné komplikace, která se označuje jako pseudomyxom peritonea. Protože část mukokél vzniká na maligním podkladě, je tento stav většinou řešen chirurgickou resekcí.
Klíčová slova:
mukokéla apendixu − pseudomyxom peritonea − apendikální mucinózní neoplazie – ultrasonografie − výpočetní tomografie
ÚVOD
Mukokéla apendixu je popisný termín pro označení dilatace apendixu. Ta vzniká v důsledku akumulace hlenu v lumen apendixu [1]. Jedná se o vzácné onemocnění. Jeho incidence je udávána v několika studiích kolem 0,2−0,7 % ze všech apendektomií. Onemocnění se vyskytuje většinou ve věku nad 50 let a relativně častěji u žen [2–4]. I v souvislosti s poměrně raritním výskytem se na mukokélu zapomíná a bývá často zaměněna za prostou apendicitidu [5]. Vzhledem k potenciálně maligní etiologii tohoto stavu je včasné rozpoznání pro osud pacienta zásadní.
Jednou ze složek epitelu sliznice apendixu jsou pohárkové buňky. Ty jsou součástí epitelu jak tlustého, tak tenkého střeva. Kromě toho se vyskytují například v epitelu dýchacích cest. Tyto buňky vytvářejí hlen, který má ve střevě a respiračním traktu především roli protektivní [6].
Etiologie a klasifikace
Příčiny vzniku mukokély apendixu lze rozdělit do dvou hlavních skupin. U skupiny neoplastických dochází v různé míře ke strukturálním změnám střevní stěny. Tyto se u nonneoplastických nevyskytují [3].
Do skupiny nonneoplastických mukokél je řazena prostá retenční cysta. Ta vzniká hromaděním hlenu v důsledku obstrukce lumen apendixu například fekolitem či při endometrióze [7]. Klasifikace neoplastických tzv. apendikálních mucinózních neoplazií prodělala v minulosti řadu změn. V současnosti jsou rozlišovány adenomy a přisedlé polypy, které dle dřívější klasifikace odpovídaly skupině hyperplastických polypů a slizniční hyperplazii. Dochází u nich ke strukturálním změnám postihujícím pouze povrchové vrstvy sliznice (nezasahují do muscularis mucosae). Další skupinou jsou low-grade a high-grade apendikální mucinózní neoplazie (LAMN, respektive HAMN). Ty patří k vůbec nejčastějším z apendikálních mucinózních neoplazií a tvoří přibližně 60 % mukokél apendixu [4]. Na rozdíl od předchozích u nich již dochází k dysplastickým změnám. Rovněž jsou patrné změny postihující hlubší vrstvy střevní stěny (submukózu a muscularis propria). Oproti adenomům může docházet k pronikání hlenu do stěny a případné penetraci mimo apendix [8]. V případě infiltrativní invaze buněk hovoříme již o mucinózním adenokarcinomu (Tab. 1). Tvoří přibližně 40 % ze všech adenokarcinomů apendixu [7,8].
Table 1. Histologická klasifikace mukokély apendixu
Tab. 1: Appendiceal mucocele histological classification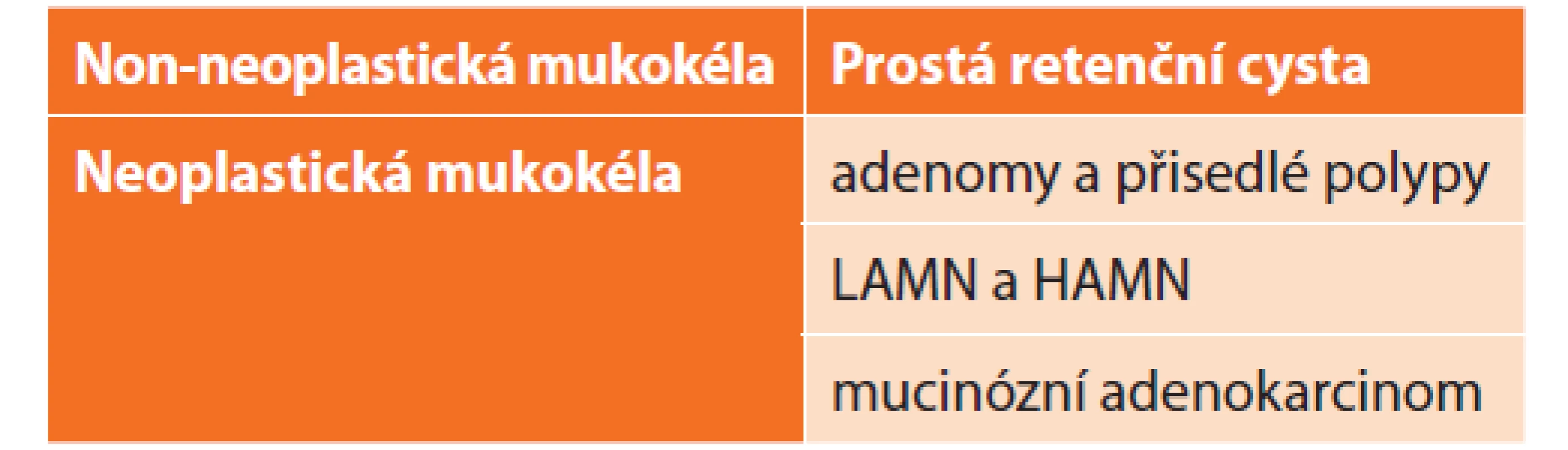
LAMN – low-grade apendikální mucinózní neoplázie;
HAMN – high-grade apendikální mucinózní neoplázieKlinický obraz u pacientů bývá nespecifický a často jsou pacienti v počátečních stadiích onemocnění asymptomatičtí. Z nejčastějších příznaků jsou uváděny bolesti v pravém hypogastriu, gastrointestinální krvácení (na podkladě intususcepce postiženého úseku střeva), obstrukce střeva či močovodu u větších mukokél [5,7].
Zvláště závažnou komplikací je ruptura apendixu s únikem hlenovitého obsahu do peritoneální dutiny. Závažným důsledkem tohoto stavu může být v další době rozvoj pseudomyxomu peritonea. Jsou-li součástí hlenu i epiteliální buňky střeva, mohou implantovat na peritoneu a pokračovat v produkci hlenu [9]. Jedná se o komplikaci, která vzniká přibližně u 10–20 % všech apendikálních mucinózních neoplazií [10]. Podle toho, zda je příčinou benigní mucinózní neoplazie, nebo mucinózní adenokarcinom rozlišujeme dvě formy – diseminovaná peritoneální adenomucinóza a peritoneální mucinózní karcinomatóza [8,10]. Příčinou vzniku mohou být i mucinózní neoplazie jiných orgánů, například ovaria [11].
Diagnostika
Mukokéla apendixu je často náhodný nález u pacientů s bolestí břicha při podezření na akutní apendicitidu. V takovém případě je zobrazovací metodou volby ultrasonografie (UZ) [2]. Typickým nálezem na UZ je cysticky dilatovaný útvar v pravém hypogastriu (Obr. 1, 2). Důležitý je průkaz jeho návaznosti na cékum. Hlen v lumen apendixu bývá uložen ve vrstvách. Vzniká tak obraz echogenních linií. Tento patognomický znak se označuje „onion skin sign“ [7]. Dalším znakem je přítomnost výrazně echogenních pruhů ve stěně útvaru, které odpovídají nástěnným kalcifikacím. Za nimi může být patrný hypoechogenní pruh v rámci dorzálního akustického zeslabení. V neposlední řadě nám může v diferenciální diagnostice pomoci i šíře samotného útvaru. Zatímco jako hraniční šíře u akutní apendicitidy bývá udávána hodnota 6−7 mm, u mukokély bývá udávána šíře přes 15 mm (senzitivita 83 %, specificita 92 %) [3].
Image 1. UZ obraz mukokély apendixu – transverzálně
Sonografie břicha. V oblasti céka tubulární, převážně anechogenní útvar, který je částečně vyplněn echogenním obsahem (červené šipky). Klinika radiologie a nukleární medicíny FN Brno a LF MU.
Fig. 1: Ultrasound image of appendiceal mucocele – transverse projection
Sonography of the abdomen. A tubular, mostly anechogenic formation is present in the area of the cecum, which is partially filled with echogenic content (red arrows). Department of Radiology and Nuclear Medicine, University Hospital Brno, Faculty of Medicine, Masaryk University.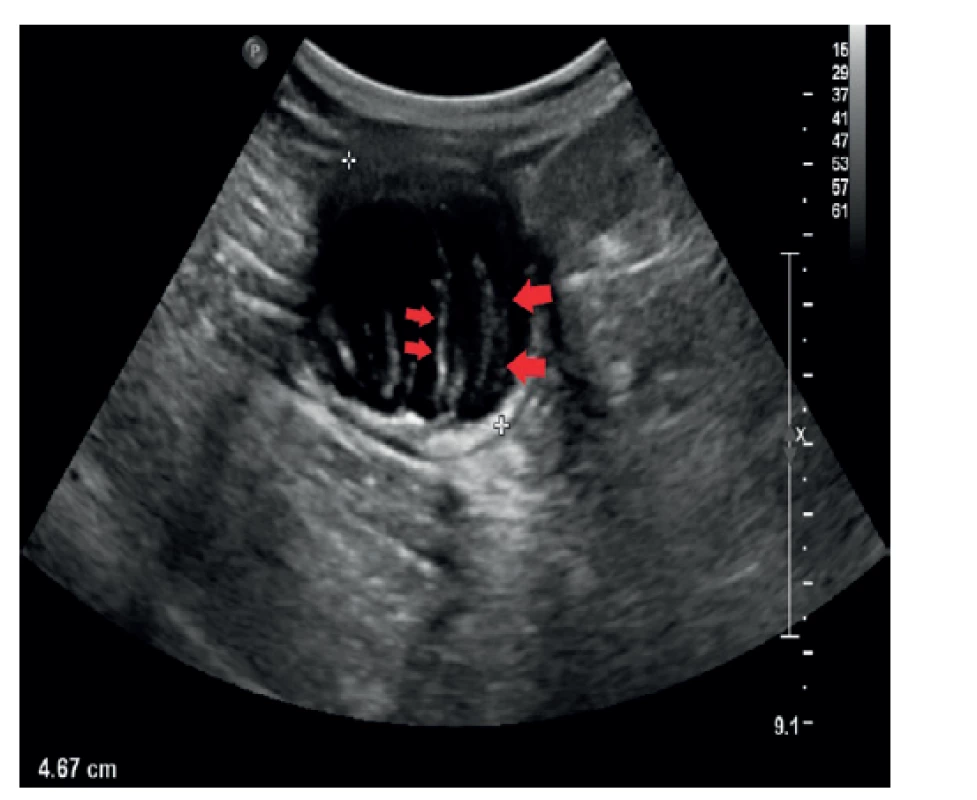
Image 2. UZ obraz mukokély apendixu – longitudinálně
Sonografie břicha stejného pacienta. V oblasti céka tubulární, převážně anechogenní útvar, který je částečně vyplněn echogenním obsahem (červené šipky). V dorzální části stěny patrné echogenní kalcifikace (žluté šipky). Klinika radiologie a nukleární medicíny FN Brno a LF MU.
Fig. 2: Ultrasound image of appendiceal mucocele – longitudinal projection
Sonography of the abdomen of the same patient. A tubular, mostly anechogenic formation is present in the area of the cecum, which is partially filled with echogenic content (red arrows). Echogenic calcifications (yellow arows) are visible in the dorsal part of the wall. Department of Radiology and Nuclear Medicine, University Hospital Brno, Faculty of Medicine, Masaryk University.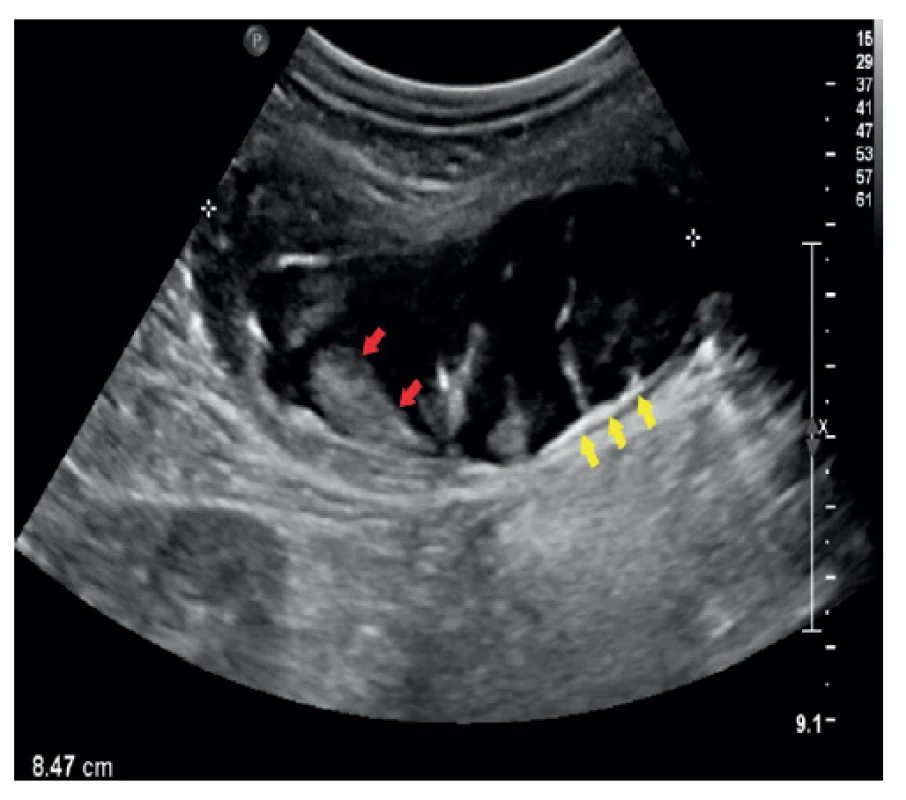
Často je tento stav ozřejmen až pomocí výpočetní tomografie (CT) [2]. Známky jsou podobné jako na UZ. V pravém hypogastriu je patrná objemnější hypodenzní formace s návazností na cékum (Obr. 3, 4). Charakteristickou známkou jsou nástěnné kalcifikace tečkovitého či zakřiveného tvaru [4,7]. Na CT jsou však čitelné v méně než 50 % případů [5,12]. Výhodou CT je možnost posouzení případných komplikací. Tou nejzávažnější je pseudomyxom peritonea. Může vzniknout spontánní rupturou apendixu nebo iatrogenně během operace [7,10]. Vyskytuje se u neoplastických variant mukokél, tedy LAMN, HAMN a adenokarcinomu [4,9]. Z toho důvodu má včasná diagnostika mukokély velký význam. CT umožní nejen posouzení bezprostředního okolí apendixu, ale umožní přehlédnutí celé peritoneální dutiny. Takto je možné posoudit rupturu apendixu s rozsevem hlenu v peritoneální dutině a zhodnotit rozsah postižení [9,10]. Existují znaky, které se častěji vyskytují u maligních forem mucinózních neoplazií, především nepravidelnosti stěny a měkkotkáňová expanze [13]. Průměr léze nad 2 cm je známkou neoplastické etiologie mukokély apendixu [12]. CT však nedokáže rozlišit jednotlivé typy apendikálních mucinózních neoplazií, které mohou být příčinou mukokély apendixu [5].
Image 3. CT obraz mukokély apendixu – axiální rovina
CT břicha s podáním kontrastní látky intravenózně, porto- -venózní fáze, stejný pacient. V oblasti céka je patrný tubulární útvar s hypodenzním obsahem (modrá hvězda). Jeho stěna je nepravidelně kalcifikovaná (žluté šipky). Klinika radiologie a nukleární medicíny FN Brno a LF MU.
Fig. 3: CT (computed tomography) scan of appendiceal mucocele – axial plane
CT of the abdomen with intravenous contrast, porto-venous phase, the same patient. A tubular formation with hypodense content is present in the area of the cecum (blue star). Its wall is irregularly calcified (yellow arrows). Department of Radiology and Nuclear Medicine, University Hospital Brno, Faculty of Medicine, Masaryk University.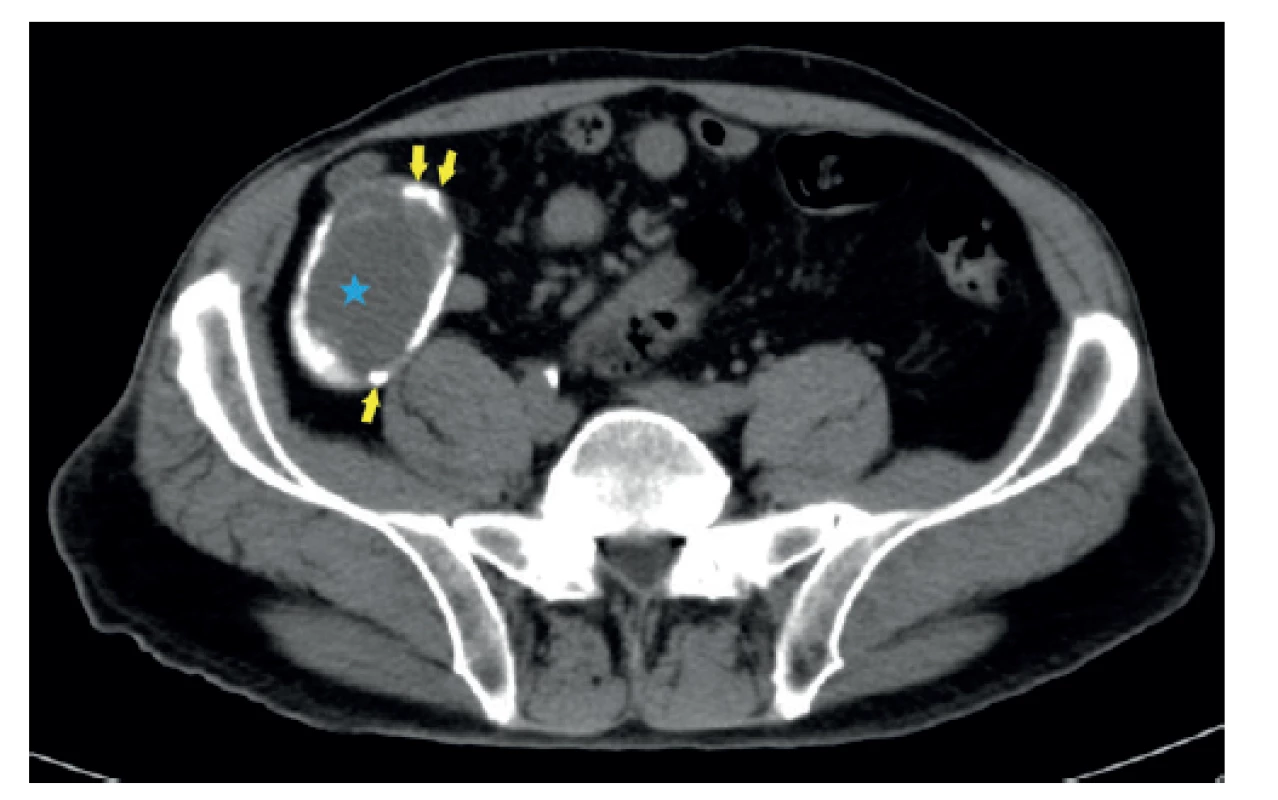
Image 4. CT obraz mukokély apendixu – koronální rovina
CT břicha s podáním kontrastní látky intravenózně, porto- -venózní fáze, stejný pacient. V oblasti céka je patrný tubulární útvar s hypodenzním obsahem (modrá hvězda). Jeho stěna je nepravidelně kalcifikovaná (žluté šipky). Klinika radiologie a nukleární medicíny FN Brno a LF MU.
Fig. 4: CT scan of appendiceal mucocele – coronal plane
CT of the abdomen with intravenous contrast, porto-venous phase, the same patient. A tubular formation with hypodense content is present in the area of the cecum (blue star). Its wall is irregularly calcified (yellow arrows). Department of Radiology and Nuclear Medicine, University Hospital Brno, Faculty of Medicine, Masaryk University.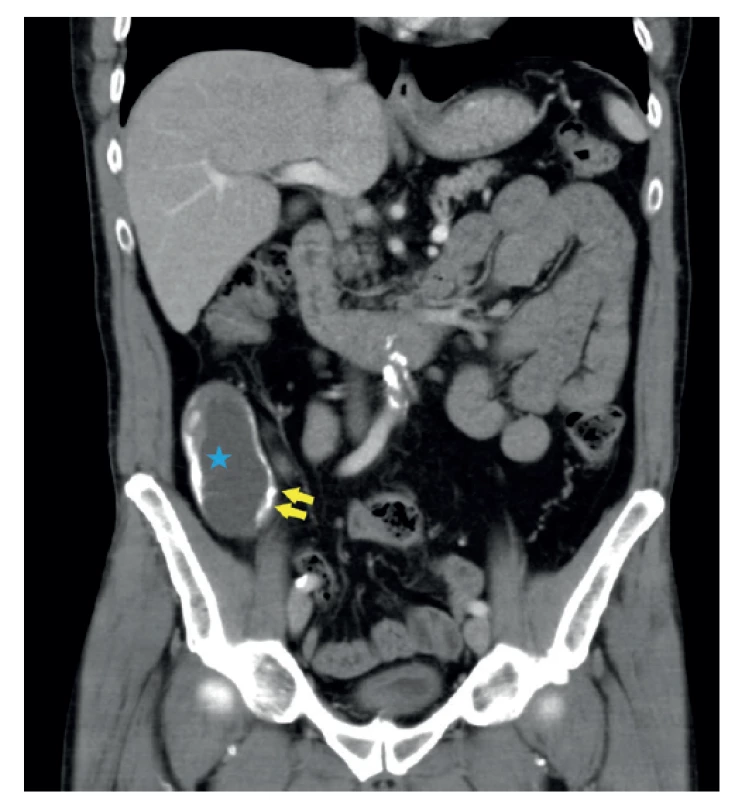
Na magnetické rezonanci (MRI) je mukokéla na T1 vážených obrazech hypointezivní či izointenzivní, podle koncentrace hlenu v lumen. Na T2 vážených obrazech je obsah hyperintenzivní [3,4,14].
Výjimečně lze mukokélu pozorovat na prostém snímku, jsou-li přítomny kalcifikace v její stěně (Obr. 5). Obrazem takového stavu je například oválný či okrouhlý kalcifikovaný útvar v oblasti pravého hypogastria [12]. Využití hybridních metod, jako je PET/CT (s radiofarmakem FDG), není vhodné vzhledem k velkému množství hlenovitého obsahu apendixu u mucinózních neoplazií [7].
Image 5. Prostý snímek břicha vstoje
Prostý snímek břicha. V sumaci s pravou lopatou kyčelní kosti kulovitý kalcifikovaný útvar (žluté šipky). Klinika radiologie a nukleární medicíny FN Brno a LF MU.
Fig. 5: Plain erect abdominal radiograph
Abdominal radiograph. A spherical calcified formation is present in the summation with the right wing of ilium (yellow arrows). Department of Radiology and Nuclear Medicine, University Hospital Brno, Faculty of Medicine, Masaryk University.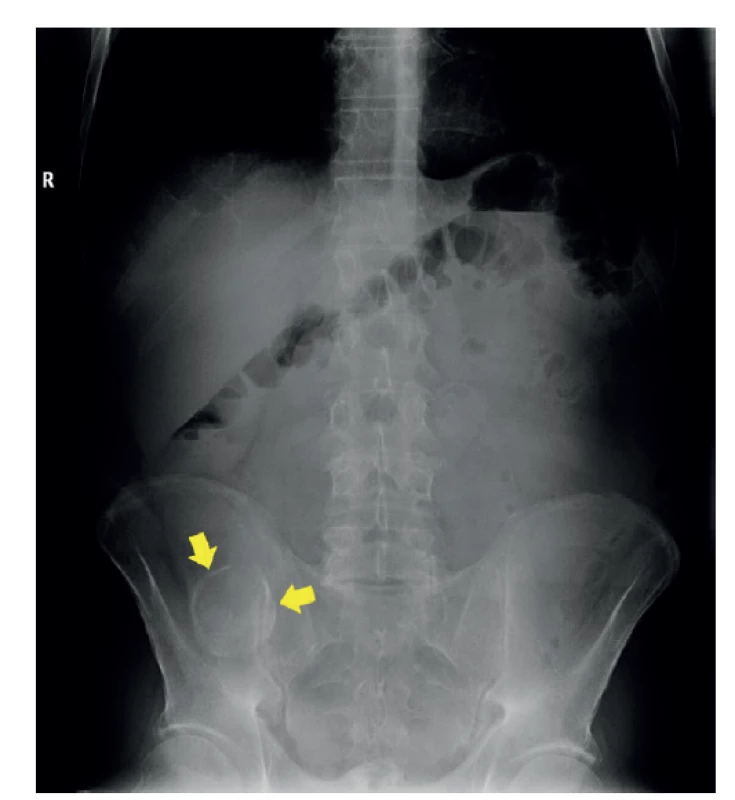
V závislosti na etiologii mukokély apendixu dochází u pacientů i k alteraci laboratorních hodnot (anémie, hodnoty onkomarkerů), nejsou však příliš specifické [5,7]. V diferenciální diagnostice benigní a maligní etiologie mukokély může pomoci i cytologická analýza hlenu [15]. Tenkojehlová biopsie se nedoporučuje pro riziko ruptury mukokély s možností peritoneálního rozsevu jejího obsahu [15,16]. K diagnostice lze využít i endoskopické metody [3]. Charakteristický obraz je popisován při kolonoskopii. V oblasti předpokládaného odstupu apendixu je patrná masa s centrálním kráterem, ze kterého vytéká hlenovitý materiál. Tento obraz je označován jako „volcano sign“ [3,7]. Nález mukokély může být náhodný při vyšetření v rámci screeningu kolorektálního karcinomu [7]. Kolorektální karcinom se vyskytuje přibližně u 20 % pacientů s mukokélou apendixu [5,7].
V diferenciální diagnostice kromě dalších expanzivních procesů v pravém hypogastriu je potřeba odlišit zejména akutní apendicitidu [5]. To je obtížné, zvláště dojde-li k infikování mukokély [12]. Při odlišení mukokély je důležitý především nález „onion skin sign“ a průměr apendixu nad 15 mm [3]. Dále je třeba myslet na cystické léze vaječníku a jiné gynekologické diagnózy (salpingitida, tuboovariální absces aj.). K rozlišení nám může pomoci absence jejich návaznosti na cékum. Dále je důležité odlišit tumorózní expanze jiné části střeva, především tumor céka [3,4,7]. Tumor céka může obturovat ústí apendixu, což může vést k hromadění hlenu v jeho lumen s dilatací a vzniká obraz mukokély [12].
Léčba
U většiny mukokél je volbou chirurgická léčba. Většinou je upřednostňována otevřená operace před laparoskopií, pro nižší riziko peroperační ruptury mukokély [12]. Její rozsah závisí jednak na etiologii mukokély, jednak na rozsahu nálezu [15]. U menších retenčních cyst či benigních neoplazií apendixu postačuje prostá apendektomie, respektive ileocekální resekce v případě, kdy není možné provedení prosté apendektomie [12]. V případě, že se histologicky jedná o LAMN či HAMN a resekční okraje jsou intaktní, postačuje prostá apendektomie [7].
Při objemnějších mukokélách s dilatací apendixu nad 2 cm, postižením zasahujícím bázi apendixu, postižením uzlin a zejména v případě mucinózního adenokarcinomu je indikována pravostranná hemikolektomie, a to z důvodu adekvátní radikality resekce. Ileocekální resekce je v dnešní době vyhrazena pro benigní nálezy nebo, jak již bylo zmíněno výše, v případech, kdy není možné provedení prosté apendektomie a definitivní histologie je příznivá [12,15]. V případě perforované mukokély je zapotřebí přehlédnutí peritoneální dutiny k vyloučení rozsevu mucinu. Na základě etiologie mukokély, cytologie ascitu a rozsahu postižení je u pseudomyxomu peritonea volbou intraperitoneální chemoterapie případně v kombinaci s cytoreduktivní chirurgií [10,15].
Vzhledem k tomu, že výskyt adenokarcinomu apendixu je velice vzácný, dle National Comprehensive Cancer Network (NCCN) z roku 2021 neexistují guidelines pro adjuvantní léčbu. V závislosti na stadiu onemocnění tak NCCN doporučuje v adjuvantní terapii adenokarcinomu apendixu postupovat podle guidelines pro kolorektální karcinom [17].
Prognóza pacientů s LAMN je velmi dobrá. 91–100% šance na přežití 3 roky od stanovení diagnózy, respektive 79–86% šance na přežití 5 let [7]. U mucinózního adenokarcinomu je přežití pacientů ovlivněno větším množstvím faktorů (např. staging, grading aj.). U lokalizovaného onemocnění ve stadiu I je prognóza přežití 5 let 74,9 %, u špatně diferencovaného adenokarcinomu ve stadiu IV je prognóza 11,3 %. Prognóza přežití 10 let u pacientů s mucinózním adenokarcinomem a provedenou hemikolektomií je 65 %, u pacientů s apendektomií jen 37 % [7,13].
U pacientů po operaci má velký význam následné pečlivé sledování, které je realizováno nejčastěji cestou CT a MRI. Význam má především u těch, kde je zvýšené riziko rekurence. U adenomů a serátních polypů není zapotřebí po operaci další sledování, protože k rekurenci nedochází ani v případě jejich ruptury [7,18]. Na základě doporučení z literatury by pacienti s LAMN s hlenem mimo lumen apendixu měli být sledováni každých 6 měsíců až 2 roky pomocí zobrazovacích metod [7]. U LAMN a HAMN s metastatickým rozsevem je vhodné dle doporučení American Society of Colon and Rectal Surgeons (ASCRS) sledování cestou CT nebo MRI. U diseminované peritoneální adenomucinózy je vhodná kontrola 2 měsíce po operaci a následně ročně déle než 5 let. U peritoneální mucinózní karcinomatózy jsou kontroly vhodné každých 6 měsíců déle než 6 let [18].
Kromě zobrazovacích metod nám při sledování pacientů mohou pomoci rovněž onkomarkery. U apendikálních mucinózních neoplazií bývají zvýšené hodnoty CEA a CA 19-9 [5,7].
ZÁVĚR
Mukokéla apendixu je relativně vzácný stav, kterým se označuje dilatovaný apendix vyplněný hlenovitým materiálem. Vedle prostých retenčních cyst a adenomů je potřeba rozlišit především LAMN, HAMN a mucinózní adenokarcinom. Závažnou komplikací u těchto stavů je pseudomyxom peritonea. Nespecifický klinický obraz mukokély je jedním z důvodů její časté záměny za akutní apendicitidu. V diagnostice jsou využívány především UZ a CT. Při detekci charakteristických známek mukokély lze pomocí těchto metod vyslovit podezření na tento stav v diferenciální diagnostice bolestí břicha. To má vliv na další management pacienta. Pomocí zobrazovacích metod však není možné přesně rozlišit benigní či maligní etiologii mukokély. Podle rozsahu postižení a etiologie mukokély je léčebnou volbou chirurgická resekce.
Seznam zkratek:
LAMN – low-grade apendikální mucinózní neoplazie
HAMN – high-grade apendikální mucinózní neoplazie
UZ – ultrasonografie
CT – výpočetní tomografie
MRI – magnetická rezonance
PET/CT – pozitronová emisní tomografie a výpočetní tomografie (hybridní metoda)
FDG – 18F-fluordeoxyglukóza
ASCRS – American Society of Colon and Rectal Surgeons
NCCN – National Comprehensive Cancer Network
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Vlastimil Válek
Klinika radiologie a nukleární medicíny
FN Brno-Bohunice
Jihlavská 20 625 00 Brno
e-mail: Valek.Vlastimil2@fnbrno.cz
Sources
1. Louis TH, Felter DF. Mucocele of the appendix. Baylor University Medical Center Proceedings 2014;27(1):33–34. doi: 10.1080/08998280.2014.11929046.
2. Demetrashvili Z, Chkhaidze M, Khutsishvili K, et al. Mucocele of the appendix: Case report and review of literature. Int Surg. 2012;97(3):266–269. doi: 10.9738/CC139.1.
3. Sharma P, Soin P, Chugh M, et al. Dilated appendix: Is there more to it? Case report and brief review of literature with radiologic-pathological correlation. J Clin Imaging Sci. 2019;9(9). doi: 10.25259/ JCIS_105_18.
4. Motyčková I, Špriňar Z, Ungermann L, et al. Mukokéla apendixu. Ces Radiol. 2007;61(4):79–81.
5. Basak F, Hasbahceci M, Yucel M, et al. Does it matter if it is appendix mucocele instead of appendicitis? Case series and brief review of literature. J Can Res Ther. 2018;14(6):1355−1360. doi: 10.4103/0973-1482.183193.
6. Birchenough G, Johansson M, Gustafsson J, et al. New developments in goblet cell mucus secretion and function. Mucosal Immunol. 2015;8(4):712−719. doi: 10.1038/mi.2015.32.
7. Overman MJ, Compton CC, Raghav K, et al. Appendiceal mucinous lesions − Up - ToDate n.d. 2020. Available from: www. uptodate.com/contents/appendiceal - mucinous-lesions.
8. Ghosh A. Classification of mucinous appendiceal neoplasm and pseudomyxoma peritonei. Journal of Pathology of Nepal 2018;8(1):1301–307. doi: 10.3126/ jpn.v8i1.19458.
9. Bevan KE, Mohamed F, Moran BJ. Pseudomyxoma peritonei. World J Gastrointest Oncol. 2010;2(1):44–50. doi: 10.4251/ wjgo.v2.i1.44.
10. Žáčik M, Kacvinská T, Pernická B, et al. Pseudomyxom peritonea. Ces Radiol. 2011;65(4):266–271.
11. Psár R, Kala Z, Krátký J. Diferenciální diagnostika peritoneálních cystických lézí se zřetelem na pseudomyxom peritonea a echinokokovou cystu. Ces Radiol. 2017;71(1):74–78.
12. Tirumani SH, Fraser-Hill M, Auer R, et al. Mucinous neoplasms of the appendix: a current comprehensive clinicopathologic and imaging review. Cancer Imaging 2013;13(1):14–25. doi: 10.1102/1470 - 7330.2013.0003.
13. Wang H, Chen Y-Q, Wei R, et al. Appendiceal mucocele: A diagnostic dilemma in differentiating malignant from benign lesions with CT. American Journal of Roentgenology 2013;201(4):590–595. doi: 10.2214/AJR.12.9260.
14. Stark C, Jousi M, Enholm B. Preoperative assessment and treatment of appendiceal mucocele complicated by acute torsion: a case report. BMC Res Notes 2014;7(1):1. doi: 10.1186/1756 - 0500-7-1.
15. Abreu Filho JGD, Lira EFD. Mucocele of the appendix: appendectomy or colectomy? J. Coloproctol. (Rio J.) 2011;31(3):276–284. doi: 10.1590/S2237 - 93632011000300008.
16. Rabie ME, Al Shraim M, Al Skaini MS, et al. Mucus containing cystic lesions “mucocele” of the appendix: The unresolved issues. International Journal of Surgical Oncology 2015. doi: 10.1155/ 2015/139461.
17. National Comprehensive Cancer Network. Colon Cancer (Version 2.2021). Available from: www.nccn.org/professionals/ physician_gls/pdf/colon.pdf.
18. Glasgow SC, Gaertner W, Stewart D, et al. The American Society of Colon and Rectal Surgeons, Clinical practice guidelines for the management of appendiceal neoplasms. Diseases of the Colon & Rectum 2019;62(12):1425−1436. doi: 10.1097/ DCR.0000000000001530.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2021 Issue 6-
All articles in this issue
- Chirurgie prsu – důležitá součást onkochirurgie
- Iodine seed localisation of non-palpable lesions in breast surgery − first experience
- Appendiceal mucocele – a radiologist’s view
- The importance of sentinel lymph node biopsy following neoadjuvant chemotherapy in patients with breast cancer: prospective multicentre trial
- Komentář k článku: Žatecký J., et al. Význam chirurgické biopsie sentinelové uzliny u pacientek s karcinomem prsu po neoadjuvantní chemoterapii: prospektivní multicentrická studie
- Preoperative CT for postoperative radiotherapy planning in breast cancer
- Komentář k článku A. Hlávky a kol. Předoperační CT pro plánování pooperační radioterapie karcinomu prsu
- Role of the radiologist during neoadjuvant systemic therapy for breast cancer
- Phyllodes tumor and its malignization into invasive ductal carcinoma − a case report
- Aneurysm of pancreaticoduodenal arcade caused by medial arcuate ligament syndrome – case report and review of literature
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Iodine seed localisation of non-palpable lesions in breast surgery − first experience
- Appendiceal mucocele – a radiologist’s view
- Phyllodes tumor and its malignization into invasive ductal carcinoma − a case report
- Aneurysm of pancreaticoduodenal arcade caused by medial arcuate ligament syndrome – case report and review of literature
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

