-
Medical journals
- Career
Navigace v páteřní chirurgii založená na intraoperačním CT zobrazení: zkušenost s iniciálními 295 implantáty
Authors: P. Barsa 1; R. Fröhlich 1; F. Šebek 2; P. Suchomel 1
Authors‘ workplace: Neurochirurgické oddělení, Neurocentrum, Krajská nemocnice Liberec, a. s. primář: Prof. MUDr. P. Suchomel, Ph. D. 1; Radiologické oddělení, Krajská nemocnice Liberec, a. s., primář: MUDr. L. Endrych 2
Published in: Rozhl. Chir., 2014, roč. 93, č. 1, s. 16-20.
Category: Original articles
Overview
Úvod:
Práce popisuje metodiku spinální navigace založené na intraoperačním CT zobrazení a výsledky iniciální série pacientů.Materiál a metodika:
V období od listopadu 2012 do října 2013 bylo během 50 operací zavedeno za pomoci navigace celkem 295 šroubů, u nichž jsme hodnotili přesnost zavedení, intraoperační komplikace a dostupnost metody pro konkrétní páteřní etáž.Výsledky:
Z celkového množství 295 šroubů zavedených ve všech etážích páteře od C0 do S1 jsme nalezli 4 nepřesně zavedené pedikulární šrouby (1,3 %): šroub v L5 prořezával dolní kortikális pediklu, jeden šroub v obratlích Th 5 a Th 6 penetroval přední okraj obratlového těla v délce do 3 mm a pedikulární šroub v C3 penetroval horní krycí lištu těla. Žádná z těchto komplikací nebyla zdrojem morbidity a důvodem k reoperaci. Intraoperační CT společně s navigačním postupem znamenalo průměrně 30minutové prodloužení operačního času a iniciální zobrazení společně s kontrolou přesnosti zavedení představovaly vyšší radiační zátěž pro pacienta.Závěr:
Naše počáteční zkušenosti prokázaly, že spinální navigace založená na intraoperačním CT zobrazení je přesná metoda zavedení páteřních implantátů. Její užití znamená nižší chirurgickou morbiditu a vyšší bezpečnost pacienta. Tento benefit by měl vyvážit vyšší radiační expozici pacienta a delší operační čas.Klíčová slova:
páteřní operace – chirurgická technika – intraoperační zobrazení – výpočetní tomografie – navigaceÚVOD
Technologický rozvoj, který charakterizuje celou současnou epochu, zasahuje zcela přirozeně i do oblastí chirurgie. Přínosem spojeným se zaváděním nových technologií do praxe by měla být zvýšená bezpečnost, nižší výskyt komplikací a s tím spojený pokles sekundárních nákladů na léčbu. Další progres může vyústit v minimalizaci přístupu, vznik nových operačních taktik a finálně ve změnu paradigmatu s mnohem agresivnějším a přitom fyziologičtějším přístupem k chirurgické léčbě.
Na poli neurochirurgie se od 90. let minulého století objevují systémy bezrámové stereotaktické navigace (frameles stereotactic navigation systems) [1]. Jejich funkce spočívá v principu vysoce přesného sledování pohybu označených nástrojů v operačním poli. Známé výchozí body operačního pole (markery) jsou ještě před započetím výkonu registrovány proti identickým bodům zachyceným během předoperačního zobrazovacího vyšetření (nejčastěji MR) a takto konfirmovaný prostor operačního pole chirurg používá k prostorové orientaci uvnitř mozkových anatomických struktur, podobně jako je tomu při užití navigačních systémů v automobilové dopravě. Přestože je popsaný postup zatížen určitým stupněm nepřesnosti daným především pohyby mozkových struktur během retrakce a resekce mozkové tkáně (brain shift), metoda doznala širokého klinického uplatnění a stala se standardem v intrakraniální chirurgii [2].
V případě spinálních operací bylo užití identického principu složitější. Složitost spočívá v tom, že na rozdíl od intrakraniálních struktur, jejichž anatomické umístění je u konkrétního jedince relativně konstantní, vzájemné uspořádání jednotlivých obratlů se neustále mění. Interpretace anatomického uspořádání pohyblivé páteře, tak jak je zachytilo předoperační radiologické zobrazení, je s časovým odstupem prakticky nemožné. S výjimkou jednotlivých obratlů a nepohyblivých segmentů páteře (ankylóza) tak není možné registrovat anatomické úseky páteře způsobem, který by odpovídal předoperačnímu uspořádání. Následné operování by se stalo značně nebezpečným. I přes tato úskalí se navigační techniky začaly v páteřní chirurgii objevovat v 90. letech minulého století. Spinální navigační systém založený na optoelektronickém principu navrhl na základě laboratorních prací v roce 1995 Nolte et al. [3]. Jeho funkčnost a bezpečnost v klinické praxi popsal prostřednictvím srovnávací studie s fluoroskopicky vedenými operacemi o pět let později Laine et al. [4]. V průběhu uplynulých let se metodika navigovaných výkonů vyvíjela. Průlomem však je až recentní zavedení peroperační 3D fluoroskopie [5] a mnohem přesnějšího intraoperačního CT [6] jako výchozích zobrazení pro navigované spinální výkony. Intraoperační zobrazení zachytí úsek páteře v takovém anatomickém postavení, které bude chirurg instrumentovat. Takto by měla být zabezpečena přesnost a bezpečnost jednotlivých kroků. V následujícím sdělení autoři seznamují s klinickými zkušenostmi, které získali během navigovaných spinálních výkonů založených na intraoperačním CT zobrazení.
Materiál a metodika
Metodika
Pozice pacienta během navigovaných operačních výkonů se neliší od polohování pacienta během klasických fluoroskopicky vedených operací. Během rozmístění operační skupiny musí být zohledněna potřeba kontinuální kontroly operačního pole kamerou. Poloha operačního pole by současně měla být volena tak, aby vertikální osa instrumentovaného segmentu pokud možno korespondovala s osou „gantry“ mobilního CT skeneru (BodyTom™, Neurologica, Danvers, USA) (Obr. 1).
Image 1. CT skener těsně před sejmutím intraoperačního obrazu Fig. 1: The movable CT scanner just before taking the intraoperative scans 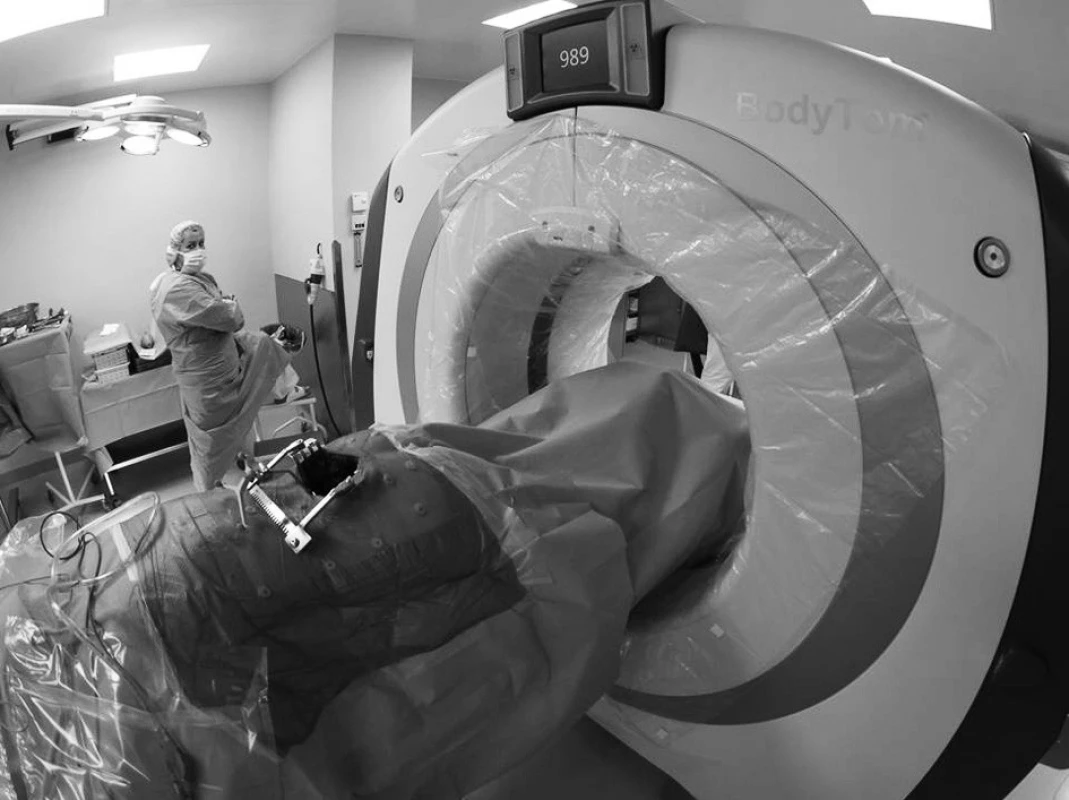
Do okolí středočárového kožního řezu umisťujeme 10 výchozích značek. Tyto plastové samolepicí terčíky dodává výrobce navigačního systému (Stealth™, Medtronic, Minneapolis, USA) a po dokončení skeletizace cílového úseku páteře slouží k registraci operačního pole. Dalšími prvky registrace operačního pole (konfirmace identických bodů operačního pole s body zobrazenými peroperačním CT) jsou: navigační rám Stealth připevněný k pevnému spinóznímu výběžku jednoho z instrumentovaných obratlů (Obr. 2) a případně identifikovatelné body kostěného povrchu obratlů. Pohyblivý celotělový 32vrstevný CT skener následně sejme obraz určeného úseku páteře včetně registračních prvků a ten je ve formátu DICOM automaticky odeslán do navigačního systému cestou ethernetového spojení. Pro účely páteřní navigace používáme helikální skeny o tloušťce vrstvy 1,4 mm. Obraz je do trojrozměrné podoby rekonstruován v navigačním systému Stealth, který v režimu zobrazení měkkých tkání vykreslí kožní povrch včetně výchozích značek. V režimu 3D zobrazení kalcifikovaných tkání potom identifikujeme povrchové struktury páteře. Do takto připraveného obrazu obratlů zanášíme virtuální trajektorie implantátů. Máme přitom možnost sledovat průběh trajektorie v sagitální, koronární i transverzální rovině a vedle toho nám navigační systém prostřednictvím programu „probe view“ dává možnost zobrazit průchod virtuálního implantátu kostní strukturou, podobně jako je tomu v případě endosonografického vyšetření. Tímto způsobem definujeme délku a průměr zamýšleného implantátu.
Image 2. Operační pole během registrace Plastové terčíky výchozích markerů umístěné na kůži v okolí rány a navigační rám Stealth připevněný k pevnému spinóznímu výběžku slouží k registraci, v ruce chirurga je potom navigovaná sonda. Fig. 2: The operating field during the registration Fiducial skin markers placed around the skin incision and the Stealth reference-frame tracking device attached onto the spinous process help to accurately match the computer reconstructed CT scans with the real surgical space; navigated pointer in the surgeon’s hand. 
Přesnou pozici navigačního rámu připevněného na spinózní výběžek jednoho z instrumentovaných obratlů, stejně jako okamžitou pozici všech navigovaných instrumentů snímá elektrooptická kamera. Tato kamera funguje jako poziční senzor, když sleduje pozici pasivních infračervených odrazek nebo infračervených světelných diod (LED) připevněných v definovaném seskupení na povrch nástrojů. Dotykem hrotu navigační sondy registrujeme všech deset výchozích značek připevněných na povrch kůže, případně známé body operačního pole. Další kroky při zavádění implantátů jsou vedeny v zaregistrovaném poli s tím, že pasivními reflektory nebo světelnými diodami můžeme vybavit nejen nejrůznější sondy, ale také vodič vrtačky nebo dláto.
Samotný postup instrumentace vede námi vytvořený plán navigace. Prvním krokem je vyhledání místa vstupu šroubu (entry point). Toto místo určíme prostřednictvím navigované sondy a na povrchu obratle je označíme kulovou frézou. Prohlubeň by měla být dostatečně veliká tak, aby poskytla oporu pro technický vrták, kterým trajektorii v určené délce a orientaci předvrtáme. Po vyvrtání cesty pro šroub buď předřezáváme do kosti závit, nebo přímo implantát zavádíme. V případě víceetážových instrumentací připevňujeme referenční rám ke spinóznímu výběžku co nejblíže středním partiím instrumentovaného úseku, zatímco instrumentaci začínáme od periferie (například při stabilizaci L3-L5 připevníme rám na L4 a nejprve instrumentujeme L3 a L5). Předcházíme tak eventuálnímu vychýlení referenčního rámu během implantace.
Po zavedení implantátů dokončíme dekompresní, případně rekonstrukční část operace a finálně fixujeme jednotlivé segmenty vnitřního fixatéru. Správnou pozici implantátů konfirmujeme ještě během výkonu prostřednictvím mobilního CT skeneru (Obr. 3).
Image 3. Příklad anatomicky správného zavedení pedikulárních šroubů v etáži druhého hrudního obratle Oba šrouby sledují osu pediklů a jejich hroty jsou umístěny subkortikálně. Fig. 3: Correct anatomical position of pedicle screws inserted into the second thoracic vertebra Both shafts follow the axis of the pedicle with subcortical position of the tips. 
Soubor pacientů
V průběhu prvních 11 měsíců přítomnosti mobilního CT skeneru na našem pracovišti (listopad 2012 až říjen 2013) byla technologie navigovaných spinálních výkonů založených na intraoperačním CT zobrazení užita u 49 pacientů, u kterých jsme během 50 operací zavedli 295 šroubů. Skupina operovaných sestávala z 25 mužů a 24 žen průměrného věku 56,3 roku (rozsah 25–79, medián 60 let). Poměrné zastoupení diagnóz, pro něž jsme navigovanou instrumentaci indikovali, koresponduje se spektrem chirurgických výkonů běžného neurochirurgického pracoviště s většinovým zastoupením pacientů operovaných pro degenerativní onemocnění v bederní oblasti. Přesné údaje o indikacích k operačnímu výkonu popisuje Graf 1 a anatomickou distribuci implantátů potom Graf 2.
Graph 1. Podíl jednotlivých diagnóz v odoperovaném souboru pacientů Graph 1: Proportion of diagnosis in the group of operated patients 
Graph 2. Anatomická distribuce implantátů Graph 2: Anatomical distribution of the implants 
VÝSLEDKY
Z celkového počtu 295 zavedených spinálních implantátů jsme nesprávné zavedení diagnostikovali u 4 šroubů (1,3 %). V jednom případě jsme zaznamenali penetraci závitů šroubu kaudální kortikális pediklu L5 (ověřeno pooperačně), v případě jednoho šroubu v hrudních segmentech Th5 a Th6 jsme CT kontrolou zjistili perforaci hrotu šroubu přes ventrální stěnu obratle do 3 mm a jeden z pedikulárních šroubů C3 penetroval horní krycí lištu obratlového těla. Nesprávná pozice obou hrudních šroubů byla upravena ještě před uzávěrem operační rány. V případě žádného ze zavedených šroubů nedošlo k poranění neurovaskulárních struktur nebo laceraci durálního vaku, korektní zavedení šroubů vyloučilo zlomení instrumentovaného pediklu a nebyly shledány klinické konsekvence, které by operatéra přiměly k reoperaci s optimalizací pozice implantátu.
Během navigovaných operací založených na intraoperačním CT obrazu jsme nezaznamenali případ, kdy by přehlednost operovaného úseku páteře byla narušena obezitou pacienta, hůře radiologicky vyšetřitelnou anatomickou lokalizací (C-Th přechod) nebo artefakty vzniklými v radiologickém stínu kovových nástrojů. Kvalita zobrazení anatomických struktur během pooperačních CT vyšetření nevedla k záměně operovaných segmentů.
Po dokončení registrace operačního pole propočítává navigační systém přesnost procesu registrace. Průměrná hodnota u námi operovaných pacientů činila 0,47 mm (rozsah 0,2–1,0 mm) a veškeré tyto kalkulované hodnoty byly dostatečné k tomu, abychom bezpečně vedli instrumentaci. Vyšší přesnosti bylo obecně dosahováno během větších rozměrů registrovaného pole.
Metoda navigovaného zavedení šroubů založeného na intraoperačním CT zobrazení byla použitelná ve všech anatomických etážích páteře a dosud jsme se nesetkali se situací, že bychom byli nuceni konvertovat navigovaný výkon v operaci fluoroskopicky vedenou. Průměr gentry přístroje BodyTom™ (80 cm) umožnil provést akvizici obrazu i u obézních nemocných a tento faktor zatím rovněž nebyl důvodem konverze. Poměrně velký úhlový rozptyl vyžaduje ve vybraných situacích změnu postavení kamery tak, aby byla schopna přesně sejmout pozici navigovaných nástrojů. Změna pozice kamery předpokládá spolupráci sálového personálu a představuje jen nepatrnou časovou prodlevu v řádu sekund.
S použitím navigace založené na intraoperačním CT zobrazení souvisí navýšení počtu operačních kroků. K novým operačním úkonům patří: pořízení iniciálního skenu, zpracování CT obrazu, plánování trajektorie a registrace operačního pole. Řádné provedení těchto kroků znamenalo v naší sestavě podle rozsahu instrumentované oblasti a složitosti anatomie 20–40minutové navýšení operačního času. S prodloužením operačního času souviselo prodloužení délky narkózy a prodloužení periody, po kterou byla otevřena (i když sterilně kryta) operační rána.
Použití navigace založené na intraoperačním CT zobrazení zcela eliminuje radiační zátěž personálu během zavádění šroubů, když se po dobu skenování operované oblasti chirurgický i anesteziologický tým pohybuje v oblasti mimo dosah rentgenového záření. Akvizice CT obrazu znamená vyšší radiační zátěž pro pacienta. Tato radiační zátěž je v našem souboru charakterizována průměrnými hodnotami CTDI vol 63,8 mGy a DLP 1660,3 mGy.cm (medián 65,6 mGy a 1619 mGy.cm).
DISKUZE
Navigovaná páteřní instrumentace se na sérii 295 zavedených implantátů ukázala být přesnou a bezpečnou metodou s chybovostí v případě 1,3 %. Jednalo se o iniciální sérii 50 konsekutivních operačních výkonů, kdy jsme se rozhodli prověřit funkčnost systému a odhalit případné nedostatky. Z tohoto pohledu byly veškeré kroky operací anatomicky kontrolovány chirurgem. V případě vůbec prvních pacientů jsme během zavádění implantátů z důvodů bezpečnosti použili také skiaskopickou kontrolu. Po získání pocitu bezpečnosti jsme spoléhali výlučně na virtuální realitu navigačního systému.
Snaha o maximální využití systému nás vedla k užití navigace i při instrumentaci bederních obratlů, tedy v situacích, kde bychom srovnatelných výsledků, měřeno přesností zavedení a klinickou bezpečností, dosáhli i za standardního skiaskopického vedení operace. Zvolený postup však výrazně přispěl k časnému získání klinických zkušeností týmu, které byly zúročeny v komplikovanějších oblastech horní krční páteře a u obratlů krčně-hrudního přechodu. Současně jsme během bederních stabilizací získali zkušenost s navigací instrumentů velkého úhlového rozsahu. Intersegmentální úhly mohou v souvislosti s bederní lordózou dosahovat až desítek stupňů. Za této situace nemusí být kamera optoelektronického systému schopna odečíst pozici registrovaného instrumentu v poli. Změna pozice kamery provedená za spolupráce sálového personálu tuto situaci vyřeší. Jedná se však o situaci ukazující na slabinu optoelektronického navigačního systému a lze předpokládat, že elektromagnetický navigační systém nezávislý na viditelnosti bodů operačního pole může tyto problémy eliminovat [7].
K tématům diskuze dále patří časová náročnost a radiační zátěž. Trvání operačního výkonu prodlužuje pořízení iniciálního skenu, zpracování CT obrazu, plánování trajektorie a registrace operačního pole. Přibližně půlhodinová časová prodleva zjištěná během našich operací je patrná především u stabilizace krátkých úseků páteře [8]. S počtem instrumentovaných segmentů se však časový rozdíl v porovnání s fluoroskopicky vedenými operacemi snižuje a předpokládáme, že především u rozsáhlých operací deformit páteře nebude časový rozdíl významný. Teoreticky by časová prodleva navigovaných výkonů mohla být zkrácena automatickou registrací, kterou již některé navigační systémy nabízejí. V otázce radiační zátěže přináší výše popsaný operační postup vyšší radiační zátěž pacientovi, ale zcela eliminuje radiační expozici personálu, který je během akvizice CT obrazu mimo exponovanou oblast [9]. Oba momenty, tedy jak prodloužení operačního času, tak vyšší radiační zátěž pacienta, by měly být vyváženy bezpečností samotného operačního zákroku.
Další technologický vývoj v této oblasti může sledovat jak možnou automatickou registraci, tak zkvalitnění přehlednosti operačního pole. Obou cílů lze dosáhnout úpravami parametrů elektrooptického systému, případně zmíněnou náhradou za jinou navigační modalitu. Celý vývoj v této oblasti může dále vyústit v minimalizaci operačního přístupu a v robotizaci spinálních instrumentací. Klinická zkušenost operatéra podepřená anatomickými a biomechanickými znalostmi, stejně jako odevzdaný profesionální přístup celého týmu však i nadále budou předpokladem optimálního výsledku operace.
ZÁVĚR
Navigace založená na intraoperačním CT obraze představuje další z cest vedoucích k přesnějšímu zavedení implantátu do páteřních struktur. Naše iniciální zkušenosti ověřily funkčnost systému v podmínkách páteřní operativy a potvrdily možnost použití ve všech anatomických etážích. Vysoká přesnost zavedení implantátů potvrzuje předpoklady použití navigace během operačních výkonů v terénu deformit, dysplastických změn páteře a těžkých úrazů a v oblastech anatomicky komplikované krční páteře a junkce krční a hrudní oblasti. Předchozí klinické zkušenosti, stejně jako zodpovědný týmový přístup jsou předpokladem dobrých morfologických i klinických výsledků.
MUDr. Pavel Barsa, Ph.D.
Neurochirurgické oddělení, Neurocentrum
Krajská nemocnice Liberec a.s.
Husova 10
460 63 Liberec I
e-mail: pavel.barsa@nemlib.cz
Sources
1. Golfinos JG, Fitzpatrick BC, Smith LR, Spetzler RF. Clinical use of a frameless stereotactic arm: results of 325 cases. J Neurosurg 1995;83 : 197–205.
2. Willems PW, van der Sprenkel JW, Tulleken CA, Viergever MA, Taphoorn MJ. Neuronavigation and surgery of intracerebral tumours. J Neurol 2006;253 : 1123–36.
3. Nolte LP, Zamorano LJ, Jiang Z, Wang Q, Langlotz F, et al. Image-guided insertion of transpedicular screws. A laboratory set-up. Spine 1995;20 : 497–500.
4. Laine T, Lund T, Ylikoski M, Lohikoski J, Schlenzka D. Accuracy of pedicle screw insertion with and without computer assistance: a randomized controlled clinical study in 100 consecutive patients. Eur Spine J 2000;9 : 234–240.
5. Džupa V, Krbec M, Kadeřábek R, Rusnák R, Douša P, et al. Peroperační CT navigace u operací páteře a pánve: první zkušenosti. Rozhl Chir 2013;92 : 379–384.
6. Fan Chiang CY, Tsai TT, Chen LH, Lai P.L, Fu TS, et al. Computed tomography-based navigation-assisted pedicle screw insertion for thoracic and lumbar spine fractures. Chang Gung Med J 2012;35 : 332–8.
7. Amiot LP, Lang K, Putzier M, Zippel H, Labelle H. Comparative results between conventional and computer-assisted pedicle screw installation in the thoracic, lumbar and sacral spine Spine 2000;25 : 606–14.
8. Sasso RC, Garrido BJ. Computer-assisted spinal navigation versus serial radiography and operative time for posterior spinal fusion at L5-S1. J Spinal Disord Tech 2007;20 : 118–122
9. Bandela JR, Jacob RP, Arreola M, Griglock TM, Bova F, et al. Use of CT-based intraoperative spinal navigation: management of radiation exposure to operator, staff, and patients. World Neurosurg 2013;79 : 390–4.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2014 Issue 1-
All articles in this issue
- Erektilní dysfunkce jako následek spinálního traumatu
- Laparoskopická cholecystektomie u dětí a adolescentů
- Navigace v páteřní chirurgii založená na intraoperačním CT zobrazení: zkušenost s iniciálními 295 implantáty
-
Je chirurgie štítné žlázy a příštítných tělísek opravdu bezpečná?
Je vhodná pro jednodenní chirurgii? - Biliární stent jako příčina ileózního stavu
- Pánevní exenterace v léčbě pokročilých nádorů malé pánve
- Totální pelvická exenterace – strategie výkonu
- Derivace moči po radikální cystektomii
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Derivace moči po radikální cystektomii
-
Je chirurgie štítné žlázy a příštítných tělísek opravdu bezpečná?
Je vhodná pro jednodenní chirurgii? - Pánevní exenterace v léčbě pokročilých nádorů malé pánve
- Biliární stent jako příčina ileózního stavu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

