-
Medical journals
- Career
Karcinom žaludku – výskyt a řešení komplikací chirurgické léčby
Authors: R. Vrba; Č. Neoral; R. Aujeský
Authors‘ workplace: I. chirurgická klinika FN Olomouc, přednosta: doc. MUDr. Č. Neoral, CSc.
Published in: Rozhl. Chir., 2010, roč. 89, č. 3, s. 178-182.
Category: Monothematic special - Original
Overview
Autoři se ve svém sdělení zabývají výskytem a léčbou komplikací chirurgické terapie karcinomu žaludku. Na I. chirurgické klinice bylo za posledních pět let operováno celkem 149 nemocných s diagnózou karcinomu žaludku. Radikální resekční výkon byl proveden u 121 nemocných. Horní polární resekce žaludku byla provedena u 7 pacientů. Paliativní výkon nebo exploraci podstoupilo 21 pacientů. Závažná perioperační komplikace nebyla v našem souboru zaznamenána. V pooperačním průběhu se v naší sestavě vyskytly tyto komplikace: píštěl v ezofagojejunoanastomóze celkem (8x), píštěl v pahýlu duodena (1x), subfrenický absces (2x), adhezivní ileus (1x). V delším časovém horizontu od operace byla ve dvou případech diagnostikována striktura ezofagojejunoanastomózy, dva nemocní měli hernii v jizvě. Ve dvou případech došlo k exitu nemocného. U jednoho pacienta na základě respiračního selhání s ARDS syndromem při dehiscenci ezofagojejunoanostomózy, druhý nemocný exitoval na hepatorenální selhání při cirhóze jater. Komplikacím se nelze zcela vyhnout po žádném operačním výkonu. Pokud vzniknou, je nutné jejich včasné odhalení a zahájení odpovídající léčby.
Klíčová slova:
karcinom žaludku – komplikace léčby – chirurgická terapieÚVOD
Karcinom žaludku je závažné maligní onemocnění horní etáže trávicího ústrojí. Kurativní terapií je radikální chirurgický výkon subtotální nebo totální gastrektomie. Součástí operační léčby je vždy lymfadenektomie, v současnosti je jednoznačně akceptována lymfadenektomie v rozsahu D2. Pokud jsou při výkonu respektována všechna kritéria onkologické radikality, jde o rozsáhlou resekční a rekonstrukční operaci. V průběhu chirurgické terapie může dojít ke vzniku komplikací, které lze rozdělit na lokální (krvácení, píštěl, absces, ranné komplikace) a celkové (kardiální, respirační a metabolické).
MATERIÁL A METODIKA
Na I. chirurgické klinice bylo za posledních pět let operováno 149 nemocných s diagnózou karcinomu žaludku, resekční výkon byl proveden u 128 nemocných. Radikálním výkonem byla totální nebo subtotální gastrektomie, operace byly provedeny vždy klasickým operačním způsobem. Totální gastrektomie byla provedena celkem u 109 nemocných, subtotální u 12 nemocných. Součástí výkonu byla vždy lymfadenektomie v D2 rozsahu, splenektomie byla provedena u 103 pacientů, pasáž trávicího ústrojí byla obnovena s využitím Rouxovy kličky. U totální gastrektomie byl u všech nemocných konstruován rezervoár z tenké kličky J tvaru. U sedmi nemocných byl proveden chirurgický výkon menšího rozsahu, horní polární resekce. Jednalo se o polymorbidní nemocné ve vyšších věkových kategoriích. U zbytku pacientů byla provedena explorace nebo paliativní gastroenteroanastomóza.
VÝSLEDKY
V pooperačním období jsme u 116 (90 %) nemocných po resekčním výkonu nezaznamenali žádnou komplikaci. Nejčastější komplikace v našem souboru byla píštěl v ezofagojejunoanastomóze, která byla prokázána celkem u 8 (7,3 %) nemocných. Na našem pracovišti ezofagojejunoanastomózu konstruujeme s využitím kruhových staplerů o průměrech 21, 25 a 29 mm. Ve většině případů v naší sestavě nemocných byl ke konstrukci anastomózy využit stapler o průměru 25 mm – celkem 81 (74 %) pacientů, stapler o průměru 29 mm byl použit u 15 (15 %) a 21 mm u 13 (11 %) nemocných. Píštěl v anastomóze se v pooperačním období vyskytla v šesti případech při použití stapleru s průměrem 21 mm a dvakrát u stapleru s průměrem 25 mm. V jednom případě (0,8 %) byla prokázána píštěl v oblasti slepě uzavřeného pahýlu duodena. Píštěl potvrdilo RTG vyšetření s použitím vodné kontrastní látky. Konzervativní parenterální terapie byla u většiny nemocných úspěšná. (Obr. 1, 2) V jednom případě bylo nutno provést operační drenáž subfrenického prostoru pro vydatnou píštěl. Subfrenický absces v oblasti lůžka sleziny byl prokázán u 2 nemocných (1,6 %). U prvního pacienta byla pod CT kontrolou provedena cílená drenáž abscesu pigtailem (Obr. 3). Ve druhém případě byla drenáž provedena klasicky operačně pro nepříznivou lokalitu abscesové kolekce pro perkutánní drenáž. U jedné nemocné (0,8 %) byla 30. den od primární operace provedena adhezeolýza pro adhezivní ileus.
Image 1. Píštěl v ezofagojejunoanastomóze po totální gastrektomii při kontrolní pasáži sedmý pooperační den Fig. 1. Fistula in esophagojejunal anastomosis following total gastrectomy, observed on a control passage view on postoperative Day 7 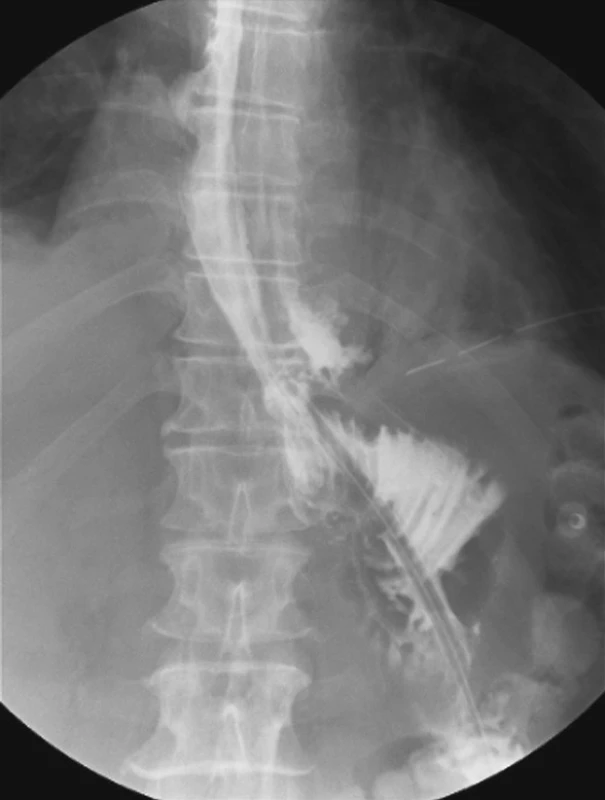
Image 2. Kontrolní pasáž po konzervativní léčbě 21. den od operace bez průkazu píštěle Fig. 2. Control passage view following conservative therapy on postoperative Day 21, no fistula detected 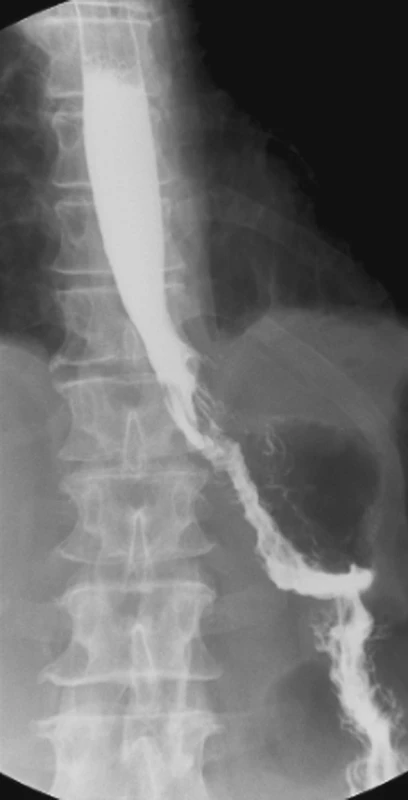
Image 3. Drenáž abscesu v levém hypochondriu perkutánně pod CT kontrolou Fig. 3. CT-controlled drainage of an abscess in the left hypochondrium 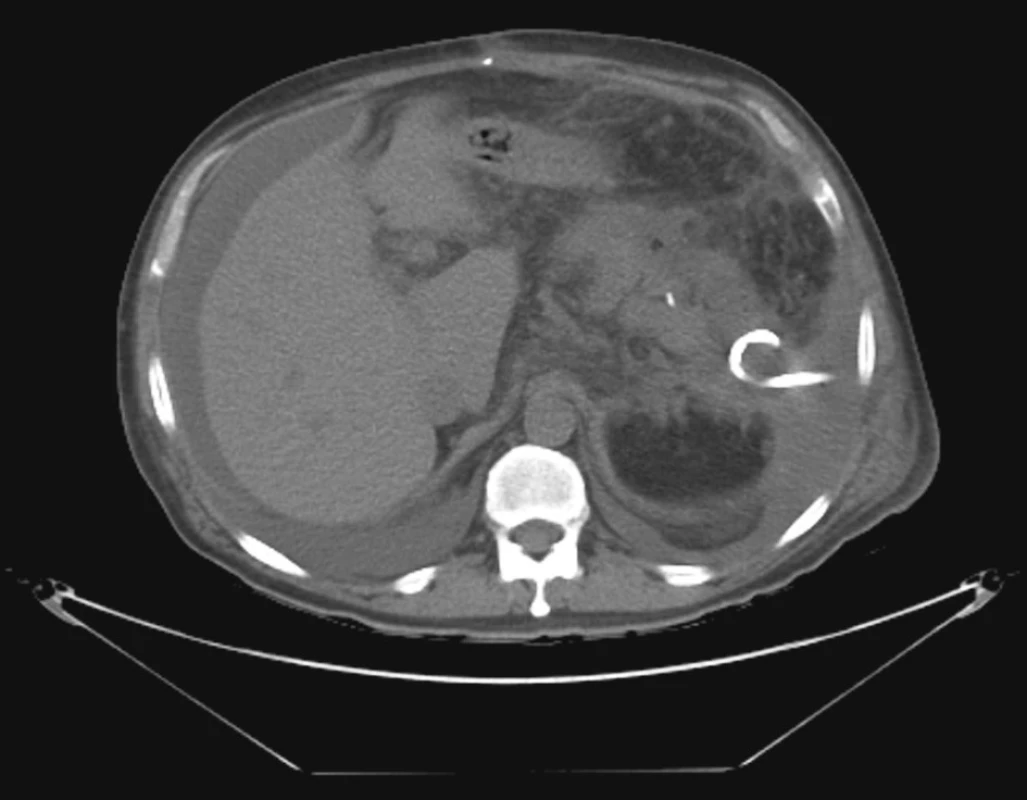
V delším časovém horizontu bylo 119 (94 %) pacientů bez komplikací. Z pozdních komplikací jsme v našem souboru zaznamenali dvakrát hernii v jizvě (1,6 %) a u dvou pacientů strikturu ezofagojejunoanastomózy (1,8 %). Hernie v jizvě byla v obou případech řešena plastikou s využitím sítky. Striktura ezofagojejunoanastomózy byla prokázána pasáží horní etáže GIT a endoskopickým vyšetřením, biopsie ze striktury vyloučila malignitu (Obr. 4). Intervenčním radiologem byla s efektem provedena dilatace striktury vysokotlakým balónem (Obr. 5).
Image 4. Striktura v ezofagojejunoanastomóze po totální gastrektomii Fig. 4. Esophagojejunal stricture following total gastrectomy 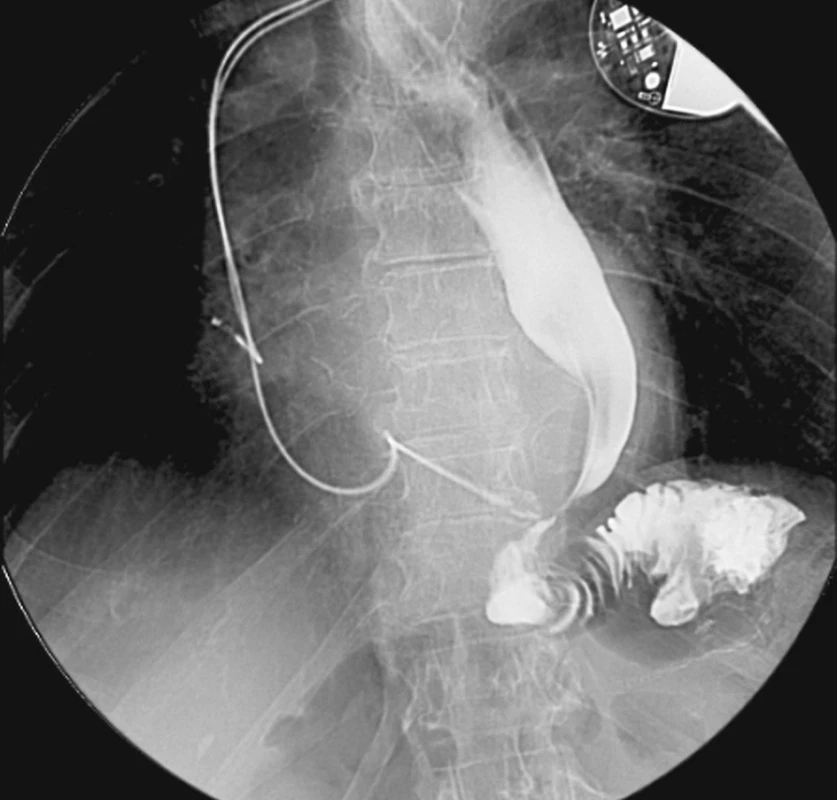
Image 5. Stav po balónové dilataci striktury ezofagojejunoanastomózy Fig. 5. Condition following balloon dilation of the esophagojejunal stricture 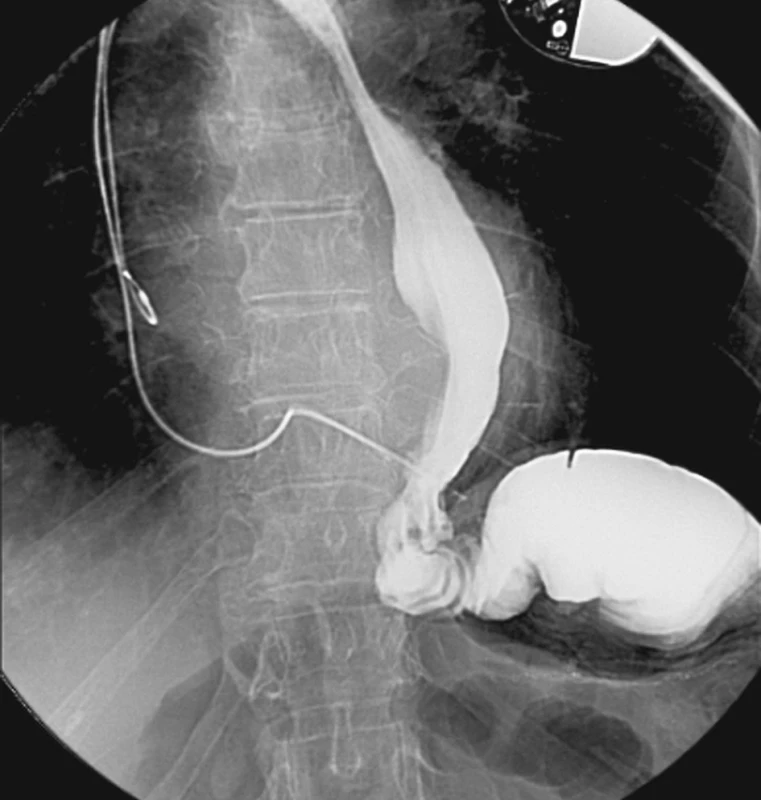
Table 1. Seznam komplikací totální a subtotální gastrektomie za roky 2004–2008 Tab. 1. List of complications of total and subtotal gastrectomy during 2004–2008 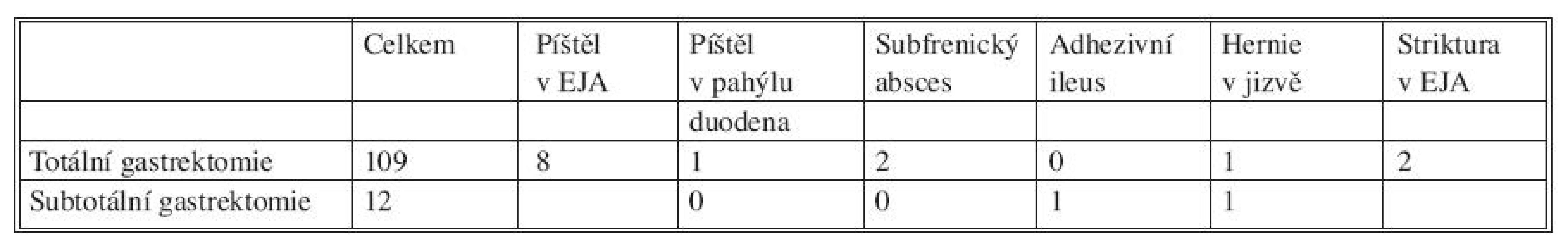
Nemocniční mortalita byla v našem souboru 1,6 %. V sestavě nemocných jsme zaznamenali u jednoho pacienta exitus 8. den od operace na hepatorenální selhání při cirhóze jater. Další nemocný exitoval 54. pooperační den na následky respiračního selhání s ARDS syndromem při dehiscenci ezofagojejunoanastomózy.
DISKUSE
Morbidita chirurgického výkonu pro karcinom žaludku se pohybuje okolo 30 %, mortalita by neměla přesáhnout 10 % [13, 14, 15, 17]. Výrazný rozdíl v morbiditě a mortalitě při totální a subtotální gastrektomii není v literatuře ve velkých randomizovaných souborech popisován [16, 17]. Za rizikové faktory operačního výkonu většina autorů jako Siewert, Becker, Yamamoto, Bonenkamp a jiní považují věk, počet přidružených onemocnění, provedenou splenektomii, lymfadenektomii a distální resekci pankreatu [10, 17, 18, 19].
Do perioperačních komplikací lze zařadit krvácení a poranění orgánů břišní dutiny. Frekvence komplikací se pohybuje v rozmezí 2,5–4 % [1, 2]. Z magistrálních cév jsou nejvíce poraněním a krvácením ohroženy větve coeliackého trunku a slezinná žíla. K poranění břišní aorty a dolní duté žíly může dojít v ojedinělých případech při provedení rozšířené lymfadenektomie v rozsahu D3 [22].
Poraněním parenchymatózních orgánů jsou ohroženy zejména levý jaterní lalok, pankreas a slezina. Při provedení D2 lymfadenektomie podle zavedených kritérií by nemělo dojít k poranění struktur v oblasti hepatoduodeálního vazu.
U tumorů lokalizovaných v oblasti kardie s nutností preparace v mediastinu může dojít při poranění pleury k rozvoji pneumotoraxu, který lze ošetřit během, nebo po operaci založením hrudní drenáže.
Mezi nejčastější komplikace v pooperačním období patří krvácení, zánětlivé komplikace v břišní dutině, píštěle a dehiscence anastomóz na trávicím ústrojí, vznik pankreatické píštěle [3, 4, 5, 9, 10]. Incidence komplikací je ve velkých sestavách operovaných nemocných (Nobuoka, Oh, Herbella, Guili, Becker, Sasako) popisovaná v rozmezí 3–18 % [4, 9, 10, 12, 17, 22]. Při radikálně provedené lymfadenektomii se může z otevřené lymfatické cévy objevit lymfokéla s kolekcí tekutiny [2]. Mezi méně závažné stavy v pooperačním období lze zařadit ranné komplikace (absces, serom, dehiscence rány) [6].
Pooperační krvácení se manifestuje hypovolemií s možností rozvoje hemoragického šoku, incidence krvácení se vyskytuje v odborné literatuře okolo 10 % [9, 12]. Po stanovení diagnózy je indikovaná akutní chirurgická revize s ošetřením krvácení.
Výskyt zánětlivých komplikací břišní dutiny se u velkých publikovaných sestav nemocných rozchází od 3 %, které jsou uváděny v práci jihokorejských autorů (Oh) [9] až do 21 % u italských autorů (Guili) [12]. Na základě klinického stavu nemocných a zobrazovacích metod (CT nebo ultrasonografické vyšetření) je potvrzena diagnóza. Terapie spočívá v drenáži abscesové kolekce, metodou volby je perkutánní drenáž pod CT kontrolou [20, 21]. Při nepříznivé lokalizaci abscesu je indikovaná klasická operační drenáž.
Vznikem píštěle anastomózy je ohrožena zejména ezofagojejunoanastomóza po totální gastrektomii, literární zdroje uvádějí výskyt píštěle v rozmezí od 4 do 19 % [9, 12]. Píštěl nebo dehiscence anastomózy je prokázána pasáží horní etáže GIT s aplikací vodné kontrastní látky. Při prokázané masivní píštěli až dehiscenci anastomózy a alteraci celkového stavu nemocného je indikovaná operační revize s drenáží dané lokality. Při klinicky dobrém stavu nemocných a minimální píštěli v anastomóze lze postupovat konzervativně. Kontrolní pasáž v časovém odstupu potvrdí zhojenou anastomózu.
Pankreatickou píštělí jsou ohroženi nemocní v případě, že součástí operace je resekce slinivky, která je nejčastěji resekována pro penetraci tumoru žaludku do pankreatu [4]. V literatuře (Nobuoka, Yamamoto) je udáván výskyt píštěle u nemocných s resekcí pankreatu okolo 15–20 %, což je vyšší číslo než u pacientů, u kterých je k totální gastrektomii připojena pouze splenektomie [4, 12]. Pankreatická píštěl se potvrdí zvýšenou hladinou amyláz v sekretu z břišního drénu [11]. Terapie je konzervativní spočívá v podání syntetických derivátů somatostatinu a plné parenterální terapii. Při kolekci tekutiny je provedena perkutánní drenáž. Pokud není konzervativní terapie efektivní, je indikována chirurgická revize s resekcí nebo drenážním výkonem na pankreatu [10].
Za komplikaci v delším časovém horizontu od operačního výkonu lze považovat strikturu ezofagojejunoanastomózy, která se manifestuje dysfagickými potížemi a váhovým úbytkem. Vznikem striktury je ohroženo zhruba 6 % nemocných po totální gastrektomii [7, 8]. Diagnóza striktury je stanovena RTG vyšetřením s kontrastní látkou. Endoskopické vyšetření je nezbytné k vyloučení maligního procesu v oblasti striktury. Terapií je dilatace striktury pod RTG kontrolou vysokotlakým balónem. Názory na výskyt recidivy stenózy ezofagojejunoanastomózy se v literárních zdrojích shodují (Ahmed, Ukjela), nutnost opakovaných dilatací je v literatuře udávána až v 70 % případů [7, 8].
V různém časovém horizontu od operace se mohou objevit typické komplikace abdominálních operací jako je adhezivní ileus. Výskyt adhezí je v literatuře udáván u 3 % všech laparotomií. Ve 20 % se objeví do 30 dnů od laparotomie, do jednoho roku se vyskytnou v 10 % [20]. Další možnou komplikací je hernie v jizvě po operačním výkonu [9]. Terapie uvedených komplikací je chirurgická.
ZÁVĚR
V referované sestavě byly zaznamenány některé typické komplikace operovaných nemocných pro karcinom žaludku. Procento jejich výskytu se u našich nemocných pohybovalo pod hranicí čísel publikovaných v odborné literatuře. Komplikace nelze zcela eliminovat u žádného operačního výkonu, jejich výskyt po chirurgické léčbě karcinomu žaludku nemusí mít pro nemocné fatální následky, pokud jsou léčeny podle správného terapeutického algoritmu.
MUDr. Radek Vrba, Ph.D.
I. chirurgická klinika LF UP a FN
I. P. Pavlova 6
775 20 Olomouc
e-mail: radek.vrba@fnol.cz
Sources
1. Siewert, J. R., Stein, H. J., Bottcher, K. Lymphadenektomie bei Tumoren des oberen Gastrointestinaltrakts. Chirurg, 1996, 67, 877–888.
2. Šimša, J., Leffler, J., Hoch, J., Schwarz, J., Bavor, P. Karcinom žaludku a D2 lymfadenektomie – technika, možné komplikace. Rozhl. Chir., 2004, 1, 6–11.
3. Kajihara, K., Wada, H., Mochinaga, H., Shigemasa, Y., et al. Two cases of advanced gastric cancer postoperative severe complicatoins after neoadjuvant chemoterapy. Gan To Kagaku Ryoho, 2008, 35, 2074–2076.
4. Nobuoka, D., Gotohda, N., Konishi, M., Nakagohri, T., Takahashi, S., Kinoshita, T. Prevention of postoperative pancreatic fistula after total gastrectomy. World J. Surg., 2008, 32, 2261–2262.
5. Lo, S. S., Wu, C. W., Shen, K. H., Hsien, M. C., Lui, W. Y. Higher morbidity and mortality after combined total gastrectomy and pankreaticosplenectomy for gastric cancer. World J. Surg., 2002, 26, 678–682.
6. Černý, J. Špeciálna chirurgia, Chirurgia trávicej rúry. Osveta, 1990.
7. Ahmed, J., Martin, J., Ikrauddin, S., Schauefer, P., Slivka, A. Endoscopic ballon dilatation of gastroenteric anastomotic stricture after laparoscopic gastric bypass. Endoscopy, 2003, 35, 725–728.
8. Ukjela, A., Afonso, B. B., Pimentel, R., Szomstein, S., Rosenthal, R. Outcome of endoscopic ballon dilataton of strictures after laparoscopic gastric bypass. Surg. Endosc., 2008, 22, 1746–1750.
9. Oh, S. J., Choi, W. B., Song, J., Hyung, W. J., Choi, S. H, Noh, S. H. Complications requiring reoperation after gastrectomy for gastric cancer: 17 years experiance in a single institute. J. Gastrointest. Surg., 2009, 13, 239–345.
10. Yamamoto, N., Oshima, T., Sato, T., Makino, H., Nagano, Y., et al. Upper abdominal body shape is risk factor for postoperative pancreatic fistula after splenectomy for advanced gastric cancer: a retrospective study. World J. Surg. Oncol., 2008, 10, 109.
11. Herbella, F. A., Tineli, A. C., Wilson, J. L. jr., Del granda J. C. Gastrectomy for gastric cancer: is the pancreas safe. J. Gastrointest. Surg., 2008, 12, 1912–1914.
12. Guili, R. Complications after gastrectomy and D 2 lymphadenectomy. J. Surg. Oncol., 2002, 10, 172–176.
13. Devessa, S. S., Silverman, D. T., Young, J. L., et al. Cancer incidence and mortality trends among whites in the United States, 1947–1984. J. Nat. Cancer Inst., 1987, 79, 701–742.
14. Bonenkamp, J. J., Songun, I., Hermans, J., Sasako, M., Welvaart, et al. Randomised comparison of morbidity after D1 and D2 disection for gastric cancer in 996 Dutch patiens. Lancet, 1995, 345, 745–748.
15. Brady, M. S., Rogatko, A., Dent, L. L., Shiu, M. H. Effect of splenectomy on morbidity and survival following curative gastrectomy for carcinoma. Ann. Surg., 1991, 126, 359–364.
16. Bozzetti, F., Marubini, E., Bonfani, G., et al. Total versus subtotal gastrectomy. Surgical morbidity and mortality rates a multicenter Italian randomized trial. Ann. Surg., 1997, 226, 613–620.
17. Becker, H. D., Hohenberger, W., Junginger, T., Schlag, P. M. Chirurgická onkologie. Grada, 2005, 291–338.
18. Bonenkamp, J. J., Hermans, J., Sasako, J.,van de Velde, C. J. H. Extend lymph node dissection for gastric cancer. N. Engl. J. Med., 1999, 340, 908.
19. Siewert, J. R., Boettcher, K., Stein, H. J., et al. Relevant prognosis factor in gastric cancer: ten - year results of the German Gastric Cancer Study. Ann. Surg., 1998, 228, 449.
20. Yamada, T., et al. Textbook of gastroenterology. Lippincott Williams Williams, fourt edition, 2003.
21. Lambiase, R. E. Percutaneous absces and fluid drainage : a critical review. Cardiovasc. Intervent. Radiol., 1991, 14, 143.
22. Sasako, M., Sano, T., Yamamoto, S., Kurokawa, Y., Nashimoto, A., et al. D2 lymphadenectomy alone or with para-aortic nodal dissection for gastric cancer, N. Engl. J. Med., 2008, 31, 453–462.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2010 Issue 3-
All articles in this issue
- Karcinom žaludku a současnost
- Karcinom žaludku – výskyt a řešení komplikací chirurgické léčby
- Iatrogenní poranění žlučových cest
- Naše zkušenosti s Free Hand kamerou
- Prodloužená profylaxe tromboembolismu při resekci kolorekta pro malignitu
- Počet uzlin u resekcí tlustého střeva pro kolorektální karcinom
- Jaterní metastázy jiného než kolorektálního původu
- Moderní algoritmy diagnostiky a léčby anorektálních píštělí na klinickém pracovišti – kazuistiky
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Jaterní metastázy jiného než kolorektálního původu
- Moderní algoritmy diagnostiky a léčby anorektálních píštělí na klinickém pracovišti – kazuistiky
- Iatrogenní poranění žlučových cest
- Počet uzlin u resekcí tlustého střeva pro kolorektální karcinom
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

