-
Medical journals
- Career
Mapování povrchového žilního systému před a po operaci varixů – literární souhrn specifických aspektů při vyšetřování duplexní sonografií
Authors: L. Hnátek 1; G. Hnátková 2
Authors‘ workplace: Chirurgické oddělení Nemocnice Atlas a. s., Zlín 1; Interní oddělení Nemocnice Atlas a. s., Zlín 2
Published in: Rozhl. Chir., 2010, roč. 89, č. 11, s. 707-712.
Category: Monothematic special - Original
Overview
Úvod:
Duplexní sonografie je zlatým standardem při vyšetřování žilního systému dolních končetin. Její význam je velmi často podceňován především chirurgy před zahájením vlastního operačního výkonu. Význam mapování povrchového žilního systému nabyl ještě větší důležitosti s rozvojem endovaskulárních termoablací insuficientních žil.Cíl:
Cílem této shrnující práce je vyzvednout anatomicko-topografické poměry jednotlivých významných anatomických struktur při mapování povrchového žilního systému.Materiál a metodika:
Zde je popsán průběh vena saphena magna a parva a jejich ústí do hlubokého žilního systému včetně jednotlivých přítoků daných oblastí. V textu nejsou opomenuty ani venae perforantes. Je kladen důraz na zobrazení daných struktur v B-módu sono obrazu a jejich vztah k okolním anatomickým strukturám.Závěr:
Je nutné dodržet jednotlivá doporučení při vyšetření žilního systému a následně dodržet pravidla jednotlivých chirurgických postupů. Jedině tak lze cíleně odstranit patologické zdroje refluxu a insuficientní žíly inter - a epifasciálního žilního systému. Tím se ve významném procentu vyhneme časným recidivám, nebo progresi onemocnění. V neposlední řadě tak eliminujeme následky vlastního chirurgického výkonu, které bývají především po „klasických“ výkonech mnohdy devastující a nejen kosmeticky, ale i funkčně nepřijatelné.Klíčová slova:
duplexní ultrasonografie – mapování žilního systému dolní končetinyÚVOD
Duplexní sonografie je nejčastějším vyšetřovacím postupem při diagnostice chronické žilní insuficience (CVI). Výsledky mnohých terapeutických modalit jsou hodnoceny a publikovány právě na základě vyšetření duplexní sonografií, přesto dosud bylo publikováno jen malé množství studií a konsenzů, které by systematicky shrnovaly jednotlivá doporučení pro jednotlivá stadia CVI včetně specifických situací.
CÍL
Cílem této práce je upozornit na topograficko-anatomické poměry, které je třeba si uvědomit při vyšetřování duplexní sonografií v rámci přípravy pacienta k operaci povrchového žilního systému. Význam a náročnost takového vyšetření narůstá především v případě řešení recidivy varikozit nebo v případě plánování endovaskulárního zákroku a hodnocení nálezu po jeho provedení.
Základním úskalím při mapování povrchového žilního systému je jeho velmi pestrá variabilita. Klíčový moment zde hraje anatomická nomenklatura, která byla v poslední době upravována a bohužel tato její nově standardizovaná podoba není v odborné veřejnosti dosud vždy používána.
ULTRASONOGRAFICKÉ ZNAKY ANATOMIE POVRCHOVÉHO ŽILNÍHO SYSTÉMU
Vena saphena magna (VSM)
Povodí VSM je nejčastějším cílem chirurgických zákroků nejen v rámci operace varikozit, ale i v tepenné rekonstrukční chirurgii. Před těmito výkony je však nutné podrobné zmapování a popis dané oblasti, aby pak zvolený zákrok mohl být uskutečněn co nejpřesněji nebo zda je vůbec nutné či možné jej provést.
Průběh VSM je spojen s určitými klíčovými body a specifickými rysy, které je třeba v průběhu vyšetření respektovat. Asi nejznámějším znakem je tzv. „Egyptské oko“. Poprvé byl tento charakteristický znak pro uložení kmene (VSM) do fasciální duplikatury, tak zvaného saphena-kompartmentu, popsán Baillym. Detailní charakteristiky saphaena-kompartmentu byly popsány před nedávnem Caggiatim. Označení „egyptské oko“ se vžilo z typického obrazu v příčném řezu dané oblasti (Obr. 1). Toto uložení VSM umožňuje oddiferencovat ostatní paralelně procházející podkožní větve.
Image 1. Recidiva varikozit z ponechané VES Fig. 1. Relapses of varicosities of the retained VES 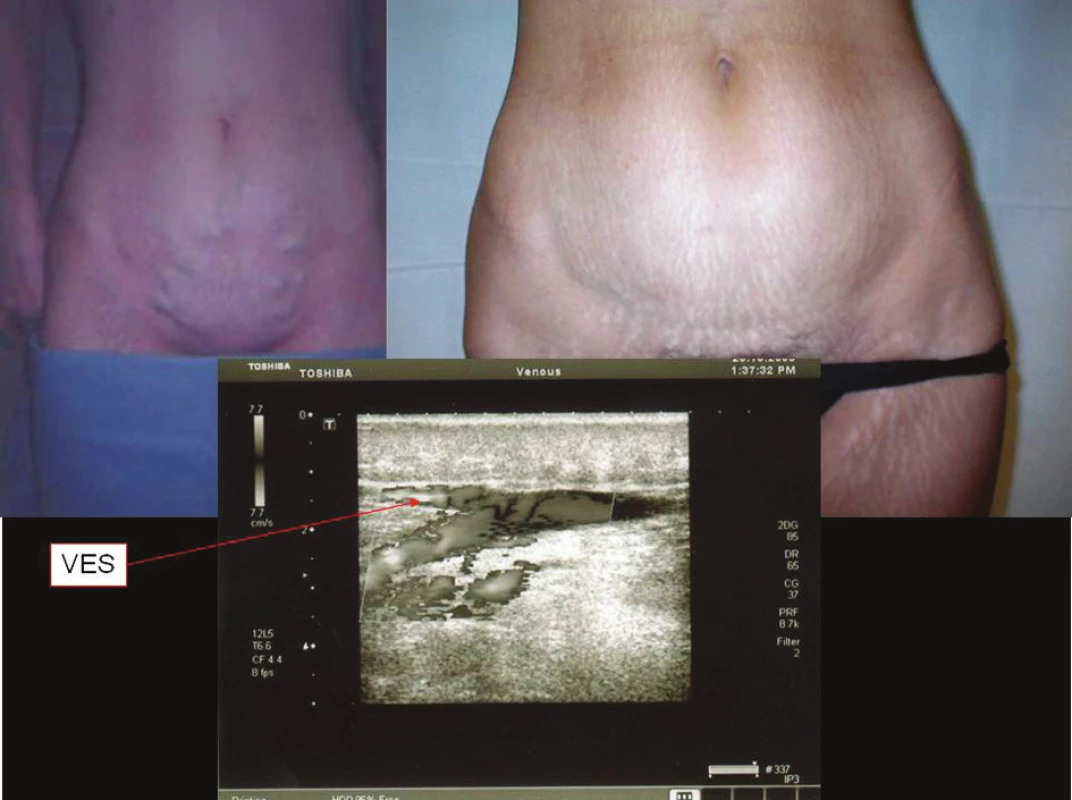
Při mapování žilního systému je však třeba být pozorný v horní třetině stehna. V této oblasti totiž velmi často prochází taktéž ve vlastním interfasciálním prostoru vena saphena accesoria anterior (VSAA) a může zde vytvářet obraz druhého „egyptského oka“. VSAA jde laterálně od VSM. Typickým znakem je, že VSAA je v jedné linii s hlubokým cévním svazkem, tedy arteria (AF) et vena femoralis (VF). Obě žíly jak VSM, tak VSAA mají společné ústí v oblasti safeno-femorální junkce (SFJ). Těsně před tímto soutokem, pak mohou jít společně v jednom interfaciálním prostoru (Obr. 2). Směrem do periferie, na rozhraní proximální a střední třetiny, pak VSAA vystupuje do epifasciálního prostoru. V některých případech dominuje obraz jednoho interfaciálně uloženého kmene s druhou diskrétní žílou. Na rozhraní proximální a distální třetiny pak dominantní kmen opouští interfaciální prostor a do periferie pokračuje interfasciálně jen minoritní céva. V této situaci se jedná o hypoplazii VSM, v případě, že v interfasciálním prostoru prakticky zaniká, jedná se o aplazii VSM. Zajímavý je fakt, že mnozí autoři se liší v jejím popisu ve smyslu, délky, průměru, průběhu apod. [1, 2]. Ricci udává ve své studii z roku 2002, že VSAA je insuficientní u 14 % pacientů s varikozitami. A mnohdy se u nich nevyskytuje insuficience VSM (Obr. 3).
Image 2. Varikozity při insuficienci VSAA a VSAP Fig. 2. Varicosities in VSAA and VSAP insufficiencies 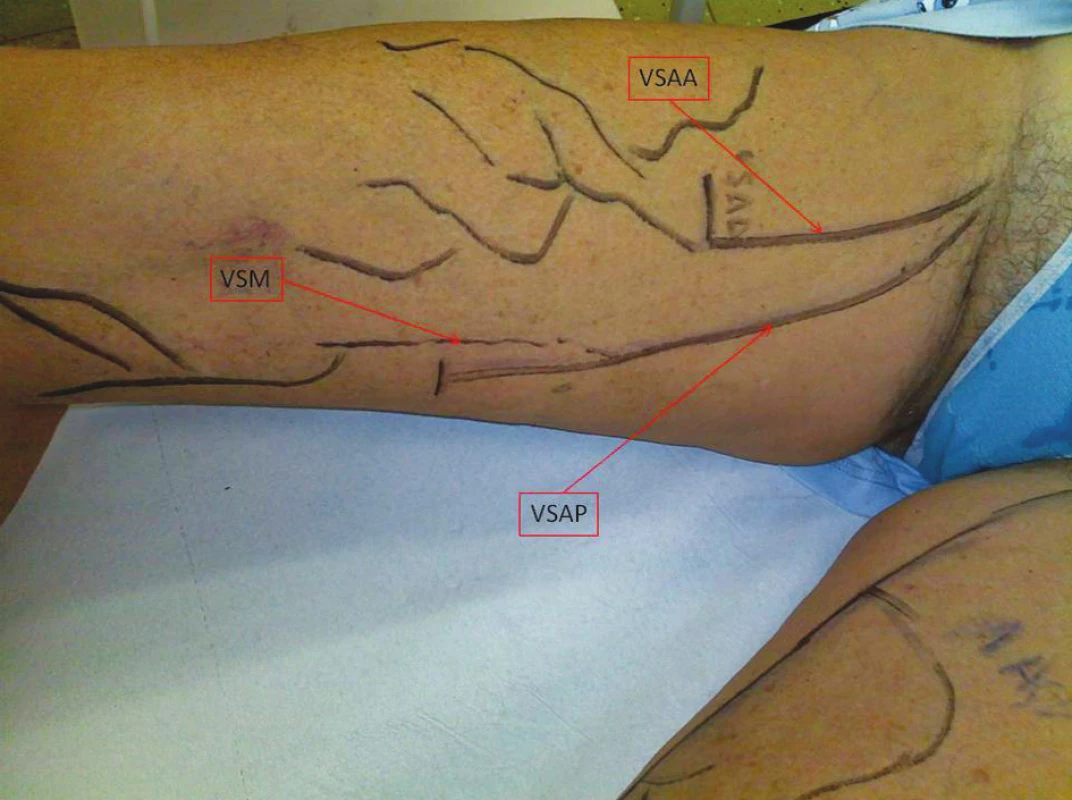
Image 3. Recidiva varikozit z ponechané VPES Fig. 3. Relapses of varicosities of the retained VPES 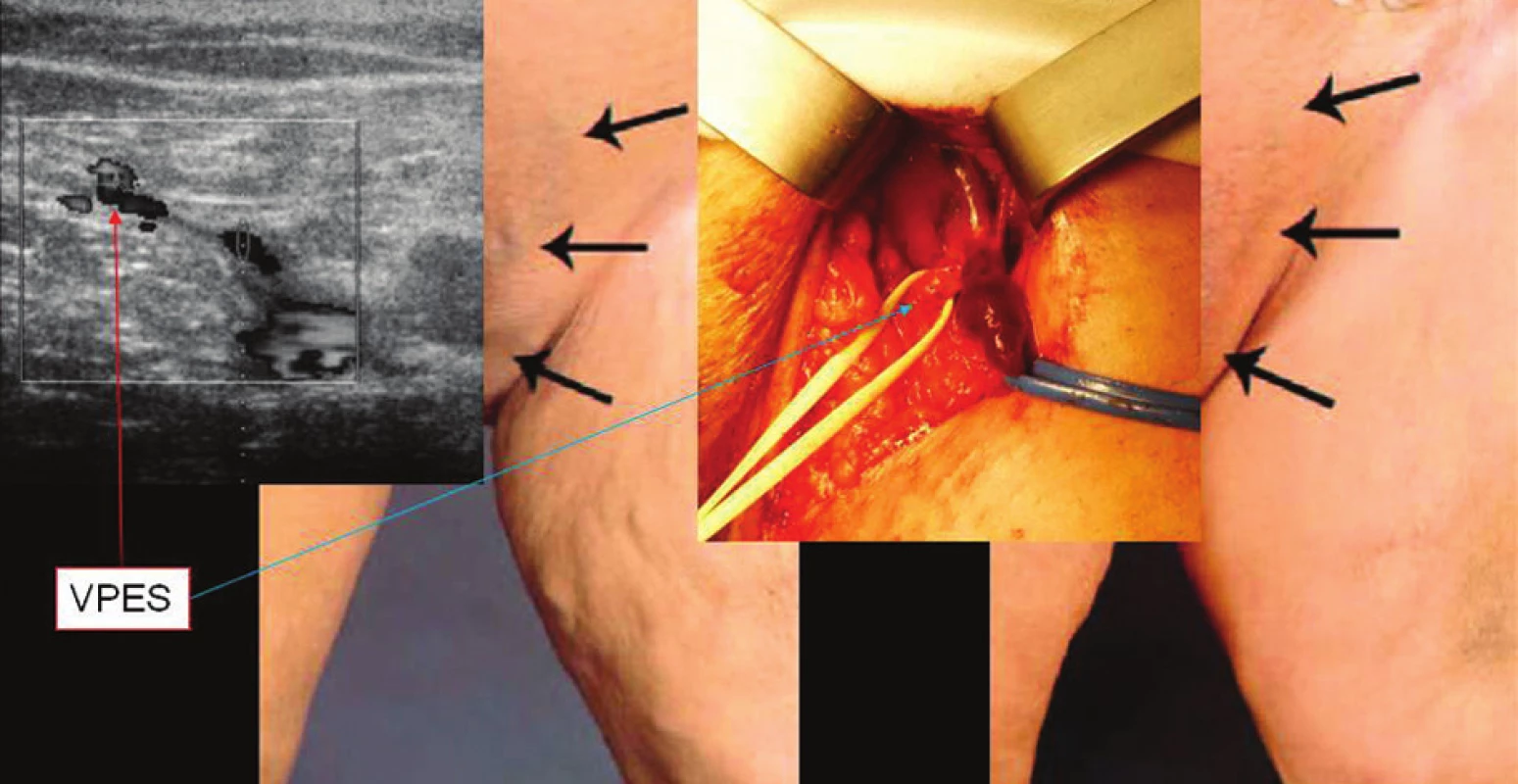
Vena saphena accesoria posterior (VSAP) je další významnou strukturou oblasti stehna. Jde o žílu, která jde v oblasti stehna paralelně s VSM. V některých případech se jedná o přítok VSM, jindy jde o samostatný přítok SFJ. Jde mediálně od VSM, její výskyt je méně častý jak VSAA (Obr. 3). Pro dokončení popisu povrchového žilního systému dané oblasti je nutno zmínit též tzv. laterální žilní systém (extension lateralis). Ten se nachází na laterální straně stehna a bérce. Existuje zde i teorie, že se jedná o rudiment embryonální vena marginalis lateralis. Zůstaneme-li na přední straně stehna, je nutné ještě zmínit vena circumflexa femoris anterior, která je přítokem VSM nebo VSAA. Tato žíla může pocházet z laterálního žilního systému.
Dalším pro diagnostiku kritickým bodem je oblast průběhu VSM těsně pod kolenem, resp. mezi hranou tibie a mediální části m. gastrocnemius. V dané oblasti je nutno oddiferencovat vlastní VSM od jejich větví, resp. přítoků. VSM si zachovává svou polohu v interfasciálním prostoru, ale obraz typického egyptského oka je vdané oblasti špatně identifikovatelný. Proto je zde charakteristická poloha VSM v trojúhelníku, jehož strany vymezují tibia, mediální část m. gastrocnemius a fascia saphena (Obr. 4). Pokud v takto vymezeném prostoru žádnou žílu nevidíme, můžeme též hovořit o aplazii VSM. Takto definovaná orientace vdané oblasti je popsána v jiné práci Ricciho taktéž z roku 2002.
Image 4. Topograficko-anatomické poměry VSM v oblasti kolene Fig. 4. Topographic-anatomical relationships of VSM in the knee region 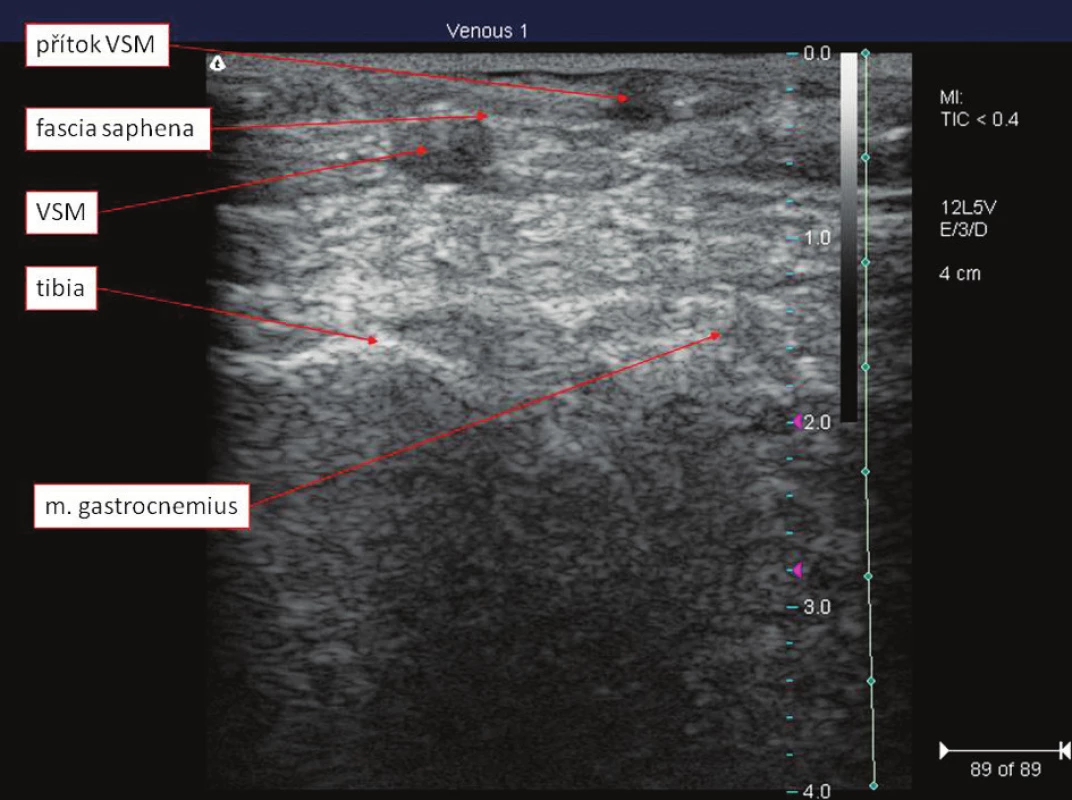
Mezi anatomy je v poslední době diskutována vena circumflexa femoris posterior (VCFP). Ta patří mezi žíly stehna, protože ústí do VSM nebo do VSAP. Ve svém průběhu jde dorzálně a může být pokračováním vena saphena parva (VSP). Právě tento fakt je diskutován v práci Brennera a jeho kolegů. Ti na základě vyšetření anatomických preparátu vytvořili hypotézu, že VSP je přítokem VSM a sapheno-popliteální junkce (SPJ) je jen perforátor. Tato práce byla prezentována na flebologickém kongresu v Monacu září 2009.
Safeno-femorální junkce (SFJ)
SFJ je sice součástí povodí VSM, ale vzhledem k tomu, že je jedním z klíčových bodů v rámci etiologie křečových žil, uvádím ji samostatně. Procento, ve kterém je tato oblast příčinou vzniku varikozit se liší podle různých literárních zdrojů a to v rozmezí 34–53 % [3, 4]. Naopak procento recidiv varikozit z dané oblasti je poměrně jednotné a to 20–26 % [5, 6].
Ovšem nejen problematika etiologie varikozit je předmětem diskusí. Tím hlavním problémem v posledních letech je „spor“ mezi zastánci klasických chirurgických výkonů a protagonisty endovaskulárních zákroků. Respektive, je správné neprovádět u endovaskulárních zákroků crossectomii? U zastánců otevřené chirurgie je pak diskutováno co je neovaskularizace a co chyba chirurga? Významem zmínění těchto otázek je upozornit na velmi specifické nálezy po těchto výkonech, se kterými se setkáváme v naší praxi a umět je správně interpretovat.
U endovaskulárních zákroků není podle prací Pichota a Proebstleho nutno provádět crossectomii. Nástroj k jejich provedení (optické vlákno, radiofrekvenční elektroda) se pak zavádí na vzdálenost 1–2 cm od SFJ. Po takto provedených výkonech pak zůstává pahýl SFJ (Obr. 5).
Image 5. SFJ při a po endovaskulární operaci RFITT, VSM po RFITT (RFITT = Radiofrequent Induced Thermo-Terapy) Fig. 5. SFJ during and after endovascular RFITT surgery, VSM after RFITT (RFITT = Radiofrequent Induced Thermo- Terapy), 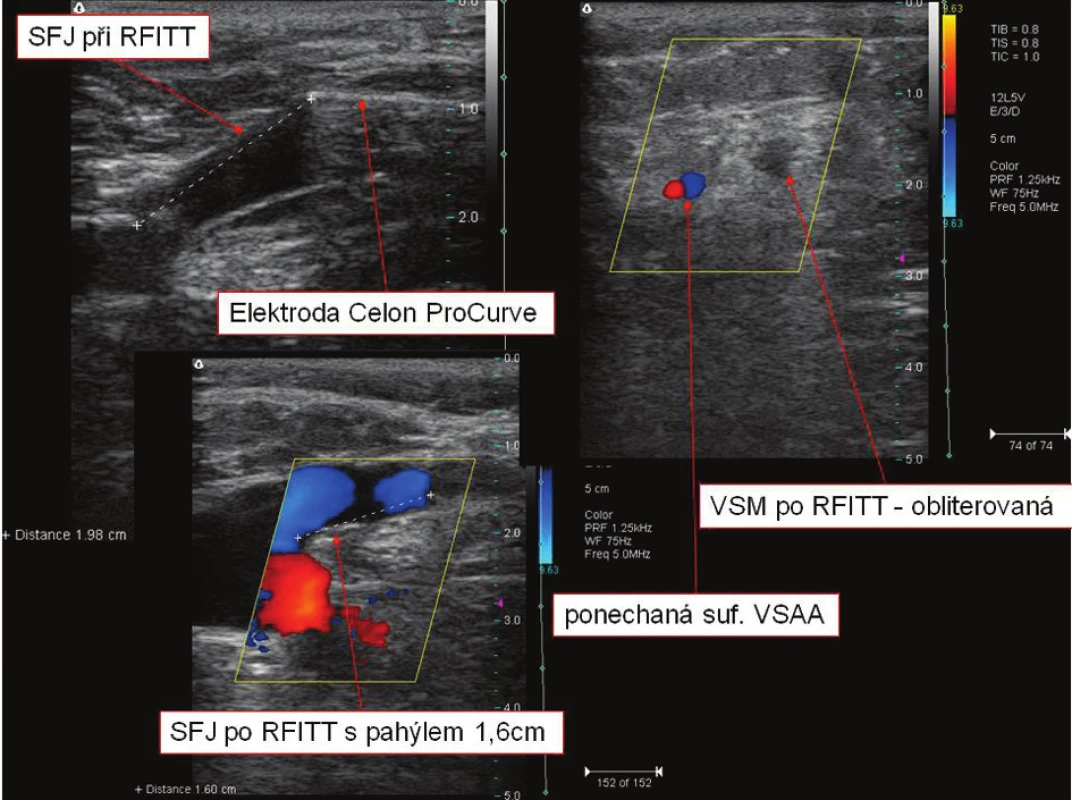
Naopak v případě „klasického“ zákroku je provedení crossectomii nepostradatelné. Crossectomie je podle současných doporučení definována jako podvaz a protnutí veškerý přítoků SFJ. VSM se pak musí ligovat přímo na vena femoralis (VF). Ale právě diskuze kolem neovaskularizace ukazují nutnost být ještě radikálnější a důslednější [7]. Podle závěrů těchto studií jsou pak doporučovány postupy, jako je uzávěr hilus saphenus [8, 9] nebo provedení patche v místě ligace a protětí VSM na VF [10] a podobné zákroky, které mají za úkol plnit funkci anatomické bariery a zabránit tak vzniku neovaskulátu. Ovšem vždy se jedná o zákrok rozsáhlejší a tudíž i spojený s vyšším procentem komplikací [11]. Pro sonografistu „nechirurga“ provádějící mapování dané oblasti nejsou tyto diskuse zásadní. Jeho úkolem je precizní zmapování zdroje refluxu v dané oblasti. Jedná se především, do kterých přítoků junkce se šíří reflux, kde je jeho počátek ve smyslu, od které chlopně a ve které žíle.
Při mapování opět vycházíme z anatomických poměrů dané oblasti, které jsou velmi variabilní. Ústí VSM disponuje konstantní terminální chlopní, jejíž pozice je nejpodrobněji popsána v anatomické studii Muhlbergera publikované v časopise Phlebologie v roce 2007. Ten popisuje její výskyt v 88,5 % ve vzdálenosti od 0 do l,4 cm od VF. Druhá chlopeň od ústí VSM je označována jako preterminální a je ve vzdálenosti od 1,4 do 8,2 cm od VF v 89,2 %. Mezi těmito chlopněmi se nachází hlavní přítoky SFJ. Z oblasti ležící proximálně od SFJ přicházejí vena circumflexa ilium superficialis (VCIS), vena epigastrica superficialis (VES) a vena pudenda externa superficialis (VPES). Tyto žíly nemusí být přítomny pouze jednotlivě, ale mohou být zmnoženy. V klinice se uplatňují především při recidivě varikozit, pokud jsou ponechány v rámci nedůsledně provedené crossectomie (Obr. 6) při insuficienci terminální chlopně.
Image 6. Recidiva varikozit z VPES samostatně ústící do VFC Fig. 6. Relapses of VPES varicosities, VPES emptying into VFC 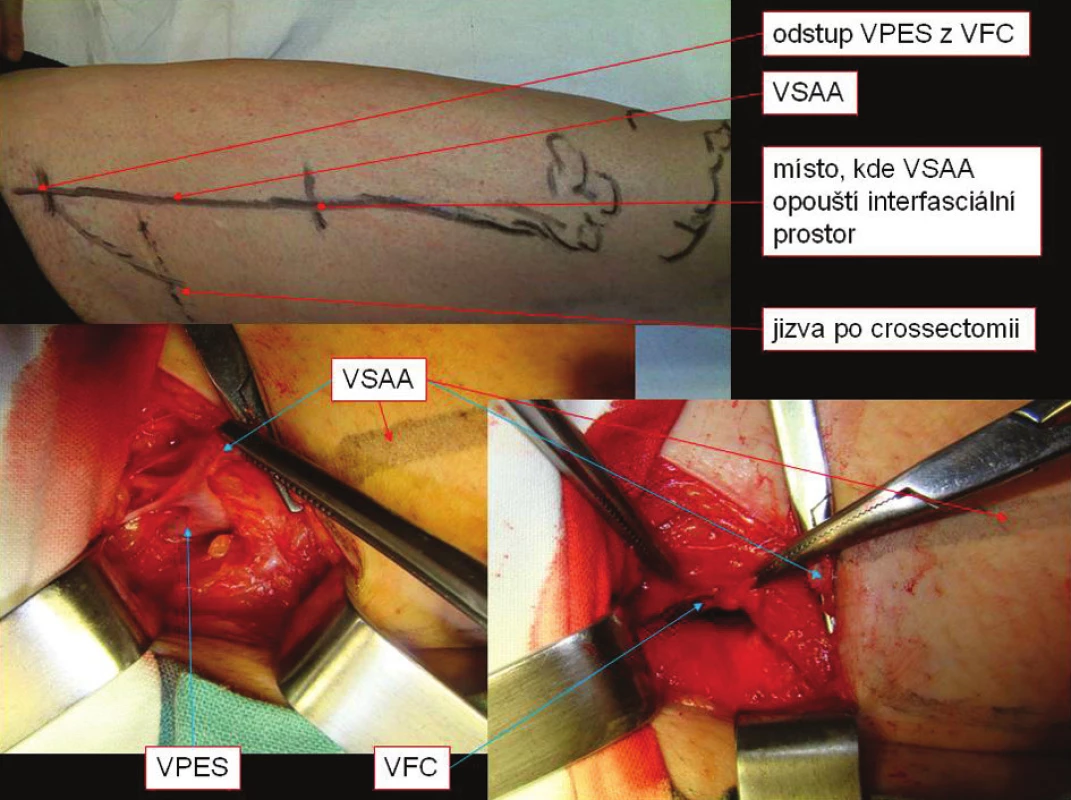
Velmi specifickou situaci může způsobovat VPES. Ta totiž ne vždy ústí přímo do SFJ, ale mnohdy samostatně přímo do VFC nebo do VF. V případě jejího zmnožení jedna větev může ústit do SFJ a jiná přímo do hlubokého žilního systému. VPES samostatně se vlévající do hlubokého žilního systému může být přehlédnuta při prováděné crossectomii a stát se tak při insuficienci VFC nebo VF příčinou recidivy varikozit. Při vyšetřování duplexní sonografií, tak může nález simulovat insuficientní ponechanou SFJ, protože VPES bývá výrazně dilatována (Obr. 7, 8). V takovéto situaci je třeba si uvědomit, kde je daný nález detekován. Při proximálně ústící VPES je žíla detekována až v oblasti tříselného vazu. V případě distálního ústí je tento nález pod inguinální rýhou a to až 3 cm. Z periferie pak ústí do SFJ vena saphena accesoria anterior a to ve vzdálenosti lem od VF v 41 %. V oblasti preterminální chlopně pak většinou ústí VSAP. V úhlu vymezeném VSM a VSAA bezprostředně u ústí se nachází konstantní lymfatická uzlina. Ta bývá zvětšená především po zákrocích, při zánětech a jiných patologických procesech na dané dolní končetině.
Image 7. Neovaskularizace v SFJ Fig. 7. Neovascularization in SFJ 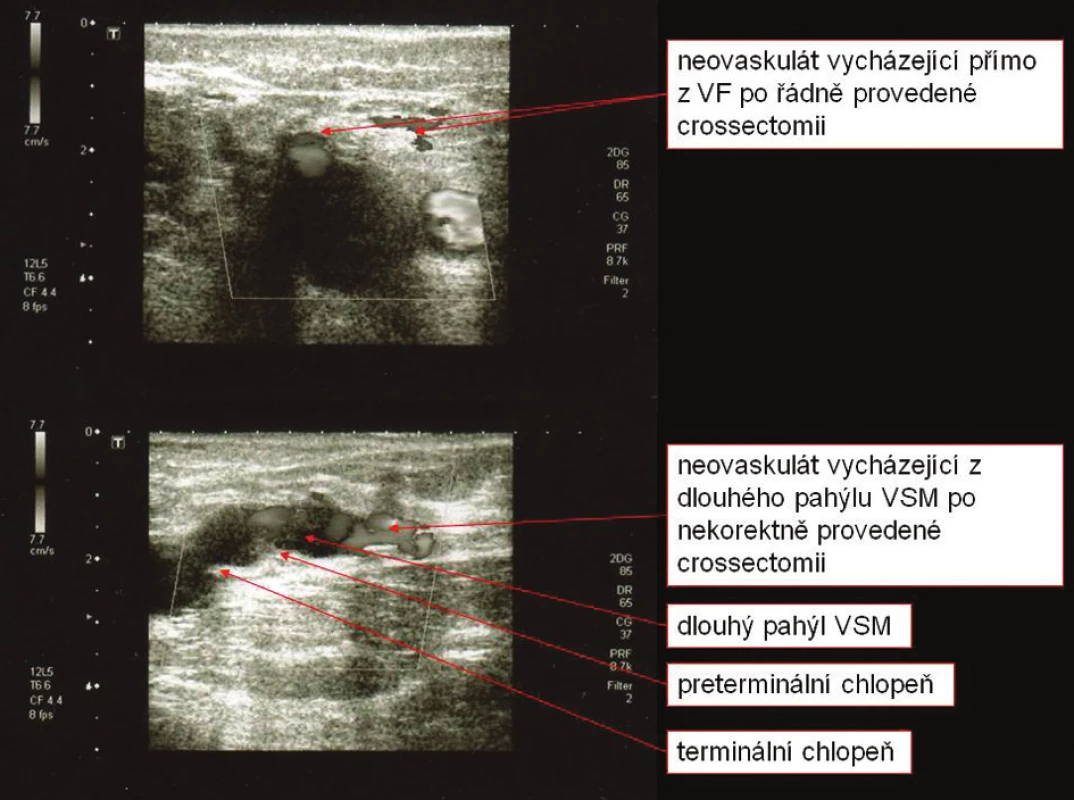
Image 8. Anatomie SFJ Fig. 8. SFJ anatomy 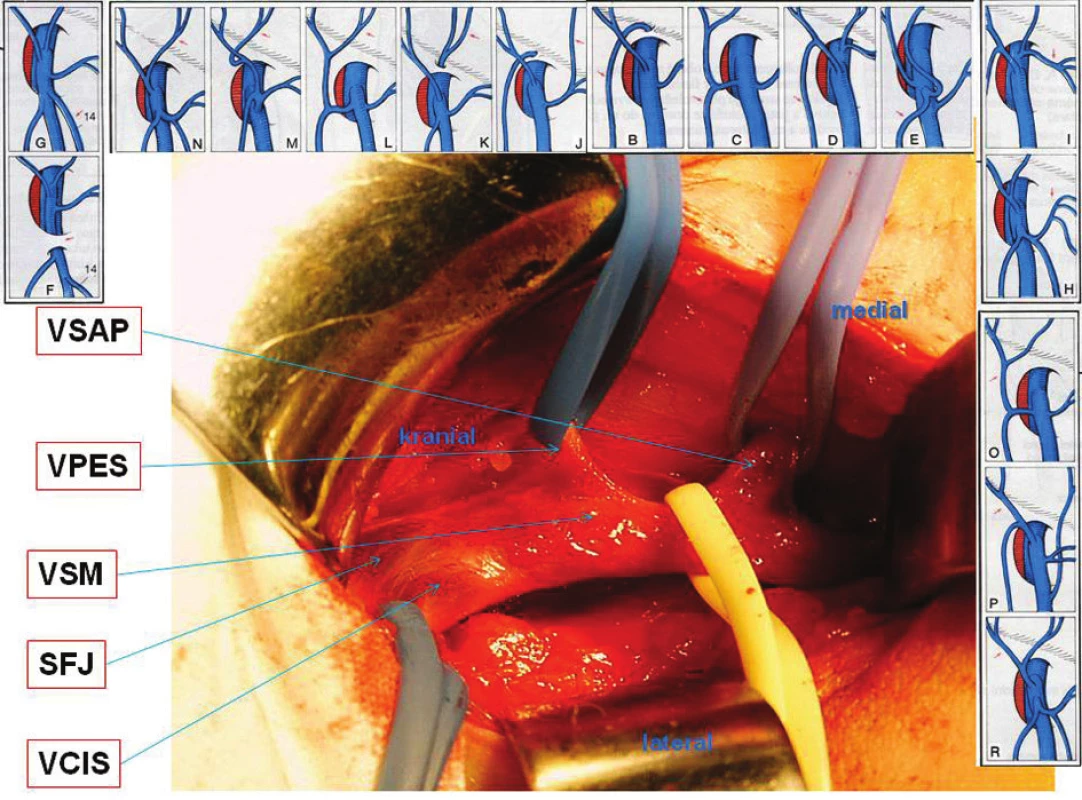
Zůstaneme-li ještě u hodnocení nálezu v oblasti crosse v případě recidivy varikozit, nalezneme v literatuře velmi rozdílné výsledky popisu neovaskulátu. Neovaskularizace bývá velmi často zpochybňována, ale její definice je zakotvena v REVAS klasifikaci. Procento příčiny recidivy v důsledku neovaskularizace po deklarované řádně provedené crossectomii se pohybuje od 5 % do 65 %. Geier a kol. takto rozdílné výsledky přisuzují limitaci duplexní sonografie přesně identifikovat neovaskulát (Obr. 9).
Image 9. Samostatně ústící VPES do VFC a způsobující recidivu varikozit Fig. 9. VPES, individually emptying into VFC and causing relapses of varicosities 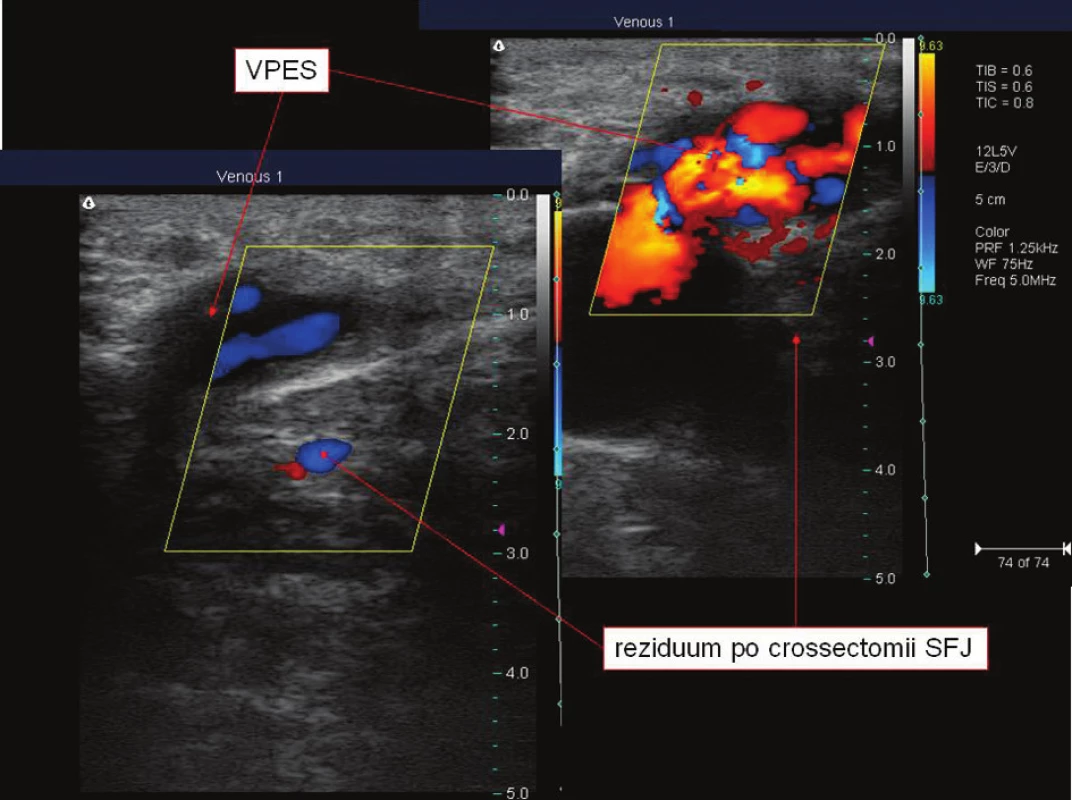
Vena saphena parva (VSP)
Vedle povodí VSM je povodí VSP dalším významným komplexem podílejícím se v etiologii křečových žil. VSP začíná u zevního kotníku a jde nejprve latero-dorzálně a následně dorzálně na bérci. V popliteální oblasti anastomózuje s vena poplitea (VP). Je též uložena v interfasciálním kompartmentu. V distální části VSP je obraz na příčném řezu velmi obdobný jako u VSM, proximálně pak nabírá tvaru trojúhelníku. Tento tvar je způsoben hlavami m. gastrocnemius a fascia saphena, které tento prostor vymezují. VSP bývá někdy zdvojena, případně i ztrojena, avšak vždy jsou všechny kmeny uloženy uprostřed kompartmentu.
Safeno-popliteální junkce (SPJ) a jeho anatomické varianty
Základní a nejčastější variantou je anastomóza VSP do proximální části VP společným ústí s Giacominiho žílou (GV). Jednotlivé gastroknemické žíly ústí do VP samostatně nebo přes společné ústí VSP a VG. Další variantou je plynulý přechod VSP do GV, přičemž zůstává tenká komunikace s VP. Třetí varianta je volné pokračování VSP do GV, přičemž zcela chybí komunikace s VP. Naprostá většina ústí VSP do VP je mezi 2–4 cm proximálně od rýhy ohybu kolene, v 25 % je to výš a jen zřídka níž [12]. Zajímavé výsledky přinesla metaanalýza Cretona z roku 2005, kde v případě populace bez žilního onemocnění ve 46,6 % je ústí VSP výše jak 7 cm od rýhy ohybu kolene, naproti tomu u populace s insuficienci VSP je její ústí uvnitř fossa poplitea (tedy 0–7 cm od linie ohybu kolene) v 57–93,7 %. Lemasle ve své studii popisuje stranové poměry ústí VSP. Na čistě posteriomí straně je ústí VSP v 15 %, posteromediální 30 %, posterolaterální v 12 %, laterální v 45 % a v 1 % anterolaterální. Terminální úsek VSP obdobně jako VSM obsahuje též dvě chlopně. Terminální je v bezprostřední blízkosti vena poplitea a preterminální chlopeň, která se nachází obvykle v místě odstupu GV. Co se týče ústí gastroknemických žil, je jejich ústí do SPJ podle různých studií mezi 10–30 % [13].
Cranial extension (kraniální pokračování) VSP
Kraniální pokračování VSP bylo poprvé popsáno v roce 1873 Giacominim. Následovala celá řada dalších anatomických i sonografických studií popisujících danou anatomickou strukturu. Ta se v 95 % nachází hluboko v těsné blízkosti fascie. V ultrazvukovém obrazu se distální část kraniální extenze zobrazuje v interfasciálním prostoru trojúhelníkovitého tvaru, který se podobá právě proximálnímu kompartmentu VSP. Tento prostor je ohraničen mediálně m. semitendinosus, laterálně m. biceps femoris. Prostor pak uzavírá fascia scarpi, která překrývá rýhu mezi svaly.
Gillotem byly popsány varianty proximálního ústí kraniální extenze VSP. První možností je ústí do gluteální oblasti jako jedna žíla nebo rozdělení do povrchových a hlubokých větví dané oblasti. Další možností je vyústění do hlubokého žilního systému končetiny jako posteriorní nebo posterolaterální perforátor. Někdy může končit jako četné povrchové a hluboké větve zadní strany stehna. Jednou z variant je též přechod do VCFP a následně pak z mediální strany stehna komunikovat s VSM. Tato poslední varianta se označuje jako Giacominiho žíla. Ve skutečnosti však neexistuje žádná ideální z výše popsaných varianta proximálního ukončení kraniální extenze VSP. Ve většině případů se jedná o jejich kombinaci. V klinice má znalost těchto anatomických poměrů význam především při detekci zdroje refluxu, protože se tak může přenášet reflux z perianálních žil, proximálních stehenních perforátorů, VSM resp. SPJ do VSP. Ve spojitosti s kraniální extenzí bývá někdy popisován tzv. „obrácený výstupní“ reflux z SPJ do VSM nebo varixů zadní strany stehna.
Větve VSP a kraniální extenze
Zde za zmínku stojí jedna osobitná žíla, která byla poprvé popsána Doddem. Jedná se o véna fosae popliteae. Ta probíhá v podkoží po zadní straně lýtka mnohdy paralelně s VSP a ústí odděleně, většinou laterálně, od ní do VP.
Venae perforantes
Perforátory představují spojky mezi hlubokým a povrchovým žilním systémem. Vyznačují se značnou variabilitou ve smyslu stavby, průběhu, spojení, velikostí a taktéž dělením. Je celkem popsáno 40 konstantních perforátorů. Jejich označení je v klinické praxi často nazýváno dle jednotlivých autorů, kterými byly poprvé popsány. Mnohdy tato označení jsou zavádějící a pro přesnou orientaci na končetině nevyhovující. Proto je třeba popisovat jejich pozici topograficky.
- Vena perforantes pedis se dělí na dorzální, mediální, laterální a plantární.
- Venae perforantes malleolaris se označují jako mediální, anteriorní a laterální.
- Venae perforantes cruris rozdělujeme do čtyř základních skupin.
Venae perforantes mediales cruris dělíme na venae perforantes paratibiales a tibiales posteriores. Paratibiální spojují kmen VSM nebo její větve s venae tibiales posteriores nebo svalovými žilami lýtka a leží v blízkosti mediální strany tibie. V minulosti tyto perforátory byly označovány jako Shermanovy perforátory střední části bérce a jako Boydovi perforátory proximálního bérce.
Venae perforantes tibiales posteriores spojují zadní obloukové žíly s vv. tibiales posteriores. V minulosti označované jako Cockettovy perforátory. Místo aby se označovaly čísly I, II, III, je třeba použít dělení topografické, tedy horní, střední a dolní. Venae perforantes anteriores cruris procházejí skrze fascie svalů kompartmentu tibialis anterior a spojují anteriorní větve VSM s vv. tibiales anteriores.
Venae perforantes laterales cruris spojují laterální povrchový žilní plexus s vv. peroneae.
Venae perforantes posteriores cruris se dělí na mediální gastroknemické (na mediální straně lýtka), laterální gastroknemické (na laterální straně lýtka), venae perforantes musculi solei (dříve Mayovy perforátory středního lýtka). Tyto pak spojují žíly m. soleus s VSP. Do této skupiny též patří para-achilární perforátory (dříve Bassiho perforátory) spojující peroneální žíly s VSP.
Venae perforantes genu dělíme na mediální a laterální kolenní perforátory, supra a infrapatelární perforátory a perforátory fossa poplitea.
Venae perforantes femoris se dělí na perforátory adduktorového kanálu na mediální straně stehna (dříve Doddovy perforátory), dále na inguinální perforátory spojující VSM případně její větve s VF, anteriorní stehenní perforátory procházející skrze m. quadriceps femoris, laterální a posteriorní perforátory. Ty poslední se pak dělí na posteromediální (procházejí skrze adduktory), sciatické (jsou ve střední linii dorzálního stehna), posterolaterální, které prochází skrze m. semitendinosus a m. biceps femoris (dříve Hachovy perforátory). Do této skupiny též patří pudendální perforátory.
Venae perforantes glutei se dělí na horní, střední a dolní [14].
Popis lokalizace perforátorů má pro klinickou praxi význam především v případě jejich insuficience, kde jsou jako zdroj refluxu. Zatím však panuje obecná nejednotnost, kdy je vhodné tyto žíly odstranit, či podvázat. Je stanovena definice insuficientního perforátorů, tzn. musí mít průměr > 3mm a musí být detekován regurgitační čas více jak 0,5 s [15]. Chirurgie perforátorů je poměrně pestrá od invazivních postupů až po moderní endovaskulární zákroky. Ty se uplatňují především při řešení nejvyšších stadií žilní insuficience.
ZÁVĚR
Popis povrchového žilního systému, kde je místo patologie popsáno v souladu s topografickými poměry, je pak pro chirurga použitelný k volbě cíleně vedeného zákroku. Je třeba si uvědomit, klinický nález i s použitím tužkového doppleru (continuing wawes CW) má pouze 30% výtěžnost v diagnostice ve srovnání se správně provedenou duplexní sonografií [16]. Precizní mapování povrchového žilního systému se uplatňuje především při moderních endovaskulárních zákrocích, které jsou vedeny čistě cíleně a striktně pod sono kontrolou. Jednotné topografické názvosloví tak poskytuje srozumitelný jazyk mezi diagnostiku provádějícím angiologem a zákrok provádějícím chirurgem. Díky tomu se tak vyhneme situacím, kdy má pacient po operaci ještě větší potíže než před zákrokem. V případě recidivy varikozit je pak možno řešit cíleně příčinu recidivy a prolongovat tak disease free interval na maximum. Obzvláště důležité je takto postupovat u pacientů s ulcerací žilní etiologie, kde správně provedený zákrok vede k urychlení zhojení ulcerace [17]. Znalost anatomických poměrů též umožní správně zhodnotit kontrolní pooperační nález a potvrdit tak správnost provedení zákroku, případně upozornit na rezidua, která zůstala nepovšimnuta. Z tohoto důvodu považujeme za vhodné, když chirurg provádějící intervenci si sám, v rámci přípravy pacienta, dokáže zkontrolovat na duplexní sonografii jednotlivá místa patologie.
MUDr. Jiří Duben, Ph.D.
Lazy I/3360
760 01 Zlín
e-mail: jiriduben@gmail.com
Sources
1. The thigh extensit of the lesser saphenous vein: from Giacomini‘s observations to ultrasound scan imaging. J. Vasc. Surg., 2003; 37 : 558–563.
2. The femoropopliteal vein. Ultrasound anatomy, diagnosis, and office surgery. Dermatos. Surg., 1996; 22 : 57–62.
3. Ambulatory conservative hemodynamic management of varicose veins: critical analysis of results at 3 years. Ann. Vasc. Surg., 2000; 14 : 376–384.
4. Saphenous vein sparing surgery: principles, techniques and results. J. Cardiovasc. Surg., 1998; 39 : 151–162.
5. Einteilung der Rezirkulationen im Bein: anatomische und physiologische Grundlagen der CHIVA-Methode. Phlebologie, 1/2002.
6. Recurrent varicose veins: assessment of the saphenofemoral junction. Br. J. Surg., 1994; 81 : 373–375.
7. Unvermeidbares Rezidiv und Neoreflux nach korrekter Véna saphena magna Crossektomie: Neovaskularisation? Phlebologie, 2003; 32 : 96–100.
8. Naht des Hiatus saphenus und Krossenligatur mit Teflon reduziert die Quote retikularer Magnakrossenrezidive: eine prospektive randomisierte Studie über 5-7 Jahre. Phlebologie, 2007; 36: A8.
9. Closure of the cribriform fascia: an efficient anatomical barrier against postoperative neovascularisation at the saphenofemoral junction? A prospective study. Eur. J. Vasc. Endovasc. Surg., 2007, Sep; 34(3): 361–366.
10. Silicone patch saphenoplasty to prevent repeat recurrence after surgery to treat recurrent saphenofemoral incompetence: long-term follow-up study. J. Vasc. Surg., 2004 Jul; 40(1): 98–105.
11. Early and late complications of silicone patch saphenoplasty at the saphenofemoral junction. J. Vasc. Surg., 2006 Dec; 44(6): 1285–1290.
12. Variations of connections to the saphenous systém in limbs with primary varicose veins: a study in 1481 limbs by duplex ultrasound scanning. J. Phlebol., 2002; 2 : 11–17.
13. Anatomical features of those perforating veins of the leg which frequently or infrequently become incompetent. In: May R, Partsch H, Staubesand J (eds). Perforating veins. München: Urban & Schwarzenberg, 1981 : 49–59.
14. Duplex-Ultraschalluntersuchung der Venen der unteren Extremitäten bei chronischer Veneninsuffizienz; UIP-Konsensusdokument Teil II: Anatomie. Phlebologie, 2006; 35 : 31–42.
15. Investigation of chronic venous insufficiency: A konsensus statement (France, March 5-9, 1997). Circulation, 2000; 102: E126–E163.
16. An evaluation of Doppler ultrasound and photoplethysmography in the investigation of venous insufficiency. Aust. N. Z. J. Surg., 1992; 62 : 270–275.
17. Endovenose Lasertherapie mit dem 980-nm - Diodenlaser bei Ulcus cruris venosum. Phlebologie, 2007; 36 : 177–230.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2010 Issue 11-
All articles in this issue
- Traumatická atlantoaxiálna rotačná fixácia u dieťaťa
- Intratorakální struma – nediagnostikovaná – přece odoperovaná
- Axilárna disekcia v manažmente chirurgickej liečby invazívneho karcinómu prsníka u postmenopauzálnych pacientok
- Torze omenta – neobvyklá příčina náhlé příhody břišní
- Abdominální katastrofa – defekt stěny břišní komplikovaný střevní píštělí – strategie léčby
- Segmentální absence muscularis propria stěny tračníku – vzácná příčina perforace tračníku v těhotenství
- Mucinózní adenokarcinom apendixu – kazuistika
- Intraoperační radioterapie v multimodalitní léčbě lokálně pokročilého karcinomu rekta
- Pětileté sledování nemocných po operaci světlobuněčného karcinomu ledviny
- Lymfatické mapování a biopsie sentinelových uzlin s použitím kombinované metodiky in vivo aplikace Patentblue a radiokoloidu a ex vivo detekce metastatického postižení lymfatických uzlin u kolorektálního karcinomu
- Poranění pánve z pohledu urogynekologie. Souborný referát
- Mapování povrchového žilního systému před a po operaci varixů – literární souhrn specifických aspektů při vyšetřování duplexní sonografií
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Mucinózní adenokarcinom apendixu – kazuistika
- Abdominální katastrofa – defekt stěny břišní komplikovaný střevní píštělí – strategie léčby
- Pětileté sledování nemocných po operaci světlobuněčného karcinomu ledviny
- Torze omenta – neobvyklá příčina náhlé příhody břišní
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

