-
Medical journals
- Career
Použití biodegradabilních materiálů v léčbě kostních cyst u dětí
Authors: L. Plánka; Š. Ondruš; J. Škvařil; D. Starý; P. Gál
Authors‘ workplace: Klinika dětské chirurgie, ortopedie a traumatologie FN Brno, přednosta: prof. MUDr. Petr Gál, Ph. D.
Published in: Rozhl. Chir., 2008, roč. 87, č. 11, s. 585-589.
Category: Monothematic special - Original
Overview
Cíl:
K nejčastějším benigním lytickým kostním procesům ohrožujících pevnost kosti patří juvenilní kostní cysty. Pokud nedojde ke spontánnímu vyhojení cysty, což bývá urychleno po vzniku patologické zlomeniny nebo po zavedení osteosyntetického materiálu do cysty, je nutné provést výplň dutiny cysty. Z minulosti známe mnoho možných náhrad defektu, a to s použitím kortikoidů, autoštěpů, allo-štěpů až po nově zaváděné metody aplikace syntetických anorganických náhradních biomateriálů. Cílem naší studie bylo ověřit možnost použití takového materiálu v léčbě benigních kostních cyst u dětí.Materiál a metodika:
Sledovaný soubor byl tvořen 20 pacienty ve věkovém rozmezí 10–17 let léčených na KDCHOT v letech 2004–2007 pro diagnózu juvenilní kostní cysty aplikací trikalcium fosfátu. Hodnotili jsme počet operací a tím nutných hospitalizací a celkových anestezií, peroperační komplikace, pooperační komplikace, délku hospitalizace a výsledky léčby podle Neerových hodnotících kritérií včetně časového intervalu ke zhojení cysty. Získané výsledky byly navíc hodnoceny v závislosti na lokalizaci cysty.Výsledky:
Z výsledků léčby podle Neerových hodnotících kritérií vyplývá, že 90 % cyst se zhojilo bez nutnosti dalších operačních výkonů. Špatný výsledek – nutnost dalších operačních výkonů z důvodu nestability oslabeného skeletu – byl u 2 pacientů. Peroperační a perioperační komplikace byly nevýznamné, průměrná doba hospitalizace byla 4 dny a průměrná doba do zhojení cysty po primární nebo sekundární perkutánní výplni byla 15 měsíců v rozsahu od 13 do 20 měsíců.Závěr:
Sledovaná metoda aplikace trikalcium fosfátu snižuje počet operací nutných k vyléčení defektu, není zatížena závažnými perioperačními ani peroperačními komplikacemi a lze ji provádět za velmi krátké hopistalizace pacienta.Klíčová slova:
trikalcium fosfát – patologická zlomenina – juvenilní kostní cysta – dětský věkÚVOD
Častým problémem dětské chirurgie a traumatologie jsou patologické zlomeniny v místě kostního defektu, což je nejčastější způsob klinické manifestace jinak benigního lytického procesu kostí dětského a adolescenčního skeletu. Je potom záležitostí spolupráce dětského traumatologa a ortopeda, aby společně stanovili optimální postup léčby a následné péče.
K nejčastějším benigním lytickým kostním procesům ohrožujících pevnost kosti patří juvenilní kostní cysty. Jsou to benigní, tekutinu obsahující kostní dutiny vystlané membránou, která je složena z řídké cévnaté pojivové tkáně s roztroušenými buňkami osteklastického typu. Jsou diagnostikovány většinou v dětském a adolescenčním věku mezi 5. a 20. rokem. Nejčastější lokalitou jsou proximální konce dlouhých kostí a to hlavně proximální humerus a proximální femur. U starších pacientů je lokalizace odlišná, vyskytují se častěji v oblasti patní kosti, pánve, metatarzů nebo metakarpů. Častěji jsou postiženi chlapci v poměru 2 : 1. Juvenilní kostní cysty ohrožují rostoucí skelet poškozením růstových zón kosti a vznikem patologických zlomenin vzhledem k výraznému oslabení kosti.
Dalšími častými benigními procesy ohrožujícími kostní stabilitu jsou neosifikující kostní fibromy, fibrózní dysplazie, enchondromy a aneuryzmatické kostní cysty. Solitární kostní cysta je většinou asymptomatická, bývá často diagnostikována náhodně při RTG vyšetření traumatu nebo až při patologické fraktuře postižené oblasti skeletu. V případě patologické zlomeniny může docházet k částečnému vyplnění dutiny novotvořenou kostí, výjimečně při opakovaných patologických zlomeninách i k vyhojení cysty. Má poměrně charakteristický rentgenový obraz, jedná se o projasnění ohraničené jemnou sklerotickou kostí se ztenčelou kortikalis, může být rozdělena septy různé tloušťky.
Ve většině případů jsme schopni správné diagnostiky již z prostého RTG snímku, při diagnostických rozpacích je indikováno MR vyšetření a eventuálně biopsie.
Z hlediska etiologie je popsána v literatuře možnost traumatické etiologie na podkladě intramedulárního hematomu, mitigované infekce, cystické degenerace benigních kostních lézí, místní poruchy růstu, blokády žilního oběhu nebo synoviální původ léze.
Solitární kostní cysta je afekce, která nikdy nemalignizuje, ale má značnou tendenci k recidivám. Z hlediska vzdáleností kostní cysty od růstové chrupavky přilehlé k cystě jsou náchylné k recidivám cysty vzdálené do 0,5 cm od růstové zóny, tzv. aktivní cysty, z hlediska věku jsou popisovány recidivy hlavně u pacientů do 10 let věku (až 38 %), u pacientů nad 10 let věku pouze kolem 15 %. Nejčastější lokalitou cysty byl humerus a to v jeho diafyzární oblasti po 10. roce věku dítěte, co svědčí o odrůstání cysty od proximální fýzy v dětském věku. Druhou nejčastější lokalitou byl proximální humerus u mladších dětí, následován oblastí proximálního femuru, distální fibuly a patní kosti (Tab. 1).
Table 1. Počet pacientů u jednotlivých anatomických lokalit cyst Tab. 1. Patient rates in individual anatomical cyst locations 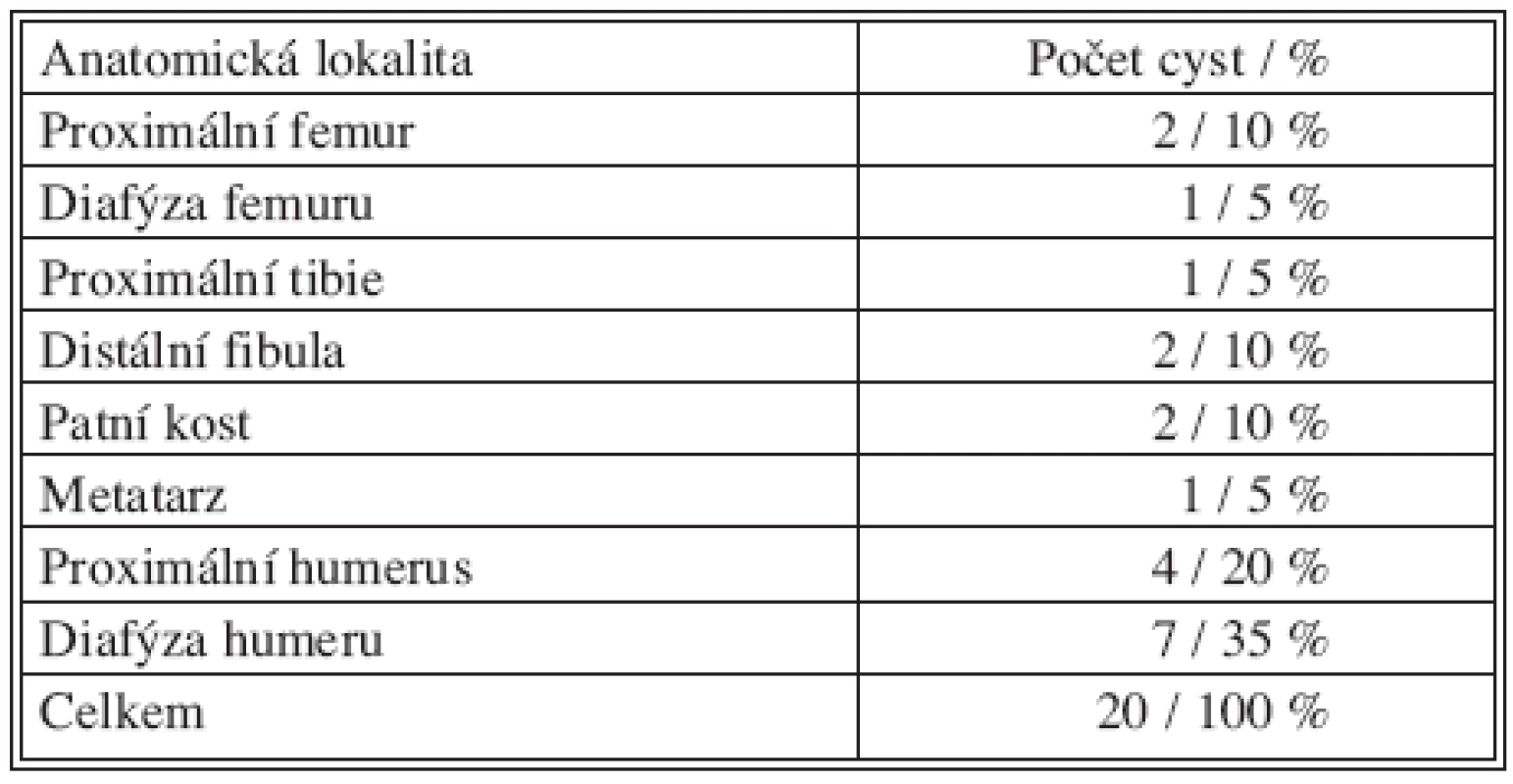
Pokud nedojde ke spontánnímu vyhojení cysty, což bývá urychleno po vzniku patologické zlomeniny nebo po zavedení osteosyntetického matriálu do cysty, je nutné provést výplň dutiny cysty. Z minulosti známe mnoho možných náhrad defektu, a to s použitím autoštěpů, alloštěpů nebo syntetických anorganických náhradních biomateriálů. Scaglietti v roce 1979 publikoval výsledky léčby prostých kostních cyst opakovanou aplikací methylprednisolon acetátu. K použití glukokortikoidu ho vedlo složení tekutiny v cystě, která má charakter transudátu a vliv glukokortikoidů na vstřebávání transudátů při kloubní synovialitidě. Výsledky tříletého sledování cyst u pacientů léčených touto metodou byly velmi slibné, popisoval uspokojivé výsledky u 90 % cyst u kterých došlo k pozitivní reakci na aplikaci na kortikoid a u 60 % došlo prakticky ke kompletnímu zhojení. Tato metoda se stala nejrozšířenější. Další studie uvedené metody léčby juvenilních kostních cyst ale neprokázaly tak vysokou úspěšnost léčby, nicméně její použití se stalo metodou první volby v léčbě kostních cyst na konci 20. století a na některých pracovištích přetrvává dodnes.
Autogenní štěpy jsou kortikální, kortikospongiózní nebo spongiózní štěpy, které jsou odebrány nejčastěji z os ilium, tibie nebo fibuly. Výhodou autoštěpů je vysoká biologická aktivita, rychlá integrace a možnost revaskularizace. Nevýhodou je omezené množství autoštěpů a to hlavně v dětském věku, prodloužení operačního času a zvýšení krevní ztráty, zásah na zdravé končetině s prodloužením rekonvalescence a nebezpečí pooperačních komplikací v oblasti odběru autoštěpů, u dětí i poškození apofýzy kyčelní kosti (Arrington, 1996).
Allogenní štěpy jsou většinou kadaverózního původu, v případě dětí je jinou možností odběr štěpu od rodičů. Po vzniku kostních bank je tato metoda využívána hlavně u masivních kostních defektů, velké strukturální allografty se používají při řešení náhrad části dlouhých kostí a kloubních konců kostí po radikálních resekcích tumorózních afekcí skeletu. Výhodou alloštěpů je možnost naplánování aplikace většího množství i velikosti osteochondrálního allograftu. Nevýhodou je možnost imunogenetické odpovědi příjemce a nebezpečí přenosu nemocí.
Alternativy kostních štěpů v ortopedii a traumatologii můžeme rozdělit na 3 základní skupiny:
1. strukturální kostní náhrady – cementy – polymetylmetakrylát, Norian SRS, TrueBond
2. osteogenní agens
- demineralizovaná kostní matrix (Grafton, Dynagraft) ve formě prášku nebo gelu s osteoindukčními vlastnostmi
- kostní morfogenetické proteiny – rhBMP 2 s povzbudivými in vivo výsledky u psů
- osteogenní protein BMP 7 se slibnými výsledky u lidí při léčbě pseudoartróz a kostních defektů
3. náhrady spongiózní kosti
- kalciumfosfátová keramika
- hydroxyapatit
- kalciumsulfát.
V poslední době se dostávají do popředí zájmu nové resorbovatelné biomateriály, které v organismu postupně degradují a jsou nahrazovány plně funkčním vlastní kostní tkání. Po méně úspěšných začátcích zaznamenala lékařská věda a poslední dobou i klinická praxe velký posun v úspěšnosti aplikací resorbovatelných biomateriálů. Jejich výhodou je, že jsou schopny osteoindukce, čili přirozeného procesu resorpce a novotvorby kosti. Zlepšování biologických vlastností vstřebatelných biokeramik se dosahuje pomocí kolagenních materiálů nebo tkáňových materiálů jako jsou autologní kostní dřeň, nebo specifické kostní morfogenetické proteiny a tkáňové faktory. Jako nejvhodnější biomateriál se zdá být Trikalciumfosfát – Ca3(PO4)2. První experimenty s kalciumfosfátem byli již v roce 1920, výroba jako náhrada kostní tkáně začala od roku 1980. Základními vlastnostmi trikalciumfosfátu při aplikaci in vivo je jeho bioaktivita, schopnost osteokondukce, osteoindukce a resorbovatelnost. Osteoinduktivita materiálu stimuluje vývoj mezenchymálních buněk na kostní buňky a indukuje tak tvorbu nové kostní tkáně (Burger, 2007). V pozdějších stadiích v tělním prostředí v důsledku hydrolytické koroze a aktivní fagocytózy dochází k postupné dezintegraci materiálu a jeho resorpci a nahrazování nově se vytvářející kostní tkání.
Cílem předkládané studie bylo zhodnocení výsledků nové metody léčby juvenilních kostních cyst u dětí aplikací trikalciumfosfátu (ChronOs inject, SYNTHES, Švýcarsko). Sledovali jsme výsledky léčby podle Neerových kritérií, počet nutných operací (aplikací), pooperační komplikace a délku hospitalizace pacienta.
MATERIÁL A METODA
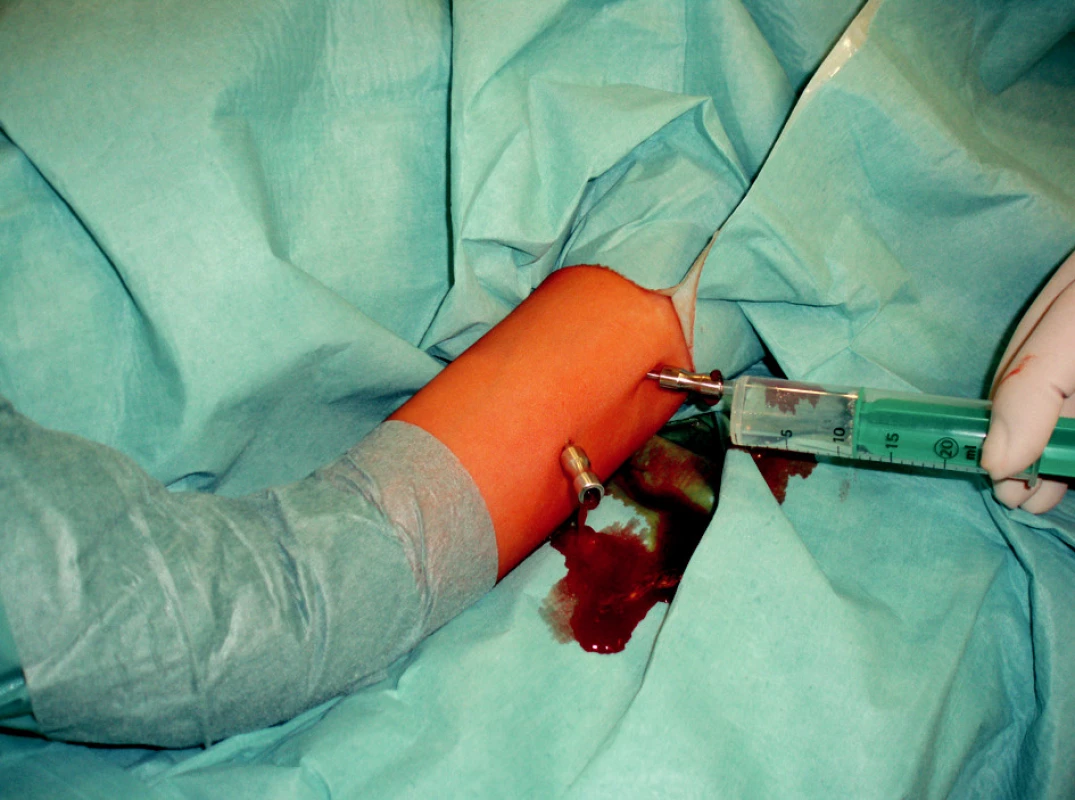
Sledovaný soubor byl tvořen 36 pacienty ve věkovém rozmezí 10–17 let léčených na KDCHOT v letech 2004 – 2007 pro diagnózu benigního kostního defektu aplikací trikalcium fosfátu. Aplikačně výhodná formy trikalcium fosfátu byla na trh uvedena v roce 2004 a KDCHOT je první pracoviště v ČR, které zavedlo jeho použití ve výše uvedených indikacích. Injektabilní forma trikalcium fosfátu (ChronOs inject, SYNTHES, Schwitzerland) je nachystána v aplikačních stříkačkách, nelze ho míchat s dalším substrátem kromě ředící tekutiny, a proto jsme upustili od původně uvažovaného míchání syntetického materiálu s kostní dření. Po standardní přípravě sterilního operačního pole byl punktován jeden pól dutiny cysty punkční jehlou, fixace kostní jehly v kortikalis je většinou pevná, není potřeba další stabilizace. Při velmi jemné stěně cysty je nutné dávat pozor abychom plošně neprolomili kortikalis, vznik defektu by mohl ohrozit perkutánní výplň cysty pro riziko extraosseálního úniku materiálu. Druhá kostní jehla byla zavedena do druhého polu cysty a mohla být provedena laváž celé dutiny s následnou aplikací injektabilního materiálu (Obr. 1).
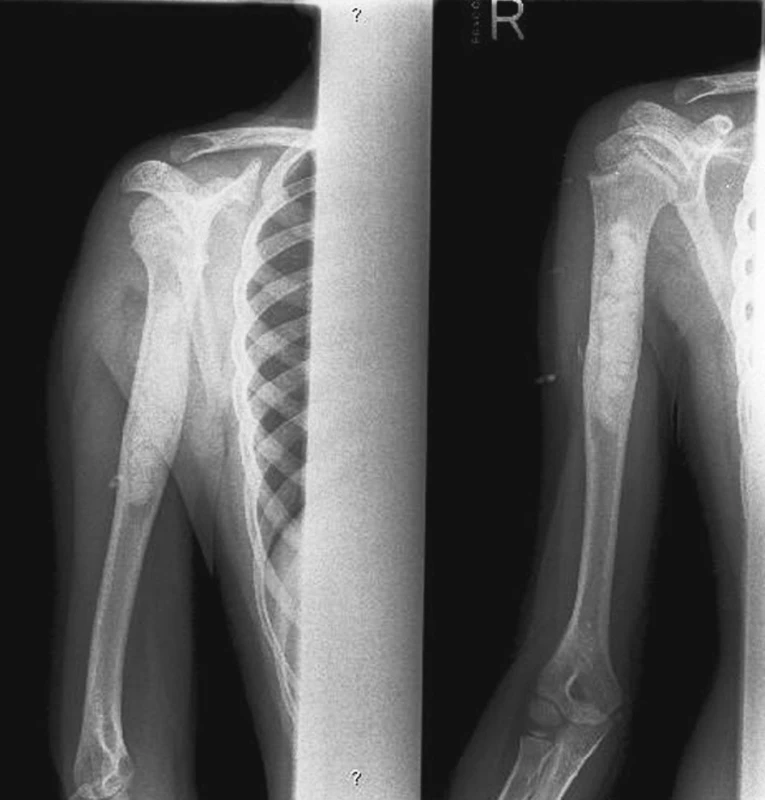
Kontrola pooperačního průběhu byla prováděna za hospitalizace a následně během ambulantních kontrol, výsledky léčby byly sledovány pomocí RTG vyšetření po 3 měsících (Obr. 2). V případě, že nedocházelo k vyhojování cysty, následovala další aplikace se stejnou RTG monitorací.
V souboru pacientů s minninvazivní aplikací ChronOs inject jsme hodnotili počet operací a tím nutných hospitalizací a celkových anestezií, peroperační komplikace, pooperační komplikace, délku hospitalizace a výsledky léčby podle Neerových hodnotících kritérií včetně časového intervalu ke zhojení cysty. Získané výsledky byly navíc hodnoceny v závislosti na lokalizaci cysty.
VÝSLEDKY
U 20 pacientů jsme provedli celkem 23 operačních výkonů. U 2 pacientů se jednalo o opakovaný výkon z důvodu nedostatečného vyplnění cysty při primární výplni, u 1 pacienta pro recidivu cysty po kompletní výplni v oblasti diafýzy humeru (Tab. 2). U 16 pacientů se zhojila cysta po první výplni (80 %), u dalších 2 pacientů došlo ke zhojení po 2. výplni. Z výsledků léčby podle Neerových hodnotících kritérií vyplývá, že 90 % cyst se zhojilo bez nutnosti dalších operačních výkonů (Tab. 3). Špatný výsledek – nutnost dalších operačních výkonů z důvodu nestability oslabeného skeletu byl u 2 pacientů. U obou pacientů se jednalo o cystu v lokalitě diafýzy humeru.
Table 2. Počet cyst a operací v jednotlivých anatomických lokalitách Tab. 2. Numbers of cysts and procedures in individual anatomical cyst locations 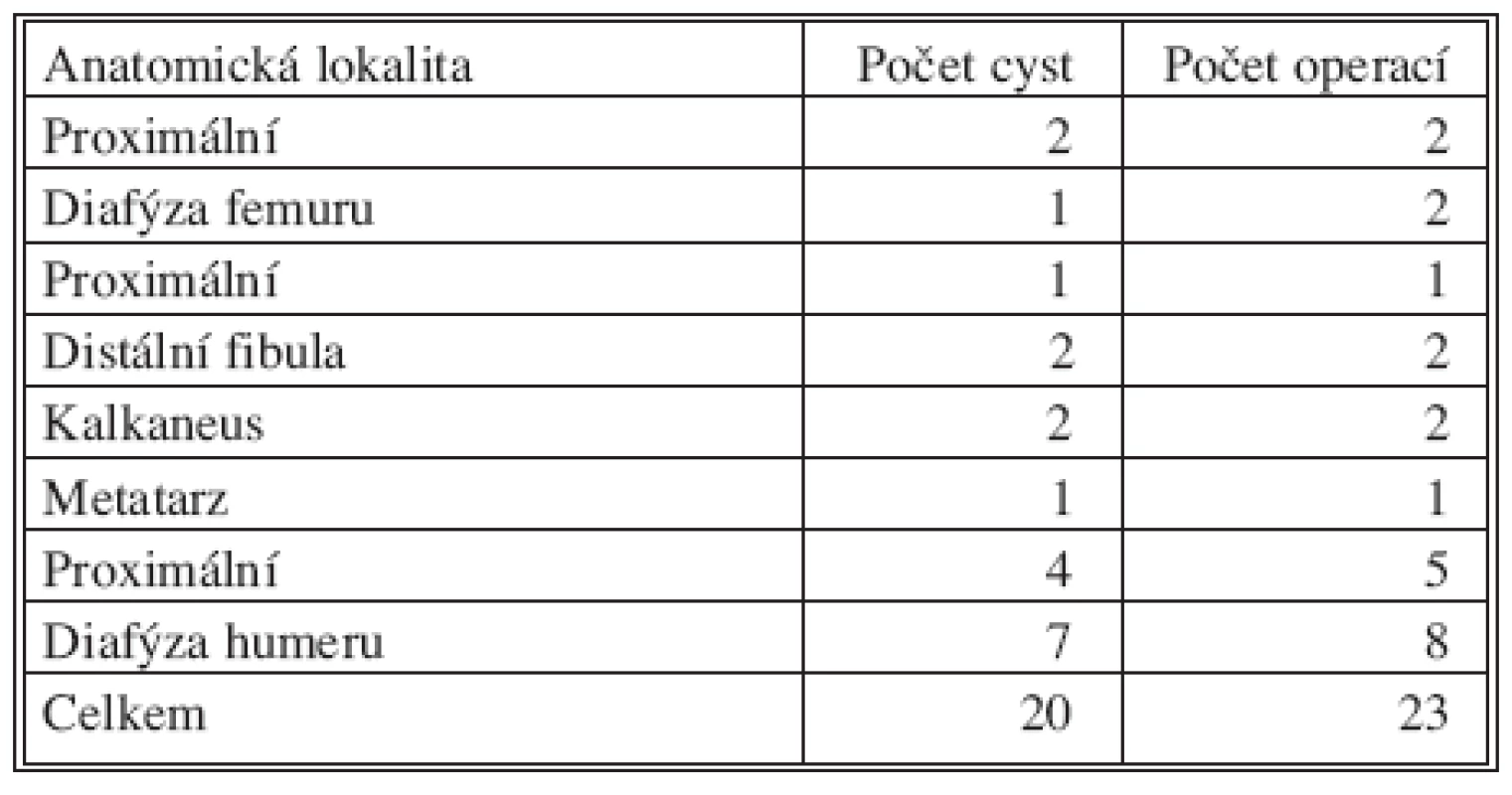
Table 3. Výsledky léčby – Neer klasifikace Tab. 3. Treatment outcomes – Neer classification 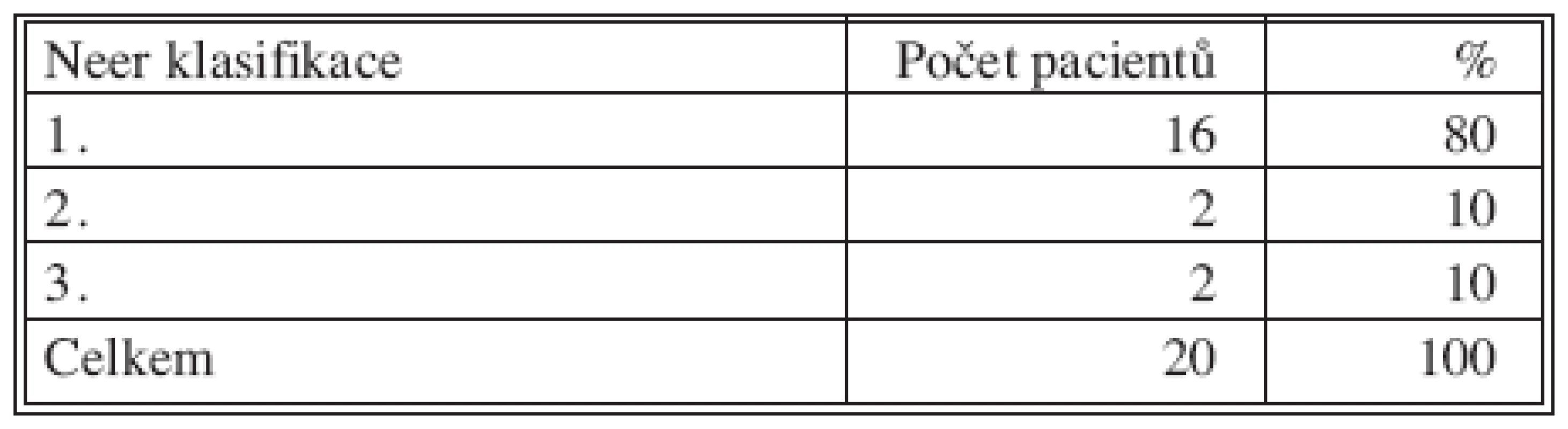
K peroperačním komplikacím řadíme extraosseální únik syntetického materiálu u 2 pacientů, u 1 pacienta únik do oblasti deltoidní burzy při aplikaci do cysty proximálního humeru a u 1 pacienta do burzy pes anserinus při aplikaci do proximální tibie. U obou pacientů byl následně pooperační průběh bez komplikací a extraosseálně aplikovaný materiál se postupně vstřebával bez klinických příznaků.
V rámci pooperačních komplikací jsme zaznamenali bolesti, febrilie a sekreci z oblasti punčních přístupů do cysty. Bolesti v oblasti aplikace trvající více než 1 den od výplně cysty jsme zaznamenali u 5 pacientů. Febrilie nad 38 st. druhý den po aplikaci jsme zaznamenali u 1 pacienta – lokalita diafýzy femuru. U 3 pacientů docházelo po operaci k sekreci z oblasti punkčních přístupů, které se zklidnilo u všech do 14 dnů bez terapie.
Průměrná doba hospitalizace byla včetně opakované aplikace u 3 pacientů 4 dny. Průměrnou dobu hospitalizace u jednotlivých anatomických lokalit ukazuje tabulka 4.
Table 4. Průměrná doba hospitalizace pacientů Tab. 4. Average duration of hospitalization 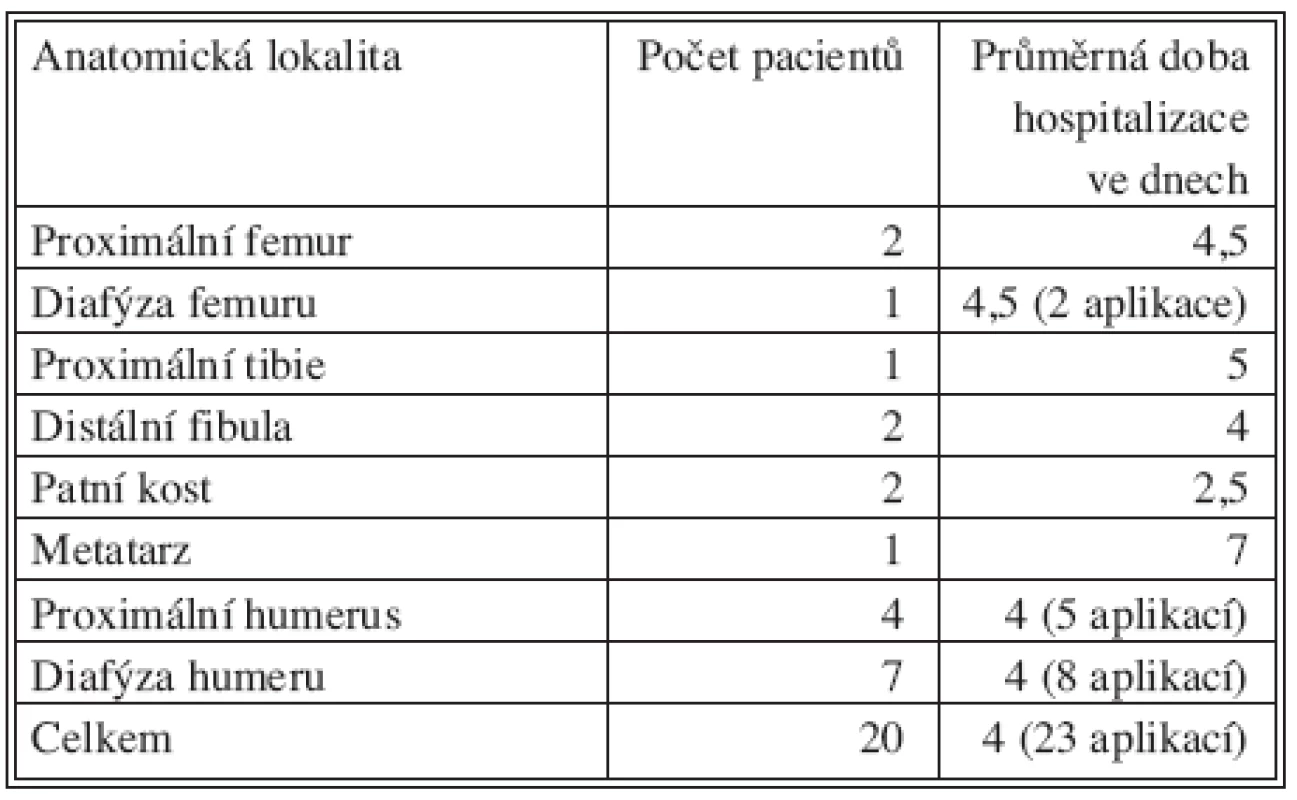
U 18 pacientů se zhojením cysty po primární nebo sekundární perkutánní výplni cysty byla průměrná doba do zhojení 15 měsíců v rozsahu od 13 do 20 měsíců.
DISKUSE
Ve světové literatuře jsou v rámci miniinvazivních metod popisovány nejčastěji punkce kostních cyst s následnou aplikací metyprednisolon acetátu [6, 8], autologní kostní dřeně [2, 3, 7, 9] nebo jenom vícečetné návrty cysty s proplachem. Další možnosti jsou intramedulární transfixace nitrodřeňovými implantáty, aplikace kanalizovaného šroubu k dekompresi cysty izolovaná nebo s exkochleací cysty [5, 1]. Primárně otevřené operace nejsou doporučovány z důvodů vyšších rizik operace. Jsou publikovány výsledky jednotlivých metod a srovnávací studie jednotlivých miniinvazivních metod i metod otevřených operací.
Zhodnocení terapie aplikací steroidů do cysty podává Hashemi-Nejad [8]. Hodnotí metodu u 32 pacientů, 4 pacienti (13 %) zhojeno – Neer 1, 20 pacientů (62 %) – Neer 2 a 8 (25 %) pacientů recidiva – Neer 3. Počet aplikací kolísal mezi jednou a šesti aplikacemi steroidu do cysty, po první aplikaci udává hojení cysty u 13 (41 %) pacientů.
Srovnávací studie aplikace steroidů a aplikace autologní kostní dřeně [9] popisuje úspěšnost při první aplikaci steroidu 23 % a první aplikaci antologní kostní dřeně 52 %, po druhé aplikaci 63 % a 80 %. Průměrný počet aplikací byl 2,19 (1–5) a 1,57 (1–3). Průměrný interval ke známkám hojení cysty byl 12,5 a 14,3 měsíce.
Tsuchyia [10] popisuje metodu otevřené kyretáže cysty z krátkého operačního přístupu a zavedení kanalizovaného šroubu k dekompresi cysty. Z 26 pacientů popisuje recidivu – Neer 3 u 3 pacientů, reziduální defekty u 4 pacientů – Neer 2 a u 19 zhojení cysty – Neer 1. Jedná se však o otevřenou, ne miniinvazivní metodu.
Většina metod dává podobné výsledky léčby, a proto někteří autoři udávají jako hlavní důvod tendence k vyléčení jenom vlastní kostní punkci a dekompresi cysty tímto defektem.
K nové metodě léčby juvenilních kostních cyst nás vedly neuspokojivé výsledky předchozí metody léčby opakovanými punkcemi s aplikací DepoMedrolu s nutností dalších, otevřených operačních výkonů s výplni cyst spongioplastikou. K výplni cyst a dalších benigních kostních defektů skeletu ohrožující stabilitu kosti – hlubších metafyzárních fibrózních defektů, neossifikujících fibromů, enchondromů, defektů u fibrosní dysplazie jsme používali syntetický trikalciumfosfát ve formě ChronOs granulí, které jsme však nemohli využít k miniinvazivní, perkutánní aplikaci. Až možnost využití resorbovatelného tekutého materiálu ChronOs inject, po přípravě ve formě pasty, nás vedla k využití k minninvazivní výplni cyst tímto materiálem. U ostatních benigních defektů nelze využít injektabilní vlastnosti materiálu z důvodu nutnosti exkochleace obsahu defektu. Výhodou oproti ostatním minninvazivním metodám – aplikací steroidů, autologní kostní dřeně, je to, že po zatvrdnutí materiálu při kompletní výplni cysty je oblast cysty stabilnější. Mohli jsme si dovolit, na rozdíl od předchozích metod, při aplikaci v oblasti horních končetin režim bez omezení již po propuštění z hospitalizace a případě aplikace v lokalitě dolních končetin jenom krátkodobé odlehčení s časnou plnou zátěží.
Při zavádění metody u prvních pacientů s mininvazivní výplní jsme měli technické problémy s přípravou materiálu a ztratili jsme celkem 3 balení ChronOs injectu, důvodem byli technické problémy při míchání, časování přípravy materiálu a problémy s aplikační pistolí. Po získání praktických zkušeností s přípravou a aplikací jsme již technické problémy neměli.
Bolest v pooperační péči byla zaznamenána pacienty jako bolest tlakového charakteru, kterou si vysvětlujeme přetlakem v dutině původní cysty při kompletní výplni aplikační tlakovou pistolí. Terapií bylo podávání analgetik, po kterých potíže postupně odeznívali. Terapií febrílií u jednoho pacienta bylo prolongované podávání antibiotik na rozdíl od profylaktického podání u ostatních pacientů bez dalších komplikací.
Délka hospitalizace byla hlavně na začátku studie delší, abychom mohli monitorovat eventuální pooperační komplikace, následně jsme postupně dobu hospitalizace zkracovali. Jsme přesvědčeni, že metoda léčby popisována ve studii je možná perspektivně i v rámci jednodenní hospitalizace vzhledem k příznivému pooperačnímu průběhu.
ZÁVĚR
Naše klinická studie ukazuje velmi dobré výsledky léčby benigních kostních defektů u dětí novou metodou miniinvazivní aplikace injektabilního trikalcium fosfátu. Tato metoda snižuje počet operací nutných k vyléčení defektu, není zatížena závažnými perioperačními ani peroperačními komplikacemi a lze ji provádět za velmi krátké hospitalizace pacienta. Na základě těchto výsledků a na základě výsledku obdobných studií byla tato metoda stanovena jako metoda první volby při léčbě benigních kostních defektů na naší klinice.
MUDr. L. Plánka, Ph.D.
Kamínky 13
634 00 Brno
e-mail: lplanka@seznam.cz
Sources
1. Ahn, J. I., Park, J. S. Pathological fractures secondary to unicameral bone cysts. Int. Orthop., 1994; 18 : 20–22.
2. Arazi, M., Senaran, H., Memik, R., Kapicioglu, S. Minimally invasive treatment of simple bone cyst with percutaneous autogenous bone marrow injection. Orthopaedics, 2005; 28 : 108–202.
3. Arrington, E. D., et al. Complications of iliac crest bone graft harvesting. Clin. Orthop., 1996; 329 : 300–309.
4. Burger, E. L., Patel, V. Calcium phosphates as bone graft extenders. Orthopedics, 2007; 30; 939–943.
5. Campanacci, M., Capanna, R., Picci, P. Unicameral and aneuryzmal bone cysts. Clin. Orthop., 1986; 204 : 25–36.
6. Chang, C. H., Stanton, R. P., Glutting, J. Unicameral bone cysts treated by injection of bone marrow or methylprednisolone. J. Bone Joint Surg. /Br/, 2002; 84-B: 407–412.
7. Docquier, P. L., Delloye, C. Treatment of simple bone cysts with aspiration and a single bone marrow injection. J. Pediatr. Orthop., 2003; 23 : 766–773.
8. Hashemi-Nejad, A., Cole, W. G. Incomplete healing of simple bone cysts after steroid injections. J. Bone Joint Surg. /Br/, 1977; 79-B: 727–730.
9. Cho, H. S., Oh, J. H., Kim, H. S., Kang, H. G., Lee, S. H. Unicameral bone cysts: s comparison of injection of steroid and rafting with autologous bone marrow. J. Bone Joint Surgery /Br/, 2007; 89, 222–226.
10. Tsuchyia, H., Abdel-Wanis, M. E., Uehara, K., Tomita, K., et al. Cannulation of simple bone cyst. Joural of bone and joint Surgery (Br), 2002; 84 : 245–248.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2008 Issue 11-
All articles in this issue
- Miniinvazivní chirurgie v České republice
- Závislost úbytku hmotnosti na velikosti neožaludku po laparoskopické bandáži žaludku
- Biliárny ileus – naďalej reálna komplikácia cholecystolitiázy
- První výsledky studie bipolární RFITT koagulace vyšších vyšších stadií hemoroidální nemoci
- Operační léčba zlomenin diafýzy humeru
- Použití biodegradabilních materiálů v léčbě kostních cyst u dětí
- Hybridní roboticky asistovaná operace, aortobifemorální bypass s rekonstrukcí kýly v jizvě
- Kontinentní nálevové stoma u dětí s dysfunkcí pánevních orgánů
- Terapie lymfokély po transplantaci ledviny
- Výsledky transperitoneální laparoskopické nefrektomie pro renální adenokarcinom
- Poranění růstové zóny proximální tibiální epifýzy v dětském věku a možnosti její léčby
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Použití biodegradabilních materiálů v léčbě kostních cyst u dětí
- Biliárny ileus – naďalej reálna komplikácia cholecystolitiázy
- Operační léčba zlomenin diafýzy humeru
- Miniinvazivní chirurgie v České republice
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career