-
Medical journals
- Career
Léčba infekce cévní protézy a aorto-enterické píštěle jako pozdní komplikace rekonstrukčního výkonu na abdominální aortě – kazuistika
Authors: S. Wasiková; R. Staffa; Z. Kříž; P. Piskač
Authors‘ workplace: II. chirurgická klinika, FN u sv. Anny v Brně, přednosta: doc. MUDr. Z. Gregor, CSc.
Published in: Rozhl. Chir., 2007, roč. 86, č. 10, s. 522-524.
Category: Monothematic special - Original
Overview
Infekce cévní protézy je závažným diagnostickým a terapeutickým problémem. Včasná diagnóza a adekvátní léčba je zásadní pro osud pacienta. Prezentujeme kazuistiku šedesátiletého muže s infekcí aortobifemorální protézy a aortoduodenální píštělí. Infekce protézy byla potvrzena metodou FDG-PET. Následně dochází k masivnímu krvácení do trávicího traktu, pacient je indikován k urgentnímu chirurgickému výkonu. Je provedena totální explantace bifurkační protézy a pro rozvoj ischemie dolních končetin následuje v jedné době axilobifemorální bypass. Pacient je 8 měsíců po operaci v dobré kondici, bez pohybového omezení.
Klíčová slova:
aorto-enterální píštěl – infekce cévní protézy – FDG-PET – axilobifemorální bypassÚVOD
Infekce cévní protézy patří k nejzávažnějším a nejobávanějším komplikacím v tepenné rekonstrukční chirurgii. Preventivní antibiotická terapie může riziko redukovat, nikoliv však eradikovat. Incidence se pohybuje v rozmezí 1–6 %. Pacienti většinou přicházejí s nespecifickými symptomy a prodleva v léčbě může vést k život ohrožující sepsi nebo ke krvácení. Terapeutický postup při infekci cévního implantátu závisí na mnoha faktorech jako jsou akutnost stavu, lokalizace a rozsah infekce a virulence infekčního agens.
KAZUISTIKA
Šedesátiletý muž po implantaci aorto-bifemorální protézy před sedmi lety pro Lerichův syndrom byl na naši ambulanci přivezen RZP pro kolapsový stav nejasné etiologie a náhle vzniklou bolest pravé dolní končetiny. V laboratorních nálezech byla zjištěna anémie a leukocytóza. Při vyšetření per rectum byla zjištěna enteroragie. Bylo provedeno gastrofibroskopické vyšetření s nálezem drobné slizniční fisury na gastroezofageálním přechodu a bulbitidy duodena. Při kolonoskopickém vyšetření byly sneseny polypy. Uvedená vyšetření však neprokázala jednoznačný zdroj krvácení. Kardiální příčina kolapsového stavu byla vyloučena. Ultrazvukové vyšetření dutiny břišní ukázalo v místě anastomózy cévní protézy k aortě hypoechogenní lem šíře do 1 cm, jenž byl verifikován pomocí vyšetření CT (Obr. 1). Bylo vysloveno podezření na pseudoaneuryzma v místě anastomózy v důsledku infekce cévní protézy při možné aorto-duodenální píštěli, která však gastrofibroskopicky nalezena nebyla. Infekce cévní protézy byla následně potvrzena fluorodeoxyglucoso pozitronovou emisní tomografií (FDG-PET). Na FDG-PET scanech se zobrazuje hypermetabolická tkáň v okolí aortobifemorální protézy (Obr. 2), což svědčí pro přítomnost zánětu. Následující den se u pacienta, předtím oběhově stabilního, náhle objevuje hemateméza a čerstvá melena provázená poklesem krevního tlaku. Stav vyžadoval urgentní chirurgickou revizi.
Image 1. Předoperační CT: lem v místě anastomózy cévní protézy k aortě šíře do 1 cm Fig. 1. Preoperative CT: 1 cm wide margin at the point of the upper anastomosis 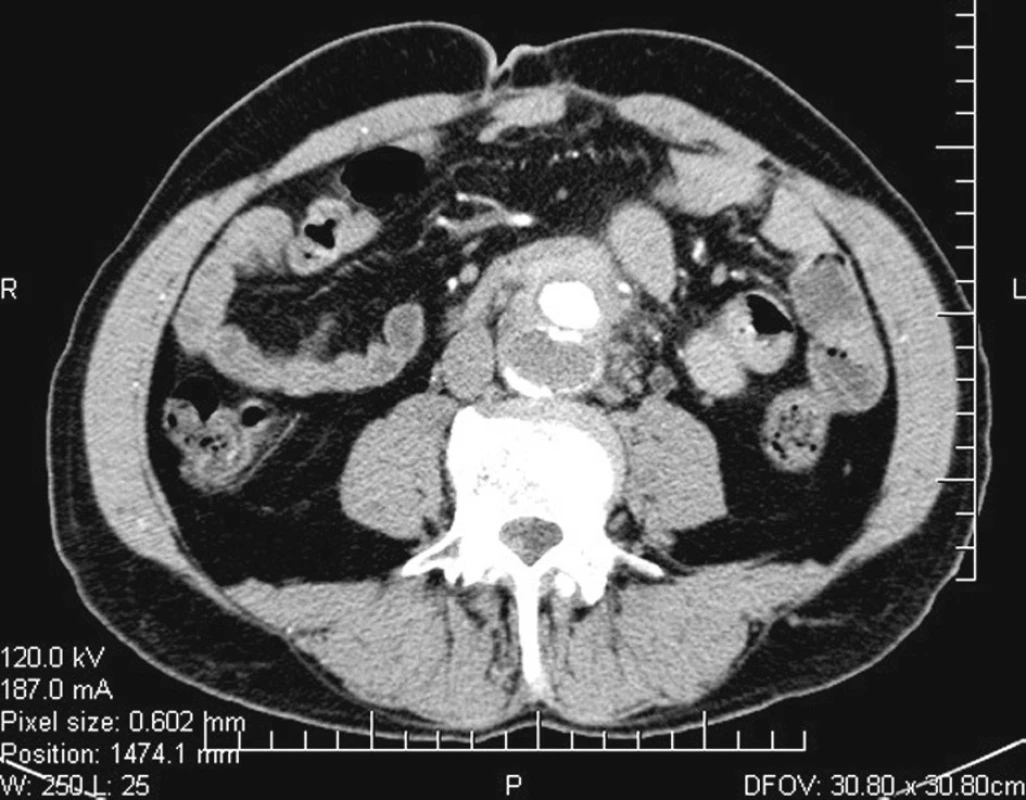
Image 2. Předoperační FGD-PET scan zobrazuje hypermetabolickou tkáň v okolí aortobifemorální protézy Fig. 2. Preoperative FDG-PET scan shows hypermetabolic tissue in the neighbourhood of the aortobifemoral prosthesis 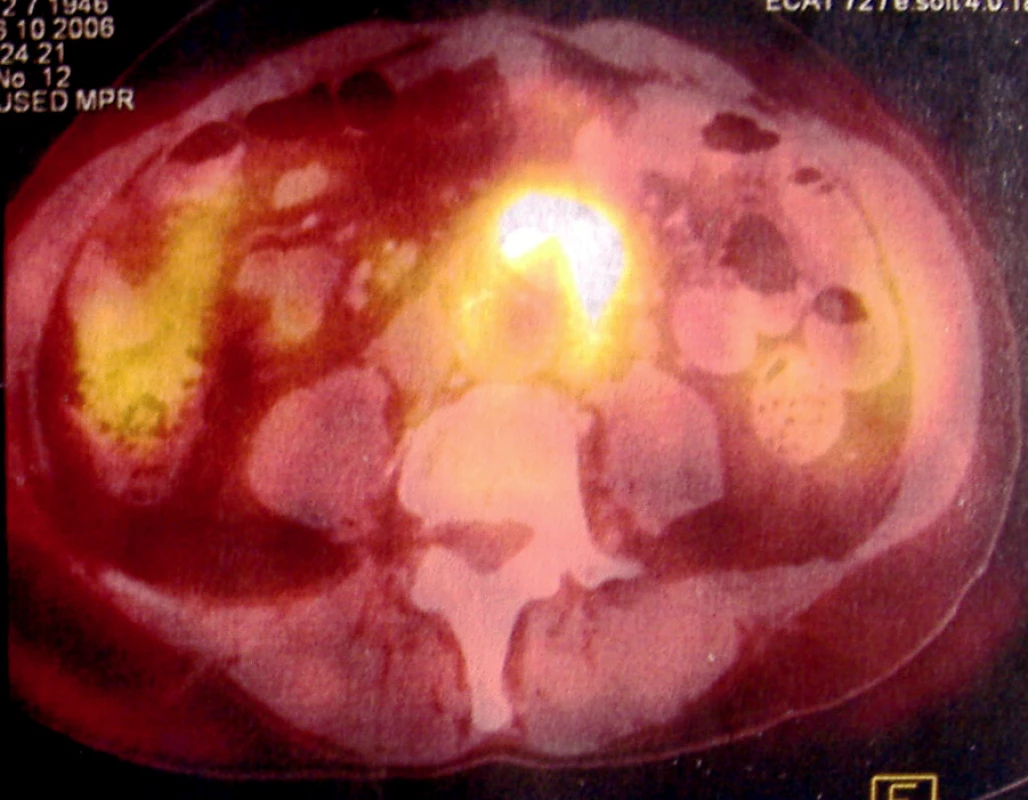
Při operačním výkonu byl potvrzen zapáchající purulentní absces kolem cévní protézy a aortoduodenální píštěl s otvorem v duodenu velikosti 3 cm s navalitými chronickými okraji. Vzhledem k evidentní vysoké virulenci infekce bylo rozhodnuto o totální explantaci aortobifemorální protézy s následnou suturou abdominální aorty subrenálně a suturou duodena. Krvácení z aorty bylo zastaveno, pacient se tlakově stabilizoval. Dochází však k rychlému rozvoji těžké ischemie obou dolních končetin, proto bylo v jedné době po přerouškování pacienta přistoupeno ke druhé fázi operace, při které byl implantován axilobifemorální bypass nestlačitelnou protézou zleva. Pro rozvoj compartment syndromu byla provedena fasciotomie bérce levé dolní končetiny, po které se u pacienta rozvíjí akutní respirační selhání zřejmě v důsledku reperfuze předtím ischemických dolních končetin. Postupně byl pacient hemodynamicky stabilizován, operační rány se zhojily per primam. Vzhledem k obavě z reinfekce v tříslech byla po konzultaci s antibiotickým střediskem nasazena odpovídající dlouhodobá antimikrobiální terapie. Pro vyloučení přítomnosti abscesu v břiše a v malé pánvi bylo 10. pooperační den provedeno CT vyšetření (Obr 3, 4). Postupně dochází k poklesu zánětlivých markerů. Defekt po fasciotomii na bérci je překryt Tierschovou plastikou. Pacient chodí, je propuštěn do domácího ošetřování. Osm měsíců po operaci je v dobré kondici, bez pohybového omezení s kvalitními pulzacemi na periferii obou dolních končetin.
Image 3. Pooperační CT: nejsou známky abscesu v retroperitoneu po explantaci infikované protézy. Laterálně vlevo v příčném řezu zachycený průchodný axilobifemorální bypass nestlačitelnou protézou vedený podkožím Fig. 3. Postoperative CT: there are no signs of an abscess in the retroperitoneum after removal of the infected prosthesis. Laterally left in a transverse slice there is a patent axillobifemoral bypass with an incompressible prosthesis passing through a subcutaneous tunnel 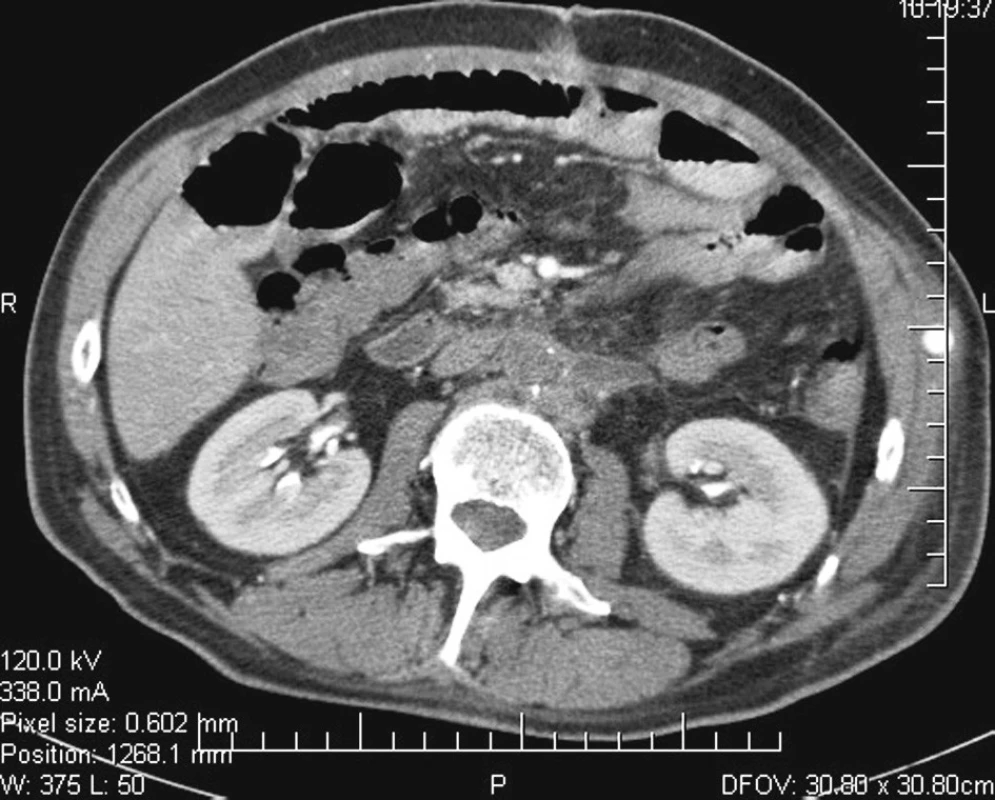
Image 4. Pooperační CT: nejsou známky abscesu v malé pánvi. Laterálně vlevo v příčném řezu zachycená bifurkace průchodného axilobifemorálního bypassu Fig. 4. Postoperative CT: there are no signs of an abscess in the pelvic cavity. Laterally left in a transverse slice, we can see the bifurcation of a patent axillo-bifemoral bypass 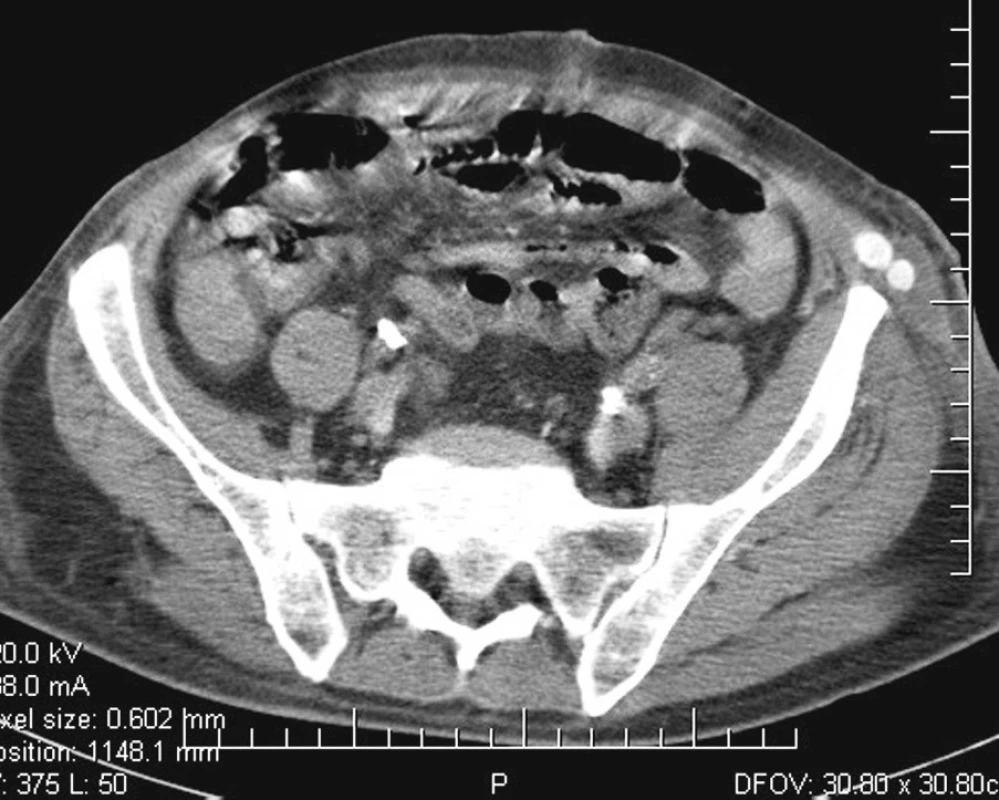
DISKUSE
Včasná diagnóza infikované cévní protézy je pro další osud pacienta zásadní. Diagnóza se kromě klinického a laboratorního nálezu opírá o ultrasonografii, CT nebo MR vyšetření. Další možností jak odhalit infekci cévní protézy je vyšetření metodou FDG-PET. Metoda je založena na detekci akumulace radioizotopem značených leukocytů v místě zánětu, kde je patrná zvýšená utilizace glukózy. FDG-PET se doporučuje v případech, kdy jiné zobrazovací metody nevedly k jednoznačnému závěru [1, 2].
Sekundární aortoenterická píštěl po cévní rekonstrukci na břišní aortě není častou, ale potenciálně fatální komplikací. Hlavním manifestním příznakem je často intermitentní krvácení do trávicího ústrojí. Na možnost aortoenterální píštěle by mělo být vždy pomýšleno u pacientů po implantované cévní protéze v oblasti břišní aorty s příznaky gastrointestinálního krvácení, přičemž gastrofibroskopický nález může být často negativní [3]. Pro detekci píštěle a včasnou diagnózu je proto vhodné kombinovat endoskopické vyšetření s CT nebo MR vyšetřením. Jediným možným řešením aortoenterální píštěle je chirurgická léčba [4, 5].
Cílem při terapii infikované cévní protézy je zachování života pacienta a jeho končetin. K dosažení tohoto cíle je nutná eradikace infekce a zároveň zajištění adekvátního prokrvení končetin pomocí vhodně zvolené tepenné rekonstrukce [6].
Klasická léčba spočívá v explantaci infikované náhrady a následné extra-anatomické rekonstrukci nejčastěji axilobifemorální. Po explantaci bifurkační protézy je aorta pod renálními tepnami uzavřena a odizolována od okolí omentoplastikou. V případě duodenálního defektu se úsek s píštělí exciduje a uzavírá dvojvrstevnou anastomózou, u rozsáhlejších defektů duodena je možno použít gastrojejunální Roux anastomózu. Hlavní výhodou extraanatomické rekonstrukce cévní protézou je minimalizace času, kdy jsou končetiny ischemizované, rekonstrukce je však ohrožena reinfekcí a je zatížena nižší dlouhodobou průchodností.
U nízkovirulentních infekcí je akceptovatelnou variantou parciální resekce cévní protézy a její in situ náhrada Rifampicinem napuštěnou cévní protézou nebo tzv. stříbrnou protézou, vždy s následnou omentoplastikou [7]. Jinou, zatím však obecně málo používanou variantou, je extirpace protézy a její náhrada čerstvým tepenným allograftem nebo štěpem z vena femoralis superficialis [8, 9, 10].
ZÁVĚR
Včasná diagnóza a adekvátní chirurgická léčba infekce cévní protézy je rozhodující pro osud pacienta. Nejnovější nukleární diagnostické metody (FDG-PET) umožní stanovit diagnózu dříve, než se infekce u pacienta plně rozvine. Totální explantace infikované cévní protézy, sutura duodena a následná extra-anatomická rekonstrukce nadále zůstává metodou volby léčby pacientů s aortoenterální píštělí a infikovanou aortální náhradou.
MUDr. S. Wasiková
II. chirurgická klinika FN u sv. Anny
Pekařská 53
656 91 Brno
e-mail: sabina.wasikova@fnusa.cz
Sources
1. Fukuchi, K., Ishida, Y., Higashi, M., Tsunekawa, T., Ogino, H., Minatoya, K., Kiso, K., Naito, H. Detection of aortic graft infection by fluorodeoxyglucose positron emission tomography: Comparison with computed tomographic findings. J. Vasc. Surg., 2005, Nov; 42(5): 919–925.
2. Štádler, P., Bělohlávek, O., Špaček, M., Michálek, P. Diagnosis of vascular prosthesis infection with FDG-PET/CT. J. Vasc. Surg., 2004; 40 : 1246–1247.
3. Probst, A., Bittinger, M., Eberl, T., Jakob, R., Zinkl, K., Heiss, A., Eser, R., Häckel, T., Messmann, H. Aortoduodenal fistula as a cause of gastrointestinal bleeding – difficulties in endoscopic diagnosis. Zeitschrift für Gastroenterologie, 2006, Mar; 44(3): 239–244.
4. Limani, K., Place, B., Philippart, P., Dubail, D. Aortoduodenal fistula following aortobifemoral bypass. Acta Chir. Belg., 2005, Apr; 105(2): 207–209.
5. Armstrong, P., Back, M., Wilson, J., Shames, M., Johnson, B., Bandyk, D. Improved outcomes in the recent management of secondary aortoenteric fistula. J. Vasc. Surg., 2005, Oct; 42(4): 660–666.
6. Bliziotis, I. A., Kapaskelis, A. M., Kasiakou, S. K., Falagas, M. E. Limitations in the management of aortic graft infections. Ann. Vasc. Surg., 2006, Sep; 20(5): 669–671. Epub, 2006 ,May 27.
7. Oderich, G., Bower, T., Cherry, K., Panneton, J. Jr., Sullivan, T., Noel, A., Carmo, M., Cha, S., Kalra, M., Gloviczki, P. Evolution from axillofemoral to in situ prosthetic reconstruction for the treatment of aortic graft infections at a single center. J. Vasc. Surg., 2006, Jun; 43(6): 1166–1174.
8. da Gama, A. D., Rosa, A., do Carmo, G., Moura, C. The use of superficial femoral veins in reconstructive surgery of aortic prosthesis infection (Clagett‘s operation). Rev. Port Cir. Cardiotorac. Vasc., 2004, Apr-Jun; 11(2): 101–105.
9. D’Addio, V. J., Clagett, G. P. Surgical Treatment of the Infected Aortic Graft: Introduction. ACS Surgery Online. 2002; ©2002
10. Clagett, G. P., Valentine, R. J., Hagino, R. T. Autogenous aortoiliac/femoral reconstruction from superficial femoral-popliteal veins: feasibility and durability. J. Vasc. Surg., 1997, Feb; 25(2): 255–266; discussion 267–270.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2007 Issue 10-
All articles in this issue
- Interdisciplinární přístup k řešení mnohočetných tepenných aneuryzmat u pacienta s osmou recidivou incizionální kýly – kazuistika
- Endovaskulární léčba stenóz karotických tepen s použitím cerebrální protekce: pětileté zkušenosti
- Léčba infekce cévní protézy a aorto-enterické píštěle jako pozdní komplikace rekonstrukčního výkonu na abdominální aortě – kazuistika
- Biliárny ileus – zriedkavá komplikácia cholecystolitiázy
- Role intersticiální brachyterapie v multimodalitní léčbě solidních tumorů
- Chirurgická léčba karcinomu prsu v MOÚ
- Nádorová kmenová buňka – nový pohled v onkologii?
- Nový přístup k léčbě jaterních metastáz: manuálně asistovaná laparoskopická radiofrekvenční resekce jater
- Autofluorescenčná videotorakoskopia – prvé vlastné skúsenosti
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Biliárny ileus – zriedkavá komplikácia cholecystolitiázy
- Chirurgická léčba karcinomu prsu v MOÚ
- Endovaskulární léčba stenóz karotických tepen s použitím cerebrální protekce: pětileté zkušenosti
- Nádorová kmenová buňka – nový pohled v onkologii?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

