-
Medical journals
- Career
Rituximab v liečbe primárnych glomerulopatií – naše skúsenosti
Authors: Karol Graňák 1; Matej Vnučák 1; Margaréta Pytliaková 2; Udovít Laca 1; Marián Mokáň 3; Ivana Dedinská 1
Authors‘ workplace: Chirurgická klinika a Transplantačné centrum, Univerzitná nemocnica Martin a Jesseniova lekárska fakulta, Univerzity Komenského 1; Klinika anesteziológie a intenzívnej medicíny, Univerzitná nemocnica Martin a Jesseniova lekárska fakulta, Univerzity Komenského 2; I. interná klinika, Univerzitná nemocnica Martin a Jesseniova lekárska fakulta Univerzity Komenského 3
Published in: Vnitř Lék 2021; 67(E-3): 3-7
Category: Original Contributions
Overview
Úvod: Od roku 2012, keď iniciatíva „The Kidney Disease: Improving Global Outcomes publikovala prvé odporúčania pre manažment a liečbu glomerulárnych chorôb, došlo k enormnému pokroku v porozumení patogenézy, identifikácii nových diagnostických biomarkerov a liečbe týchto ochorení. Rituximab sa stal liečebnou možnosťou so sľubným efektom u pacientov s primárnymi chorobami glomerulov, čo potvrdzujú viaceré klinické štúdie, kde viedol k významnej redukcii proteinúrie a zníženiu incidencie relapsov základného ochorenia. V práci prezentujeme naše skúsenosti s liečbou rituximabom.
Materiál a metódy: Retrospektívne sme analyzovali 9 pacientov s primárnou glomerulopatiou rezistentnou na štandardnú imunosupresívnu liečbu, u ktorých bol podaný rituximab ako rescue liečba. Vyhodnotili sme vplyv indukčnej liečby rituximabom na vývoj kvantitatívnej proteinúrie (KVPÚ).
Výsledky: Vyhodnotením 24 hodinovej KVPÚ pred začatím liečby a po jej ukončení sme v našej skupine pacientov dokázali štatisticky signifikantný pokles KVPÚ ihneď po poslednej dávke rituximabu. Nezaznamenali sme významnú zmenu obličkových funkcií.
Záver: Rituximab predstavuje účinnú alternatívu v terapeutických postupoch primárnych glomerulopatií, obzvlášť v prípadoch rezistencie na štandardnú imunosupresívnu liečbu, s čím sa stotožňujú aj nami prezentované klinické skúsenosti.
Klíčová slova:
primárna glomerulopatia – Proteinuria – rituximab
Zoznam skratiek
ANCA – antineutrophil cytoplasmic antibody – protilátka proti cytoplazme neutrofilov
anti-PLA2R – protilátky proti receptorom pre fosfolipázu A2
CB – celkové bielkoviny
CKD-EPI – chronic kidney disease – epidemiology collaboration
CNI – calcineurin inhibitor – kalcineurínový inhibítor
eGFR – estimated glomerular filtration rate – glomerulárna filtrácia
FSGS – fokálno-segmentálna glomeruloskleróza
CHCHO – chronická choroba obličiek
CHKaTC – Chirurgická klinika a Transplantačné centrum
Ig – imunoglobulín
KDIGO – the kidney disease: improving global outcomes
KVPÚ – kvantitatívna proteinúria
MENTOR – Membranous Nephropathy Trial of Rituximab
MMF – mykofenolát mofetil
MPGN – membráno-proliferatívna glomerulonefritída
TAC – tacrolimus – takrolimus
THSD7A – protilátky proti doméne trombospondínu typu I obsahujúcej proteín 7A
TO – transplantácia obličky
UNM – Univerzitná nemocnica Martin
Úvod
Od roku 2012, keď iniciatíva „The Kidney Disease: Improving Global Outcomes (KDIGO) publikovala prvé odporúčania pre manažment a liečbu glomerulárnych chorôb, došlo k enormnému pokroku v porozumení patogenézy, identifikácii nových diagnostických biomarkerov a liečbe týchto ochorení (1). Napríklad, už ich nie je možné viac aplikovať v prípade idiopatickej membánovej nefropatie, ako vyplýva zo záverov pracovnej skupiny KDIGO 2019. Tento fakt vychádza z objavu nových autoprotilátok proti receptorom pre fosfolipázu A2 (anti-PLA2R), ktoré umožňujú monitoring ochorenia, ako aj z výsledkov recentných klinických štúdií, komparatívnych kohortových štúdií a meta-analýz (2). Pravdepodobne najviac prelomovou z nich bola štúdia MENTOR (Membranous Nephropathy Trial of Rituximab) porovnávajúca rituximab a cyklosporín A, ktorá poukázala na nadradenosť liečby rituximabom v účinnosti a bezpečnosti (3).
Membránová nefropatia je najčastejšou príčinou nefrotického syndrómu v kaukazskej rase, ktorá v 40 až 50 % prípadov progreduje v priebehu 10 rokov do terminálneho štádia chronickej choroby obličiek (CHCHO) (4). Celkovo 70 až 80 % týchto pacientov má cirkulujúce protilátky anti-PLA2R a 1 až 3 % má protilátky proti doméne tombospondínu typu I obsahujúcej proteín 7A (THSD7A) (5, 6). Podľa KDIGO odporúčaní je indikovaná imunosupresívna liečba po úvodnej podpornej terapii v prípade perzistujúceho nefrotického syndrómu (7). Jednou z možností je podávanie glukokortikoidov v alternujúcom režime a cyklofosfamidu, ktoré sa však spájajú s klinicky významnými nežiaducimi účinkami (2). Druhou efektívnou možnosťou, preferovanou v USA a Kanade, sú kalcineurínové inhibítory (CNI – calcineurin inhibitors). Ich ukončenie je však asociované so zvýšenou incidenciou relapsu aktívnej nefropatie (8). V prípade membránoproliferatívnej glomerulonefritídy (MPGN) je podľa súčasných odporúčaní zvažovaná liečba kortikoidmi, cytotoxickými preparátmi s alebo bez plazmaferézy v štádiu nefrotickej proteinúrie s poklesom renálnych funkcií. Pre použitie mykofenolát mofetilu (MMF), cyklosporínu A a takrolimu sú dostupné len obmedzené klinické dáta, a v konečnom dôsledku sa zdá byť celkový benefit štandardnej imunosupresívnej terapie pri MPGN značne limitovaný a kvalita evidencie je slabá (9). Častým glomerulárnym ochorením je fokálno-segmentálna glomeruloskleróza (FSGS), ktorá je identifikovaná v 35 % bioptických nálezov u dospelých s idiopatickým nefrotickým syndrómom (10). U pacientov po transplantácii obličky (TO) je spojená s vysokou mierou rekurencie v štepe. Recentná multicentrická medzinárodná štúdia TANGO zistila 32 % incidenciu rekurencie FSGS v transplantovanej obličke s následnou mierou straty funkcie štepu 39 % (11). Primárnou liečbou je podávanie kortikoidov, v prípade kontraindikácie CNI. Steroid-rezistentná forma FSGS je častá, vyskytuje sa v 40–60 % prípadov, indikované sú CNI alebo iné alternatívne preparáty ako cyklofosfamid alebo MMF (10).
V posledných rokoch sa v manažmente glomerulárnych chorôb upriamila pozornosť na biologickú liečbu namierenú voči B lymfocytom. Rituximab je monoklonálna protilátka viažúca sa na CD20 receptor na povrchu nezrelých, zrelých a aktivovaných B buniek, avšak nie na kmeňových a plazmatických bunkách (12). Účinok je preto selektívnejší v porovnaní s cyklofosfamidom (3). Rituximab sa tak stal liečebnou možnosťou so sľubným efektom u pacientov s primárnymi chorobami glomerulov ako FSGS, idiopatická membánová nefropatia a systémových autoimunitných ochorení s postihnutím obličiek, čo potvrdzujú viaceré klinické štúdie, kde viedol k významnej redukcii proteinúrie a zníženiu incidencie relapsov základného ochorenia (9). V tejto práci prezentujeme naše skúsenosti s rituximabom v terapii primárnych glomerulopatií.
Materiál a metódy
Retrospektívne sme analyzovali dospelých pacientov s primárnou glomerolopatiou, ktorým bola podaná liečba rituximabom cestou hospitalizácie na Chirurgickej klinike a Transplantačnom centre Univerzitnej nemocnice v Martine (CHKaTC UNM). Podanie rituximabu bolo u pacientov indikované ako rescue liečba pri zlyhaní štandardnej imunosupresívnej terapie. Rituximab bol aplikovaný u každého pacienta v dávke 375 mg/m2 4 krát v týždenných odstupoch. Podávanie prebiehalo formou krátkej hospitalizácie pre riziko syndrómu z uvoľnenia cytokínov. U každého pacienta sme zaznamenali pohlavie, vek, základnú diagnózu, typ imunosupresívnej liečby. Z laboratórnych parametrov sme pri každej návšteve zaznamenali hodnotu sérového kreatinínu, glomerulárnej filtrácie (eGFR – estimated glomerular filtration rate) stanovenej pomocou formuly chronic kidney disease – epidemiology collaboration (CKD-EPI), krvný obraz. Pred začatím a po ukončení celej liečby sme stanovili hodnotu kvantitatívnej proteinúrie z 24 hodinového zberu moču, hodnotu sérového albumínu a celkových bielkovín.
Výsledky
Do sledovania boli zaradení celkovo 9 pacienti, z toho boli 8 muži a jedna žena. Priemerný vek pacientov bol 49,7 ± 11,6 rokov. Z hľa diska základnej diagnózy malo 5 pacientov histologicky potvrdenú membránovú glomerulopatiu, 4 pacienti MPGN a jeden pacient FSGS. Všetci pacienti boli nastavení na imunosupresívnej liečbe, každý z nich užíval kortikoidy (prednizón alebo metylprednizolón), pričom traja pacienti ho dostávali formou monoterapie, štyria pacienti dostávali kombinovanú liečbu s MMF, jeden s cyklosporínom A a jednému bol aplikovaný cyklofosfamid. V tabuľke 1 sú zaznamenané hodnoty kreatinínu, eGFR, KVPÚ, sérového albumínu a celkových bielkovín u všetkých pacientov počas sledovaného obdobia. Stanovili sme priemernú hodnotu kreatinínu počas každej kontroly pre celý súbor a následne v závislosti od typu glomerulárnej choroby. Zistili sme, že v priebehu liečby nedošlo k významnej zmene obličkových funkcií vyplývajúcich z hodnôt sérového kreatinínu a vypočítanej eGFR (graf 1 a 2). Vyhodnotením 24 hodinovej KVPÚ pred začatím liečby a po jej ukončení sme v našej skupine pacientov dokázali štatisticky signifikantný pokles KVPÚ ihneď po poslednej dávke rituximabu (graf 3). K poklesu KVPÚ došlo pri všetkých troch typoch glomerulárnej choroby (graf 4). V tomto čase sme zaznamenali vzostup hodnôt sérového albumínu a celkových bielkovín u všetkých sledovaných pacientov (tabuľka 1).
Graph 1. Vývoj priemernej hodnoty kreatinínu počas sledovaného obdobia bez závislosti od typu glomerulárnej choroby 
Graph 2. Vývoj priemernej hodnoty kreatinínu počas sledovaného obdobia v závislosti od typu glomerulárnej choroby 
Graph 3. Pokles priemernej KVPÚ po liečbe rituximabom 
Graph 4. Pokles KVPÚ po liečbe rituximabom v závilosti od typu glomerulárnej choroby 
Table 1. Základné laboratórne markery počas sledovaného obdobia 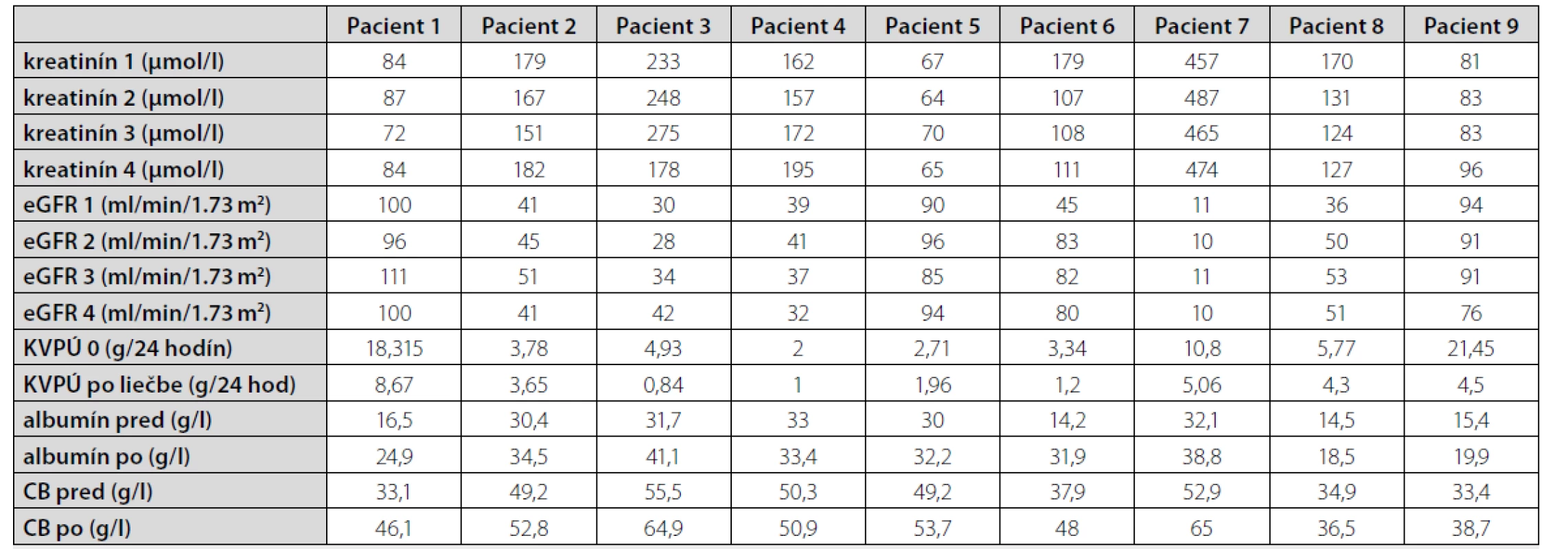
eGFR – glomerulárna filtrácia, KVPÚ – kvantitatívna proteinúria, CB – celkové bielkoviny Diskusia
V analýze našich pacientov sme zistili, že liečba rituximabom viedla k štatisticky významnej redukcii 24 hodinovej KVPÚ a to ihneď po absolvovaní mesačného terapeutického režimu. Zároveň sme u týchto pacientov nezaznamenali zmenu renálnych funkcií na základe vývoja sérového kreatinínu a eGFR.
Efektivita a bezpečnosť rituximabu bola najlepšie preukázaná v skupine pacientov s primárnou membránovou nefropatiou. V roku 2017 boli publikované výsledky francúzskej multicentrickej randomizovanej štúdie GEMRITUX porovnávajúcej rituximab so štandardnou antiproteinurickou liečbou. Z celkovej vzorky 75 pacientov dostávala polovica 6 mesačnú štandardnú neimunosupresívnu liečbu, druhej polovici bol infúzne aplikovaný rituximab v dávke 375 mg/m2 2 krát s týždňovým odstupom. Analýza nedosiahla primárny cieľ, kedy po 6 mesiacoch liečby nebol prítomný rozdiel v navodení parciálnej alebo kompletnej remisie proteinúrie medzi liečebnými režimami. Post hoc vytvorená observačná fáza však preukázala signifikantne vyšší počet remisií v skupine s rituximabom v 17 mesiaci (13). Dôležité závery priniesla minulý rok štúdia MENTOR, ktorá porovnávala rituximab a cyklosporín A u dospelých s indiopatickou membránovou nefropatiou. Randomizovala 130 pacientov s proteinúriou ≥ 5 g/deň napriek 3 mesačnej blokáde systému renín-angiotenzín-aldosterón na skupinu liečenú orálnym cyklosporínom A po dobu 12 mesiacov a skupinu, ktorej boli podané dve infúzie rituximabu, každá 1 000 mg, s odstupom 14 dní. V prípade parciálnej odpovede v 6 mesiaci sa liečba rituximabom zopakovala. Táto analýza preukázala, že liečba rituximabom bola non-inferiórna k liečbe cyklosporínom v navodení kompletnej alebo parciálnej remisie v 12 mesiaci a bola superiórna v udržaní remisie v 24 mesiaci (3). V blízkej dobe očakávame výstupy zo štúdie STARMEN porovnávajúcu, aktuálne prvo-líniovú liečbu, cyklofosfamid spoločne so steroidom (Ponticelliho schéma) s kombináciou rituximabu s takrolimom (TAC – tacrolimus) a štúdie RI-CYCLO hodnotiacu bezpečnosť a efektivitu rituximabu verzus cyklofosfamid/ steroid (14, 15). Tie môžu byť podkladom pre obmedzenie alkalyzujúcich preparátov ako prvo-líniovej liečby, ktoré sú typické vysokým výskytom vážnych nežiaducich účinkov.
Rituximab sa zdá byť efektívny v liečbe imunoglobulin (Ig) - asociovanej MPGN, obzvlášť u tých prípadov, ktoré sú spojené s monoklonálnou gamapatiou, chronickou lymfocytovou leukémiou a kryoglobulinémiou, avšak limitáciu môžu predstavovať nežiaduce účinky, predovšetkým infekčné. Na druhej strane u C3 glomerulopatie asociovanej s komplementom a chorobe denzných depozitov viaceré práce nepreukázali efektívnosť tejto liečby (9). V prípade FSGS je použitie rituximabu u steroid-rezistentnej formy zdokumentované iba v kazuistikách a malých nekontrolovaných sériách prípadov (10). Dostupné dáta ukazujú, že môže byť účinný v liečbe rekurentnej FSGS po TO, avšak pre potvrdenie sú potrebné randomizované klinické štúdie. Okrem toho boli títo pacienti zvyčajne liečení kombináciou preparátov a preto ťažko s presnosťou určiť efektivitu špecifického lieku (16, 17). Z ostatných typov glomerulárnych chorôb priniesli posledné roky dôležité výsledky v liečbe rituximabom pri lupusovej nefritíde. Komparatívna Indická štúdia na vzorke 222 pacientov s biopticky verifikovanou lupusovou nefritídou priamo porovnávala nízko-dávkovaný, vysoko-dávkovaný cyklofosfamid, MMF a rituximab v indukčnej liečbe. Autori potvrdili, že vysoko-dávkovaný cyklofosfamid a rituximab predstavujú najefektívnejšie terapeutické stratégie v tejto skupine pacientov, pričom rituximab bol obzvlášť efektívny v liečbe relabujúcej formy (18). Efektivita v liečbe ANCA (antineutrophil cytoplasmic antibody – protilátky proti cytoplazme neutrofilov)-asociovanej vaskulitídy bola potvrdená už v roku 2010 multicentrickou randomizovanou dvojito-zaslepenou štúdiou na 197 ANCA pozitívnych pacientoch s Wegenerovou granulomatózou alebo mikroskopickou polyangitídou, liečba rituximabom bola non - -inferiórna k cyklofosfamidu v navodení remisie a pravdepodobne nadradená pri relabujúcom ochorení (19). Aktuálne u nás disponujú oficiálnou indikáciou na liečbu rituximabom práve pacienti s ANCAasociovanou vaskulitídou.
V našej analýze je limitáciou malá vzorka liečených pacientov a heterogenita súboru z hľadiska typu glomerulárnej choroby. Okrem toho sme zaznamenali navodenie remisie nefrotickej proteinúrie iba v prvom mesiaci keď bola ukončená liečba rituximabom, pričom sme nesledovali schopnosť udržania navodenej remisie a riziko relapsu z dlhodobejšieho hľadiska.
V našej skupine pacientov sme podávali rituximab v dávke 375 mg/m2 4 krát v týždenných odstupoch. Alternatívnym režimom je podanie 1 gramu v 1. a 15. deň s možným opätovným podaním 1 gramu za 6 mesiacov. Na našom pracovisku používame originálny preparát a pre nedostupnosť nevyšetrujeme jeho hladinu a prítomnosť protilátok proti rituximabu v krvi pacientov. Pred začatím liečby je dôležité sérologicky vylúčiť prítomnosť nepoznanej hepatitídy B, C a tuberkulózy (HBsAg, anti-HCV, Quantiferon). Počas liečby sme u pacientov nezaznamenali žiadne nežiaduce účinky rituximabu. Po absolvovaní mesačnej liečby boli pacienti nastavení na kombinovanú imunosupresiu, konkrétne jeden na kombináciu TAC + MMF + steroid, 3 na TAC + steroid a 5 na MMF + steroid. Každému pacientovi bol po podaní 1. dávky rituximabu nasadený trimetoprim-sulfametoxazol na 6 mesiacov ako prevencia pneumónie spôsobenej Pneumocystis jirovecii.
Záver
Na základe dostupných dát možno konštatovať, že rituximab predstavuje účinnú alternatívu v terapeutických postupoch primárnych glomerulopatií, obzvlášť v prípadoch rezistencie na štandardnú imunosupresívnu liečbu. S týmto tvrdením sa stotožňujú aj nami prezentované klinické skúsenosti. V blízkom čase možno dokonca očakávať, že vo vybraných skupinách, ako napríklad primárna membránová nefropatia alebo lupusová nefritída, bude tvoriť súčasť prvo-líniovej indukčnej liečby.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Matej Vnučák, PhD.
Chirurgická klinika a Transplantačné centrum, Univerzitná nemocnica Martin
Kollárova 2, 036 01 Martin, Slovenská republika
Článek přijat redakcí: 5. 10. 2020
Článek přijat po recenzích k publikaci: 29. 4. 2021
Sources
1. Floege J, Barbour SJ, Cattran DC et al. Management and treatment of glomerular diseases (part 1): conclusions from a Kidney Disease: Improving Global Outcomes (KDIGO) Controversies Conference. Kidney Int. 2019; 95(2): 268–280.
2. Rojas-Rivera JE, Carriazo S, Ortiz A. Treatment of idiopathic membranous nephropathy in adults: KDIGO 2012, cyclophosphamide and cyclosporine A are out, rituximab is the new normal. Clin Kidney J. 2019; 12(5): 629–638.
3. Fervenza FC, Appel GB, Barbour SJ et al. Rituximab or Cyclosporine in the Treatment of Membranous Nephropathy. N Engl J Med. 2019; 381(1): 36–46.
4. Troyanov S, Wall CA, Miller JA et al. Idiopathic membranous nephropathy: definition and relevance of a partial remission. Kidney Int 2004; 66 : 1199–1205.
5. Beck LH jr, Bonegio RG, Lambeau G et al. M-type phospholipase A2 receptor as target antigen in idiopathic membranous nephropathy. N Engl J Med 2009; 361 : 11–21.
6. Tomas NM, Beck LH jr, Meyer-Schwesinger C et al. Trombospondin type-1 domain - containing 7A in idiopathic membranous nephropathy. N Eng J Med 2014; 371 : 2277–2287.
7. Kidney Disease: Improving Global Outcome (KDIGO) Glomerulonephritis Work Group. KDIGO clinical practice guideline for glomerulonephritis. Kidney Int Suppl 2012; 2 : 139–274.
8. Alfaadhel T, Cattran D. Management of membranous nephropathy in Western countries. Kidney Dis (Basel) 2015; 1 : 126–137.
9. Rudnicki M. Rituximab for Treatment of Membranoproliferative Glomerulonephritis and C3 Glomerulopathies. Biomed Res Int. 2017; 2017 : 2180508.
10. Beaudreuil S, Lorenzo HK, Elias M et al. Optimal management of primary focal segmental glomerulosclerosis in adults. Int J Nephrol Renovasc Dis. 2017; 10 : 97–107.
11. Uffing A, Pérez-Sáez MJ, Mazzali M et al. Recurrence of FSGS after Kidney Transplantation in Adults. Clin J Am Soc Nephrol. 2020; 15(2): 247–256.
12. Němec P. Rituximab (MabThera®) – nový biologický lék v terapii revmatoidní artritidy. Vnitr Lek 2007; 53(11): 1199–1210.
13. Dahan K, Debiec H, Plaisier E et al. Rituximab for Severe Membranous Nephropathy: A 6-Month Trial with Extended Follow-Up. J Am Soc Nephrol. 2017; 28(1): 348–358.
14. Rojas-Rivera J, Fernández-Juárez G, Ortiz A et al. A European multicentre and open - -label controlled randomized trial to evaluate the efficacy of Sequential treatment with TAcrolimus-Rituximab versus steroids plus cyclophosphamide in patients with primary Membranous Nephropathy: the STARMEN study. Clin Kidney J 2015; 8 : 503–510.
15. Scolari F. Rituximab versus steroids and cyclophosphamide in the treatment of idiopathic membranous nephropathy (RI-CYCLO) https://clinicaltrials.gov/ct2/show/ NCT03018535 (6 August 2019, date last accessed).
16. Tsagalis G, Psimenou E, Nakopoulou L et al. Combination treatment with plasmapheresis and rituximab for recurrent focal segmental glomerulosclerosis after renal transplantation. Artif Organs. 2011; 35(4): 420–425.
17. Cho JH, Lee JH, Park GY et al. Successful treatment of recurrent focal segmental glomerulosclerosis with a low dose rituximab in a kidney transplant recipient. Ren Fail. 2014; 36(4): 623–626.
18. Goswami RP, Sircar G, Sit H et al. Cyclophosphamide versus mycophenolate versus rituximab in lupus nephritis remission induction. JCR: Journal of Clinical Rheumatology. J Clin Rheumatol. 2019; 25(1): 28–35.
19. Stone JH, Merkel PA, Spiera R et al. Rituximab versus cyclophosphamide for ANCA - -Associated vasculitis. N Engl J Med. 2010; 363(3): 221–232.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2021 Issue E-3-
All articles in this issue
- Rituximab v liečbe primárnych glomerulopatií – naše skúsenosti
- Diferenciální diagnóza: „primární“ nebo sekundární diabetes aneb má význam u pacientů s diabetes mellitus 2. typu skrínovat Cushingův syndrom?
- Biomarker GDF-15 v kardiologii
- Transformace IgM-MGUS do Waldenströmovy makroglobulinemie u 2 z 6 pacientů v průběhu léčby syndromu Schnitzlerové
- Recidivující asfyktická zástava oběhu – neobvyklá manifestace SLE
- Jaterní cirhóza a těhotenství: kazuistika a přehled literatury
- Co může diabetolog udělat pro svého pacienta po iCMP?
- Zkušenost s péčí o pacienty s covidem-19 ve Velké Británii
- Právní aspekty aplikace střevního mikrobiomu
- Evropský a světový kongres o hypertenzi 2021
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Jaterní cirhóza a těhotenství: kazuistika a přehled literatury
- Biomarker GDF-15 v kardiologii
- Recidivující asfyktická zástava oběhu – neobvyklá manifestace SLE
- Rituximab v liečbe primárnych glomerulopatií – naše skúsenosti
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

