-
Medical journals
- Career
Změny úrovně sekundární prevence ischemické choroby srdeční mezi lety 1995–2017 v České republice: porovnání studií EUROASPIRE I, II, III, IV a V
Authors: Otto Mayer Jr 1,2; Jan Bruthans 1,3; Martina Rychecká Za Investigátory Studií Euroaspire I V V České Republice 1
Authors‘ workplace: II. interní klinika LF UK a FN Plzeň 1; Biomedicínské centrum LF UK v Plzni 2; Centrum kardiovaskulární prevence 1. LF UK a Thomayerovy nemocnice, Praha 3
Published in: Vnitř Lék 2018; 64(12): 1190-1199
Category: Original Contributions
Overview
Východisko:
Náležitě prováděná sekundární prevence je pro životní vyhlídky pacientů přinejmenším stejně důležitá jako léčba v akutním stadiu infarktu myokardu. Série studií EUROASPIRE hodnotila, nakolik byly principy sekundární prevence (definované dle platných doporučení) implementovány do klinické praxe u pacientů se stabilizovanou ischemickou chorobou srdeční (ICHS). V této analýze ukazujeme, jak se adherence k těmto doporučeným principům měnila mezi roky 1995 a 2017 u českého vzorku projektu EUROASPIRE.
Metodika:
Analýza porovnává 5 nezávislých kohort vyšetřených v letech v letech 1995/1996, 1999/2000, 2006/2007, 2012/2013 a 2016/2017 a zahrnující pacienty alespoň 6 měsíců po hospitalizaci pro akutní koronární příhodu či koronární revaskularizaci.
Výsledky:
Porovnávané soubory představovaly 331, 410, 489, 493 a 406 subjektů. Preskripce základní farmakoterapie se v průběhu sledovaného období zásadně zlepšila, zejména v případě statinů narostla vice než 12krát (ze 7,3 % na 92,1 %). Proporce pacientů s koronární revaskularizaci stoupla ze 49 % na 94 %. Prevalence hypercholesterolemie a špatně kontrolovaného krevního tlaku signifikantně poklesla z 98 % na 52 % a z 64 % na 49 %, resp. Proporce aktivních kuřáků se významněji nezměnila. Prevalence manifestního diabetu nejprve stoupla do roku 2006 vice než 2krát, v dalším období je ale již znatelný pokles (i když zatím nikoliv k výchozím hodnotám z roku 1995).
Závěr:
Přestože se adherence k cílovým hodnotám v některých jednotlivých faktorech výrazně zlepšila, globální dosažení doporučených principů sekundární prevence je stále daleko svému optimu.
Klíčová slova:
doporučení – EUROASPIRE – ischemická choroba srdeční – mortalita – sekundární prevence
Úvod
Léčba v akutním stadiu a sekundární prevence jsou dvě komplementárně propojené procedury zásadně určující osud pacientů s ischemickou chorobou srdeční (ICHS) a vaskulárními chorobami obecně. Lze tedy dovodit, že pokrok, který jsme u nás v akutním managementu infarktu myokardu zaznamenali, by mohl přijít i z (velké) části vniveč, pokud nebude následován důslednou sekundární prevencí. Praktická realizace sekundární prevence ICHS je již počínaje rokem 1994 poměrně podrobně definována sérií tzv. Společných evropských doporučení pro kardiovaskulární prevenci (Guidelines) [1–5]. Její těžiště spočívá především v kontrole základních rizikových faktorů (RF) aterosklerózy, dále pak specifických režimových opatřeních a podávání některých lékových skupin s prokázaným přínosem z hlediska redukce rizika fatálních i nefatálních kardiovaskulárních příhod.
Je jasné, že není možno určité doporučení pouze vyslovit, ale také nutno zpětně ověřit jeho implementaci do klinické praxe. Ještě podstatnější je, zdali i v reálném životě vedlo k zamýšlenému účinku (tj. v konkrétním případě redukci kardiovaskulárního rizika). Série studií EUROASPIRE [6–9] (a nyní máme k dispozici již celkem 5 nezávislých kohort tohoto dlouhodobého projektu) má za úkol objektivizovat, nakolik se principy definované příslušnými doporučeními odrazily v reálné praxe (a to především ve smyslu, nakolik pacienti se stabilizovanou ICHS splňují cílové hodnoty jednotlivých ovlivnitelných RF) Předložená analýza je založena na českých datech projektu EUROASPIRE, tak jak vznikala mezi lety 1995 a 2017.
Metoda
Všechny studijní procedury byly realizovány v souladu s principy Správné klinické praxe a etickými standardy ve smyslu Helsinské deklarace z roku 1964 a pozdějších dodatků. Protokoly jednotlivých částí projektu byly vždy schváleny lokální Etickou komisí a písemný Informovaný souhlas získán ode všech zařazených probandů. Všechna data jsou skladována a zpracována v souladu se Zákonem na ochranu osobních údajů a směrnicí GDPR Evropské komise.
Design studie a studovaná populace
Předložená analýza je koncipována jako deskriptivní průřezová survey, srovnávající 5 nezávislých podobně selektovaných kohort pacientů s klinicky manifestní a stabilizovanou ischemickou chorobou srdeční, vyšetřených v letech 1995–96, 1999–2000, 2006–2007, 2012–2013 a 2016–2017 jako české vzorky studií EUROASPIRE I, II, III, IV a V. Výběr vzorku je detailně popsán jinde [6–9]. Krátce, v každé jednotlivé studii byli vždy retrospektivně identifikováni pacienti spadající do některé z následujících diagnostických kategorií podle závěrečné diagnózy v propouštěcí zprávě: akutní nebo elektivní koronární bypass či perkutánní koronární angioplastika, akutní infarkt myokardu nebo prokázaná koronární ischemie (dle závěru ošetřujícího lékaře). Výběr pacientů byl zahájen u nejrecentnějších případů, ale ne dříve než 6 měsíců po příslušné hospitalizaci a pokračoval zpětně v čase, dokud nebylo dosaženo počtu 525 pacientů mladších 71 let v době přijetí k hospitalizaci (studie EUROASPIRE I a II). Výběr v EUROASPIRE III-V zahrnoval i pacienty ve věku 71–80 let a celkový soubor tak byl rozšířen na 600 pacientů. Hospitalizace pacientů proběhla ve Fakultní nemocnice Plzeň či Institutu klinické a experimentální medicíny Praha, které poskytují všechny typy kardiologické péče (tj. péče o akutní stavy ICHS, intervenční kardiologii a kardiochirurgii) se spádovou oblastí více než 500 000 obyvatel.
Vyšetřovací procedury
Všechny vyšetřovací procedury byly realizovány opět podle standardního protokolu studie EUROASPIRE (EA) a jsou zase detailněji popsány jinde [6–8]. Vyšetření obsahovalo základní demografické charakteristiky, individuální rodinou a osobní anamnézu kardiovaskulárních chorob, informace o životním stylu a užívanou farmakoterapii. Dále proběhly následující vyšetřovací procedury: měření tělesné výšky a hmotnosti v lehkém spodním prádle pomocí automatických vah SECA 707 (ve studiích EA I a II) či SECA 701 (EA III-V) s připojeným měřidlem (váhy byly náležitě kalibrovány vždy před zahájením každé ze studií). Obvod pasu byl měřen ocelovou krejčovskou mírou v místě největšího objemu trupu. Krevní tlak (TK) byl zprůměrován ze 2 měření vsedě pomocí automatického sfygmomanometru (Takeda UA731 ve studii EA I, Omron 711 v EA II, Omron M5-I v EA III a Omron M6 v EA IV a EA V) na pravé ruce a pomocí příslušně široké manžety. Série srovnávacích studií byla provedena ke zjištění srovnatelnosti naměřených hodnot z jednotlivých kohort. Počet vydechovaných částic oxidu uhelnatého byl měřen pomocí přístroje Smokerlyser (Bedfont Scientific, Upchurch, UK) k verifikaci udávaného kuřáckého habitu (a za aktivní kuřáky byly považováni ti, kteří tento fakt buď sami uvedli, nebo přesáhli hranici 10 ppm CO ve vydechovaném vzduchu). Odběr krve byl realizován z venepunkce po přinejmenším 12hodinovém lačnění a všechna laboratorní vyšetření realizována v sérii ze vzorků zamražených při -80 °C. Laboratorní vyšetření zahrnovalo stanovení celkového (T-C) a HDL-cholesterolu (HDL-C), triglyceridů (TG) a glykemie a bylo realizováno buď v centrální laboratoři příslušné studie EUROASPIRE či v laboratořích Ústavu klinické biochemie a hematologie FN Plzeň na analyzátoru Cobas Mira (Roche, Basel, Switzerland) a komerčně dostupných kitů. LDL-cholesterol (LDL-C) byl kalkulován pomocí Friedewaldovy rovnice, tj. LDL = T-C – HDL – (TG/2,22). Glykovaný hemoglobin byl stanoven ionexovou kapalinovou chromatografii pomocí analyzátoru G7 fy TOSOH (Tokyo, Japan). Vzájemná srovnatelnost metodik stanovení byla opět testována pomocí opakovaných analýz a všechny detaily jsou opět popsány jinde [6–9].
Zpracování dat
Mortalita subjektů byla zjišťována k 31. 3. 2018 na základě databáze Ústavu zdravotnických informací a statistiky, včetně udávané primární příčiny (diagnózy) úmrtí. Data byla statisticky analyzována pomocí software STATISTICA 8 (StatSoft Inc, Tulsa, OK, USA). Kontinuální proměnné byly kategorizovány vždy s ohledem na cílové hodnoty podle v době vyšetření platných doporučení (tj. 1., 2., 3., 4. a 5. Společná evropská doporučení) [1–5] a příslušné definice jsou uvedeny v relevantních sekcích.
Výsledky
Základní charakteristiky souborů a jejich vývoj
Celkem bylo ve všech 5 srovnávaných kohortách identifikováno 2 850 pacientů se stabilizovanou ICHS, z čehož se 2 123 (74,5 %) dostavilo k vyšetření. Základní demografická charakteristiky a průřezové hodnoty jednotlivých RF udává tab. 1. Vzhledem k tomu, že průměrný věk probandů v jednotlivých kohortách (EA I-V) vzrůstal (a k markantnějšímu skoku došlo zejména mezi kohortou EA II a EA III), byla všechna data systematicky adjustována na věk. Mezi roky 1995 a 2017 došlo k signifikantnímu nárůstu BMI a obvodu pasu, zatímco krevní tlak vykazoval opačný trend. K zásadnímu snížení došlo zejména v LDL, jehož průměrné koncentrace klesly o takřka 1,4 mmol/l. Naopak hodnoty lačné glykemie nejprve poměrně zásadně stoupaly mezi lety 1994 a 2007, v dalším sledovaném období je však již sledovatelný naopak jejich pokles (takže průměrné hodnoty lačné glykemie na začátku a na konci sledovaného období jsou v podstatě stejné). S ohledem na odlišná selekční kritéria (zvýšení věkového limitu probandů do 80 let) jsme také zvláště hodnotili pouze období 2006–2017 (EA III-V), ale pozorované trendy se v průměrných hodnotách základních rizikových faktorů (s výjimkou výše popsané lačné glykemie) zásadněji nelišily od globálního trendu EA I-V.
Table 1. Základní průřezové charakteristiky a rizikový profil pacientů sledovaných v kohortách EUROASPIRE I–V (průměr – standard deviation/SD) 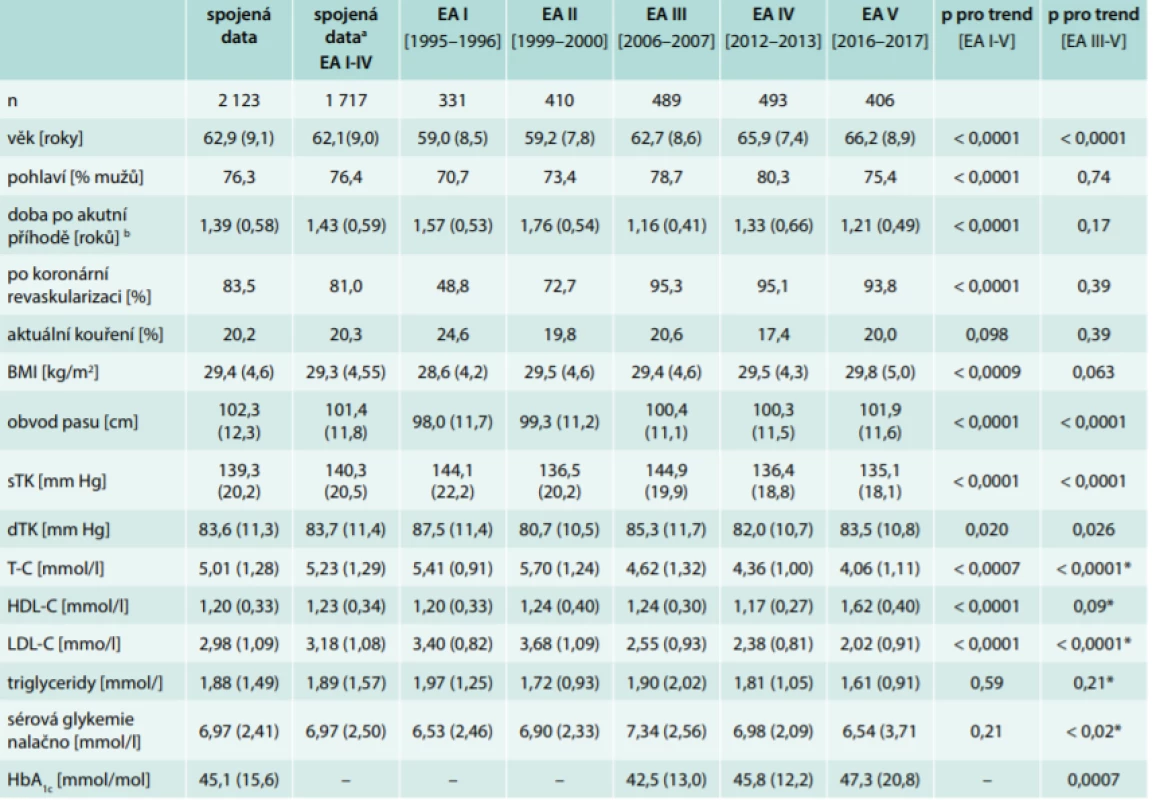
a použita pro analýzu mortality
b doba mezi zařazovací příhodou (hospitalizace pro infarkt či elektivní revaskularizaci) a vyšetřením ve studii EUROASPIRE
HbA1c– glykovaný hemoglobin HDL – high density lipoprotein LDL – low density lipoprotein p – adjustovány na věk a pohlaví (s výjimkou těchto parametrů samotných) TK – krevní tlakZměny terapie a kontroly rizikového profilu
Z hlediska managementu v akutním stadiu choroby došlo v průběhu sledovaného období zejména k masivnímu nárůstu koronárních revaskularizací a maximum tohoto jevu lze pozorovat mezi lety 1995–2006 (tab. 1). Ještě strmější trend byl v preskripci základní farmakoterapie v sekundární prevenci (tab. 2). Zejména užívání statinů narostlo mezi roky 1995 a 2017 z asi 7 % na více než 92 %, podobně vzrostla i preskripce inhibitorů angiotenzin konvertujícího enzymu (ACEI) či sartanů (z asi 24 % na 79 %), antidiabetik (z asi 10 % na 29 %), o něco méně markantně i preskripce betablokátorů (z 57 % na více než 80 %).
Table 2. Kategorizované hodnoty hlavních rizikových faktorů a udávaná základní medikace 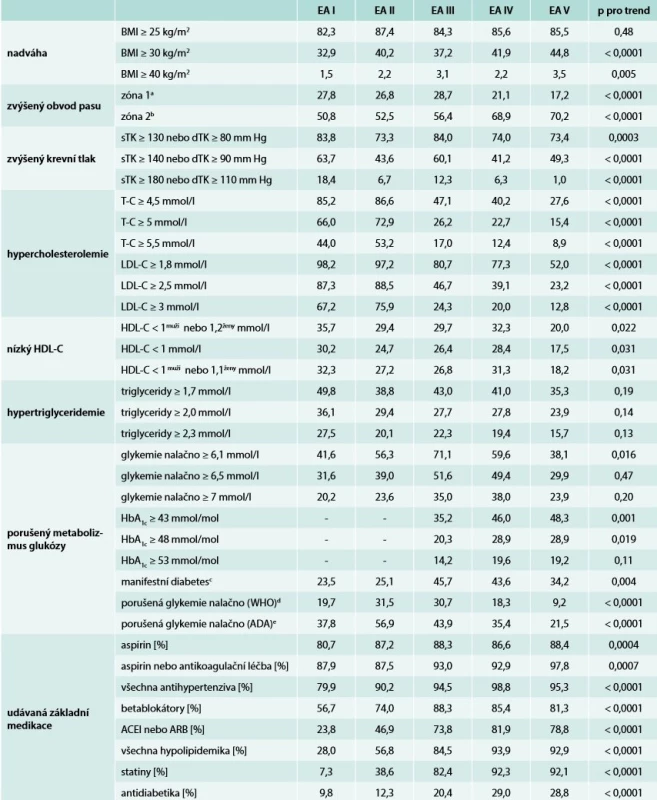
a 94–101 cm u mužů či 80–87 cm u žen
b ≥ 102 cm u mužů či≥ 88 cm u žen
c glykemie nalačno ≥ 7 mmol/l anebo léčba antidiabetiky
d glykemie nalačno 6,1–6,9 mmol/l, ale bez léčby antidiabetiky
e glykemie nalačno 5,6–6,9 mmol/l, ale bez léčby antidiabetiky
ADA – American Diabetic Association ACEI – inhibitor angiotenzin konvertujícího enzyme ARB – blokátor receptoru pro angiotenzin II BMI – index tělesné hmotnosti/Body Mass Index DM – manifestní diabetes mellitus dTK – diastolický krevní tlak HbA1c – glykovaný hemoglobin p – adjustovány na věk a pohlaví sTK – systolický krevní tlak WHO – World Heart OrganizationZ hlediska kontroly základních rizikových faktorů nutno na prvním místě konstatovat, že zastoupení aktivních kuřáků se mezi lety 1995–2017 významněji nemění (tab. 1). Kontrolu ostatních konvenčních rizikových faktorů (k různě definovaným léčebným cílům) shrnuje tab. 2. Prevalence nadváhy se v průběhu sledovaného období zdánlivě neměnila, ale „uvnitř“ této kategorie vykazuje zastoupení pacientů s obezitou poměrně zásadní vzestup (z asi 33 % na 45 %); podobný významně vzestupný trend lze najít v abdominální obezitě (zvýšeném obvodu pasu). Kontrola TK dosti kolísala a nelze určit jednoznačný trend, avšak pacientů přesahujících nejběžnější cílovou hodnotu < 140/90 mm Hg nebylo v žádném ze sledovaných období nikdy méně než 40 %, zatímco při použití striktnějšího cíle < 130/80 mm Hg činila non-adherence k této hodnotě minimálně 73 % souboru (tab. 2). Markantněji se v průběhu času zlepšila kontrola hypercholesterolemie, i když zase na konci sledovaného období současnou cílovou hodnotu LDL < 1,8 mmol/l stále nesplňovalo až 52 % analyzovaných pacientů.
Informaci o kontrole porušeného glukózového metabolizmu nutno rozdělit do dvou poloh. Na jedné straně sama prevalence diabetu narostla mezi lety 1995 a 2006 takřka 2krát (z asi 23 % na 46 %) a pozorovaný pokles (z asi 46 % na 34 %), v druhé části polovině sledovaného období (2006–2017) ještě tento nárůst zdaleka nevyrovnal; ekvivalentní trend lze pozorovat i v případě porušené glykemie nalačno. Protože však zároveň stoupala preskripce antidiabetik (z asi 10 % na 29 %), celková proporce pacientů s lačnou glykemií ≥ 7 mmol/l klesla na konci sledovaného období zase k asi 24 %.
Vzhledem k tomu, že se doporučené cílové hodnoty RF během více než 20letého sledovaného období dosti měnily, tab. 3 udává také non-adherenci k v době vyšetření platným doporučením. Souhrnně lze říci, že kontrola byla značně variabilní a nelze najít jednoznačnou souvislost mezi zpřísněním cílové hodnoty a zlepšení kontroly příslušného RF. Adherenci k doporučené cílové hodnotě jsme ještě analyzovali i z hlediska, kolik z 5 základních RF má pacient náležitě kontrolováno. Zastoupení těch, co měli náležitě kontrolovaný celý rizikový profil (tj. všech 5 RF) zůstávalo po celé sledované období velmi nízké (2–4 % příslušných souborů) a stejně tak se ani zásadněji neměnila proporce těch, kteří přesahovali 1, 2 nebo 3 cílové hodnoty RF.
Table 3. Cílové hodnoty základních rizikových faktorů dle 1., 2., 3., 4. a 5. společných evropských doporučení pro kardiovaskulární prevenci a reálná adherence k těmto principům (proporce non-adherentních pacientů [%]) ![Cílové hodnoty základních rizikových faktorů dle 1., 2., 3., 4. a 5. společných evropských doporučení
pro kardiovaskulární prevenci a reálná adherence k těmto principům (proporce non-adherentních
pacientů [%])](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/912dadfc62ea9d648f775480f23fad24.png)
a hodnoty platné v době vyšetření (tj. EA I odpovídá 1. doporučením,… atd), faktory jejichž léčebný cíl se neměnil (BMI, kouření) zde nejsou uvedeny, ale použity pro další výpočty
b na základě T-C v EA I, dle LDL-C v EA II-V
c na základě glykemie nalačno v EA I-II, dle HbA1c v EA III-V, poměr se vztahuje pouze k počtu manifestních diabetiků
d vztahuje se k výše zmíněným pěti hlavním faktorům
e cílová hodnota nebyla v příslušných doporučeních definovánaZměny mortality
Mortalita byla zjišťována u 1 717 probandů vyšetřených v rámci EA I-IV a základní charakteristiky tohoto podsouboru jsou rovněž uvedeny v tab. 1. Celkem v této kohortě k 31. 3. 2018 zemřelo 580 pacientů při mediánu (interkvartilovém rozpětí) sledování 11,3 (5,5–17,7) roků; 341 úmrtí bylo deklarováno jako kardiovaskulárních (podle ICD-10 diagnózy uvedené jako primární příčina úmrtí na úmrtním listu) Celkové 5leté mortality v jednotlivých srovnávaných kohortách (EA I-V) a dále pak specifické mortality z kardiovaskulární příčiny či pro malignitu jsou uvedeny v tab. 4. Jakkoliv bylo možno sledovat určité kolísání (jdoucí zřejmě především na vrub odlišností ve věkové skladbě), při srovnání hrubé (neadjustované) mortality po celé sledované období nebyl prokazatelný žádný signifikantní trend. Pokud jsme ovšem mortalitu adjustovali na věk a pohlaví, statisticky signifikantní pokles bylo možno najít teprve na samém konci sledovaného období (tj. mezi EA III a EA IV). Pacienti vyšetření v rámci kohorty EA IV vykazovali o 39 % nižší riziko úmrtí, resp. o 48 % nižší riziko úmrtí z kardiovaskulární příčiny (po adjustaci na věk a pohlaví, použito bylo Coxova modelu proporcionálního rizika). Stejný trend byl pozorován i v případě, že mortalitní riziko bylo adjustováno i na ostatní rizikové faktory (kouření, BMI, systolický krevní tlak, LDL a lačnou glykemii), koronární revaskularizaci a základní medikaci (betablokátory či sartany, statiny a antidiabetika) [HRR (poměr rizik) pro celkovou mortalitu činilo 0,51 (95% CI: 0,34–0,77), p = 0,001; a pro kardiovaskulární 0,50 (95% CI: 0,31–0,81)]. Na celém souboru (spojených kohortách (EA I-IV) jsme se rovněž pokusili identifikovat, které ze sledovaných faktorů nejvíce přispívají k mortalitnímu riziku. Při použití Coxova modelu a celkové 5leté mortality jako závislé proměnné, pouze zvýšená lačná glykemie [HRR 1,36 (95% CI: 1,01–1,92)], spolu s věkem [HRR 1,08 (95 % CI: 1,06–1,11)], pohlavím [HRR 2,18 (95 % CI: 1,43–3,33)] a anamnézou koronární revaskularizaci [HRR 0,63 (95 % CI: 0,41–0,96)] vstoupily do regrese jako významné prediktory (a velmi podobný byl i výsledek, pokud jsme jako závislou proměnnou použili kardiovaskulární mortalitu).
Table 4. Mortalita u pacientů kohort EUROASPIRE I-IV [%] ![Mortalita u pacientů kohort EUROASPIRE I-IV [%]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/b6df34717c473e7d660a9d527e803ab9.png)
a Coxův model proporcionálních rizik [HRR (95%CI), poměr rizik (95% intervaly spolehlivosti)], model zahrnuje i věk a pohlaví pacientů Diskuse
Hlavní smyslem naší analýzy bylo objektivizovat na dobře definovaných kohortách, jaký je skutečný dopad Společných evropských doporučení (Guidelines) [1–5] na realizaci sekundární prevence u stabilizovaných pacientů s ICHS (a to po celé období, po které jsou tato vydávána). Pokud bychom otázku úrovně sekundární prevence zúžili pouze na to, jaká je adherence k doporučeným terapeutickým standardům (tj. zejména cílovým hodnotám jednotlivých rizikových faktorů, jak byly příslušnými doporučeními definovány), vypadala by situace spíše pesimisticky. Počet pacientů, jejichž rizikový profil byl rigorózně kontrolován k náležitým léčebným cílům, zůstává po celé dlouhé období existence doporučení (počínaje rokem 1994) prakticky zanedbatelný (neboť v žádné z 5 srovnávaných kohort nepřesáhl 4 % pacientů). Naopak zastoupení těch non-adherentních k 3 a více léčebným cílům bylo vždy > 40 % (což není právě lichotivý výsledek) a vlastně vzájemná proporce počtu nedodržených léčebných cílů zůstává po celé sledované období (1995–2017) až překvapivě totožná (viz tab. 3). To by mohlo implikovat domněnku, že jak lékaři, tak i dotčení pacienti obsah doporučení v praxi příliš v potaz neberou (a daleko větší impakt tak může mít dejme tomu marketing farmaceutických firem).
Při bližším pohledu na analyzovaná data lze ale najít nejen nepříznivá, ale i pozitivní zjištění. První příznivou zprávou může být již věková struktura jednotlivých studovaných souborů, v nichž průměrný věk našich probandů narůstá. Např. mezi roky 2006 a 2017 (kdy již byla stejná metodika výběru probandů, tj. všichni do 80 let věku) stoupl průměrný věk v našich kohortách o takřka 4 roky. To by mohlo odrážet jak posun manifestací ICHS do vyššího věku (tedy vliv prevence), tak i nižší fatalitu (tedy vliv spíše kurativy), a toto je koneckonců i v souladu i s klesajícím trendem úmrtnosti na kardiovaskulární choroby v ČR (viz data UZIS, např. http://dx.doi.org/10.1787/888933623647). Další velmi příznivou zprávou je pokračující vysoká úroveň managementu infarktů v době akutní manifestace ve smyslu realizované koronární intervence. Ta se zásadně zvedla již v letech 1999/2000 a po roce 2006 až do současnosti se v podstatě ustálila někde mezi 90–95 %. Jakkoliv akutní management není přímo součástí sekundární prevence, jeho náležitá realizace nejen že zásadně zvyšuje šanci pacientů akutní fázi infarktu myokardu přežít, ale i zachovat si takový funkční status, aby mohli reálně ze sekundární prevence vůbec profitovat. Analýza českých dat založená na populačním modelu IMPACT [10] ukázala, že na poklesu úmrtnosti na ICHS mezi roky 1985 a 2007 se asi ze 7,5 % podílela právě léčba v akutním stadiu infarktu myokardu, tj. direktní angioplastika (a můžeme důvodně předpokládat, že i po roce 2007 relativní impakt této „technologie“ na osud pacientů ještě dále narůstal). Když jsme také analyzovali mortalitu během hospitalizace a v průběhu prvního roku u 4 224 pacientů hospitalizovaných mezi lety 2007–2015 ve FN Plzeň pro infarkt myokardu, činila 13,7 % (dosud nepublikovaná data). To představuje méně než polovinu počtu, který býval pozorován v předcházející epoše [11] a tento pokles časné mortality lze asi nejvíce připsat na vrub právě akutnímu managementu pacientů.
Podobně potěšitelná zůstává i preskripce základních léčiv s prokázaným benefitem v sekundární prevenci (aspirin či antikoagulancia, ACEI či sartany a betablokátory), která se přinejmenším ve dvou nejrecentnějších kohortách (EA IV a V) pohybovala okolo 80 % (resp. až 98 % v případě aspirinu/antiakoagulancií). V preskripci těchto lékových skupin se pohybujeme zhruba kolem průměru ostatních zemí, hodnocených v projektu EUROASPIRE (v případě ACEI/sartanu dokonce nad ním) a její zásadnější zvyšování již zřejmě očekávat nelze (neboť se zde narazí na kontraindikace, zejména ve smyslu pomalé tepové frekvence nebo habituálně nižšího TK).
Jak již bylo konstatováno výše, situace je nejednoznačná v oblasti kontroly jednotlivých rizikových faktorů k doporučeným hodnotám. Na prvním místě nutno zmínit kuřácký habitus. Je sice fakt, že prevalence kouření je v našem souboru pacientů s ICHS nižší, než kolik by tato hodnota činila ve srovnatelném vzorku obecné populaci (jak ukazují např. zcela recentní data ze studie postMONICA či jiných analýz [12]), tento rozdíl se ale stále zmenšuje. Také pro potěšitelně vysoké množství aktivních kuřáků (a u mužů je to až 50 %) představuje proběhlý infarkt natolik alarmující životní událost, že k rozhodnutí přestat kouřit dojdou (naštěstí) sami a spontánně. Lze se i uklidňovat faktem, že při srovnání s ostatními evropskými zeměmi se s prevalencí okolo 20 % stále udržujeme někde u celoevropského průměru (ten např. v EA V činí 22 %, přičemž nejvyšší prevalence byla tradičně v Itálii s až 29 %!); racionálnější je ale srovnávat se spíše s těmi nejlepšími (např. Švédsko s 10 % či nám dosti podobné Slovinsko s 12 % aktivních kuřáků). Na druhé straně, dlouhodobý přístup k problematice kouření po infarktu myokardu nelze nazvat jinak než nihilistický! Prakticky všechna doporučení pro prevenci kardiovaskulárních shodně zdůrazňují kruciální nutnost profesionální pomoci s překonáním kuřácké závislosti a fakt, že by intervence měla být zahájena co možná nejdříve, tj. již v době hospitalizace pro kardiovaskulární příhodu [1–5,13]. Ve skutečnosti jsme např. v žádné (!) z kontrolovaných propouštěcích zpráv pacientů, vyšetřených posléze jako kohorta EA V, nezaznamenali jakoukoliv aktivní snahu pacienta po infarktu myokardu odeslat např. do protikuřácké poradny či mu předepsat medikaci pomáhající závislost na nikotinu překonat (a i pouhé dvouslovné doporučení charakteru „přestaňte kouřit“ bylo možno najít v propouštěcích zprávách jen zcela vzácně). Tento přístup ostatně asi není naším národním specifikem, neboť protikuřácká intervence byla i v ostatních analyzovaných zemích realizována v podobně minimálním procentu (v souhrnu pouze jen 4 % pacientů využilo služeb profesionální poradny a stejně mizivá byla preskripce vareniclinu či bupropionu). Abychom také všechno nenechávali jen na ošetřujících lékařích, ani komunitní podpora v kuřácké intervenci není zrovna charakteristikou naší společnosti (což se projevilo i v málem nekončící debatě okolo tzv. protikuřáckého zákona) a bohužel jen málokterému kuřákovi asi přijde na mysl, že zapalovat si před člověkem, který se z dobrých důvodů snaží přestat kouřit, není právě nejférovější přístup.
Podobně neradostně se jeví situace v oblasti nadváhy a obezity. Jak je možno odvodit z našich dat, nejen že se prevalence nadváhy pohybuje v dosti alarmujících hodnotách okolo 85 % a bez jakékoliv tendence k poklesu, ale dokonce „uvnitř“ této kategorie dochází k přesunu směrem k vyššímu zastoupení pacientů s obezitou (BMI ≥ 30) či její vysloveně maligní formou (BMI ≥ 40). V prevalenci obezity jsme se mezi ostatními evropskými zeměmi dostali dokonce až na 4. místo a tento nepříznivý vývoj bohužel koreluje i s podobným vývojem v obecné populaci. Možnosti jak tuto situaci zvrátit jsou značně omezené a pravděpodobně vyžadují již spíše celospolečenský přístup (tj. „výchovu“ celé populace ke zdravějšímu životním stylu, počínaje již nejmladšími věkovými skupinami a zřejmě i určité legislativní úpravy) – zatím je cekem evidentní, že v této snaze selháváme. Stejně minimální je naše paleta terapeutických prostředků (např. v podobě antiobezitik či nefarmakologických technologii v léčbě obezity) a i těch několik málo, které připadají teoreticky v úvahu, nejsou na rozsah problému naprosto dimenzovány (existující antiobezitické přístupy si obvykle kladou cíl jedince se zcela maligní obezitou přesunout do pásma sice bezpečnější, ale stále velmi extrémní obezity). Jediná intervenční studie, zaměřená na farmakologickou léčbu obezity v sekundární prevenci ICHS (tj. SCOUT) dopadla z hlediska kardiovaskulárního rizika negativně [14].
Ani data o kontrole hypertenze nevyznívají jednoznačně. Na jedné straně je potěšitelný fakt, že prakticky vymizeli pacienti s těžkou nekontrolovanou hypertenzí (tj. TK > 180/100 mm Hg), kterých v nejnovější kohortě bylo již jen asi 1 %. Preskripce antihypertenzní léčby v sekundární prevenci rovněž významně narostla a pohybuje se nyní okolo 95–98 % (i když asi ne všechna antihypertenziva byla podávána s úmyslem snížení TK – to se týká především betablokátorů). Na druhé straně, kontrola k doporučené hodnotě TK výrazně osciluje (viz tab. 2) a i non-adherence k doporučené hodnotě zůstává až překvapivě vysoká (více než 50 % v poslední kohortě). Důvodů je asi celá řada a jistě to bude již popsaný vzestup prevalence obezity a relativní nárůst věku pacientů s ICHS. Lze připustit i určité zkreslení našich dat: pacienti mohou na nestandardní situaci představovanou naším screeningovým vyšetřením reagovat i vyšším TK, než je jejich obvyklá hodnota. Svou roli ale také může hrát dlouhodobě neujasněná koncepce, jak důrazně má být TK v sekundární prevenci vlastně kontrolován. Pokud se podíváme na jednotlivá doporučení počínaje rokem 1994, nejprve zde byla tendence cílovou hodnotu TK snižovat (tab. 3, 1. řádek) a to tak, že 4. společná doporučení již viděla jako optimální všem pacientům s vaskulární chorobou TK kontrolovat jednotně < 130/80 mm Hg [4]. V následném období (kdy převládla představa tzv. J křivky [15]), došlo zase naopak k pohybu cílové hodnoty zpátky k hodnotě 140/90 mm Hg [5,13]. A nakonec další změnu přinesla studie SPRINT [16], jejíž výsledky „vrací do hry“ pro změnu intenzivnější antihypertenzní léčbu v sekundární prevenci. Lze tedy důvodně očekávat, že nižší cílové hodnoty by se v budoucnosti mohly opět vrátit. Takto protichůdné změny náhledu na kontrolu TK tedy mohou v lékařích i pacientech vyvolávat neopodstatněný dojem, že na tomto parametru vlastně moc nezáleží (samozřejmě, opak je pravdou!).
Je neoddiskutovatelné, že kontrola hypercholesterolemie zaznamenala po dobu našeho sledování obrovské zlepšení, což zrcadlí už jenom čistě pokles v průměrných hodnotách LDL o takřka 1,40 mmol/l (dle epidemiologických důkazů i výsledků statinových studií by takový pokles mohl být teoreticky provázen více než 50% poklesem relativního rizika velké kardiovaskulární příhody [17,18]). Důvodem je bezpochyby masivní nárůst preskripce statinů, která ze skromných začátků (asi 7 % v letech 1995–96) narostla na více než 90 % po roce 2012. Bohužel však stále u našich pacientů plně nevyužíváme potenciál náležitého dávkování statinu. Je celkem evidentní (a to již více než 10 let), že intenzivní léčba statinem v nejvyšší existující dávce (80 mg atorvastatinu či 40 mg rosuvastatinu) vede také k vyšší protekci ve smyslu recidiv fatálních a nefatálních kardiovaskulárních příhod [17]. Do praxe však tento fakt proniká stále velmi neochotně a náležité dávkování statinu dodržovalo v poslední kohortě jen necelých 23 % pacientů (v roce 2012 toto bylo zcela zanedbatelných 2,4 %). Zcela minimálně se také využívá kombinační léčby s ezetimibem (necelá 2 %), kterou by podle jiné naší analýzy pro nedosažení aktuální cílové hodnoty LDL (< 1,8 mmol/l) vyžadovalo takřka 60 % pacientů s ICHS [19]. Nové obzory nám v kontrole hypercholesterolemie v sekundární prevenci otevírají PCSK9 inhibitory [20], díky jejichž enormní hypolipidemické účinnosti bychom mohli teoreticky dosáhnout náležité kontroly LDL až u takřka 100 % pacientů (z ekonomických důvodů je toto sice zatím jen „hudba budoucnosti“, ale to ovšem neznamená, že bychom tuto možnost měli zcela ignorovat – recentně je tato léčba v sekundární prevenci dostupná jako tzv. centrová).
Posledním RF, jehož kontrola bude do celkové efektivity sekundární prevence zasahovat zřejmě zcela zásadně, je diabetes mellitus a porucha glukozového metabolizmu obecně. Jak vyplývá z našich dat, prevalence diabetu rostla zejména do roku 2006 zcela explozivně (z asi 24 % na takřka 46 %) a to zřejmě nebylo možno připsat na vrub pouze vyššímu věku pacientů kohorty EA III. K tomuto již tak vysokému počtu diabetiků asi musíme navíc připočítat i skupinu prediabetických pacientů s tzv. porušenou glykemií nalačno (tj. ≥ 5,6 mmol/l). Podle jiné z našich analýz tato skupina vykazuje stejné mortalitní riziko jako ta s již manifestovaným diabetem [21]. Pokud přijmeme tuto tezi, mělo v roce 2006 „normální“ glukózový metabolizmus jen (dosti neuvěřitelných) 10 % pacientů! Nutno také připomenout, že kromě věku byl porušený glukozový metabolizmus mezi konvenčními rizikovými nejsilnějším prediktorem mortalitního rizika nejen v této naší analýze, ale podobný výsledek dala i analýza celoevropských dat [22]. Za snad povzbuzující lze označit fakt, že právě roce 2006 (v kohortě EA III) dosáhla „epidemie“ diabetu v sekundární prevenci možná již svého vrcholu a v dalších dvou kohortách je již zřetelný klesající trend (souhrnně bylo zastoupení diabetu plus porušené glykemie nalačno v EA V „jen“ asi 56 %). Oproti roku 2006 se také zlepšují naše terapeutické možnosti: dosti zásadně se rozšířilo „portfolio“ antidiabetik a máme dokonce již k dispozici i látky s prokázaným mortalitním benefitem (jakkoliv ještě nikoliv vysloveně v sekundární prevenci [23,24]) I v této naší analýze lze prokázat markantní nárůst preskripce antidiabetik a zlepšuje se dokonce již i kontrola k doporučené cílové hodnotě (která ještě v kohortě EA II z roku 1998 byla fakticky asi nedosažitelným cílem).
V naší analýze jsme rovněž měli možnost hodnotit mortalitu ve 4 starších kohortách projektu. Je samozřejmě jasné, že analyzované soubory nejsou dostatečně velké, abychom z nich mohli činit nějaké dalekosáhlejší závěry, a navíc je zda řada dalších proměnných. Je celkem jasné, že např. vzestup mortality mezi kohortou EA II a III lze asi především připsat na vrub odlišné věkové struktury (ostatně rozdíl po adjustaci právě na věk prakticky vymizel). Naopak již statisticky významný pokles mezi EA III a IV můžeme teoreticky připsat výše popsané zlepšující se situaci z hlediska prevalence diabetu, ale to by muselo být potvrzeno ještě na jiné a hlavně větší kohortě. Každopádně lze ale konstatovat, že celková mortalita u stabilizovaných pacientů s chronickou ICHS je u nás relativně příznivá (okolo 2 % za rok)
Naše studie má samozřejmě řadu limitací. Především zahrnuje pouze stabilizované pacienty, neboť ti s nejtěžším průběhem zemřeli mezi propuštěním z hospitalizace a vyšetřením v naší studii, či se díky své fyzické inkapacitě nebyli schopni dostavit (totéž platí i pro pacienty s těžkou non-kompliancí k léčbě, kteří také pravděpodobně na pozvánku k vyšetření převážně nerespondovali). Na druhé straně, tento nedostatek možná naše závěry paradoxně posiluje z hlediska klinické interpretace, neboť naše analýza je tak zúžena pouze na ty z pacientů, kteří jsou schopni ze sekundární prevence jednoznačně profitovat. Naši probandi také vesměs pocházejí z blízkého okolí velkých nemocnic univerzitního typu a lze tušit, že mimo velké aglomerace může být situace dosti odlišná (horší?).
Závěr
Závěrem můžeme konstatovat, že přes nesporný pokrok v některých oblastech v sobě realizace sekundární prevence v klinické praxi skrývá ještě velký nevyužitý potenciál ke zlepšení osudu pacientů se stabilizovanou ICHS. Pokud bychom také měli identifikovat jednotlivý faktor, pro který je aktuálně největší šance efektivně situaci zlepšit, je to bezpochyby intenzifikace hypolipidemické léčby. Naopak velkou výzvou zůstává u pacientů s ICHS alarmující prevalence diabetu.
Předkládaná analýza byla realizována za grantové podpory Agentury zdravotnického výzkumu Ministerstva Zdravotnictví (grant 17–29520A), dále pak fondu Specifického výzkumu Univerzity Karlovy (grant SVV 260 393) a Výzkumného programu PROGRES Univerzity Karlovy (projekt Q39).
Použili jsme také data z předcházejících studií EURASPIRE, realizované pod záštitou Evropské kardiologické společnosti (ESC). Projekt EUROASPIRE byl do České republiky přinesen z iniciativy prof. Jaroslava Šimona (zemřel v roce 2010), tehdy jako člena Pracovní skupiny preventivní kardiologie ESC, která tento projekt spustila.
Zejména bychom ale chtěli poděkovat všem spolupracovníkům, kteří v posledních 22 letech jednotlivé studie EUROASPIRE s námi realizovali (podle abecedního pořádku):
V. Adámková**, J. Bělohoubek**, R. Cífková*, J. Filipovský, J. Jeschke, M. Galovcová**, J. Gelžinský, P. Haman, J. Hrbková, P. Karnosová, A. Krajčoviechová*, S. Mareš, M. Mateřánková, M. Patraulea, M. Plášková*, H. Rosolová, J. Seidlerová, Z. Skodova**, V. Svobodová, K. Timoracká, J. Vaněk a P. Wohlfart* (II. interní klinika LF UK a FN Plzeň; *Centrum kardiovaskulární prevence 1. LF UK a Thomayerovy nemocnice Praha; **Pracoviště preventivní kardiologie IKEM Praha).
prof. MUDr. Otto Mayer jr., CSc.
II interní klinika LF UK a FN Plzeň
Doručeno do redakce 5. 11. 2018
Přijato po recenzi 15. 11. 2018
Sources
- Pyorala K, De Backer G, Graham I et al. Prevention of coronary heart di1. Pyorala K, De Backer G, Graham I et al. Prevention of coronary heart disease in clinical practice. Recommendations of the Task Force of the European Society of Cardiology, European Atherosclerosis Society and European Society of Hypertension. Eur Heart J 1994; 15(10): 1300–1331.
- Prevention of coronary heart disease in clinical practice. Recommendations of the Second Joint Task Force of European and other Societies on coronary prevention. Eur Heart J 1998; 19(10): 1434–1503.
- De Backer G, Ambrosioni E, Borch-Johnsen K et al. European guidelines on cardiovascular disease prevention in clinical practice. Third Joint Task Force of European and Other Societies on Cardiovascular Disease Prevention in Clinical Practice. Eur Heart J 2003; 24(17): 1601–1610.
- Graham I, Atar D, Borch-Johnsen K et al. European guidelines on cardiovascular disease prevention in clinical practice: full text. Fourth Joint Task Force of the European Society of Cardiology and other societies on cardiovascular disease prevention in clinical practice (constituted by representatives of nine societies and by invited experts). Eur J Cardiovasc Prev Rehabil 2007; 14(Suppl 2): S1-S113. Dostupné z DOI: <http://dx.doi.org/10.1097/01.hjr.0000277983.23934.c9>.
- Perk J, De Backer G, Gohlke H et al. European Guidelines on cardiovascular disease prevention in clinical practice (version 2012). The Fifth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of nine societies and by invited experts). Eur Heart J 2012; 33(13): 1635–1701. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehs092>.Erratum in Eur Heart J 2012; 33(17): 2126.
- EUROASPIRE. A European Society of Cardiology survey of secondary prevention of coronary heart disease: principal results. EUROASPIRE Study Group. European Action on Secondary Prevention through Intervention to Reduce Events. Eur Heart J 1997; 18(10): 1569–1582. Erratum in Eur Heart J 1998; 19(2): 356–357.
- Lifestyle and risk factor management and use of drug therapies in coronary patients from 15 countries; principal results from EUROASPIRE II Euro Heart Survey Programme. Eur Heart J 2001; 22(7): 554–572. Dostupné z DOI: <http://dx.doi.org/10.1053/euhj.2001.2610>.
- Kotseva K, Wood D, De Backer G et al. EUROASPIRE III: a survey on the lifestyle, risk factors and use of cardioprotective drug therapies in coronary patients from 22 European countries. Eur J Cardiovasc Prev Rehabil 2009; 16(2): 121–137. Dostupné z DOI: <http://dx.doi.org/10.1097/HJR.0b013e3283294b1d>.
- Kotseva K, Wood D, De Bacquer D et al. EUROASPIRE IV: A European Society of Cardiology survey on the lifestyle, risk factor and therapeutic management of coronary patients from 24 European countries. Eur J Prev Cardiol 2016; 23(6): 636–648. Dostupné z DOI: <http://dx.doi.org/10.1177/2047487315569401>.
- Bruthans J, Cifkova R, Lanska V et al. Explaining the decline in coronary heart disease mortality in the Czech Republic between 1985 and 2007. Eur J Prev Cardiol 2014; 21(7): 829–839. Dostupné z DOI: <http://dx.doi.org/10.1177/2047487312469476>.
- Norgaard ML, Andersen SS, Schramm TK et al. Changes in short - and long-term cardiovascular risk of incident diabetes and incident myocardial infarction – a nationwide study. Diabetologia 2010; 53(8): 1612–1619. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–010–1783-z>.
- Movsisyan NK, Sochor O, Kralikova E et al. Current and past smoking patterns in a Central European urban population: a cross-sectional study in a high-burden country. BMC Public Health 2016; 16 : 571. Dostupné z DOI: <http://dx.doi.org/10.1186/s12889–016–3216–5>.
- Piepoli MF, Hoes AW, Agewall S et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts): Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur J Prev Cardiol 2016; 23(11): np1-np96. Dostupné z DOI: <http://dx.doi.org/10.1177/2047487316653709>.
- James WP, Caterson ID, Coutinho W et al. Effect of sibutramine on cardiovascular outcomes in overweight and obese subjects. N Engl J Med 2010; 363(10): 905–917. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1003114>.
- Turnbull F, Neal B, Ninomiya T et al. Effects of different regimens to lower blood pressure on major cardiovascular events in older and younger adults: meta-analysis of randomised trials. BMJ 2008; 336(7653): 1121–1123. Dostupné z DOI: <http://dx.doi.org/10.1136/bmj.39548.738368.BE>.
- Wright jr. JT, Williamson JD, Whelton PK et al. A Randomized Trial of Intensive versus Standard Blood-Pressure Control. N Engl J Med 2015; 373(22): 2103–2116. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1511939>.
- Baigent C, Keech A, Kearney PM et al. Efficacy and safety of cholesterol-lowering treatment: prospective meta-analysis of data from 90,056 participants in 14 randomised trials of statins. Lancet 2005; 366(9493): 1267–1278. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(05)67394–1>. Erratum in Lancet 2005; 366(9494):1358.Lancet 2008; 371(9630): 2084.
- Grundy SM, Cleeman JI, Merz CN et al. Implications of recent clinical trials for the National Cholesterol Education Program Adult Treatment Panel III guidelines. Circulation 2004; 110(2): 227–239. Dostupné z DOI: <http://dx.doi.org/10.1161/01.CIR.0000133317.49796.0E>.
- Vorlíčková P, Mayer O, Bruthans J et al. The changes in achievement of target LDL-cholesterol levels between 2006 and 2017 in Czech patients with chronic coronary heart disease. Cor Vasa 2018; June 6. Dostupné z DOI: <http://dxdoi.org/10.1016/j.crvasa.2018.05.002>.
- Sabatine MS, Giugliano RP, Keech AC et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med 2017; 376(18) :1713–1722. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1615664>.
- Slezak D, Mayer O, Bruthans J et al. The Prognostic Importance of Impaired Fasting Glycemia in Chronic Coronary Heart Disease Patients. Exp Clin Endocrinol Diabetes 2018; Aug 29. Dostupné z DOI: <http://dx.doi.org/10.1055/a-0684–9601>.
- De Bacquer D, Dallongeville J, Kotseva K et al. Residual risk of cardiovascular mortality in patients with coronary heart disease: the EUROASPIRE risk categories. Int J Cardiol 2013; 168(2): 910–914. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ijcard.2012.10.051>.
- Zinman B, Wanner C, Lachin JM et al. Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med 2015; 373(22): 2117–2128. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1504720>.
- Marso SP, Daniels GH, Brown-Frandsen K et al. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med 2016; 375(4): 311–322. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1603827>.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2018 Issue 12-
All articles in this issue
- Souhrn konsenzu EAS týkajícího se kauzálního vztahu mezi lipoproteiny o nízké hustotě a aterosklerotickými kardiovaskulárními onemocněními zpracovaný výborem České společnosti pro aterosklerózu
- Společné stanovisko odborných společností k předepisování PCSK9 inhibitorů
- Komentář k nejdůležitějším a nejnovějším studiím s inhibitory PCSK9
- Zánět a ateroskleróza
- Bilirubin: od nevýznamného katabolického produktu k závažnému predikčnímu faktoru infarktu myokardu
- U HDL-cholesterolu již zřejmě neplatí „čím výše, tím lépe“
- Současné pohledy na metabolický syndrom
- Lipoprotein(a) – kardiovaskulární rizikový faktor: význam a možnosti terapie
- Proč nebrzdit volný pád LDL-cholesterolu a nepomlouvat statiny
- Kombinovaná hypolipidemická léčba
- Inhibítory PCSK9 a diabetes mellitus
- Změny úrovně sekundární prevence ischemické choroby srdeční mezi lety 1995–2017 v České republice: porovnání studií EUROASPIRE I, II, III, IV a V
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Lipoprotein(a) – kardiovaskulární rizikový faktor: význam a možnosti terapie
- Současné pohledy na metabolický syndrom
- Proč nebrzdit volný pád LDL-cholesterolu a nepomlouvat statiny
- Kombinovaná hypolipidemická léčba
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

