-
Medical journals
- Career
Diagnostika a léčba komunitní pneumonie – v jednoduchosti je klíč k úspěchu
Authors: Vítězslav Kolek; Petr Jakubec; Stanislav Losse
Authors‘ workplace: Klinika plicních nemocí a tuberkulózy LF UP a FN Olomouc
Published in: Vnitř Lék 2017; 63(11): 770-775
Category: Reviews
Overview
Pneumonie je nejčastější infekční onemocnění, které vyžaduje neustálou pozornost. Je definována jako akutní zánětlivé onemocnění postihující plicní alveoly, respirační bronchioly a plicní intersticium. V posledních letech je patrná snaha zracionalizovat přístup k pneumoniím a využít současné způsoby podávání účinných antibiotik ke snížení výskytu komplikací, omezení počtu hospitalizací a zkrácení délky léčby. Při znalosti většiny potenciálních agens převažuje léčba empirická, která je navíc podpořena znalostí regionální epidemiologické situace, dobrou diagnostikou a zkušenostmi s racionální antibiotickou léčbou. Velmi důležitá je kategorizace pacienta podle možných rizik komplikací a mortality. Z toho následně vyplývá zvolený způsob léčby: ambulantní nebo formou hospitalizace.
Klíčová slova:
komunitní pneumonie – kritéria léčby – prognóza – výskytEpidemiologie
Pneumonie se vyskytují po celém světě a ve všech věkových kategoriích. Jde o jedno z nejzávažnějších onemocnění vůbec. Ročně na ně umírají asi 3 800 000 lidí a jsou nejčastější příčinou úmrtí dětí do 5 let věku, ročně vzniká asi 420 000 000 případů, ale jde jen o kvalifikovaně odhadovaná data [1]. Pneumonie významně ekonomicky zatěžují zdravotní systémy a je zřejmé, že toto zatížení lze snížit díky racionální a včasné antibiotické léčbě [2,3]. Je patrná souvislost mezi množstvím podávaných antibiotik a vyšším výskytem rezistencí patogenů, ale na druhé straně také s poklesem mortality a počtu hospitalizací [4]. Očekávané epidemiologické trendy předpokládají spíše mírný pokles ve výskytu i mortalitě, ale poslední studie v USA ukazují, že počet hospitalizací pro pneumonie u starších osob neklesá [4]. V rozvojovém světě je výskyt pneumonií těžko přesně doložitelný, ale je nepochybně vyšší než v rozvinutých zemích. Existuje zřejmý vztah mezi stavem výživy a obecnou úrovní hygieny, především hygieny chrupu a dutiny ústní. Se stoupajícím věkem nastupuje imunosenescence, což se projevuje nárůstem výskytu pneumonií. V ČR je podle ÚZIS počet hospitalizací pacientů nad 18 let 200/100 000 a u nemocných nad 50 let je to 450/100 000. Očekává se postupný pokles mortality, zatím je ale obtížné tuto skutečnost hodnotit, protože obecně respiračních infekcí přibývá a počet hospitalizací v rozvinutých zemích neklesá. Výskyt pneumonie může příznivě ovlivnit především vakcinace chřipkovou a pneumokokovou vakcínou [5,6]. Za efektivní se rovněž pokládá doporučení ukončit kouření u kuřáků, jinak je ale obtížné trendy výskytu nemoci posuzovat. V ČR ročně postihne více než 100 000 obyvatel, z nichž asi 3 000 nemoci podlehnou.
Definice
Pneumonie je akutní zánět v oblasti respiračních bronchiolů, alveolárních struktur a plicního intersticia [1]. Klinicky je stav definován jako nález čerstvého infiltrátu na skiagramu hrudníku spolu s nejméně 2 příznaky infekce respiračního traktu (nejčastěji kašel, dále dušnost, bolest na hrudníku, teplota a poslechový nález).
Používá se epidemiologické rozdělení [1,7]:
- komunitní pneumonie, tj. získané v běžném životním prostředí mimo nemocniční zařízení, jsou vyvolány různými infekčními původci většinou dobře citlivými na antibiotika
- nozokomiální pneumonie jsou získané v souvislosti s pobytem v nemocnici, specifickou skupinu představují pneumonie tzv. ventilátorové
Lékaři pracující v ambulantní praxi se setkávají především s komunitními pneumoniemi, ale s nozokomiální pneumonií je nutno počítat i u pacientů až 14 dní po jejich propuštění z nemocnice. Infekční agens je poznáno zpravidla pouze méně než v 50 % případů a léčba se vede racionálně empiricky. Tato léčba by měla probíhat podle klinických doporučení, která vycházejí z tradic i aktuálních studií a vyvíjejí se v čase [1,7–9]. Správná aplikace klinických doporučení snižuje mortalitu [10].
Etiologie
Zdrojem nákazy jsou nejčastěji mikroaspirace mikrobů nazofaryngu samotného pacienta nebo se infekce šíří vzdušnou cestou. Predisponující faktory jsou opakované virové respirační infekce, kouření, srdeční selhání, alkoholizmus, CHOPN a jiná chronická respirační onemocnění, tělesná vyčerpanost, primární nebo sekundární poruchy imunity, asplenie, uremie, alterace vědomí, dysfagie, chronické onemocnění ledvin, maligní onemocnění, špatně kompenzovaný diabetes, dlouhodobé či opakované hospitalizace a aplikace antimikrobních přípravků [8,9]. Při vzniku pneumonie se obecně uplatňuje stav imunity, jejíž oslabení věkem mohou urychlit přidružená onemocnění. Velmi důležitý je vliv mikrobiomu a každá změna mikrobiologické rovnováhy v dolních respiračních cestách. Nejčastější příčinou komunitní pneumonie jsou Streptococcus pneumoniae, Haemophilus influenzae, Mycoplasma pneumoniae, Chlamydophila pneumoniae, méně často Moraxella catarrhalis a Staphylococcus aureus, vzácně Legionella pneumophila. V současnosti trvají nejasnosti v chápání významu onemocnění způsobených atypickými patogeny. Při důsledném sérologickém vyšetřování se ukazuje, že jejich podíl dosahuje více než 30 %. Studie z praxe sledující výskyt pomocí metod polymerázové řetězové reakce (polymerase chain reaction – PCR) naopak ukazují, že jejich podíl je minimální [11,12]. Podobně nepřesná data jsou k dispozici u infekcí smíšených [13]. Je pravděpodobné, že podrobnější mikrobiologická data nebudou dostupná ani v budoucnu, protože v poslední době detekce komunitních patogenů obecně klesá [14,15].
Klinický obraz
Klinický obraz se většinou rozvíjí podle rozsahu postižení plicního parenchymu a celkového stavu pacienta. Onemocnění může probíhat lehce, středně závažně až těžce podle několika mezinárodně stanovených kritérií. Ambulantně lze bezpečně léčit pouze lehké pneumonie. Typickými příznaky jsou náhlé febrilie, někdy spojené s třesavkou a zimnicí, případně se rozvíjí pozvolně se zvyšující subfebrilie po předchozím zánětu horních cest dýchacích. Kašel může být suchý nebo s expektorací různé kvality a kvantity včetně hemoptýzy. Dále se může přidružit pleurální bolest a dušnost, které mohou být různého stupně v závislosti na rozsahu plicní infiltrace. Poslechovým nálezem jsou chrůpky, trubicové, kompresivní nebo oslabené dýchání, může být slyšet krepitus. Při lehčích průbězích pneumonií bývá i jen minimální poslechový nález. Poklep bývá ztemnělý v oblasti výpotku, nad ním může být bubínkový. V RTG obraze je typická různě rozsáhlá a různě homogenní infiltrace nebo retikulonodulace. Výpotek bývá nástěnný, někdy může být ohraničený, uložený interlobárně nebo subpulmonálně. V rámci celkových projevů se objevují bolesti hlavy, svalů a kloubů, nauzea, zvracení a pocity slabosti. Jako průvodní jev se vyskytuje zejména u pneumokokových pneumonií herpes labialis. Obtížně poznatelná může být pneumonie u seniorů, při níž jsou minimální respirační příznaky a nebývají teploty. Nemoc se může projevit snížením aktivity, zmateností nebo nechutenstvím, aniž by nemocní udávali dušnost nebo kašel. U seniorů jsou respirační příznaky někdy potlačeny, ale zhoršuje se imobilita, dostavují se deliria, akutní srdeční potíže (fibrilace síní), bolesti břicha a rozvíjí se sepse.
Diagnóza
Je třeba zvážit anamnestické údaje, rychlost nástupu potíží, charakter teplot, celkové projevy onemocnění a také věkové faktory. Skiagram hrudníku ve dvou projekcích a jeho řádné vyhodnocení jsou u dospělých nemocných nepodkročitelným minimem. Infiltrát však nemusí být přítomen u dehydratovaných nemocných, při leukopenii nebo emfyzému. Původce nákazy může odhalit izolace agens ze sputa nebo z krve, pozitivní průkaz antigenu pneumokoků nebo legionel v moči, sérologické nebo PCR vyšetření. Mikrobiologické testy nejsou vždy při ambulantním vyšetření nezbytné, ale mohou pomoci při neúčinnosti podané antibiotické léčby a výběru jiného antibiotika [1,7,14]. Určitý význam má zvýšení CRP > 60 mg/l, může být přítomna leukocytóza s posunem doleva (15 % nesegmentovaných leukocytů). Provádění jiných laboratorních testů se nepokládá za přínosné [7–9]. V ambulantní praxi však tato vyšetření nemají zásadní význam pro volbu iniciální léčby. O to více je potřeba využít mikrobiologické testy u těžších forem spojených s hospitalizací. Často se vyplatí odebírat materiál cíleně z dolních dýchacích cest např. pomocí bronchoskopie.
Diferenciální diagnostika
Podobné klinické příznaky mohou mít plicní karcinom, tuberkulóza, plicní embolie nebo kardiální onemocnění. Proto je nutné při neustupujících potížích a radiologickém nálezu (non responding pneumonia) diagnostické metody zásadně rozšířit.
Prognóza
Prognóza je dána uvedenými věkovými a jinými rizikovými faktory, výrazně se zhoršuje u polymorbidních nemocných, především s malignitou. Léčba antibiotiky je zvláště u těžkých pneumonií jen dílčí součástí komplexní péče o konkrétní nemocné. Nicméně prognóza se zásadně zlepšuje a výskyt komplikací klesá, pokud se antibiotikum podá co nejdříve, nejlépe do 8 hod od stanovení diagnózy. Ambulantní kontrola se provádí kontaktem po 2–3 dnech léčby a dále za týden až 14 dní po ukončení léčby včetně skiagramu hrudníku [8,9]. Podle rozsáhlé americké studie z běžné ambulantní praxe provedené na 251 947 dospělých pacientech s pneumonií dojde asi u každého čtvrtého z nich k selhání prvního antibiotika. 71 % z těchto pacientů potřebovalo výměnu antibiotika a 21 % další antibiotikum, 5 % bylo hospitalizováno a 3 % potřebují urgentní péči [16]. Rizikové aspekty selhání jsou věk a komorbidity, prokázání Streptococcus pneumoniae a překvapivě i ženské pohlaví. Výběr iniciálního antibiotika měl pro prognózu minimální význam. V podstatně menší multicentrické studii provedené v ČR došlo k selhání prvního antibiotika v 32 %, hospitalizace byla nutná u 6 % z nich [17]. Bohužel je třeba konstatovat, že i přes zavedení moderních účinných antibiotik do rutinní klinické praxe je pneumonie mezi infekčními procesy nejčastější příčinou úmrtí.
Prevence a profylaxe
Morbidita i mortalita pneumonií je sice stále mezi infekčními nemocemi nejvyšší, klesla však vlivem zavedení moderní antibiotické terapie (ATB) a pravděpodobně i očkování proti chřipce. Očkování dospělých protichřipkovou vakcínou je vhodné především u osob nad 65 let věku, nad 50 let, jestliže mají chronické respirační nebo kardiální onemocnění. Výskyt pneumonií pneumokokové etiologie lze ovlivnit očkováním dětí i dospělých pneumokokovou vakcínou, která se rovněž doporučuje u populace starší 65 let a opakovaně u osob v riziku, především se sníženou imunitou. Používá se 13valentní konjugovaná vakcína (PCV 13), která obsahuje purifikované kapsulární polysacharidy Streptococcus pneumoniae konjugované s netoxickým difteriovým toxinem. Další vakcínou je 23valentní vakcínou z purifikovaných kapsulárních polysacharidových antigenů (PPSV 23). Vakcíny jsou cíleny na snížení invazivních pneumokokových nákaz. Účinnost v prevenci „invazivních pneumonií“ v dospělé populaci byla prokázána řadou studií i jejich metaanalýzou [18], účinnost na neinvazivní pneumonie je prokázána méně přesvědčivě. Z chronických plicních nemocí mají nejvyšší riziko vzniku pneumonie idiopatická plicní fibróza, chronická obstrukční plicní nemoc a astma. U nich přináší kombinované očkování proti chřipce i pneumokokům významné snížení zdravotních rizik i nákladů na zdravotní péči.
Terapie
V případě zjištění pneumonie je zásadní co nejrychlejší empirické podání antibiotika (do 8 hod od potvrzení diagnózy) a ohodnocení rizika komplikací u konkrétního pacienta. Při hospitalizaci je ideální podat antibiotikum již během příjmu – do 1 hod od diagnózy. Celková doba léčby se u současných antibiotik doporučuje 5–10 dnů, déle je nutná v individuálních případech dle klinického a laboratorního nálezu u infekcí způsobenými atypickými agens a gramnegativními patogeny [7–9].
Indikaci hospitalizace lze objektivizovat podle řady kritérií, nejjednodušší a přitom dobře použitelná jsou kritéria německá [12]. Ta se řídí jednoduchým rozdělením na lehké, středně těžké a těžké pneumonie dle kritérií CRB-65 (tab. 1). Při středně těžkém a těžkém průběhu je hospitalizace potřebná. Vhodná je při přítomnosti jednoho kritéria, nutná při přítomnosti 2 kritérií. Umístění na JIP (těžká pneumonie) je nutné při přítomnosti 3 nebo 4 kritérií z uvedené škály CRB-65. S hospitalizací není možno otálet u starších polymorbidních nemocných, při rozsáhlém RTG nálezu (oboustranné postižení, výpotek, rozpadový proces) nebo při zjištění respirační insuficience ověřené pulzní oxymetrií. Je však nutno také zvážit riziko delší hospitalizace a celkového zhoršení funkčního stavu u seniorů, kteří by jinak mohli zůstat v domácí léčbě nebo v zařízení s pečovatelskou službou.
Table 1. Rozhodování o hospitalizaci dle kritérií CRB-65 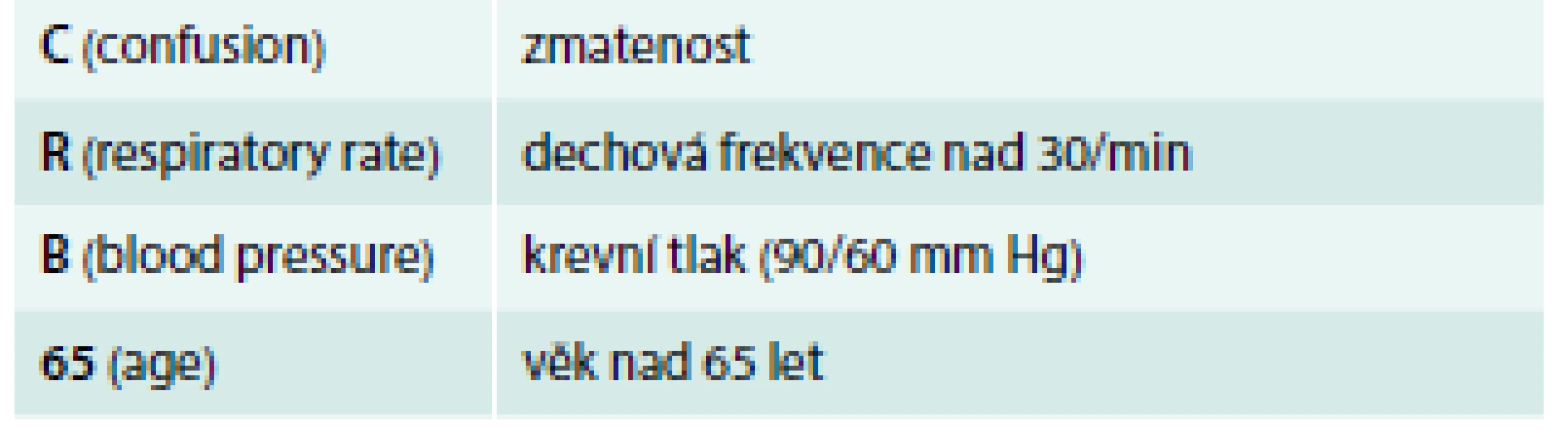
Ambulantně se empiricky většinou podává amoxicilin, lze však podat i jiná účinná antibiotika (cefalosporiny 2. generace, makrolidy nebo doxycyklin), preference je bez znalosti agens obtížná (tab. 2) [19]. V těchto souvislostech není dost dokladů pro tvrzení, že některé antibiotikum je účinnější než jiné. Ryze praktické doporučení zní: používejte antibiotika, s nimiž máte zkušenosti a která nejsou u konkrétního pacienta potenciální škodlivá svými vedlejšími účinky. Nicméně je jistě velmi důležité sledovat stav rezistence patogenů vůči jednotlivým skupinám antibiotik v komunitě. V některých zemích je doslova alarmující. Zvláště je obava z přenesené rezistence na fluorochinolony [20]. Je třeba si uvědomit, že amoxicilin (včetně formy kombinované s inhibitorem betalaktamáz), stejně jako cefalosporiny jsou účinné pouze na pneumokoky a jiná typická agens, nikoliv na Mycoplasma pneumoniae a Chlamydophila pneumoniae. Makrolidy jsou účinné na pneumokoky a atypická agens, ale velmi málo na Haemophilus influenzae nebo Moraxella catarrhalis. Doxycyklin se uznává pro výhodnou cenu, ale i dostatečnou účinnost na pneumokoky i atypická agens. Aminopeniciliny s inhibitory betalaktamáz jsou vhodné u starších polymorbidních nemocných nebo při průkazu kmenů Haemophilus influenzae nebo Moraxella catarrhalis produkujících betalaktamázy. Při alergii na peniciliny lze alternativně podat cefalosporiny 2. generace. Při neúspěchu s prvním antibiotikem je možné antibiotikum vyměnit nebo přidat 2. antibiotikum do kombinace (aminopenicilin + makrolid). V ambulanci se lze již opřít o výsledky mikrobiologických testů spíše jen teoreticky a cílená léčba je většinou možná až po selhání prvního antibiotika. Součástí celkové terapie při febrilních stavech je podávání antipyretik, analgetik při bolestech, antitusik při suchém, dráždivém kašli, a naopak mukolytik při produktivní fázi.
Table 2. Empirické podávání antibiotik v ambulanci v ČR 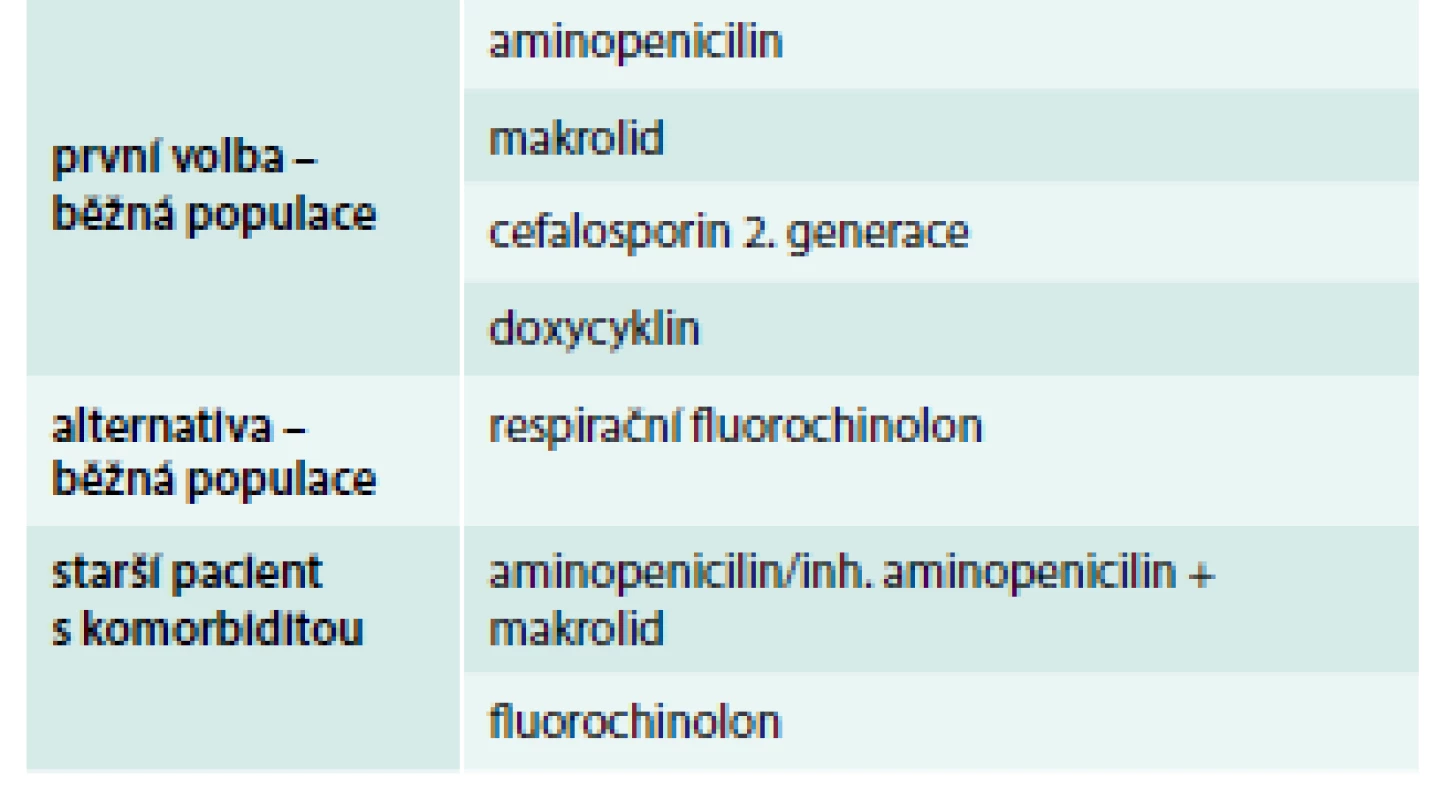
Při hospitalizaci se iniciálně podávají antibiotika rovněž empiricky, zásadou číslo jedna je rychlost podání. Doporučení v konkrétních případech ukazuje tab. 3.
Table 3. Doporučená antibiotika při hospitalizaci 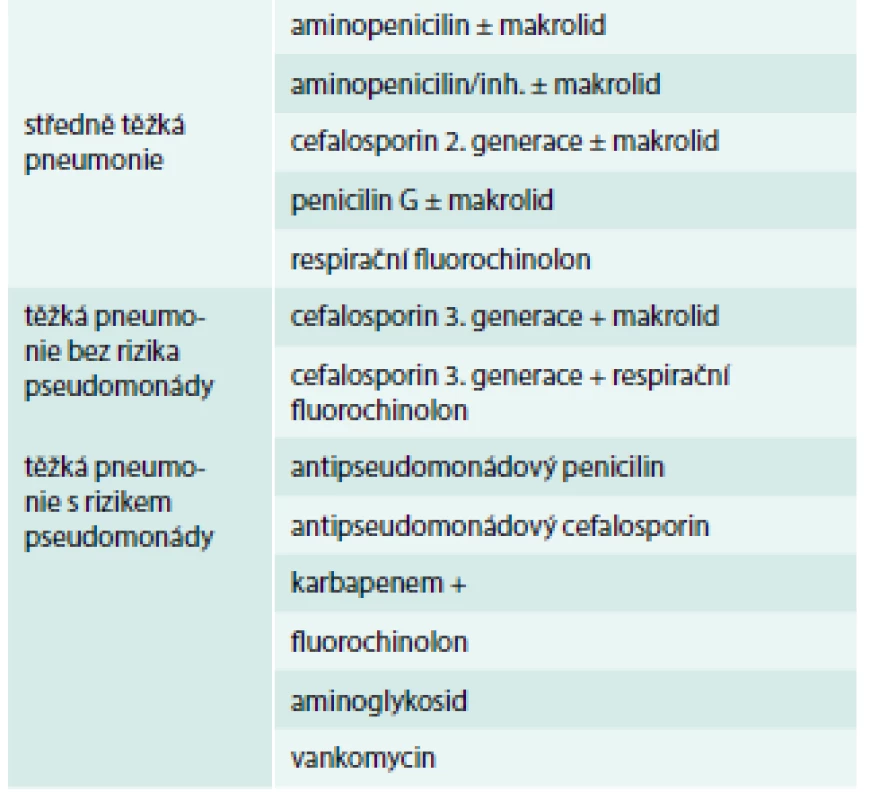
Stále se diskutuje o podání kombinace makrolidů a aminopenicilinů v iniciální léčbě. Metaanalýzy ukázaly při podávání kombinace až 22% snížení mortality [21,22]. Cílenou léčbu se znalostí agens a jeho citlivosti k antibiotikům lze použít až po získání výsledků z mikrobiologických testů (tab. 4). Tyto informace mohou být relevantní při selhání antibiotika první volby a je možné je také využít pro deeskalaci léčby směrem k účinnému antibiotiku užšího spektra účinku. Při hospitalizaci se vyplatí kategorizovat pacienty vzhledem k riziku výskytu pseudomonády, protože léčba pseudomonádových infekcí je rozdílná a většinou vyžaduje kombinaci antibiotik. Během hospitalizace je potřeba sledovat všechny komorbidity a předcházet jejich dekompenzaci. Důležitý je klid na lůžku a podávání tekutin (3–4 litry denně). U těžké pneumonie je léčba individuální ve vztahu k celkovému stavu pacienta [23]. Tato jednotka má svou definici a kritéria diagnostiky i léčby. Je třeba počítat s neinvazivní ventilací, hlavně u nemocných s chronickou obstrukční plicní nemocí (CHOPN) a s nastupujícím syndromem akutního respiračního selhání (ARDS), podávají se nízkomolekulární hepariny. Je třeba sledovat riziko nastupující sepse a šoku. Diskutuje se o významu statinů a ACE inhibitorů, které mohou snižovat riziko vzniku pneumonie i úmrtnosti na ni. V poslední době se objevily studie o podávání kortikosteroidů, které mírně zkracují dobu hospitalizace a délku trvání symptomů zánětu. Stejně tak se ověřují možnosti imunomodulace a intravenózní podávání vitaminu C a tiaminu. Nelze také podceňovat následný neuropsychický stres a fyzické následky jako jsou snížení plicních funkcí, stavy dušnosti, postinfekční kašel, artralgie nebo přetrvávající celková slabost. Pneumonie zanechává dlouhodobé následky ve smyslu snížení pocitu celkového zdraví a je indikací možné existence jiného závažného onemocnění nebo i předčasného úmrtí.
Table 4. Pneumonie – cílené podávání antibiotik 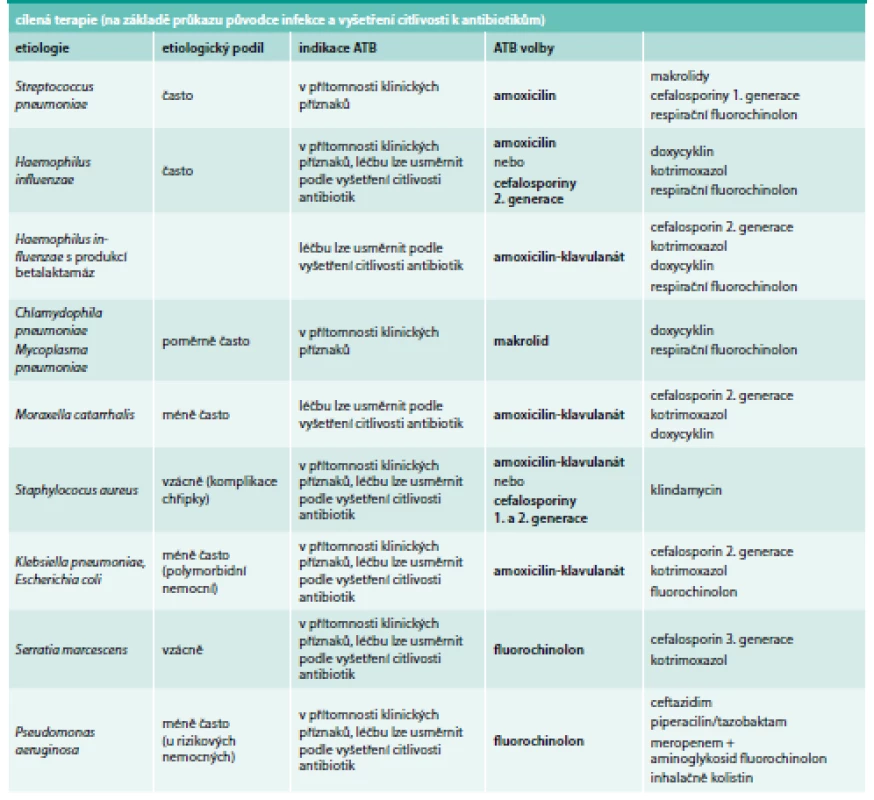
aminopeniciliny: amoxicilin, ampicilin aminopeniciliny s inhibitory betalaktamáz: amoxicilin/kyselina klavulanová makrolidy: klaritromycin, azitromycin, rovamycin cefalosporiny 2. generace: cefuroxim, cefprozil cefalosporiny 3. generace: cefixim, cefotaxim, ceftriaxon, cefpodoxim fluorochinolony: ciprofloxacin, ofloxacin respirační fluorochinolony: levofloxacin, moxifloxacin aminoglykosidy: gentamycin, amikacin, kanamycin, tobramycin, kolomycin antipseudomonádové peniciliny: piperacilin-tazobaktam antipseudomonádové cefalosporiny: ceftazidim, cefepim karbapenemy: meropenem/tazobaktam, imipenem, aztreonam Praktické výstupy z poslední doby se snaží o simplifikaci preference antibiotik, což může usnadnit rychlost rozhodování, zvýšit komunikaci mezi lékaři a úspěšnost léčby. Takto vzniklo poslední britské doporučení pro iniciální léčbu pneumonie ve vztahu k závažnosti stavu vypracované organizací NICE (tab. 5). Jde o nejjednodušší návod, jak rychle nasadit iniciální léčbu a dále pacienta sledovat [24]. Délka léčby se zkrátila na nezbytnou dobu zvláště u lehkých pneumonií, při tradiční preferenci amoxicilinu se doporučují kombinace s makrolidy u středně těžkých a těžkých pneumonií. Prognostické faktory při hospitalizaci vyhodnotila jedna z mála prospektivně vedených studií poslední doby [25]. Ukázalo se, že různá používaná kritéria (IDSA/ATS, CURB nebo A-DROP) jsou srovnatelně spolehlivá a že prakticky použitelnými negativně prognostickými faktory jsou stoupající věk, hypotermie, vyšší dechová frekvence, urea a hypalbuminemie. Nicméně zásadní byla přítomnost CHOPN (OR: 1,77; 95% CI: 1,13–2,76), malignity (OR: 2,25; 95% CI: 1,25–4,06), respiračního selhání – PaO2/FiO2 ≤ 250 (OR: 3,15; 95% CI: 1,93–5,14) a potřeba mechanické ventilace (OR: 2,99; 95% CI: 1,75–5,12). Důležitým je poznatek, že kombinace azitromycinu a betalaktamového antibiotika signifikantně redukovala 30denní mortalitu (OR: 0,50; 95% CI: 0,26–0,97).
Table 5. Nové britské doporučení iniciální antibiotické léčby pneumonie 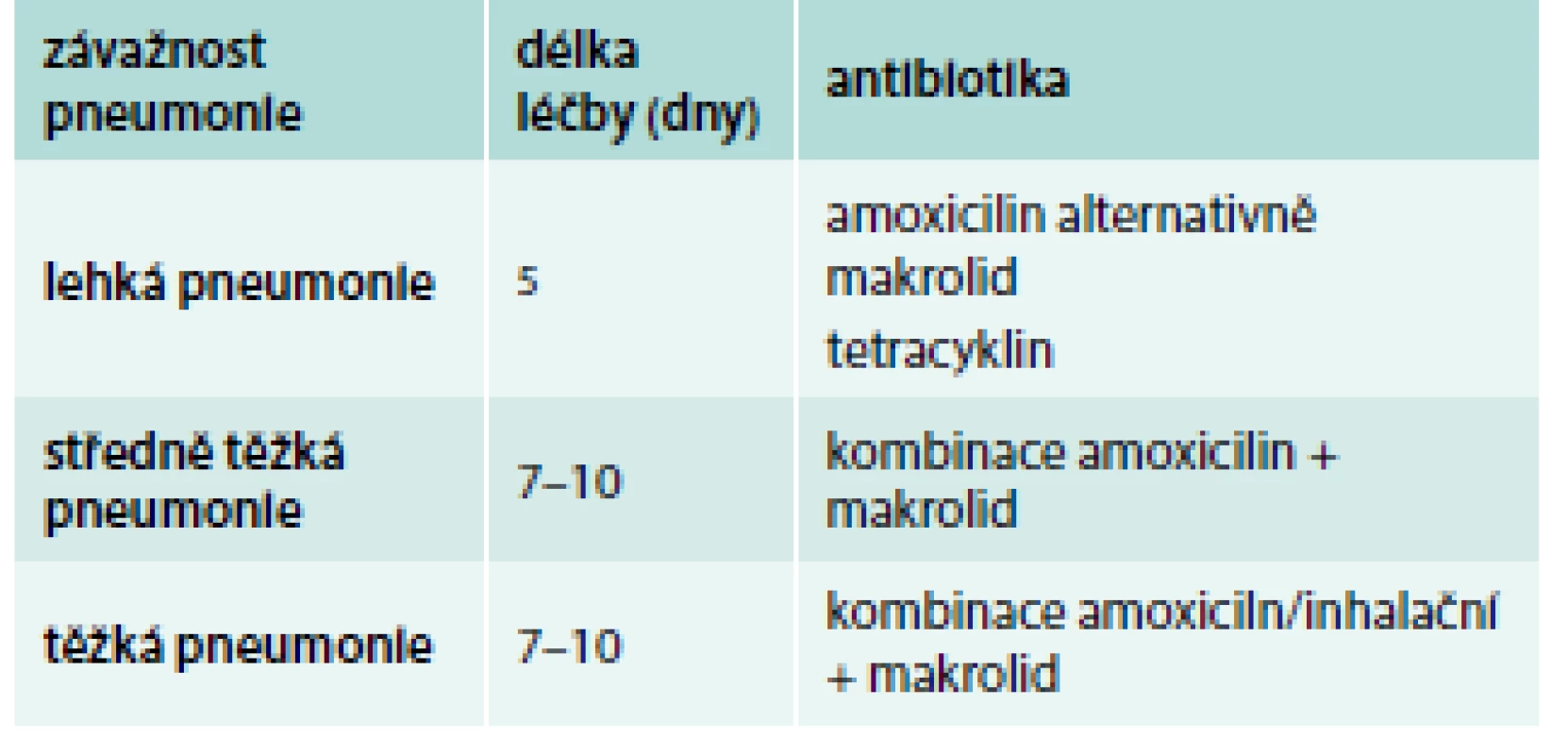
Závěr
Závěrem je možno konstatovat, že při známém spektru komunitních agens je potřeba zjednodušit empirickou léčbu komunitních pneumonií tak, aby mohla být podána co nejrychleji. Je třeba znát základní účinky běžně podávaných antibiotik, podávat je v dostatečné dávce a jen po nezbytně potřebnou dobu. Zcela zásadní je individuální vyhodnocení celkového stavu pacienta a jeho přidružených onemocnění.
prof. MUDr. Vítězslav Kolek, DrSc.
vitezstav.kolek@fnol.cz
Klinika plicních nemocí a tuberkulózy LF UP a
FN Olomouc
www.fnol.cz
Doručeno do redakce 18. 8. 2017
Přijato po recenzi 26. 9. 2017
Sources
1. Kolek V, Kolář M, Kašák V et al. Diagnostika a léčba komunitně získané pneumonie dospělých. Vnitř Lék 2011; 57(10): 858–866.
2. Niederman MS, McCombs JS, Unger AN et al. The cost of treating community-acquired pneumonia. Clin Ther 1998; 20(4): 820–837.
3. Guest JF, Morris A. Community-acquired pneumonia: the annual cost to the National Health Service in the United Kingdom. Eur Respir J 1997; 10(7): 1530–1534.
4. Gibson GJ, Loddenkemper R, Lundbäck B et al. Respiratory health and disease in Europe: the new European Lung White Book. Eur Respir J 2013; 42 : 559–563. Dostupné z DOI: <http://dx.doi.org/10.1183/09031936.00105513>.
5. File TM. Community-acquired pneumonia. Lancet 2003; 362(9400): 1991–2001.
6. Barlow GD, Lamping DL, Davey PG et al. Evaluation of outcomes in community-acquired pneumonia: a guide for patients, physicians, and policy-makers. Lancet Infect Dis 2003; 3(8): 476–488.
7. Woodhead M, Blasi F, Ewig S et al. Guidelines for the management of adult lower respiratory tract infections--full version. Clin Microbiol Infect 2011; 17(Suppl 6): E1-E59. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1469–0691.2011.03672.x>.
8. Mandell LA, Wunderink RG, Anzueto A et al. Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults. Clin Infect Dis 2007; 44(Suppl 2): S27-S72.
9. Macfarlane JT, Boldy D. 2004 update of BTS pneumonia guidelines: What´s new? Thorax 2004; 59(5): 364–366.
10. Dean NC, Silver MP, Bateman KA et al. Decreased mortality after implementation of a treatment guideline for community-acquired pneumonia. Am J Med 2001; 110(6): 451–457.
11. Kolek V, Fojtů H, Grygárková I et al. Pneumonie vyžadující hospitalizaci: výsledky dvouleté multicentrické studie v České republice. Int Med Prax 2002; 4(7): 347–352.
12. Pletz MW, Ewig S, Lange C et al. Update Pneumonie 2012. Dtsch Med Wochenschr 2012; 137(44): 2265–2284. Dostupné z DOI: <http://dx.doi.org/10.1055/s-0032–1305297>.
13. de Roux A, Ewig S, García E et al. Mixed community-acquired pneumonia in hospitalised patients. Eur Respir J 2006; 27(4): 795–800.
14. Gleason PP, Meehan TP, Fine JM et al. Associations between initial antimicrobial therapy and medical outcomes for hospitalized elderly patients with pneumonia. Arch Intern Med 1999; 159(21): 2562–2572.
15. Smith SB, Ruhnke GW, Weiss CH et al. Trends in Pathogens Among Patients Hospitalized for Pneumonia From 1993 to 2011. JAMA Intern Med 2014; 174(11): 1837–1839. Dostupné z DOI: <http://dx.doi.org/10.1001/jamainternmed.2014.4344>.
16. McKinnell J, Class P, Blumberg P et al. Clinical Predictors of Antibiotic Failure in Adult Outpatients with Community-Acquired Pneumonia. Am J Respir Crit Care Med 2017; 195: A2644. Dostupné z WWW: <http://www.atsjournals.org/doi/abs/10.1164/ajrccm-conference.2017.195.1_MeetingAbstracts.A2644>.
17. Kolek V, Bartoš V, Fojtů H et al. Studie PAP – Pneumonie v ambulantní péči. Stud Pneumol Phthiseol 2007; 67(4): 146–154.
18. Moberley S, Holden J, Tatham DP et al. Vaccines for preventing pneumococcal infection in adults. Cochrane Database Syst Rev 2013; (1): CD000422.Dostupné z DOI: <http://dx.doi.org/10.1002/14651858.CD000422.pub3>.
19. Kolek V, Vágnerová I et al. Kapesní původce ambulantní léčbou respiračních infekcí. Maxdorf: Praha 2016. ISBN 978–80–7345–490–6.
20. Ho PL, Tse WS, Tsang KWT et al. Risk factors for acquisition of Levofloxacin-resistant Streptococcus pneumoniae: A case-control study. Clin Infect Dis 2001; 32(5): 701–707.
21. Waterer GW, Somes GW, Wunderrink RG. Monotherapy may be suboptimal for severe bacteraemic pneumococcal pneumonia. Arch Intern Med 2001; 161(15): 1837–1842.
22. Martinez JA, Horcajada JP, Almela M et al. Addition of a macrolide to a beta-lactam-based empirical antibiotic regimen is associated with lower in-hospital mortality for patients with bacteremic pneumococcal pneumonia. Clin Infect Dis 2003; 36(4): 389–395.
23. Soo Hoo GW, Wen YE, Nguyen TV et al. Impact of clinical guidelines in the management of severe hospital-acquired pneumonia. Chest 2005; 128(4): 2778–2787.
24. Eccles S, Pincus C, Higgins B et al. Pneumonia. Diagnosis and management of community and hospital-acquired pneumonia in adults. BMJ 2014; 349:g6722. Dostupné z DOI: <http://dx.doi.org/10.1136/bmj.g6722>.
25. Ito A, Ishida T, Tokumasu H et al. Prognostic Factors in Hospitalized Community-Acquired Pneumonia. A Retrospective Study of a Prospective Observational Cohort. BMC Pulm Med 2017; 17(1): 78. Dostupné z DOI: <http://dx.doi.org/10.1186/s12890–017–0424–4>.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2017 Issue 11-
All articles in this issue
- Cílené vyhledávání nemocných s chronickou obstrukční plicní nemocí: stručný přehled
- Asthma bronchiale v kontextu vnitřního lékařství
- Diagnostika a léčba komunitní pneumonie – v jednoduchosti je klíč k úspěchu
- Nozokomiální pneumonie
- Pneumonie u imunokompromitovaných
- Idiopatická plicní fibróza. Umíme ji vždy správně diagnostikovat a léčit?
- Exogenní alergické alveolitidy: minimum pro praxi
- Sarkoidóza – nadále záhadné onemocnění
- Současný přístup k diagnostice, léčbě a prevenci tuberkulózy
-
Non-CF bronchiektázie dospělých: stručný přehled pro praxi
Dokument Sekce chorob s bronchiální obstrukcí České pneumologické a ftizeologické společnosti České lékařské společnosti J. E. Purkyně - Cystická fibróza dospělých
- Kardiovaskulární riziko spánkové apnoe a kazuistika
- Komplikace po transplantaci plic
- Nemalobuněčný karcinom plic
- Malobuněčný karcinom plic: epidemiologie, diagnostika a léčba
- Maligní mezoteliom pleury – dosud nepokořený nádor
- Spirometrie – základní vyšetření funkce plic
- Postavení bronchologie v pneumologické diagnostice
- Ultrasonografické vyšetření hrudníku v rukou lékaře klinika
- Neinvazivní ventilace
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Spirometrie – základní vyšetření funkce plic
- Neinvazivní ventilace
- Pneumonie u imunokompromitovaných
- Malobuněčný karcinom plic: epidemiologie, diagnostika a léčba
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

