-
Medical journals
- Career
Moderní trendy v inzulinoterapii
Authors: A. Adamíková; J. Rybka
Authors‘ workplace: Diabetologické centrum, koordinátorka MU Dr. Alena Adamíková, Ph. D., Interní klinika IPVZ Krajské nemocnice T. Bati, a. s., Zlín, přednosta prim. MU Dr. Jiří Latta
Published in: Vnitř Lék 2013; 59(6): 440-443
Category: 80th birthday prof. MUDr. Karla Horkého, DrSc., FACP (Hon.)
Overview
Pacienti s diabetem mellitus 2. typu mají dvojnásobně zvýšené riziko vývoje kardiovaskulárních onemocnění než pacienti bez diabetu a až 2/ 3 pacientů s diabetes mellitus 2. typu mohou zemřít na srdeční příhodu nebo cévní mozkovou příhodu, pokud se nepodaří ovlivnit riziko postupy, které zahrnují snížení krevního tlaku, hladiny cholesterolu, glykemie a zanechání kouření. Doporučení ADA/ EASD pro léčbu diabetu mellitu 2. typu zdůrazňují, že léčba má být vedena tak, aby se snížilo riziko kardiovaskulárních komplikací a nežádoucích účinků, především hypoglykemických příhod. Řada klinických studií, např. DCCT ‑ EDIC, UKPDS, prokázala význam intenzivní terapie inzulinem pro dosažení normoglykemie, poklesu rizika mikroangiopatických komplikací a kardiovaskulárního rizika. Studie ORIGIN s inzulinem glargin dokumentovala bezpečnost terapie dlouhodobým inzulinovým analogem a také redukci vzniku nového diabetu z prediabetických stadií. Inzulinoterapie se vzhledem k řadě pozitivních výsledků studií s inzulinovými analogy v algoritmu terapie posunula do druhé linie, hned za terapii metforminem a změnou životního stylu.
Klíčová slova:
inzulinová analoga – diabetes mellitus 2. typu – hypoglykemie – kardiovaskulární onemocněníÚvod
Současné postupy v léčbě diabetu mellitu 2. typu jsou ovlivněny výsledky velkých klinických studií a novými léky, ke kterým patří inkretiny a inhibitory SGLT ‑ 2. Inzulinoterapie získala nové místo v systému léčby, posunula se do časnějších stadií vývoje diabetu. Studie posuzují nejen efektivitu antidiabetické terapie, ale také bezpečnost pro pacienta. Krátkodobé efekty léčby jsou posuzovány poklesem hodnoty HbA1c v 1 – 2ročních studiích a rizikem vzniku hypoglykemických příhod. Dlouhodobé výsledky se soustřeďují na pokles kardiovaskulárního rizika, výskyt chronických diabetických komplikací a také na karcinogenní riziko. Mohou tak podstatně ovlivnit další použití antidiabetika v algoritmuterapie [1].
Studie zaměřené na intenzivní terapii u diabetiků 2. typu
UKPDS studie (the United Kingdom Prospective Diabetes Study) randomizovala 4 000 diabetiků 2. typu a srovnávala intenzivní léčbu sulfonylureou, metforminem a inzulinem s konvečními dietními postupy. Rozdíl v hodnotě HbA1c mezi intenzivně a konvenčně léčenou skupinou byl 0,9 % (7 % oproti 7,9 %). V intenzivně léčené skupině bylo riziko komplikací spojených s diabetem o 12 % nižší, o 10 % nižší úmrtí spojené s diabetem a o 6 % nižší pro všechny příčiny mortality. O 25 % došlo ke snížení mikrovaskulárních komplikací včetně nutnosti provádět retinální fotokoagulaci, makrovaskulární komplikace v aktivní části studie nebyly ovlivněny. V následném sledování se však došlo v původně intenzivně léčené skupině ke statisticky signifikantnímu snížení rizika infarktu myokardu (p = 0,014) a také snížení rizika mortality (HR = 0,87; p = 0,006). A to přesto, že došlo k vyrovnání hodnot HbA1c v obou skupinách. Nálezy jsou přisuzovány tzv. metabolické paměti v intenzivně léčené skupině od počátku vzniku onemocnění. Dále 730 diabetiků 2. typu ze studie UKPDS bylo randomizováno k terapii metforminem nebo jen dietou. V metforminové skupině došlo k 30% redukci komplikací spojených s diabetem a 42% redukci celkové mortality [2,3].
Studie ACCORD (the Action to Control Vascular Risk in Diabetes Study Group) sledovala 10 251 pacientů průměrného věku 62,2 roku s hodHbA1c 8,1 %, kteří byli léčeni intenzivní terapií s cílem dosáhnout HbA1c pod 6 % a standardní terapií s cílem HbA1c 7 – 7,9 %. Během 3,5letého sledování zemřelo 257 pacientů v intenzivně léčené skupině oproti 203 ve standardně léčené (p = 0,04). V intenzivně léčené skupině byly hmotnostní přírůstky více než 10 kg a častější hypoglykemie vyžadující pomoc druhé osoby (p < 0,001). Vzhledem ke zvýšené mortalitě byla studie předčasně ukončena. Zvýšení mortality bylo přisuzováno nárůstu závažných hypoglykemických příhod [4].
Ve studii ADVANCE bylo 11 140 pacientů s diabetem mellitem 2. typu randomizováno do standardní anebo intenzivně léčené skupiny, kde byl podáván gliklazid společně s dalšími antidiabetiky s cílem získat HbA1c ≤ 6,5 %. Během 5 let došlo ke snížení mikrovaskulárních komplikací (9,4 % oproti 10,9 %, p = 0,01), a to redukci incidence nefropatie (4,1 % oproti 5,2 %, p = 0,006) s nesignifikantním ovlivněním retinopatie (p = 0,05), ovlivnění větších makrovaskulárních příhod, úmrtí na kardiovaskulární příčiny, úmrtí ze všech příčin bylo rovněž statisticky nesignifikantní. Výskyt závažných hypoglykemických příhod byl větší v intenzivně léčené skupině (2,7 % oproti 1,5 %, p < 0,001) i když absolutní riziko nebylo závažné [5].
Ve studii VADT (the Veterans Administration Diabetes Trial) 1 791 diabetiků 2. typu bylo léčeno intenzivně a standardně a v intenzivně léčené skupině se podařilo dosáhnout HbA1c 6,9 % oproti 8,4 % ve druhé skupině. Neprokázal se signifikantní rozdíl v prvním výskytu kardiovaskulární příhody ani mikrovaskulárních komplikací. V intenzivně léčené skupině byl výskyt vedlejších účinků, hlavně hypoglykemických příhod, 24,1 % oproti 17,6 % ve standardně léčené [6].
Inzulinová analoga v léčbě diabetu mellitu 2. typu
Deficit inzulinové sekrece spojený s defektem účinku inzulinu a hyperglukagonemií vede u diabetiků 2. typu k excesivnímu uvolnění hepatické glukózy a snížení periferní absorpce glukózy. Následná hyperglykemie a zvýšení volných mastných kyselin způsobuje ztrátu funkce b buněk a zvyšuje apoptózu. V některých studiích se prokázalo [7], že již ve stadiu porušené glukózové tolerance je ztraceno až 40 % b buněk. V retrospektivní analýze [8] výsledků časné inzulinoterapie u nově diagnostikovaných diabetiků 2. typu bylo dokumentováno, že iniciální inzulinová terapie zabezpečí lepší dlouhotrvající remisi než primární zahájení perorální antidiabetické léčby, zřejmě zlepšením funkce b buněk.
Doporučení pro léčbu diabetu mellitu 2. typu dle ADA/EASD (American Diabetes Association/European Association of the Study of Diabetes) [9] zdůraznilo péči orientovanou na pacienta, s minimalizací nežádoucích účinků, především hypoglykemií a snížením kardiovaskulárního rizika. V algoritmu terapie se inzulin přesunul do druhé linie léčby za terapii metforminem. Inzulin je používán v této časné úrovni jako bazální inzulin a s výhodou jsou používána dlouhodobě působící bazální analoga, které se kombinují s perorálními antidiabetiky.
Celá řada studií treat ‑ to ‑ target se zabývala kombinací perorálních antidiabetik s bazálním inzulinovým analogem glarginem titrovaným dle glykemie nalačno. Ve sdružené analýze [10] 2 171 pacientů z 11 studií tohoto typu nejmenší počet symptomatických hypoglykemií s hodnotami pod 2,8 mmol/ l byl ve skupině, kde byl glargin kombinován jen s metforminem – 0,67 příhod/ pacienta/ rok oproti 1,05 příhod/ pacienta/ rok při kombinaci se sulfonylureou a 1,56 hypoglykemií/ pacienta/ rok při kombinaci sulfonylurea/ glargin/ metformin (p = 0,0576). Ve sdružené analýze [11] dat 607 pacientů s diabetes mellitus 2. typu ze 17 treat ‑ to ‑ target, kde byl in-zulin glargin podáván jen s metformi-nem, byl prokázán konzistentně nízký výskyt hypoglykemických příhod při dosažení požadovaných cílů kompenzace – méně než 1 hypoglykemie/ /pacienta/ rok.
Časnou terapií inzulinem se zabývala studie ORIGIN (Outcome Reduction with an Initial Glargine INtervention) [12]. Cílem multicentrické mezinárodní studie, ve které bylo randomizováno 12 500 pacientů, bylo stanovit, zda substituční inzulinová léčba glarginem vedená k cílové hodnotě glykemie nalačno 5,3 mmol/ l může snížit kardiovaskulární morbiditu a/ nebo mortalitu u jedinců s vysokým kardiovaskulárním rizikem s poruchou glukózové tolerance, zvýšenou glykemií nalačno nebo nově zjištěným diabetem mellitem 2. typu. Ve studii se podařilo terapií inzulinem glargin dosáhnout požadovanou glykemii nalačno, hodnotu HbA1c pod 6,5 % již během 1. roku a udržet po celou dobu 6,2 roku. Ve studii tedy bylo až 3násobné zvýšení pravděpodobnosti dosažení a udržení hodnoty HbA1c. Výskyt závažných hypoglykemií byl ≤ 1 na 100 osobo-roků, 43 % pacientů nezaznamenalo žádnou hypoglykemii přes dosažení normoglykemie. Incidence kardiovaskulárních příhod (nefatální infarkty myokardu, nefatální cévní mozkové příhody nebo kardiovaskulární úmrtí) a celková mortalita při terapii glarginem zůstala signifikantně neovlivněna. Nebyl zjištěn ani statistický důkaz o interakci mezi účinky inzulinu glargin a ω ‑ 3 - mastných kyselin pro jakýkoli primární či sekundární end--point (p > 0,14). Nedošlo k ovlivnění výskytu mikrovaskulárních komplikací, ani onkologických onemocnění. Pacienti s prediabetem léčení inzulinem glargin měli o 28 % menší pravděpodobnost vzniku nového diabetu (25 % vs 31 %; OR 0,72; 95% CI 0,58 – 0,91; p = 0,006). Substudií studie ORIGIN byla studie GRACE [13], ve které bylo zařazeno 1 184 pacientů s kardiovaskulárním onemocněním a/ nebo kardiovaskulárními rizikovými faktory plus zvýšená glykemie nalačno, porušená glukózová tolerance nebo nově vzniklý diabetes mellitus 2. typu. Pacienti měli buď inzulin glargin, nebo standardní péči a dvojitě slepou terapii s 1g kapslemi ω ‑ 3 - mastných kyselin (n ‑ 3FA) s možnými efekty na aterosklerózu. Primárním výstupem bylo sledování změny v maximální intimomediální tloušťce a. carotis communis, bifurkace a a. carotis interna, sekundárním výstupem byla změna v maximální intimomediální tloušťce společné karotidy a společně karotidy plus bifurkace. Terapie inzulinem glargin v intenzivně léčené skupině oproti standardní léčbě vedla k nesignifikantní změně v primárním výstupu (rozdíl 0,0030 ± 0,0021 mm/ rok, p = 0,145) a k signifikantní redukci v sekundárním výstupu (rozdíly 0,0033 ± 0,0017 mm/ rok, p = 0,049 a 0,0045 ± 0,0021 mm/ rok, p = 0,032). V terapii n ‑ 3FA nebyl signifikantní rozdíl mezi léčbou a placebem. Autoři uzavřeli, že inzulin glargin titrovaný k normoglykemii u pacientů s KV onemocněním a/ nebo KV rizikovými faktory a dysglykemií redukoval progresi intimomediální tloušťky karotid. Na studii ORIGIN navazuje následné sledování studie ORIGINALE (ORIGIN And Legacy Effects), která má potenciál během 2 roků zjistit efekt původní aktivní intervence glarginem na úmrtí z KV příčin, incidenci nefatálních infarktů myokardu, cévních mozkových příhod plus revaskularizačních výkonů, hospitalizací pro srdeční selhání a výskyt mikrovaskulárních komplikací. Výsledky studie budou k dispozici v roce 2014 (tab. 1) [14].
Table 1. Vliv intenzivní terapie diabetu na mikrovaskulární komplikace, kardiovaskulární onemocnění a mortalitu. Souhrn velkých klinických studií. 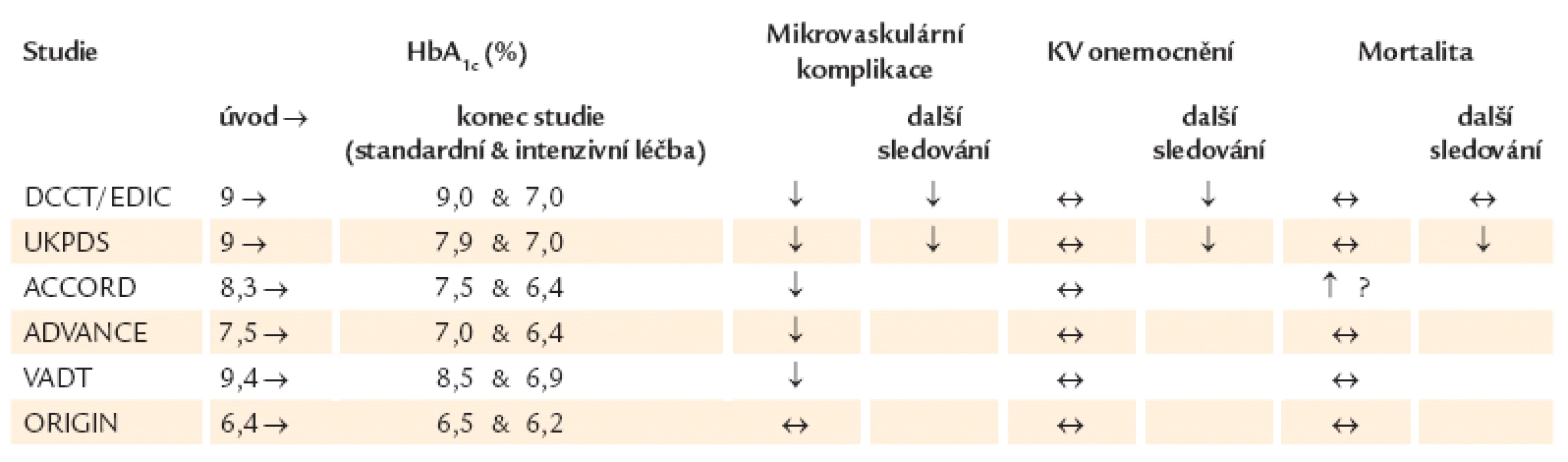
Novým dlouhodobě působícím inzulinovým analogem je inzulin degludec. Degludec má stabilní profil účinku a ultradlouhodobý efekt trvání přes 42 hod. Po subkutánní injekci tvoří solubilní multi‑hexamery. V 52týdenní studii [15] byl porovnáván degludec a glargin u 1 030 diabetiků 2. typu neuspokojivě kompenzovaných perorálními antidiabetiky. V hodnotě HbA1c nebyl signifikantní rozdíl, glykemie nalačno byla signifikantně nižší s degludecem (p = 0,005) a rovněž počet nočních hypoglykemií byl nižší při terapii degludecem o 36 % (p = 0,04). Vzhledem k dlouhodobému účinku inzulinu byla publikována studie, která se zabývala dávkováním degludecu 3krát týdně (pondělí, středa, pátek) ve srovnání s glarginem 1krát denně u 927 diabetiků 2. typu ve 26týdenním sledování. Porovnání z hlediska riziko/ přínos hlavně z hlediska hypoglykemických příhod nepodpořilo dávkovací schéma 3krát týdně [16]. Inzulin má připravovány studie se zaměřením na kardiovaskulární riziko.
Při zhoršení kompenzace pacienta léčeného inkretiny je možná i kombinace GLP‑1 analog s inzulinem, opět s dlouhodobě působícím analogem. Ve studii [17] postupná intenzifikace léčby metformin plus liraglutid plus detemir vedla u 52 % pacientů k dosažení HbA1c < 7 % při zachování původního hmotnostního úbytku z úvodu léčby GLP‑1 analogem. Také ve studii GetGoal Duo 1 [18] kombinující lixisenatid a inzulin glargin se snížila postprandiální glykemie o 3,16 mmol/ l a HbA1c klesl na 6,96 %.
Terapii dlouhodobě působícím analogem při další progresi diabetu a nedosažení požadovaných cílů kompenzace je možné postupně intenzifikovat přidáváním krátkodobě působících analog k hlavním jídlům s ponecháním terapie metforminem a/nebo s inhibitory DPP ‑ 4 (dipeptidylpeptidázy ‑ 4). Alternativou k těmto inzulinovým režimům bazál/ bolus je využití premixů (směsných inzulinů) s analogy o různém obsahu krátkodobě působícího analoga. V 48týdenní studii PARADIGM [19] u 426 diabetiků 2. typu neuspokojivě kompenzovaných perorálními antidiabetiky byl podáván inzulin lispro mix 25 1krát denně oproti inzulinu glargin. Dle kompenzace dávka lispro mix 25 byla postupně intenzifikována až na 3 denní dávky a léčba glarginem byla intenzifikována přidáváním lispra k hlavním jídlům. V obou skupinách bylo dosaženo podobné hodnoty HbA1c, postprandiálních glykemií, hypoglykemických příhod i hmotnosti. Mezi skupinami nebyl statisticky signifikantní rozdíl.
Závěr
Diabetes mellitus 2. typu je chronické progresivní onemocnění spojené s vysokou kardiovaskulární morbiditou a mortalitou. Léčba vyžaduje postupnou kombinaci antidiabetik. V algoritmu se inzulinoterapie posunula do časnějších stadií. Cílem je nejen dosažení požadované kontroly glykemie, ale i šetření funkce β buněk, minimalizace nežádoucích účinků, zvláště hypoglykemií a snížení kardiovaskulárního rizika.
MU Dr. Alena Adamíková, Ph.D.
www.kntb.cz
e‑mail: adamikova@bnzlin.cz
Doručeno do redakce: 30. 4. 2013
Sources
1. Rendell M. The path to approval of new drugs for diabetes. Expert Opin Drug Saf 2013; 12 : 195 – 207.
2. UKPDS Group. Intensive blood glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes. Lancet 1998; 352 : 837 – 853.
3. Holman RR, Paul SK, Bethel MA et al. 10‑year follow‑up of intensive glucose control in type 2 diabetes. N Engl J Med 2008; 359 : 1577 – 1589.
4. The Action to Control Cardiovascular Risk in Diabetes Study Group. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008; 358 : 2545 – 2559.
5. The ADVANCE Collaborative Group. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med 2008; 358 : 2560 – 2572.
6. Duckworth W, Abraira C, Moritz T et al. Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med 2009; 360 : 129 – 139. Erratum in: N Engl J Med 2009; 361 : 1028.
7. Kjems LL, Kirby BM, Welsd M et al. Decreasein beta‑cell mass leads to impaired pulsatile insulin secretion, reduced postprandial hepatic insulin clearance, and relative hyperglucagonemia in the minipig. Diabetes 2001; 50 : 2001 – 2012.
8. Chon S, Oh S, Kim SW et al. The effect of early insulin therapy on pancreatic beta‑cell function and long‑term glycemic control in newly diagnosed type 2 diabetic patients. Korean J Intern Med 2010; 25 : 273 – 281.
9. Inzucchi SE, Bergenstal RM, Buse JB et al. Management of hyperglycemia in type 2 diabetes: a patient ‑ centered approach. Position statement of the American Diabetes Association (ADA) and the European Association fot the Study of Diabetes (EASD). Diabetes Care 2012; 35 : 1364 – 1379.
10. Fonseca V, Gill J, Zhou R et al. An analysis of early insulin glargine added to metformin with or without sulfonylurea: impact on glycaemic control and hypoglycaemia. Diab Obes Metab 2011; 13 : 814 – 822.
11. Owens D, Dain MP, Landgraf W. Early onset of glycaemic improvements after insulin initiation with glargine in T2DM patients uncontrolled with OADS. CODHy 2012 abstrakt 113 [online] [cit. 06 - 02 - 2013]. Available from: www.codhy.com/ 2012/ abstract_list.aspx.
12. Gerstein HC, Bosch J, Dagenais GR et al. ORIGIN Trial Investigators. Basal insulin and cardiovascular and other outcomes in dysglycemia. N Engl J Med 2012; 367 : 319 – 328.
13. Lonn EM, Bosch J, Diaz R et al. Effect of insulin glargine and n ‑ 3FA on carotid intima ‑ media thickness in people with dysglycemia at high risk for cardiovascular events. Diabetes Care 2013; 5 : 1 – 9.
14. Bergenstal RM, Bailey C, Kendall DM. Type 2 diabetes: assessing the relative risks and benefits of glucose-lowering medications. Am J Med 2010; 123: e9–e18.
15. Zinman B, Philis ‑ Tsimikas A, Handelsman Yet al. Effect of insulin degludec on glycaemic control and nocturnal hypoglycaemia compared with insulin glargine: a 1‑year trial in insulin‑-naive patients with type 2 diabetes. Diabetologia 2012; 55 (Suppl 1): S22.
16. DeVries JH, Ratner RE, Bode BW et al. Two phase 3 trial of three ‑ times weekly insulin degludec versus once ‑ daily insulin glargine in insulin‑naïve people with type 2 diabetes. Diabetologia 2012; 55 (Suppl 1): S21.
17. Rosenstock J, DeVries JH, Seufert J et al. A new type 2 diabetes treatment paradigm: sequential addition of liraglutide to metformin and then basal insulin detemir. Diabetes 2011; 60 (Suppl 1): A76.
18. Rosenstock J, Forst T, Aronson R et al. Once ‑ daily lixisenatide added on to consistently titrated insulin glargine plus oral agents in type 2diabetes: the GetGoal ‑ Duo 1 study. Diabetologia 2012; 55 (Suppl 1): S333.
19. Bowering K, Reed VA, Felicio J et al. A study comparing insulin lispro mix 25 with glargine plus lispro therapy in patients with type 2 diabetes who have inadequate glycaemic control on oral antihyperglycaemic medication: results of the PARADIGM study. Diabet Med 2012; 29: e263 – e272.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2013 Issue 6-
All articles in this issue
- Adherence a perzistence se zaměřením na léčbu hypertenzních pacientů
- Diuretika v monoterapii a v kombinaci s diuretiky a nediuretiky v léčbě hypertenze
- Hypertenze u pacientů s polycystickými ledvinami – incidence, patogeneze, prognóza, terapie
- Primární hyperaldosteronizmus: častá forma sekundární hypertenze s vyšším kardiovaskulárním rizikem
- Chronická obstrukční plicní nemoc pohledem nových doporučení – souhrn aktuálního fenotypově zaměřeného standardu České pneumologické a ftizeologické společnosti pro internisty
- Účinnost léčby anagrelidem u nemocných s Ph‑ negativními myeloproliferativními chorobami: ovlivnění výskytu trombózy ve výstupech Registru pacientů s diagnózou esenciální trombocytemie a trombocytemie provázející jiné myeloproliferativní onemocnění léčených Thromboreductinem® ke konci roku 2012
- Počátky České kardiologické společnosti a české kardiologie
- Moderní trendy v inzulinoterapii
- Vplyv tuhosti aorty na centrálnu hemodynamiku a na kardiovaskulárny systém
- Lipidy a veľkosť lipoproteínových častíc u pacientov s novozisteným a doposiaľ neliečeným diabetes mellitus 2. typu
- Metabolický syndróm a prediabetické stavy
- Rezistentná hypertenzia v staršom veku
- Epigenetická cytostatika a jejich role v protinádorové léčbě
- Environmentálny estrogén bisfenol A a jeho účinky na organizmus človeka
- Jak ovlivňuje gravidita onemocnění hypofýzy
- Diferenciálna diagnóza a liečba hyponatriémie
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Diferenciálna diagnóza a liečba hyponatriémie
- Jak ovlivňuje gravidita onemocnění hypofýzy
- Diuretika v monoterapii a v kombinaci s diuretiky a nediuretiky v léčbě hypertenze
- Environmentálny estrogén bisfenol A a jeho účinky na organizmus človeka
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

